¶ TIGR、CASY、CERO提升3D细胞培养效率
提高产量、减少人工操作——改进实验结果

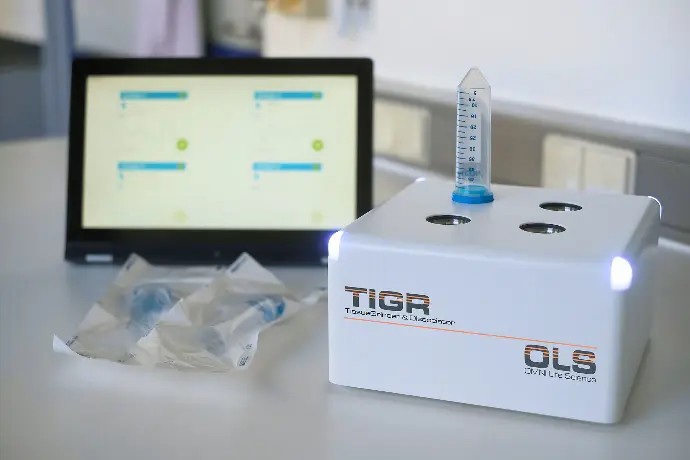
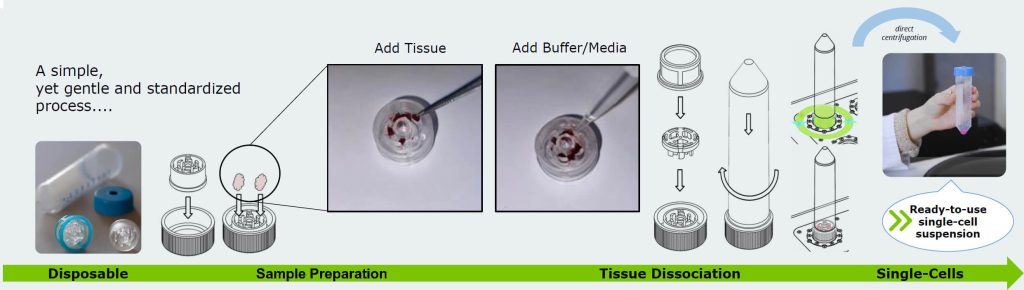
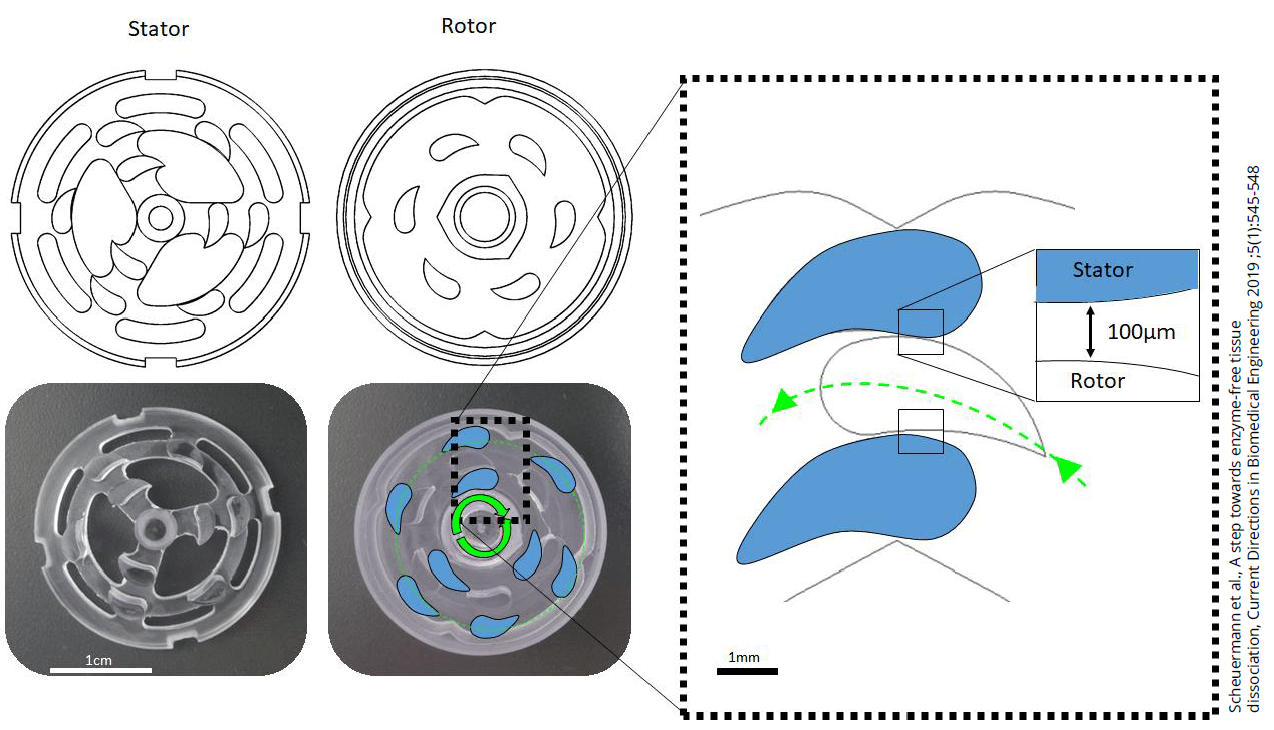
¶ 1.TIGR – Tissue Grinder & Dissociator 组织研磨与分散器
 |
 |
 |
|
|
|
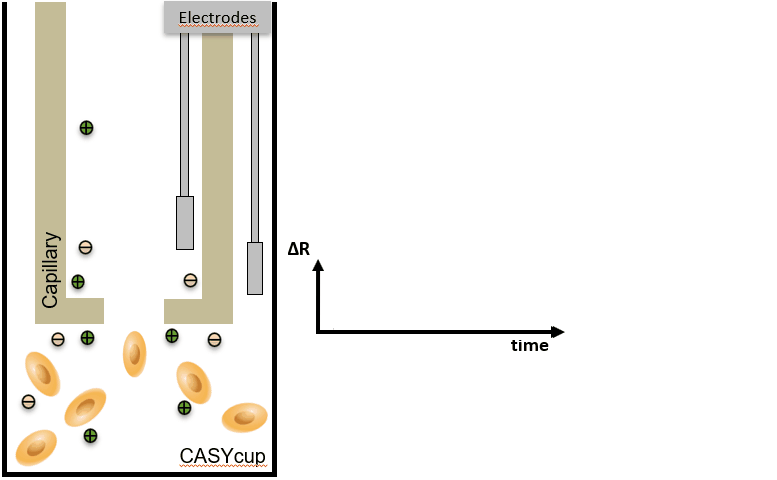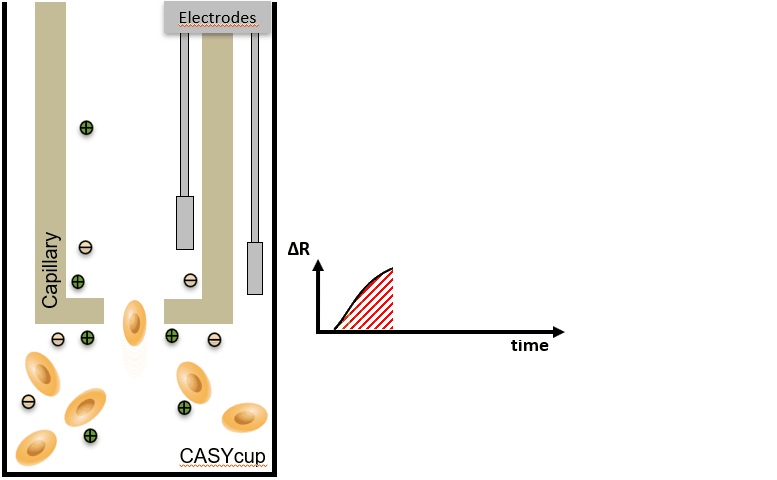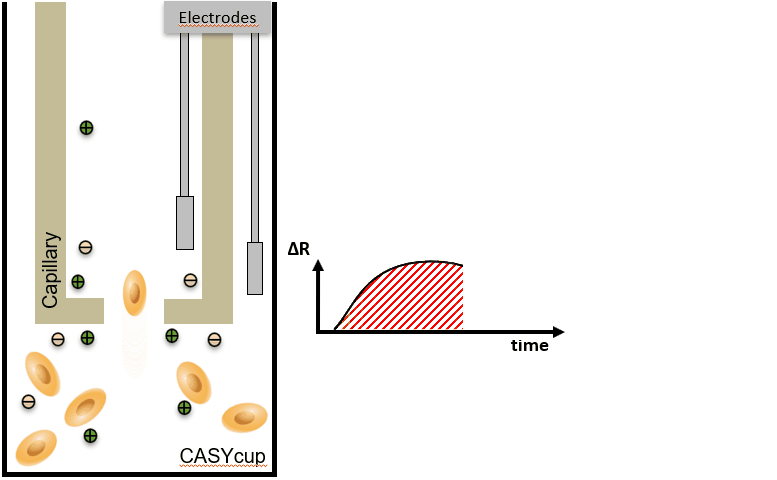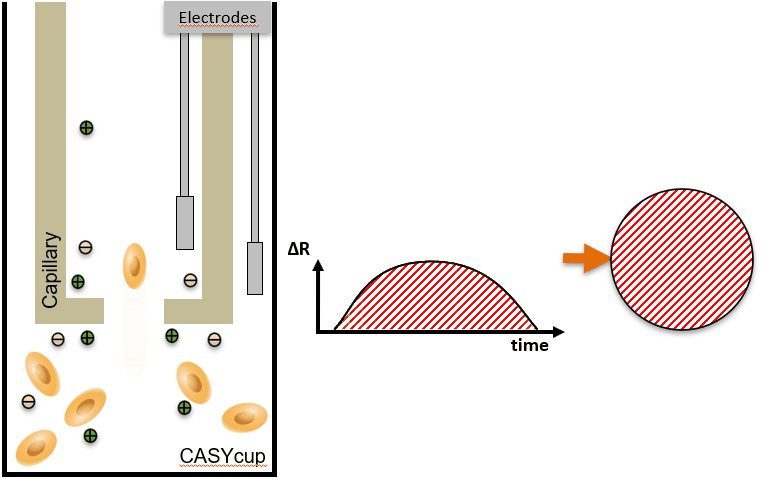
¶ 2.CASY – Cell counter & Analyzer 细胞计数分析仪
CASY 的主要原理 – 计数 & 体积
|
 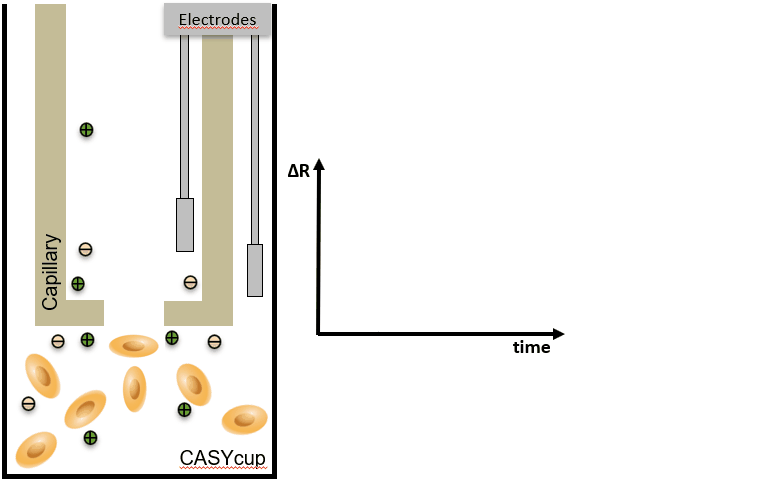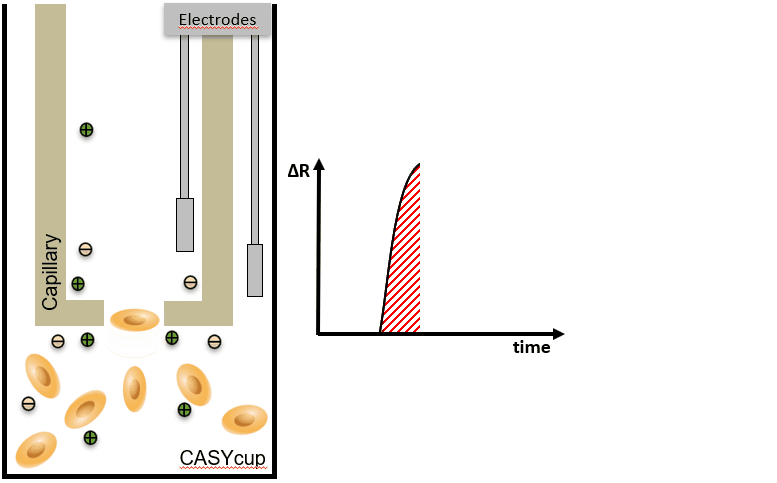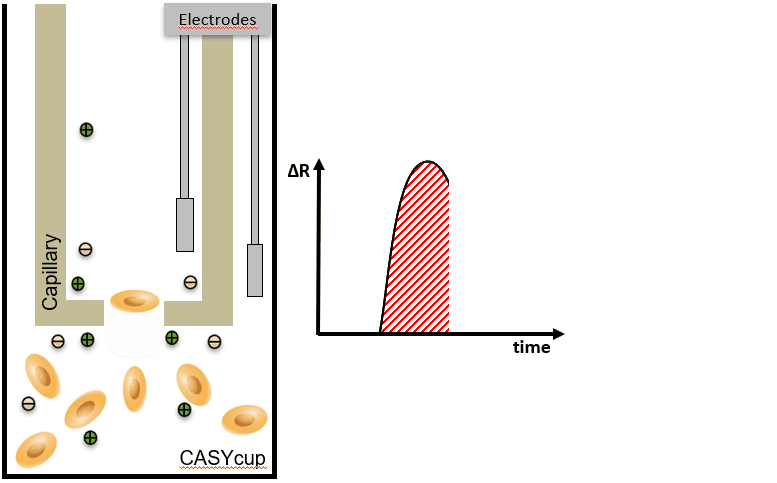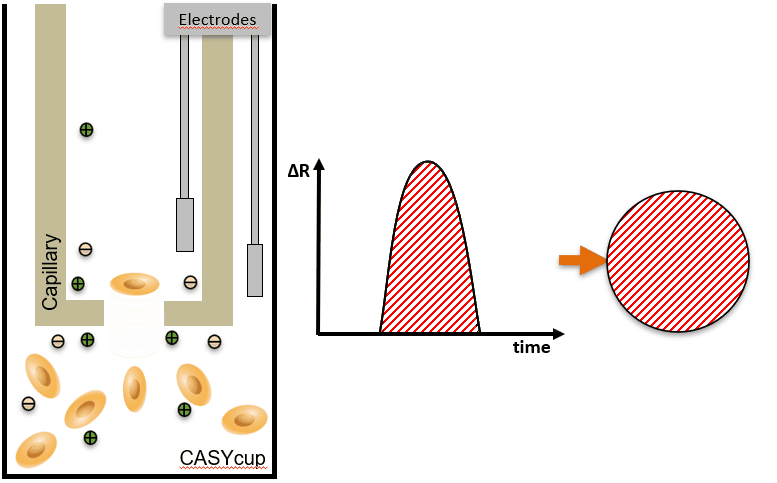 |
|
|
|
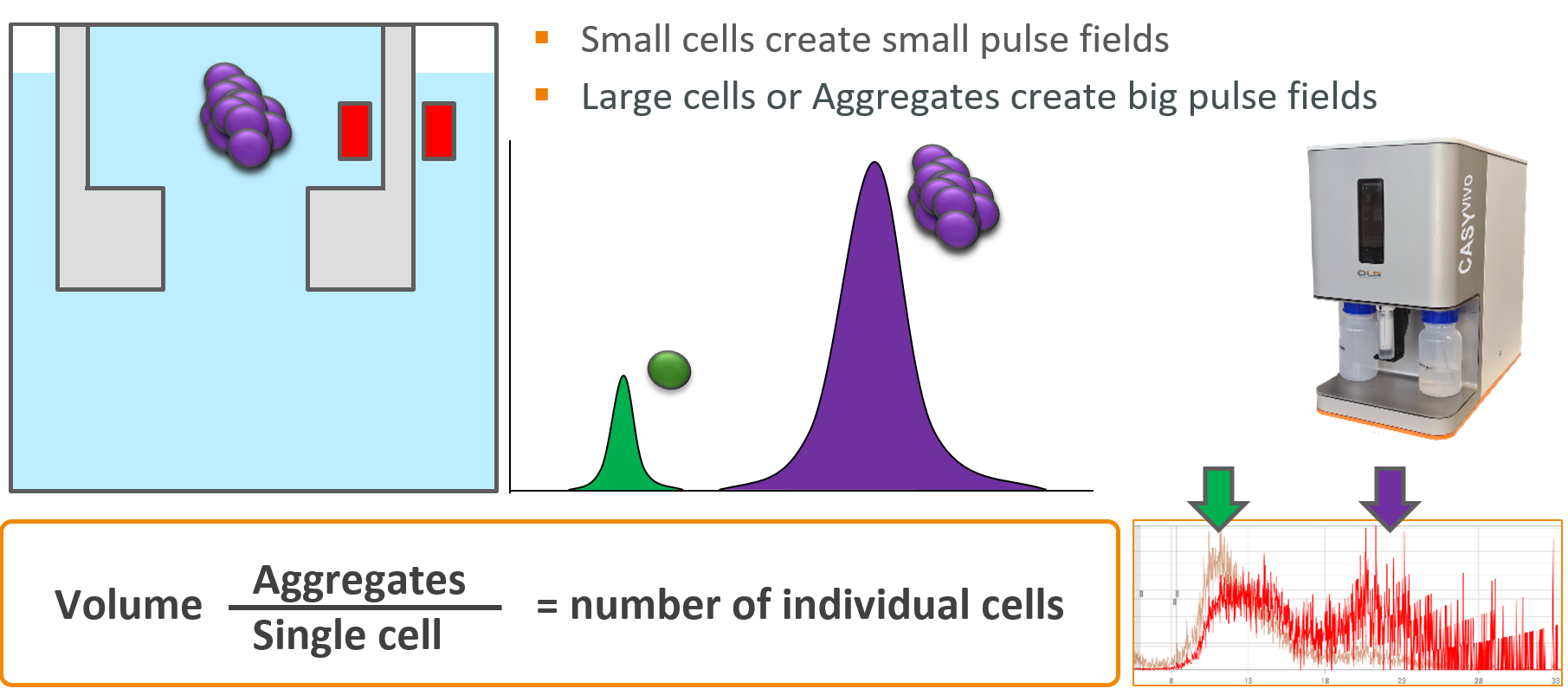
CASY的最重要特点:聚集物校正
 |
||
|
细胞聚团会导致细胞计数不准确,因为大脉冲通常会被误解为单个细胞的信号,而实际上是多个细胞的聚集。为了校正这种影响,CASY系统提供了聚集物校正功能,通过分析脉冲的大小来区分聚集物和单个细胞。 | Volume / Aggregates = number of individual cells:该公式表明,通过计算细胞或聚集物的体积并与聚集物的数量进行比较,可以推算出单个细胞的数量。CASY系统通过此公式来校正聚集物的影响,从而提供更精确的细胞计数。 |
|
体积检测与精度:
聚集体校正:
死细胞的影响:
|
||
¶ 3.CERO 3D Incubator & Bioreactor 全自动3D细胞培养仪
 |
 |
|
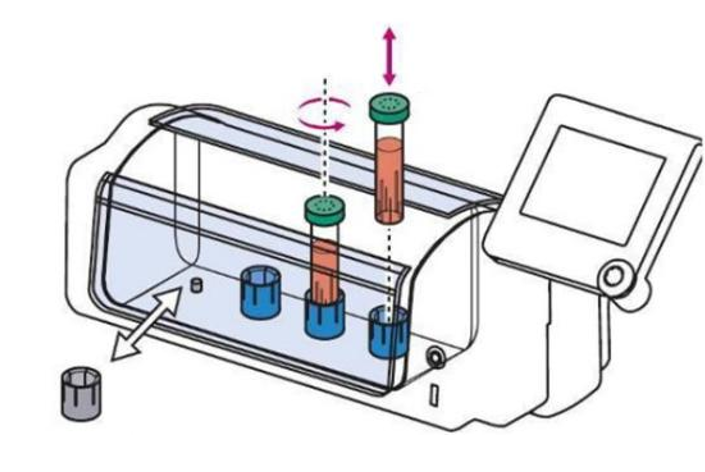
4个独立控制的管道(4 individually controlled tubes):
小型台式设计(Small footprint benchtop Incubator):
最低剪切力的均质化翅片(Homogenization fins for lowest shear forces in bi-directional rotation):
温度和二氧化碳控制(Controlled CO2 & temperature):
在线pH监测(Online pH monitoring):
通气帽(Vented cap):
|
|
 |
|
|
简易操作与标准化(Easy handling & Standardization):
|
典型的类器官样本,来自NSCLC肺癌(H1299细胞),这表明该方法适用于复杂的肿瘤类器官培养,尤其在癌症研究中有广泛的应用。 |
|
每3到7天操作一次,操作时间约为4分钟(Hands on as limited as ~4 min every 3 to 7 days):这种标准化操作方法极大地减少了人工操作时间,3D类器官培养可在较长的时间内减少人工干预,仅需每3到7天进行简单操作,节省了大量时间。 每管可培养超过80,000个类器官(> 80.000 organoids (~500μm) per tube):这种操作可以在每个培养管中培养超过80,000个直径约为500微米的类器官,表明该方法具有很高的细胞培养效率。 |
|
|
干细胞扩增(Expansion of Stem Cells):
|
类器官培养(Organoids from Domes or Tissue):
|
|
干细胞分化(Differentiation of Stem Cells):
|
共培养实验(Perform Co-Cultures):
|
|
长期培养(Long term cultivation):
无凋亡(No apoptosis over much extended periods):
几个月或更长时间(Several months or more):
|
CAR巨噬细胞的生产(Production CAR Macrophages):
|
|
维持组织片段(Maintaining Tissue pieces):
|
|
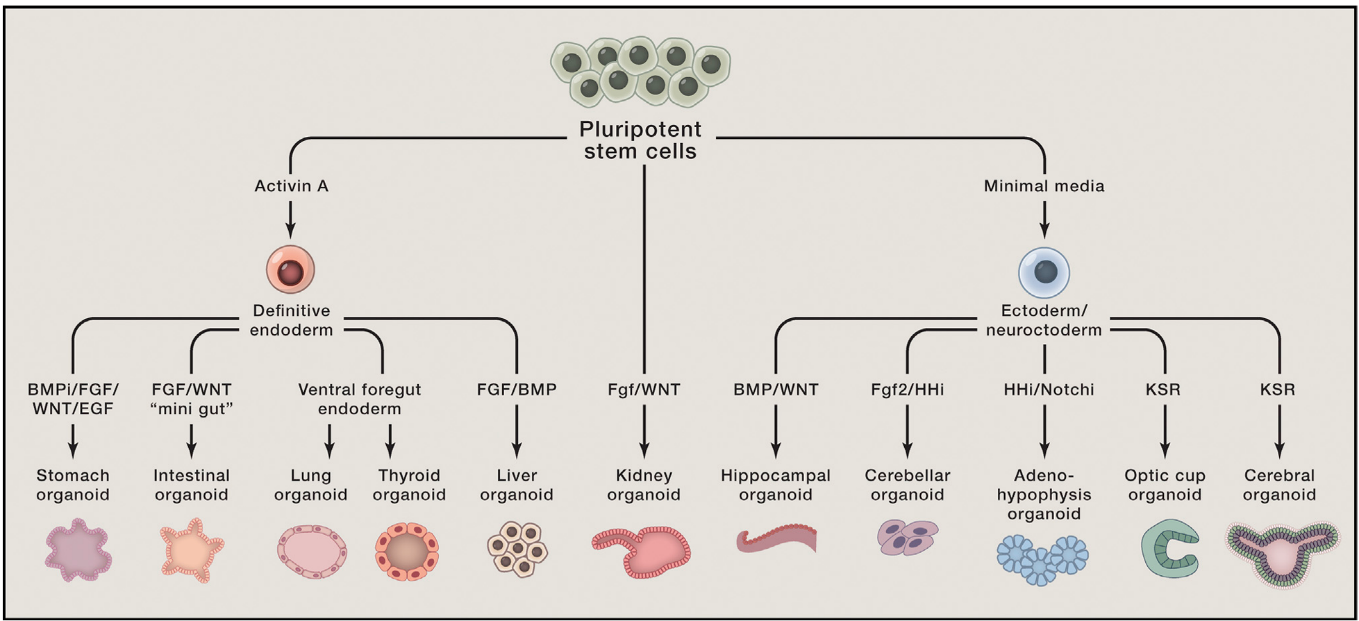 |
¶ 1. 多能干细胞(Pluripotent stem cells)
¶ 2. 分化路径图中将多能干细胞的分化路径分为两个主要的胚层:内胚层和外胚层/神经外胚层。每个胚层的分化过程由特定的因子控制。 ¶ 内胚层(Endoderm)
¶ 外胚层/神经外胚层(Ectoderm/Neuroectoderm)
|
|
多能干细胞(Pluripotent Stem Cells, PSC)的扩增与分化过程 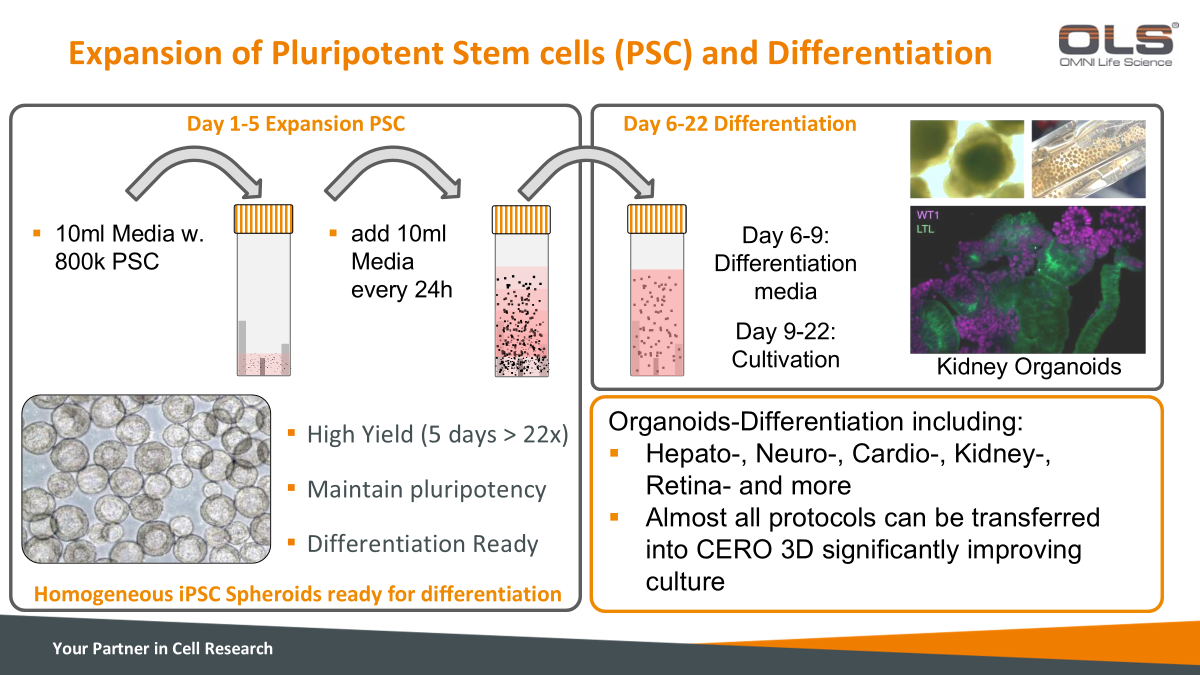 |
|
¶ Day 1-5: 扩增多能干细胞(Expansion of PSC)
¶ Day 6-22: 分化阶段(Differentiation),肾脏类器官的形成
|
|
|
¶ 类器官分化(Organoids Differentiation)
|
| 准备分化的类胚状体 | |
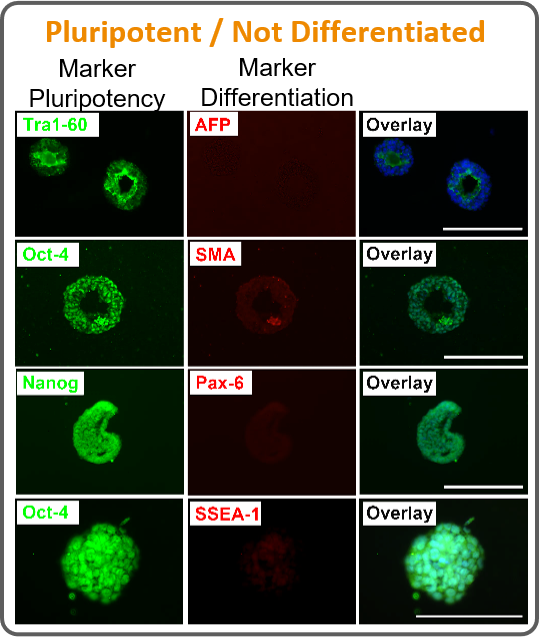 ¶ Pluripotent / Not Differentiated (多能性/未分化)
|
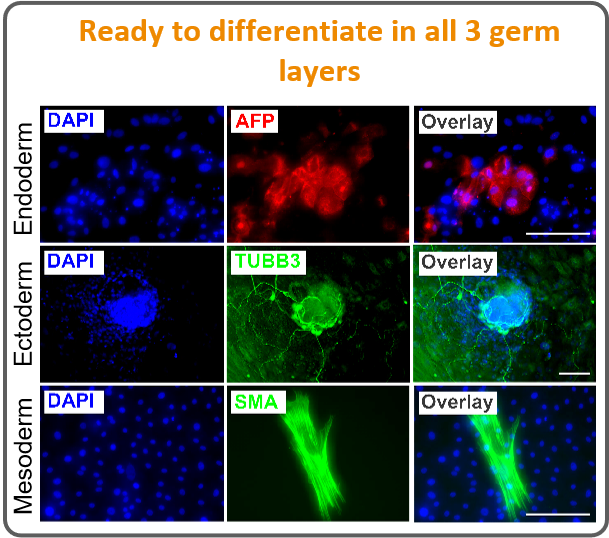 ¶ Ready to differentiate in all 3 germ layers (准备向所有三个胚层分化)
|
| 文章:Elanzew, et. al.; A reproducible and versatile system for the dynamic expansion of human pluripotent stem cells in suspension; Biotechnol. J. 2015, 10, 1589–1599 | |
| 提高了心肌细胞的纯度和质量 | |
 |
 |
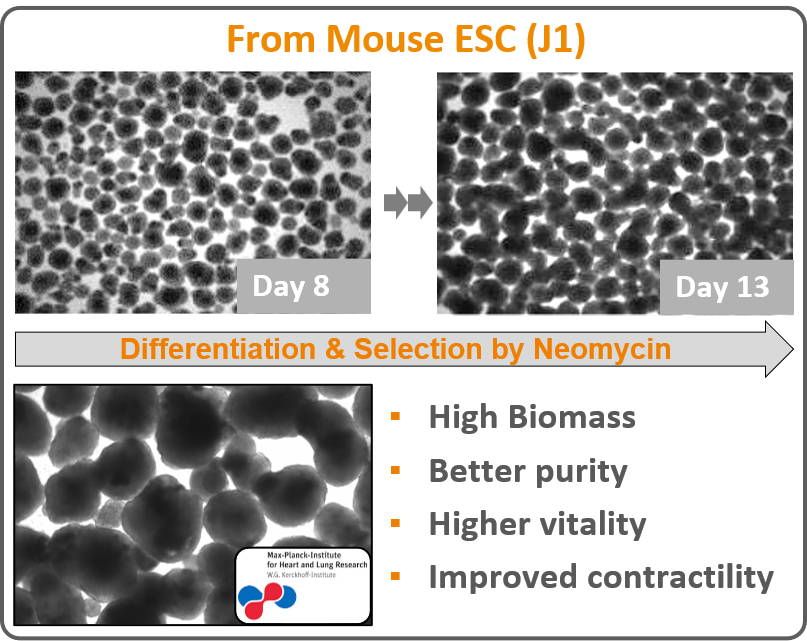
¶ 1. 从小鼠ESC分化为心肌细胞(From Mouse ESC (J1))
|
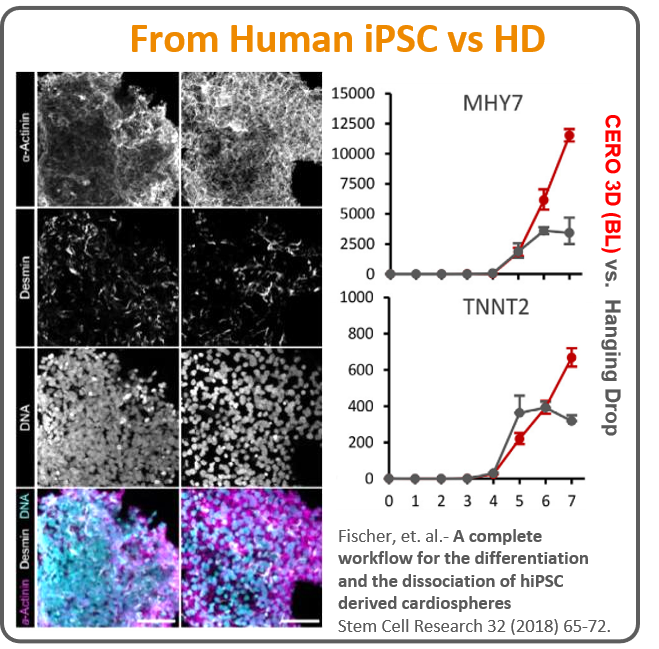
¶ 2. 从人类iPSC分化为心肌细胞(From Human iPSC vs HD)
MHY7与TNNT2的表达:图右侧展示了MHY7和TNNT2两个心肌细胞标记物在不同培养方法下的表达量对比。使用CERO 3D系统(红色曲线)与传统的悬滴法(灰色曲线)相比,CERO 3D系统在心肌细胞分化过程中表现出更高的标记物表达量。
|
¶ 3. 心肌细胞的纯度和质量(Improved Purity & Quality of Cardiomyocytes)
|
|
| 从人类诱导多能干细胞(iPSC)分化得到的视网膜类器官(Retina Organoid) | |
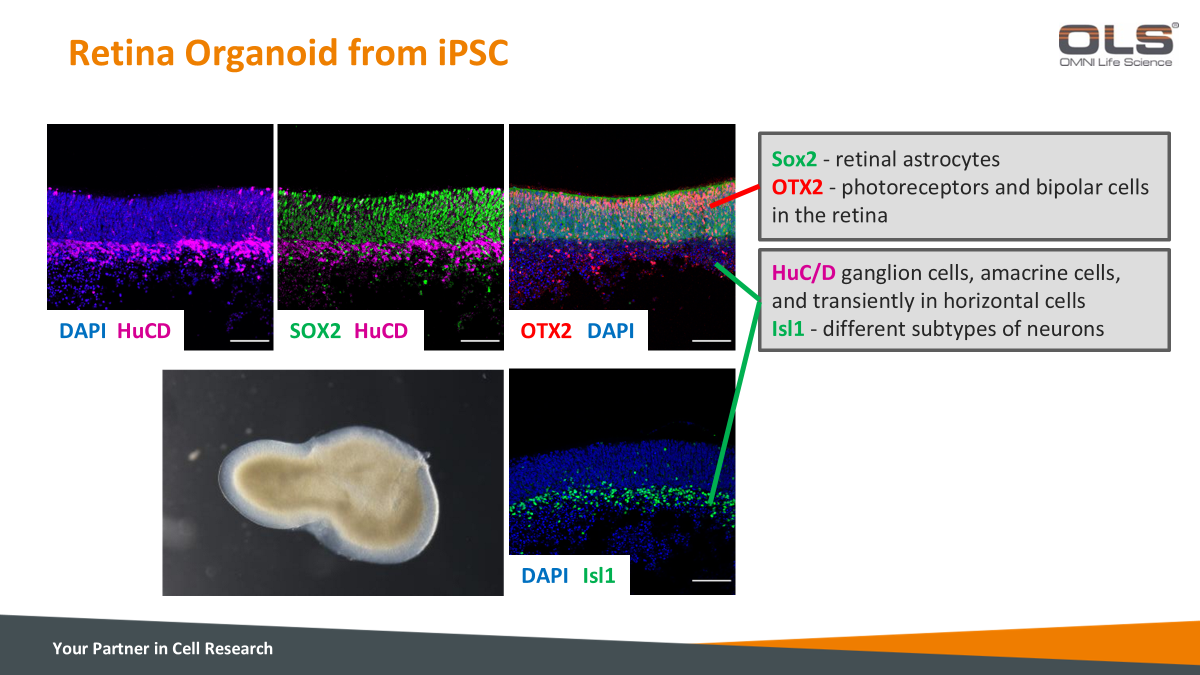 ¶ 细胞层次与定位
¶ 应用与意义视网膜类器官的应用:通过这种方式获得的视网膜类器官能够用于研究视网膜的发育、疾病模型(如视网膜退行性疾病)、药物筛选和再生医学。研究人员可以通过在体外模拟视网膜的发育过程,深入研究各种眼科疾病的机制,并寻找潜在的治疗方法。 从iPSC分化到视网膜类器官:这表明,iPSC具有巨大的潜力,通过合适的培养条件和分化因子,可以生成复杂的三维视网膜类器官。这一过程的成功应用为眼科相关的研究和治疗提供了新的方向。 |
|
|
DAPI:是一种常用于染色细胞核的染料,标记细胞核为蓝色。图中显示了类器官的细胞核分布。 HuCD:是一种神经系统细胞的标志物,通常标记神经元。绿色荧光显示HuCD标记的神经元。图中可以看到HuCD标记的细胞在视网膜类器官中均匀分布。 SOX2:SOX2是视网膜胶质细胞的标志物,它在视网膜的星形胶质细胞中表达。在图中,SOX2被标记为绿色,并与HuCD共同显示,以帮助区分神经元和胶质细胞。 OTX2:OTX2是视网膜光感受器细胞和双极细胞的标志物。它是一个关键的转录因子,有助于视网膜发育。在图中,OTX2用红色荧光标记,显示在视网膜的内外层区域,标志着这些细胞的存在。 Isl1:Isl1是多种神经元亚型的标志物,在图中的绿色标记中显示。它在视网膜中标记不同类型的神经元,尤其是在视网膜的某些区域,涉及到不同亚型的神经元(如视网膜神经节细胞等)。 |
|
|
视网膜类器官(Retina Organoid):这是通过iPSC分化得到的三维视网膜类器官,模拟了视网膜的结构。图中展示了在不同时间点的类器官结构,包含了多层的神经细胞,具有典型的视网膜层状结构。 标记的细胞类型:
|
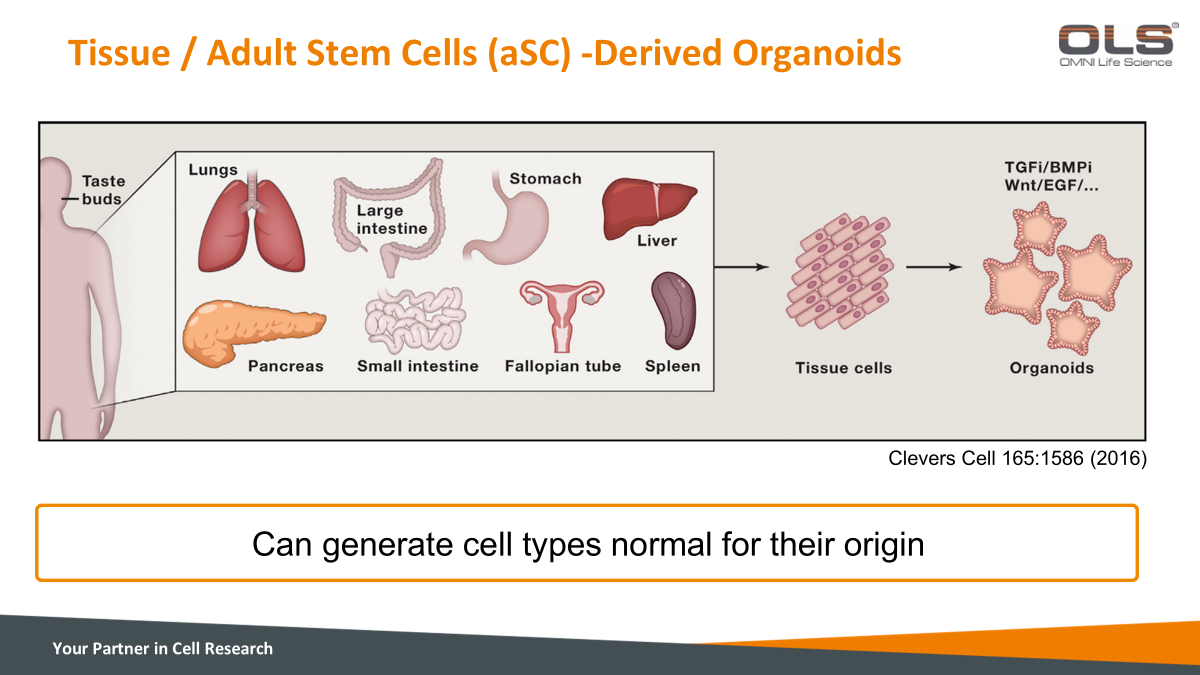
| 从不同组织类型的成人干细胞分化为各种器官模型 |
|
¶ 1. 成人干细胞(aSC)来源的器官
这些器官模型(类器官)代表了从成人组织来源的干细胞生成的多种不同器官类型。 ¶ 2. 生成过程
|
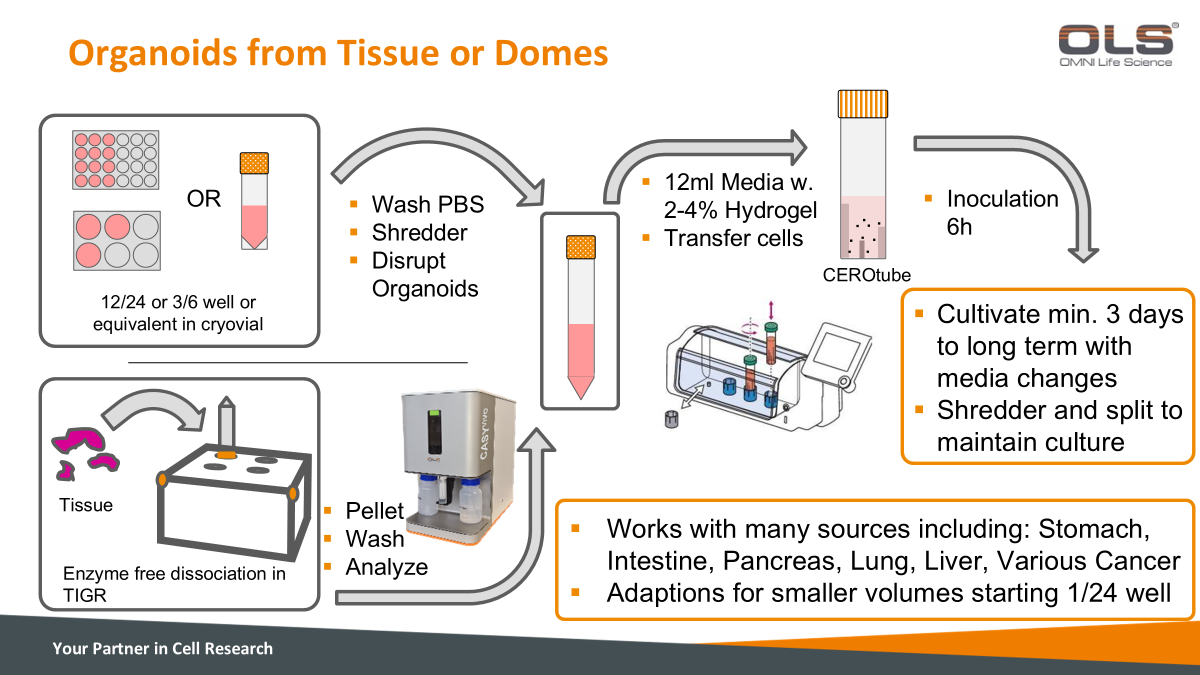
| 从组织或类器官培养中提取并进一步分化的过程 | |
|
|
|
¶ 转移至CERO系统培养
|
¶ 使用TIGR进行酶无分解处理
|
¶ 接种和培养
|
| 扩大人类结肠癌类器官的生产规模 |
|
通过不同细胞接种浓度(4% Matrigel)进行规模化生产 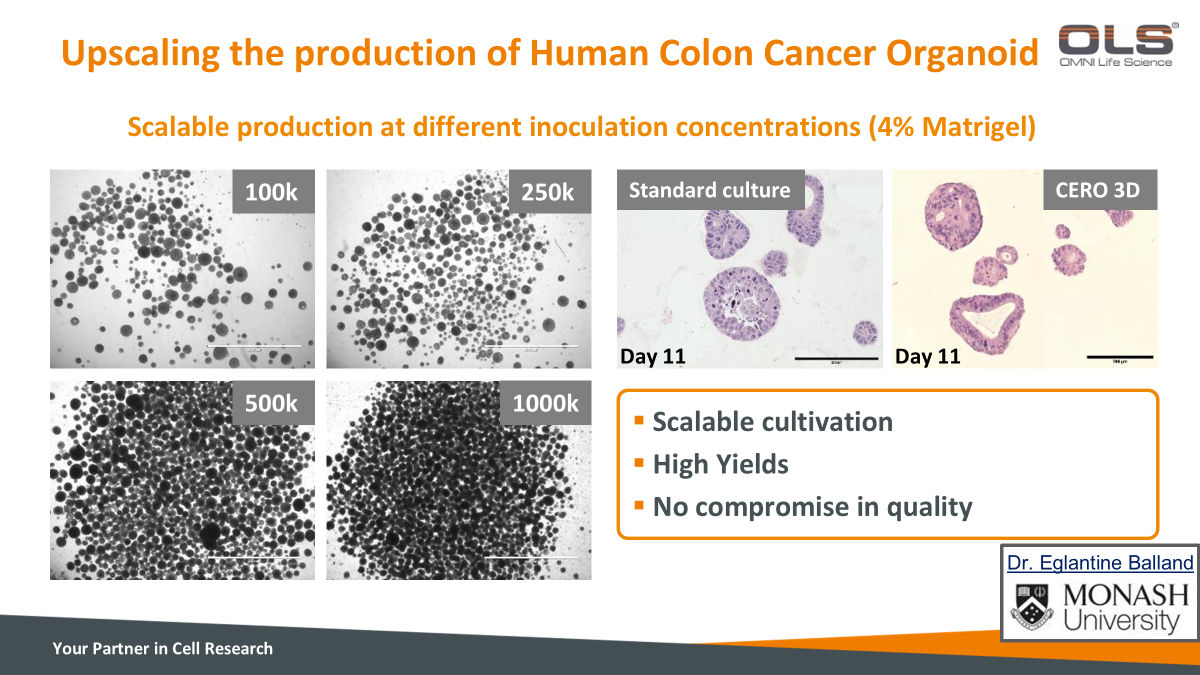 可扩展的培养(Scalable cultivation) 高产量(High Yields) 质量不妥协(No compromise in quality) |
¶ 1. 细胞接种浓度对类器官形态的影响
¶ 2. 标准培养与CERO 3D培养的比较
|
| 人类乳腺癌类器官的形态 | |
|
在不同Matrigel浓度和细胞接种量条件下培养的乳腺癌类器官的形态 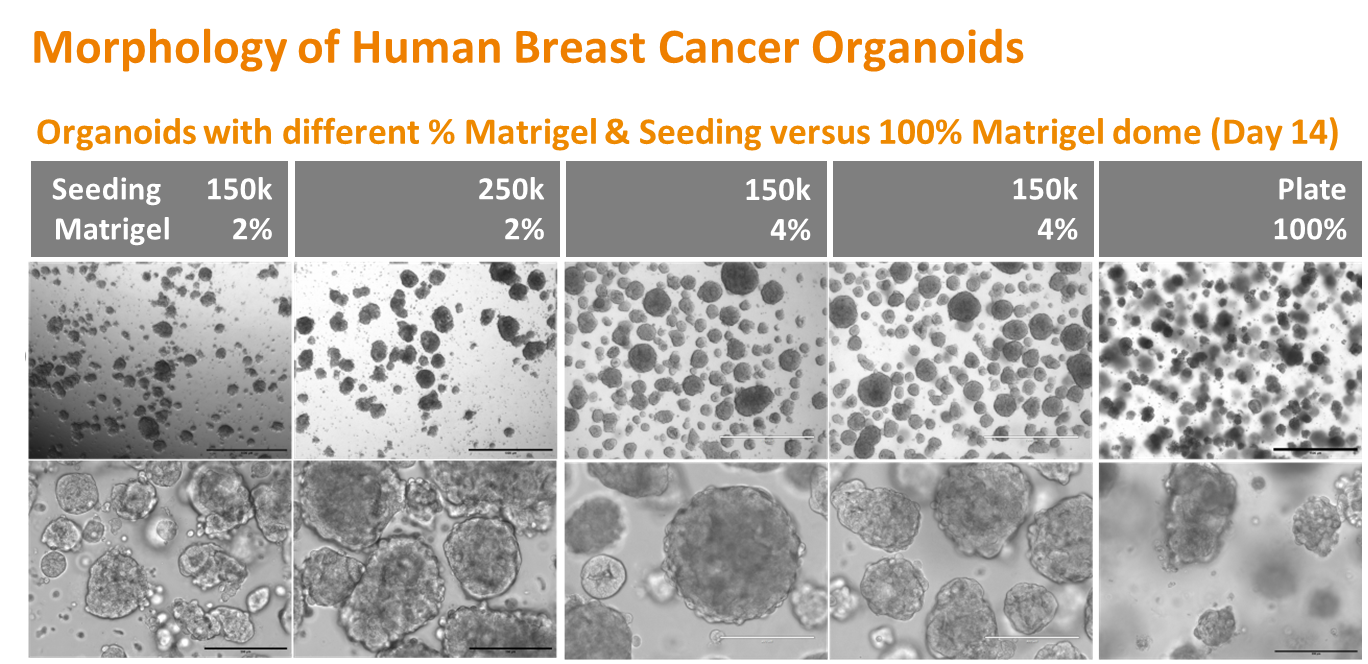 |
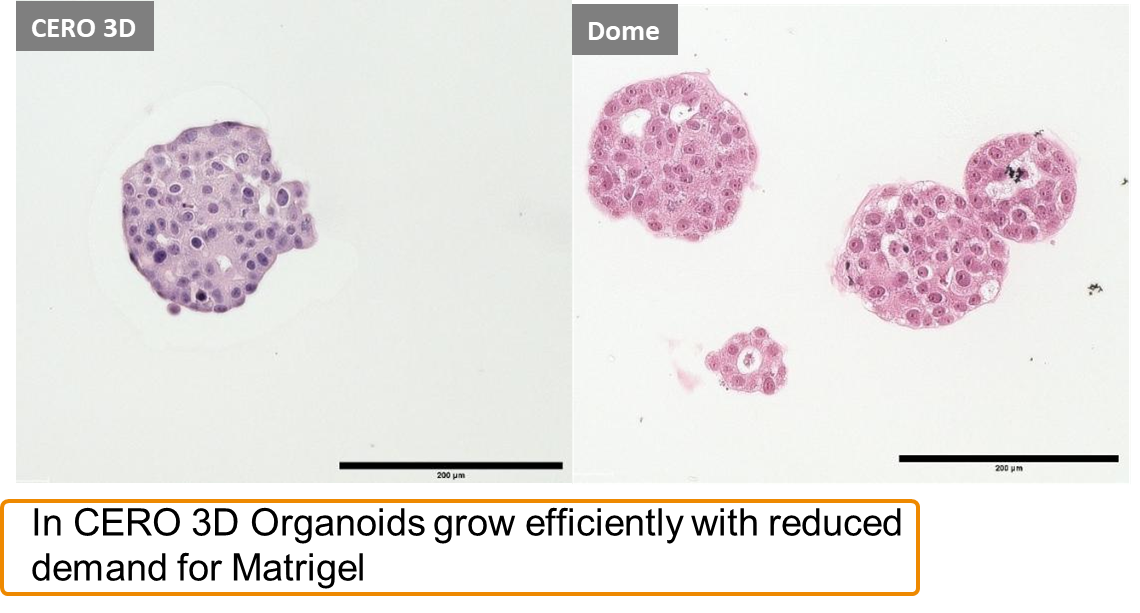 |
|
这张图展示了在不同Matrigel浓度和细胞接种量条件下培养的乳腺癌类器官的形态。 ¶ 图左侧:
¶ 图中间:
¶ 图右侧:
¶ 对比:
|
¶ CERO 3D与传统Dome方法的比较这张图比较了CERO 3D系统与传统的Dome培养方法下乳腺癌类器官的组织学结构。 ¶ 左侧:CERO 3D
¶ 右侧:Dome
¶ 组织学对比:
¶ 总结:这张图突出了CERO 3D系统相较于传统Dome方法的优势,表现为更高的类器官生长密度和更好的结构化,显示出CERO 3D在类器官培养中的优越性。 |
| 人类乳腺癌的最佳成本与培养条件 |
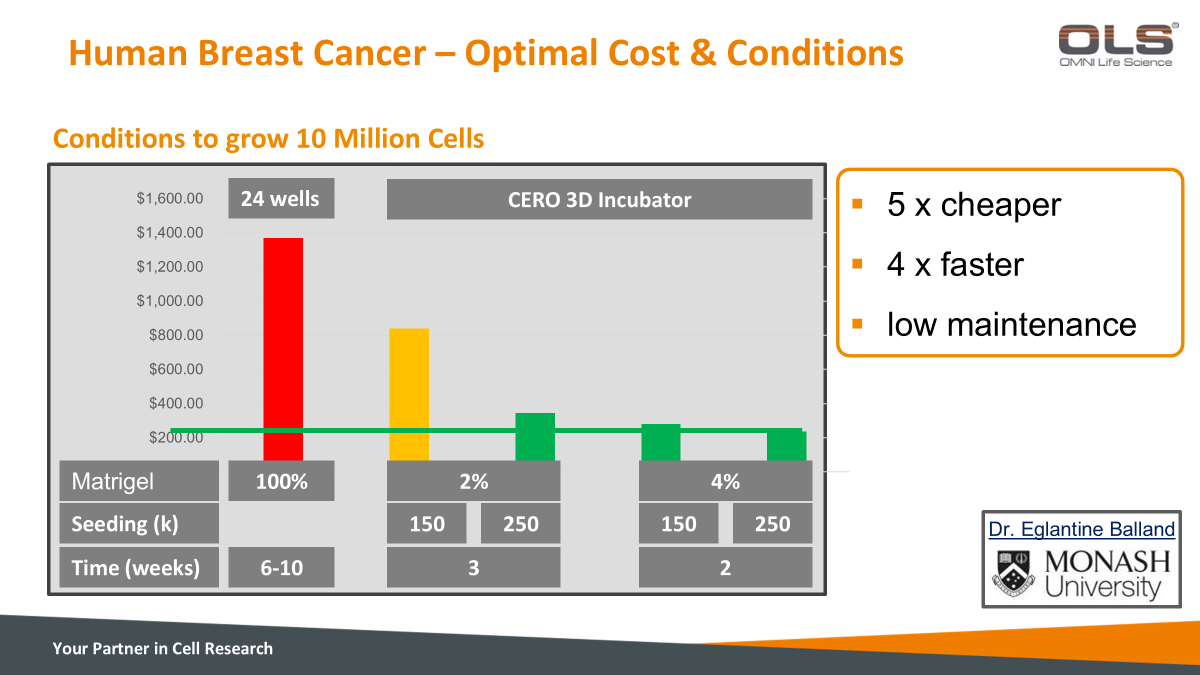 |
¶ 图表左侧:
¶ 图表右侧:
|
| 来源于小鼠成年神经干细胞(aNSCs)的脑类器官 | |
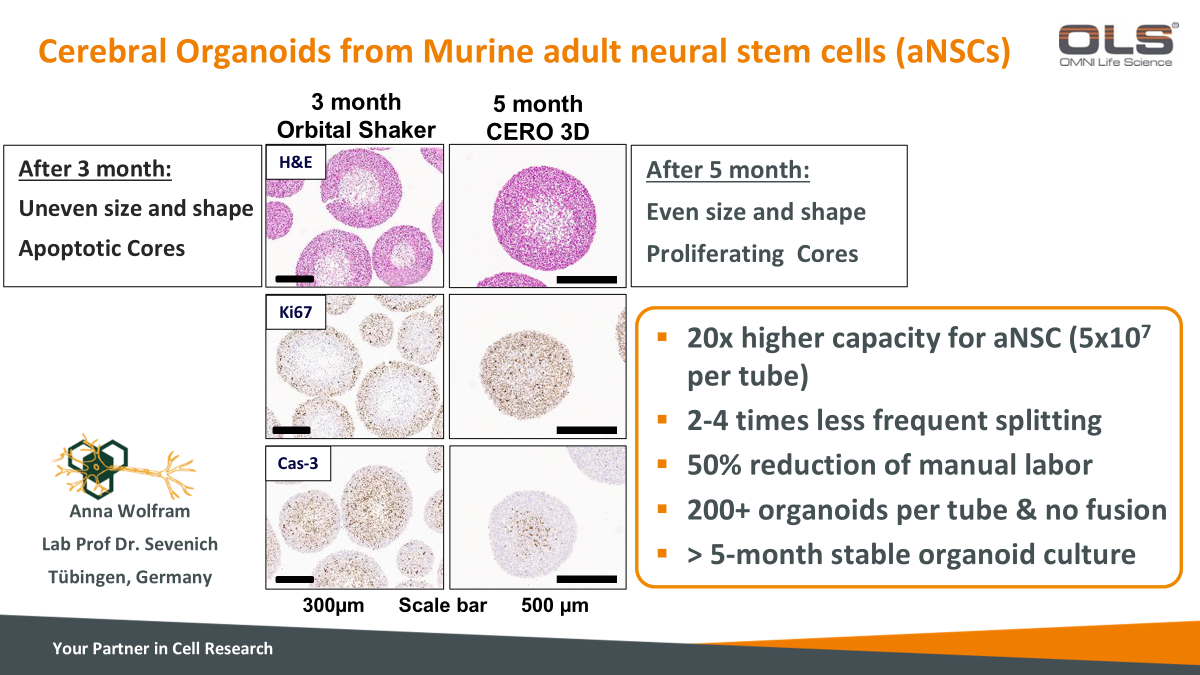 |
|
¶ 3个月培养 - Orbital Shaker(摇床方法):
|
¶ 5个月培养 - CERO 3D系统:
|
|
20倍更高的容量:
减少2-4倍的频繁传代:
降低50%的人工操作:
每个培养管中可获得超过200个类器官,无融合现象:
5个月稳定的类器官培养:
|
|
| 胶质瘤类器官(glioma assembloids)作为肿瘤模型 | |
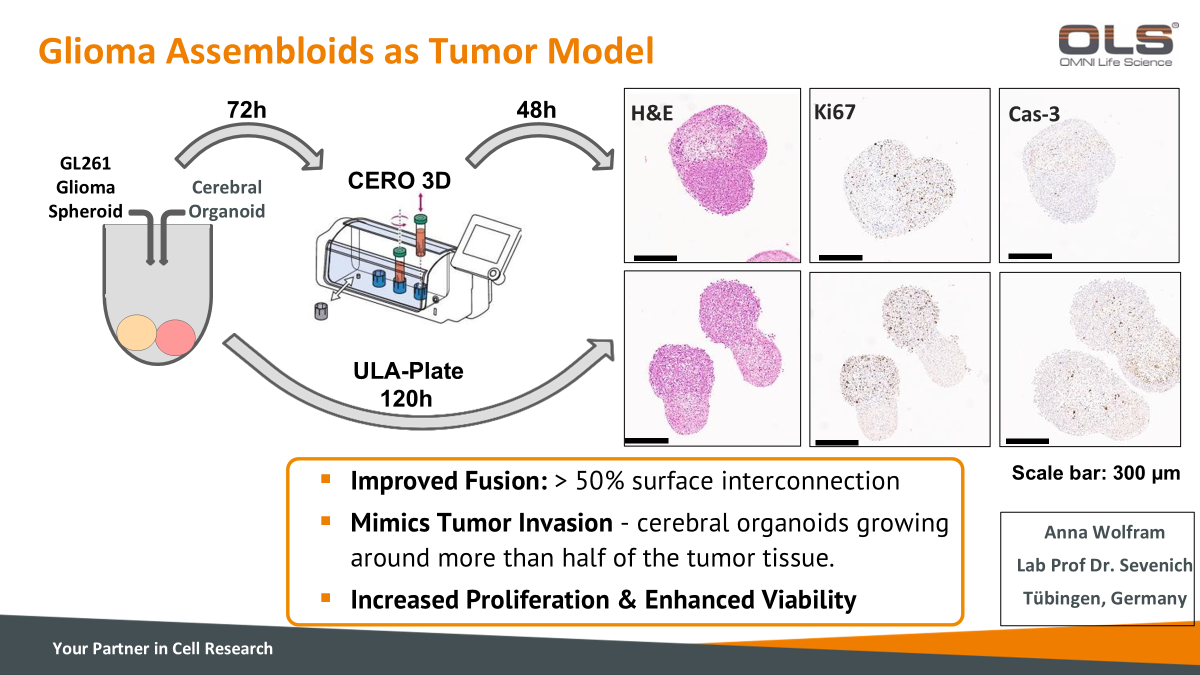 |
|
¶ 第一种方法:步骤:将 GL261 胶质瘤球状体 和 大脑类器官 放在一起,首先共培养72小时。 接着:将培养物转入CERO培养系统继续培养48小时。 这个方法的目的:是通过模拟一个较短时间的相互作用和融合过程,利用CERO培养系统进一步促进细胞之间的交互和融合。CERO系统提供的三维培养环境有助于模拟更复杂的细胞行为,包括肿瘤细胞侵袭和相互作用。 |
¶ 第二种方法:步骤:将 GL261 胶质瘤球状体 和 大脑类器官 一起,直接用低吸附板培养120小时。 这个方法的目的:是在没有中间转移到CERO系统的情况下,通过持续的培养使这两种细胞在较长时间内融合与生长,观察它们在标准环境中的表现。 |
| 第一种方法:72小时的共培养后,再转入CERO培养48小时。这个组合方法展示了GL261 胶质瘤球状体和大脑类器官在CERO系统中的融合效果。您可以观察到,使用CERO系统后,细胞的融合性有显著改善,球状体和类器官之间有更强的表面连接,并且细胞更为均匀,具有更强的增殖能力。 | 第二种方法:直接在低吸附板上培养120小时。相比于第一种方法,这种直接培养方式的细胞表面连接性较弱,细胞形态较为不规则,缺乏明显的表面融合。虽然细胞增殖仍然存在,但没有CERO系统提供的优化条件,细胞形态和增殖速度较低。 |
|
改善融合性:CERO 3D培养组的细胞显示出更强的表面连接性,超过50%的细胞相互融合形成了较为紧密的结构,而低吸附板培养组则显示出较差的融合性。 模拟肿瘤侵袭:CERO 3D培养系统模拟了肿瘤的生长和侵袭,类器官能够更好地围绕肿瘤组织生长,这对于研究肿瘤细胞的侵袭性具有重要意义。 提高增殖与存活:使用CERO 3D培养系统可以显著提高胶质瘤细胞的增殖能力和存活率,减少了细胞凋亡,促进了肿瘤模型的健康生长。 |
|
| 成人干细胞(adult stem cells)源的胃类器官(Gastro Organoids) |
 |
|
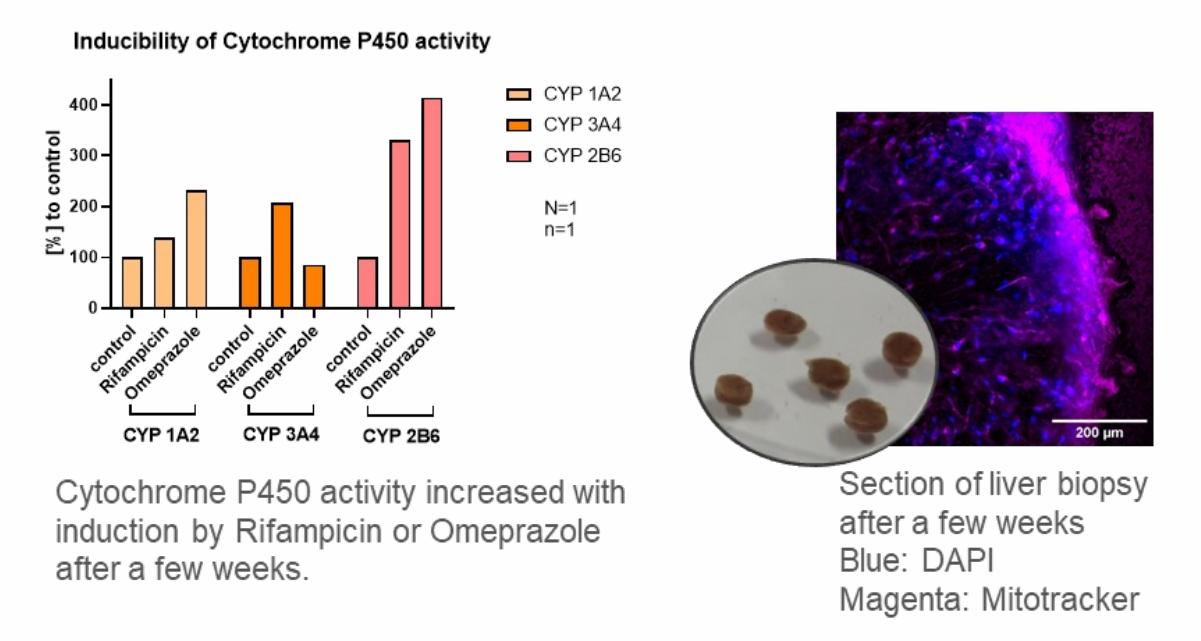
| 器官外植体的成功培养 |
 |
|
培养步骤:
实验对象与应用:
培养条件:
|