¶ Parsortix PR1循环肿瘤细胞分离富集操作
原文件下载地址:https://fb.biokingdom.top/f/19c2307c8af84deeb5e9/
¶ 1.产品概述
Portrait+ CTC染色试剂盒可用于识别上皮和间充质类型的循环肿瘤细胞(CTCs),以及经历上皮-间充质转化(EMT)的肿瘤细胞。EMT是癌细胞中的一个关键转变步骤,与肿瘤进展、耐药性发展和转移密切相关。EMT导致上皮标志物(如EpCAM)的表达丧失、细胞粘附能力丧失,并获得间充质标志物(如波形蛋白)的表达,同时伴随迁移和侵袭能力的增强。有研究表明,处于部分EMT状态的混合表型细胞相比具有明显表型的细胞更具攻击性。
Portrait+ CTC染色试剂盒包含用于免疫荧光染色的试剂和耗材,用于从血液样本中富集的细胞。血液样本必须在使用Portrait+ CTC染色试剂盒前,通过Parsortix®仪器进行处理。性能评估是基于在采集后72至144小时内,使用Streck Cell-Free DNA BCT®收集的样本进行的。Portrait+ CTC染色试剂盒可能与其他血液采集管兼容,例如BD K2-EDTA真空采血管®,但性能需由用户自行验证。
Portrait+ CTC染色试剂盒采用两步法,首先通过细胞离心技术将通过Parsortix仪器采集的细胞群体沉积到CellKeep™载玻片上,然后将附着在载玻片上的细胞与荧光标记的抗体混合物一起染色,用于识别和计数不同表型的细胞。CellKeep载玻片作为染色支撑物,最大限度地保持了通过Parsortix仪器从血液样本中采集的CTCs。
免疫荧光是一种广泛应用于生物样本中特定抗原检测的技术,基于抗体-抗原结合和荧光检测原理。Portrait+ CTC染色试剂盒使用冻干抗体混合物,其中包括一种核染料(Hoechst—在DAPI通道下成像)和针对感兴趣标志物的抗体(具体信息见下文)。抗体混合物中抗体与荧光分子的直接偶联消除了与二级抗体非特异性结合相关的问题,并减少了不必要的孵育/洗涤步骤,从而缩短了处理时间并减少了细胞损失。冻干(冷冻干燥)偶联抗体混合物使其能够长期储存并保持活性。将抗体组合为一种混合物也减少了移液和分装时间,减少了相关错误。
抗体混合物中包含以下标志物面板:
- 上皮面板:包括四种细胞角蛋白,使用Alexa Fluor® 488染料进行检测。(在FITC通道下成像,通常呈绿色)
- 间充质面板:包括波形蛋白及在间充质肿瘤中上调的额外跨膜蛋白,使用Alexa Fluor® 555染料进行检测。(在Cy3通道下成像,通常呈橙色)
- 血液谱系面板:包括CD45等血液细胞标志物,以及淋巴细胞、巨噬细胞、粒细胞、单核细胞、成纤维细胞和具有巨核细胞潜力的细胞所表达的其他抗原,使用Allophycocyanin (APC)进行检测。(在Cy5通道下成像,通常呈红色)
¶ 2. 警告与注意事项
在测试样本之前,请阅读本使用说明书(IFU)的所有内容。在处理血液样本之前,请参阅相关的Parsortix仪器用户指南。材料安全数据表(MSDS)可根据要求提供。
Portrait+ CTC染色试剂盒仅应与以下材料一起使用:
- 通过Parsortix仪器从血液样本中采集的细胞。
- 沉积到CellKeep载玻片上的细胞,且这些细胞需经过丙酮固定。
请注意,基于甲醛的固定液和酸性固定液与Portrait+ CTC染色试剂盒不兼容。
警告:通过Parsortix仪器采集的细胞群体及与这些细胞接触的任何其他材料(如CellKeep载玻片)必须视为可能传播传染性病原体的生物样本。请按照当地法规处理和处置所有危险材料。所有工作应在适当的实验室 containment 级别进行,并使用适当的安全设备。
注意:在处理采集物、本试剂盒及其组件时,务必遵循普遍预防措施和当地实验室的个人防护程序。必要时,佩戴适当的防护设备(如实验服、手套和眼部防护)。
注意:以下行为可能导致结果不准确或不足,应避免:
- 未按照程序操作
- 未按说明存储和处理试剂
- 使用过期试剂
- 使用未校准的设备
注意:请勿使用出现浑浊的试剂,并应立即妥善处置。
注意:抗体混合物和染色载玻片必须尽量避免暴露于光线,尤其是强光(或显微镜光)。所有步骤应尽可能在黑暗环境中进行,或使用防光容器。
请查阅制造商提供的材料安全数据表(MSDS),以了解协议中描述但未在试剂盒中提供的任何化学品。
用户必须根据适用的法规和公司/机构要求接受培训。如需关于Parsortix仪器、CellKeep载玻片或Portrait+ CTC染色试剂盒的具体培训,请联系ANGLE。
必须始终按照本使用说明书(IFU)中的说明使用质量控制载玻片(参见第7.1节)。
¶ 3.操作的局限性
仅供研究使用。不应用于诊断程序。结果不能用于患者管理。
¶ 4.提供的材料
- 1 × 包装说明书
- 10 × CellKeep载玻片
- 1 × CellKeep去附器
- 20 × CellKeep吸液帽
- 1 × Portrait+ CTC染色试剂盒PBS瓶(标有蓝点)
- 1 × Portrait+ CTC染色试剂盒抗体瓶(冻干):足够染色10片载玻片(标有绿点)
¶ 5.材料存储与稳定性
未开封的试剂盒应储存在室温(+18°C - +25°C)下,竖直放置,避免光照和潮湿。
各个试剂盒组件的有效期已标注在标签上。
开封后,重悬缓冲液瓶应储存在室温(+18°C - +25°C)下。抗体瓶重溶后应储存在+4°C(+2°C - +8°C),并在重溶后3个月内使用。
所有组件应始终避免暴露于热源和光源,并在使用后立即恢复到相关存储条件。
注意:CellKeep载玻片和吸液帽是一次性消耗品,仅供一次使用。
¶ 6.所需但未提供的材料
质量控制载玻片
- 去离子水
- 丙酮 ≥99.9%(用于固定前应冰冷(-20°C);至少在使用前一小时放入-20°C冰箱中)
- 胎牛血清(FBS),过滤并热灭活(建议将20 µL FBS分装并储存于-20°C,直到使用)
- 1×磷酸盐缓冲液(PBS)
- 1×氯化钾(KCl)溶液,约3 M(在水中)
- 抗褪色封片液
- 湿式封片密封剂
- Parsortix仪器
- GEN3P6.5RUO Parsortix分离盒
- GEN3C Parsortix清洗盒
- 加热板,温度范围:+37°C(±1°C)
- Fisher Scientific Cytospin™ 4细胞离心机,按配置使用
- CellKeep Cytospin适配器包(ANGLE产品代码CLK-ADT-01)
- 离心机,300–15200 rpm,适用于15 mL Falcon管和细胞处理管
- 微型离心机,最大转速:7000 rpm,适用于1.5 mL Eppendorf管
- 荧光显微镜系统(例如BioView Allegro Plus或同类设备);规格:
- DAPI:λex 380-400 nm,λem 410-480 nm(用于核标记物检测)
- FITC:λex 480-510 nm,λem 515-540 nm(用于上皮标记物检测)
- Cy3:λex 525-555 nm,λem 575-600 nm(用于间充质标记物检测)
- Coplin瓶或等效容器(每片待染色载玻片一个)
- 15 mL Falcon管或等效容器
- 1.5 mL Eppendorf管或等效容器
- 22 mm x 22 mm 方形玻璃盖玻片
- 12 mL 聚苯乙烯尿液分析管
- 细胞处理管(CPT)
- 载玻片染色托盘
- 细胞系:SKBR3(ATCC目录号#HTB-30™)、Hs 578T(ATCC目录号#HTB-126)
所需但未提供的材料应按照相关制造商的说明进行使用和处理。
¶ 7. 操作步骤
注意:确保≥99.9%的丙酮在使用前至少放置在-20°C的冰箱中一小时。这将用于细胞固定;每片载玻片需要50 µL。
¶ 7.1 质量控制载玻片的制备
质量控制载玻片通过使用细胞处理管(CPT)制备,获得外周血单核细胞(PBMC)和红细胞(RBC)的悬液,并添加培养的SKBR3和Hs 578T癌细胞。
¶ 7.1.1 从CPT制备PBMC/RBC悬液
- 按照制造商的说明,从健康志愿者采集血液至CPT管(4 mL或8 mL)。
- 将样本倒置八(8)次以重新整合血浆。
- 打开CPT管,取20 µL血液转移至Eppendorf管中,并为后续使用保留。
- 紧闭CPT管盖,在室温下以1800 × 重力加速度(g)离心15分钟,离心刹车设置为9。
- 离心后,倒置CPT管八(8)次以混合PBMC与血浆。
- 将PBMC和血浆倒入15 mL Falcon管中,并以300 × g离心5分钟,离心刹车设置为9。
- 可以看到少量的PBMC的灰白色沉淀。去除上清液,保留沉淀。
- 倒置含沉淀的管子,轻轻将管边在一次性擦拭纸上擦拭,以去除剩余的上清液。
- 根据表1添加适量的PBS和全血到沉淀中,重新悬浮,制备PBMC/RBC悬液。
| CPT体积 | PBS体积(用于重悬) | 全血体积 |
| 4 mL | 600 µL | 6 µL |
| 8 mL | 1200 µL | 12 µL |
| 表1:CPT悬液的PBS和全血添加量 | ||
¶ 7.1.2 癌细胞稀释液的制备
- 获取未标记的、活的SKBR3和Hs 578T细胞系稀释液。
- 确定细胞稀释液的浓度,并将每种细胞稀释至100个细胞/µL。
¶ 7.1.3 质量控制样本的制备(建议每批染色制备一个)
- 根据表2中的体积,将PBS、制备好的PBMC/RBC悬液以及稀释后的SKBR3和Hs 578T细胞加入到1.5 mL低结合Eppendorf管中。
| PBS(µL) | 205 |
| PBMC/RBC悬液(µL) | 1 |
| SKBR3稀释液 (100 细胞/µL) | 2 |
| Hs 578T稀释液 (100 细胞/µL) | 2 |
| 最终体积(µL) | 210 |
| 表2:单个质量控制样本的制备 | |
¶ 7.2 样本采集与CellKeep载玻片的制备
¶ 7.2.1 制备干燥缓冲液
- 从冰箱/冰柜中取出所需体积的无菌、热灭活的FBS(每片载玻片需要20 µL),提前一小时使其达到室温(+18°C - +25°C)。
- 使用表3中的试剂和体积制备干燥缓冲液。
| 试剂 | 每片载玻片 (µL) | 2片载玻片 (µL) | 10片载玻片 (µL) |
|---|
| 3M KCl | 5 | 10 | 50 |
| 去离子水 (diH2O) | 175 | 350 | 1750 |
| FBS | 20 | 40 | 200 |
| 总计 | 200 | 400 | 2000 |
| 表3:干燥缓冲液的组成和体积 | |||
¶ 7.2.2 CellKeep载玻片的制备
准备固定液:将≥99.9%的丙酮放入-20°C冰箱中至少一小时,用于细胞固定(每片载玻片需要50 µL)。
准备载玻片:取下CellKeep载玻片漏斗的盖子。
采集Parsortix样本:
- 从Parsortix分离盒中直接采集细胞至CellKeep漏斗中。
- 操作时,将Parsortix采集管靠近漏斗内壁,使样本沿漏斗壁缓慢流下(见图1)。

对于对照样本的制备:
- 使用移液器,将整个对照样本(210 µL)轻轻加入CellKeep漏斗中,使样本沿漏斗内壁缓慢流下。
注意事项:
- 切勿让采集管或移液器吸头接触显微镜载玻片上的样本区域。
- 固定漏斗盖:将CellKeep载玻片漏斗的盖子重新拧紧。
注意:在取下或重新安装漏斗盖或吸液帽时,应平稳握住漏斗底部,以防漏斗过早脱落(见图2)。

- 将CellKeep载玻片放入CellKeep Cytospin适配器中。适配器具有上部和下部的支架,用于固定CellKeep载玻片(见图3)。

- 插入载玻片:将CellKeep载玻片的顶部(带注释标签的一侧)首先插入CellKeep Cytospin适配器的上部支架中(见图4a)。
- 固定载玻片:轻轻将CellKeep载玻片平放到CellKeep Cytospin适配器中,并从顶部边缘施压,使载玻片固定在下部支架下方(见图4b)。

|

|
按压CellKeep Cytospin适配器的侧臂,将其插入Cytospin 4离心机的一个槽位中。确保漏斗朝向转子中心,下部支架朝下。将侧臂对齐转子板上的槽位,然后轻轻将适配器下放至槽中。适配器到达槽底时,松开侧臂,使其牢固锁定在槽位内(见图5a至5d)。

|

|

|

|
重要提示:确保根据离心的CellKeep载玻片数量对Cytospin 4进行适当平衡调整。
离心设置:
- 加速度:低速
- 转速:2000 RPM
- 时间:5分钟
按下“Start”键启动离心。
完成后操作:
- 按压侧臂以解锁组件(逆向操作见图5a、5b),从槽位中取出CellKeep Cytospin适配器。
- 从适配器中取出CellKeep载玻片。
- 取下CellKeep载玻片漏斗盖,旋上CellKeep吸液帽(见图6a、6b)。

|

|
吸液帽操作:将吸液帽放置五分钟,以吸收液体。
注意:吸液帽的效率可能略有差异,吸收所有液体所需的时间可能有所不同。
移除吸液帽:液体全部被吸收后,取下吸液帽并丢弃。
添加干燥缓冲液:轻轻移液200 µL干燥缓冲液到漏斗中,使缓冲液沿漏斗内壁流下(见图7)。
注意:
- 切勿直接将缓冲液移液到样本区域,以免细胞被冲走。
- 切勿用移液器吸头接触样本区域。

重新安装盖子和适配器:将盖子重新拧紧到CellKeep载玻片漏斗上,并将CellKeep Cytospin适配器重新装入Cytospin 4(参考图4a、4b和图5a至5d)。
离心设置:将Cytospin 4设置为与第一次离心相同的参数:
- 加速度:低速
- 转速:2000 RPM
- 时间:5分钟
按下“Start”键启动离心。
完成后操作:
- 从CellKeep Cytospin适配器中取出CellKeep载玻片。
- 取下CellKeep载玻片漏斗盖,旋上第二个CellKeep吸液帽(参考图6a、6b)。
等待吸液:等待五分钟,让第二个吸液帽吸收液体。
移除吸液帽:取下并丢弃第二个吸液帽,将盖子重新拧回到CellKeep载玻片漏斗上。
插入载玻片分离器:将CellKeep载玻片插入载玻片分离器中(见图8a、8b)。

|

|
- 移除漏斗:用一只手固定载玻片分离器,另一只手拉出CellKeep载玻片上的漏斗(见图9a、9b)。

|

|
- 移除玻璃载玻片:从下部塑料外壳中取出显微镜玻璃载玻片(见图10a、10b)。
注意:请勿移除载玻片上的硅胶垫圈,也不要触碰样本区域。
- 加热干燥:将显微镜玻璃载玻片放置在设定为37°C的加热板上,静置一小时。
注意:如果加热板配有盖子,请勿合上盖子,否则会妨碍显微镜玻璃载玻片的干燥。
 |
 |
| 图10a,b:从下部塑料外壳中取出显微镜玻璃载玻片。 | |
转移载玻片:取下干燥的显微镜玻璃载玻片,放置在载玻片染色托盘上。
固定细胞:用移液器将50 µL冰冷的丙酮逐滴滴加到样本区域。
冷冻处理:将载玻片置于-20°C冰箱中冷冻5分钟以固定细胞。
干燥载玻片:从冰箱中取出载玻片。如果样本区域仍有残余丙酮,可轻轻在吸水纸上晃动载玻片,然后在室温下干燥约10分钟。
注意:请勿移除载玻片上的硅胶垫圈。
储存载玻片:载玻片可在染色前存储于-20°C,最多保存一个月。
¶ 7.3 冻干抗体配方的重溶
配制1× PBS Casein溶液:在含有100 µL 5× PBS Casein的试剂瓶中加入400 µL去离子水,立即配制出1× PBS Casein溶液。
注意:运输过程中,液体可能积聚在瓶盖内。在打开前,使用微型离心机对试剂瓶进行短暂离心以排出盖内的液滴。
重溶抗体配方:缓慢向抗体配方试剂瓶中加入330 µL 1× PBS Casein溶液以进行重溶。
丢弃剩余的1× PBS Casein溶液。
悬浮:静置1分钟后,轻轻上下移液以充分悬浮内容物。
检查是否完全溶解:如果仍有固体物质可见,则再静置1分钟并重复悬浮步骤。
储存抗体配方:在染色载玻片后,如有剩余的重溶抗体配方,将其储存于+4°C(+2°C – +8°C),并在3个月内使用完毕。
¶ 7.4 CellKeep载玻片的免疫荧光染色
注意:在使用前,确保抗褪色封片液已在实验台上静置至少1小时,使其达到室温。
重水化载玻片:
- 用移液器将100 µL 1× PBS缓慢逐滴滴加到载玻片的样本区域上。
- 在室温下孵育20分钟。
准备抗体混合液:
- 在每批载玻片染色前,重新悬浮抗体混合液,并将试剂瓶置于微型离心机中,以7000 rpm在室温下离心5分钟。
- 注意:如果微型离心机的转子槽不适配试剂瓶,可将抗体混合液倒入1.5 mL Eppendorf管中再进行离心。
去除多余液体:
- 轻轻晃动载玻片,使其在吸水纸上滴干,去除所有多余液体。
添加抗体混合液:
- 不需重新悬浮抗体混合液,从溶液顶部吸取,使用移液器将30 µL重溶的抗体混合液滴加到载玻片上的圆形样本区域。
注意:请勿触碰载玻片表面。
孵育:将载玻片置于黑暗环境中,在室温下孵育45分钟。
准备洗涤溶液:在孵育期间,为每片染色载玻片准备一个Coplin瓶,填充1× PBS溶液。
移除多余液体:孵育完成后,轻轻晃动载玻片,使其在吸水纸上滴干,去除多余液体。
洗涤载玻片:
- 将载玻片轻轻浸入已填充PBS的Coplin瓶中,重复三次。
- 每片载玻片使用单独的Coplin瓶以避免交叉污染。
再次去除多余液体:轻轻晃动载玻片,使其在吸水纸上滴干。
移除硅胶垫圈:用镊子夹住硅胶垫圈,向上拉起并远离载玻片表面进行移除(见图11)。

注意:请勿触碰样本区域。
去除多余水分:使用干净的实验室擦拭纸轻轻接触载玻片边缘,吸去剩余的多余水分。
添加封片液:用移液器在载玻片顶部滴加10 µL封片液。
覆盖盖玻片:小心地将盖玻片放置在封片液上方。
- 先让盖玻片的一侧边缘接触CellKeep载玻片,再轻轻压下另一侧,以避免空气泡困在样本区域。
- 如有气泡,缓慢将其挤到样本区域的边缘。
固化:将载玻片置于黑暗环境中,在室温下固化30分钟。
密封盖玻片:用小刷子将少量湿式封片密封剂涂抹在盖玻片的每个边缘,确保密封剂覆盖盖玻片的边缘并与CellKeep载玻片重叠(见图12)。

干燥载玻片:将载玻片置于室温环境中避光干燥30分钟。
存储:干燥后,将载玻片放入载玻片收纳册中,储存于+4°C(+2°C – +8°C)环境下,至少保存8小时后方可进行成像。
成像时间:载玻片应在染色后72小时内完成成像。
¶ 8. 成像与结果解释
¶ 8.1 载玻片的适用性评估
使用低倍物镜观察:
- 选择10×低倍物镜和规定的滤光片,对样本区域进行观察。
评估标准:
- 核清晰度:所有细胞核(DAPI信号)应清晰可见,且彼此不重叠。
- 核分布:细胞核应在样本区域内均匀分布,且不应有大面积无细胞的空白区域。
- 阳性信号:阳性荧光信号应明亮、清晰且易于评估。
- 背景质量:背景应为暗色,并且相对无荧光模糊现象。
注意事项:
- 如果观察结果不符合以上标准,请参考故障排除(第11节)进行问题诊断和解决。
¶ 8.2 对照载玻片的成像与结果解释
对照载玻片的重要性:
- 荧光显微镜和相关成像软件的性能可能存在差异。与供体样本载玻片同时染色的对照载玻片必须用于确定每个供体样本的曝光/增益设置,以确保结果的高灵敏度和高特异性。
成像准备:
- 使用10×低倍物镜和DAPI滤光片,调整焦深,熟悉对照样本中PBMC和掺入的癌细胞(SKBR3和Hs 578T)的形态特征。
细胞特征:
- 肿瘤细胞:通常比PBMC体积更大。
- 避免干扰区域:避免观察坏死区域以及充满大量碎屑/纤维的区域。
选择合适的观察区域:
- 选择一个核分布良好、包含PBMC、SKBR3和Hs 578T细胞的样本区域(如可能)。
调整成像设置:
- 根据需要在不同通道之间切换,按照以下建议调整每个通道的成像强度,以确保荧光信号的最佳显示和评估。
注意:在成像过程中,确保对照样本的观测结果用于验证供体样本的成像参数和结果解释的可靠性。
¶ 8.2.1 FITC通道调整(上皮标志物)
调整曝光/增益设置:
- 在FITC通道中,调整曝光和增益设置,使对照载玻片上的SKBR3细胞清晰可见。
- 至少80%的SKBR3细胞应显示与图13中图片1至7相当的FITC信号强度。
评估信号强度:
- 大多数SKBR3细胞的信号强度应类似于图13中图片2至4中的细胞。
信号阴性判定:
- FITC信号强度低于图13中图片8的细胞应被视为上皮(FITC)阴性。
注意:此步骤确保了上皮标志物信号的准确性,并提供了参考标准以判定阳性和阴性细胞。
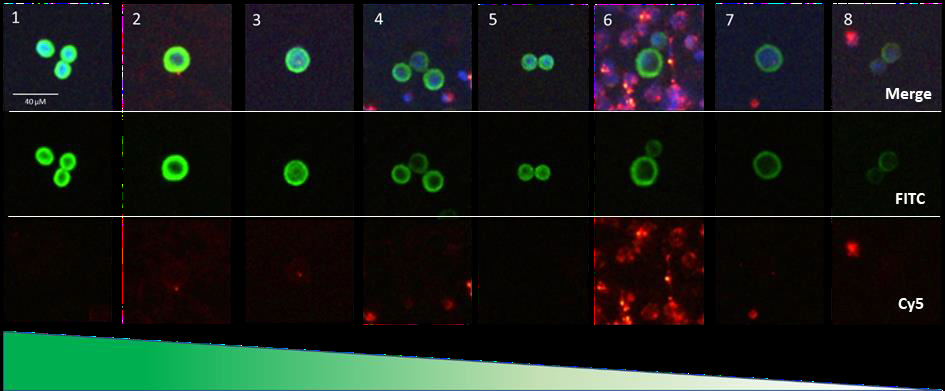
8.2.2 Cy3通道调整(间充质标志物)
调整曝光/增益设置:
- 在Cy3通道中,调整曝光和增益设置,使对照载玻片上的Hs 578T细胞清晰可见。
- 至少80%的Hs 578T细胞应显示与图14中图片1至7相当的Cy3信号强度。
评估信号强度:
- 大多数Hs 578T细胞的信号强度应类似于图14中图片2至4中的细胞。
信号阴性判定:
- Cy3信号强度低于图14中图片8的细胞应被视为间充质(Cy3)阴性。

¶ 8.2.3 Cy5通道调整(血液谱系标志物)
调整曝光设置:
- 在Cy5通道中,调整曝光参数,使血细胞清晰可见并显示一致的明亮信号,同时大多数癌细胞(如SKBR3和Hs 578T)不应显示Cy5信号。
- 参考图13和图14,确保信号分布符合预期。
注意事项:
- Cy5信号不在可见光波长范围内,需要通过显微镜相机观察,而非目镜。
¶ 8.2.4 预期结果
对照载玻片染色的充分性:
- 染色对照载玻片被认为是充分的。
SKBR3细胞预期表现:
- 大多数SKBR3细胞应具有核(DAPI+)、FITC+(上皮标志物阳性)且Cy5-(血液谱系标志物阴性)的特征。
Hs 578T细胞预期表现:
- 大多数Hs 578T细胞应具有核(DAPI+)、Cy3+(间充质标志物阳性)且Cy5-(血液谱系标志物阴性)的特征。
通过上述标准,可以验证染色和成像参数是否适合进一步分析样本。
¶ 8.3 供体样本成像与结果解释
¶ 8.3.1 概述
注意:在定位感兴趣细胞时,应使用10×低倍物镜。但在对供体样本进行成像时,使用高倍物镜可以更清晰地观察细胞细节。
通过该检测方法识别的细胞可表型分类为以下循环肿瘤细胞(CTC)类别:
- 上皮型CTC:DAPI+,FITC+,Cy3-,Cy5-
- 间充质型CTC:DAPI+,FITC-,Cy3+,Cy5-
- EMT型CTC(上皮-间充质转化):DAPI+,FITC+,Cy3+,Cy5-
尽管不同组别的染色模式和信号强度存在差异,它们共享以下典型形态特征:
- 形状多样:包括圆形、椭圆形、延长形及细胞簇。间充质型CTC通常呈现更延长的形态,但三种CTC表型均可观察到各种形状。
- 尺寸特征:CTC通常比白细胞更大,但与培养的癌细胞相比,CTC的体积明显更小。
- 排除标准:直径小于10 μm的细胞不应被视为CTC。
注意事项:该标准仅适用于单个CTC。在CTC簇中,无法准确测量单个细胞的尺寸。
细胞核特征:CTC始终具有核结构。尽管CTC的核形态可能有所不同,但其核通常表现为染色质浓缩(更明亮的DAPI信号),而白细胞的核则显得较为弥散。使用保存细胞(如Streck Cell-Free DNA BCTs)可减少这一差异,因为固定后的细胞核更清晰可见。
多核CTC的稀有性:多核CTC很少见。一般认为,癌细胞的核质比(核体积与细胞质体积的比例)较高。这一点不应与细胞质非常少的细胞混淆,后者是未成熟PBMC的典型特征(详见第8.4节)。
Cy5阴性:CTC在Cy5通道中为阴性,除了在较大的CTC-PBMC簇中可能观察到的残留染色信号。
¶ 8.3.2 上皮型CTC
FITC信号特征:
- 在上皮型CTC中,上皮标志物的染色(FITC)通常呈环状分布。
信号强度的变化:
- 相同供体中的CTC以及不同供体之间的FITC信号强度可能会有所差异。
阳性信号的判定:
- 无论强度如何,阳性信号应明显比PBMC中的背景信号更亮。PBMC由于细胞器含有多种能被488 nm激光激发的化合物,会在FITC范围内产生自发荧光(见图15)。
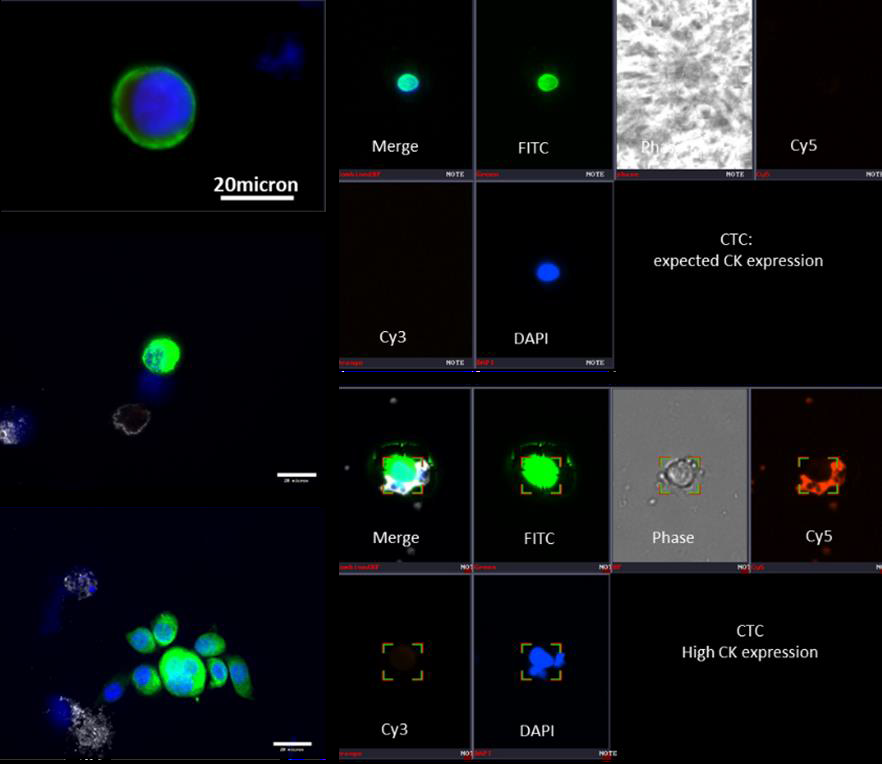 图15:上皮型CTC的代表性图像 左侧: 右侧: 显微镜系统:
合并图像颜色:
|
¶ 8.3.3 间充质型CTC
信号定位:
- 在间充质型CTC中,间充质标志物的信号主要分布于细胞质和细胞骨架中。
细胞质较少的细胞:
- 对于细胞质较少的细胞,应谨慎评估(详见第8.4节)。
信号强度的变化:
- 相同供体的CTC以及不同供体之间,间充质标志物的表达强度可能存在差异。
PBMC的影响:
- PBMC可能表达波形蛋白(Vimentin),因此在评估间充质信号分布时需要特别注意,同时核查Cy5信号的存在情况(见图16)。
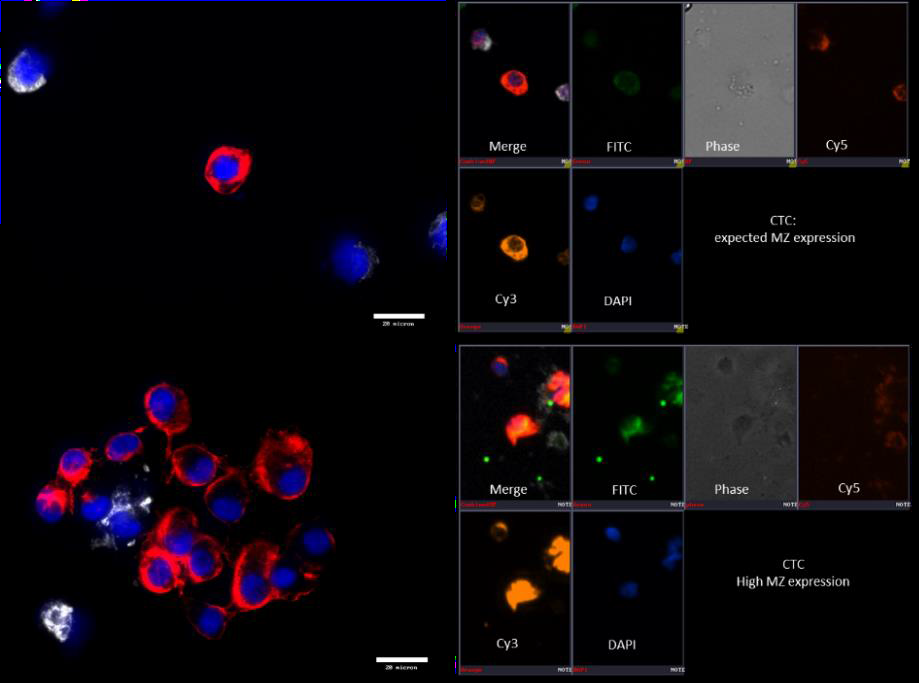 图16:间充质型CTC的代表性图像 左侧: 右侧: 显微镜系统:
合并图像颜色:
|
¶ 8.4 类似CTC的细胞
有两种细胞可能被误判为CTC:
- 间充质阳性且血液谱系标志物阴性的PBMC。
- 巨核细胞及其前体细胞。
¶ 8.4.1 间充质阳性CTC样细胞
波形蛋白(Vimentin)是间充质染色面板中的标志物之一,但PBMC也可表达波形蛋白。因此,基于Cy5信号的阴性选择对于准确的CTC分类至关重要。然而,在使用Streck Cell-Free DNA BCTs的健康志愿者样本中,观察到部分波形蛋白阳性但血液谱系标志物阴性的细胞。通过以下形态特征可以帮助区分和排除这些细胞(见图17):
- 直径:10-15微米,形状呈椭圆或圆形。
- Cy5信号:缺失或呈点状分布。
- FITC信号:缺失。
- Cy3信号:低阳性(信号强度较低),且集中在细胞骨架中呈尖峰状分布。
- 核与细胞质:核较大,几乎完全缺少细胞质。
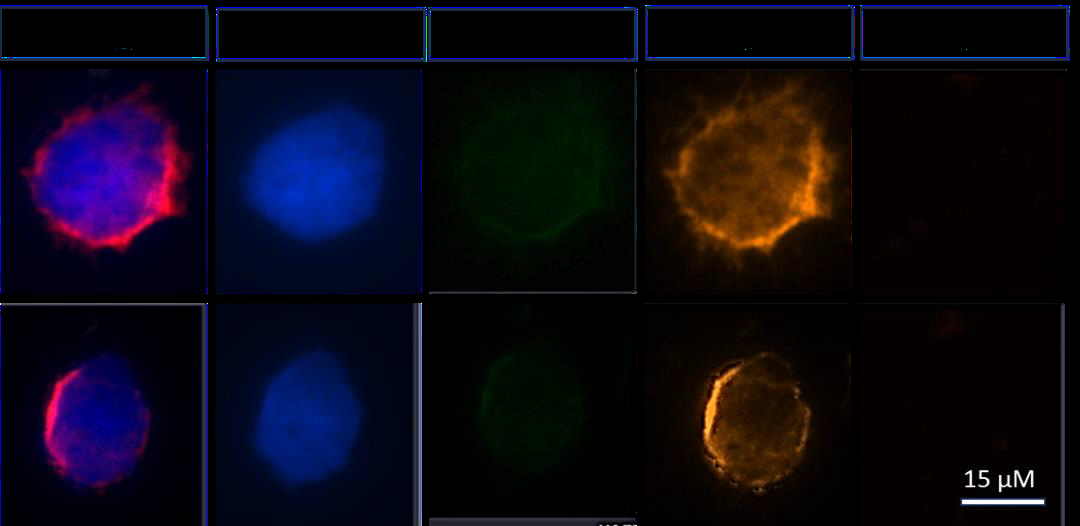 图17:间充质阳性类似CTC细胞的代表性图像 描述: 成像系统:
合并图像颜色:
|
¶ 8.4.2 巨核细胞
巨核细胞是具有核的大型细胞,其上皮信号较低。它们的直径变化较大,通常在20-80微米之间。大约80%的巨核细胞会表达血液谱系标志物,因此不会被识别或计数为CTC。剩余的20%可以通过以下形态学特征与CTC区分:
形态特征:
- 巨核细胞通常具有较大的细胞核,而细胞质极少。
- 上皮信号较低或呈弥散分布,并集中于细胞核,与典型CTC的上皮标志物定位不同。CTC的上皮标志物通常定位于细胞骨架,在细胞核周围呈环状分布(如图15所述)。
图像参考:
- 巨核细胞的代表性图像展示了这些细胞的典型形态和荧光信号分布(见图18)。
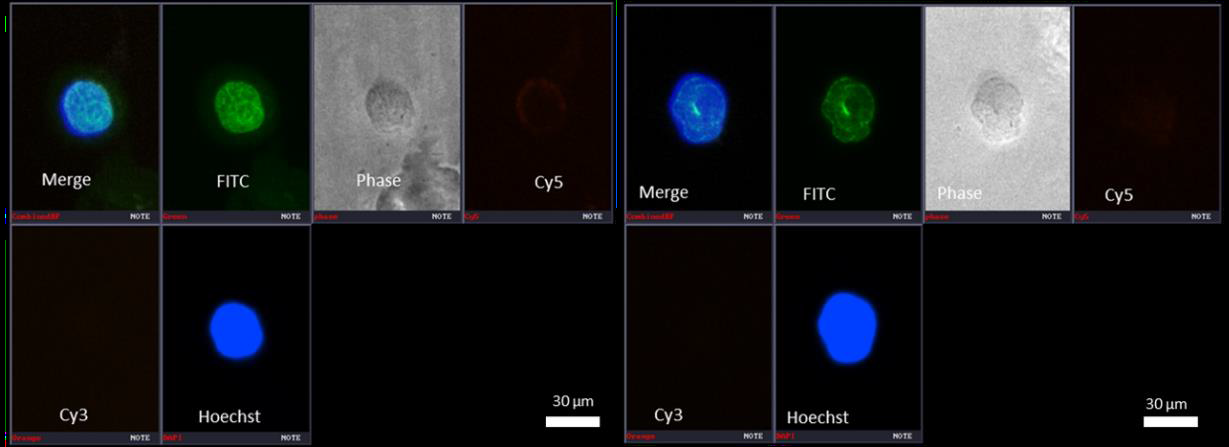 图18:巨核细胞的代表性图像 描述: 成像系统:
合并图像颜色:
|
¶ 9. 质量控制
对照载玻片必须与供体样本载玻片同时染色,以评估染色性能并设置用于CTC识别和计数的成像参数。
制备要求:
对照样本和载玻片的制备方法详见第7.1节和第7.2节。
评估要求:
按照第8.2节中描述的方法对载玻片进行评估,并确保满足第8.1节中列出的载玻片适用性标准。
处理异常情况:
如果评估结果未满足标准,则不得报告实验结果,应参考第11节 故障排除,以确定并解决问题。
¶ 10. 干扰物质
以下物质已在用于制备采集样本的血液中进行测试,结果表明它们不会影响使用Portrait+ CTC染色试剂盒的抗体染色质量和适用性:
血细胞比容异常:
- 女性血液中血细胞比容高达60%或低至25%。
- 男性血液中血细胞比容高达65%或低至30%。
高白蛋白水平:60 mg/mL
高甘油三酯水平:5 mg/mL
不兼容物质:
基于甲醛的固定液和酸性固定液与Portrait+ CTC染色试剂盒不兼容。
¶ 11. 故障排除
¶ 11.1 吸液作用受阻
| 可能原因 | 解决措施 |
|---|
| 吸液帽存储不当 | 确保吸液帽存储在阴凉干燥的地方,并在使用前不要从包装中取出。 |
| 吸液帽位置不正确 | 确保吸液帽完全拧紧到漏斗组件上,并避免发生螺纹交错。 |
| 气泡阻塞吸液帽进液口 | 从漏斗上取下吸液帽后重新安装,以清除气泡。 |
¶ 11.2 信号弱或无信号
| 可能原因 | 解决措施 |
| 载玻片上细胞数量少或无 | 确保按照Parsortix仪器的说明书(IFU)正确执行CTC捕获操作。 |
| 确保CTC采集过程符合本IFU的要求。 | |
| 确保样本区域未被触碰、擦拭或刮伤。 | |
| 确保载玻片的处理和操作均符合本IFU要求。 | |
| 抗体未按IFU正确重溶 | 确保抗体混合物使用试剂盒提供的稀释液按正确体积进行重溶。 |
| 确保抗体混合瓶中无可见的残留粉末。 | |
| 样本固定不当 | 确保按本IFU的描述,使用正确的固定试剂、体积和孵育时间/温度对载玻片进行固定。 |
| 成像不正确 | 确保显微镜上配备正确的成像滤光片。 |
| 在扫描之前,确保通过对照样本设置曝光/增益参数。 |
¶ 11.3 核重叠或细胞分布不均
| 可能原因 | 解决措施 |
|---|
| 血液存储不当 | 确保血液存储在推荐的温度范围内(+18°C 至 +25°C),且存储时间不得短于或长于推荐的时间。 |
| 离心操作不当 | 确保按照本说明书(IFU)的要求处理和制备载玻片。 |
¶ 11.4 染色不均
| 可能原因 | 解决措施 |
|---|---|
| 样本区域未被抗体混合液均匀覆盖 | 确保样本区域均匀覆盖抗体混合液,且无气泡存在。 |
¶ 11.5 细胞形态受损
| 可能原因 | 解决措施 |
|---|---|
| 血液存储不当 | 确保血液存储在推荐的温度范围内(+18°C 至 +25°C),且存储时间不得短于或长于推荐的时间。 |
| 样本固定不正确 | 确保按照本说明书(IFU)的要求,使用正确的试剂、体积以及孵育时间和温度对载玻片进行固定。 |
| 离心操作不当 | 确保按照本说明书(IFU)的要求正确处理和制备载玻片。 |
¶ 11.6 非特异性信号或背景噪声过高
| 可能原因 | 解决措施 |
|---|---|
| 冻干抗体混合液未完全重溶 | 确保冻干抗体混合物在重溶前正确沉积在试剂瓶底部。如果重溶后仍可见残余物,静置额外1分钟后使用移液器重新悬浮。 |
| 重溶后未进行离心或染色前未离心 | 按照IFU要求对重溶的抗体混合物进行离心,确保离心后试剂瓶内有沉淀,并在移液时避免扰动沉淀。切勿在离心后重新悬浮抗体混合物。 |
| 载玻片安装不正确或封片介质固化不良 | 确保使用10μL封片液安装载玻片,且在放置盖玻片时避免施加过大压力。 |
| 确保没有空气泡被困在样本中,并在盖玻片边缘正确涂抹密封剂。 | |
| 确保封片液在成像前已完全固化。 | |
| 洗涤技术不正确 | 确保样本区域完全浸没在1× PBS中并重复洗涤三次。 |
| 成像设置不正确 | 在扫描前,通过对照样本设置正确的曝光/增益参数。 |
| 干燥缓冲液制备/使用不当 | 确保按正确浓度比例配制干燥缓冲液(KCl和FBS)。 |
| 确保吸液后载玻片上剩余的干燥缓冲液最少,避免过多残留影响染色效果。 |
¶ 11.7 载玻片上细胞少或无细胞,细胞漂浮在载玻片上
| 可能原因 | 解决措施 |
|---|---|
| 载玻片安装不正确,封片介质固化不良 | 确保使用10 µL封片液正确安装载玻片,并放置盖玻片时避免施加过大压力。 |
| 确保没有空气泡被困在样本中,并在盖玻片边缘涂抹密封剂。 | |
| 确保封片液在成像前已完全固化。 | |
| 干燥缓冲液制备或使用不当 | 确保按正确浓度配制干燥缓冲液(包括KCl和FBS)。 |
| 确保吸液后载玻片上残余干燥缓冲液最少,以免影响染色效果和细胞附着。 | |
| 样本固定不正确 | 确保按照IFU中的要求,使用正确的试剂、体积和孵育时间/温度对载玻片进行固定。 |
| 离心操作不当 | 确保按照IFU中的步骤正确制备载玻片,避免因离心不足或过度导致细胞漂浮或流失。 |
| 样本采集不正确 | 按照Parsortix仪器IFU的要求正确执行CTC捕获操作。 |
| 按照本IFU的要求正确进行CTC采集。 | |
| 载玻片操作不当 | 确保样本区域未被触碰、擦拭或刮擦。 |
| 按照IFU的要求正确处理载玻片,避免操作不当影响细胞的分布和附着。 |