¶ CERO微流控3D肠道肿瘤模型应用于纳米药物递送
2021年Linda Elberskirch等人于“Journal of Drug Delivery Science and Technology”发表了一篇微流控3D肠道肿瘤模型用于纳米药物的研究的论文。
在肠道肿瘤的治疗中,纳米颗粒药物递送系统为提升药物靶向性和治疗效果带来了新希望。然而,肠道的黏液层既是药物的障碍,也可能成为药物靶点。传统的二维细胞模型难以模拟纳米颗粒在复杂肠道环境中的行为,因此,科学家们迫切需要更真实的体外模型来模拟体内条件!! !
那么此刻“CERO 3D细胞类器官培养系统”,这款科研利器便发挥了极大的助力。CERO系统通过旋转培养方式生成了具有微绒毛和粘液层的3D肠道肿瘤球体,模拟了体内环境,提高了研究的生理相关性,为纳米颗粒药物递送的研究提供了一个更接近真实肠道肿瘤的体外模型。
紧接着这个肿瘤的体外模型参与了微流控3D肠道肿瘤模型的制备:
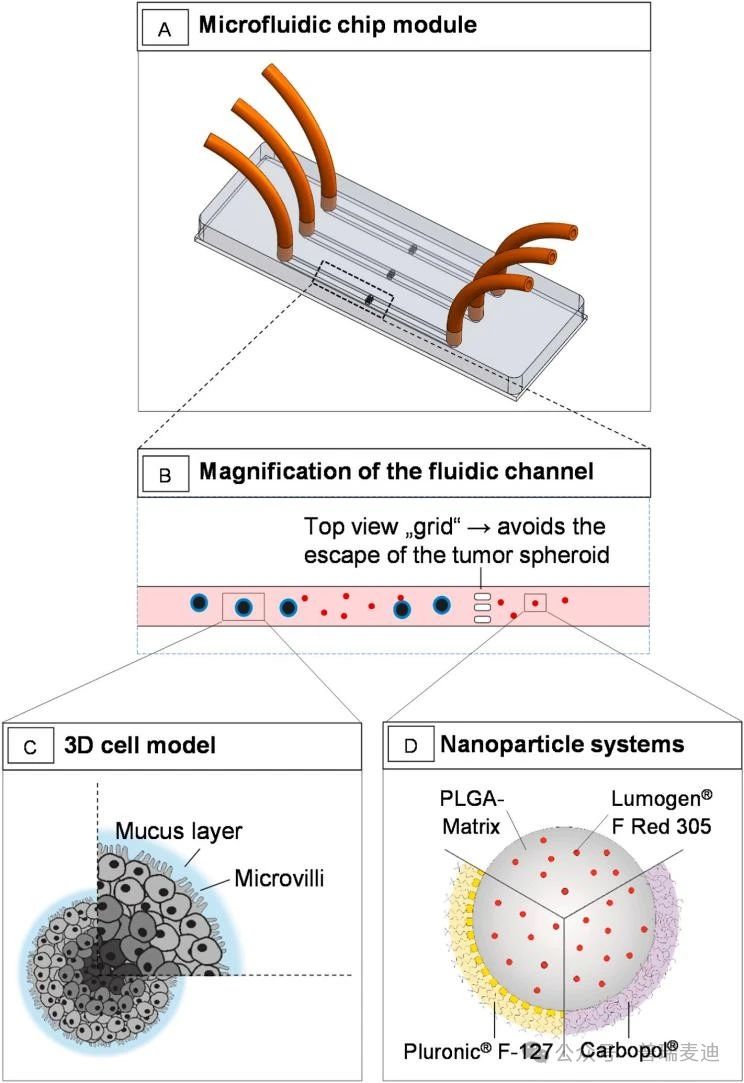
¶ 为什么微流控3D模型如此重要?
研究者们引入了三维肿瘤球体模型。相比二维模型,三维肿瘤球体能更好地模拟体内肿瘤的结构。CERO系统通过旋转培养方式促进了HT29-MTX-E12细胞形成3D肿瘤球体。
¶ CERO培养出3D肿瘤球
Corning球体微板培养5天培养出球体;
球体被转到CERO培养管中,并在CERO系统中进行旋转培养产生肿瘤球。
这些球体模拟了肠道肿瘤的微观结构,包括活性外层细胞、中间层的静止细胞和坏死核心。
在CERO系统中,3D肿瘤球体表面能够形成微绒毛和粘液层,这些特征对于模拟肠道肿瘤的自然环境至关重要。微绒毛和粘液层的存在对于研究纳米颗粒的吸附和渗透能力非常重要,因为它们是肠道肿瘤表面的重要组成部分。
为了进一步提高模型的真实度和实验效率,研究人员通过微流控技术设计了一个动态流体环境。该系统不仅能够模拟肠道的流体流动和蠕动运动,还能帮助研究人员评估纳米颗粒在流体剪切力作用下的停留时间和渗透能力。那么与动态流体环境与之对应的是静态环境。
¶ 动静处理两者的区别是
¶ 静态处理
在第十天,将五个球体一批转移到24孔细胞悬浮多孔板中,并在静态条件下培养两天,直到它们形成了一个坏死核心。
在静态条件下,将纳米颗粒或自由Lumogen® F Red 305化合物稀释在培养基中,与球体一起孵育3小时。
¶ 动态处理
球体被放置在微流控芯片系统中,并通过蠕动泵以100微升/分钟的速度循环培养基。
培养基中的纳米颗粒或自由Lumogen® F Red 305化合物在流动条件下与球体接触,模拟了体内的流体剪切力。
¶ 总结
静态处理提供了一个无流体流动的环境,而动态处理则模拟了体内的流体动力学条件,包括流体剪切力和流动对药物递送系统的影响。动态处理因此更能反映药物在实际体内的分布和作用,有助于提高体外实验与体内实验结果的一致性。