¶ 《科学进展》Science Advances| 研究论文
¶ 冠状病毒
¶ 唐氏综合征脑类器官中的脉络丛缺陷增强SARS-CoV-2的嗜神经性
穆罕默德·R·沙克尔1,2†*、安德里·斯隆查克3†、巴哈·阿尔姆哈纳维1、肖恩·D·莫里森1、 朱利安·D·J·森格3、贾斯汀·库珀-怀特1,2,4、亚历山大·A·赫罗米赫3,5‡、恩斯特·J·沃尔维唐1,2‡*
1 澳大利亚昆士兰大学生物工程与纳米技术研究所,布里斯班,昆士兰州 4072,澳大利亚。
2 昆士兰大学干细胞工程与再生工程中心(UQ StemcARe),昆士兰大学,昆士兰大学干细胞与再生工程卓越中心(UQ StemcARe),澳大利亚昆士兰州布里斯班市,邮编4072。
3 昆士兰大学化学与分子生物科学学院,澳大利亚昆士兰州布里斯班市圣露西亚校区,邮编4072。
4 昆士兰大学化学工程学院,澳大利亚昆士兰州布里斯班市,邮编4072。
5 澳大利亚传染病研究中心卓越中心(5Gvn卓越中心),澳大利亚昆士兰州布里斯班市。
*通讯作者。电子邮箱:m.shaker@uq.edu.au(M.R.S.); 5Gvn卓越研究中心,澳大利亚传染病研究中心,布里斯班,昆士兰州,澳大利亚。
*通讯作者。邮箱:m.shaker@uq.edu.au (M.R.S.);e.wolvetang@uq.edu.au (e.J.W.)
†这些作者对本工作贡献相同。
‡这些作者对本工作贡献相同。
唐氏综合征(DS)个体为何对SARS-CoV-2诱导的神经病理更易感,其机制尚未明确。脉络丛(ChP)在屏障功能和免疫调节中起关键作用,并表达ACE2受体及染色体21编码的TMPRSS2蛋白酶,提示其在建立大脑SARS-CoV-2感染中的重要作用。为探究此问题,我们利用DS及同基因正常倍体iPSC构建了脑类器官(ChPCOs),其结构由功能性皮层神经元核心与外周功能性类脉络丛上皮组成。DS-ChPCOs重现了DS异常的皮层发育特征,并揭示类脉络丛上皮的纤毛发生和上皮细胞极性存在缺陷。研究进一步证明,类脉络丛上皮会促进SARS-CoV-2在皮层神经元中的感染与复制,且该现象在DS中更为显著。抑制TMPRSS2和弗林蛋白酶活性可使DS-ChPCOs中的病毒复制降至正常倍体水平。该模型可用于解析脉络丛在嗜神经病毒感染及正常倍体前脑发育中的作用,并为筛选针对SARS-CoV-2诱导神经病变的疗法提供平台。
版权©2024作者,保留部分权利;独家被许可人美国科学促进会。不对原始美国政府作品提出权利要求。根据知识共享署名许可4.0(CC BY)分发。
¶ 引言
脉络丛(ChP)是一种高度血管化的分泌组织,位于脊椎动物大脑的各个脑室内(1)。在成年人大脑中,ChP每天可产生高达500毫升的脑脊液(CSF),从而支持中枢神经系统(CNS)功能(1),同时防止免疫细胞浸润到CNS(1);在发育过程中,它还能产生多种信号因子,协调皮层发育和神经发生。早期发育阶段,侧脑室(LV)ChP(LVChP)原基与直接相邻的皮质边缘(大脑重要的组织中心区域)共同被特化,二者均分泌并响应诸如Notch、WNT和骨形态发生蛋白(BMP)等形态发生素(2)。这一发育路径确保ChP始终与大脑皮层紧密相邻,且这种解剖学上的毗邻关系终身保持(3)。人类侧脑室、第三脑室和第四脑室的ChP在转录水平上具有异质性。人类第四脑室ChP似乎比其他ChP更早完成分化(4)。人类ChP在发育2周后通过建立紧密连接、获得离子通道(如 电压门控通道)和转运蛋白而具备屏障、分泌和运输功能,这些组件在发育过程中持续变化(5)。迄今为止,哺乳动物ChP的发育研究主要依赖于动物模型(6–8),但这些发育过程在多大程度上适用于人类仍不明确。人类诱导多能干细胞(hiPSC)衍生的三维(3D)模型为探究ChP在发育及神经退行性疾病等病理过程中的作用提供了研究途径。为模拟人类小脑皮层,已开发出多种三维类器官模型,这些模型能够从人类胚胎干细胞(hESC)出发,在体外构建出类似小脑皮层的结构(9, 10)这两种ChP类器官模型均随时间推移逐渐成熟,最终与成人人类ChP组织日益相似。Pellegrini等人(9)开发的ChP类器官模型在第46天检测到神经前体细胞和神经元存在,与大脑皮质类器官不同,这些细胞在ChP类器官成熟过程中逐渐减少。这些ChP类器官模型对研究严重急性呼吸综合征冠状病毒2(SARS-CoV-2)感染对人类ChP的影响具有重要意义。随着脑室下区类器官的成熟逐渐减少。这些脑室下区类器官模型在研究严重急性呼吸综合征冠状病毒2(SARS-CoV-2)感染对人类大脑的影响方面发挥了关键作用(10, 11)。例如,研究证实SARS-CoV-2能有效感染并破坏脉络丛上皮,导致该血脑屏障发生渗漏(11);随后作者进一步表明,感染SARS-CoV-2的脉络丛类器官会出现细胞死亡率升高和炎症基因上调的现象(10)。
唐氏综合征(DS)是一种基因组疾病,发病率为每700至1000例活产中有1例(12),其病因是存在一条额外的21号染色体(HSA21)。HSA21的额外拷贝(21号染色体三体)会导致神经病理学改变,如皮质层状结构紊乱(13)、小脑组织与功能异常(14)以及海马齿状回细胞减少(15)。DS大脑皮层还表现出兴奋性神经元减少(16)、星形胶质细胞和抑制性神经元生成增加(17),以及少突胶质细胞分化和髓鞘形成缺陷(18)。发育中的DS大脑和DS小鼠模型(19)进一步显示脑室扩大,这与涉及纤毛功能的HSA21基因PCNT和PCP4剂量增加有关,且此前已有报道指出人类DS成纤维细胞存在纤毛缺陷(20)。先前研究发现,源自DS诱导多能干细胞的大脑类器官能够重现DS大脑发育异常的多个方面(21),包括皮质神经元生成缺陷(22)和阿尔茨海默病(AD)样病理特征(23)。越来越多的临床证据表明,与二倍体对照人群相比,DS患者感染SARS-CoV-2后住院风险增加4倍、死亡风险增加10倍,且这一风险无法完全用共病解释(24, 25)。有假说认为,对COVID-19病理的易感性增加,部分可归因于HSA21染色体上干扰素(IFN)通路基因的基因剂量增加所引发的过度干扰素反应,部分则源于全身免疫系统功能缺陷(26, 27)——该缺陷此前已被证实与唐氏综合征患者细菌及病毒感染风险升高相关(28–30)。另一种可能是跨膜丝氨酸蛋白酶2(TMPRSS2)的剂量增加发挥了作用,该HSA21基因编码的蛋白酶能促进SARS-CoV-2刺突蛋白与血管紧张素转换酶2(ACE2)受体结合(31)。SARS-CoV-2的嗜神经性日益被认为是导致长期认知与感觉障碍(长新冠)的潜在驱动因素(32)。然而,由于唐氏综合征患者本身存在一系列进行性、个体间差异显著的认知缺陷,且早发型阿尔茨海默样疾病风险急剧增高,因此SARS-CoV-2感染对其认知功能的长期影响难以量化。此外,SARS-CoV-2从母体垂直传播至胎儿会在多大程度上干扰大脑发育,以及这是否会对唐氏综合征患者的大脑发育产生更严重影响,仍有待明确。
在此,我们报告了生成的人皮质脑类器官,这些类器官不仅被功能性脉络丛样上皮包围,而且包含发育中的皮质细胞类型(ChPCOs)。我们证明这些ChPCOs表现出唐氏综合征典型的神经病理学改变,如少突胶质祖细胞减少。我们进一步发现唐氏综合征ChPCOs表现出异常的纤毛发生和脉络丛样上皮的极性缺陷。引人注目的是,我们发现ChPCOs的脉络丛样上皮区室显著促进了SARS-CoV-2的神经侵袭和嗜神经性,且在唐氏综合征中这一现象更为明显。我们进一步研究表明,使用美国食品药品监督管理局批准的抑制TMPRSS2活性的药物、弗林蛋白酶抑制剂以及瑞德西韦进行治疗,可将唐氏综合征类器官中的SARS-CoV-2复制降低至与整倍体组相当的水平,这表明唐氏综合征脉络丛样上皮中TMPRSS2基因剂量增加可能参与其中,并提示ChPCOs是识别能减轻SARS-CoV-2对成熟和发育中中枢神经系统影响药物的合适模型。
¶ 结果
¶ ChP器官样体的自组装再现了胚胎发育过程
人类神经外胚层(hNEct)细胞被预设为仅发育成前体组织(33),并注定在背侧形成皮质、腹侧形成皮质边缘,后者随后分化为脉络丛。因此,我们推断hNEct细胞可作为生成自组织皮质类器官(COs)的合适起始群体,这类器官将由脉络丛样上皮衍生的脑室结构所包绕(本文称为ChPCOs)。我们使人类ES和iPSC细胞系(图 S1A)(包括H9(34)、WTC(35)和G22(35))经SB与LDN双重SMAD抑制处理3天,高效产生了能生成神经干细胞的hNEct细胞,其特征为表达SOX2与NESTIN(图S1B)。随后将hNEct细胞转移至超低吸附六孔板,在添加碱性成纤维细胞生长因子(bFGF)的N2培养基中形成3D聚集体,由此生成具有神经上皮层的球状结构(图 1A,第7天)及中央多个表达SOX2的玫瑰花结结构(图S1C)。为模拟皮质半球分泌BMP4和WNTs的过程——该过程在体内将背侧皮质半球定位为脑室-皮质交界区(ChP)(36),我们用BMP4和CHIR99021处理这些球体以促进ChP形成(图1A和图S1C)。由于已知BMP4信号量会促进脉络丛谱系分化而牺牲神经谱系(9,10),我们在ChPCO方案的最初4天中,将hNEct暴露于递增剂量的BMP4。低剂量BMP4(2.5纳克)以由外向内模式将早期类器官中表达SOX2的细胞比例降低至 ,并进一步被采纳为最佳浓度(图 S1D);将剂量增加至50纳克/毫升BMP4后,如预期那样进一步降低了表达SOX2的细胞比例(图S1D)。通过定量聚合酶链反应(qPCR)对皮层边缘基因(MSX1/2)和脉络丛基因(AQP1、TTR和KLOTHO)的mRNA水平进行量化显示,经21天CHIR99021和BMP4处理后,MSX1/2表达显著诱导,随后在第28天至第84天急剧下降(图1C),表明皮层边缘被诱导。与这些数据一致,横截面类器官显示在第14天时,折叠上皮细胞中共表达皮层边缘标记物MSX1/2和LMX1A蛋白(图 1D)。在第21天至第28天之间,我们检测到类器官周围出现薄层上皮(图 1A),qPCR证明脉络丛标记物AQP1、TTR和KLOTHO同时上调(图1C)。与这些观察结果一致,免疫染色显示这些上皮层表达明确的脉络丛标记物TTR和LMX1A蛋白(图1D)。类器官大小在前28天内逐渐增加(图 1B),直至平均核心直径达到1.2毫米(图1B),并在第56天和第120天达到1.9毫米的最终直径(图1B)。高分辨率3D成像显示单个类器官中出现多个脉络丛样上皮,形成覆盖整个类器官的完整上皮层,这由紧密连接标记物ZO1标示(图 1E)。这些细胞也强表达KLOTHO——一种已知在小鼠脉络丛中表达的防衰老蛋白(34),证实了KLOTHO在脉络丛样上皮中的表达在进化上是保守的,并表明其在这些细胞中的作用可以用这些人脉络丛类器官进行研究。为证明该系统的可重复性,我们用不同的人诱导多能干细胞(hiPSC)系生成了ChPCOs(图S2,A和B),发现超过77%的类器官展现出包裹类器官的特征性薄层TTR+阳性上皮层,且不依赖于细胞系、克隆或批次(图 S2C)。我们进一步发现这些类器官能够长期存活(目前已在培养中存活1年)而无明显退化迹象。总之,我们的数据证明,该方案重现了皮层边缘模式化和脉络丛样上皮形成的体内发育阶段,并概述了一种生成包裹于脉络丛样上皮中的人脑类器官的快速方案。
为了进一步简化实验流程,我们尝试在不将hNEct球体嵌入Matrigel的情况下生成ChPCOs。然而,未嵌入基质胶的类器官经BMP4和CHIR99021处理28天后,未能形成包裹类器官的薄层上皮结构,并导致培养体系中大量细胞死亡(图 S1E)。这表明细胞外基质(ECM)在体外脉络丛形态发生过程中起着关键作用。
我们随后比较了第28天和第56天ChPCOs与非BMP4和CHIR99021处理的COs的批量RNA转录组。这表明在第28天和第56天的胆管上皮样组织(ChPCO)中,皮质血红素和胆管上皮标志物的表达随时间推移普遍增加,暗示在体外培养超过28天后,胆管上皮样组织的发育仍在持续进行,其水平显著高于第56天COs中观察到的数据(图S2D)。这些数据与我们观察到的现象一致:第56天ChPCOs中的脉络丛样上皮由薄层折叠上皮构成,并延伸出表达脉络丛标记物(TTR+与LMX1A+)的立方上皮细胞(图1D),此特征与人胎儿脉络丛上皮的观察结果相符(1)。在体内环境中,骨形态发生蛋白与音猬因子梯度沿神经管背轴分别调控侧脑室脉络丛与第四脑室脉络丛的发育,从而形成具有差异转录组特征的脉络丛组织(37)。在第28天与第56天,我们的ChPCOs显示出与侧脑室脉络丛相关基因(而非第四脑室脉络丛相关基因)的显著富集(图1F与图S2E),这与实验方案中使用骨形态发生蛋白4处理而未添加音猬因子的设计相符;且这些基因在ChPCOs中的表达水平再次高于第56天的COs(图1G)。在全转录组层面,仅ChPCOs(而非COs)与成人脉络丛组织表现出高度相关性(图 1H与图 S2F),该结果与此前已发表的脉络丛类器官模型结论一致(9, 10)。
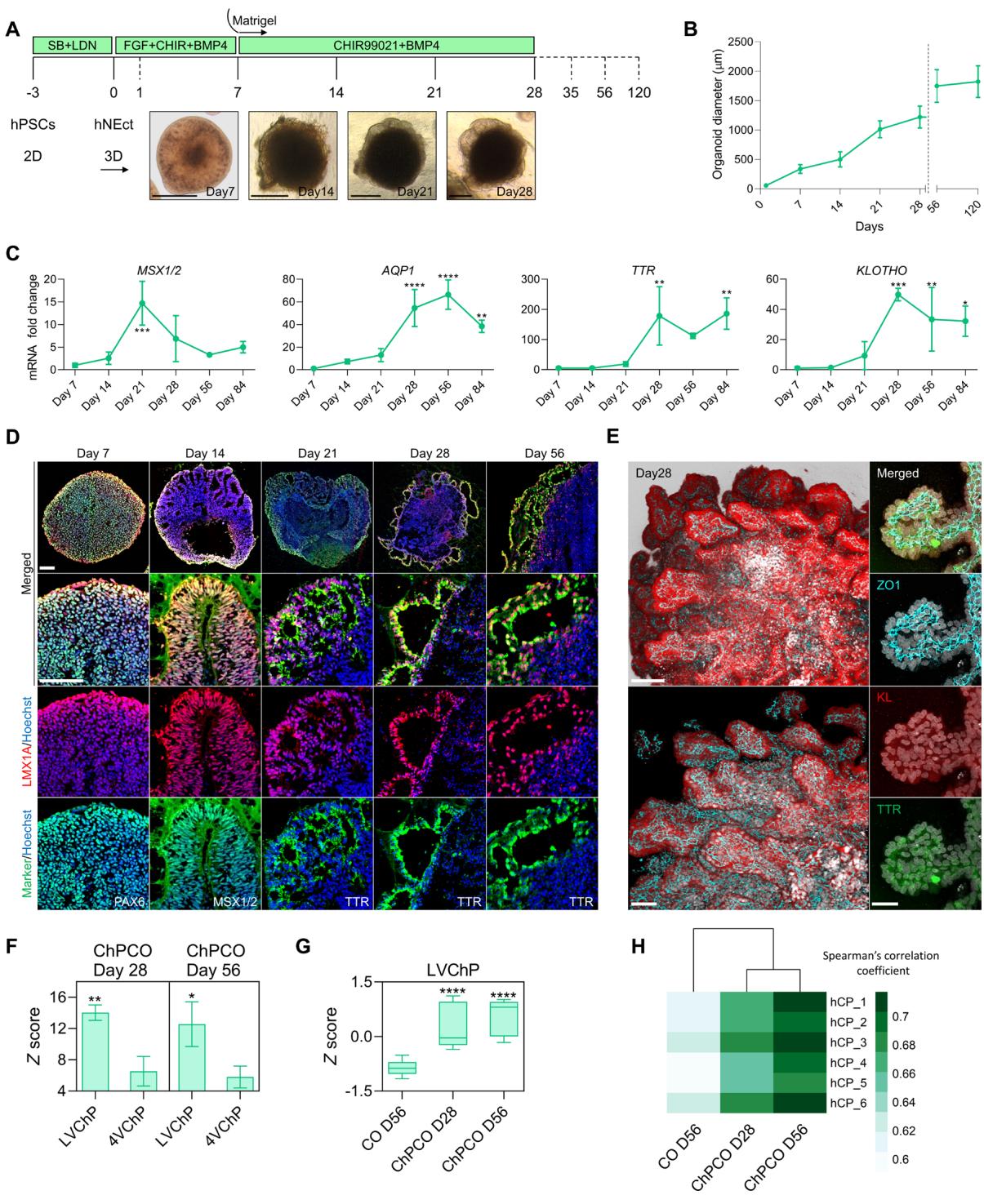
图1. 从神经外胚层三维培养生成人类自组织多重脉络丛类器官。(A) 从人干细胞生成脉络丛类器官的策略示意图。下方明场图像显示类器官在体外随时间发展的阶段。比例尺: 微米。(B) 脉络丛类器官在 体外的生长曲线图。数据显示为均值 标准差。 ;总计156个类器官数据汇总于表 。© MSX1/2、AQP1、TTR和KLOTHO的qRT-PCR结果。数值以GAPDH水平归一化,并相对于第7天数值表达。数据为均值 标准差; 。 , , , (单因素方差分析)。(D) 类器官切片免疫染色显示PAX6(绿色)、LMX1A(红色)、MSX1/2(绿色)、LMX1A(红色)、TTR(绿色)和LMX1A(红色)蛋白表达,Hoechst 33342(蓝色)复染核。比例尺: 微米。(E) 分化第42天脉络丛类器官的整体免疫染色。左图显示多个脉络丛样上皮组织被KLOTHO(红色)和ZO1(青色)染色,比例尺: 微米。右图为单个脉络丛样上皮的 倍放大图像,显示ZO1(青色)、KLOTHO(红色)和TTR(绿色)染色,比例尺: 微米。(F) 按列(三次重复合并)的平均Z分数图,显示来自批量RNA测序的lvchP和4vchP基因分布。数据显示为均值 标准差。 , (Student t检验)。(G) 箱形图显示从脉络丛类器官和对照类器官批量RNA测序获得的lvchP标记基因分布。数据显示为最小值至最大值。 001(单因素方差分析)。所用单个基因见图 。(H) 热图比较脉络丛类器官和对照类器官的批量RNA测序与44-70岁捐献者成人脉络丛样本的Spearman相关系数(104例)。
脉络丛类器官中脉络丛样上皮的进行性成熟为确定这些自组织的类脉络丛上皮层在ChPCOs中是否表现出与体内脉络丛相似的特性,我们随后检测了上皮极性的建立、线粒体丰度、纤毛发生及脑脊液分泌情况(38)。我们首先评估了类脉络丛上皮中上皮极性的建立,该过程受紧密连接、间隙连接、粘附连接及基底膜调控(图2A)。与其他脉络丛类器官模型一致(9),批量RNA测序数据显示,与COs相比,ChPCOs中与这些结构相关的基因随时间推移逐渐富集(图2B、C及附图S3A)。qPCR分析显示特定紧密连接基因(如CLDN11和CLDN12)逐渐增加(附图S3B),尽管CLDN2仅在28天时显著上升(图2D)。同样,间隙连接基因GJB2与粘附连接基因CDH5、PCDH18的mRNA水平也逐步升高(图 2D及附图 S3B),这与紧密连接标记物ZO1在类脉络丛上皮层中广泛连续的表达模式相符(附图S3C)。紧密连接的建立对脉络丛分化为特定基底组分也至关重要(39),因此我们进一步探究ChPCOs的类脉络丛上皮细胞是否呈现对正常脉络丛上皮功能关键的膜蛋白顶-基底极性。通过标记分别富集于极化类脉络丛上皮顶侧与基底侧的ZO1和层粘连蛋白,揭示了基底膜与顶极性的正确形成(图2F)。我们认为ChPCOs中类脉络丛上皮极性的建立——这是维持脉络丛稳态、脑脊液分泌、神经营养因子运输及屏障功能所必需的——表明我们的ChPCOs中的类脉络丛上皮应具备产生脑脊液及形成有效屏障的潜力。RNA测序分析证实,与56天的COs相比,28天ChPCOs中编码脉络丛分泌蛋白的基因显著富集(图 2G),且其表达量随ChPCOs进一步发育大幅提升(图2G,ChPCOs第56天)。我们检测到已知在脑脊液中分泌并能刺激室管膜神经干细胞增殖的生长因子IGF2(40)、参与血液蛋白摄取与向脑脊液递送的细胞外基质基因(如SPARC)(41),以及多种与脑脊液生成和分泌相关的酶、分泌蛋白和膜蛋白的表达(图 2H)。 与先前研究(9)一致,染色显示在第28天,ChPCOs的ChP样上皮中,参与脑脊液分泌的水通道蛋白1(AQP1)呈现正确的顶端定位(图2I)。随后我们采用多重酶联免疫吸附试验(ELISA)检测培养介质中ChPCOs释放的分泌组蛋白,发现与COs相比,ChPCOs的CST3和B2M显著增加(图2J)。这与脉络丛类器官分泌人脑脊液蛋白的能力相符(9)。然而,ChPCOs与COs的APP分泌丰度相近(图 2J)。
脉络丛初级纤毛对于调节脑脊液的流动和运输至关重要,其可根据长度、运动性和细胞纤毛数量进行表征(42)。在体内,脉络丛主要由多纤毛上皮细胞构成,每簇纤毛数从四到八根不等,但也包含一小部分参与化学和/或渗透感受的脉络丛细胞,这些细胞向脑脊液中延伸出一根初级纤毛(43)。这些细胞类型在人类胚胎中如何及时程特化仍 largely 不明。由于脉络丛类器官的生成高度模拟了正常脉络丛在体内的渐进性时序形态发生过程(图 1),且透射电镜在脉络丛类器官外围识别到微绒毛结构(图2E),我们检测了培养14、21、28和56天的人类脉络丛类器官的纤毛发生过程。批量RNA测序证实,相较于脑类器官,脉络丛类器官中纤毛相关基因呈现显著且渐进性富集(图3A)。使用ARL13B抗体对纤毛进行免疫染色显示,脉络丛类器官中的人类脉络丛样上皮细胞具有纤毛结构(图3B),且纤毛长度随时间显著增加,在第14、21、28和56天的平均值分别为0.7、1.6、2.3和 微米(图3C)。第14天时,发育中的脉络丛包含几乎等量的单纤毛和多纤毛TTR表达细胞,随后多纤毛细胞逐渐增加至第21天的约 、第28天的 以及第56天的 ,同时伴随着单纤毛脉络丛样上皮细胞的减少(图3D)。文献报道哺乳动物脉络丛样上皮细胞的纤毛数量存在种间差异,从大鼠每个细胞4-8根到蝾螈每个细胞50根不等(1)。我们的数据显示,在培养第14天至第56天期间,脉络丛类器官中人类脉络丛样上皮细胞的单细胞纤毛数量随时间发生显著转变,至第56天时 的脉络丛样上皮细胞每个细胞具有5-9根纤毛(图3E)。批量RNA测序数据显示纤毛回收相关基因随时间未见显著变化(图S3E)。综上所述,这些发现表明自组装的脉络丛类器官重现了体内脉络丛纤毛发生的关键特征,提示脉络丛类器官或可为研究唐氏综合征(19)和Bardet-Biedl综合征(44)等疾病提供有用模型——在这些疾病中,有缺陷的初级纤毛分别被认为会导致脑室扩大和脑积水。
¶ 皮质组织中的特化功能细胞区室在ChPCOs中形成
除了上述脉络丛成分外,脉络丛-皮质类器官还具有其他神经分区。在胚胎发育过程中,由神经外胚层衍生的头端神经管在背内侧端脑和背侧皮质板处形成脉络丛(33)。我们通过检测已知在类器官中表达的不同皮质神经元标记物的表达情况,研究了这些皮质板层的关键细胞区室是否在我们的类器官中形成,除了类皮质板样上皮(图4A)之外。我们发现PAX6 mRNA随时间逐渐减少(图4B),同时层VI、V、IV和II/III的神经元标记物相应增加,分别表现为TBR1、CTIP2、SATB2和CUX1/2的表达升高(图 4B)。对中线切面类器官进行这些神经元蛋白染色显示,在第28天即可观察到皮质TBR1+和CTIP2+神经元的分化(图4C和图S4A),而SATB2+和CUX1+神经元直到类器官成熟(图4C)第56天才被检测到。皮层各层的特化发生在由ChP样上皮细胞形成的类脑室结构附近(图4C和图S4A)。同样,在分化第56天,ChPCOs和COs中也会出现以胶质纤维酸性蛋白(GFAP)为标志的星形胶质细胞(图4D),但在第28天的ChPCOs中则未发现(图S4C),这符合星形胶质细胞生成约在50天左右开始的观点(45)。此外,我们在第56天检测到表达PDGFRA和CNPase的少突胶质细胞(图S3D),并在第150天的成熟类器官中观察到髓鞘基本蛋白(MBP)与神经丝蛋白的共定位(图4E),表明髓鞘化过程已启动。进一步理解脉络丛类器官(ChPCO)模型的结构特征,我们分析了第28天(图4,F和G)及第56天(图4H)的ChPCO连续切片,分别采用SOX2、DCX、TBR2和SATB2染色标记神经祖细胞、早期定向神经元祖细胞、深层中间神经祖细胞以及浅层皮质神经元(图4,F至H)。研究发现SOX2+阳性细胞更靠近脉络丛样结构表面,而其他标记细胞则位于内部且远离脉络丛样组织(图4,F至I)。类似地,皮质神经元在ChPCO的皮质组织中呈全域分布(图4,G至I)。
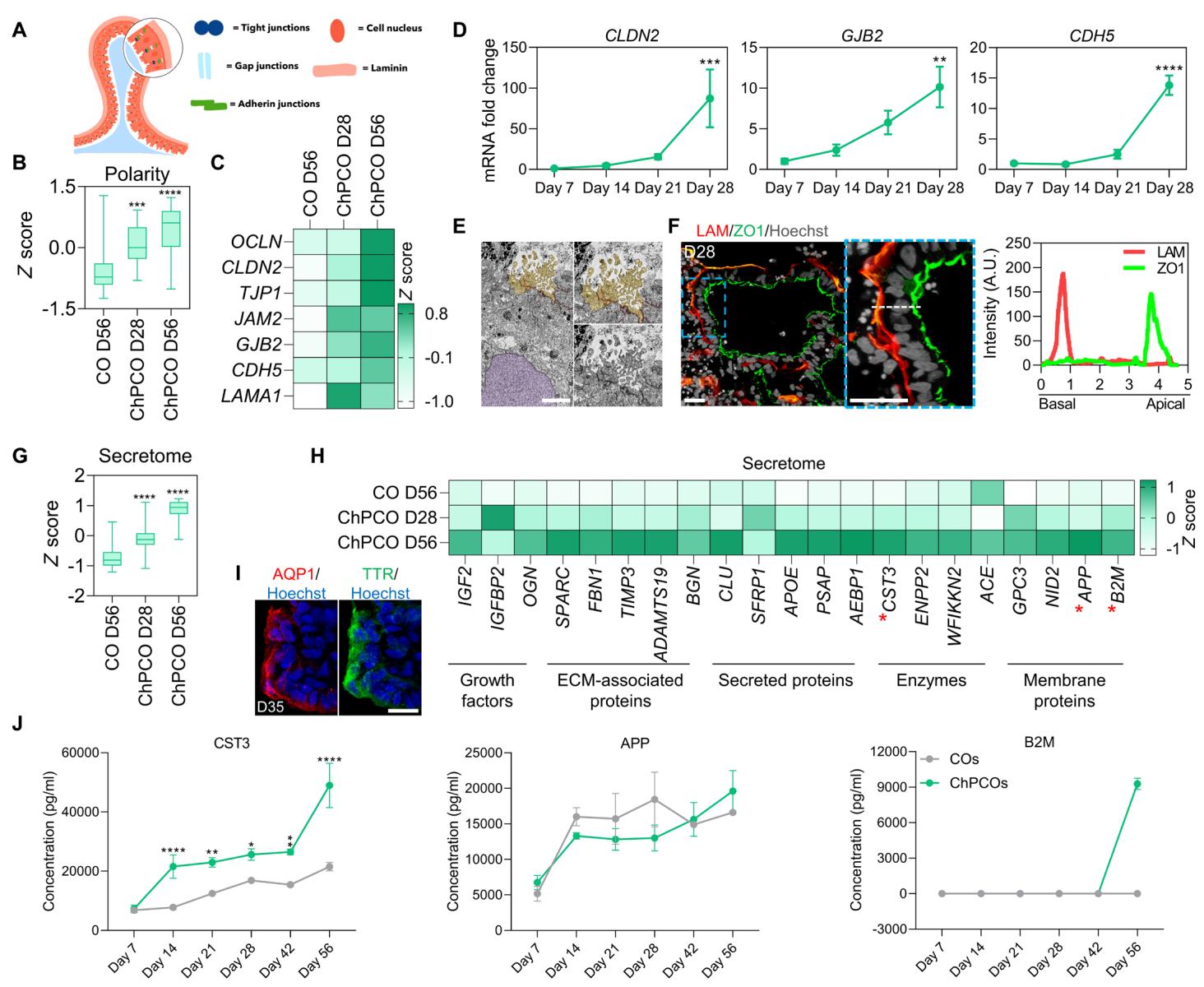
图2. ChPCOs中脉络丛样上皮的发育与功能分析。(A) 脉络丛顶底极性示意图。(B) 箱形图展示从大量RNA测序数据中获得的极性基因分布[列于©和图 S3A],数据范围为最小值至最大值。 , (单因素方差分析)。© 大量RNA测序中代表性顶底极性基因热图,数值以z分数显示。(D) ChPCOs中顶底极性基因的qRT-PCR分析。所有值均以GAPdh标准化并相对于第7天数值表示。数据为均值 标准差。 , , (单因素方差分析)。 。(E) 第28天ChPCOs透射电镜图像显示高密度线粒体、顶侧紧密连接、微绒毛(浅棕色)及细胞核(浅紫色)。比例尺:250纳米。(F) ChPCO切片层粘连蛋白(红)与ZO1蛋白(绿)染色,Hoechst 33342复染。比例尺: 微米。白色虚线表示图中脉络丛样上皮顶底方向上层粘连蛋白与ZO1表达的平均强度分布。(G) 箱形图展示从大量RNA测序获得的脑脊液分泌组基因分布[列于(h)],数据呈现为最小值至最大值。 (单因素方差分析)。(H)从大量RNA测序获得的脑脊液分泌组基因热图,数值为z分数。红色星号代表(J)中ELISA实验所选基因。(I) ChPCO切片脉络丛样上皮水通道蛋白AQP1(红)与TTR(绿)免疫染色,Hoechst 33342复染。比例尺: 微米。(J) Luminex多重检测/ELISA显示ChPCOs培养基中脑脊液分泌组蛋白标志物。数据为均值 标准差; 。 , , (单因素方差分析)。
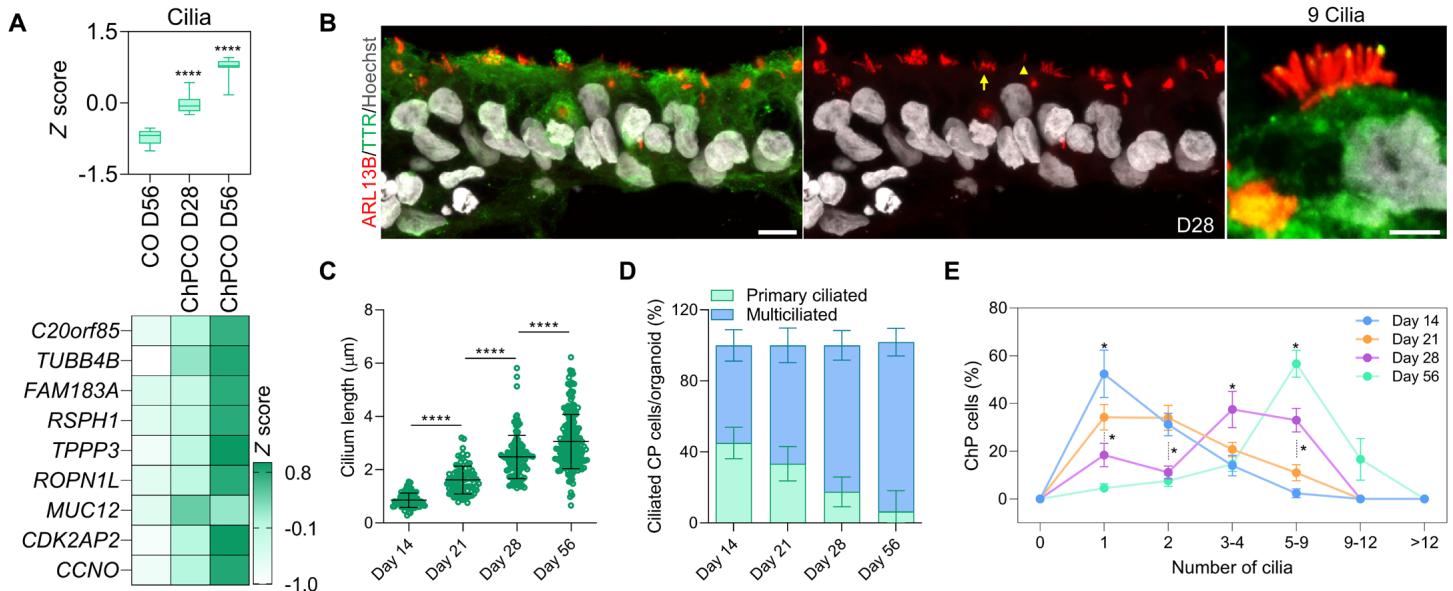
图3. 脉络丛样上皮细胞纤毛发生的发育与功能分析。(A) 箱形图显示第28天和第56天chPcOs以及第56天cOs批量RNA测序获得的纤毛相关标记基因(热图下方列出)分布。数据以最小值至最大值呈现,缺口以中位数为中心。 (单因素方差分析)。下方热图为纤毛相关标记基因表达谱,数值以z分数显示。(B) 第28天免疫染色chPcO切片分析,显示TT标记(绿色)的脉络丛样上皮细胞纤毛中ARl13B(红色)蛋白表达。切片用Hoechst 33342复染。比例尺 ;放大图像比例尺 。黄色箭头指示多纤毛细胞;黄色箭头指示单纤毛细胞。© 分化第1、21、28和56天chPcOs纤毛长度定量分析。数据以均值 标准差表示; (单因素方差分析)。独立实验次数 。散点代表单个纤毛长度。(D) 堆叠条形图显示分化第7、21、28和56天chPcOs中人脉络丛样上皮细胞中单纤毛与多纤毛细胞的百分比。数据以均值 标准差表示。独立实验次数 。(E) 培养第14、21、28和56天chPcOs纤毛数量分布。数据以具有单根初级纤毛或多纤毛的脉络丛细胞百分比呈现。各时间点最小样本量n 。实验总数 ;分析类器官总数 。数据以均值 标准差表示。Kolmogorov-Smirnov检验,* 。各时间点分析的类器官数量与实验次数汇总于附表 。
为评估皮层神经元的功能特性,我们首先确认成熟神经元分别表现出突触前与突触后标记物SYT1和HOMER1的表达与并列分布(图5A),以此作为突触接触的形态学证据。随后采用高密度多电极阵列(MEA)对关键电生理参数进行表征(图5B)。MEA分析检测到ChPCOs从第28天开始出现自发电活动(图5B展示了第56天的典型波形记录)。随着时间推移,自发神经放电/簇发放电频率呈现渐进性增长(图5,C至F)。值得注意的是,当ChPCOs中观察到GFAP+阳性细胞时(图4D),第56天的放电频率出现显著提升。然而与COs相比,ChPCOs在第56天的簇发放电频率并未显著增加(图 5D)。我们推测这种差异可能源于两种类器官中存在不同比例的神经元亚型。我们注意到,56天龄的ChPCOs中谷氨酸能(GLUR3+)与γ-氨基丁酸能(GABA+)神经元相邻分布(图5G),这与在体皮层发育过程中γ-氨基丁酸能抑制性神经元的分化模式一致(46)。使用GABA受体拮抗剂荷包牡丹碱( )处理可显著提高脉络丛类器官的放电频率(图5H 和图S4E),证实了抑制性突触传递的存在;而急性给予谷氨酸( )与N-甲基-d-天冬氨酸(NMDA)( )处理同样显著提升放电频率(图5H 和图S4E),证明了功能性谷氨酸能与GABA能神经元的存在。这些数据共同表明,在培养第56天的脉络丛类器官中,包含兴奋性与抑制性神经回路的神经网络已充分建立。
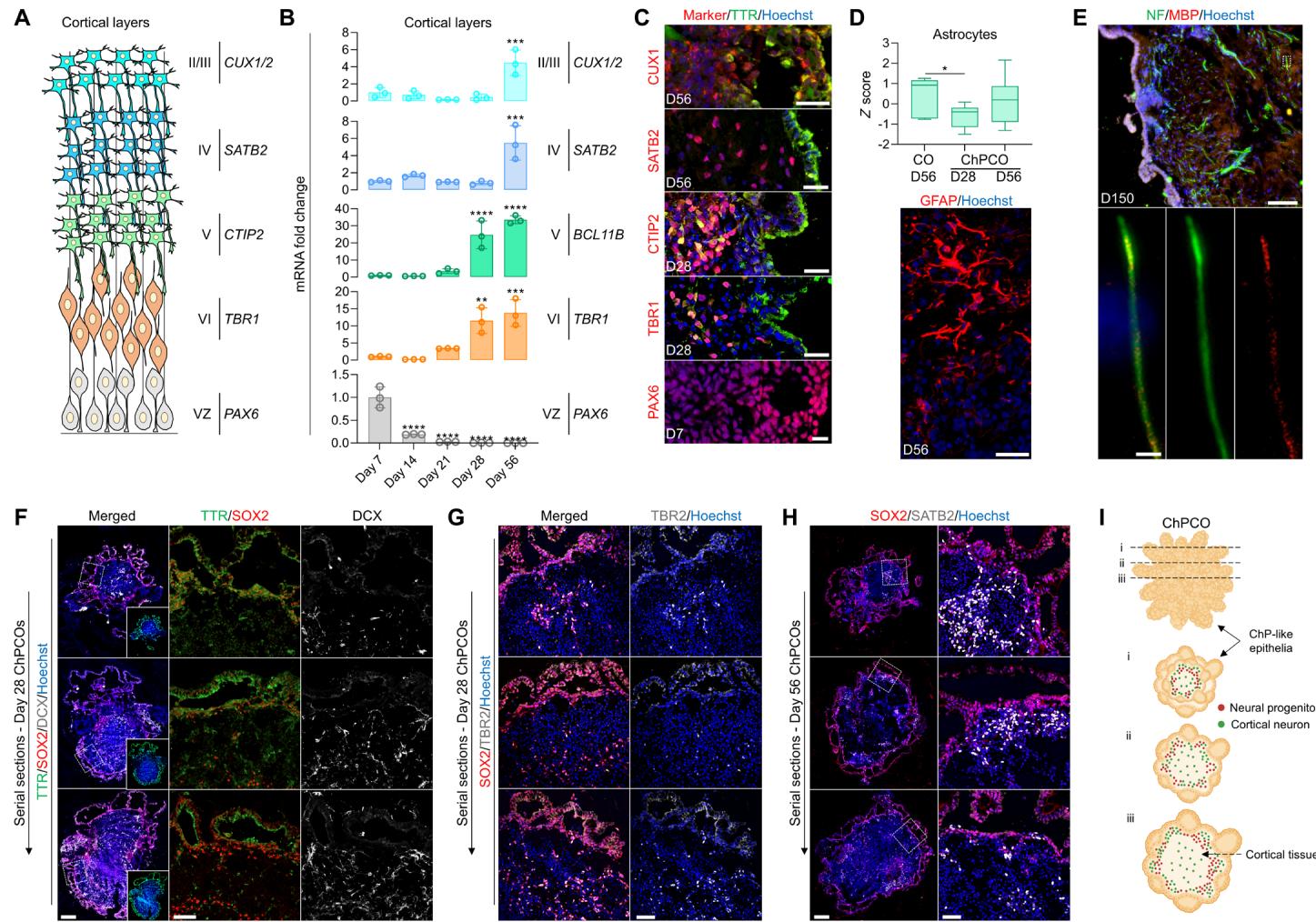
图4. 人脑类器官在培养过程中包含逐渐成熟的皮质神经元。(A) 皮质板层发育示意图:vZ为脑室区。(B) 脑室区基因PAX6与皮质神经元层基因(TBR1、CTIP2、SATB2及CUX1/2)的实时定量PCR检测结果。所有数值均以GAPdh为内参进行标准化,并相对于第7天数值呈现。数据表示为均值 标准差;经单因素方差分析, 、 、 。样本数N 。© 人脑类器官切片免疫染色显示PAX6(红)、TBR1(红)、CTIP2(红)、SATB2(红)及CUX1(红),并用Hoechst 33342复染。比例尺:PAX6为 微米,TBR1、CTIP2及SATB2为 微米,CUX1为 微米。(D) 箱形图展示批量RNA测序获得的星形胶质细胞基因(列于图 S4B)表达分布。数据以最小值至最大值呈现。经单因素方差分析, 。下图为人脑类器官切片经GFAP(红)免疫染色及Hoechst 33342复染。比例尺 微米。(E) 人脑类器官切片免疫染色显示神经丝蛋白(绿)与MBP(红)标记的髓鞘化神经元,Hoechst 33342复染(蓝)。比例尺1 微米。白色虚线框标注下方放大区域。放大图比例尺 微米。(F) 人脑类器官连续切片免疫染色显示DCX(灰)、SOX2(红)及TTR(绿)。比例尺 微米。白色虚线方框标注比例尺为 微米的放大区域。(G) 人脑类器官连续切片免疫染色显示TBR2(灰)与SOX2(红)。比例尺 微米。(H) 人脑类器官连续切片免疫染色显示SATB2(灰)与SOX2(红)。比例尺 微米。白色虚线方框标注比例尺为 微米的放大区域。(I) 人脑类器官神经区室结构示意图。
唐氏综合征脉络丛类器官重现了唐氏综合征脑部病理的关键方面唐氏综合症(DS)由21号染色体三体引起,会导致发育迟缓和智力缺陷(47)。人类发育中的DS大脑和Ts65Dn DS小鼠模型还表现出少突胶质细胞分化和髓鞘形成的缺陷(18)。此外,21号三体成纤维细胞显示出纤毛形成和功能的减少(20),这使得DS大脑成为在ChPCO类器官中建模的特别有趣的研究对象。因此,我们利用源自DS患者(DS18)的iPSC细胞系及其同基因型二倍体对照iPSC细胞系(EU79)(48)生成了ChPCO类器官(图 6A)。DS ChPCO类器官的大小与二倍体类器官相当(图 S5A),表明两者生长速率相似。通过量化至少由EU79和DS18细胞系生成的三批不同ChPCO类器官显示,无论是整倍体还是唐氏综合征细胞系来源的ChPCO,均能稳定形成类似脉络丛的上皮结构和皮质组织区域,且不同批次间的细胞比例保持一致(图6 B和C)。为更细致表征同源DS与整倍体ChPCO,我们对第28天的类器官进行了RNA-seq分析(每批次三个类器官, )(图6D、图S5B及表格S1)。分析表明整倍体与DS类器官呈现显著差异的转录谱(图S5B),其中相较于同源整倍体类器官,DS类器官有962个基因表达上调、997个基因表达下调(图6D及表格S1)。在差异表达最显著的500个基因中,有22个( )位于HSA21染色体(图S5D),其中四个基因(MX2、TMPRSS2、ADAMTS5 和 RUNX1)与病毒感染相关(图 S5D)。对DS类器官中上调基因的富集分析显示,这些基因在神经系统发育、纤毛运动与能动性、细胞黏附以及基底膜基因等多个类别中均有富集(图6E)。然而,在脉络丛或分泌组相关基因中未观察到变化(图S5C)。免疫印迹数据证实,与整倍体类器官相比,DS脉络丛类器官中非基质胶组分的细胞外基质蛋白有所增加(图S6K)。值得注意的是,与整倍体组相比,DS类器官中离子转运相关基因显著上调(图S6J)。DS类器官在一组纤毛发生标志物的表达上呈现显著上升(图7A)。相比之下,免疫染色结果显示使用ARL13B抗体对纤毛进行免疫染色显示,在56天龄的唐氏综合征脉络丛类器官中,ChP样上皮细胞主要为单纤毛结构(图7,B和C),且纤毛化ChP样上皮细胞数量显著少于对应的整倍体ChPCOs(图7D),尽管两组间平均纤毛长度相近(图S6F)。意外的是,我们还在唐氏综合征类器官中检测到顶基极性标志基因(图S6A)和蛋白(图S6C)的显著改变。为深入探究细胞极性可能存在的缺陷,我们使用与上皮细胞顶基极性相关的ZO1和E-钙黏蛋白(49),以及已知在人脉络丛细胞膜表达的β-连环蛋白(50)对整倍体与唐氏综合征类器官进行染色(图7,E和F)。在整倍体类器官中,这些蛋白质按预期正确分隔至ChP样上皮的相应区域(图7,E和F)。然而,在DS18和G21细胞系衍生的唐氏综合征类器官中,ZO1常错误定位于非顶端区域,并与β-连环蛋白在基底外侧域共定位(图7E和图S5G)。此外,唐氏综合征ChP样上皮中的E-钙黏蛋白未表现出与整倍体组相同的分布模式(图7F)。在二倍体ChP样上皮中,E-钙粘蛋白富集于最顶端区域,并向基底侧向区域延伸,在DS组中,在更广泛的区域观察到显著的E-CADHERIN染色,顶端区域与ZO1重叠处有明显富集(图7F)。这些观察结果表明,DS类器官中脉络丛样上皮的顶基底极性遭到破坏。我们量化了脉络丛样上皮细胞基底外侧区域ZO1与 -CATENIN的重叠百分比(49)。我们发现,在整倍体EU79和G22系的ChPCOs中,分别有 和 的脉络丛样上皮细胞的ZO1在基底外侧区域共定位(图 7G)。然而,在DS DS18和G21系的ChPCOs中,ZO1分别在 和 的脉络丛样上皮细胞的基底外侧区域保持共定位(图7G)。
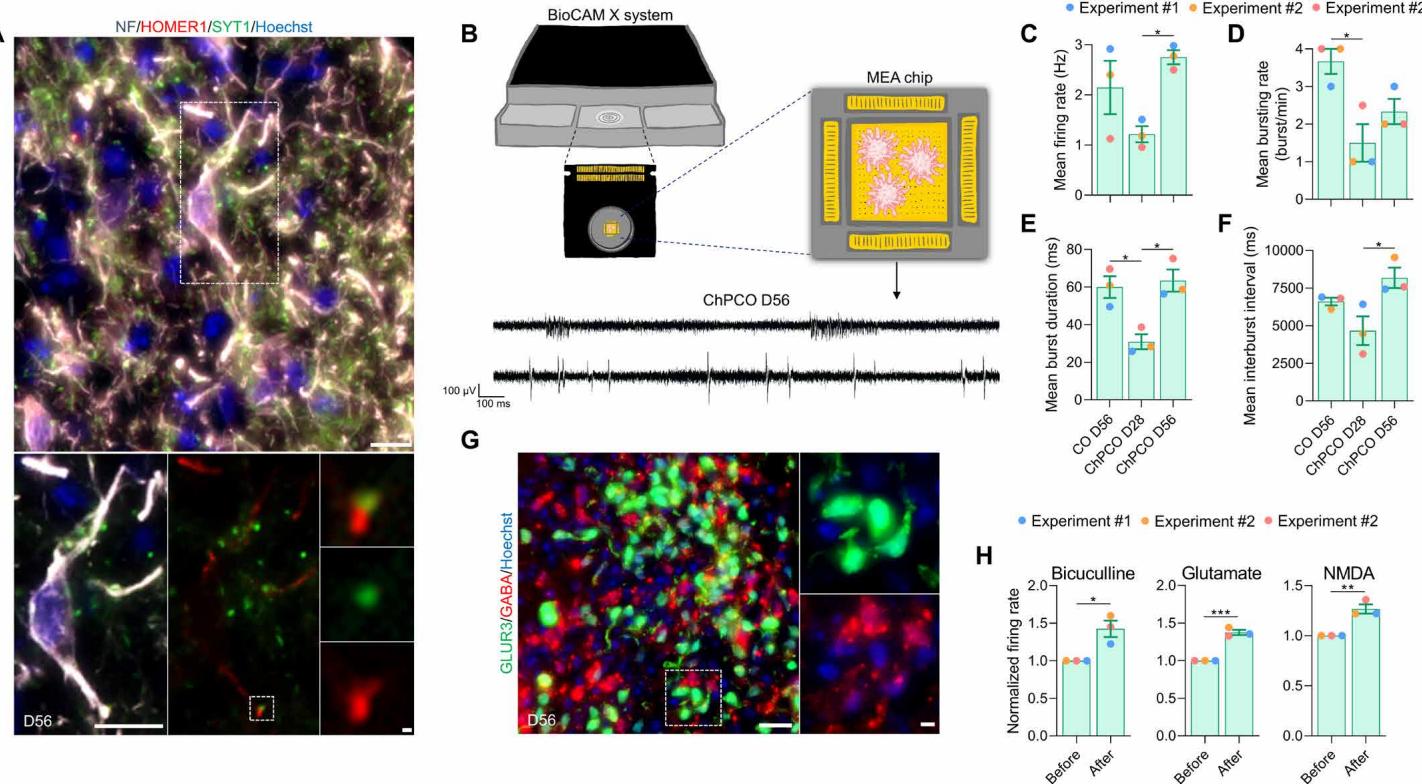
图5. ChPCOs中皮质神经元的功能分析。(A) 第56天chPcO切片免疫染色分析显示,神经元后突触和前突触分别由神经丝蛋白(灰色)、hOMeR1(红色)和SYnt1(绿色)标记。比例尺为 。白色虚线矩形框指示下方所示神经元的放大图像,比例尺为 。白色虚线方框指示连接的前后突触放大图像,比例尺为 。(B) chPcOs在MeA上进行细胞外记录的示意图。下方为第56天在chPcOs中记录的神经活动代表性瞬态图。比例尺:水平100毫秒,垂直 微伏。(C至F) 条形图显示第28天和第56天chPcOs神经活动模式与第56天cOs相比的变化。条形图表示放电率©、平均爆发率(d)、平均爆发持续时间(e)和平均爆发间期(F)的均值 标准差。 ,单因素方差分析。实验总数 ;分析的类器官总数 。各时间点分析的类器官数量和实验次数总结于表格 。(G) 第56天切片chPcOs的放大图像,显示谷氨酸能(GlUR3,绿色)和GABA能(GABA,红色)神经元的免疫染色。所有切片均用Hoechst 33342(蓝色)复染。比例尺为 ;放大图像比例尺为 。(H) 条形图显示药物治疗前后平均放电率模式的变化。使用的药物如下: 谷氨酸、 NMDA和 荷包牡丹碱。 , , ,Student’s t检验。
我们进一步注意到,少突胶质前体细胞(OPCs)的所有标记基因在培养28天的DS类器官中均出现下调(图 S6B),这一现象在蛋白质层面通过Western blotting得到证实(图S6C)。对类器官切片的免疫荧光染色显示,在整倍体ChPCOs的皮层组织区域细胞中能清晰检测到SOX10蛋白表达(图S6D),定量分析则表明DS类器官中SOX10阳性细胞数量显著减少。
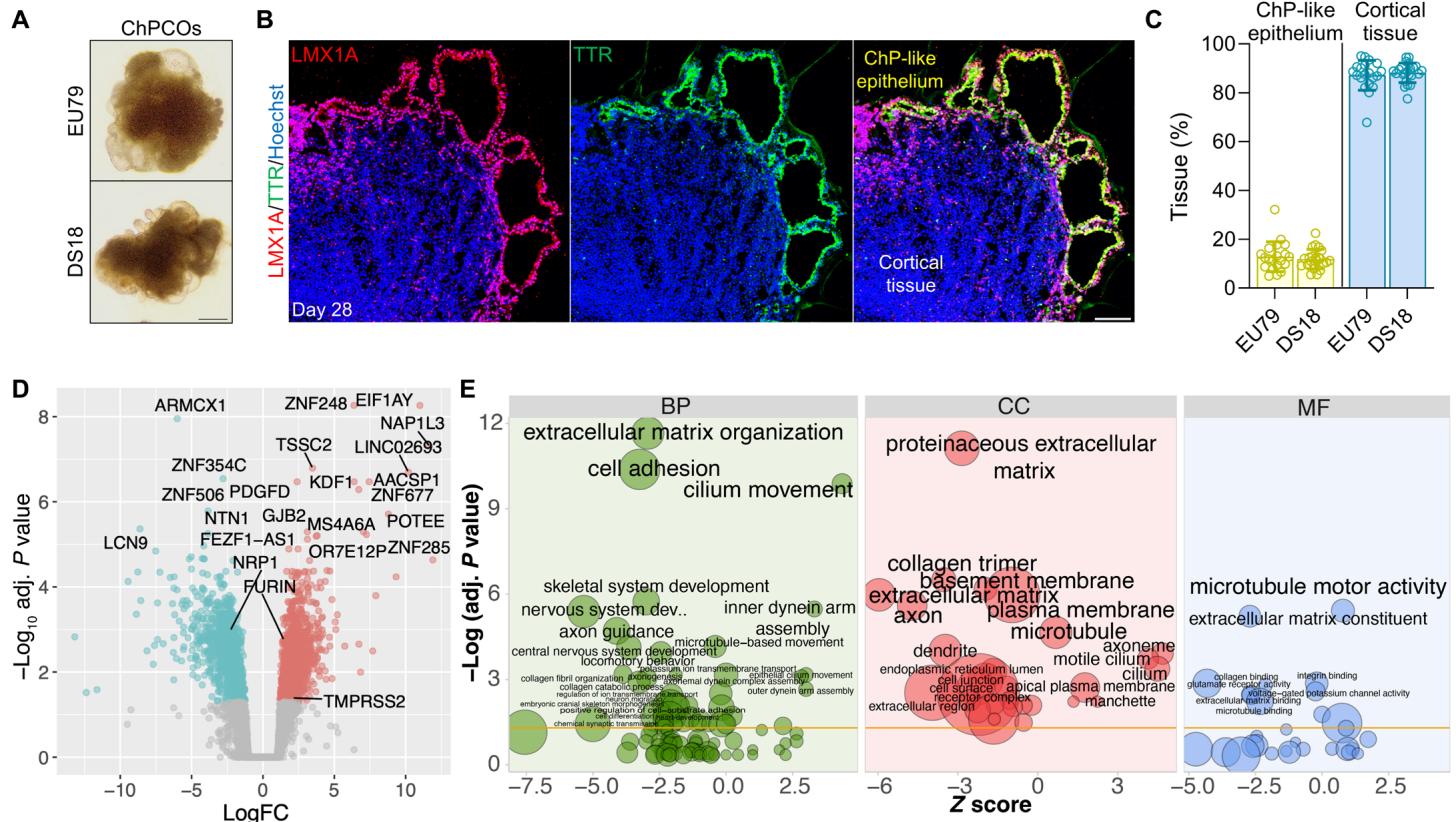
图6. ChPCO模型模拟唐氏综合征的转录谱。(A) 第28天整倍体与唐氏综合征iPSC来源chPCO的典型明场图像。比例尺: 。(B) 第28天整倍体iPSC来源chPCO经LMX1A(红色)与TTR(绿色)免疫染色的典型图像,切片经Hoechst 33342(蓝色)复染。比例尺: 。© 至少三组不同整倍体(EU79)与唐氏综合征(DS18)hiPSC来源chPCO中脉络丛样上皮与皮质组织区域的量化分析。单点代表单个类器官。实验总数 ;分析类器官总数 。各时间点分析的类器官数量与实验次数汇总于表 。(D) 第28天整倍体与唐氏综合征chPCO差异表达基因火山图。显著上调基因标为红色,下调基因标为青色,标注最显著差异基因及TMPRSS2、FURIN、NRP1基因。(E) 唐氏综合征chPCO相较于整倍体类器官的差异表达基因GO富集分析。Z值表示各条目相关基因表达量的累积增减,气泡大小与对应GO条目关联的差异基因数量成正比。BP:生物过程;CC:细胞组分;MF:分子功能。
与整倍体对照组相比,DS脉络丛脑类器官(图S6E)。这促使我们检测HSA21基因OLIG2的表达情况——该基因在发育中的前脑背侧少突胶质细胞生成中发挥作用(51),但发现该基因在DS脉络丛脑类器官中的mRNA水平表达下调(图S5D)。随后的蛋白质印迹与类器官切片免疫荧光染色分别证实,相较于整倍体类器官,DS脉络丛脑类器官中OLIG2蛋白表达降低且表达该蛋白的细胞数量减少(图S5,E和F)。综上,这些发现表明DS脉络丛脑类器官重现了DS脑病理的关键特征。
¶ SARS-CoV-2可高效感染DS ChPCOs
鉴于DS个体对SARS-CoV-2更具易感性(24, 25),我们接下来希望评估ChPCOs在模拟SARS-CoV-2感染人类中枢神经系统方面的效用。我们首先分析了未感染整倍体及DS脉络丛类器官的RNA-seq数据集,以探究决定SARS-CoV-2细胞入侵的宿主基因表达情况。SARS-CoV-2可通过内体入侵途径穿透易感细胞,该途径需要病毒结合受体ACE2,并经由蛋白酶弗林对病毒刺突蛋白的切割得以促进;此外,病毒也可通过细胞表面途径(直接融合)进入细胞,该途径还需依赖TMPRSS2对刺突蛋白进行裂解(52)。我们的RNA测序数据显示,DS类器官中ACE2基因表达水平稳健,与整倍体类器官中观察到的水平相近(图8A)。正如预期,对于位于HSA21上的基因,TMPRSS2在DS类器官中的表达显著高于整倍体类器官(图8A)。我们进一步发现,虽然FURIN基因不位于HSA21上,但DS类器官中的FURIN表达较整倍体类器官增加了三倍(图5A)。蛋白质印迹分析证实,与整倍体类器官相比,DS类器官中TMPRSS2和FURIN的丰度更高(图8B)。免疫染色同样证实,在脉络丛样上皮细胞中ACE2、TMPRSS2和FURIN的表达水平远高于ChPCO类器官的皮质组织部分(图8C和图S6G)。因此,这些数据表明我们的ChPCOs表达了SARS-CoV-2感染所需的受体和蛋白酶,从而可能构成研究DS个体中SARS-CoV-2中枢神经系统感染的合适实验模型。这也提示,脉络丛样上皮细胞可能促进病毒进入中枢神经系统,因为其表达的TMPRSS2和FURIN水平高于神经元。

图7. DS来源的ChPCO中纤毛发生与顶-基底极性分析。(A) 箱形图显示第31天chPCO批量RNA测序获得的纤毛基因(热图中列出)分布。数据范围为最小值至最大值。通过单因素方差分析, 。纤毛基因热图下方数值显示为z分数。(B) 第56天chPCO的ARl13B(红色)与ttR(绿色)免疫染色,hoechst 33342复染。比例尺 。白色虚线框表示放大区域。© 堆叠条形图展示chPCO中类chP上皮细胞含单个纤毛与多个纤毛的细胞百分比。数据为均值 标准差。 \Nu = 3 \sb { \circ } 。 0.05; (单因素方差分析)。实验总数 ;分析类器官总数 (汇总于表 S8)。(D) chPCO中纤毛数量分布。实验总数 ;分析类器官总数 (汇总于表 S8)。数据以均值 标准差表示。Kolmogorov-Smirnov检验, 。(E) 第56天chPCO切片的 -catenin(红色)、ZO1(绿色)、ttR(品红)免疫染色,hoechst33342(蓝色)复染。比例尺 。白色虚线框表示放大区域。白色箭头指示ZO1在基底外侧区域分布。比例尺 。(F) 第56天chPCO的e-cadherin(红色)与ZO1(绿色)免疫染色,hoechst 33342(蓝色)复染。比例尺 。白色虚线框表示放大区域。比例尺 。白色箭头指示ZO1在基底外侧区域分布。黄色箭头指示e-cadherin在顶侧区域富集。(G) 第56天chPCO中类chP上皮的ZO1错误定位百分比。数据以均值 标准差表示。 (Student’s t检验)。 。
为评估类脉络丛上皮对大脑类器官感染SARS-CoV-2易感性的影响,我们使用106个病灶形成单位(FFUs)的SARS-CoV-2病毒分别感染培养28天的整倍体与唐氏综合征脉络丛类器官72小时(图8D和图S9D),并通过定量逆转录聚合酶链反应(RT-PCR)检测SARS-CoV-2核衣壳蛋白、RdRp(图 8E)、包膜蛋白及刺突蛋白基因(图 S6H)的表达水平。结果显示,与脉络丛类器官相比,普通类器官的SARS-CoV-2感染率较低,且唐氏综合征脉络丛类器官的病毒基因表达量显著高于整倍体脉络丛类器官。
为确认SARS-CoV-2的增殖性感染,我们在感染后0、24、48和72小时检测了培养上清液中的病毒滴度,结果显示DS组在24和48小时具有感染性病毒的滴度显著高于整倍体组(图8F)。接下来,我们检测了SARS-CoV-2感染细胞在脉络丛类器官中的空间分布。SARS-CoV-2感染后,DS类器官中表达SARS-CoV-2刺突蛋白的细胞比例显著高于整倍体类器官(图 8,G和H),这与较高的病毒RNA水平一致(图 8E和图 S6H)。对免疫染色结果的分析EU79和DS18来源的脑器官进一步证实了少数皮层细胞感染SARS-CoV-2的现象(图S9C)。这与先前研究结果一致,即相较于普通脑类器官,具备脉络丛样组织的类器官对SARS-CoV-2的易感性更高(10, 11)。我们在SARS-CoV-2实验过程中进一步量化了ChPCOs中脉络丛样上皮与皮层组织的占比。与上述数据(图6C)相似,各组细胞比例基本一致(图S8,C和D),仅EU79类器官感染SARS-CoV-2后脉络丛样上皮有轻微增加。这些发现表明DS ChPCOs中SARS-CoV-2感染增强并非由脉络丛细胞数量增加导致。鉴于ChPCOs同时包含脉络丛样上皮与皮层组织,且SARS-CoV-2相关受体和蛋白酶在脉络丛样上皮中的表达量显著高于皮层组织(图8C与图S6G),我们进一步比较了ChPCOs内部这两种组织对SARS-CoV-2的细胞感染易感性。结果一致显示,DS脉络丛样上皮与皮层组织中SARS-CoV-2刺突蛋白阳性细胞数量显著高于整倍体类器官(图8I)。通过泛神经元标记物(NEUN)染色,我们发现皮层组织中大量神经元已被SARS-CoV-2感染(图8J,黄色箭头)。这些受感染神经元多数呈现细胞核碎裂现象(图 S7,D和E),提示SARS-CoV-2感染可能诱发神经元死亡。
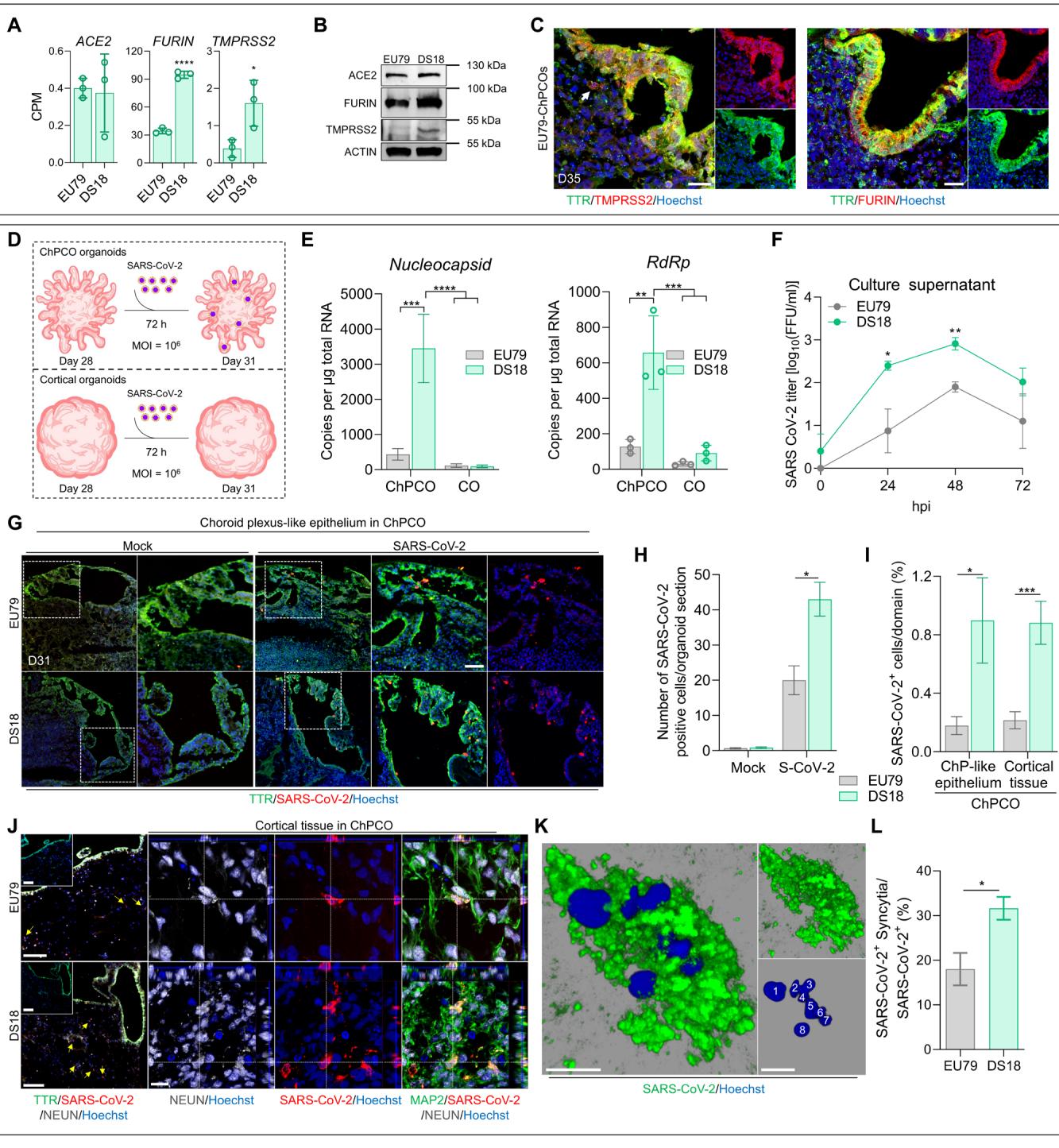
图8. SARS-CoV-2可有效感染ChPCO类器官而非CO类器官。(A)第31天ChPCO类器官中ACE2、FURIN及TMPRSS2来源的RNA测序读段丰度。数据为平均值 标准差。 , (学生t检验)。 。(B)Western blot检测第31天ChPCO类器官中ACE2、FURIN、TMPRSS2及Actin蛋白水平。(C)整倍体ChPCO类器官切片经TMPRSS2(红)、FURIN(红)、TTR(绿)染色及Hoechst 33342复染。比例尺: 微米。(D)SARS-CoV-2感染实验示意图。(E)第31天类器官中SARS-CoV-2核衣壳蛋白与RdRp检测结果。数据为平均值 标准差。 , , (双因素方差分析)。 \Nu = 3 \sb { \circ } 。(F)SARS-CoV-2( )处理后ChPCO上清液病毒滴度。数据为平均值 标准误。 ; , (学生t检验)。(G)SARS-CoV-2( FFU)或模拟感染( FFU SARS-CoV-2)后ChPCO切片经TTR(绿)、SARS-CoV-2刺突蛋白(红)染色及Hoechst 33342复染。比例尺: 微米。( )ChPCO中SARS-CoV-2阳性细胞统计图。数据为平均值 标准误。 (学生t检验)。统计样本为n 的15个ChPCO切片。(I)ChPCO内SARS-CoV-2阳性细胞百分比统计图。数据为平均值 标准误。 , (学生t检验)。统计样本为n 的15个ChPCO切片。(J)ChPCO切片经TTR(绿)、SARS-CoV-2刺突蛋白(红)、NeuN(灰)染色。比例尺: 微米。正交投影为共聚焦z-堆叠图像,经MAP2(绿)、SARS-CoV-2核衣壳蛋白(红)、NeuN(灰)染色及Hoechst 33342复染。比例尺: 微米。黄色箭头标示受感染神经元。(K)SARS-CoV-2阳性合胞体三维重构与最大Z平面投影。白色数字标记独立细胞核。比例尺: 微米。(L)感染后72小时SARS-CoV-2阳性合胞体百分比统计图。数据为平均值 标准误。 (学生t检验)。统计样本为n 的15个ChPCO切片。
接下来,我们研究了SARS-CoV-2感染ChPCOs后的细胞学效应。我们在受感染的细胞中观察到合胞体存在(图8K和图S6I),且唐氏综合征(DS)类器官中的合胞体数量较整倍体ChPCOs显著增加(图8L)。值得注意的是,所有合胞体均出现在DS类器官的皮质组织感染细胞中(图8的K、L以及图S6I),而在脉络丛样上皮细胞中未见明显合胞体形成。通过逐层分析共聚焦Z轴平面,我们在感染72小时后的单个DS皮质细胞中最多识别出八个细胞核(图8K)。综上,我们的数据表明:利用ChPCOs作为三维人体细胞模型,我们成功揭示了SARS-CoV-2对脉络丛样上皮细胞的显著嗜性,这种嗜性导致皮质组织细胞的有效感染,并在DS组中引发更显著的合胞体形成——这可能通过脑内细胞间融合作用促进病毒传播。
¶ SARS-CoV-2感染后DS ChPCOs的转录失调
为了进一步探究脉络丛类器官(ChPCOs)对SARS-CoV-2感染的细胞反应,我们对暴露于SARS-CoV-2 72小时的第31天整倍体与21三体ChPCOs进行了RNA测序。我们首先检测了比对至SARS-CoV-2基因组的读数,发现唐氏综合征(DS)ChPCOs中的SARS-CoV-2 RNA载量显著高于整倍体类器官(图9A)。大部分病毒来源的读数定位于病毒基因组的3’末端区域,该区域代表活跃转录的亚基因组RNA子集,从而进一步证实了感染细胞中的病毒RNA复制(图9B)。主成分分析显示不同组别的生物学重复样本聚类良好,且样本在第一维度依据基因型、第二维度依据SARS-CoV-2感染状态实现分离(图 9C)。该分析进一步揭示,两组中感染SARS-CoV-2的整倍体与21三体类器官在转录水平上均与未感染类器官存在差异(图9C)。使用斯皮尔曼秩相关进行的层次聚类分析对前500个变异程度最高的基因进行相关性分析表明,SARS-CoV-2阳性的整倍体和唐氏综合征组类器官在转录水平上与其他两组SARS-CoV-2阴性组存在差异(图 S7A)。相较于感染SARS-CoV-2的整倍体类器官,我们进一步确认了TMPRSS2与FURIN基因的显著上调(图 S7B),而ACE2在两组的表达水平保持相当(图 S7B)。比较SARS-CoV-2感染与未感染的唐氏综合征脉络丛类器官,发现1058个上调基因和215个下调基因(图 9D及附表S2);而在感染与未感染的整倍体脉络丛类器官对比中,则发现1118个上调基因和758个下调基因(图 9E及附表S3)。这表明SARS-CoV-2感染会引发大规模的转录调控紊乱。
接下来,我们研究了在唐氏综合征类器官中特异响应而在整倍体类器官中无响应的SARS-CoV-2相关基因。共鉴定出392个上调基因与219个下调基因(图9F及附表S4)。值得注意的是,这些基因广泛分布于整个基因组中,仅七个位于21号染色体(图9的G、J面板)。对差异表达基因进行的基因本体论和通路富集分析显示,DS18脉络丛类器官在以下过程中表现出显著更强的激活:细胞增殖负调控、凋亡过程正调控、细胞周期停滞以及磷脂酰肌醇3-激酶(PI3K)-Akt信号通路(图9的H、I面板及图S7C)。该结果与此前研究发现一致——SARS-CoV-2会加剧脉络丛类器官的细胞死亡(文献10)。值得关注的是,在感染SARS-CoV-2的类器官中未观察到明显的干扰素通路激活,干扰素刺激基因(ISGs)的表达亦无差异(图9H及附表 S4)。
考虑到受感染类器官中促凋亡途径的激活(图9H和表S4),72小时感染后SARS-CoV-2病毒滴度的快速下降(图8F)最可能的原因是:通过程序性细胞死亡快速清除易感细胞,而非通过先天免疫机制实现病毒清除。为验证这一点,我们进一步检测了促凋亡基因的表达情况(表S5),并评估了SARS-CoV-2感染前后的细胞死亡率。在感染前,唐氏综合征类器官显示出与凋亡过程相关基因的低表达(图S8A),这与先前认为唐氏综合征细胞对凋亡敏感性较低的研究结论一致(53)。然而,唐氏综合征类器官暴露于SARS-CoV-2后,促凋亡基因的表达发生显著改变(图S8A)。免疫染色进一步证明,与整倍体类器官相比,SARS-CoV-2感染后的唐氏综合征类器官中cleaved caspase-3阳性细胞显著增加(图 S8B)。与细胞粘附和细胞外基质重塑相关的多个基因上调(图9F和H)表明,脉络丛类器官中受感染的脉络丛样上皮细胞可能向脑脊液屏障发出信号,促进SARS-CoV-2侵入(54, 55)。总体而言,这些转录组分析结果与以下观点一致:SARS-CoV-2能有效感染唐氏综合征脉络丛类器官,导致SARS-CoV-2侵入、细胞周期与增殖缺陷,并增加皮层神经元的细胞死亡。
¶ TMPRSS2抑制剂降低SARS-CoV-2对DS类器官的感染
由于HSA21三倍体化导致的DS转录失调,可能导致更严重COVID-19的风险升高,这可能至少部分归因于TMPRSS2产量增加(31)。鉴于我们在DS类器官中检测到TMPRSS2表达量增加了三倍(图8A和B),我们随后评估了TMPRSS2抑制剂阿沃拉司他、卡莫司他和那法司他对SARS-CoV-2有效感染的影响(图10A)。根据先前研究的建议(56,57),唐氏综合征脉络丛类器官先用有效剂量的抑制剂预处理6小时,并在后续72小时的SARS-CoV-2感染期间持续给药。接着,我们比较了24和48小时感染后与未经抑制剂处理的SARS-CoV-2感染整倍体及DS18类器官产生的病毒滴度。所有抑制剂均显著降低了唐氏综合征脉络丛类器官上清液中24和48小时感染后的病毒滴度,降至与SARS-CoV-2感染整倍体类器官相当的水平(图 10B)。与avoralstat或camostat相比,nafamostat在唐氏综合征类器官中对SARS-CoV-2感染的抑制作用最强(图10B),并在48小时感染后完全消除了类器官中的感染性病毒(图10B)。值得注意的是,三种TMPRSS2抑制剂中任何一种的处理均完全阻断了病毒在整倍体类器官中的复制(图S8E)。 总体而言,这些结果表明TMPRSS2介导的病毒途径(直接膜融合)是SARS-CoV-2在脑组织感染的主要进入方式。此外,我们旨在测试经nafamostat预处理的类器官在SARS-CoV-2感染后是否表现出细胞死亡减少。对切片类器官的免疫染色发现,整倍体和唐氏综合征脉络丛类器官中SARS-CoV-2阳性细胞显著减少(图 S9A)。此外,我们还发现以裂解的caspase-3为标志的细胞死亡显著减少(图S9B)。这一观察结果与nafamostat的功能相符,即干扰刺突蛋白的激活,从而阻碍病毒在体内的复制和传播,而非阻止SARS-CoV-2的初始感染。
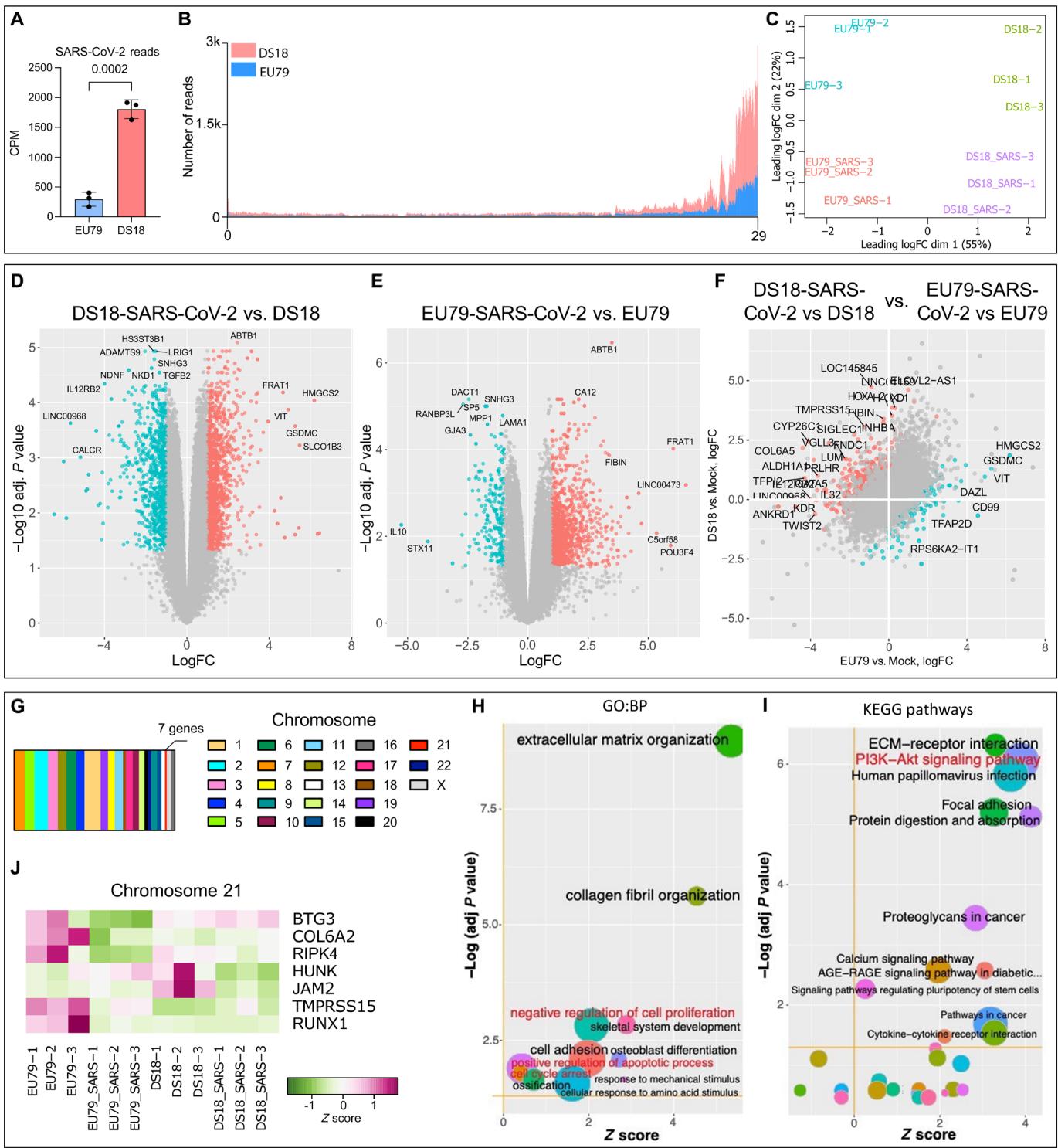
图9. 二倍体与21三体脑脉络丛类器官感染SARS-CoV-2后的转录分析。(A) 二倍体(eU79)与21三体(dS18)脑脉络丛类器官中SARS-CoV-2来源RNA-seq读段的丰度读段计数经文库大小标准化。误差棒表示标准差。统计学分析采用Student’s t检验。(B) SARS-CoV-2来源RNA-seq读段在病毒基因组上的分布。21三体(dS18)数据以红色显示,二倍体(eU79)数据以蓝色显示。© 未感染与SARS-CoV-2感染的人脑脉络丛类器官(二倍体eU79与21三体dS18)RNA-seq读段计数的多维尺度分析分布图。(D与E) 火山图分别凸显21三体(D)与二倍体(E)脑脉络丛类器官在SARS-CoV-2感染后相较于模拟感染的差异表达基因。(F) 散点图展示dS18与eU79脑脉络丛类器官在SARS-CoV-2诱导的基因表达变化差异。在(D)至(F)中,显著(FDR校正P值 )上调与下调(表达水平至少两倍变化)的基因分别以红色和青色标示。多数差异表达基因已标注。(G) (F)中鉴定的SARS-CoV-2应答差异表达基因在各染色体上的分布情况。(H) GO与(I) KEGG通路富集分析展示(F)中差异表达基因的功能特征。Z分数表示每个功能术语相关基因表达水平的累积增减。气泡大小与对应GO术语相关的差异表达基因数量成正比。(J) SARS-CoV-2感染与未感染的dS18和eU79脑脉络丛类器官中,(F)鉴定的21号染色体相关基因的表达情况。
考虑到唐氏综合征大脑类器官相比整倍体对照也表现出更高的弗林蛋白酶水平(图8,A至D),我们随后评估了弗林蛋白酶抑制剂 decanoyl-RVKR-CMK 对DS与整倍体类器官中病毒复制的影响。刺突蛋白的弗林蛋白酶切割并非SARS-CoV-2入侵的必要条件,但能显著增强病毒感染性(58)。弗林蛋白酶抑制剂处理完全阻断了SARS-CoV-2在整倍体类器官中的复制(图 10,C和E),这表明在脑组织中,弗林蛋白酶活性对于SARS-CoV-2通过膜融合途径入侵至关重要。使用FDA批准的新冠药物瑞德西韦处理也观察到相同效果(图10,C和E)。然而,该弗林蛋白酶抑制剂对DS类器官中病毒复制的影响较弱。尽管decanoyl-RVKR-CMK在感染后24小时和48小时使病毒滴度显著降低10倍,但未能完全清除病毒,而瑞德西韦则实现了完全清除(图10,D和E)。这可由DS脉络丛类器官中更高丰度的TMPRSS2和弗林蛋白酶解释(图8,A至C)。另一方面,不断进化的SARS-CoV-2奥密克戎变异株被弗林蛋白酶切割的效率较低,但对TMPRSS2抑制剂更敏感(59)。这促使我们评估弗林蛋白酶抑制剂对DS和整倍体类器官中奥密克戎BA.5复制的影响。萘莫司他与瑞德西韦处理均完全阻断了奥密克戎BA.5在DS和整倍体类器官中的病毒复制(图10,F至H)。虽然弗林蛋白酶抑制剂在两组中均显著降低病毒复制(图 10,F和G),但与萘莫司他和瑞德西韦相反,该抑制剂未能完全清除奥密克戎BA.5(图10,F至H)。综上,这些实验为脉络丛类器官可作为模型用于筛选抑制特定遗传背景(本例为21三体)下SARS-CoV-2神经病理的药物提供了概念验证。
¶ 讨论
先天性疾病涵盖多种脑室周围白质病变,例如脑室周围囊肿、弥漫性绒毛增生、脂肪瘤及斯蒂尔-韦伯综合征(60)。例如,脑室周围囊肿常见于18三体综合征和艾卡迪综合征胎儿,其中脑室周围囊肿会导致脑脊液积聚引发脑积水(61)。许多脑室-脑室间隔异常与其他脑部结构畸形相关,包括皮层发育异常。因此,建立能够探究此类疾病(特别是脑室-脑室间隔发育早期功能受损疾病)细胞分子机制的人体体外模型具有重要价值,有望开发出缓解发育期或成年期脑室-脑室间隔功能障碍的治疗策略。本文建立了一种快速可靠的制备方案,可生成含多重类ChP上皮结构的类器官。这些类器官形成脑室,包裹着发育中的功能性皮质神经元细胞。我们证明,包裹类器官的类ChP上皮层在细胞和分子层面均呈现成熟体内ChP的典型特征。这些ChPCO中的皮质细胞(祖细胞和神经元)与类ChP上皮细胞均源自共同祖细胞——hNEct细胞。该细胞可通过CRISPR技术实现高效扩增与基因修饰,从而构建多种疾病模型。
代表多个脑区的类器官已被成功构建(62, 63),其中包括脉络丛(ChP)类器官(9, 10)。佩莱格里尼等人(9)通过单细胞RNA测序证实,其构建的脉络丛类器官中存在皮质神经元;随后,脉络丛类器官被用于验证脉络丛样上皮细胞对SARS-CoV-2病理过程的易感性(10, 11)。已知骨形态发生蛋白4(BMP4)信号通路可诱导神经上皮细胞分化为脉络丛,同时抑制神经谱系的形成(9, 10)。近期研究采用高浓度BMPs构建出几乎完全由脉络丛样上皮细胞组成的类器官(9, 10)。相比之下,我们使用了约低10倍浓度的BMP4,既允许神经谱系的特化并进一步分化为皮质神经细胞,同时仍能让脉络丛-皮质类器官(ChPCOs)中形成脉络丛样上皮组织。这一观点得到了验证(图S1D):我们发现不同浓度的BMP4会改变神经祖细胞的含量。近年来,从人多能干细胞(hPSCs)体外诱导生成人神经上皮细胞(hNEct)的技术,已成为传统单层培养和3D类器官模型中前脑细胞生成的关键手段(35, 64, 65)。本研究中,我们利用hNEct细胞片的发育潜能,构建了复杂的3D脉络丛-皮质类器官(ChPCOs)模型:在该模型中,皮质神经元和脉络丛样上皮细胞这两个不同脑区细胞,由共同的、能自组织的hNEct祖细胞同步发育而来,并通过相互作用促进脑室样结构的形成。我们使用了不同的人多能干细胞系构建ChPCOs,证实了该方案的可重复性。ChPCOs包含体内成熟脉络丛的关键特征,包括顶-基底极性的建立。ChPCOs的时序转录组数据表明其具备产生脑脊液(CSF)的潜力;我们通过多重酶联免疫吸附测定(ELISA)检测ChPCO培养体系中胱抑素C(CST3)、淀粉样前体蛋白(APP)和β2微球蛋白(B2M)的含量,进一步证实了这些脑脊液蛋白的分泌。我们还发现,进化上保守的抗衰老蛋白克洛索(KLOTHO)在ChPCOs的人脉络丛结构中表达——已知克洛索蛋白对多种神经和精神疾病具有保护作用(34)。此外,我们证实ChPCOs中的人脉络丛样上皮细胞在分化过程中,每个细胞可伸出多达9根纤毛;随着时间推移,纤毛类型从以初级纤毛为主显著转变为80%的多纤毛,且单根纤毛的平均长度从0.8 μm增加至3 μm。这一发现与近期一项研究的结果一致:该研究报道,体内脉络丛细胞的多纤毛细胞比例会随时间增加至80%,纤毛长度也会达到3 μm(66)。此外,该研究揭示脉络丛纤毛终生保持 结构,而轴丝纤毛 在断奶后逐渐消失。然而我们的数据显示,随时间推移与纤毛重吸收相关基因未发生显著变化。鉴于节点纤毛通常存在于胚胎发育阶段,对决定机体左右不对称性起关键作用,而轴丝纤毛参与多种组织器官中细胞表面的运动与流体流动,这些数据表明此类脉络丛类器官与人类胎儿脉络丛密切相关,因而可能同时存在节点纤毛与轴丝纤毛,且轴丝纤毛不发生退化。需进一步研究以确认这些纤毛亚型属于可运动的 轴丝型、不可运动的 轴丝型抑或 运动型节点状变体。本文描述的脉络丛类器官可为探索人类脉络丛样上皮细胞亚群中轴丝组织结构与多样性提供重要模型,这可能揭示其在脉络丛功能、皮质发育以及人类脑缺陷(如脑积水)形成中的各自作用。
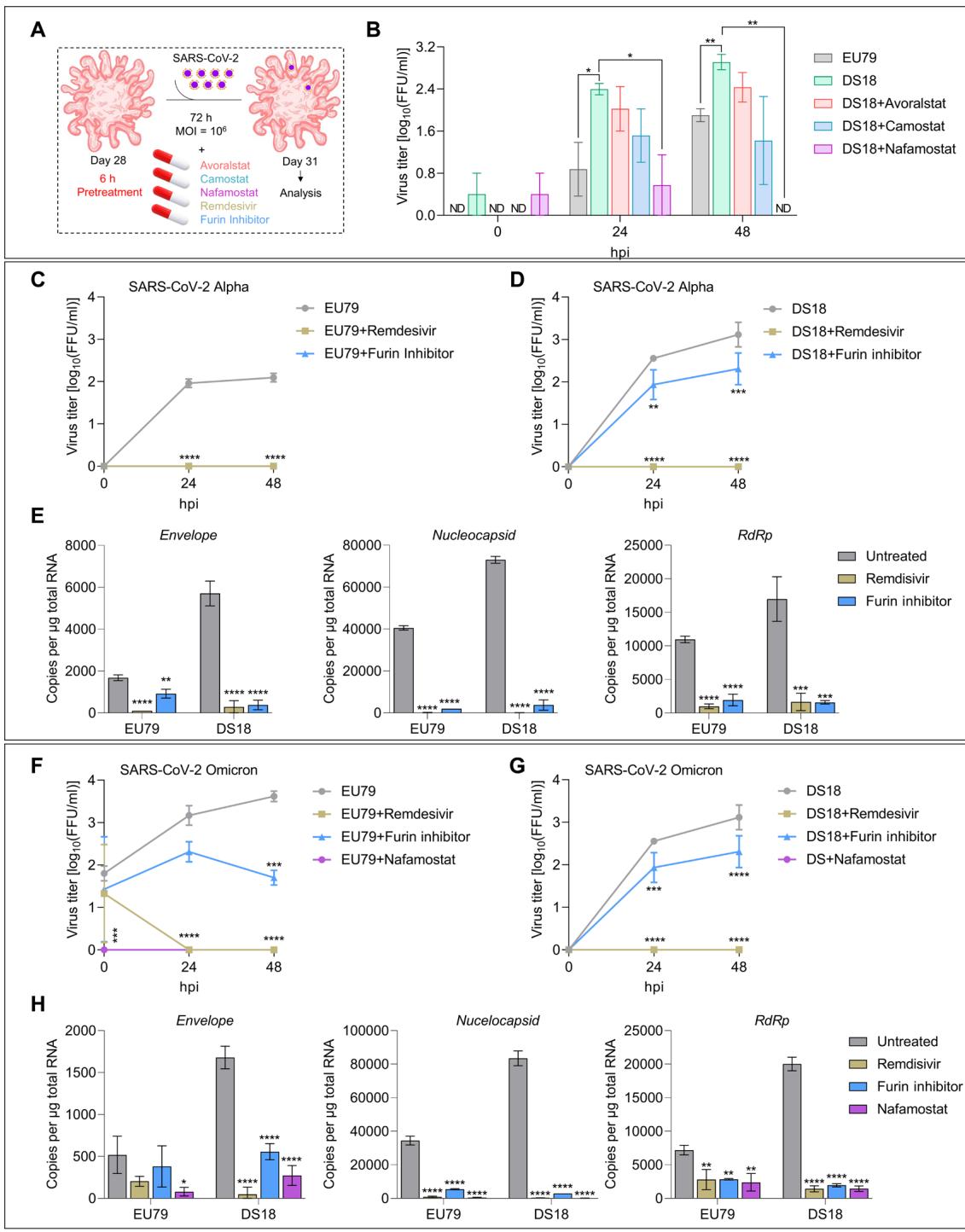
图10. 针对ChPCOs中TMPRSS2活性的FDA批准抑制剂的药物筛选。(A) SARS-CoV-2感染方案示意图。瑞德西韦在感染后立即加入并在感染期间持续给药72小时。(B) 经 TMPRSS2抑制剂处理的感染chPcO上清液中病毒滴度定量。数据以均值 SEM表示。 , (Student’s t检验)。 ;类器官数 汇总于表 。© 经 弗林蛋白酶抑制剂和 瑞德西韦处理的感染chPcO上清液中病毒滴度定量。数据以均值 SEM表示。 汇总于表 S8; (双因素方差分析)。(D) 经 弗林蛋白酶抑制剂和 瑞德西韦处理的感染chPcO上清液中病毒滴度定量。数据以均值 SEM表示。 汇总于表 S8; , , (双因素方差分析)。(E) 第31天chPcOs中SARS-CoV-2包膜蛋白、核衣壳蛋白及RdRp的表达图谱。数据以均值 表示。 , (单因素方差分析)。 汇总于表 。(F) 经 弗林蛋白酶抑制剂、 瑞德西韦及 萘莫司他处理的感染chPcO上清液中病毒滴度定量。数据以均值 表示。 汇总于表 S8。 , (双因素方差分析)。(G) SARS-CoV-2 Omicron毒株( )感染后,经 弗林蛋白酶抑制剂、 瑞德西韦及 萘莫司他处理的chPcO上清液中病毒滴度定量。数据以均值 SEM表示。 3汇总于表 S8。 , (双因素方差分析)。(H) 第31天eU79和dS18 chPcOs中SARS-CoV-2 Omicron毒株包膜蛋白、核衣壳蛋白及RdRp基因表达图谱。数据以均值 表示。 , , (单因素方差分析)。 汇总于表 。
在ChPCOs的皮层组织中,SOX2阳性细胞的分布较为分散,可见于脉络丛样上皮附近及远端。这些SOX2阳性细胞在分化过程中参与形成不同的皮层神经元层。因此,这些皮层神经元并未表现出与内源性大脑相似的排列模式或分层结构。这一现象突显了关于这些类器官内皮层组织架构的重要观察结果。显然,类器官中的皮层组织模式并未复现发育中大脑内源性皮层组织所具备的复杂精密结构(图 4I)。数据表明,虽然类器官成功模拟了大脑结构的某些方面,但此局限性揭示了一个需要进一步研究的关键领域,可能为类器官技术的改进提供指导。ChPCOs中发育中的功能性皮层细胞与脉络丛样上皮细胞并列存在的独特优势在于:可利用患者特异性iPSC系或基因组编辑对照iPSC,研究脉络丛介导的神经发育缺陷,如唐氏综合征的脑室扩大和Bardet-Biedl综合征的脑积水。由于此类神经发育缺陷可能发生在胚胎发育极早期,在人类体系中难以研究,而我们的模型为揭示新型疾病进程及评估旨在挽救脉络丛畸形、促进正常皮层脑发育的药理干预措施效果提供了独特机遇。未来的挑战在于控制hNEct来源的脉络丛样上皮的前后轴特性,同时维持皮层神经元的成熟。近期已实现利用类器官系统融合大脑不同区域的技术,并用于分析复杂神经发育缺陷(67, 68)。类似地,建立具有侧脑室的ChPCOs应能促进构建包含海马等结构的第四脑室脉络丛,例如通过精准调控音猬因子激活,未来可能为在全脑体外三维模型中建立并研究具有复杂网络的前后轴特性提供契机。
我们成功利用多种hPSC细胞系及一种iPSC细胞系制备出ChPCOs,这表明在不同实验条件下诱导ChP形成的方案具有强鲁棒性(图 S2C)。此外,这些ChPCOs可进行培养并进一步成熟,培养周期可延长至目前最长1年。ChPCOs包含前脑组织的基本和功能要素(图4和5)。这些特性使ChPCOs成为研究脉络丛在神经发育异常和神经炎症过程中作用的理想模型系统。
在发育中的前脑中,Olig2最初在腹侧神经干细胞中表达,随后在背侧表达并产生少突胶质细胞(51)。OLIG2是HSA21基因,近期研究发现其在唐氏综合征诱导多能干细胞衍生的腹侧前脑类器官神经干细胞群中过度表达(21)。相比之下,我们发现与整倍体类器官相比,源自DS iPSCs的脉络丛类器官在基因和蛋白水平上均出现OLIG2下调。这种差异很可能源于本研究生成的脉络丛类器官具有背侧前脑特性,我们推测DS脉络丛类器官中OLIG2的下调可能是该模型中OPC标志物(SOX10和PDGFRA)下调的基础。我们进一步发现DS细胞系衍生的脉络丛类器官存在纤毛形成缺陷和脉络丛样上皮极性破坏。与既往研究一致(69),CSF生成相关基因在DS与整倍体类器官间未发现变化。因此,DS类器官中脉络丛样上皮的极性缺陷可能导致其离子转运相关基因表达改变。我们发现不同DS iPSC系衍生的脉络丛类器官表现出不同程度的DS病理外显率,这与既往研究指出DS个体疾病外显率存在差异的现象相符(70),进一步支持DS表型严重程度受遗传背景影响的观点。DS胎儿、2D神经元培养及DS hiPSC衍生的皮质脑类器官均显示星形胶质细胞生成增加(16,71)。相反,我们对前500个变异基因的RNA-seq数据分析未检测到星形胶质细胞相关基因表达水平变化(表S1)。我们推测脉络丛类器官未能复现DS大脑发育的这一特征,可能因其培养方案需长期暴露于BMP4(图1A),而BMP4已知可促进星形胶质细胞分化(72),这或许掩盖了DS与整倍体组间星形胶质细胞生成的内在差异。我们观察到DS脉络丛类器官中细胞粘附和ECM重塑相关基因上调,这种现象在感染(图 9、F和H,及图 S6K)与未感染(图 6E)SARS-CoV-2的情况下均存在。这与既往研究报道一致:DS细胞(如心肌细胞(73)、皮肤成纤维细胞(74)和脐带细胞(75))中涉及细胞粘附和ECM组织的分子广泛失调,这被认为可对DS个体提供特定癌症类型的保护作用(76)。在大脑中,DS神经细胞(包括星形胶质细胞(77)和神经元(78,79))表现出细胞粘附和ECM相关基因失调,而神经祖细胞(77)则未出现。这表明细胞粘附和ECM重塑的改变可能在DS大脑中全局性发生,潜在地影响DS个体的大脑发育和功能。
产前获得的病毒感染可能对发育中的胎儿大脑产生破坏性影响(80)。数份临床报告显示,妊娠期感染SARS-CoV-2的女性所娩出的婴儿中,有 在12月龄时出现发育迟缓现象(81, 82)。值得注意的是,神经发育性病变与早产无关,这表明SARS-CoV-2具有特定的神经嗜性机制,而非仅仅导致妊娠并发症(83)。体外实验表明,SARS-CoV-2对人类脉络丛(10)、神经元(84)和星形胶质细胞(85)具有神经侵袭和嗜神经特性,提示SARS-CoV-2可能影响早期大脑发育。鉴于TMPRSS2基因位于21号染色体,且流行病学研究已发现唐氏综合征(DS)人群对SARS-CoV-2存在显著易感性(其COVID-19相关住院风险增加4倍,死亡风险增加10倍)(24, 25),我们利用DS脉络丛类器官(ChPCOs)作为模型研究SARS-CoV-2感染。在暴露于SARS-CoV-2后,我们观察到DS iPSCs来源的ChPCOs中脉络丛样上皮细胞被大量感染,并随后入侵皮层组织。由于皮层类器官(COs)感染程度较轻,ChPCOs中的脉络丛样上皮细胞很可能作为病毒“复制中枢”,支持病毒入侵并扩散至其他皮层细胞,这与既往研究指出的尸检脑组织中COVID-19神经系统症状与脉络丛屏障细胞紊乱相关(86)的结论一致。我们在此模型中发现,TMPRSS2和FURIN(而非ACE2和NRP1)在DS ChPCOs的脉络丛样上皮细胞中显著上调。如前所述,DS ChPCOs还表现出脉络丛上皮极性缺陷。脉络丛上皮极性的紧密连接可作为入侵屏障并阻碍病毒内吞作用。因此,DS类器官中TMPRSS2剂量增加与脉络丛样上皮紧密连接缺陷可能共同促进SARS-CoV-2侵入及后续神经病理变化。基因表达研究显示DS个体、DS iPSCs及DS Ts65D小鼠模型存在全基因组转录组失调(87)。DS个体在病毒性呼吸道感染期间会出现过度免疫反应等严重并发症(29)。近期研究表明脉络丛中I型干扰素(IFN-I)表达具有年龄依赖性,并对大脑功能产生负面影响(88)。人类脉络丛中也存在IFN-I表达特征(88)。这些数据揭示了脉络丛中慢性衰老诱导的IFN-I特征(常与抗病毒反应相关)(88)。另一方面,DS个体因免疫应答受损而在病毒感染期间出现严重并发症(53)。在无任何可检测感染的情况下,DS个体表现出慢性过度活跃的IFN反应(89),以及多种已知作用于IFN信号下游的细胞因子和趋化因子水平升高(90)。这部分归因于IFN受体(IFNRs)由人类21号染色体(HSA21)编码(89)。虽然我们发现多个与病毒感染相关的HSA21基因(MX2、TMPRSS2、ADAMTS5和RUNX1)在ChPCOs中表达,但未检测到IFN受体及IFN信号通路分子的失调,且31日龄ChPCOs及SARS-CoV-2感染的ChPCOs中普遍缺乏IFN相关基因表达。相反,我们观察到感染ChPCOs细胞的凋亡通路激活和死亡(图S8,A和B)。但需注意,有研究显示脉络丛在SARS-CoV-2感染后通过多种IFN相关通路广泛上调炎症基因表达(8)。因此,采用空间转录组学技术或分离31日龄ChPCOs的皮层与脉络丛样区域,可能揭示特定炎症基因集合是否仅在DS脉络丛样成分中富集。
我们进一步发现,使用美国食品药品监督管理局(FDA)批准的药物(阿沃拉司他、卡莫司他、萘莫司他)抑制跨膜丝氨酸蛋白酶2(TMPRSS2)可显著降低所有类器官中的SARS-CoV-2复制,这表明TMPRSS2是病毒进入整倍体(EU)和唐氏综合征(DS)脉络丛-皮质类器官(ChPCOs)细胞所必需的。与先前报道一致(91),我们发现萘莫司他抑制SARS-CoV-2感染和复制的效力高于阿沃拉司他和卡莫司他。此前有研究表明,人类神经元仅低水平表达血管紧张素转换酶2(ACE2),且不表达TMPRSS2(92)。而本研究中我们发现,脉络丛样上皮细胞高表达TMPRSS2和弗林蛋白酶(furin),且在唐氏综合征(DS)类器官中其表达水平进一步升高(图8A、B)。我们的数据显示,抑制TMPRSS2会显著影响病毒的感染和复制,这进一步凸显了该受体在SARS-CoV-2感染ChPCOs过程中的重要作用,并为“表达TMPRSS2的脉络丛样上皮细胞是SARS-CoV-2感染和传播的主要储存库”提供了额外证据。抑制弗林蛋白酶也能显著减少DS ChPCO中的病毒复制,而在整倍体ChPCO中,弗林蛋白酶抑制可彻底清除病毒。已知弗林蛋白酶对病毒刺突蛋白的切割有助于病毒进入细胞(但并非绝对必需),因此这些数据表明:在缺乏弗林蛋白酶活性时,DS ChPCO可能仍有足够量的TMPRSS2以支持病毒进入;然而,在TMPRSS2表达量较低的整倍体类器官中,弗林蛋白酶可能是SARS-CoV-2感染所严格必需的。此外,我们发现使用FDA批准的COVID-19治疗药物瑞德西韦(remdesivir)处理后,整倍体和DS ChPCO中的病毒均被彻底清除,这与该药物对SARS-CoV-2的高效抑制作用相符(93)。
我们的研究结果显示,唐氏综合征脉络丛器官样体对SARS-CoV-2感染的易感性升高,这与临床研究报道的唐氏综合征个体对重症COVID-19具有医疗脆弱性的结论相符(25, 94)。这种增强的易感性可能与其既有的健康脆弱性密切相关:例如唐氏综合征个体常表现为免疫系统功能受损,这可能削弱机体对病毒建立强效防御的能力,从而促使病毒进入脑部——正如本研究所观察到的现象。此外,唐氏综合征群体普遍存在的心脏缺陷和呼吸系统问题可能进一步加剧其对SARS-CoV-2的易感性。具体而言:合并心脏缺陷的唐氏综合征个体可能出现心血管功能减退,导致重要器官供氧不足;而SARS-CoV-2主要攻击的呼吸系统在唐氏综合征个体中本就存在结构异常与功能受限;受损的心血管功能可能加重心脏负荷,导致感染期间出现更严重的临床结局。这些因素的交互作用揭示了基础健康状况与唐氏综合征个体感染SARS-CoV-2后重症风险升高之间的复杂关联。这些健康挑战可能共同放大SARS-CoV-2对神经系统的影响,强调在评估该脆弱群体的病毒感染风险时必须综合考虑其整体健康背景。
总之,我们的研究强调了ChPCOs在唐氏综合征等神经发育疾病建模及(冠状病毒)病毒研究中的相关性,并指出蛋白酶蛋白(TMPRSS2、FURIN)作为抑制SARS-CoV-2嗜神经性的重要治疗靶点的价值。ChPCOs应能进一步助力识别和筛选针对未来新发病毒的疗法,并为涉及ChP功能异常的先天性疾病建模提供支持。
¶ 材料与方法
¶ 人类胚胎干细胞培养和一氧化碳生成
人胚胎干细胞H9(来自威斯康星国际干细胞库,WiCell研究所的WA09细胞)、WTC iPSC(由B. Conklin馈赠)、G22、DS18及EU79 iPSC细胞系(本实验室保存)均按照STEMCELL Technologies公司方案(详见https://www.stemcell.com/maintenance-of-human-pluripotent-stem-cells-in-mtesr-1.html),在基质胶(STEMCELL Technologies,货号354277)上进行无饲养层培养,使用mTeSR培养基(STEMCELL Technologies,货号85851),具体方法如我们近期报道所述(95)。
¶ ChP-CO 生成
为生成ChPCOs,将hPSC集落以 至 密度接种于铺有人胚胎干细胞专用基底膜基质(STEMCELL Technologies,目录号354277)的六孔板中(96)。在进行神经外胚层诱导前,使用mTeSR培养基维持hPSC集落1天。为生成神经外胚层集落,将hPSC集落在N2培养基中培养3天:培养基成分为DMEM/F12(Gibco,目录号11320-33)、 B-27补充剂(Gibco,目录号17504044)、 补充剂(Gibco,目录号17502-048)、 MEM非必需氨基酸(Gibco,目录号11140-050)、 青霉素/链霉素(Gibco,目录号15140148)及 -巯基乙醇(Gibco,目录号21985-023),并添加双SMAD抑制剂SB-431542( )和LDN 193189( )。每日更换含抑制剂的新鲜N2培养基。第四天,如我们近期报道的方法(35),使用分散酶( )剥离诱导形成的神经外胚层集落以形成神经球。随后4天中,这些神经球每日在补充了bFGF( ;R&D Systems,目录号233-FB-01M)、 CHIR99021(Sigma-Aldrich,目录号SML1046-5MG)及BMP4( )(Thermo Fisher Scientific,目录号PHC9391)的N2培养基中培养。接着将模式化神经球包埋于基质胶(STEMCELL Technologies,目录号354277)中,并转换为终末分化培养基DMEM-F12(Gibco,目录号11320-33):包含神经基础培养基(Gibco,目录号A35829-01)、 (Gibco,目录号17502-048)、 培养基中添加 胰岛素(Sigma-Aldrich)、 GlutaMAX、 MEM非必需氨基酸(Gibco,目录号11140-050)、 青霉素/链霉素(Gibco,目录号15140148)、 培养基中添加 -巯基乙醇(Gibco,目录号21985-023)及 B-27补充剂(Gibco,目录号17504044),并添加3 CHIR99021与BMP4( )。每周更换三次新鲜培养基。所有实验均遵循昆士兰大学伦理指导原则,并获昆士兰大学人类研究伦理委员会批准(批准号2019000159)。
¶ 定量逆转录聚合酶链反应
类器官总RNA的提取方法如前所述(97)。对于qPCR,使用 提取的RNA,通过第一链cDNA合成试剂盒(Thermo Fisher Scientific,货号K1612)制备互补DNA(cDNA)。采用SYBR Green(Applied Biosystem,货号A25742),PCR标准反应条件参照制造商说明设置。病毒RNA定量时,使用1 总RNA通过qScript cDNA SuperMix(Quanta Bio,货号95548)进行逆转录。cDNA按1:10稀释后,取 该溶液作为qRT-PCR的模板使用。qPCR在Applied Biosystem QuantStudio 6仪器上采用QuantiNova SYBR Green PCR试剂盒(Qiagen,货号208056)进行。通过将样本的Ct值与通过相同引物对终点RT-PCR生成的DNA标准品扩增所得标准曲线进行比较,确定RNA拷贝数。PCR引物采用美国国家生物技术信息中心(NCBI)免费在线系统设计,所有RT-qPCR引物列于表 S6。所有实验对每个样本进行生物学三重重复,表达值均以各样本的甘油醛-3-磷酸脱氢酶(GAPDH)表达值进行标准化。使用GraphPad Prism 9计算并绘制平均值与标准差。
¶ 免疫组织化学
组织处理与免疫组织化学(IHC)实验流程参照文献(98)所述进行。简言之,将类器官在室温下用 多聚甲醛固定60分钟,随后用 磷酸盐缓冲盐水在室温下洗涤3次,每次10分钟。固定后的类器官浸入 的PBS配制的 蔗糖溶液,待其沉降后置于干冰上用最佳切割温度化合物(O.C.T.)与 蔗糖按3:2比例混合的包埋剂中进行包埋。将包埋组织连续切片为14微米厚度,贴附于Superfrost载玻片(赛默飞世尔科技,产品编号SF41296)上。 进行IHC时,先将类器官切片在室温下用 洗涤3次(每次10分钟),随后用含 牛血清白蛋白(BSA)(西格玛奥德里奇,产品编号A9418-50G)与 Triton X-100的 PBS封闭1小时。一抗于 孵育过夜后,用PBS在室温下洗涤3次(每次10分钟)。对于免疫细胞化学实验(99),细胞在室温下用含 PFA的1×PBS固定10分钟,随后按上述方法用 洗涤、封闭并添加一抗。 组织与细胞在室温下与相应二抗孵育1小时后进行封片及成像。整体封片操作参照先前方法(100)。所有样本均使用Hoechst 33342(英杰公司,产品编号H3570)进行复染。图像采集依托昆士兰大学生物医学科学院影像平台,使用共聚焦显微镜(徕卡TCS SP8)完成。本研究使用的一抗信息列于表 S7。Alexa Fluor 488–、Alexa Fluor 546–及Alexa Fluor 633–标记的二抗购自Jackson ImmunoResearch实验室。
¶ RNA测序
RNA采用TRI试剂(美国Sigma-Aldrich公司)从三组独立类器官池中提取,方法参照前期文献(101)。RNA完整性通过TapeStation 4200系统(美国安捷伦公司)检测,选取RIN > ≥8的样本使用TrueSeq RNA建库试剂盒v2 A组(美国Illumina公司)进行文库构建。经条形码标记的cDNA文库混合后,使用NextSeq 500/550高通量75循环试剂盒v2.5(美国Illumina公司)在Illumina NextSeq 500测序仪上进行测序。图像采集、处理及fastq数据拆分均按仪器内置软件流程完成,操作步骤参照前期文献(102) 。
¶ 差异基因表达分析
使用FastQC软件v.0.72对原始测序数据进行质量控制。随后使用Trimmomatic软件v.0.36.6按以下参数修剪读取序列:ILLUMINACLIP : TruSeq3-SE : 2 : 30 : 10,LEADING : 32,TRAILING : 32,SLIDINGWINDOW : 4 : 20,MINLEN : 16。将修剪后的读取序列通过Bowtie2 v.2.4.4比对至SARS-CoV-2基因组(GISAID收录编号:EPI_ISL_944644)。使用Integrative GenomicViewer v.2.13.1(美国博德研究所)对已比对的读取序列进行可视化与定量分析。人类源读取序列通过HISAT2 v.2.2.1比对至hg38基因组组装。基因计数采用featureCounts v2.0.1完成,计数模式设为“Union”,链特异性设置为“无链特异性”,特征类型为“外显子”,ID属性为Gene_ID。
差异基因表达分析使用edgeR v.4.2进行。低丰度读数[<每百万计数(cpm)]从数据集中移除,并采用M值修剪均值(TMM)方法对文库大小和组成偏倚进行标准化。通过多维尺度分析对标准化数据进行分析,并用于构建拟似然负二项广义对数线性模型。随后对对比组ChP-NC、DS18_ChP-EU79_ChP、SARS_DS18-Mock_DS18及SARS_EU79-Mock_EU79应用Treat检验(glmTreat),以识别组间表达差异至少达一个对数 的基因。对对比组(SARS_DS18-Mock_DS18)-(SARS_EU79-Mock_EU79)应用拟似然F检验(glmQLFTest),以识别DS18类器官中特异性受感染影响的基因。若错误发现率(FDR)矫正后的P值 ,则认定基因存在差异表达。使用ggplot2 v.3.3.2绘制基因表达数据。通过DAVID v6.8数据库进行基因本体论和京都基因与基因组百科全书(KEGG)通路富集分析。将富集数据与表达值整合后,采用GOplot v.1.0.2 R包计算z分数并运用ggplot2 v.3.3.2绘图。热图使用gplots v3.1.2程序包的heatmap.2函数生成。
¶ 透射电子显微镜
透射电子显微镜(TEM)检测依照文献(103)进行。简言之,将类器官置于含 戊二醛和 多聚甲醛的 二甲砷酸钠缓冲液( 配制)中, 固定过夜。首先在室温下用0.1M二甲砷酸钠缓冲液洗涤类器官三次,每次10分钟;随后室温浸入 锇酸溶液( 锇酸与 二甲砷酸盐缓冲液混合)中处理90分钟。将染色液更换为 铁氰化钾溶液(4. 二甲砷酸盐缓冲液与 铁氰化钾混合),室温处理90分钟。接着用去离子水在室温下洗涤类器官三至五次,直至水相完全澄清,随后将类器官浸入硫代卡巴肼溶液0.1g 硫代卡巴肼(需锁柜保存)溶于10 ml水]中, 处理45分钟。为去除背景染色,在室温下用去离子水洗涤类器官四至五次,随后浸入0.1 M二甲砷酸盐缓冲液配制的 锇酸溶液中,室温处理30分钟。再次用水洗涤以消除黑色背景。将洗涤后的类器官浸入 醋酸铀酰溶液中 过夜处理,随后转入 天冬氨酸溶液中 孵育30分钟。孵育后的类器官用去离子水洗涤三次,在室温下静置30分钟。对于包埋处理,类器官在室温下通过一系列乙醇浓度梯度( 、 、 、 、 、 和 )各脱水30次。随后用Durcupan树脂在室温下浸渗12小时。包埋后的类器官在 下固化48小时,再进行修块和成像。
¶ 多重ELISA
用于研究脑脊液生物标志物(CST3、APP和B2M)水平的类器官培养基分别在第7、14、21、28、42和56天进行收集。采用人源磁珠Luminex检测试剂盒(R&D Systems,产品编号LXSAHM-03)按照制造商说明书对收集培养基中的CST3、APP和B2M水平进行检测,并使用MAGPIX仪器(Luminex Corp.)读取数据。
¶ MEA记录与分析
培养于终末分化培养基中的完整类器官,在记录前被转移至MEA板[4096通道,具备细胞级分辨率( ),覆盖大区域(最大 ),每通道采样频率 ,3Brain公司]并在BioCAM X系统(3Brain公司)中进行记录。移除各孔内培养基直至仅存薄层液体,使类器官在 温度与5%CO2条件下贴附电极网格。记录过程中向预热培养基添加 谷氨酸(Sigma-Aldrich,货号G1251-100G)或 NMDA(Sigma-Aldrich,货号M3262-25MG)以刺激类器官神经元活动。为记录对ChPCOs的抑制性药理效应,向培养基中添加 M荷包牡丹碱(Bicuculline,Sigma-Aldrich,货号14340-25MG)。基线活动记录在不添加药物条件下进行。数据导出为.csv文件后采用BrainWave软件分析。平均放电频率计算采用精确时序峰电位检测算法(PTSD),阈值设置为背景噪声标准差8倍以上,设定2毫秒峰值存续期,且每次检测到峰电位后施加2毫秒不应期。爆发事件检测采用最大峰电位间隔2毫秒、最小峰电位数5个的标准。
¶ Western印迹
Western blotting实验按照先前描述的方法进行(34)。简要来说,使用含有蛋白酶和磷酸酶抑制剂混合液(Roche)的Pierce RIPA缓冲液(Thermo Fisher Scientific,货号89900)裂解类器官。采用超声破碎仪处理类器官后,使用Pierce BCA蛋白定量试剂盒(Thermo Fisher Scientific,货号23227)按照制造商说明定量蛋白浓度。提取的蛋白质在 加热10分钟后上样。等量蛋白通过Mini-PROTEAN TGX Stain-Free预制胶(Bio-Rad,货号4568044)进行分离。采用iBlot 2 PVDF迷你转印栈(Invitrogen,货号IB24002)进行转膜。室温下用 脱脂牛奶/TBST溶液 tris-HCl (pH 7.6), , Tween 20封闭膜1小时,随后与一抗(用 BSA稀释)在 孵育12小时。本实验所用一抗详见表S6。孵育后的膜用 TBST在室温下洗涤三次,每次10分钟,随后与二抗(用 脱脂牛奶/ TBST按1:5000稀释)室温孵育1小时。最后,将孵育后的膜在室温下用 TBST再洗涤三次,每次10分钟,并使用Clarity Western ECL底物(Bio-Rad,货号170-5060)进行显色。
¶ SARS-CoV-2感染脉络丛类器官
SARS-CoV-2 分离株 QLD1517/2021(Alpha 变异株,GISAID登录号 EPI_ISL_944644)第 2 代,采集自感染者的鼻咽抽吸物,由昆士兰州卫生部昆士兰健康法医与科学服务中心提供。获得的分离株在 Vero E6-TMPRSS2 细胞上进行扩增以制备病毒储备液。病毒滴度通过在 Vero E6 细胞上进行的免疫荧光灶形成测定法确定。将类器官置于含 FFU 病毒的 培养基中,于 孵育 6 小时,随后移除接种物,将类器官清洗三次后置于 新鲜培养基中维持培养。于感染后 0、24、48和 72 小时采集培养液以监测病毒复制情况。类器官预先在含 TMPRSS2 抑制剂(avoralstat、camostat 或 nafamostat)或 弗林蛋白酶抑制剂 D-RVKR-CMK 的培养基中孵育 6小时。药物处理后,以每枚类器官 的剂量用 SARS-CoV-2 感染过夜。SARS-CoV-2 感染后立即加入瑞德西韦( M)。随后移除接种物,将类器官清洗三次后置于含相同浓度相应药物的培养基中。
¶ 免疫荧光灶形成试验
细胞培养液以十倍系列稀释法在含 胎牛血清的DMEM中制备,每个稀释度取 感染预先铺于96孔板的 个Vero E6细胞。 孵育接种物1小时后,每孔加入 覆盖培养基。该覆盖培养基由M199培养基[含 胎牛血清、链霉素( ml)、青霉素( )及 ( 升)]与 羧甲基纤维素(美国Sigma-Aldrich)按1:1比例混合而成。感染后第1天,移除覆盖培养基,将细胞板浸入冰镇 丙酮(以 BS稀释)于 固定1小时。后续步骤在PC2实验室进行。细胞单层经干燥后,用Clear Milk封闭液(每孔 ,美国Pierce)封闭60分钟。病毒刺突蛋白采用1:1000稀释的CR3022小鼠单克隆抗体(每孔 )孵育1小时进行检测,随后用含 Tween 20的磷酸盐缓冲液洗涤五次,再与1:1000稀释的山羊抗小鼠IRDye 800CW二抗(每孔 ,美国LI-COR)孵育1小时,并进行五次PBST洗涤。所有抗体均采用Clear Milk封闭缓冲液(美国Pierce)稀释,孵育过程均在 进行。最后使用Odyssey CLx成像系统(美国LI-COR)扫描平板,参数设置如下:通道 与700、强度 自动、分辨率 、质量 中等、焦距 毫米。统计病毒复制斑数量并计算病毒滴度。
¶ 统计分析
正态分布数据以独立实验的平均值 ± 标准差表示。对于非正态分布数据,则采用中位数 ± 标准差表示数值。生物重复次数及样本量均在图注中注明。t检验以及单因素或双因素方差分析(ANOVA)分别用于比较两组及两组以上的数据。Tukey事后分析用于与单一对照组进行比较。Kolmogorov-Smirnov检验用于评估分布差异。统计分析使用GraphPad Prism 9软件进行。最小统计学显著性定义为P< 0.05。
¶ 补充材料
该PDF文件包含:图S1至S9以及表S1至S8的图注
本手稿的其他补充材料包括:附表S1至S8
¶ 参考文献
- M. P. Lun, E. S. Monuki, M. K. Lehtinen, 脉络丛-脑脊液系统的发育与功能。《自然综述:神经科学》16, 445–457 (2015) - PMC - PubMed
- T. Shimogori, V. Banuchi, H. Y. Ng, J. B. Strauss, E. A. Grove, 表达BMP、Wnt和FGF蛋白的胚胎信号中心相互作用以模式化大脑皮层。《发育》131, 5639–5647 (2004) - PubMed
- D. F. Emerich, S. J. Skinner, C. V. Borlongan, A. V. Vasconcellos, C. G. Thanos, 脉络丛在大脑的兴起、衰退与修复中的作用。Bioessays 27, 262–274 (2005) - PubMed
- M. G. Netsky, S. Shuangshoti, 《健康与疾病中的脉络丛》(Butterworth-Heinemann, 2013)
- N. R. Saunders, K. M. Dziegielewska, K. Møllgård, M. D. Habgood, 胎儿与新生儿脑屏障机制的生理学与分子生物学。《生理学杂志》596, 5723–5756 (2018) - PMC - PubMed
- L. Zhu, L. R. Stein, D. Jin, K. He, G.-Q. Yu, L. Zhan, T. E. Larsson, L. Mukherjee, Klotho调控脉络丛中的脑-免疫系统界面。Proc. Natl. Acad. Sci. U.S.A. 115, e11388–e11396 (2018)
- K. Oshio, H. Watanabe, Y. Song, A. Verkman, G. T. Manley, 缺失脉络丛水通道蛋白Aquaporin-1的小鼠脑脊液生成和颅内压降低。FASEB J. 19, 76–78 (2005)
- P. A. Johnson, 《脉络丛及其对发育神经发生的影响》。《神经科学前沿》8, 340 (2014) - PMC - PubMed
- L. Pellegrini, C. Bonfio, J. Chadwick, F. Begum, M. Skehel, M. A. Lancaster, 《具有脑脊液生成功能的人类中枢神经系统屏障形成类器官》。《科学》369, eaaz5626 (2020)
- F. Jacob, S. R. Pather, W.-K. Huang, F. Zhang, S. Z. H. Wong, H. Zhou, B. Cubitt, W. Fan, C. Z. Chen, M. Xu, M. Pradhan, D. Y. Zhang, W. Zheng, A. G. Bang, H. Song, J. Carlos de la Torre, G. I. Ming, 人类多能干细胞衍生的神经细胞与脑类器官揭示SARS-CoV-2神经嗜性主要靶向脉络丛上皮细胞。《细胞·干细胞》27, 937–950.e9 (2020)
- L. Pellegrini, A. Albecka, D. L. Mallery, M. J. Kellner, D. Paul, A. P. Carter, L. C. James, M. A. Lancaster, SARS-CoV-2感染脑脉络丛并破坏人脑类器官中的血-脑脊液屏障。《细胞·干细胞》27, 951–961.e5 (2020)
- S. E. Parker, C. T. Mai, M. A. Canfield, R. Rickard, Y. Wang, R. E. Meyer, P. Anderson, C. A. Mason, J. S. Collins, R. S. Kirby, A. Correa, 2004–2006年美国部分出生缺陷的全国出生患病率估计值更新。《畸形学》88, 1008–1016 (2010)
- J. A. Golden, B. T. Hyman, 《21三体综合征中颞上侧新皮层的发育异常》。《神经病理学与实验神经学杂志》53, 513–520 (1994)
- B. L. Shapiro, 《小脑发育不稳定性及其与唐氏综合征的相关性》, 收录于《唐氏综合征大脑中的蛋白质表达》, G. Lubec 编 (施普林格维也纳出版社, 2001年), 第11–34页
- S. Guidi, E. Ciani, P. Bonasoni, D. Santini, R. Bartesaghi, 唐氏综合征胎儿小脑中广泛存在的增殖障碍与细胞减少。《脑病理学》21, 361–373 (2011)
- S. Guidi, P. Bonasoni, C. Ceccarelli, D. Santini, F. Gualtieri, E. Ciani, R. Bartesaghi, 唐氏综合征胎儿海马区神经元总数减少:神经发生障碍和细胞死亡增加所致。《脑病理学》18, 180–197 (2008)
- L. Chakrabarti, T. K. Best, N. P. Cramer, R. S. E. Carney, J. T. R. Isaac, Z. Galdzicki, T. F. Haydar, Olig1和Olig2的三重复制导致唐氏综合征的发育性脑缺陷。Nat. Neurosci. 13, 927–934 (2010)
- J. L. Olmos-Serrano, H. J. Kang, W. A. Taylor, J. C. Silberberg, F. Cheng, Y. Zhu, M. Pletikos, L. Jankovic-Lapan, N. P. Cramer, Z. Galdzicki, J. Goodrich, A. Peters, C. Setareh, I.德拉莱, J. A. Golden, T. F. Haydar, N. Sehested, 唐氏综合征发育脑转录组揭示了有缺陷的少突胶质细胞分化与髓鞘形成过程。《神经元》89, 1208–1222 (2016)
- M. Lavoie, T. Nakahara, S. Asada, K. Ishihara, K. Amano, A. Shimohata, H. Sogo, K. Yamakawa, 唐氏综合征小鼠脑室扩大由Pcp4剂量依赖性纤毛功能障碍引起。《人类分子遗传学》26, 923–931 (2017)
- D. F. Galati, K. D. Sullivan, A. T. Fan, J. M. Espinosa, C. G. Pearson, 21三体抑制纤毛形成和功能。《发育细胞》46, 641–650.e6 (2018)
- Xu Rong, A. T. Bronner, S. Li, Liu Junjie, H. Jin, H. Xue, Pang Zhipeng, Jin Wenyuan, R. P. Hart, Liu Yang, Jiang Peng, Olig2在基于人类诱导多能干细胞的唐氏综合征类器官及嵌合小鼠模型中驱动异常神经发育表型。《细胞干细胞》24, 908–926.e8 (2019)
- Tang Xiaoyang, Xu Lei, Wang Jing, Hong Yan, Wang Yong, Zhu Qi, Wang Dong, Zhang Xiaoyang, Liu Chunyu, Fang Kehan, Han Xu, Wang Shuo, Wang Xin, Xu Min, A. Bhattacharyya, Guo Xu, Lin Min, Liu Yang, DSCAM/PAK1通路抑制逆转唐氏综合征患者iPSC来源脑类器官的神经发生缺陷。《临床研究杂志》131, e135763 (2021)
- I. Ali, P. A. Goh, A. Murray, E. Portelius, E. Gkanatsiou, G. Gough, K. Y. Mok, D. Koschut, R. Brunmeir, Y. J. Yeap, N. L. O’Brien, J. Groet, X. Shao, S. Havlicek, N. R. Dunn, H. Kvartsberg, G. Brinkmalm, R. Hithersay, C. Startin, S. Hamburg, M. Phillips, K. Pervushin, M. Turmaine, D. Wallon, A. Rovelet-Lecrux, H. Soininen, E. Volpi, J. E. Martin, J. N. Foo, D. L. Becker, A. Rostagno, J. Ghiso, Krsnik, G. Imić, Kostović, Mitre, A. Strydom, E. Fisher, F. Wiseman, D. Nizetic, J. Hardy, V. Tybulewicz, A. Karmiloff-Smith, P. T. Francis, K. Blennow, A. Strydom, J. Hardy, H. Zetterberg, D. Nilsson, S. C. Londdown, 患者特异性阿尔茨海默样病理在21三体脑类器官中揭示BACE2为人类大脑中基因剂量敏感的AD抑制因子。《分子精神病学》26, 5766–5788 (2021)
- A. K. Clift, C. A. C. Coupland, R. H. Keogh, H. Hemingway, J. Hippisley-Cox, 唐氏综合征患者的COVID-19死亡风险:一项针对800万成年人的队列研究结果。Ann. Intern. Med. 174, 572–576 (2020)
- A. Hüls, A. C. S. Costa, M. Dierssen, R. A. Baksh, S. Bargagna, N. T. Baumer, A. C. Brandão, A. Carfi, M. Carmona-Iragui, B. A. Chicoine, S. Ghosh, M. Lakhanpaul, C. Manso, M. A. Mayer, M. D. C. Ortega, D. R. de Asua, A.-S. Rebillat, L. A. Russell, G. Sgandurra, D. Valentini, S. L. Sherman, A. Strydom, 《唐氏综合征个体对重症COVID-19的医学脆弱性——来自21三体综合征研究学会和英国ISARic4c调查的数据》。EClinicalMedicine 33, 100769 (2021)
- B. L. P. Bloemers, G. M. Van Bleek, J. L. L. Kimpen, L. Bont, 唐氏综合征儿童先天免疫系统的明显异常。《儿科杂志》156, 804–809.e5 (2010)
- P. Araya, Katherine A. Waugh, Kelly D. Sullivan, Nicholas G. Núñez, E. Roselli, Keith P. Smith, Ross E. Granlas, Angela L. Rachubinski, Estrada B. Enriquez, Eric T. Butcher, R. Mintz, Katherine D. Tuttle, Tulia C. Bruno, M. Marchioni, Joaquín M. Espinosa, 21三体综合征使T细胞谱系失调,趋向于伴随干扰素过度活跃的自免疫易感状态。《美国国家科学院院刊》116, 24231–24241 (2019)
- R. Pérez-Padilla, R. Fernández, C. García-Sancho, F. Franco-Marina, O. Aburto, H. López-Gatell, I. Bojórquez, 《2009年甲型H1N1流感病毒与唐氏综合症患者》, 《新发传染病》16, 1312–1314 (2010) - PMC - PubMed
- B. L. P. Bloemers, A. M. Van Vugt, M. E. Veldman, R. J. B. J. Hemke, C. J. M. Broers, K. Van Den Ende, J. L. L. Kimpen, J. L. M. Strengers, L. J. Bont, 《唐氏综合征:呼吸道合胞病毒细支气管炎的一个新型危险因素——一项前瞻性出生队列研究》。《儿科杂志》120, e1076–e1081 (2007)
- M. Chan, J. J. Park, T. Shi, F. Martinón-Torres, L. Bont, H. Nair, R. S. V. Network, 唐氏综合征儿童中呼吸道合胞病毒(RSV)相关急性下呼吸道感染的负担:一项系统评价与荟萃分析。《全球健康杂志》7, 020413 (2017)
- Chen Xiaoqing, Xing Zhe, Chen Qidong, R. J. Salvi, Zhang Xu, B. Tycko, W. C. Mobley, Yu Yiner, 唐氏综合征年龄相关临床表现的机制分析。《衰老神经科学前沿》13, 700280 (2021)
- S. R. Stein, S. C. Ramelli, A. Grazioli, J.-Y. Chung, M. Singh, C. K. Yinda, C. W. Winkler, J. Sun, J. M. Dickey, K. Ylaya, S. H. Ko, A. P. Platt, P. D. Burbelo, M. Quezado, S. Pittaluga, M. Purcell, V. J. Munster, F. Belinky, M. J. Ramos-Benitez, E. A. Boritz, I. A. Lach, D. L. Herr, J. Rabin, K. K. Saharia, R. J. Madathil, A. Tabatabai, S. Soherwardi, M. T. McCurdy; NIH COVID-19 Autopsy Consortium, K. E. Peterson, J. I. Cohen, E. de Wit, K. M. Vannella, S. M. Hewitt, D. E. Kleiner, D. S. Chertow, SARS-CoV-2感染及其在人体和脑中的尸检留存证据。《自然》612, 758–763 (2022)
- G. Caronia-Brown, M. Yoshida, F. Gulden, S. Assimacopoulos, E. A. Grove, 皮质边缘调节新皮质的大小和模式。《发育》141, 2855–2865 (2014) - PubMed
- M. R. Shaker, J. Aguado, H. K. Chaggar, E. J. Wolvetang, Klotho抑制人类脑类器官中的神经元衰老。NPJ 衰老机制与疾病 7, 18 (2021)
- M. R. Shaker, Z. L. Hunter, E. J. Wolvetang, 用于在体外模拟大脑神经元衰老的皮质脑类器官的稳健且高度可重复生成方法。J. Vis. Exp. (可视化实验杂志), e63714 (2022)
- M. Watanabe, Y.-J. Kang, I. M. Davies, S. Meghpara, K. Lau, C.-Y. Chung, J. Kathiriya, A.-K. Hadjantonakis, E. S. Monuki, BMP4足以诱导脉络丛上皮源自胚胎干细胞的神经上皮前体细胞的命运。《神经科学杂志》32, 15934–15945 (2012)
- M. P. Lun, M. B. Johnson, K. G. Broadbelt, M. Watanabe, Y.-J. Kang, K. F. Chau, M. W. Springel, A. Malesz, A. M. Sousa, M. Pletikos, 脉络丛空间异质性转录组编码位置身份并促进区域性脑脊液生成。《神经科学杂志》35, 4903–4916 (2015)
- S. A. Liddelow, 脉络丛与血-脑脊液屏障的发育。《神经科学前沿》9, 32 (2015) - PubMed
- Z. Redzic, 血-脑屏障与血-脑脊液屏障的分子生物学:相似性与差异性。《中枢神经系统液体与屏障》8, 3 (2011)
- M. K. Lehtinen, M. W. Zappaterra, X. Chen, Y. J. Yang, A. D. Hill, M. Lun, T. Maynard, D. Gonzalez, S. Kim, P. Ye, A. J. D’Ercole, E. T. Wong, A. S. La Mantia, C. A. Walsh, 脑脊液为神经前体细胞提供增殖微环境。《神经元》69, 893–905 (2011)
- S. A. Liddelow, K. M. Dziegielewska, K. Møllgård, T. N. Phoenix, S. Temple, J. L. VandeBerg, N. R. Saunders, SPARC/骨粘连蛋白:大脑发育过程中将白蛋白靶向输送至血脑脊液界面的内源性机制。《欧洲神经科学杂志》34, 1062–1073 (2011)
- K. Narita, S. Takeda, 脉络丛纤毛:其在脑积水及其他领域的作用。《细胞神经科学前沿》9, 39 (2015) - PubMed
- M. K. Lehtinen, C. S. Bjornsson, S. M. Dymecki, R. J. Gilbertson, D. M. Holtzman, E. S. Monuki, 脉络丛与脑脊液:在发育、疾病与治疗中新兴的作用。《神经科学杂志》33, 17553–17559 (2013)
- B. Banizs, M. M. Pike, C. L. Millican, W. B. Ferguson, P. Komlosi, J. Sheetz, P. D. Bell, E. M. Schwiebert, B. K. Yoder, 纤毛功能障碍导致室管膜与脉络丛功能改变并引发脑积水形成。《发育》132, 5329–5339 (2005)
- J. Mariani, V. Simonini Maria, D. Palejev, L. Tomasini, G. Coppola, M. Szekely Anna, L. Horvath Tamas, M. Vaccarino Flora, 利用诱导多能干细胞体外模拟人类皮质发育。《美国国家科学院院刊》109, 12770–12775 (2012)
- O. Marín, U. Müller, 新皮层中GABA能神经元与谷氨酸能神经元的谱系起源。《当前神经生物学观点》26, 132–141 (2014)
- M. Dierssen, 唐氏综合征:三体模式下的大脑。《自然综述·神经科学》13, 844–858 (2012)
- J. A. Briggs, J. Sun, J. Shepherd, D. A. Ovchinnikov, T.-L. Chung, S. P. Nayler, L.-P. Kao, C. A. Morrow, N. Y. Thakar, S.-Y. Soo, T. Peura, S. Grimmond, E. J. Wolvetang, 无整合诱导多能干细胞模拟唐氏综合征病因的遗传与神经发育特征。《干细胞》31, 467–478 (2013)
- K. Nagaoka, T. Udagawa, J. D. Richter, CPEB介导的ZO-1 mRNA定位是上皮紧密连接组装与细胞极性所必需的。《自然·通讯》3, 675 (2012)
- A. Parichha, V. Suresh, M. Chatterjee, A. Kshirsagar, L. Ben-Reuven, T. Olender, M. M. Taketo, V. Radosevic, M. Bobic-Rasonja, S. Trnski, M. J. Holtzman, N. Jovanov-Milosevic, O. Reiner, S. Tole, 经典Wnt信号通路的组成性激活破坏脉络丛上皮命运。《自然·通讯》13, 633 (2022)
- K. Ono, H. Takebayashi, K. Ikeda, M. Furusho, T. Nishizawa, K. Watanabe, K. Ikenaka, Olig2前体细胞在前脑分化的区域性与时间依赖性变化及其对背侧皮质星形胶质细胞发育的影响。《发育生物学》320, 456–468 (2008)
- M. Hoffmann, H. Kleine-Weber, S. Schroeder, N. Krüger, T. Herrler, S. Erichsen, T. S. Schiergens, G. Herrler, N.-H. Wu, A. Nitsche, M. A. Müller, C. Drosten, S. Pöhlmann, SARS-CoV-2细胞侵入依赖ACE2与TMPRSS2并可被临床验证的蛋白酶抑制剂阻断。《细胞》181, 271–280.e8 (2020)
- I. De Tomà, M. Dierssen, 唐氏综合征与SARS-CoV-2的网络分析识别COVID-19的风险与保护因素。《科学报告》11, 1930 (2021)
- I. Gomes, K. Karmirian, J. T. Oliveira, C. Da S. G. Pedrosa, M. A. Mendes, F. C. Rosman, L. Chimelli, S. Rehen, 一名14月龄儿童中枢神经系统的SARS-CoV-2感染:完整尸检病例报告。《柳叶刀·美洲区域健康》2, 100046 (2021)
- L. Zhang, L. Zhou, L. Bao, J. Liu, H. Zhu, Q. Lv, R. Liu, W. Chen, W. Tong, Q. Wei, Y. Xu, W. Deng, H. Gao, J. Xue, Z. Song, P. Yu, Y. Han, Y. Zhang, X. Sun, X. Yu, C. Qin, SARS-CoV-2突破血脑屏障伴随基底膜破坏而无紧密连接改变。《信号转导与靶向治疗》6, 337 (2021)
- Y. J. Sun, G. Velez, D. E. Parsons, K. Li, M. E. Ortiz, S. Sharma, P. B. McCray, A. G. Bassuk, V. B. Mahajan, 基于结构的系统发育识别阿伏司他为TMPRSS2抑制剂,可防止小鼠感染SARS-CoV-2。《临床研究杂志》131, e147973 (2021)
- X. Hu, J. H. Shrimp, H. Guo, M. Xu, C. Z. Chen, W. Zhu, A. Zakharov, S. Jain, P. Shinn, A. Simeonov, M. D. Hall, M. Shen, 通过虚拟筛选发现TMPRSS2抑制剂。bioRxiv 2020.12.28.424413 [预印本] (2021) https://doi.org/10.1101/2020.12.28.424413
- S. Xia, Q. Lan, S. Su, X. Wang, W. Xu, Z. Liu, Y. Zhu, Q. Wang, L. Lu, S. Jiang, 弗林蛋白酶切位点在SARS-CoV-2刺突蛋白介导的膜融合中的作用(存在或不存在胰蛋白酶条件下)。《信号转导与靶向治疗》5, 92 (2020)
- D. Yamasaki, I. Kimura, H. Nasser, Y. Morioka, N. Naoki, J. Ito, K. Uryu, M. Tsuda, J. Zachradnik, K. Shirakawa, R. Suzuki, M. Kishimoto, Y. Kosugi, K. Kohyama, T. Hara, M. Toyota, Y. L. Tanaka, E. P. Butler-Tanaka, R. Shimizu, H. Ito, L. Wang, Y. Oda, Y. Alba, M. Sasaki, K. Nagata, K. Yoshimatsu, H. Asakura, M. Nagashima, K. Sadaie, K. Yoshimura, J. Kuramochi, M. Seki, R. Fujiki, A. Kaneda, T. Shimada, T.-A. Nakata, S. Sakao, T. Suzuki, T. Ueno, A. Takahashi-Kondo, K. J. Ishii, G. Schreiber, H. Sawa, A. Saito, T. Irie, S. Tanaka, K. Matsuno, T. Fukuhara, T. Ikeda, K. Sato, SARS-CoV-2 Omicron BA.2刺突蛋白的病毒学特征。Cell 185, 2103–2115.e19 (2022)
- R. M. Naeini, J. H. Yoo, J. V. Hunter, 儿童脉络丛病变的频谱。《美国X线学杂志》192, 32–40 (2009)
- P. K. Eid, L. M. Volls, A. H. Prip, K.-A. Madsen, G. Lindstad, 《特发性正常压力脑积水中脉络丛脑脊液示踪剂清除延迟》。J. Cereb. Blood Flow Metab. 40, 1849–1858 (2020)
- K. Grenier, J. Kao, P. Diamandis, 人类神经退行性疾病的三维建模:脑类器官迈向成熟期。《分子精神病学》25, 254–274 (2020)
- Qian Xu, Song H, Ming G. I., 脑类器官:进展、应用与挑战。《发育》146, dev166074 (2019)
- A. Chandrasekaran, H. X. Avzajer, A. O’Halloran, L. N. Lessin, K. Molnár, L. Laszlo, T. Bélák, A. Tóglási, K. Peshti, A. Mike, 2D与3D神经诱导方法在从人类诱导多能干细胞生成神经祖细胞中的比较。《干细胞研究》25, 139–151 (2017)
- M. R. Shaker, G. Pietrogrande, S. Martin, J.-H. Lee, W. Sun, E. J. Wolvetang, 在类器官中快速高效地生成髓鞘化人少突胶质细胞。《细胞神经科学前沿》15, 631548 (2021)
- K. H. Ho, A. Candat, V. Scarpetta, M. Faucourt, S. Weill, C. Salio, E. D’Este, M. Meschkat, C. A. Wurm, M. Kneussel, C. Janke, M. M. Magiera, A. Genovesio, A. Meunier, M. Sassoè-Pognetto, M. S. Brill, N. Spassky, A. Patrizi, 脉络丛携带节点样纤毛,这些纤毛自成年早期阶段即发生轴丝退化。《发育细胞》58, 2641–2651.e6 (2023)
- J. A. Bagley, D. Reumann, S. Bian, J. Lévi-Strauss, J. A. Knoblich, 《融合脑类器官模拟脑区间相互作用》。Nat. Methods 14, 743–751 (2017)
- Xiang Yi, Tanaka Yū, Baris Çakır, Brent Patterson, Kim Ki-Yong, Sun Peng, Kang Young-Jun, Zhong Ming, Liu Xin, He Shan, 干细胞来源的丘脑类器官与皮层类器官融合时形成相互投射。《细胞·干细胞》24, 487–497.e4 (2019)
- J. R. Atack, S. I. Rapoport, M. B. Schapiro, 唐氏综合征患者脑脊液生成正常。Neurobiol. Aging 19, 307–309 (1998)
- R. J. Roper, R. H. Reeves, 理解唐氏综合征表型的基础。《公共科学图书馆·遗传学》2, e50 (2006)
- C. Chen, P. Jiang, H. Xue, S. E. Peterson, H. T. Chen, A. E. McCann, M. M. Palastro, S. Li, D. E. Plishker, L. C. Laurent, J. F. Loring, Y. Liu, W. Deng, 由患者来源的人诱导多能干细胞揭示星形胶质细胞在唐氏综合征中的作用。Nat. Commun. 5, 4430 (2014)
- B. Gámez, E. Rodriguez-Carballo, F. Ventura, BMP信号在端脑神经细胞特化和成熟中的作用。《细胞神经科学前沿》7, 87 (2013) - PubMed
- A. Conti, F. Fabbrini, P. D’Agostino, R. Negri, D. Greco, R. Genesio, M. D’Armiento, C. Olla, D. Paladini, M. Zannini, L. Nitsch, 《21号染色体三体人类胎儿心脏中线粒体与细胞外基质基因的表达改变》。BMC Genomics 8, 268 (2007)
- T. R. Grossman, A. Gamliel, R. J. Wessels, O. Tali-Lramalem, K. Jepsen, K. Okorodudu, J. R. Korenberg, K. L. Peterson, M. G. Rosenfeld, R. Bodmer, E. Bier, 《DSCAM与COL6A2的过表达协同导致先天性心脏缺陷》。PLOS Genetics 7, e1002344 (2011)
- E. Karousou, X. Stachtea, P. Moretto, M. Viola, D. Vigetti, M. L. D’Angelo, L. Raio, F. Ghezzi, F. Pallotti, G. De Luca, N. K. Karamanos, A. Passi, 关于唐氏综合症病理生物学的新见解——透明质酸合酶-2的过表达受胶原蛋白VI α2链调控。FEBS J. 280, 2418–2430 (2013)
- J. Bénard, N. Béron-Gaillard, D. Satgé, 唐氏综合征对乳腺癌具有保护作用:个体细胞微环境是关键吗?《国际癌症杂志》113, 168–170 (2005)
- B. Pomroy-Badell, W. T. Farmer, E. V. Jones, S. Jesa, J. B. Kacerovsky, A. Myhr, H. Peng, J. L. Lefebvre, J. Druin, A. Haier, C. Ernst, K. K. Murai, 人类iPSC衍生的唐氏综合征星形胶质细胞显示出全基因组范围的基因表达紊乱、黏附特性改变以及细胞动力学增强。《人类分子遗传学》29, 785–802 (2020)
- P. K. Gonzalez, C. M. Roberts, V. Font, C. Jacobson, G. H. Stein, C. D. Link, 《染色体21二体性或三体性的基因匹配人类诱导多能干细胞转录组分析》。PLOS ONE 13, e0194581 (2018)
- Huo Quan, Qu Yang, Yuan Fang, Ma Liang, Yao Liang, Xu Ming, Hu Yong, Ji Jia, A. Bhattacharyya, Zhang Shoucheng, Liu Yang, 利用患者iPS细胞模拟唐氏综合征揭示GABA能神经元的细胞与迁移缺陷。《干细胞报告》10, 1251–1266 (2018)
- J. Mlakar, M. Korva, N. Tul, M. Popović, M. Poljsak-Prijatelj, J. Mraz, M. Koren, K. Rešman Rus, T. Vesnaver Vipotnik, V. Fabjan Vodušek, A. Vizjak, J. Pižem, M. Petrović, T. Avšič-Županc, 寨卡病毒与微头畸形相关。《新英格兰医学杂志》374, 951–958 (2016)
- M. Ayed, A. Embaireeg, M. Kartam, K. More, M. Alqallaf, A. Alnafisi, Z. Alsaffar, Z. Bahzad, Y. Buhamad, H. Alsayegh, W. Al-Fouzan, H. Alkandari, 宫内暴露于母体SARS-CoV-2感染导致的婴儿神经发育结局:科威特的一项全国性前瞻性研究。medRxiv 2021.11.12.21266291 [预印本] (2021) https://doi.org/10.1101/2021.11.12.21266291
- A. G. Edlow, V. M. Castro, L. L. Shook, A. J. Kaimal, R. H. Perlis, 孕期SARS-CoV-2检测阳性母亲的子代在一岁时的神经发育结局。medRxiv 2021.12.15.21267849 [预印本] (2021) https://doi.org/10.1101/2021.12.15.21267849
- A. G. Edlow, V. M. Castro, L. L. Shook, A. J. Kaimal, R. H. Perlis, 孕期SARS-CoV-2检测阳性母亲的婴儿在1岁时的神经发育结局。JAMA Netw. Open 5, e2215787 (2022)
- A. Ramani, L. Müller, P. N. Ostermann, E. Gabriel, P. Abida-Islam, A. Müller-Schiffmann, A. Mariappan, O. Goureau, H. Gruell, A. Walker, M. Andrée, S. Hauka, T. Houwaart, A. Dilthey, K. Wohlgemuth, H. Omran, F. Klein, D. Wieczorek, O. Adams, J. Timm, C. Korth, H. Schaal, J. Gopalakrishnan, SARS-CoV-2靶向三维人脑类器官的神经元。EMBO J. 39, e106230 (2020)
- L. Wang, D. Sievert, A. E. Clark, S. Lee, H. Federman, B. D. Gastfriend, E. V. Shusta, S. P. Palecek, A. F. Carlin, J. G. Gleeson, 一种人三维神经-血管周围"组装体"促进星形胶质细胞发育并能够模拟SARS-CoV-2神经病理学。Nat. Med. 27, 1600–1606 (2021)
- A. C. Yang, F. Kern, P. M. Losada, M. R. Agam, C. A. Maat, G. P. Schmartz, T. Fehlmann, J. A. Stein, N. Schaum, D. P. Lee, K. Calcuttawala, R. T. Vest, D. Berdnik, N. Lu, O. Hahn, D. Gate, M. W. McNerney, D. Channappa, I. Cobos, N. Ludwig, W. J. Schulz-Schaeffer, A. Keller, T. Wyss-Coray, 重症COVID-19患者大脑和脉络丛细胞类型的失调。Nature 595, 565–571 (2021)
- A. Letourneau, F. A. Santoni, X. Bonilla, M. R. Sailani, D. Gonzalez, J. Kind, C. Chevalier, R. Thurman, R. S. Sandstrom, Y. Hibaoui, M. Garieri, K. Popadin, E. Falconnet, M. Gagnebin, C. Gehrig, A. Vannier, M. Guipponi, L. Farinelli, D. Robyr, E. Migliavacca, C. Borel, S. Deutsch, A. Feki, J. A. Stamatoyannopoulos, Y. Herault, B. Van Steensel, R. Guigo, S. E. Antonarakis, 唐氏综合征全基因组基因表达失调的域。Nature 508, 345–350 (2014)
- K. Baruch, A. Deczkowska, E. David, J. M. Castellano, O. Miller, A. Kertser, T. Berkutzki, Z. Barnett-Itzhaki, D. Bezalel, T. Wyss-Coray, I. Amit, M. Schwartz, 脉络丛的衰老诱导型I干扰素反应对大脑功能产生负面影响。Science 346, 89–93 (2014)
- K. D. Sullivan, H. C. Lewis, A. A. Hill, A. Pandey, L. P. Jackson, J. M. Cabral, K. P. Smith, L. A. Liggett, E. B. Gomez, M. D. Galbraith, J. DeGregori, J. M. Espinosa, 21三体持续激活干扰素反应。eLife 5, e16220 (2016)
- S. Cetiner, O. Demirhan, T. C. Inal, D. Taste mir, Y. Sertdemir, 唐氏综合征儿童外周血T细胞亚群、自然杀伤细胞及血清细胞因子水平分析。Int. J. Immunogenet. 37, 233–237 (2010)
- T. Hempel, L. Raich, S. Olsson, N. P. Azouz, A. M. Klingler, M. Hoffmann, S. Pöhlmann, M. E. Rothenberg, F. Noé, 卡莫司他和萘莫司他抑制SARS-CoV-2细胞进入辅助因子TMPRSS2的分子机制。Chem. Sci. 12, 983–992 (2021)
- J. W. Park, X. Wang, R.-H. Xu, 揭示长新冠患者持续性嗅觉丧失的奥秘。Int. J. Biol. Sci. 18, 4795–4808 (2022)
- J. H. Beigel, K. M. Tomashek, L. E. Dodd, A. K. Mehta, B. S. Zingman, A. C. Kalil, E. Hohmann, H. Y. Chu, A. Luetkemeyer, S. Kline, D. Lopez de Castilla, R. W. Finberg, K. Dierberg, V. Tapson, L. Hsieh, T. F. Patterson, R. Paredes, D. A. Sweeney, W. R. Short, G. Touloumi, D. C. Lye, N. Ohmagari, M.-D. Oh, G. M. Ruiz-Palacios, T. Benfield, G. Fätkenheuer, M. G. Kortepeter, R. L. Atmar, C. B. Creech, J. Lundgren, A. G. Babiker, S. Pett, J. D. Neaton, T. H. Burgess, T. Bonnett, M. Green, M. Makowski, A. Osinusi, S. Nayak, H. C. Lane, 瑞德西韦治疗COVID-19——最终报告。N. Engl. J. Med. 383, 1813–1826 (2020)
- J. M. Espinosa, 唐氏综合征与COVID-19:一场完美风暴?Cell Rep. Med. 1, 100019 (2020)
- M. R. Shaker, A. Kahtan, R. Prasad, J.-H. Lee, G. Pietrogrande, H. C. Leeson, W. Sun, E. J. Wolvetang, A. Slonchak, 神经表皮生长因子样蛋白2在人类少突胶质细胞类型中表达。《细胞发育生物学前沿》10, 803061 (2022)
- B. Al-Mhanawi, M. B. Marti, S. D. Morrison, P. Gupta, M. Alani, P. G. Noakes, E. J. Wolvetang, M. R. Shaker, 生成富集少突胶质细胞的无包埋脑类器官的方案。STAR Protoc. 4, 102725 (2023)
- J.-H. Lee, M. R. Shaker, E. Lee, B. Lee, W. Sun, 小鼠胚胎神经干细胞神经球分化过程中的神经核心形成。Stem Cell Res. 43, 101691 (2020)
- M. R. Shaker, J. Y. Kim, H. Kim, W. Sun, 体外二次神经管来源胚胎神经干细胞的鉴定和表征。Stem Cells Dev. 24, 1171–1181 (2015)
- M. R. Shaker, J.-H. Lee, S.-H. Park, J. Y. Kim, G. H. Son, J. W. Son, B. H. Park, I. J. Rhyu, H. Kim, W. Sun, 前后轴Wnt-RA梯度决定发育中脊髓神经祖细胞的粘附和迁移特性。Stem Cell Rep. 15, 898–911 (2020)
- J.-H. Lee, H. Shin, M. R. Shaker, H. J. Kim, S.-H. Park, J. H. Kim, N. Lee, M. Kang, S. Cho, T. H. Koo, J. W. Kim, M.-R. Song, S.-H. Kwon, D. W. Han, S. Lee, S.-Y. Choi, I. J. Ryu, H. Kim, D. Kim, I.-J. Cho, W. Sun, 生产重现神经管形态发生的人类脊髓类器官。《生物医学工程》6, 435–448 (2022)
- A. Slonchak, X. Wang, J. Aguado, J. D. J. Shen, H. Chaggar, M. E. Franey, K. Yan, F. J. Torres, A. A. Amaria, R. Ballea, Y. X. Seto, N. Peng, D. Watson, E. Wolvetang, A. Sulbati, A. A. Kromhout, 寨卡病毒非编码RNA与病毒蛋白NS5协同抑制STAT1磷酸化并促进病毒发病机制。《科学进展》8, eadd8095 (2022)
- A. Slonchak, L. E. Hugo, M. E. Franey, S. Hall-Mendelson, A. A. Amaria, F. J. Torres, Y. X. Seto, N. Y. G. Peng, J. D. J. Shen, R. A. Hall, A. F. Van Den Hoek, G. J. Devine, A. A. Kromhout, 寨卡病毒非编码RNA抑制细胞凋亡并为蚊子传播病毒所需。《自然通讯》11, 2205 (2020)
- Y. Hua, P. Laserstrom, M. Helmstaedter, 基于电子显微镜连接组学的大体积整体染色。《自然通讯》6, 7923 (2015)
- S. Rodríguez-Lorenzo, D. M. Ferreira Francisco, R. Vos, B. Van Houtte, M. Lainsberger, H. Schroten, H. Ishikawa, W. Beyano, R. Brugman, G. Coijg, H. E. De Vries, 进行性多发性硬化中脉络丛分泌和神经保护功能的改变。《神经病理学通讯学报》8, 35 (2020)
¶ 致谢
经费支持:M.R.S. 获得儿童医院基金会资助(项目编号Pcc0252021);e.J.W. 获得MRFF脑白质营养不良旗舰项目——马西莫使命计划资助(项目编号ePcd000034);A.S. 获澳大利亚国家健康与医学研究委员会创意基金支持(项目编号2021272);A.A.K. 获澳大利亚国家健康与医学研究委员会创意基金(项目编号2012883)及澳大利亚传染病研究中心种子基金资助。本研究由昆士兰大学干细胞工程与再生工程中心(UQ StemcARe)资助。B.康克林(格莱斯顿心血管研究所医学部)
作者诚挚感谢惠赐Wtc iPsc细胞系。感谢昆士兰大学显微与显微分析中心(cMM)澳大利亚显微设施提供的平台以及科学技术支持。感谢Z. l. hunter完成MeA实验记录并提供示意图。感谢昆士兰卫生法医与科学服务部、昆士兰卫生部门提供SARS-CoV-2分离株。新一代测序由Ace测序公司(ScMB, UQ)完成。nGS试剂的采购得到illumina COVID匹配资助计划支持。感谢A. R. Fernandez(智利南方大学)和A. Amarilla(ScMB, UQ)提供针对SARS-CoV-2刺突蛋白的W25纳米抗体。作者贡献:M.R.S.构思、执行、分析并设计实验,解读结果并撰写论文;A.S.执行、分析并设计SARS实验,解读结果并撰写论文;B.A.、S.d.M.、J.d.J.S.执行补充实验;J.c.-W.参与研究构思;A.A.K.参与设计、解读结果并撰写论文;E.J.W.构思并指导研究,解读结果并撰写论文。所有作者审阅并最终认可论文版本。利益冲突:作者声明无利益冲突。数据与材料可用性:验证论文结论所需的所有数据均存在于论文及补充材料中。支持本研究发现的cOs与chPcOs批量RnA-seq数据已分别存入GEO-NcBi数据库,主要登录代码为GSe208575和GSe208440。