¶ 《自然》研究
¶ 爬行动物的屏状核及其在慢波睡眠中的作用
Hiroaki Norimoto1†, Lorenz A. Fenk1†, Hsing-Hsi Li1♢, Maria Antonietta Tosches1,2♢, Tatiana Gallego Flores1, David Hain1,3, Sam Reiter1,4, Riho Kobayashi1,5, Angeles Macias1, Anja Arends1, Michaela Klinkmann1 and Gilles Laurent1*
† 并列第一作者
♢ 同等贡献的共同作者
1 马克斯·普朗克脑研究所,德国美因河畔法兰克福
2 现任地址:哥伦比亚大学生物科学系,美国纽约州纽约市
3 德国法兰克福歌德大学生命科学系
4 现任地址:日本冲绳科学技术大学院大学
5 永久地址:日本名古屋市立大学药学研究科神经药理学系
* 通讯作者(GL):gilles.laurent@brain.mpg.de
https://www.nature.com/articles/s41586-020-1993-6
哺乳动物的屏状核因其与其他前脑结构的广泛连接,被假设介导从决策到意识等多种功能¹。在此我们报告,通过单细胞转录组学和病毒示踪连接技术,在一种爬行动物——澳大利亚鬃狮蜥(Pogona vitticeps)中也发现了屏状核的同源结构。在鬃狮蜥中,屏状核是慢波睡眠期间锐波产生的基础。这些锐波连同叠加其上的高频涟漪²,会传播到整个邻近的大脑皮层背侧室嵴(DVR)。单侧或双侧屏状核损伤会分别单侧或双侧抑制慢波睡眠期间的锐波-涟漪产生,但不会影响鬃狮蜥睡眠所特有的规律且快速交替的睡眠节律³。因此,屏状核本身并不参与睡眠节律的生成。神经束追踪显示,屏状核广泛投射到包括大脑皮层在内的多个前脑区域,并且它接收来自中脑和后脑等区域的汇聚输入,而这些区域在哺乳动物中已知参与觉醒/睡眠控制⁴⁻⁶。例如,对屏状核中血清素浓度进行人为的周期性调节,会导致该区域及邻近DVR中锐波产生出现相应的调节。通过转录组学方法,在龟类(蜥蜴的远亲爬行动物)中也识别出了屏状核。因此,屏状核是一种古老的结构,可能在爬行动物和哺乳动物的共同脊椎动物祖先的大脑中就已存在。由于从中脑和后脑接收上行输入、向 Forebrain 广泛投射以及在慢波睡眠期间产生锐波的作用,它可能在脑状态控制中发挥重要作用。
慢波睡眠(SWS)和快速眼动睡眠(REMS)是哺乳动物和鸟类电生理睡眠的两个主要宏观组成部分4-6,不过有些哺乳动物可能没有快速眼动睡眠7。最近在一种爬行动物——澳大利亚鬃狮蜥(Pogona vitticeps)身上发现了慢波睡眠和快速眼动睡眠的交替现象3,这表明这两种睡眠模式可能早于3.2亿年前羊膜动物的分化。鬃狮蜥的睡眠特别有趣,因为其周期非常短(在室温下≤3分钟),并且慢波睡眠和快速眼动睡眠的时间各占一半3。
鬃狮蜥慢波睡眠(SWS)的主要电生理特征是δ波段(约0-4Hz)的能量,这是由尖波的稳定出现引起的。尖波通常包含高频涟漪,形成尖波-涟漪复合体(SWR)。研究人员从背侧脑室嵴(DVR)记录到了SWR,背侧脑室嵴是蜥形纲动物大脑中主要的非皮质脑 pallial 区域。相比之下,快速眼动睡眠(REMS)的特征是宽带能量,在皮质和DVR的β波段(10-40Hz)可检测到。
¶ 慢波睡眠期间锐波的起源
正如已有报道所述,在慢波睡眠(SWS)期间,背侧脑室嵴(DVR)中会稳定出现尖波涟漪复合体(SWRs),且慢波睡眠与快速眼动睡眠(REMS)有规律地交替出现(图1ac;补充数据图1)。高频涟漪(约70-150赫兹)伴随每个尖波产生,并包含动作电位。背侧脑室嵴各记录位点的局部场电位(LFPs)高度相关(在18小时的慢波睡眠期间,峰值相关系数为0.74,2只动物的平均值),但背侧脑室嵴前内侧极(amDVR)记录到的尖波,会比更靠后或更靠外侧区域记录到的同类尖波提前至多200毫秒,具体取决于记录位点的间距(图1d-e及补充数据图1g-h),这表明存在尖波涟漪复合体的传播。
接下来,我们在ACSF中记录了背侧脑室嵴(DVR)的厚前横切片、水平切片和旁矢状切片(方法,扩展数据图2a-f)。所有配置都产生了自发性尖波涟漪复合波(SWRs),与睡眠中产生的一致:双相波形(119±40毫秒),波谷处有涟漪(约70-150赫兹)。切片中的SWRs频率低于慢波睡眠(SWS)期间(12.4±1.8次/分钟,12个切片,10只动物;而慢波睡眠期间为16.45±0.98次/分钟;来自2只睡眠动物的5个慢波睡眠时期),不过差异不显著(p=0.18,Student t检验)。与睡眠期间不同,切片中的SWR产生不会被类似快速眼动睡眠(REMS)的活动节律性地中断。我们对12个DVR神经元进行了膜片钳记录(扩展数据图2g-j);与睡眠数据一致,它们在SWRs期间通常发放0-3个动作电位,而在SWRs之间则保持沉默。在电压钳模式下(n=2),神经元在尖波期间表现出同时出现的兴奋性和抑制性输入(在电流钳模式下兴奋性占主导)。
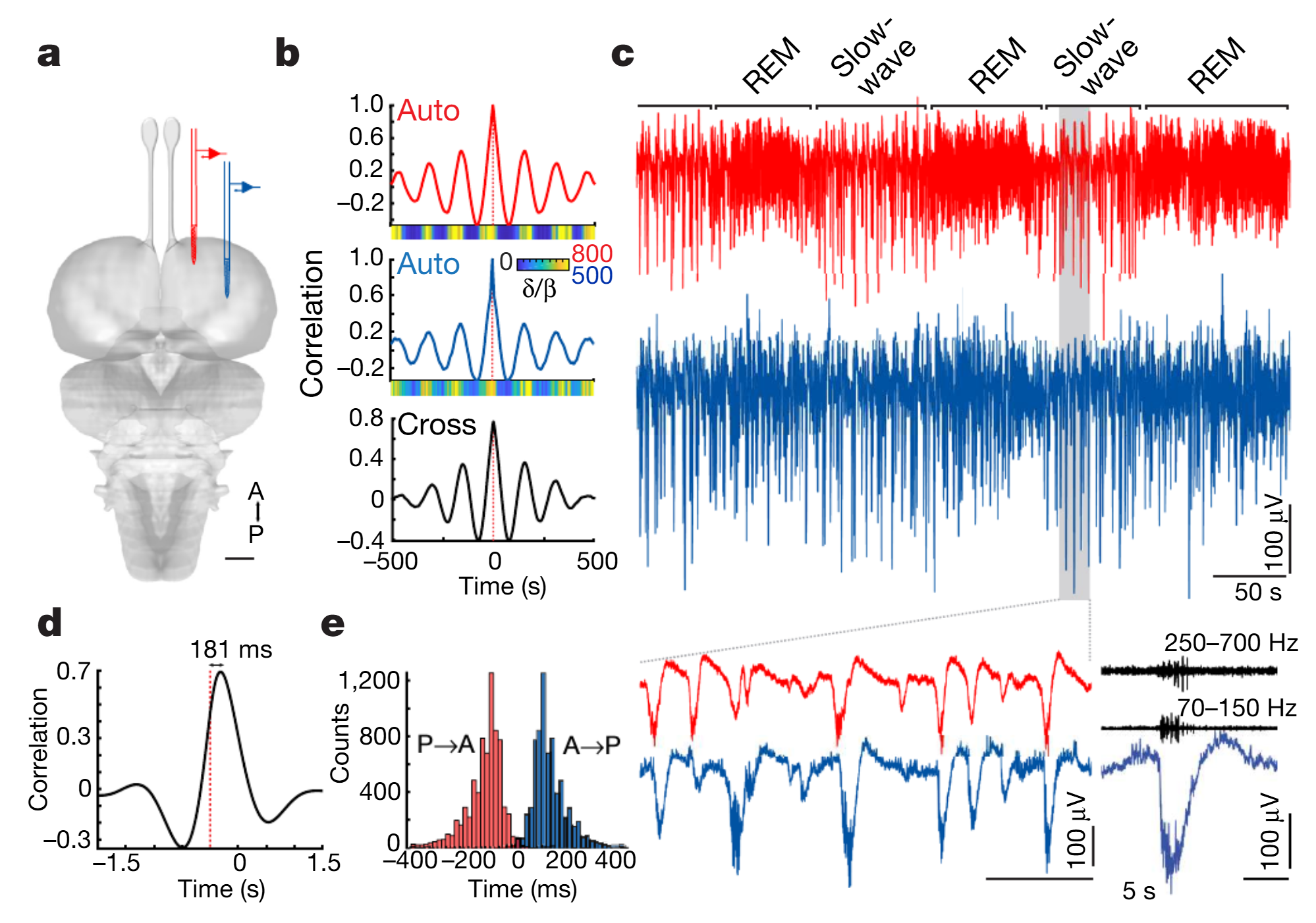
图1 | 睡眠中的鬃狮蜥的amDVR中会产生锐波涟漪(SWRs)。a,从背侧脑室嵴(DVR,皮层下)的两个位点同时记录。A,前部;P,后部。比例尺,1毫米。b,δ/β功率比的自相关和互相关,作为a中位点的时间函数,基于8小时的睡眠计算得出。彩色条带显示了单个1000秒睡眠片段中的δ/β比值。c,b中分析数据的短片段(轨迹颜色相同)。左下,慢波睡眠短片段的放大图,展示了SWR的协调性以及前后部延迟。右下,一个SWR和高通成分的细节(中、上图,黑色)。d,3.42小时慢波睡眠(SWS)期间宽带局部场电位(LFP)波形之间的互相关。参考轨迹为前部记录位点:前部位点领先。e,以前部(或后部)背侧脑室嵴中锐波为触发点,同时记录的后部(或前部)背侧脑室嵴中锐波的延迟分布。详见方法和扩展数据图1。
我们还在DVR切片上使用了多电极阵列(n=3个大脑;方法部分)。与在体观察结果一致,SWRs从前内侧极向后外侧极传播(图2a-c)。尽管传播过程包含局部角度成分,但切片平面内波的表观线性速度为39毫米/秒。我们进一步将DVR切片分为“迷你切片”(n=13,图2d)。只有来自前内侧极的迷你切片会产生SWRs,频率为11.9±1.7次/分钟(图2e-f),与对照组无差异。
¶ 单细胞RNA测序显示存在屏状核同源物
我们最近采用单细胞转录组策略,绘制了爬行动物大脑皮层的主要神经元类型图谱,并描述了鬃狮蜥背侧室嵴(DVR)内谷氨酸能细胞类型的异质性。为了表征前背侧室嵴(amDVR),我们对鬃狮蜥的单细胞进行了更深层次、更广泛的采样(方法部分)。通过对20257个细胞的转录本进行基于无监督图的Louvain聚类,我们识别出4054个皮层谷氨酸能神经元,这些神经元形成了29个谷氨酸能细胞簇(图3a和扩展数据图3)。
我们利用原位杂交(ISH)和/或免疫组织化学(IHC)检测到的集群特异性标志物的表达,在鬃狮蜥的端脑中定位了这些集群11。两个集群(19和20,图3a)映射到了amDVR,这一点从钙结合蛋白 hippocalcin(HPCA)和RNA编辑酶ADARB2等的表达中可以看出(图3b-d)。集群19和20分别对应amDVR的外侧和内侧亚区,分别通过copine 4(CPNE4)和核激素受体RORB基因的表达来标记(图3e-f)。我们重复进行了小切片SWR记录,并在事后用hippocalcin抗体标记这些切片:只有来自amDVR极部的hippocalcin阳性小切片产生了SWR(扩展数据图4)。
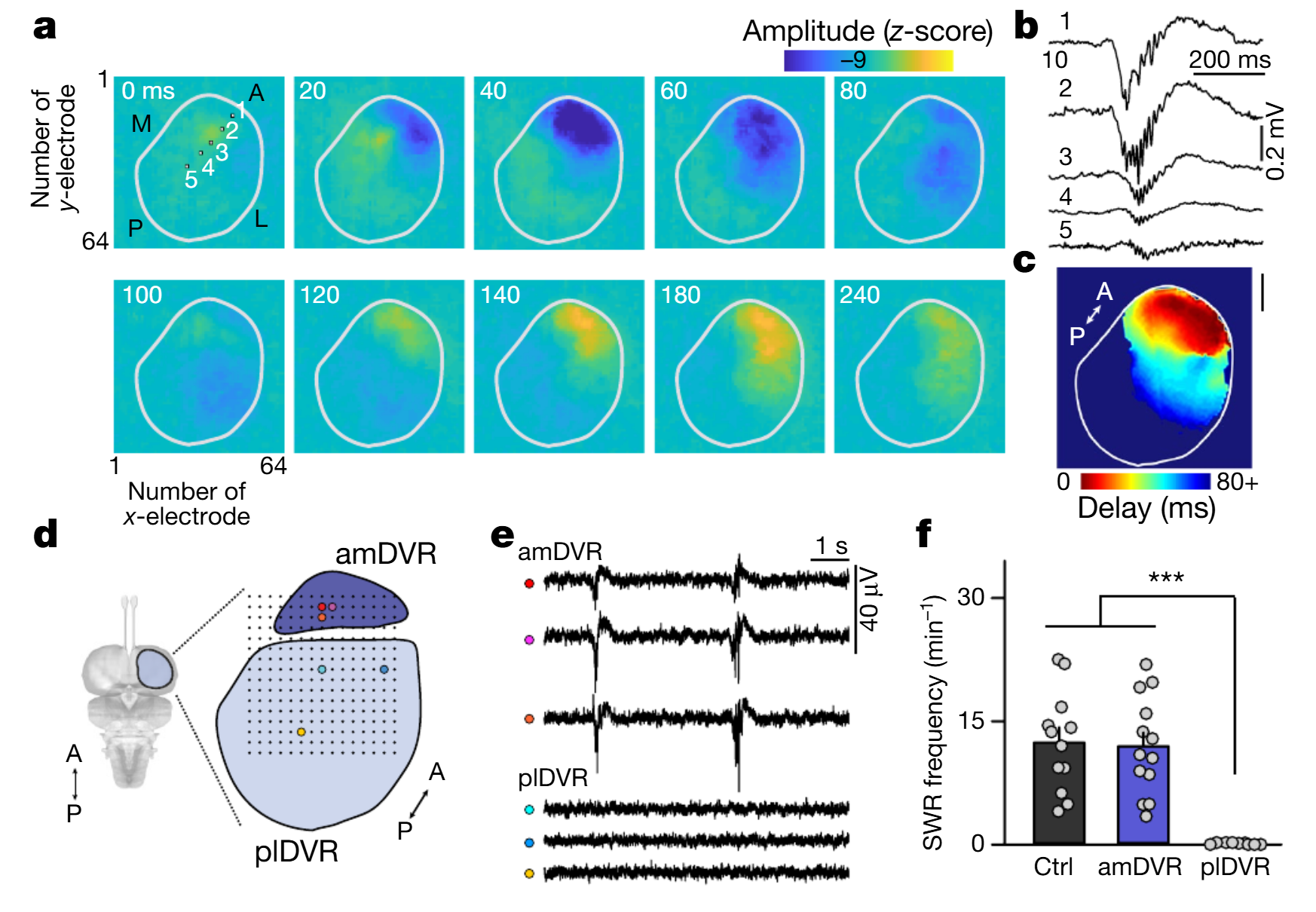
图2 | SWR在背侧脑室嵴切片中自发产生并起源于前内侧极。a-c,互补金属氧化物半导体微电极阵列(CMOS-MEA)记录的SWR在背侧脑室嵴(DVR)水平切片上的传播(另见扩展数据图2)(已勾勒轮廓)。a,20-60毫秒间隔的瞬时电压样本。方框1-5表示b中所示的记录位点。注意在前极的起始。L,外侧;M,内侧。b,a中位点1-5的SWR。注意各位点之间在振幅和起始时间上的差异。c,切片平面上的信号潜伏期(相对于最早通道;12个SWR的平均值;与a为同一切片)。比例尺,1毫米。d-f,微型切片中的SWR。252位点微电极阵列,间距200微米。d,DVR的厚水平切片被细分。e,从d中彩色位点记录的同步局部场电位(LFP)。plDVR,后外侧DVR。f,完整切片(对照组(ctrl);n=12个切片)、前内侧DVR(amDVR;n=13个微型切片)和后外侧DVR(plDVR;n=9个微型切片)中SWR的平均频率。***P<0.001。P值:对照组与amDVR组,P=1,t23=0.04;对照组与plDVR组,P=7.2×10−6;t19=6.3;amDVR组与plDVR组,P=4.6×10−6,t19=6.3(双侧邦费罗尼检验)。数据为平均值±标准误。
一些amDVR标记物(例如GNG2、SYNPR和RGS12,图3b)是已知的哺乳动物屏状核标记物12。为了进一步探究这些分子层面的相似性,我们基于联合降维分析,使用Seurat v3将鬃狮蜥的单细胞转录组映射到小鼠的细胞类型转录组上(14,方法部分)。约63%和75%的amDVR细胞(分别来自集群19和20)映射到了小鼠屏状核转录组集群(图3g),这表明鬃狮蜥的amDVR与哺乳动物的屏状核是同源的,这也与发育学观察结果一致10,15。
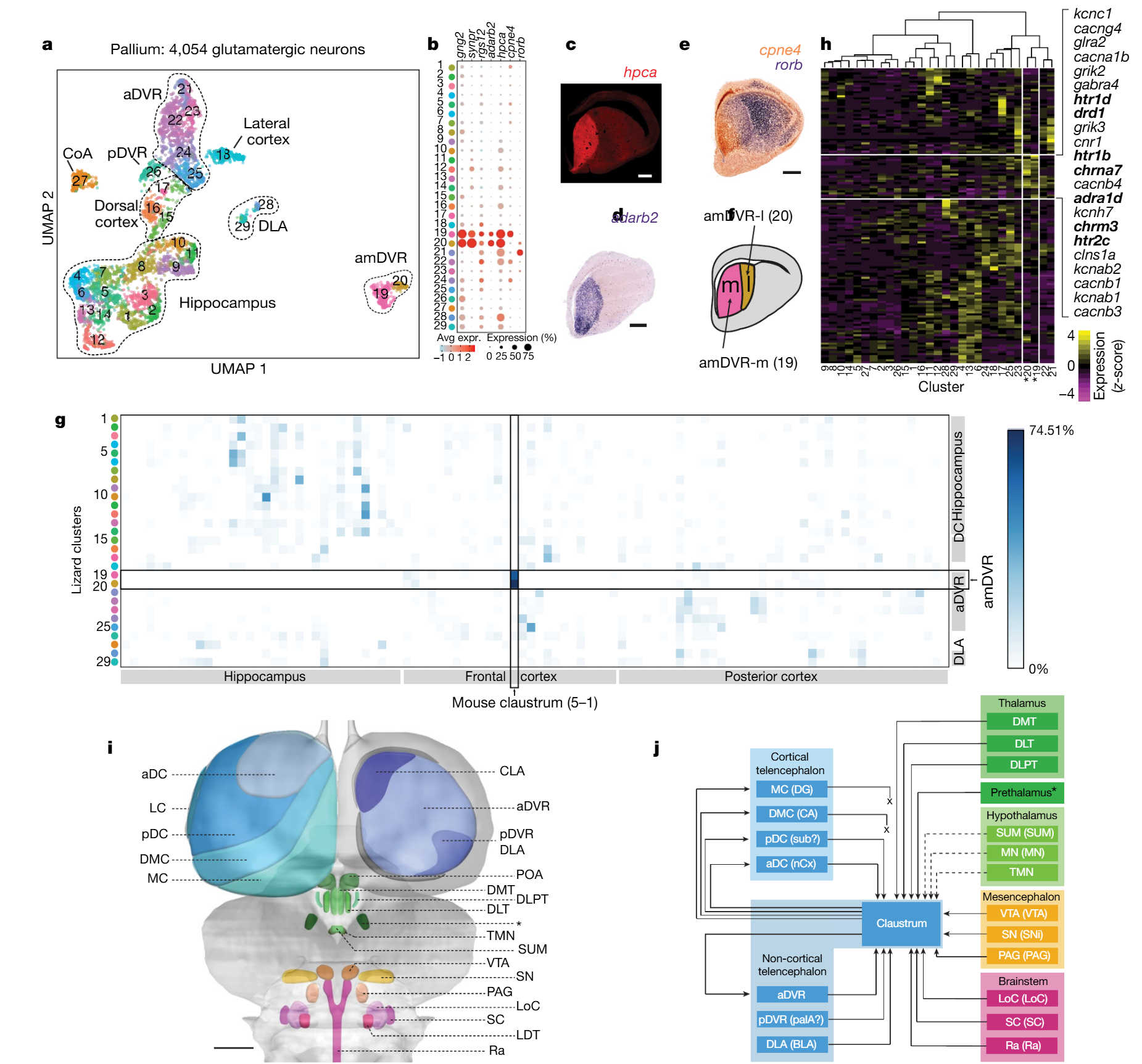
图3 | 单细胞RNA测序和病毒示踪显示,amDVR是爬行类的屏状核。a,4054个鬃狮蜥谷氨酸能大脑皮层神经元单细胞转录组的统一流形逼近与投影(UMAP)42表示。细胞按簇(1-29)进行颜色编码。CoA,皮质杏仁核;DLA,背外侧杏仁核。见扩展数据图3、5。b,在amDVR(簇19、20)中高特异性表达的标记基因在各簇中的表达情况。其中包括哺乳动物屏状核的标记物。点的大小对应检测到该基因的细胞比例,颜色代表表达水平。c-e,鬃狮蜥端脑的前部横切片,分别进行了 hippocalcin(hpca)的免疫染色(c)、adarb2的原位杂交(d)以及cpne4和rorb探针的双重原位杂交(e)。比例尺,500μm。f,显示amDVR内侧(m)和外侧(l)亚区的示意图。g,蜥蜴和小鼠簇之间的转录组相似性,以从鬃狮蜥映射到小鼠簇的单细胞转录组比例来衡量(方法;小鼠数据来自先前的研究13)。h,143个离子通道和神经递质受体基因在鬃狮蜥各簇中的平均表达(扩展数据图5)。簇19和20(标有星号)分别对应f中所示amDVR的内侧和外侧亚区。右侧列出了在amDVR中表达富集的基因,其中相关的神经递质受体基因以粗体显示。i,鬃狮蜥大脑的示意图。前脑区域(蓝色)通过单细胞RNA测序和原位杂交11确定。间脑(绿色)、中脑(橙色)和菱脑(粉红色)区域通过免疫组织化学和荧光原位杂交确定(见扩展数据图6)。aDC,前背皮质;CLA,屏状核;DLT,背外侧丘脑;DLPT,背外侧后丘脑;DMC,背内侧皮质;DMT,背内侧丘脑;LC,外侧皮质;LDT,外侧背盖核;LoC,蓝斑核;MC,内侧皮质;PAG,中脑导水管周围灰质;pDC,后背皮质;POA,视前区;Ra,中缝核;SC,蓝斑下核;SN,黑质(哺乳动物为SNi);SUM,乳头体上核;TMN,结节乳头核;VTA,腹侧被盖区。丘脑前核标有星号。比例尺,1mm。j,通过病毒示踪确定的屏状核(amDVR)与i中各区域的连接汇总。实线箭头表示存在连接;“x”表示不存在连接(无顺行和逆行标记);虚线箭头表示暂定连接(由于标记不一致)。由于无法将rAAV2-retro特异性注射到这些小区域,因此未对屏状核向pDVR或DLA的投射进行确凿测试。括号中显示了哺乳动物同源物的缩写:BLA,基底外侧杏仁核;CA,海马 ammonis区;DG,齿状回;nCx,新皮质;palA,皮质杏仁核;sub,下托。与i中一样,丘脑前核标有星号。
为了将我们的转录组学观察结果与生理学观察结果联系起来,我们分析了大脑皮层谷氨酸能集群中离子通道和神经递质受体基因的表达(在至少一个集群的≥20%细胞中检测到143个基因,详见方法部分)。这些基因足以将amDVR与其他谷氨酸能集群区分开来(扩展数据图3、5),并且包含相互关联的基因集群(模块)。其中一个在amDVR中表达富集的模块(图3h)包含去甲肾上腺素(NA)、乙酰胆碱(ACh)、多巴胺(DA)和血清素(5HT)的受体。在哺乳动物中,这些神经调节剂会影响睡眠节律,并由从下丘脑到延髓的脑核释放4、5、16-18。amDVR中的谷氨酸能神经元是少数共表达这四种调节剂受体的神经元之一(扩展数据图5)。因此,amDVR表达的受体类型与其对控制大脑状态的回路输入的敏感性相符。
¶ amDVR具有广泛的连接性
接下来,我们绘制了amDVR与推测的觉醒/睡眠控制区域的连接图(如上述数据所示),并探究amDVR是否像哺乳动物的屏状核那样1,12,19-21,与大脑皮层的其他部分广泛连接。我们尽可能识别出与哺乳动物睡眠相关核团4-6同源的鬃狮蜥核团。基于相关物种的解剖学研究(方法部分),我们利用免疫组织化学(IHC)和荧光原位杂交(FISH)技术,在鬃狮蜥的间脑、中脑和脑干中识别并绘制了这些核团(图3i,扩展数据图6),同时还包含了通过单细胞RNA测序(scRNA-seq)绘制的端脑区域(蓝色)11。
我们通过局部示踪剂注射来绘制amDVR的连接图,使用携带荧光蛋白(在CAG或hSyn启动子调控下)的rAAV2-retro进行(主要是)逆行标记(方法部分)。rAAV2-retro有时会与(主要是)顺行的AAV2/9-CB7-mcherry-WPRE共同注射,以用于注射位点的识别。由于这些示踪剂不会穿过突触,因此它们能够显示注射位点的直接靶标(AAV2/9-CB7)和来源(rAAV2-retro)。结果总结于图3j中。左侧是所有端脑结构,其与amDVR(“屏状核”)的输入和输出连接均能被检测。右侧是由于解剖学原因无法进行局部注射的较深结构。对于这些结构,仅通过来自amDVR的逆行标记来确定其与屏状核的连接。屏状核是否投射到这些区域仍有待直接验证。
内侧背侧室旁核(amDVR)的皮质输入来源为前部和后部背侧皮质(图3j,补充数据图6c)。逆行和顺行示踪剂显示,海马体(x,图3j;DMC=CA区;MC=齿状回)没有直接投射到内侧背侧室旁核,尽管内侧背侧室旁核会投射到这两个区域。在皮质下大脑皮层中,前背侧室旁核(aDVR)和后背侧室旁核(pDVR)显示出对内侧背侧室旁核的强烈投射。内侧背侧室旁核还接收来自背侧丘脑核(DMT、DLT、DLPT)、丘脑前区、下丘脑、腹侧被盖区(VTA)、黑质和中脑导水管周围灰质的输入,以及来自脑干的蓝斑核、蓝斑下核和中缝核的输入(补充数据图6)。
内侧背侧室嵴(amDVR)投射至海马(内侧皮质和背内侧皮质)、后背皮质(潜在的下托同源结构)以及前背皮质(新皮质同源结构)11。在皮质下大脑皮层中,向内背侧室嵴(aDVR)的投射密集且广泛,这与尖波传播一致(图1、2)。内侧背侧室嵴与其部分靶区之间的投射呈现出有序性:更外侧的内侧背侧室嵴投射至嘴侧内背侧室嵴;中央的内侧背侧室嵴投射至尾侧内背侧室嵴。相反,来自皮质(前背皮质和后背皮质)到内侧背侧室嵴的输入在外侧最强,在内侧最弱(在内侧皮质和背内侧皮质——海马中不存在)。
因此,amDVR与大脑皮层前脑相连,并接收来自与觉醒/睡眠控制相关区域的输入,这与许多特定于这些区域的受体基因的广泛表达相一致。基于这些转录组学和解剖学数据,我们得出结论:amDVR是哺乳动物屏状核的爬行类同源结构。
¶ 龟类的屏状核同源物
我们在鬃狮蜥和乌龟(红耳滑龟)这两种位于爬行纲进化树不同分支的物种中应用了类似的转录组学方法,以寻找红耳滑龟体内的屏状核。通过对比转录组数据(方法部分),我们发现了四个潜在的乌龟细胞集群(扩展数据图7)。这些集群中的细胞位于一个被称为皮质增厚区(PT)的区域。乌龟的皮质增厚区和蜥蜴的背侧室嵴前部(amDVR)都位于端脑前区,这与它们在端脑前外侧区具有相似的发育起源是一致的;但乌龟的皮质增厚区位于背侧室嵴前部的外侧,靠近嗅皮质,而不像鬃狮蜥的屏状核那样与背侧室嵴的其余部分融合在一起。两者的结构也有所不同:鬃狮蜥的屏状核是核状结构,由各向同性分布的多极神经元组成;乌龟的皮质增厚区则形成一个弯曲的薄片,向前背侧皮质延伸,外侧膝状体核的轴突在前往视觉皮质的途中从下方穿过该区域。事实上,乌龟皮质增厚区的主神经元(通过在背内侧皮质注射rAAV2-retro标记)呈锥形,具有顶树突和基树突(扩展数据图7d)。尽管存在这些差异,乌龟皮质增厚区的切片会产生尖波涟漪,引发背侧室嵴中的尖波涟漪,这一点与鬃狮蜥类似。因此,皮质增厚区似乎就是乌龟的屏状核,并且羊膜动物的共同祖先可能就已经存在屏状核的同源结构。
¶ 调控屏状核活动
我们开发了一种简化的体外鬃狮蜥前脑制备方法,能够在移除皮质后直接接触非皮质的大脑皮层(方法部分)。这种制备方法在屏状核和背侧室嵴(DVR)中产生了自发性的锐波涟漪(SWRs),与在体睡眠期间以及DVR/屏状核切片中记录到的情况相似(扩展数据图8)。锐波涟漪持续发生,且频率(4个大脑,21.6±5.4次/分钟)高于切片中的频率(n=13,12.4±1.8次/分钟)。屏状核活动先于DVR(扩展数据图8f),其延迟时间与睡眠期间或屏状核+DVR切片中观察到的相似(11-141毫秒,峰值平均相关性=0.57;4个大脑)。为了验证屏状核在锐波涟漪产生中的因果作用,我们在体外向屏状核选择性注射河豚毒素(TTX)(n=4,3只动物),导致屏状核长时间沉默,同时同侧DVR中的锐波涟漪也随之停止(扩展数据图8b-d)。
接下来,我们在活体中使用鹅膏蕈氨酸对单侧或双侧屏状核进行了损伤处理(方法部分;3只动物)。对睡眠状态下的损伤动物的背侧脑室嵴(DVR)进行双侧记录后发现,β活动(快速眼动期)的节律性调制未受影响,但慢波睡眠特征性的尖波涟漪(SWRs)在屏状核损伤侧消失(图4a-d,补充数据图9)。因此,屏状核是慢波睡眠期间DVR产生尖波涟漪所必需的;其作用是单侧性的;且它不参与慢波睡眠/快速眼动睡眠的交替节律。
由于屏状核接收来自哺乳动物中与睡眠-觉醒产生相关区域的直接输入,并且表达这些区域递质的受体(图3),我们测试了SWR产生对这些递质的敏感性4-6,16。多巴胺(DA)显著提高了SWR的产生率;乙酰胆碱(ACh)和5-羟色胺(5HT)则降低了其产生率(图4e)。我们选择5-羟色胺进行进一步实验。与示踪数据显示的来自中缝核的 serotonergic 输入一致,屏状核中含有5-羟色胺阳性纤维(扩展数据图10a)。浓度≥1µM的5-羟色胺可抑制SWR(n=9个屏状核+背侧脑室嵴切片,9只动物,扩展数据图10b)。HTR1D激动剂L703,664能最好地模拟这种效应(图4f),这与单细胞RNA测序(scRNA-seq)结果一致(扩展数据图5)。随后,我们用笼装5-羟色胺对切片进行灌流(方法部分):光照开始后几秒内SWR受到抑制,光照停止后则恢复(图4g、h)。
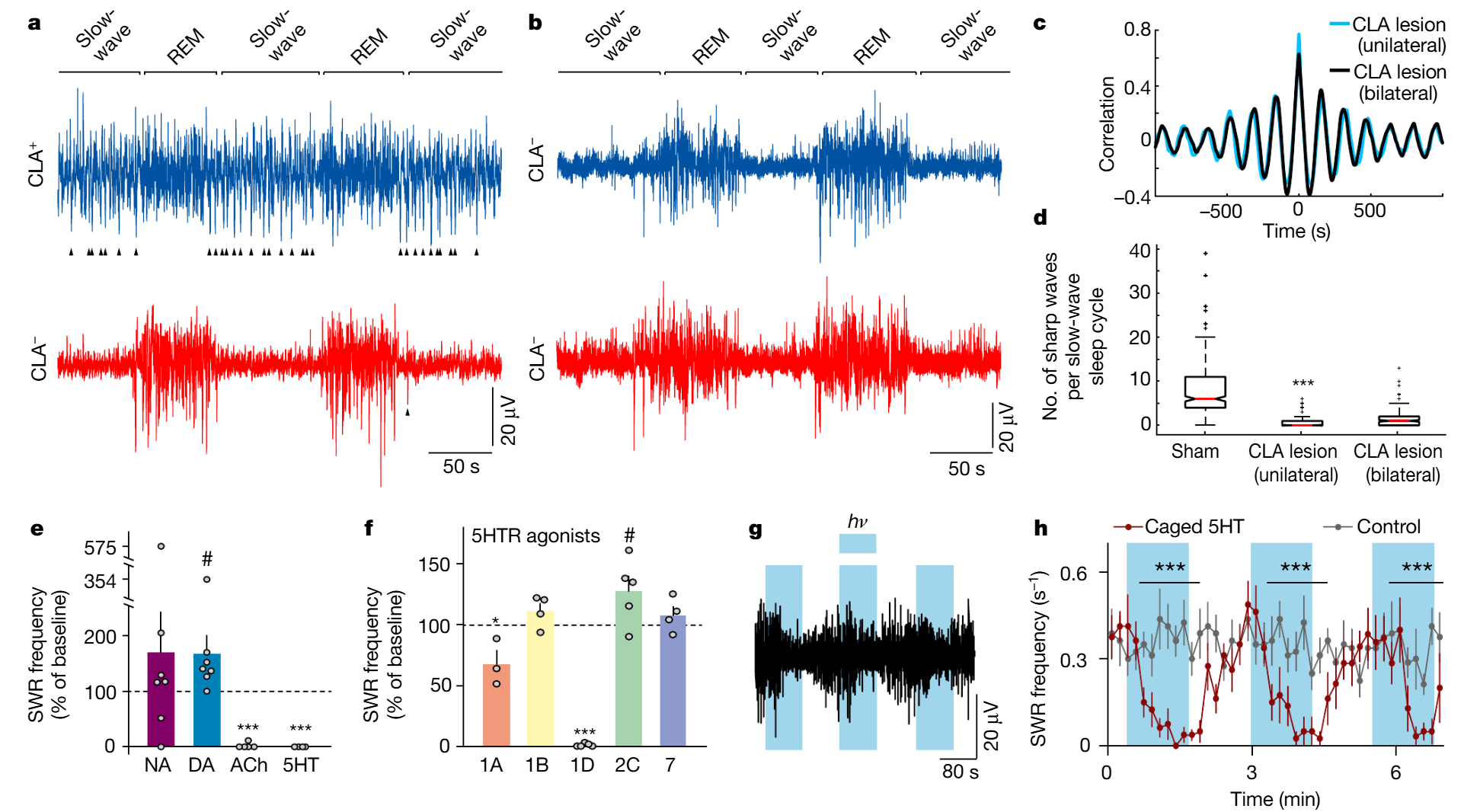
图4 | 背侧脑室嵴(DVR)中的尖波涟漪(SWR)产生依赖于屏状核的完整性和调控。a-d,蜥蜴睡眠时,鹅膏蕈氨酸诱导的屏状核损伤与尖波涟漪(另见扩展数据图9)。a,单侧屏状核损伤后,睡眠短片段显示左、右DVR的局部场电位(LFP,<150Hz)。假手术侧半球(CLA+)以蓝色显示;损伤侧半球(CLA−)以红色显示。箭头指示DVR中的尖波。睡眠节律完整,但损伤侧慢波睡眠中的尖波几乎消失。b,与a相同,为屏状核双侧损伤的蜥蜴。注意尖波消失。c,损伤动物半球间β波段(快速眼动睡眠)功率的互相关。d,假手术组和屏状核损伤组半球每个慢波睡眠周期的尖波数量。,与假手术组有显著差异;P<1.73×10−60,W=64252(威尔科克森符号秩检验;数据来自2只动物,4晚,375个周期)。箱线图详情见方法部分。e-h,DVR+屏状核切片或孤立屏状核切片的实验。e,灌流去甲肾上腺素(NA;25μM;n=7)、多巴胺(DA)激动剂SKF38393(10μM;n=7)、乙酰胆碱(ACh)激动剂卡巴胆碱(50μM;n=5)和血清素(5HT;10μM;n=4)对自发性尖波涟漪频率的影响。f,血清素受体(5HTR)激动剂对孤立屏状核切片中自发性尖波涟漪发生率的作用。n=3次实验(5HTR-1A);n=4(5HTR-1B);n=5(5HTR-1D);n=5(5HTR-2C);n=4(5HTR-7)。、*和#,与基线有显著差异;*P=8.0×10−3,T=15(双侧威尔科克森秩和检验);P=0.04,t4=−2.9;#P=0.049,t8=−2.3(配对t检验)。数据为平均值±标准误(e,f)。g,光触发的血清素解笼锁抑制CLA+DVR切片中的自发性尖波涟漪。蓝色阴影部分,光照开启(hν)。h,如g中所示的8次实验总结,时间区间为10秒。数据为平均值±标准误。对照实验中,对ACSF灌流的切片施加光脉冲。,实验组区间与对照组有显著差异;P=1.5×10−4,T=36(双侧曼-惠特尼秩和检验)。
据推测,哺乳动物的屏状核在高级认知中发挥作用1,28,29,这是因为其具有类似枢纽的连接性12,30-32。然而,由于屏状核的解剖结构特点12,33,直接的实验验证存在难度。通过单细胞RNA测序和示踪技术,我们在两种亲缘关系较远的爬行动物中发现了屏状核,这表明屏状核的起源早于羊膜动物的共同祖先。屏状核可能起源于侧脑 pallium,并且可能与鸟类中脑 pallium的部分结构相对应34,35。因此,如果屏状核在哺乳动物的高级认知中发挥作用,那么这种作用可能源于羊膜动物共同祖先的其他功能。在两种亲缘关系较远的爬行动物中,屏状核呈现出不同的结构特点,这体现在神经元形态上(有袋类哺乳动物和真兽类哺乳动物之间也存在差异36)。由于这两种爬行动物的屏状核都会产生尖波涟漪(SWRs),因此结构特点可能在尖波涟漪的产生过程中作用甚微。
屏状核参与松果蜥慢波睡眠特征性的SWRs(尖波涟漪)的产生和传递。鉴于屏状核广泛的连接性及其来自睡眠/觉醒控制区域的输入,它可能在睡眠期间参与协调前脑状态。早期在猫身上的实验描述了低频刺激屏状核后(尽管不是刺激期间)出现类似睡眠的行为。由于选择性刺激哺乳动物的屏状核存在难度,这些结果仍存在不确定性。最近在啮齿类动物中利用突触活动标志物进行的研究表明,屏状核在快速眼动睡眠期间存在活动。其他研究则认为,屏状核通过对皮质中间神经元的主要投射来关闭大脑皮层。这种作用会导致大脑皮层进入一种普遍的抑制状态,这可能在慢波睡眠的某些阶段中观察到。这些结果共同表明,哺乳动物的屏状核与睡眠之间存在初步联系。
在鬃狮蜥睡眠期间,尖波涟漪(SWRs)起源于屏状核,并传播至非皮质大脑皮层的其他部分,即哺乳动物杏仁核复合体的同源结构11。由于能够接收来自控制觉醒/睡眠区域的上行输入,屏状核处于理想位置,可作为前脑觉醒/睡眠相关状态的中继站。睡眠期间,屏状核在尖波涟漪产生和快速眼动(REM)之间交替,推测这是由交替的上行输入驱动的,而这些输入本身并不依赖屏状核的完整性。屏状核的投射表明其对大脑皮层、海马体、杏仁核和其他前脑区域具有分布式作用。在活体睡眠的鬃狮蜥中,每个尖波涟漪都与大脑皮层的短暂相位性抑制相关[与刺激实验(扩展数据图8)以及啮齿动物的研究结果一致39,40],随后会出现皮层兴奋3[与啮齿动物的CA1区-内侧前额叶皮层协调一致41]。现在必须明确这种协调背后的机制,以及屏状核接收的睡眠相关输入的性质。
¶ 致谢
我们感谢K. Steele和A. Schwartzlose在5-羟色胺免疫细胞化学和神经束追踪方面提供的帮助,感谢E. Northrup博士和G. Wexel博士提供的兽医护理,感谢T. Klappich的爬行动物护理工作,感谢S. Junek、F. Vollrath和C. Polisseni在成像和显微镜方面的帮助,感谢G. Tushev在基因组重新注释方面的帮助,感谢西班牙莱里达大学的E. Desfilis在蜥蜴神经解剖学方面的帮助,以及Laurent实验室提供的帮助和建议。本研究由马克斯·普朗克学会、欧盟第七框架计划(FP7/2007-2013)下的欧洲研究理事会(ERC资助协议编号322705)、欧盟“地平线2020”研究与创新计划下的欧洲研究理事会(ERC资助协议编号834446)和德国研究基金会(CRC1080)(G.L.)、日本学术振兴会(SPD及海外研究项目)的博士后奖学金、鼎三纪念医科学振兴财团(H.N.)以及欧洲分子生物学组织长期奖学金(ALTF 421-2017)(L.A.F.)资助。
¶ 作者贡献
H.N.和L.A.F.贡献相同,在文献目录中拥有同等的优先署名权;项目构思:H.N.、L.A.F.和G.L.;动物手术:M.K.、H.N.和L.A.F.;电生理学:H.N.、L.A.F.和S.R.;药理学:H.N.、R.K.和L.A.F.;单细胞RNA测序:M.T.G.F.、D.H.、A.M.和M.A.T.;生物信息学:M.A.T.和D.H.;示踪、解剖学和组织学:L.A.F.、H-H.L.、R.K.、M.T.G.F.、A.A.和M.K.;实验设计、数据解读与分析:H.N.、L.A.F.、H-H.L.、M.A.T.、M.T.G.F.、D.H.、S.R.和G.L.;项目管理与监督:G.L.;手稿撰写:G.L.,并结合了所有作者的意见。
¶ 利益冲突
作者声明不存在利益冲突。
¶ 材料与通信
序列、代码和链接可在https://brain.mpg.de/research/laurentdepartment/software-techniques.html找到。数据可根据请求提供。通讯方式:gilles.laurent@brain.mpg.de。
¶ 参考文献
- Saper, C. B. 和 Fuller, P. M. 睡眠-觉醒回路概述。《当代神经生物学观点》44期,186-192页,doi:10.1016/j.conb.2017.03.021(2017)。
- 韦伯(F.)和丹(Y.)。基于回路的睡眠控制探究。《自然》538期,51-59页,doi:10.1038/nature19773(2016)。
- 利亚明(O. I.)、曼格(P. R.)、里奇韦(S. H.)、穆哈梅托夫(L. M.)和西格尔(J. M.)。鲸类睡眠:一种不寻常的哺乳动物睡眠形式。《神经科学与行为评论》32期,1451-1484页,doi:10.1016/j.neubiorev.2008.05.023(2008)。
- Shein-Idelson, M.、Ondracek, J. M.、Liaw, H. P.、Reiter, S. 和 Laurent, G. 睡眠中蜥蜴的慢波、尖波、涟漪和快速眼动。《科学》352期,590-595页,doi:10.1126/science.aaf3621(2016)。
- 布扎基(G. Buzsaki)。海马体锐波-涟漪:情景记忆和规划的认知生物标志物。《海马体》25期,1073-1188页,doi:10.1002/hipo.22488(2015)。
- 瑙曼,R. K. 和洛朗,G. 收录于《神经系统的进化》第1卷(J.H. 卡斯主编)第1.25章,491-518页(爱思唯尔出版社,2017)。
- 莫雷诺(N.)和冈萨雷斯(A.)。脊椎动物杏仁核复合体的进化,特别关注无羊膜动物到羊膜动物的过渡。《解剖学杂志》211期,151-163页,doi:10.1111/j.1469-7580.2007.00780.x(2007)。
- Puelles, L. 等. 收录于《神经系统进化》第1卷(Jon H Kaas 编),519-555页(爱思唯尔出版社,2017)。
- 托谢斯(M. A.)等人。爬行动物单细胞转录组学揭示的大脑皮层、海马体和皮质细胞类型的进化。《科学》360卷,881-888页,doi:10.1126/science.aar4237(2018)。
- 王庆霞等。小鼠屏状核与皮质之间连接的组织。《比较神经学杂志》525卷,1317-1346页,doi:10.1002/cne.24047(2017)。
- 桑德斯(A.)等人。成年小鼠脑细胞的分子多样性和特异性。《细胞》174期,1015-1030.e1016页,doi:10.1016/j.cell.2018.07.028(2018)。
- Stuart, T. 等。单细胞数据的综合整合。《细胞》177卷,1888-1902.e1821页,doi:10.1016/j.cell.2019.05.031(2019)。
- Striedter, G. F. 四足动物端脑的进化。《大脑、行为与进化》49卷,179-194页(1997)。
- Scammell, T. E., Arrigoni, E. & Lipton, J. O. 觉醒与睡眠的神经环路。《神经元》93卷,747-765页,doi:10.1016/j.neuron.2017.01.014(2017)。
- 蒙蒂,J. M. 血清素对睡眠-觉醒行为的调控。《睡眠医学综述》15卷,269-281页,doi:10.1016/j.smrv.2010.11.003(2011)。
- Clement, O.、Sapin, E.、Berod, A.、Fort, P. 和 Luppi, P. H. 有证据表明,触发异相(快速眼动)睡眠的被盖区亚外侧背核神经元是谷氨酸能的。《睡眠》34卷,419-423页,doi:10.1093/sleep/34.4.419(2011)。
- 克里克,F. C. 和科赫,C. 屏状核的功能是什么?《英国皇家学会哲学会报B辑:生物科学》360卷,1271-1279页,doi:10.1098/rstb.2005.1661(2005)。
- da Costa, N. M., Fursinger, D. 及 Martin, K. A. 屏状核投射至猫视觉皮层的突触结构。《神经科学杂志》30卷,13166-13170页,doi:10.1523/jneurosci.3122-10.2010(2010)。
- Druga, R. 收录于《屏状核:结构、功能与临床神经科学》(J.R. Smythies、L.R. Edelstein 与 V.S. Ramachandran 编)第2章,29-84页(学术出版社,2014)。
- 奥尔森,C. R. 与格雷比尔,A. M. 猫屏状核中的感觉图谱。《自然》288卷,479-481页(1980)。
- 霍布森,J. A.、麦卡利,R. W. 和怀津斯基,P. W. 睡眠周期振荡:两个脑干神经元群的交互放电。《科学》189卷,55-58页(1975)。
- Pammer, L. 通过分子、光遗传学和电生理学技术探索海龟皮层功能. 博士论文,法兰克福歌德大学(2017)。
- Tervo, D. G. 等。一种设计的AAV变体可有效逆行进入投射神经元。《神经元》92卷,372-382页,doi:10.1016/j.neuron.2016.09.021(2016)。
- Oh, S. W. 等人。小鼠大脑的中尺度连接组。《自然》508卷,207-214页,doi:10.1038/nature13186(2014)。
- 哈里斯,J. A.、吴,S. W. 和曾,H. 腺相关病毒载体用于在非转基因和cre驱动小鼠中通过荧光蛋白进行顺行轴突追踪。《神经科学当前方案》第1章,第1.20.21-18单元,doi:10.1002/0471142301.ns0120s59(2012)。
- 德桑(P. H.). 收录于《爬行动物的前脑》(WK·施韦尔特菲格与WJ·斯梅茨编)第1章,1-11页(卡尔格出版社,1987)。
- Heller, S. B. 和 Ulinski, P. S. 伪龟属和锦龟属海龟膝状体皮质轴突的形态学。《解剖学与胚胎学》175卷,505-515页(1987)。
- Atlan, G. 等。屏状核支持抗干扰能力。《当代生物学》28卷,2752-2762.e2757页,doi:10.1016/j.cub.2018.06.068(2018)。
- 史密斯(Smythies, J.)、爱德斯坦(Edelstein, L.) 和拉马钱德兰(Ramachandran, V.) 关于屏状核功能的假说。《前沿整合神经科学》6卷,53页,doi:10.3389/fnint.2012.00053(2012)。
- 迪林厄姆(C. M.)、雅诺夫斯基(M. M.)、钱德拉(R.)、弗罗斯特(B. E.)和奥马拉(S. M.)。屏状核:关于其解剖结构、功能及研究计划的思考。《脑与神经科学进展》1卷,1-9页(2017)。
- Edelstein, L. R. 与 Denaro, F. J. 屏状核:其解剖学、生理学、细胞化学及功能意义的历史回顾。《细胞与分子生物学(法国努瓦西勒格朗)》50卷,675-702页(2004)。
- Goll, Y., Atlan, G. 及 Citri, A. 注意力:屏状核。《神经科学趋势》38卷,486-495页,doi:10.1016/j.tins.2015.05.006(2015)。
- 马瑟(B. N.)、卡普里奥利(R. M.)和多伊奇(A. Y.)。蛋白质组学分析揭示了屏状核和岛叶的一种新的结构定义。《大脑皮层》19卷,2372-2379页,doi:10.1093/cercor/bhn253(2009)。
- 普埃列斯,L. 收录于《屏状核》(J. 史密斯、L. 埃德尔斯坦、V. 拉马钱德兰 编)第4章,119-176页(爱思唯尔公司,2014)。
- 布里斯科(S. D.)、阿尔贝廷(C. B.)、罗威尔(J. J.)和拉格斯代尔(C. W.)。鸟类和鳄鱼前脑中的新皮质联合细胞类型。《当代生物学》28卷,686-696.e686页,doi:10.1016/j.cub.2018.01.036(2018)。
- 布坎南,K.J. 和约翰逊,J.I. 哺乳动物辐射分支中屏状核和岛叶空间关系的多样性。《纽约科学院年鉴》1225增刊1,E30-63页,doi:10.1111/j.1749-6632.2011.06022.x(2011)。
- Gabor, A. J. 和 Peele, T. L. 刺激猫的屏状核后行为的改变。《脑电图学与临床神经生理学》17卷,513-519页(1964)。
- Renouard, L. 等人。乳头体上核和屏状核在快速眼动睡眠期间激活大脑皮层。《科学进展》1卷,e1400177页,doi:10.1126/sciadv.1400177(2015)。
- Jackson, J.、Karnani, M. M.、Zemelman, B. V.、Burdakov, D. 和 Lee, A. K. 屏状核对前额叶皮层的抑制性控制。《神经元》99卷,1029-1039.e1024页,doi:10.1016/j.neuron.2018.07.031(2018)。
- Narikiyo, K. 等人。屏状核协调皮质慢波活动。bioRxiv,286773,doi:10.1101/286773(2018)。
- Siapas, A. G. 与 Wilson, M. A. 慢波睡眠期间海马涟漪与皮质纺锤波之间的协调相互作用。《神经元》21卷,1123-1128页(1998)。
- Hoops, D. 等。基于3D MRI的蜥蜴脑图谱。《比较神经学杂志》526卷,2511-2547页,doi:10.1002/cne.24480(2018)。
- 莫雷诺(N.)、多明格斯(L.)、莫罗纳(R.)和冈萨雷斯(A.)。基于调节基因和神经元标志物的表达对巴西彩龟下丘脑的分区。《比较神经学杂志》520期,Spc1-Spc1页,doi:10.1002/cne.23022(2012)。
- Medina, L.、Smeets, W. J.、Hoogland, P. V. 和 Puelles, L. 蜥蜴Gallotia galloti大脑中胆碱乙酰转移酶免疫反应性的分布。《比较神经学杂志》331卷,261-285页,doi:10.1002/cne.903310209(1993)。
- 麦金尼斯(L. McInnes)、希利(J. Healy)和梅尔维尔(J. Melville)。UMAP:用于降维的均匀流形逼近与投影。arxiv.org/abs/1802.03426(2018)。
- 布鲁斯(L. L.)和尼里(T. J.)。大壁虎腹内侧下丘脑核的传入投射。《脑行为进化》46卷,14-29页,doi:10.1159/000113255(1995)。
- 布鲁斯(L. L.)和尼里(T. J.)。大壁虎外侧和背内侧下丘脑的传入投射。《脑行为进化》46期,30-42页,doi:10.1159/000113256(1995)。
- 埃布纳,F. F. 收录于《脊椎动物脑与行为的进化》(R.B. 马斯特顿、M.E. 比特曼、C.B.G. 坎贝尔、N. 霍顿 编),115-167页(泰勒与弗朗西斯集团,1976)。
- 丰特(C.)、拉努萨(E.)、马丁内斯-马科斯(A.)、胡格兰德(P. V.)和马丁内斯-加西亚(F.)。蜥蜴端脑的隔复合体:III.传出连接及综合讨论。《比较神经学杂志》401期,525-548页(1998)。
- Hoogland, P. V. 和 Vermeulen-Vanderzee, E. 利用菜豆白细胞凝集素研究大壁虎背皮质的传出连接。《比较神经学杂志》285卷,289-303页,doi:10.1002/cne.902850302(1989)。
- Smeets, W. J. 和 Steinbusch, H. W. 壁虎前脑和中脑中去甲肾上腺素免疫反应性的分布。《比较神经学杂志》285卷,453-466页,doi:10.1002/cne.902850404(1989)。
- Smeets, W. J., Hoogland, P. V. 和 Voorn, P. 大壁虎前脑和中脑中多巴胺免疫反应性的分布:使用抗多巴胺抗体的免疫组织化学研究。《比较神经学杂志》253卷,46-60页,doi:10.1002/cne.902530105(1986)。
- ten Donkelaar, H. J., Bangma, G. C., Barbas-Henry, H. A., de Boer-van Huizen, R. 及 Wolters, J. G. 蜥蜴(Varanus exanthematicus)的脑干。《解剖学、胚胎学与细胞生物学进展》107卷,1-168页(1987)。
- ten Donkelaar, H. J. 收录于《脊椎动物的中枢神经系统 第1、2、3卷》,1315-1524页(施普林格出版社,柏林,海德堡,1998)。
- Wolters, J. G., ten Donkelaar, H. J., Steinbusch, H. W. 及 Verhofstad, A. A. 蜥蜴(Varanus exanthematicus)脑干和脊髓中血清素的分布:一项免疫组织化学研究。《神经科学》14卷,169-193页(1985)。
- Wolters, J. G., ten Donkelaar, H. J. 与 Verhofstad, A. A. 蜥蜴(Varanus exanthematicus)脑干和脊髓中儿茶酚胺的分布:基于酪氨酸羟化酶抗体的免疫组织化学研究。《神经科学》13卷,469-493页(1984)。
- Pedersen, N.P., Ferrari, L., Venner, A. 等人。乳头体上核谷氨酸神经元是觉醒系统的关键节点。《自然·通讯》8卷,1405页,doi:10.1038/s41467-017-01004-6(2017)。
¶ Methods 方法
¶ ANIMALS 动物
蜥蜴:从我们研究所的群体中获取了雌雄不限的鬃狮蜥(学名Pogona vitticeps,被称为“澳大利亚龙”),并根据性别、体型、体重、健康状况和野生型体色进行了筛选,其体重在100-400克之间。
海龟:野生型海龟(红耳滑龟或锦龟),雌雄不限,体重200至400克,购自美国威斯康星州NASCO Biology的露天繁殖群体。这些海龟饲养在我们最先进的动物设施中。
所有实验程序均按照德国动物福利指南进行:许可证编号V54-19c 20/15-F126/1005,由德国达姆施塔特行政区政府(E. Simon博士)颁发。
¶ 记录
¶ 用于慢性记录的蜥蜴手术
手术前24小时,给蜥蜴注射了镇痛药(布托啡诺:0.5毫克/千克,皮下注射;美洛昔康:0.2毫克/千克,皮下注射)和抗生素(马波沙星,马波西尔,2毫克/千克)。手术当天,先用异氟烷诱导麻醉,插管后以异氟烷(1-4体积%)维持麻醉。确认蜥蜴处于深度麻醉状态(无角膜反射)后,将其固定在立体定位仪上。手术期间,使用加热垫和食道温度探头将体温维持在32°C。用多普勒血流探测器监测心率。用手术刀切除覆盖颅骨的皮肤前,先用10%聚维酮碘溶液对该皮肤进行消毒。然后沿中线在顶眼后外侧钻一个小(约3×2毫米)的颅骨开口。用精细镊子去除覆盖前脑的硬脑膜和蛛网膜,在电极插入区域(背侧/背内侧皮质)轻轻去除软脑膜。在暴露的颅骨上涂一层紫外固化胶,将两根绝缘不锈钢丝的裸露端用紫外固化胶固定在硬膜下,作为参考电极和接地电极。
硅探针植入:将探针安装在Nanodrive(剑桥神经科技公司)上,并固定在立体定位适配器上。手术后第二天,将探针缓慢放入组织中(约0.9-1.2毫米)。用Duragel覆盖大脑,随后涂上凡士林。连接接地线后,用牙科水泥固定颅骨、开颅部位和探针。手术后,将蜥蜴从立体定位仪中取出,放在设定为32°C的加热垫上,直至从麻醉状态完全恢复。
¶ 体内电生理学
手术前一周,动物在睡眠场中适应至少2晚。熄灯前1到2小时,将蜥蜴放入睡眠场,睡眠场则置于一个3×3×3米的电磁屏蔽室内。让动物在夜间自然睡眠和活动,开灯后3到4小时将其放回原饲养箱。随后给动物喂食和供水。对慢性植入电极的成年蜥蜴的大脑皮层、前背侧脑室嵴(包括屏状核)和/或后背侧脑室嵴进行记录。电极采用32通道硅探针(间距50微米,每个位点的表面积为177平方微米;分为两排,每排16个触点)。
记录使用Cheetah Digital Lynx SX系统和HS-36前置放大器进行,前置放大器具有单位增益和高输入阻抗(约1太欧)。前置放大器通过一个前置放大器适配器连接到头部的连接器上,一根轻质屏蔽系绳电缆将前置放大器与采集系统相连。记录接地,并以其中一根参考线为参考。信号采样频率为32kHz,带宽为0.1–9000Hz。电生理轨迹通常用2阶巴特沃斯滤波器过滤至150Hz以下以进行显示。
¶ 鹅膏蕈氨酸损伤实验
为了准备屏状核损伤实验,我们在麻醉动物中使用精细镊子小心移除覆盖背侧皮质的软脑膜,并以与表面成90度角插入带斜角的石英微量吸管,插入深度为距表面1050–1150微米,且处于合适的前后(a-p)和内外(m-l)坐标位置,以到达屏状核中心。将400–600纳升的鹅膏蕈氨酸(在磷酸盐缓冲盐水(PBS,pH 7.2)中浓度为5微克/微升)以50–100纳升/分钟的速度注射(使用UMP3,美国World Precision Instruments公司产品)。注射结束后3分钟撤回注射吸管。随后,如前所述,在双侧放置两个硅记录探针进行数字视频记录(DVR)。对于假屏状核损伤组,我们在假损伤侧仅注射PBS(方法和体积相同)。术后1至6天的每个晚上都进行记录。术后24小时已能观察到损伤的效果。每个实验结束一周后,处死动物,对其大脑进行切片并染色(尼氏染色)以进行组织学确认。
¶ SWR延迟计算
尖波的检测方法如前所述(基于模板的检测3)。在整个数据集中独立检测前侧和后侧DVR探针上的尖波涟漪(SWRs)后,通过将一个探针上的尖波涟漪与第二个探针上时间最接近的尖波涟漪配对,计算探针间尖波涟漪的延迟。间隔超过500毫秒的配对将被忽略。
¶ SWS-REMS转换点的锐波波纹(SWRs)
快速眼动睡眠(REMS)和慢波睡眠(SWS)阶段及其转换时间,按先前描述的方法计算3。平均棘波涟漪(SWR)率和振幅通过对所有慢波睡眠-快速眼动睡眠转换点触发的这些数值在100毫秒区间内取平均值,并使用高斯滤波器(标准差25毫秒)对所得直方图进行平滑处理来计算。
在鹅膏蕈氨酸损伤实验中,睡眠周期是通过中值滤波后的β波段功率(10-40赫兹,如上所述)来确定的,监测时段为记录开始后3小时起的6小时内。β波段的时间进程采用2阶巴特沃斯滤波器进行0.001赫兹以上的滤波,此外还使用高斯滤波器(标准差20秒)进行平滑处理。慢波睡眠(SWS)时段被保守定义为该信号低于平均值1个标准差的时段。为避免在损伤动物中观察到的假性慢波检测(这些动物表现出低频功率降低),慢波的检测是通过对电压轨迹(低于平均值1.5-2.5个标准差)进行阈值处理实现的,处理前已采用2阶巴特沃斯滤波器进行4赫兹的低通滤波。阈值根据每个损伤实验进行调整,且每个实验中两个半球的阈值保持一致。
¶ 锐波形状统计
为了与体外和切片锐波进行比较,在体检测到的锐波使用2阶巴特沃斯滤波器进行了20Hz的低通滤波。
¶ 体外和切片制备
成年蜥蜴或乌龟用异氟烷、氯胺酮(60毫克/千克)和咪达唑仑(2毫克/千克)进行深度麻醉。角膜反射消失后,将动物断头,头部迅速转移至冷却的人工脑脊液(ACSF)溶液中(蜥蜴:126 mM氯化钠、3 mM氯化钾、1.8 mM氯化钙、4 mM氯化镁、24 mM碳酸氢钠、0.72 mM磷酸二氢钠、20 mM葡萄糖,pH 7.4;乌龟:96.5 mM氯化钠、2.6 mM氯化钾、4 mM氯化钙、2 mM氯化镁、31.5 mM碳酸氢钠、20 mM葡萄糖,pH 7.4),并通入 carbogen 气体(95%氧气、5%二氧化碳)。
体外完整皮层下标本:分离蜥蜴大脑后,用虹膜剪制备皮层下薄片。
切片制备:使用振动切片机(VT 1200S,徕卡)在冰冷、充氧的人工脑脊液(ACSF)中制备冠状、水平或矢状皮层下区域切片(厚度700微米)。让切片恢复至少60分钟,然后将其浸入充满充氧人工脑脊液的培养室中(蜥蜴:126 mM氯化钠、3 mM氯化钾、1.8 mM氯化钙、1 mM氯化镁、24 mM碳酸氢钠、0.72 mM磷酸二氢钠、20 mM葡萄糖,pH 7.4;龟:96.5 mM氯化钠、2.6 mM氯化钾、4 mM氯化钙、2 mM氯化镁、31.5 mM碳酸氢钠、20 mM葡萄糖,pH 7.4),温度保持在20–22°C。
体外/切片生理学与尖波涟漪(SWR)检测:记录期间,含氧的人工脑脊液(ACSF)(蜥蜴:126 mM氯化钠、3 mM氯化钾、1.8 mM氯化钙、1.2 mM氯化镁、24 mM碳酸氢钠、0.72 mM磷酸二氢钠、20 mM葡萄糖,pH 7.4;乌龟:96.5 mM氯化钠、2.6 mM氯化钾、4 mM氯化钙、2 mM氯化镁、31.5 mM碳酸氢钠、20 mM葡萄糖,pH 7.4)以4 ml/min的速度持续灌流,体外实验温度为18-20°C,切片实验温度为18-21°C。局部场电位(LFP)通过微电极阵列(MEA)、硅探针或充满ACSF的玻璃吸管记录。使用显微操作器将电极小心放置在目标区域。信号经2kHz低通滤波后以20kHz采样数字化。为分析尖波(SW),轨迹进一步通过2阶巴特沃斯滤波器进行20Hz低通滤波。SWR的检测阈值设为总信号标准差的3倍。对检测到的事件进行视觉检查,若为错误检测则手动剔除。持续时间少于30ms的事件也会被舍弃,因为它们通常是伪迹。在屏状核电刺激实验中,刺激脉冲持续50µs,通过双极电极传递。皮质中的多单位细胞外记录使用充满ACSF的玻璃微吸管进行。微型切片用锋利的刀片切割,表面积为0.61-3.12 mm²。
¶ CMOS微电极阵列实验
切片被放置在一个高密度MEA(3Brain AG)上,该MEA有4096个电极(电极尺寸为21×21μm;间距为81μm;64×64矩阵;面积为5.12×5.12mm)。记录期间,ACSF灌流被中断,以避免切片移动以及因ACSF流动产生的噪声。信号以18kHz采样,高通滤波器设置为1Hz。
检测到电压超过±500微伏的饱和或受损通道后,会将其从后续分析中剔除。通道数据经过20赫兹低通滤波、z分数标准化处理,在信号最强的通道上,将比平均值低5个z分数以上的波谷视为慢波(SWs)。所有通道上,这些峰值时间前后±400毫秒的信号被视为一个慢波睡眠事件(SWR episode)。为计算慢波睡眠事件的潜伏期,对每个通道的慢波睡眠事件进行平均,将平均信号降至平均值以下1个z分数的时间作为该通道慢波睡眠事件的起始时间。潜伏期是相对于最早出现慢波睡眠事件的通道的时间来计算的。未降至1个z分数以下的通道被视为具有最大潜伏期。所得的潜伏期图像通过3×3中值滤波处理,以消除不良通道的影响,并进行10倍上采样以便显示。
¶ DVR和屏状核神经元的全细胞膜片钳(WCPC)记录
长柄贴片吸管(6-8兆欧)由硼硅酸盐玻璃通过Sutter P1000电极拉制仪拉制而成。吸管内填充有内液(140mM葡萄糖酸钾、4mM氯化钠、14mM磷酸肌酸、10mM HEPES、4mM Mg-ATP、0.3mM Na-GTP、4mg/ml生物胞素)。实验在奥林巴斯BX61WI upright显微镜上进行,使用5倍和40倍水浸物镜,并在视觉引导下对细胞进行贴片。在电压钳模式下记录EPSC和IPSC,同一细胞分别钳制在-70 mV或+10 mV。使用EPC10 Quadro放大器(HEKA)同时进行膜片钳和LFP记录。
¶ 药理学
5-羟色胺盐酸盐(0.1-30μM)、氯化氨甲酰胆碱(50μM)、重酒石酸去甲肾上腺素(25μM)、氢溴酸SKF38393(10μM)、®-(+)-8-羟基-DPAT氢溴酸盐(2μM)、琥珀酸L-703,664(1μM)、盐酸CP 809,101(0.1μM)、LP44(0.2μM)和河豚毒素(20μM)在人工脑脊液(126 mM氯化钠、3 mM氯化钾、1.8 mM氯化钙、1.2 mM氯化镁、24 mM碳酸氢钠、0.72 mM磷酸二氢钠、20 mM葡萄糖,pH 7.4)中稀释至最终浓度。在切片实验中,经过5-20分钟的基线记录后,持续灌流给药。在补充数据图8的离体实验中,将溶于人工脑脊液的河豚毒素通过玻璃微吸管注入屏状核,使用10毫升注射器加压器(20-30百帕,持续15分钟)。对于5-羟色胺光解笼锁实验,灌流应用RuBi-5HT(Abcam公司,10μM),并以选定的间隔(如80秒)开启和关闭白光(400-700纳米,0.11瓦/平方厘米,TH4-200,奥林巴斯)。
我们测试了几种代谢型5-羟色胺受体激动剂。其中,1D激动剂L-703,664最能模拟5-羟色胺的作用,这与屏状核谷氨酸能神经元中5HT1D受体的高表达一致(扩展数据图5a)。5HT7受体激动剂LP44没有效果(图4f),这也与屏状核兴奋性神经元中5HT7受体的低表达相符。5HT2C受体激动剂CP 809,101增加了锐波涟漪的频率,但没有改变其振幅。
¶ 单细胞转录组学
¶ 单细胞RNA测序文库
成年雄性蜥蜴(150-400克)用异氟烷、氯胺酮(50毫克/千克)和咪达唑仑(0.5毫克/千克)深度麻醉后断头。将头部浸入冰冷的、充氧的人工脑脊液(126 mM氯化钠、3 mM氯化钾、2 mM氯化钙、4 mM氯化镁、24 mM碳酸氢钠、0.72 mM磷酸二氢钠、20 mM葡萄糖,pH 7.4)中。对大脑进行灌流以清除血管中的血液。所示数据来自四个文库,这些文库由一只雄性蜥蜴(160克,20个月大)的数据构建而成。
随后,取出大脑并将其浸入含氧的冰冷ACSF中。将大脑包埋在4%低熔点琼脂糖中,粘在振动切片机(VT1200S,徕卡)的底座上,浸入冰冷的含氧ACSF中,制备500μm厚的切片(速度:0.08毫米/秒)。在解剖显微镜(Stemi 2000-C,蔡司)下对切片进行单独检查,并解剖感兴趣的解剖区域(端脑、amDVR)。用精细剪刀(Fine Science Tools)将这些切片剪成小组织块(约500×500×500μm)。
这些被转移到解离缓冲液(20 U/ml木瓜蛋白酶、200 U/ml DNA酶I、25 μg/ml解放酶TM、1 μM河豚毒素(TTX)、100 μM D-APV)中,并用尖端直径逐渐减小的火焰抛光硅烷化玻璃移液管研磨(每个移液管约10次)。每次更换移液管后,取出上清液(解离的细胞悬液),并通过100 μm孔径的滤网过滤。
将混合的解离细胞悬液稀释至20毫升(使用不含氯化钙的Hibernate A培养基),转移到50毫升反应管中,并用直径40微米的滤网过滤。然后用长柄玻璃移液管向管底加入5毫升含4%牛血清白蛋白(BSA)的不含氯化钙的Hibernate A培养基。将溶液在4°C下以300g的离心力(最低加速度和制动)离心5分钟。移除上清液,将细胞沉淀重悬于20毫升不含氯化钙的Hibernate A培养基中。重复此步骤进行第二次梯度净化。随后,将沉淀重悬于适量(50-200微升)含氯化镁的Hibernate A培养基中,并使用Fuchs-Rosenthal细胞计数板(Brand品牌)测量细胞浓度。
然后将细胞悬液稀释至466个细胞/微升,并作为10x Chromium系统(Chemistry v3)半张芯片(四个样本)的输入,目标每个样本回收7000个细胞。按照制造商的说明进行文库构建。
最后四个文库使用Qubit荧光计(赛默飞世尔)进行定量,并在DNA测序仪(NextSeq 500,Illumina)上测序五次,平均深度为442,806,563条读数/文库。
¶ 转录组学数据分析
原始测序数据使用Cellranger v3.0(10X Genomics)进行处理。原始读数通过cellranger mkfastq函数进行解复用和过滤,采用默认设置。为生成数字基因表达矩阵,解复用后的读数通过cellranger count函数与鬃狮蜥基因组比对,将force-cells参数设为7000。在读数比对方面,我们使用相同的3’端MACE(cDNA末端大规模分析)数据和参考文献11中描述的方法,对鬃狮蜥基因组(组装版本1.1.0,NCBI登录号GCF_900067755.1,2017年4月10日)进行了重新注释。
使用Seurat v3.0软件包14在R中对数字基因表达矩阵进行了分析。根据基因数量(>800个基因/细胞)和线粒体基因百分比(>5%)对细胞进行筛选,最终得到20257个细胞,每个细胞的转录本中位数为2278个,基因中位数为1349个。通过每个细胞中检测到的转录本总数对数据进行标准化,并通过基因和转录本的数量进行回归(在ScaleData函数中设置vars.to.regress = c(“nFeature_RNA”,“nCount_RNA”))。在根据均值-方差关系估计进行方差标准化后识别可变基因(FindVariableFeature,method=”vst”),并使用排名前1000的高可变基因进行主成分分析。前30个主成分用于Louvain聚类(FindClusters,resolution=0.2)和UMAP45降维(使用默认设置的RunUMAP)。
在第一轮分析之后,研究人员使用上述相同的程序和以下设置对神经元集群(以泛神经元标志物的高表达为特征,例如突触蛋白SNAP25)进行了重新分析:每个细胞>800个基因、2000个高可变基因、30个主成分、聚类分辨率=2。这确定了33个神经元集群。在此阶段,通过谷氨酸能和γ-氨基丁酸能标志物的共表达识别出的两个双细胞集群被过滤掉,剩下29个集群中的9777个神经元(扩展数据图3)。
从这个神经元数据集中,我们识别出4054个脑皮层谷氨酸能神经元(每个细胞有1000多个基因),这些神经元共表达囊泡谷氨酸转运体SLC17A7和SLC17A6。对这些细胞的进一步亚聚类(分析设置:2000个高可变基因、34个主成分、聚类分辨率=3)得到了29个聚类(图3a和扩展数据图3)。为了确定每个聚类的特性,我们分析了具有已知组织表达模式的标记基因的表达情况(参考文献11中的数据和方法)。这使我们能够确定每个聚类所属的脑皮层区域(例如,表达ZBTB20的聚类属于海马体)。聚类特性的进一步注释(扩展数据图3)基于从转录组学数据中识别出的选择性标记物的表达或标记基因的组合。
¶ 离子通道和神经递质受体基因的分析
我们从鬃狮蜥基因组中挖掘了以下基因家族:去甲肾上腺素、乙酰胆碱、血清素和多巴胺受体,钙、氯、钠和钾通道,γ-氨基丁酸(GABA)、谷氨酸、腺苷、大麻素、甘氨酸和组胺受体。这总共得到了270个基因。其中,143个基因被保留用于进一步分析,因为它们在至少一个谷氨酸能簇中至少20%的细胞中被检测到(扩展数据图5a)。
为了计算成对的簇相关性(皮尔逊相关性,扩展数据图5b),我们使用了这143个基因的集合和平均簇表达数据(通过Seurat包中的AverageExpression函数对标准化和对数转换后的数据进行计算得到)。从相关矩阵计算出距离矩阵,并将其用于采用Ward.D2连接方法的层次聚类(R包hclust)。
将上述基因表达矩阵进行转置,以计算基因间的相关性(图3g)。基因 dendrogram 也通过层次聚类和 Ward.D2 连接法计算得出。
图3h中的热图由29个谷氨酸能簇(列)和143个基因的平均表达量(行)组成的矩阵生成。数据矩阵按列进行缩放,热图使用R包gplots中的heatmap.2函数绘制。谷氨酸能簇的树状图基于欧氏距离和Ward.D2连锁法构建。
¶ 跨物种单细胞转录组图谱绘制
为了将鬃狮蜥的单细胞转录组映射到小鼠的单细胞数据上,我们使用了参考文献13中的数据集,该数据集可在dropviz.org网站上获取。在这个数据集中,大脑皮层谷氨酸能神经元取自三个区域:“海马体”、“额叶皮层”和“后皮层”。这些解剖区域包含多种细胞类型;例如,“额叶皮层”包括屏状核,“海马体”包括下托和内嗅皮层。原始数据通过Seurat流程进行处理(标准化、缩放、可变基因选择),并根据Saunders等人(参考文献13)和dropviz.org提供的集群和亚集群标识,筛选出谷氨酸能集群及亚集群。对亚集群进行下采样,每个亚集群最多保留200个细胞,最终得到17455个细胞。
鬃狮蜥与小鼠的比较分析仅限于一对一直系同源基因,依据的是Ensembl提供的直系同源注释(鬃狮蜥基因组组装版本pv1.1和小鼠基因组组装版本GRCm38.p6,一对一直系同源基因下载于2019年5月1日)。在13273个一对一直系同源基因中,有10693个在小鼠和鬃狮蜥的数据集中均被检测到,并用于比较分析。
采用参考文献14中描述的方法对鬃狮蜥和小鼠的数据进行联合分析。简要来说,经过标准化和缩放后,在每个数据集中鉴定出1500个高可变基因。这些可变基因集的并集被用于联合典型相关分析(CCA)。随后,前15个典型成分被用于鉴定2626个转移锚点,即两个转录组空间中具有匹配邻域(“互最近邻”)的细胞对(来自Seurat的FindTransferAnchors函数)。然后,利用Seurat的TransferData函数,这些锚点被用于将鬃狮蜥细胞(“查询”数据集)投射到小鼠数据集(“参考”数据集)上。该投射基于加权分类器,该分类器根据每个细胞与转移锚点的距离分配分类分数。图3g展示了分类结果,显示了来自每个鬃狮蜥集群的单细胞映射到每个小鼠亚集群上的比例(图中未显示没有匹配蜥蜴细胞的小鼠亚集群)。
上述方法也被用于将龟类大脑皮层谷氨酸能细胞的转录组投射到鬃狮蜥的数据上(扩展数据图7a)。龟类的数据来自参考文献11。该比较基于在两个物种中检测到的9820个一对一直系同源基因。在这项分析中,每个数据集的前2000个可变基因被用于典型相关分析(CCA)。前25个典型成分被用于计算3406个转移锚点。
¶ 解剖结构
¶ 具有潜在脑状态调节作用的鬃狮蜥脑区识别
在过去几十年中,人们在许多哺乳动物物种中发现了已知在控制大脑状态方面发挥作用的区域。这些区域可以通过其位置(例如,在下丘脑、中脑或脑干内)、轴突投射以及其神经元所包含和释放的神经活性物质(以及由此产生的潜在标记基因)来识别。据我们所知,目前尚无关于鬃狮蜥(Pogona)大脑的此类描述。
但其他蜥蜴物种已对同源区域进行了解剖学研究(参考文献43、44、46-56)。这些参考文献被用于确定相关脑区,包括下丘脑中的POA、SUM57和TMN,中脑中的VTA、SN和PAG,以及脑干中的LDT、LoC、SC和Ra。通过免疫组织化学(IHC)和/或荧光原位杂交(FISH),使用适当的神经元标记物,并结合脑切片的尼氏染色,确定了鬃狮蜥中这些区域的位置和特性。酪氨酸羟化酶(TH,儿茶酚胺能神经元的标记物)被用于识别POA、VTA、SN、PAG和LoC(扩展数据图6)。胆碱乙酰转移酶(ChAT)被用于识别LDT(扩展数据图6a)。组胺(His)被用于识别TMN(扩展数据图6a)。血清素(5HT)被用于识别中缝核(扩展数据图6a)。SC的识别基于先前对LDT和LoC的识别,以及通过原位杂交(ISH)检测到的SLC17A6(囊泡谷氨酸转运体2,vGluT2,谷氨酸能神经元标记物)的表达(扩展数据图6a)。通过ISH检测SLC17A6的表达也被用于识别SUM(扩展数据图6a)(另见参考文献57)。
¶ 缩写词
LoC:蓝斑核;LDT:外侧背盖核;PAG:中脑导水管周围灰质;POA:视前区;Ra:中缝核;SC:蓝斑下核;SN:黑质;SUM:乳头体上核;TMN:结节乳头核;VTA:腹侧被盖区。
¶ 鬃狮蜥全脑图像
鬃狮蜥的脑部重建(图3i)基于通过显微CT扫描仪获取的图像以及Imaris软件(牛津仪器公司)的表面功能。相关核团的边界通过连续的系列组织切片确定。使用Voloom软件对系列图像进行对齐并组合成三维体积,然后导入Imaris中并与三维数据对齐。通过逆行追踪确定的部分区域的边界根据GFP和尼氏染色模式来界定。
¶ 免疫组织化学和原位杂交
用异氟烷、氯胺酮(60毫克/千克)和咪达唑仑(2毫克/千克)对蜥蜴进行深度麻醉,直至其足退缩反射消失。随后通过腹腔注射戊巴比妥(10毫克/千克)。在角膜反射消失后,经心脏对蜥蜴进行灌流,先用冰冷的磷酸盐缓冲盐水(PBS;1.47×10⁻³M磷酸二氢钾、8.10×10⁻³M十二水合磷酸氢二钠、2.68×10⁻³M氯化钾、1.37×10⁻¹M氯化钠),接着用含4%多聚甲醛(PFA)的PBS。脑样本在4°C下用4% PFA/PBS后固定16小时,随后在4°C下浸入30%蔗糖中24小时。在-24°C下用切片机对脑区进行冠状切片(60微米)。切片在室温(RT)下用封闭液(PBST:含0.3% Triton X-100和10%山羊血清的PBS)透化30分钟,然后在4°C下与一抗(抗GFP,A10262,Invitrogen,鸡源,1:1000;海马钙蛋白,ab24560,abcam,兔源,1:1000;ChAT-胆碱乙酰转移酶,AB144P,Merk, goat源,1:100;mTH-酪氨酸羟化酶,22941,Immunostart,鼠源,1:100;rabTH,AB152,Merk,兔源,1:200;组胺,22939,Immunostart,兔源,1:100;血清素,MAB352,Merk,大鼠源,1:100)在封闭液中孵育过夜。用PBST洗涤3次后,样本在室温下与结合适当二抗(1:500,均购自Invitrogen)的封闭液孵育4小时。随后用PBST洗涤3次。部分切片在室温下用NeuroTrace 435/455蓝色荧光尼氏染色剂(N21479,Invitrogen,1:200)在PBS中复染2小时。用PBS冲洗后,将样本用Dako荧光封片液(S3023,Dako)或Roti-Mount FluorCare DAPI(HP20.1,Carl Roth)封片。使用共聚焦系统或荧光显微镜在10倍、20倍或40倍放大倍数下获取图像。显色原位杂交和双色比色原位杂交按照参考文献11中先前描述的方案进行。
¶ 通过RNAscope进行的荧光原位杂交
蜥蜴按照上述方法深度麻醉。角膜反射消失后,通过断头处死动物。立即取出大脑,在干冰/乙醇浴中包埋于OCT中,并在–80°C下保存。使用赛默飞世尔科技的CryoStar NX70冷冻切片机将新鲜冷冻的大脑切成25µm的切片,放置在SuperFrost包被(赛默飞世尔科技)的载玻片上。一些载玻片在风干后于–80°C下保存。按照制造商的说明进行RNAScope杂交。我们对新鲜冷冻切片使用了RNAscope多重荧光检测试剂盒(Advanced Cell Diagnostics)。靶基因和探针目录号为Pv-CHAT-C2(522631-C2)和PvSLC17A6-C1(529431-C1)。使用荧光尼氏染色进行复染。载玻片用ProLong Gold Diamond抗荧光淬灭封片剂(P36970,赛默飞世尔科技)封片。使用数字切片扫描仪(Pannoramic MIDI II,3DHISTECH)在20倍放大倍数下获取图像。
¶ 神经束追踪
蜥蜴的麻醉方式与在体记录时所述相同。Lorenz Pammer对爬行动物大脑适用的AAV血清型以及合适的孵化条件进行了大量初步研究²²。示踪剂(rAAV2-retro-CAG-GFP,37825-AAVrg;rAAV2-retro-hSyn-EGFP,50465-AAVrg;AAV9-CB7.Cl.mCherry.WPRE.RBG,105544-AAV9;均购自Addgene,https://www.addgene.org)被注射到一个或两个前脑位置(例如,背内侧皮质、背侧室嵴、前背侧室嵴等)。4至6周后,按照上述方法对动物进行深度麻醉;在角膜反射消失后,通过断头法处死动物。取出大脑,进行组织学处理、切片和成像。所呈现的数据来自30个注射大脑中的18个。其余12个大脑被排除,要么是因为病毒注射失败,要么是因为注射的特异性不够。在鬃狮蜥和巴西彩龟的大脑中靶向特定区域存在难度,因为大脑松散地位于颅腔内,其相对于颅骨和可靠标志的位置因此存在变异性:大脑漂浮在脑脊液中,通过脑神经连接。因此,不存在基于颅骨标志的可靠立体定位坐标。侧脑室较大。前脑的外观也缺乏可靠的标志(例如血管或脑沟)。最后,这些动物并非标准化物种,经过多代繁殖以减少变异性。
需要注意的是,由于rAAV2-retro对所有神经元类型的感染能力并不相同23,逆行标记阴性的结果需要用其他方法进行确认。相反,使用我们所用的示踪剂估算出的连接性可能被低估了。
¶ 统计学与可重复性
除非另有说明,数据均以平均值±标准误表示。对于两组比较,我们根据情况进行了双尾非配对t检验、双尾配对t检验、Mann-Whitney秩和检验或Wilcoxon符号秩检验(均为双侧检验)。对于多重比较,我们进行了Bonferroni检验。所有统计检验的显著性水平均设定为0.05。箱线图(图4d):箱体边缘分别代表第25和第75百分位数;红色线代表中位数;须线代表离群值之前的边界;离群值(+)指超出箱体边缘1.5倍四分位距的值。实验次数和重复次数如下表所示。
| 图注编号 | 实验重复说明 |
|---|---|
| 图1b-e | 该实验独立重复7次,结果一致 |
| 图2a-c | 实验独立重复4次,结果一致 |
| 图2e | 实验独立重复次数:amDVR组13次,pIDVR组9次,结果一致 |
| 图3 | a-b、d-h组实验独立重复4次;c组实验独立重复10次,结果一致 |
| 图4a-c | 实验独立重复3次,结果一致 |
| 扩展数据图1a-d | 实验独立重复7次,结果一致 |
| 扩展数据图1h | 实验独立重复3次,结果一致 |
| 扩展数据图2b | 实验独立重复15次,结果一致 |
| 扩展数据图2g&i | 实验独立重复12次,结果一致 |
| 扩展数据图2h&j | 实验独立重复2次,结果一致 |
| 扩展数据图3f | 实验独立重复3次,结果一致 |
| 扩展数据图4a | 实验独立重复3次,结果一致 |
| 扩展数据图4b | 实验独立重复次数:amDVR组13次,pIDVR组9次,结果一致 |
| 扩展数据图6a-c | 除c5-7外,实验至少独立重复3次,结果一致;c5-7在5次实验中完成1次(见图3图例) |
| 扩展数据图8a、e-f | 实验独立重复4次,结果一致 |
| 扩展数据图8b-d | 实验独立重复4次,结果一致 |
| 扩展数据图7b | 实验独立重复3次,结果一致 |
| 扩展数据图7c | 实验独立重复5次,结果一致 |
| 扩展数据图7d | 实验独立重复4次,结果一致 |
| 扩展数据图(未标注具体编号) | 实验独立重复3次,结果一致 |
| 扩展数据图7e-g、扩展数据图8a,e-f | 实验独立重复4次,结果一致 |
| 扩展数据图8b-d | 实验独立重复4次,结果一致 |
| 扩展数据图9a-d | a组实验重复2次、b组重复2次、c组重复3次,结果一致;所有实验均验证了屏状核损毁(d)的效果 |
| 扩展数据图10a-b | a组实验独立重复2次,b组独立重复3-4次,结果一致 |
测序数据已存入NCBI序列读取档案库:生物项目PRJNA591493(蜥蜴);PRJNA408230(海龟);这些档案库和分析代码的链接可在以下网址找到:https://brain.mpg.de/research/laurent-department/software-techniques.html。可通过联系GL(gilles.laurent@brain.mpg.de)获取数据。
¶ 扩展数据图例
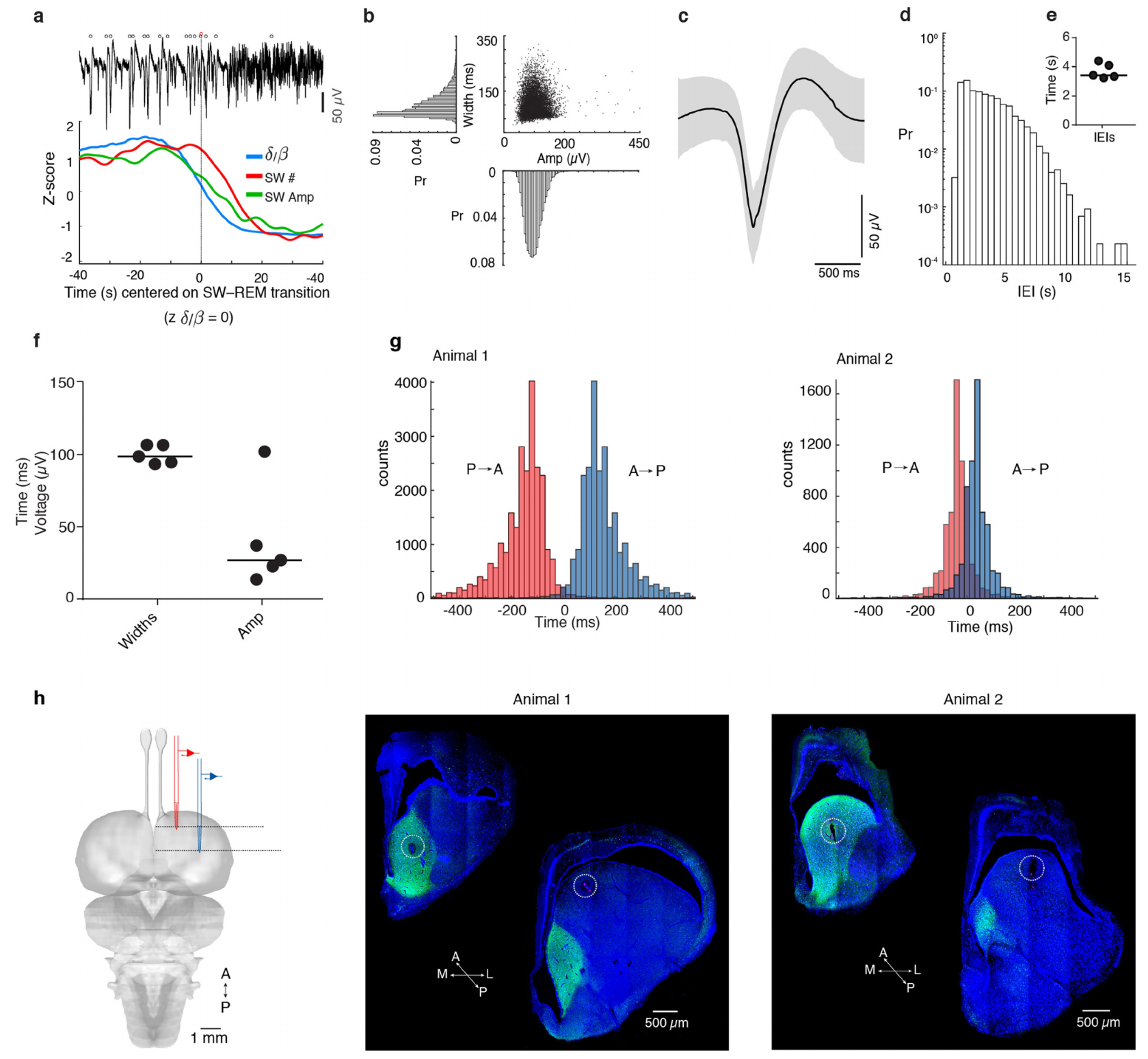
扩展数据图1 | SWR统计数据和在体传播的进一步描述。a,当动物在慢波睡眠(SW)和快速眼动睡眠(REM)之间转换时,SW的振幅和频率会发生变化。顶部:示例性局部场电位(LFP)轨迹(<150 Hz),显示在SW-REM转换点附近,尖波的振幅和频率有所降低。空心圆表示检测到的尖波(参见方法和参考文献3)。a-d中的数据来自同一只动物的单夜记录,对应于图1中的记录(前部记录位点,红色)。统计基于n = 11,123个尖波。b,图1和扩展数据图1a中动物的尖波宽度(在半峰振幅处测量)和峰值振幅的分布。c,平均尖波±1标准差(灰色),n = 11,123个尖波。d,慢波睡眠(SWS)期间记录的尖波的事件间隔(IEI)。y轴为对数刻度。e、f,来自2只动物5个夜晚记录的数据汇总。每个圆圈代表一个夜晚的平均值;黑线表示中位数。e,慢波睡眠期间的平均事件间隔(IEI)。f,平均尖波宽度和振幅(n = 8,055–13,494个尖波/晚)。g,前部(或后部)背侧脑室下区(DVR)中尖波的延迟分布,由同时记录的后部(或前部)DVR触发。数据来自3个夜晚(动物1,n = 24,501个SW)和2个夜晚(动物2,n = 13,070个SW)。h,前部背侧脑室下区(aDVR)中同步记录位点的位置(圆圈)。左图:记录配置示意图。中图和右图:共聚焦图像突出显示记录位点,通过电解损伤和应用于硅探针背面的DiI来识别。使用抗 hippocalcin 的抗体进行事后染色以确定屏状核边界(见图3)。
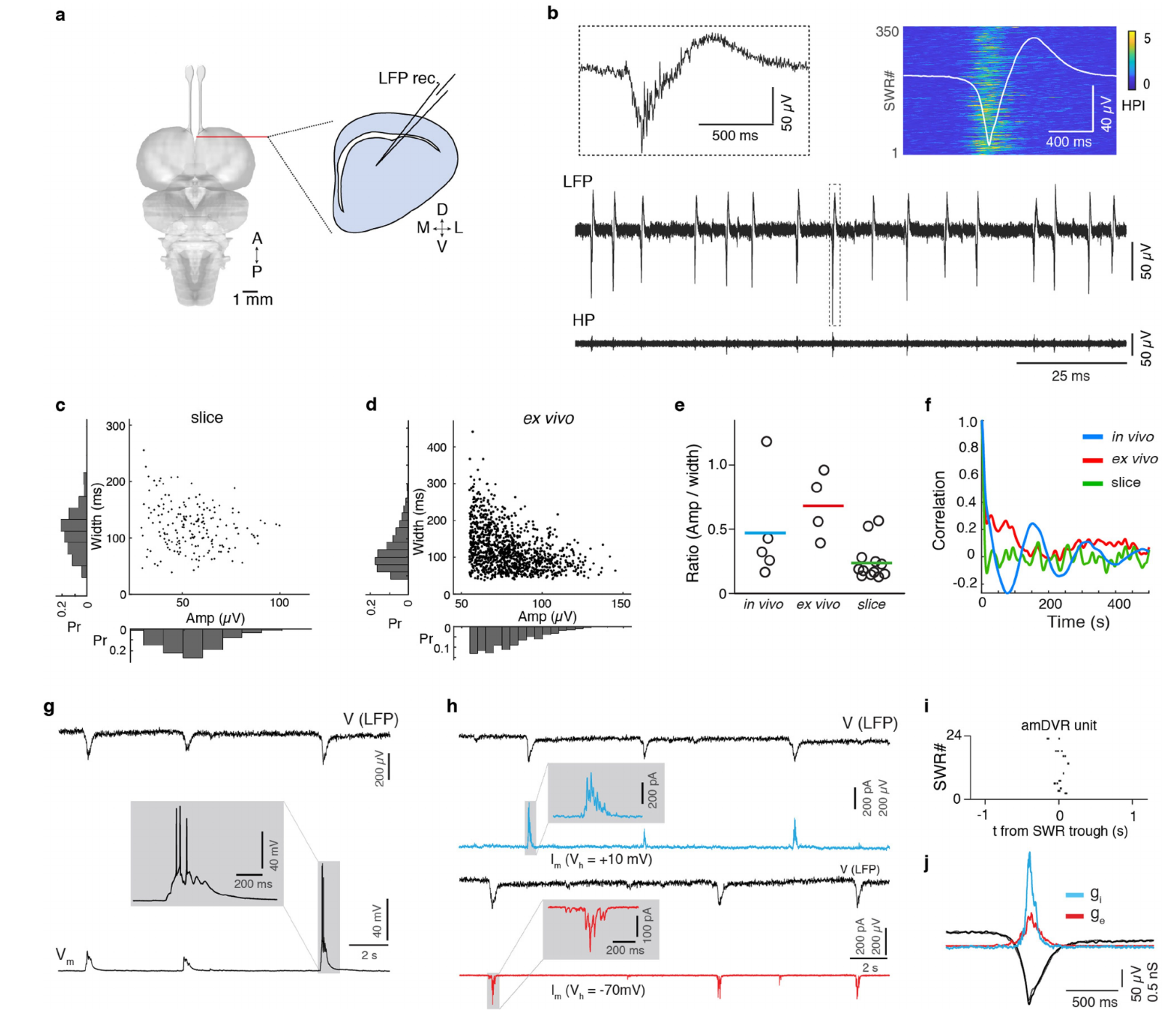
扩展数据图2 | 不同制备和记录条件下SWR统计数据的比较。a,用于场电位记录的切片制备(见方法)。b,amDVR中的自发性锐波(LFP,<150 Hz)和相应的涟漪(HP,70-150 Hz)。插图:左上,方框中放大的SWR;右上:350个涟漪;以锐波谷为对齐点的高通信号强度(HPI,>70 Hz)(叠加为平均值)。c,代表性DVR切片中SWR事件的振幅(x)和宽度(y,半最大值处的全宽)分布。d,代表性离体制备中SWR振幅和宽度的分布(如c所示)。e,振幅(μV)与宽度(ms)的比值。n = 3只动物的5个睡眠时期(在体)、4个离体脑和12个切片。彩色线:平均值。f,锐波时间的自相关函数,显示睡眠动物(在体,蓝色)中锐波产生的特征性节律调制(由于2-3分钟周期的慢波睡眠和快速眼动睡眠交替引起)在离体脑(红色)和切片(绿色)制备中均不存在。n = 3只动物的5个时期(在体)、4个离体脑和12个切片。g,DVR神经元在电流钳模式下的全细胞膜片钳(WCPC)记录(Vm)以及用玻璃微电极在邻近区域进行的LFP记录(LFP)。注意神经元的同时去极化和SWR,以及适度的神经元去极化导致偶尔放电(此处为3个动作电位)。对12个神经元重复了该实验。h,amDVR神经元在电压钳模式下的WCPC记录,分别保持在去极化(青色)和超极化(红色)的钳制电位(Vh)。注意每个SWR(LFP)时的兴奋性(红色)和抑制性(青色)电流爆发,以及期间几乎没有突触输入。i,被膜片钳记录的amDVR神经元的尖峰时间与锐波的关系。注意锁定在锐波谷(t=0),其他时候没有放电。n = 2个amDVR神经元。j,平均兴奋性(ge)和抑制性(gi)电导(分别为n = 20和21个事件)。黑色/灰色:记录到的i和e电导的平均SW。轨迹以锐波谷为对齐点。
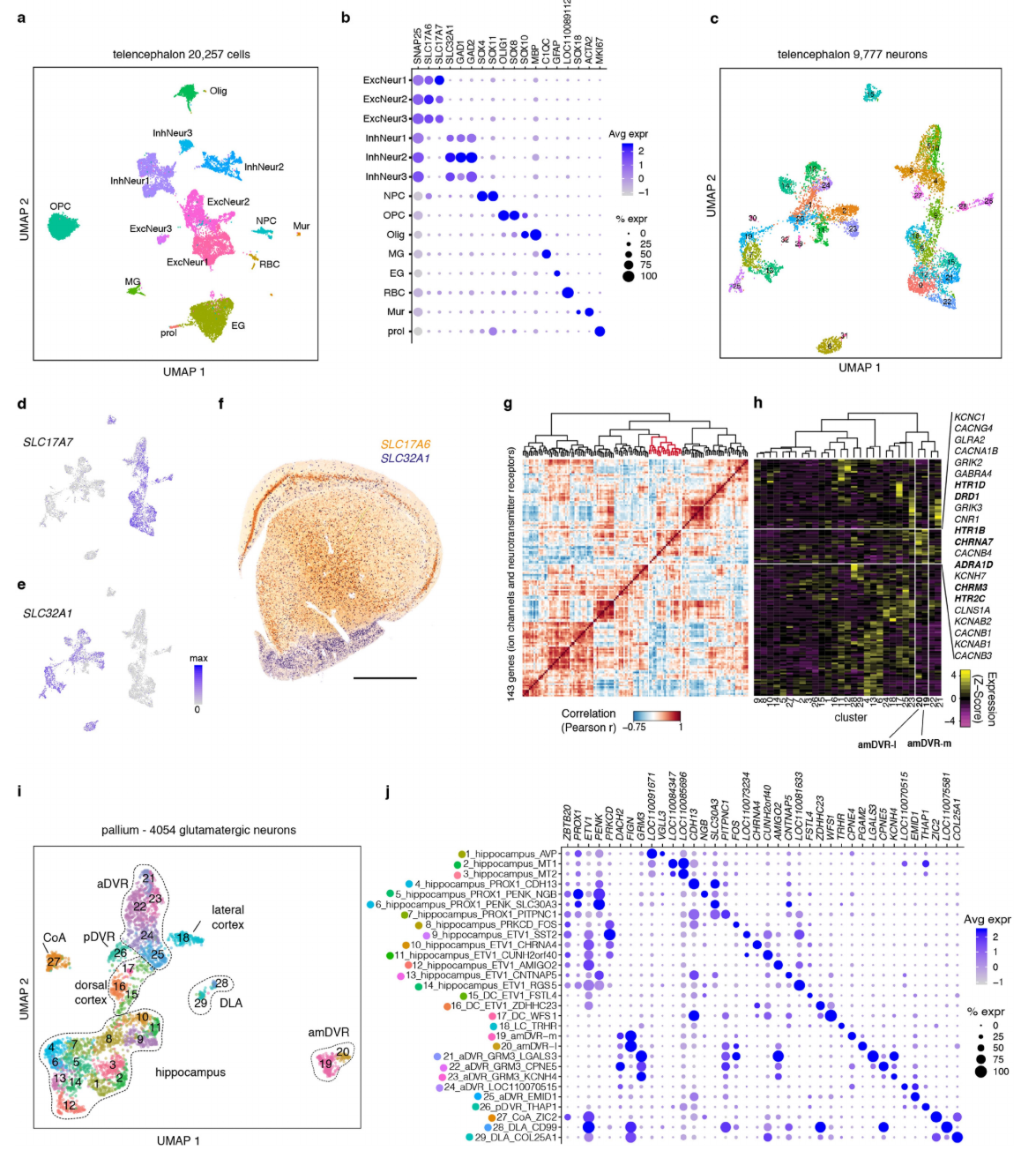
扩展数据图3 | 额外的单细胞转录组学特征分析。a,20257个鬃狮蜥端脑细胞的UMAP45展示,按集群进行颜色编码。EG:室管膜神经胶质细胞;ExcNeur:兴奋性神经元;InhNeur:抑制性神经元;MG:小胶质细胞;Mur:壁细胞;NPC:神经祖细胞;Olig:少突胶质细胞;OPC:少突胶质前体细胞;RBC:红细胞。b,点阵图显示典型细胞标志物(沿每行)在端脑细胞集群(列)中的表达情况。点的大小:集群中检测到该基因的细胞百分比;颜色:表达水平。c,9777个蜥蜴端脑神经元的UMAP展示,按集群进行颜色编码。d-e,端脑数据集中谷氨酸能神经元(SLC17A7)和GABA能神经元(SLC32A1)的UMAP展示。f,鬃狮蜥前脑前部冠状切片的双色比色原位杂交结果。比例尺:1000微米。SLC32A1(蓝色)标记亚大脑皮层中的GABA能神经元以及从亚大脑皮层迁移到大脑皮层的散在GABA能神经元。SLC17A6(橙色)标记大脑皮层区域的谷氨酸能神经元。g,在该鬃狮蜥大脑皮层谷氨酸能数据集(见扩展数据图5)中检测到的143个离子通道和神经递质受体基因表达之间的成对皮尔逊相关系数有序矩阵。基于相关系数和Ward.D2连锁法的树状图(顶部);红色表示在amDVR中表达富集的基因模块。h,在29个鬃狮蜥谷氨酸能集群中,g(及扩展数据图5)中143个基因的平均表达水平。右侧列出在amDVR中表达富集的基因。i,4054个蜥蜴大脑皮层谷氨酸能神经元的UMAP展示,按集群进行颜色编码(与图3相同)。j,点阵图显示特定集群标志物(沿行)在29个大脑皮层谷氨酸能集群(沿列)中的表达情况。点的大小:集群中检测到该基因的细胞百分比;颜色:表达水平。
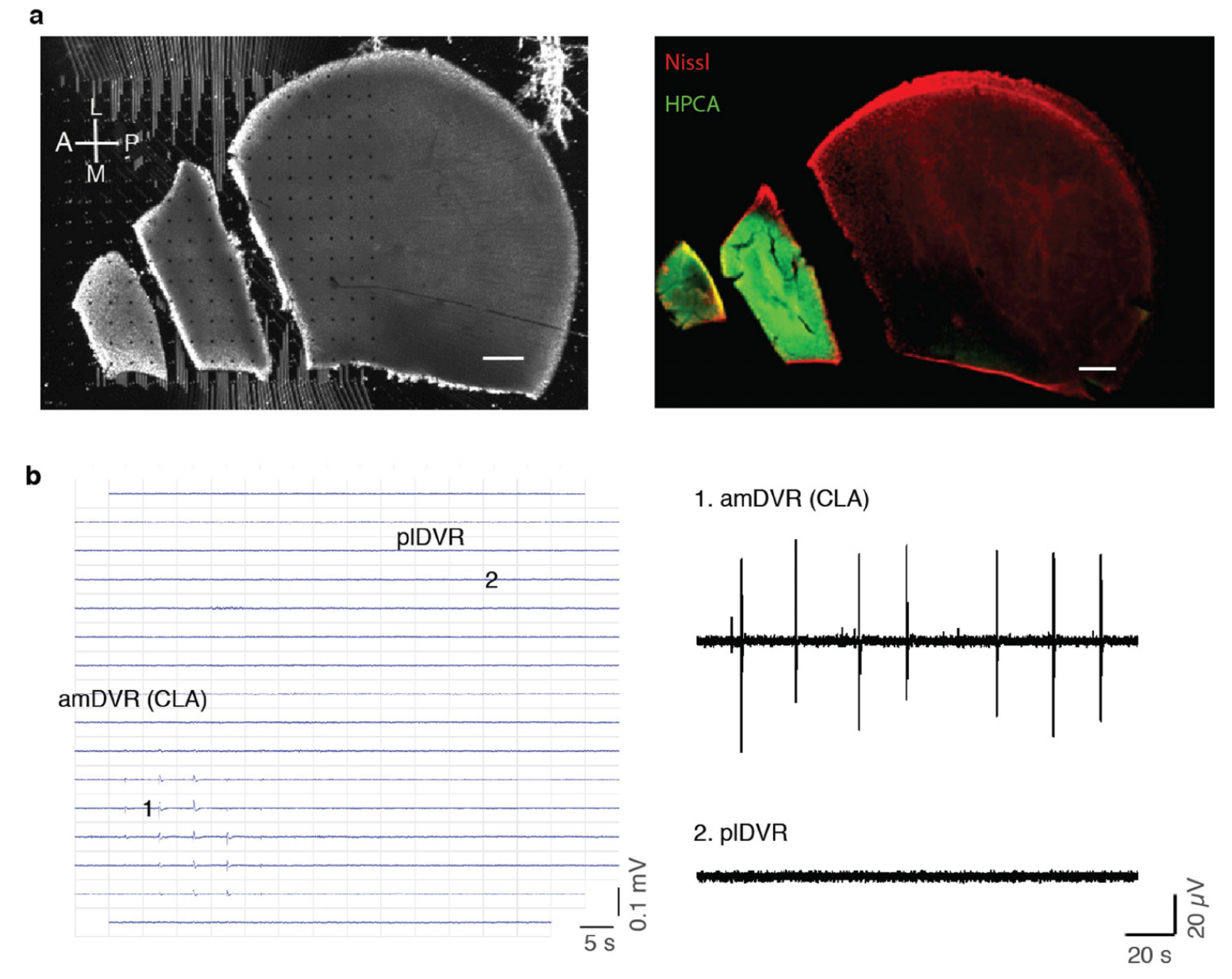
扩展数据图4 | DVR的微型切片与SWR生成的定位。a,左图,平面252通道MEA上微型DVR切片的记录配置。圆点代表电极。右图,左图中切片的事后免疫染色。红色:尼氏染色,绿色:海马钙蛋白(HPCA)。b,左图,从a中的微型切片记录到的SWR波形的空间分布。右图,从amDVR或屏状核(1)和后外侧DVR(2)记录的示例性LFP轨迹(参见左图微电极阵列上的记录位置)。总之,SWRs在amDVR中自发发生,而一旦plDVR与amDVR(屏状核)断开连接,plDVR中就不存在SWRs。
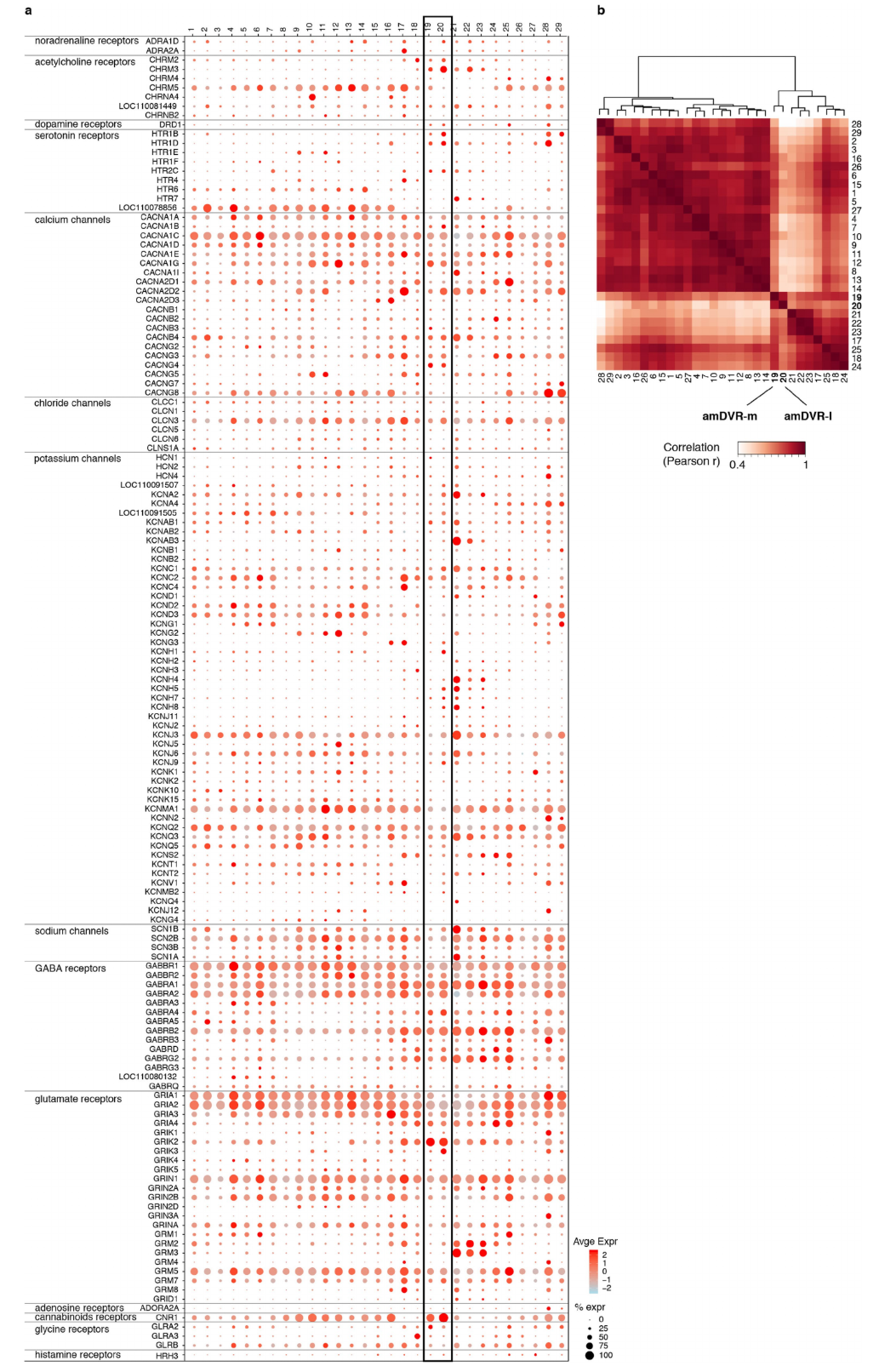
扩展数据图5 | 鬃狮蜥端脑谷氨酸能细胞簇中的离子通道和神经递质受体mRNA。a,点图显示鬃狮蜥谷氨酸能细胞簇(第1-29列)中离子通道和神经递质受体基因(行)的表达。该图仅显示在至少一个细胞簇中20%以上的细胞中检测到的基因。点的大小表示在一个细胞簇中检测到该基因的细胞百分比;点的颜色表示表达水平。细胞簇19和20(方框内)对应于amDVR或屏状核。它们的区别在于某些乙酰胆碱受体和5-羟色胺受体亚型的表达(另见图3h)。b,根据a中离子通道和神经递质受体基因的表达计算得出的细胞簇转录组有序成对皮尔逊相关矩阵。该基因集足以将amDVR细胞簇(19和20)与所有其他细胞簇区分开来。系统发育树基于皮尔逊相关性和Ward.D2连锁法构建。
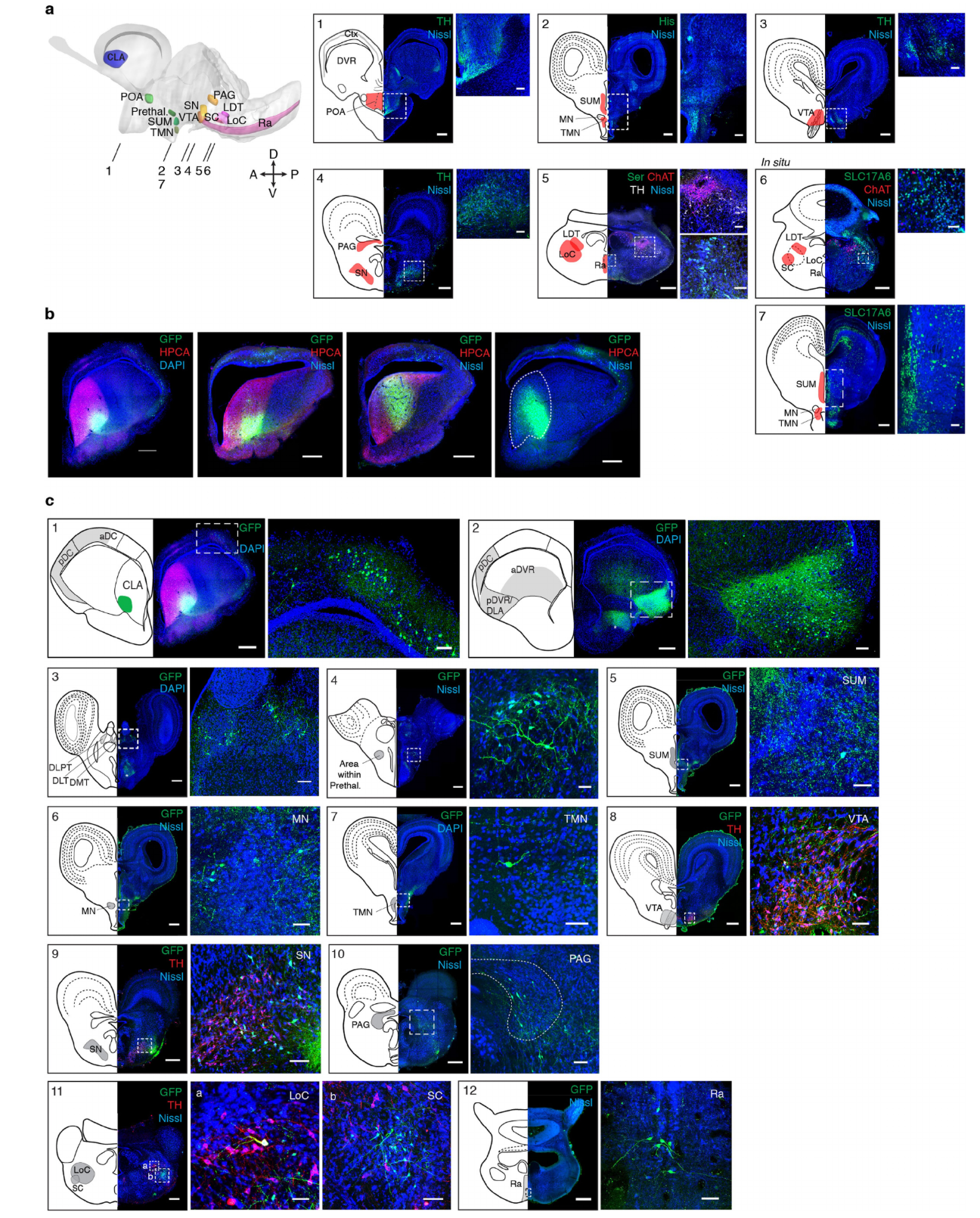
扩展数据图6 | 脑状态潜在调控区域的识别以及在屏状核注射rAAV2-retro后GFP标记神经元的分布。a,左侧为松果蜥脑矢状面示意图,显示通过免疫组织化学、原位杂交和逆行示踪定义的区域。1-7表示右侧所示横切面的水平。1-7组图:通过免疫组织化学(IHC)、原位杂交(ISH)和尼氏染色识别的相关区域(红色)的显微照片及相应示意图。比例尺:500 µm。每组图右侧:显微照片中框出区域的放大视图。比例尺:100 µm。b,AAVrg-hSyn-eGFP注射位点的识别。比例尺:500 µm。(最右侧图:未显示红色通道。)c,横切面中屏状核连接逆行标记的示例图。1-2:通过在屏状核注射rAAV2-retro显示的屏状核输入。组图1:外侧屏状核的注射位点;屏状核通过抗海马钙蛋白免疫染色(粉红色)指示;注意前背皮质(aDC)中的逆行标记细胞(框内,右侧为放大图)。组图2:与组图1为同一脑,更靠后的切片;框内标记区域为背外侧杏仁核(DLA)。3-12:显示投射至屏状核的、分布在背外侧丘脑前核(DLPT)、背外侧丘脑(DLT)、背内侧丘脑(DMT)、丘脑前核、中缝核(SUM)、内侧核(MN)、结节乳头核(TMN)、腹侧被盖区(VTA)、黑质(SN)、中脑导水管周围灰质(PAG)、蓝斑下核(LoC)和上丘(SC)中的GFP标记神经元的代表性图像。儿茶酚胺能神经元标志物酪氨酸羟化酶(TH)用于指示腹侧被盖区(VTA)、黑质(SN)和蓝斑下核(LoC)的位置。比例尺:500 µm;放大区域校准:背外侧丘脑前核(DLPT)、背外侧丘脑(DLT)、背内侧丘脑(DMT)、丘脑前核、中缝核(SUM)、内侧核(MN)、结节乳头核(TMN)、腹侧被盖区(VTA)、蓝斑下核(LoC):50 µm;黑质(SN)、中脑导水管周围灰质(PAG)、上丘(SC):100 µm。
缩写:CLA:屏状核;aDC:前背皮质;pDC:后背皮质;DMT:背内侧丘脑;DLA:背外侧(基底外侧)杏仁核;DLT:背外侧丘脑;DLPT:背外侧后丘脑;DMC:背内侧皮质;aDVR:前背侧脑室脊;pDVR:后背侧脑室脊;LC:外侧皮质;LoC:蓝斑核;LDT:外侧背盖核;MC:内侧皮质;MN:乳头体核;PAG:导水管周围灰质;POA:视前区;SC:蓝斑下核;SN:黑质;SUM:乳头体上核;TMN:结节乳头体核;VTA:腹侧被盖区。
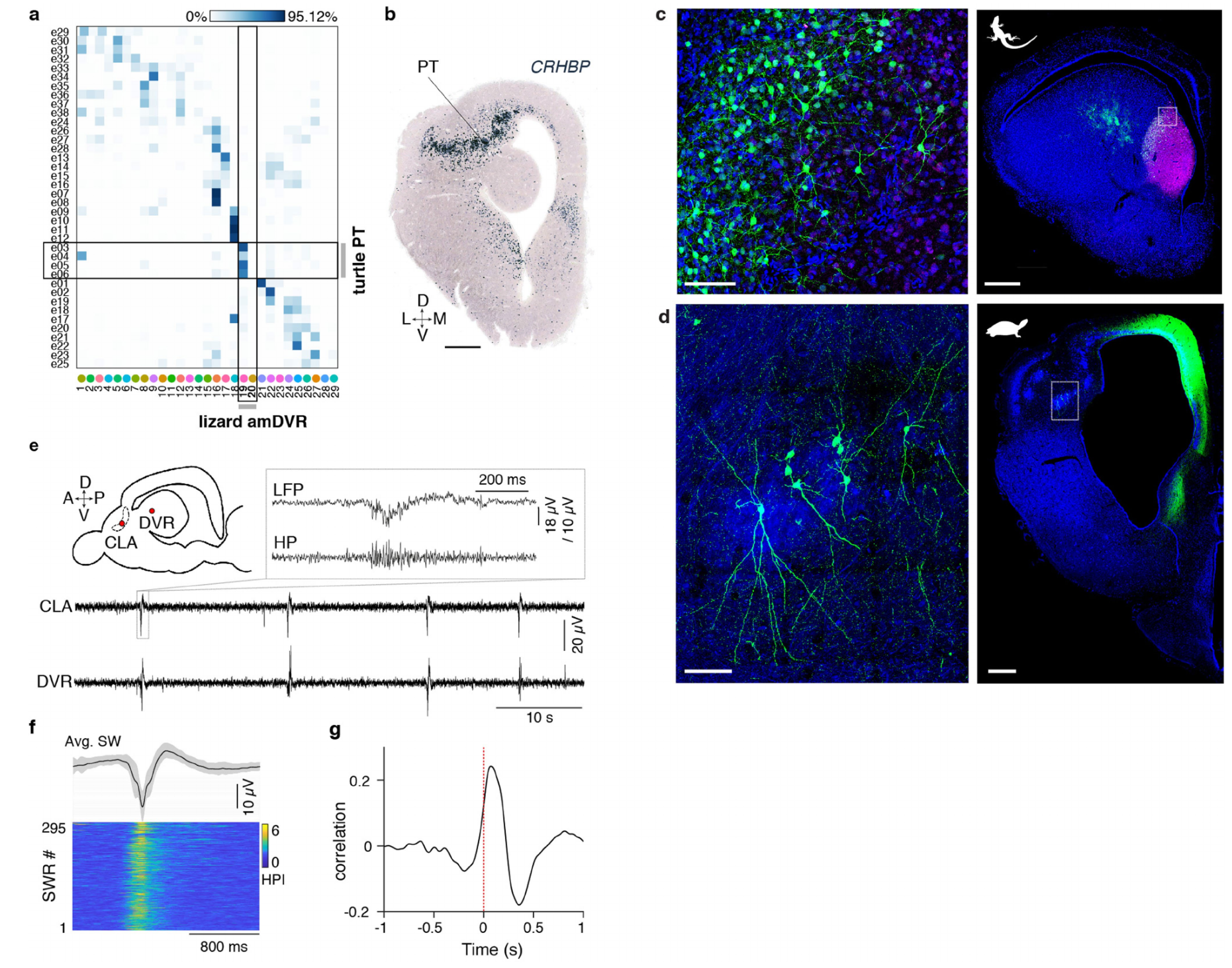
扩展数据图7 | 蜥蜴和龟的屏状核在位置和结构上存在差异,但两者都是尖波涟漪(SWRs)的自主来源。a,龟和蜥蜴细胞群之间的转录组相似性,以从龟大脑皮层数据集映射到鬃狮蜥细胞群的单细胞比例来衡量(方法部分)。注意,龟的细胞群e03-06(皮层增厚区,即PT)映射到蜥蜴的细胞群19(amDVR或屏状核)。龟的数据和细胞群来自参考文献11。b,前部横切片的原位杂交(ISH),显示PT标志物CRHBP的表达。比例尺:500μm。c,蜥蜴屏状核的结构。通过在aDVR中注射rAAV2-retro对屏状核神经元进行逆行标记(右侧)。左图:右侧图中框选区域(屏状核内)的放大图。注意多极神经元的无序分布。粉红色:抗海马钙蛋白免疫染色。校准:100μm(左);500μm(右)。d,龟屏状核的结构。通过在DMC中注射rAAV2-retro对屏状核神经元进行逆行标记(右图)。左图:右图中框选区域的放大图。注意PT层内双极神经元的排列(另见b中PT的分层)。比例尺:100μm(左);500μm(右)。e,在龟脑切片制备中同时记录到的屏状核和DVR中的自发性尖波。红点(示意图):记录位点。注意尖波(局部场电位,LFP)和高通(HP)波段的涟漪。f,底部:295个连续的自发性涟漪;高通信号强度(HPI,>70Hz)与尖波的波谷对齐。295个尖波的平均值,与波形波谷对齐;灰色:标准差(SD)。g,同时从屏状核和DVR记录的局部场电位(LFP)轨迹的代表性互相关图(参考:屏状核),显示DVR滞后于屏状核。
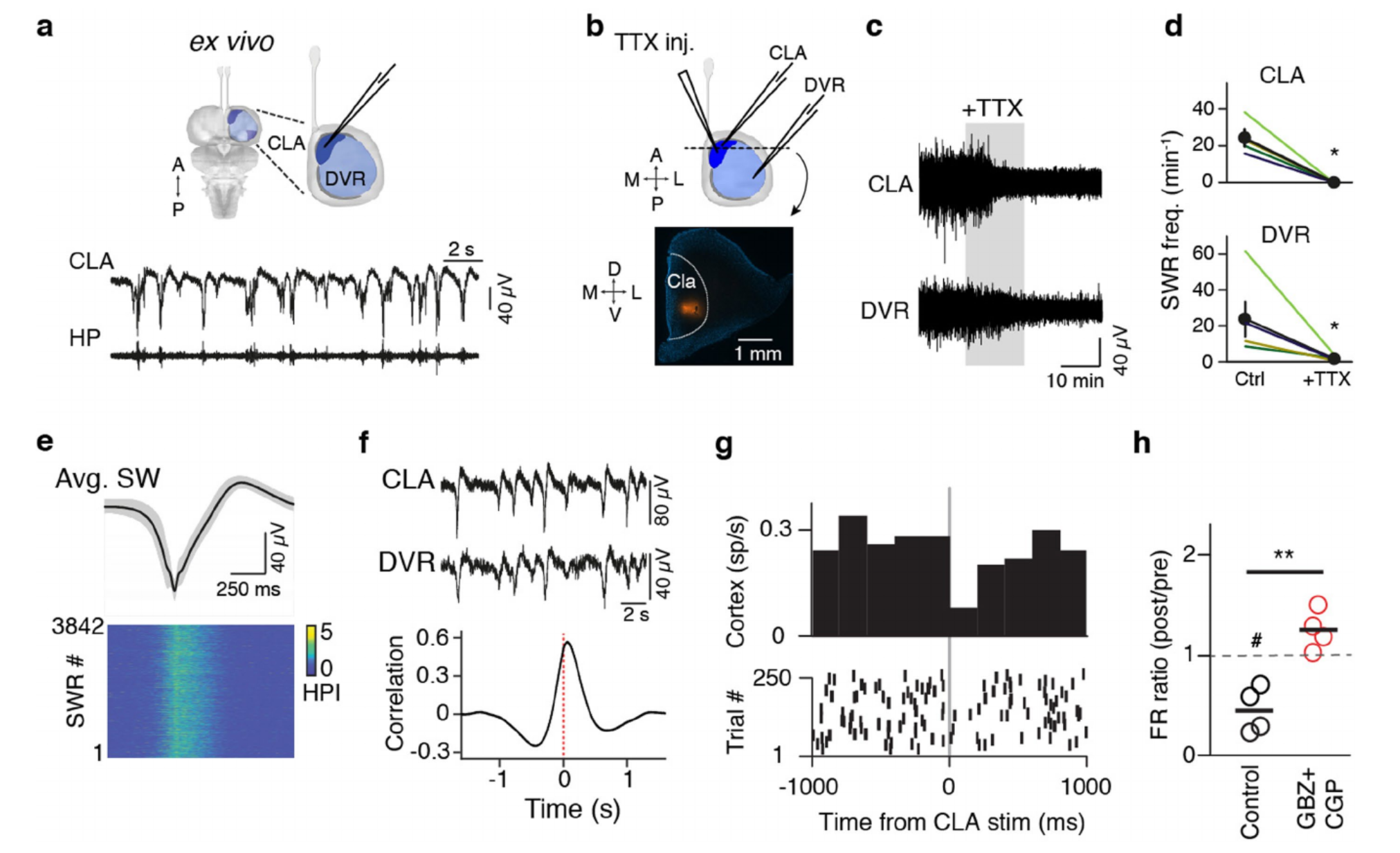
扩展数据图8 | 蜥蜴离体脑标本的锐波涟漪记录和刺激实验。a-f:移除皮质后的离体脑标本实验(a,左上)。a下,在屏状核(CLA,<150 Hz)记录到的自发性锐波涟漪。HP:70-150 Hz滤波的局部场电位,显示涟漪(下迹线)。b,在屏状核局部压力注射20μM TTX,事后用伊文思蓝评估注射情况(红色,横切面,下)。c,在屏状核注射TTX(阴影部分)可使屏状核的锐波活动沉默,也(间接)使背侧脑室嵴(DVR)的锐波活动沉默。d,对4个如c所示的实验进行分析。实心圆:平均值±标准误。屏状核:*p=0.029,T=26,双侧曼-惠特尼秩和检验。背侧脑室嵴:*p=0.029,T=26,双侧曼-惠特尼秩和检验。e,从离体前脑的屏状核记录到的3842个锐波的平均迹线(上)和标准差(阴影)(以波谷为对齐点)。下:高通信号强度(HPI,>70 Hz)以锐波波谷为对齐点,显示涟漪的对齐情况。f,上:在离体标本中同时记录同侧屏状核和背侧脑室嵴。下:同侧屏状核和背侧脑室嵴同时记录的互相关,显示屏状核比背侧脑室嵴提前约100ms。g,在完整的离体前脑中,对同侧屏状核激活时皮质多单位活动的刺激周围时间直方图。实验在正常人工脑脊液中于室温下进行,加入30µM 5-羟色胺以抑制屏状核的自发性锐波涟漪,加入50µM氨甲酰胆碱以提高皮质兴奋性。屏状核刺激:通过双极电极施加单个50µs电脉冲。用玻璃微电极记录皮质多单位活动。h,在屏状核刺激后200ms时间段与刺激前200ms时间段内测量的皮质 firing rate(FR)变化(如g所示)。对照组:如g所示。GBZ:加巴喷丁(5μM),CGP:CGP52432(GABAB受体拮抗剂,2μM),n=4个离体脑,来自3只动物,每只动物1个。对照实验显示,屏状核刺激对皮质有即时且可靠的抑制作用(#:与基线有显著差异,p=0.017,t3=4.8,双侧配对t检验)。在GABA受体阻滞剂中的刺激实验显示,此时屏状核刺激对皮质有轻微的兴奋作用(**:与对照组有显著差异,p=2.0×10-3,t6=-5.22,双侧学生t检验),表明屏状核投射既激活也抑制皮质神经元,可能通过直接的兴奋性投射和通过中间神经元的间接抑制性投射(见啮齿类动物实验参考文献39)。短水平线表示平均值。
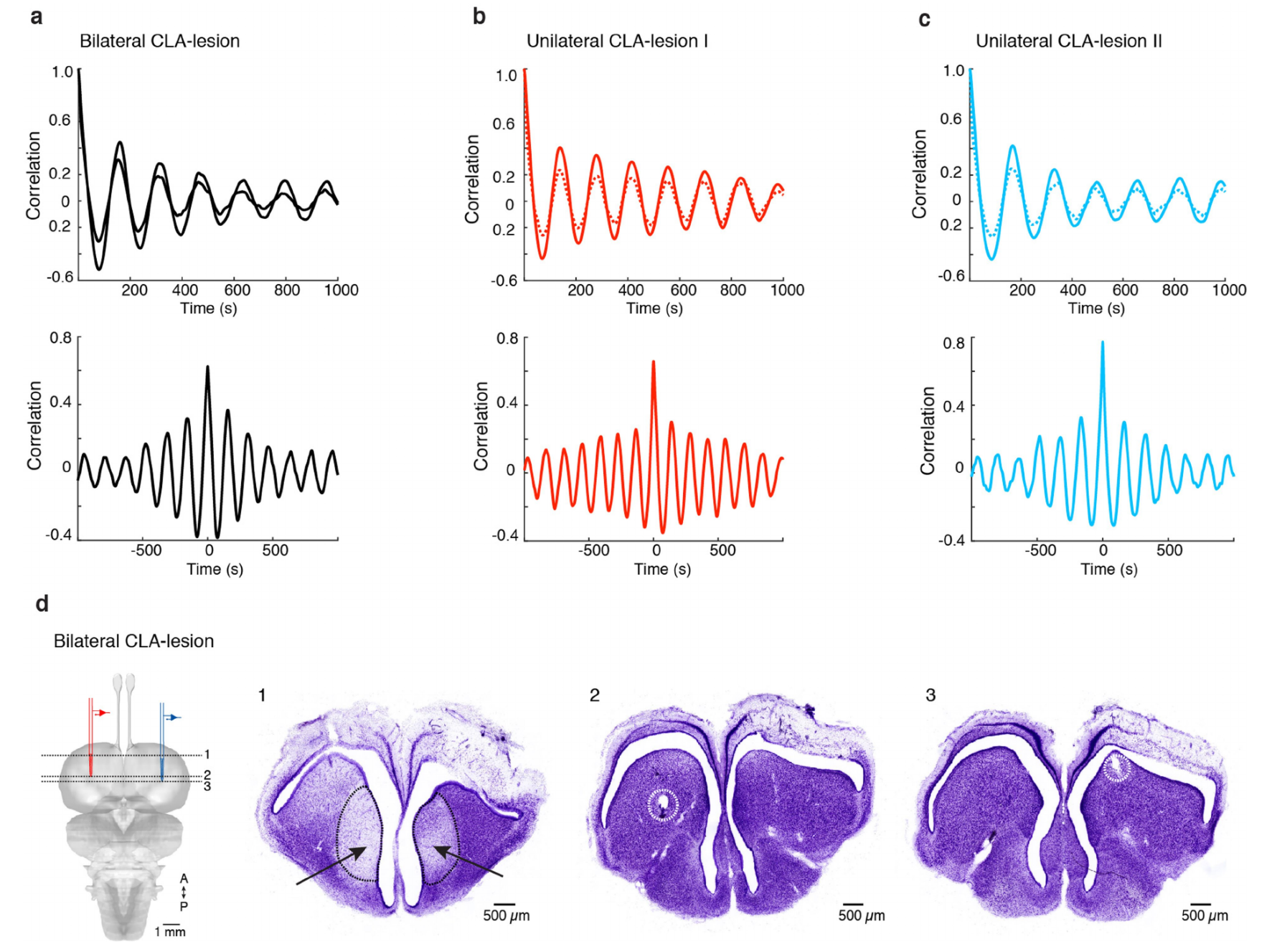
扩展数据图9 | 对睡眠中的鬃狮蜥进行体内鹅膏蕈氨酸损伤实验的进一步分析。a,在双侧屏状核损伤的动物睡眠期间,左、右背侧脑室嵴(L和R DVR)中β波段活动的自相关(上)和互相关(下)(见d中的损伤情况)。注意,屏状核损伤后睡眠节律(约3分钟周期)仍然存在,因此似乎不依赖于屏状核的完整性。b-c,与a相同,但为两只动物(I和II)的单侧鹅膏蕈氨酸损伤。未损伤(假手术)侧注射相同体积的PBS溶媒,但不含鹅膏蕈氨酸。上:虚线:假手术;实线:损伤。d,a中双侧屏状核(CLA)损伤动物(另见图4b)脑横断面的尼氏染色(1-3),处于左侧示意图所示水平。注意可见屏状核损伤(箭头,1)表现为细胞体缺失,以及左(2)和右(3)背侧脑室嵴(DVR)中的记录位点(虚线圆圈)。
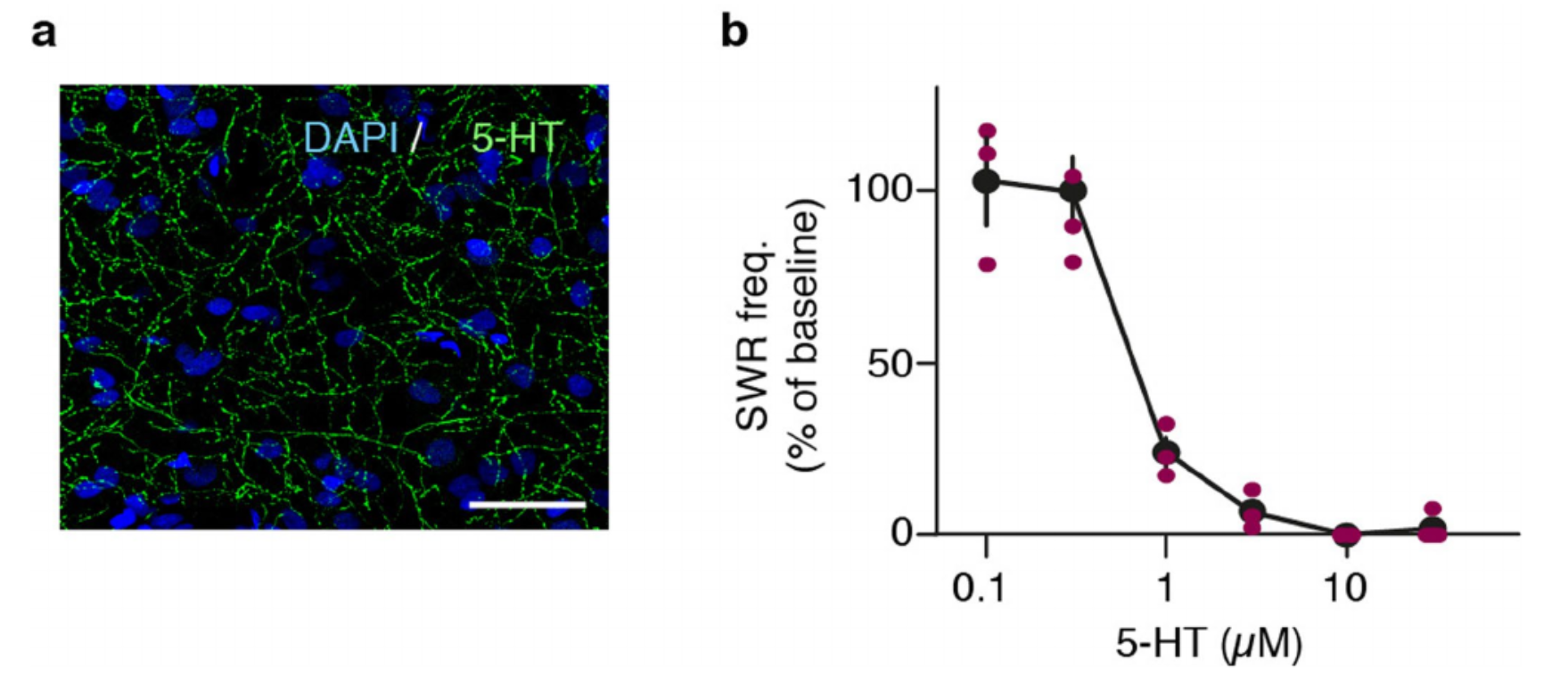
扩展数据图10 | 关于5-羟色胺投射至屏状核及其对锐波涟漪生成影响的补充数据。a,屏状核的横切面,用DAPI(蓝色,细胞核)和5-羟色胺(轴突纤维)抗体进行双重标记。注意 serotonergic 纤维的密集网状结构。比例尺:50微米。b,屏状核迷你切片中自发锐波涟漪频率与灌流5-羟色胺浓度的函数关系。红色圆圈代表单个实验(切片)。黑色代表平均值和标准误。