¶ 《生理学杂志》
¶ 鸟类视网膜中的跳跃式轴突传导
¶ 原文下载:tjp-603-6533_origin.pdf
克里斯托夫·T·布洛克,雄性T. Ahler, 克里斯蒂安·普勒,马克斯·马纳金,Dipti R. Pradhan, 马丁·格雷斯纳
首次发表:2025年8月29日 https://doi.org/10.1113/JP288664 数字对象标识符(DOI) 查看指标
同行评审历史记录可在本文的支持信息部分查看:(https://doi.org/10.1113/JP288664#support-information-section)。
¶ 摘要
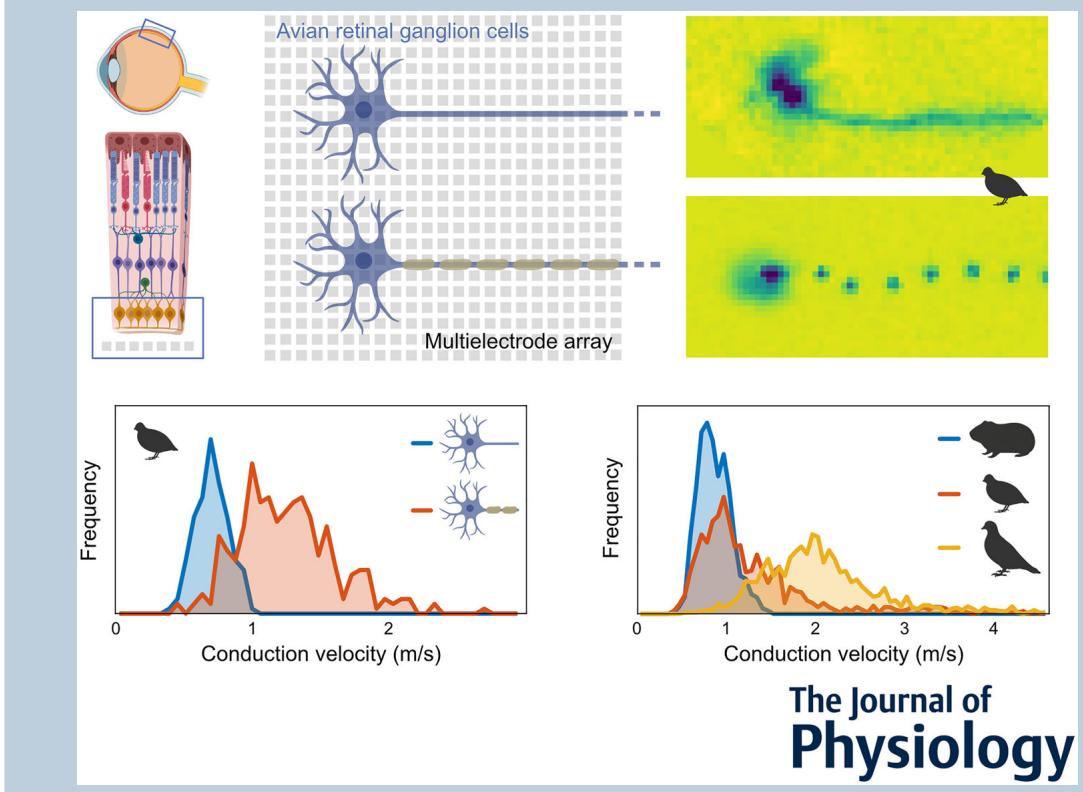
与脊椎动物神经系统的大多数部分不同,视网膜中的神经节细胞轴突通常缺乏髓鞘。在大多数物种中,神经节细胞轴突只有在离开视网膜形成视神经后才会形成髓鞘。然而,鸟类视网膜是一个显著的例外,其神经节细胞轴突在视网膜神经纤维层中部分有髓鞘。据推测,视网膜髓鞘在光学上的不利特性在进化上被其在 spike 传导速度方面的优势所抵消。通过高分辨率多电极阵列记录,我们分析了多种鸟类与哺乳动物视网膜中的 spike 传导。事实上,哺乳动物的传导速度低于鸟类。有髓鞘轴突的传导速度通常高于无髓鞘轴突。值得注意的是,一些有髓鞘轴突的传导速度低于无髓鞘轴突。解剖学分析显示,神经纤维层中的髓鞘形成伴随着郎飞氏结的形成。结间长度与轴突直径呈正相关。在生理记录中,同时活跃的结的空间范围与传导速度呈正相关。相反,结间长度和结的激活动力学是传导速度的弱预测因子。总体而言,这项研究揭示了鸟类视网膜的独特特征,并为影响神经系统传导速度的髓鞘化的功能需求和进化压力提供了见解。
¶ 要点
- 研究人员利用高分辨率多电极阵列,对多种鸟类的视网膜内跳跃式轴突 spike 传导进行了研究。
- 最高的传导速度仅在跳跃式传导的轴突中被观察到,而最低的传导速度则存在于非跳跃式传导的轴突中。然而,存在传导缓慢的有髓轴突,其传导速度与无髓轴突存在显著的重叠,这一点颇为令人惊讶。
- 动作电位的空间范围与传导速度呈强正相关。
- 结间长度与轴突直径呈正相关,且单个轴突内结间长度的变异性小于轴突间的变异性。
- 不同物种的视网膜内轴突传导速度似乎与其生态位相匹配。在鸟类中观察到的最大视网膜内 spike 传导速度比啮齿动物快四倍。
¶ 引言
髓鞘形成是脊椎动物轴突的一个普遍特征,它能实现快速的跳跃式 spike 传导。轴突被髓鞘包裹的部分会周期性地被无髓鞘的结间段中断,这些结间段富含暴露于细胞外间隙的电压门控离子通道。髓鞘形成会降低膜电容并增加膜电阻,结果是增加了膜的长度常数,减少了膜的时间常数。这使得一个被激活的结间段能够在更长的距离上使后续的结间段去极化,避免了在整个轴突上进行耗时耗能的主动 spike 生成,从而极大地提高了传导速度。
髓鞘是一种富含蛋白质和脂质的光学致密物质,在水介质中表现出强烈的光散射(Blanke等人,2023;DePaoli等人,2020)。它可能会影响视网膜神经纤维层的光学特性,光线必须穿过该层才能到达光感受器。在人类中,视网膜轴突罕见的病理性髓鞘形成(有髓视网膜神经纤维,MRNF)会导致局部视力受损(Grzybowski和Winiarczyk,2015;Lee等人,2015)。在健康的哺乳动物中,视网膜神经节细胞(RGCs)在穿过筛板之前一直保持无髓鞘状态,穿过筛板后它们形成视神经并开始髓鞘化(Fujita等人,2000)。因此,哺乳动物的视网膜通常缺乏少突胶质细胞,这种神经胶质细胞负责在中枢神经系统的其他部分形成轴突周围的髓鞘(Gao等人,2006)。在哺乳动物中,兔子是一个显著的例外,其视网膜内存在少突胶质细胞形成的髓鞘,尽管这种髓鞘仅限于视觉条纹上方的区域(Hughes,1971;Schnitzer,1985;Vaney,1980)。在鱼类中也观察到视网膜内髓鞘形成,特别是在推测的离心轴突中(Witkovsky,1971;Wolburg,1980)。
相比之下,有髓神经节细胞轴突常见于鸟类视网膜中(Imagawa等人,1999;Inoue等人,1980;Nakazawa等人,1993;Seo等人,2001;Won等人,2000)。有髓轴突的比例在视网膜不同区域存在差异(Imagawa等人,1999)。所有离心轴突在视网膜内均被描述为有髓鞘的(Wilson和Lindstrom,2011)。鸟类视网膜中髓鞘的一个显著特征是其疏松的超微结构,主要表现为大量缺乏周期间线和蛋白脂质蛋白,而这些是中枢神经系统中致密髓鞘的主要特征(Inoue等人,1980;Kohsaka等人,1980)。在鸟类视网膜中,穆勒细胞而非少突胶质细胞是主要的髓鞘形成细胞(Seo等人,2001;Won等人,2000)。视神经中仅存在致密髓鞘(Fujita等人,2001)。神经纤维层中视网膜神经节细胞轴突的髓鞘形成倾向于较粗的轴突(Nakazawa等人,1993)。
从进化的角度来看,视网膜内髓鞘形成所带来的不利光学后果,理应被 spike 传导速度的显著提升或能量效率、时间精度等方面的优势所抵消。为验证这一假设,我们研究了有髓鞘轴突和无髓鞘轴突物种的视网膜内 spike 传导速度,以及那些行为表明其视觉处理速度需求可能不同的物种。具体而言,我们利用高分辨率多电极阵列(MEA)记录了啮齿类和鸟类视网膜神经节细胞(RGC)轴突的电活动,并估算了各自的 spike 传导速度。此外,我们还从功能和解剖学角度分析了鸟类视网膜神经纤维层中的跳跃式 spike 传导。
¶ 方法
¶ 伦理审批
所有实验均按照德国联邦政府颁布的《德国动物保护法》(Tierschutzgesetz)以及欧盟关于实验动物使用的指导原则进行。实验流程已获得奥尔登堡卡尔·冯·奥西茨基大学动物福利官的批准(第4条动物实验协议),并遵循美国兽医协会(AVMA)的安乐死指导原则(Leary等人,2020)。动物的繁殖和饲养符合欧盟2010/63号指令中的标准,并获得了地方当局(下萨克森州消费者保护和食品安全局,LAVES)的批准。实验流程还符合《生理学杂志》向作者提供的清单要求(Grundy,2015;O’Halloran,2024)。
¶ 动物
幼鸽(Columba livia f. domestica)和成年豚鼠(Cavia porcellus)通过戊巴比妥(Narcoren,德国英格尔海姆勃林格有限公司)进行终末麻醉。幼欧洲鹌鹑(普通鹌鹑,Coturnix coturnix)、幼原鸡(红原鸡,Gallus gallus)和成年斑胸草雀(Taeniopygia guttata castanotis)采用断头法处死。成年C57BL/6J小鼠通过颈椎脱臼处死。研究纳入了雌雄两种性别的动物,未发现明显的性别特异性差异。所有动物均饲养在自然光照-黑暗周期下,实验在白天进行。动物可自由获取水和食物。
¶ MEA记录与分析
鸟类视网膜在林格液(100 mM氯化钠、6 mM氯化钾、1 mM氯化钙、2 mM硫酸镁、1 mM磷酸二氢钠、30 mM碳酸氢钠、50 mM葡萄糖)中进行解剖,林格液中通入了含5%二氧化碳的95%氧气混合气(Stett等人,2000)。哺乳动物视网膜在通入该混合气的埃姆斯培养基(Sigma-Aldrich GmbH,德国陶夫基兴)中进行解剖。解剖操作在红外光照下进行。哺乳动物视网膜的记录在培养室中于36.5°C的埃姆斯培养基中进行。除非另有说明,鸟类视网膜的记录在浴槽中于37.5°C的林格液中进行(图6E-H)。在大多数情况下,记录温度低于相应动物日常生理体温范围(小鼠:34.5–38°C(van der Vinne等人,2020)、35.8–38.7°C(Yasumoto等人,2015);豚鼠:37.4–38°C(Kainulainen等人,2018)、37.6–38.4°C(Thorne等人,1987);鸡:39–41.3°C(Shimmura等人,2015)、41.1–41.7°C(Savory等人,2006);鹌鹑:41–42°C(Laurila等人,2005)、39.9–42.6°C(Underwood等人,1999);斑胸草雀:39.7–41.8°C(Zagkle等人,2020)、39.2–41.4°C(Sköld-Chiriac等人,2015);鸽子:39–41.6°C(Rashotte等人,1995)、39.3–42°C(Rashotte等人,1999))。一般来说,鸟类的体温高于哺乳动物,且其体温波动也更大,具体取决于动物的活动状态(综述参见Prinzinger等人,1991)。记录时,将一小块周边视网膜以神经节细胞面朝下的方式安装在微电极阵列(MEA)上。大多数记录使用2.6×2.6 mm²的互补金属氧化物半导体(CMOS)MEA(3Brain AG,瑞士普费菲孔),其电极间距为42 µm,能够记录到足够数量的长距离轴突。我们还使用1×1 mm²、电极间距16 µm的CMOS MEA(Multichannel Systems GmbH,德国罗伊特林根)进行了少量更高空间分辨率的记录(图6E-H)。这两种系统的采样率分别为18 kHz和20 kHz。视网膜在低明视光水平下接受光刺激。
对记录进行离线分析,以分离不同细胞的锋电位。经过带通滤波(60赫兹–4千赫兹)后,利用每个电极上的阈值检测候选锋电位事件。提取锋电位发生时该电极及邻近电极上的电压波形。若相似锋电位波形的簇群表现出不应期,则将其识别为候选神经元。通过时间互相关和匹配电图像识别出同一细胞的重复记录,并将其移除。
峰电位分选后,计算了每个细胞的时空峰电位触发平均电信号(Bucci等人,2024;Greschner等人,2014;Litke等人,2004;Radivojevic等人,2017;Seifert等人,2023;Zeck等人,2011)。具体而言,对于每个电极,提取了每个峰电位前后-1.62毫秒至4.42毫秒时间段内的电压波形。所有峰电位波形均采用三次样条插值上采样至200kHz,与峰电位的胞体电压最小值对齐并取平均值。所有后续分析均使用该平均电信号。为构建时间压缩的二维电图像,根据MEA的空间布局显示每个电极处平均波形的最小值。如附图说明所示,为改善轴突的视觉呈现,对胞体电极上的信号进行了饱和处理。轴突长度不足的视网膜神经节细胞(RGCs)已被排除。分析仅限于源自RGCs的向心轴突,这通过电图像中观察到的相对于细胞体的信号传播方向得到证实。
通过对轴突上已识别空间位置之间的欧氏距离与信号波形时间进程中相应最小值进行线性回归,来估算锋电位的传导速度。基于局部最小值,在电图像中手动追踪轴突。所有进一步的分析均基于这些轴突位置。多电极记录的采样率,结合电极间距离,限制了传导速度的可检测范围。然而,通过追踪锋电位在微电极阵列(MEA)上的传播,并将传导速度定义为所有样本点的线性回归值,我们确保了传导速度的可检测范围远超所观察到的生物学范围。距离测量是在投影的空间电图像中进行的,忽略了神经纤维层中轴突可能存在的深度变化。这种投影使得所测量的轴突距离偏向于略小的值。我们通过追踪NF200阳性轴突(见下文“免疫染色和光学显微镜检查”),从解剖学角度估算了其影响,发现传导速度可能被低估了0.05±0.02%(n=20),且未考虑解剖学操作可能产生的伪影。
为了区分跳跃式传导轴突和非跳跃式传导轴突(图2),我们提取了沿轴突的连续时空信号分布。首先,将空间路径定义为沿着手动追踪的轴突线性连接的每个电极。该路径上每个电极的尖峰时间通过拟合速度来估算。 跳跃式传导轴突和非跳跃式传导轴突的区分是通过连续性指数来确定的,该指数量化了这些信号分布的平滑度。对于每个轴突,连续性指数的计算方式为信号分布上局部最大值和局部最小值的稳健平均值之比。为确保连续性指数处于0到1的范围内,在计算该比值之前,先减去整个数据集的全局最大值。 连续性指数值较低表示跳跃式传导轴突的信号分布更不连续,而值较高则表示非跳跃式传导轴突的信号分布更连续。我们对所有追踪到的轴突的连续性指数和传导速度应用了高斯混合模型。基于该模型,轴突被分别归类为跳跃式尖峰传导和非跳跃式尖峰传导两组。属于任一聚类的可能性低于0.90的视网膜神经节细胞(RGCs)被排除在进一步分析之外。 分类后,我们对跳跃式传导轴突估算了几个参数,将手动定义的局部最小值解释为郎飞氏结的位置。适当时,非跳跃式传导轴突的相应测量基于其局部最小值。
尖峰的空间范围定义为其负信号沿轴突的平均范围(图3)。具体而言,我们依次检查了轴突上的所有节点。在特定节点出现最强负偏转时,也就是尖峰位于该节点时,我们提取了所有节点的信号,根据各节点沿轴突相对于当前尖峰位置的距离对信号进行对齐,然后取信号的平均值。接着,我们估算了最近的逆向和顺向电压过零点之间的距离。排除了没有足够多可测量节点的细胞。节点振幅报告为每个轴突所有节点上最小信号的稳健平均值(图4A-D)。仅基于振幅较大的节点进行振幅测量,并不会改变整体的相关性结果。尖峰的起始持续时间定义为每个节点上信号波形从半最小值到最小值的时间的稳健平均值(图4E-H)。偏移持续时间的定义与此类似。由于所有测量都是在尖峰触发的平均电信号上进行的,因此它们可能会受到尖峰时间对齐精度的影响。特别是,尖峰速度的变化会引入抖动,因为尖峰是与体细胞尖峰的时间对齐的。较低的对齐精度可能会导致尖峰波形变宽,振幅减小。
所研究物种从视网膜背缘到视神经乳头的最大轴突长度假设如下:鸽子:约15毫米(Marshall等人,1973);斑胸草雀:约6.5毫米(Liu等人,2023);豚鼠:约8毫米(Howlett和McFadden,2007);小鼠:约3毫米(Duda等人,2025)。对于鸽子和斑胸草雀,视神经乳头被假设偏移约45度(Marshall等人,1973)。对鸽子的估算假设其飞行速度为100公里/小时。
¶ 免疫染色与光学显微镜检查
用于免疫染色时,组织在室温下用含4%多聚甲醛的0.01M磷酸盐缓冲盐水(PBS,pH 7.4)固定20-30分钟。固定后,组织用含30%蔗糖的PBS进行冷冻保护过夜,并在-20°C下保存直至使用。
免疫染色采用间接荧光法进行。视网膜全铺片在含有5%正常驴血清、1%牛血清白蛋白、1% Triton X-100和0.02%叠氮化钠的PBS稀释的一抗溶液中,于室温下孵育2-3天。本研究中使用的一抗包括抗髓鞘碱性蛋白(MBP,大鼠源,单克隆,克隆号12,Bio-Rad Laboratories,美国加利福尼亚州赫拉克勒斯,货号MCA409S,1:1000)、抗神经丝蛋白200(NF200,兔源,多克隆,Sigma-Aldrich,货号N4142,1:1000)以及抗泛电压门控钠通道(panNav,小鼠源,单克隆,克隆号K58/35,Sigma-Aldrich,货号S8809,1:1000)。二抗为驴源抗体(1:500,偶联Alexa 488、568、647,Thermo Fisher Scientific,美国马萨诸塞州沃尔瑟姆;或偶联Cy3,Jackson ImmunoResearch Laboratories,美国宾夕法尼亚州西葛罗夫),在相同的孵育液中于室温下孵育4小时。组织样本被封固在载玻片上,并用Vectashield封片剂(Vector Laboratories,美国加利福尼亚州伯灵格姆)覆盖盖玻片。载玻片和盖玻片之间使用间隔物以避免挤压组织。
概览图像堆栈是使用共聚焦激光扫描显微镜(Leica TCS SL,徕卡显微系统有限公司,德国韦茨拉尔)拍摄的,该显微镜配备了×40/NA 1.25油浸物镜。为获取panNav簇的高分辨率图像及相应的尺寸测量数据,使用×63/NA 1.32油浸物镜采集图像堆栈。所有共聚焦堆栈的z轴增量均为0.2 µm。为测量结间长度和轴突直径,使用配备电动载物台及×40/NA 1.3油浸物镜的徕卡DM6B荧光显微镜沿轴突进行图像堆栈的平铺扫描。单个图块的自动采集和拼接在徕卡LASX软件包中进行。使用Fiji中的分段线工具测量沿单个NF200阳性轴突上panNav簇(即郎飞结)之间的距离。结间长度测量为panNav阳性簇中心之间的距离。请注意,用于解剖学测量的结间长度定义包括近结区和结旁区,指的是panNav簇之间的完整距离。每次结间长度测量均同时测量轴突直径,方法是在给定的一对簇之间的大致中点处,画一条横跨神经丝阳性区域的正交线。为测量panNav簇的长度和直径,每个簇手动选择一个图像平面,以包含整个管状结构的最大直径。使用大津法对感兴趣区域进行阈值处理。单个长度值代表每个簇两侧壁测量值的平均长度。所有显微图像的图版均显示最大强度侧视图或z投影,这些操作在Fiji中完成。最终图像的亮度和对比度在Adobe Photoshop中进行调整。
¶ 统计分析
所有测试和分析均在MATLAB(MathWorks公司,美国马萨诸塞州纳蒂克)中进行。在结果部分,测量值以平均值±标准差的形式报告。稳健平均值定义为数据中间80%部分的平均值。未进行进一步的离群值筛选。报告了相关系数的95%置信区间的上下限。在所有情况下,均拒绝了所研究参数(活动节点数量、节点振幅、节点起始持续时间)与传导速度零相关的检验。所有分布间差异的检验均采用Wilcoxon秩和检验,且在所有情况下均拒绝了中位数相等的假设。为分析轴突内部和轴突之间的结间长度变异(图6B),使用了四分位离散系数(Bonett,2006)。轴突间的离散系数通过有放回抽样进行了 bootstrap 计算。
¶ 结果
¶ 电图像揭示跳跃式锋电位传导
我们采用大规模MEA记录来研究视网膜内轴突髓鞘化对尖峰传导的影响。这些阵列的高电极密度使得能够详细分析所记录神经元的时空电活动(Bucci等人,2024;Greschner等人,2014;Litke等人,2004;Radivojevic等人,2017;Seifert等人,2023;Zeck等人,2011)。电极层面的、尖峰触发的平均电活动有助于了解尖峰如何沿着视网膜神经节细胞(RGC)的轴突传播。通过对所记录细胞的电活动进行最小投影以压缩时间维度(电图像,图1),突出了其空间结构。正如预期的那样,可以区分出高振幅的胞体区域、周围的树突区域以及伸向视盘的轴突。
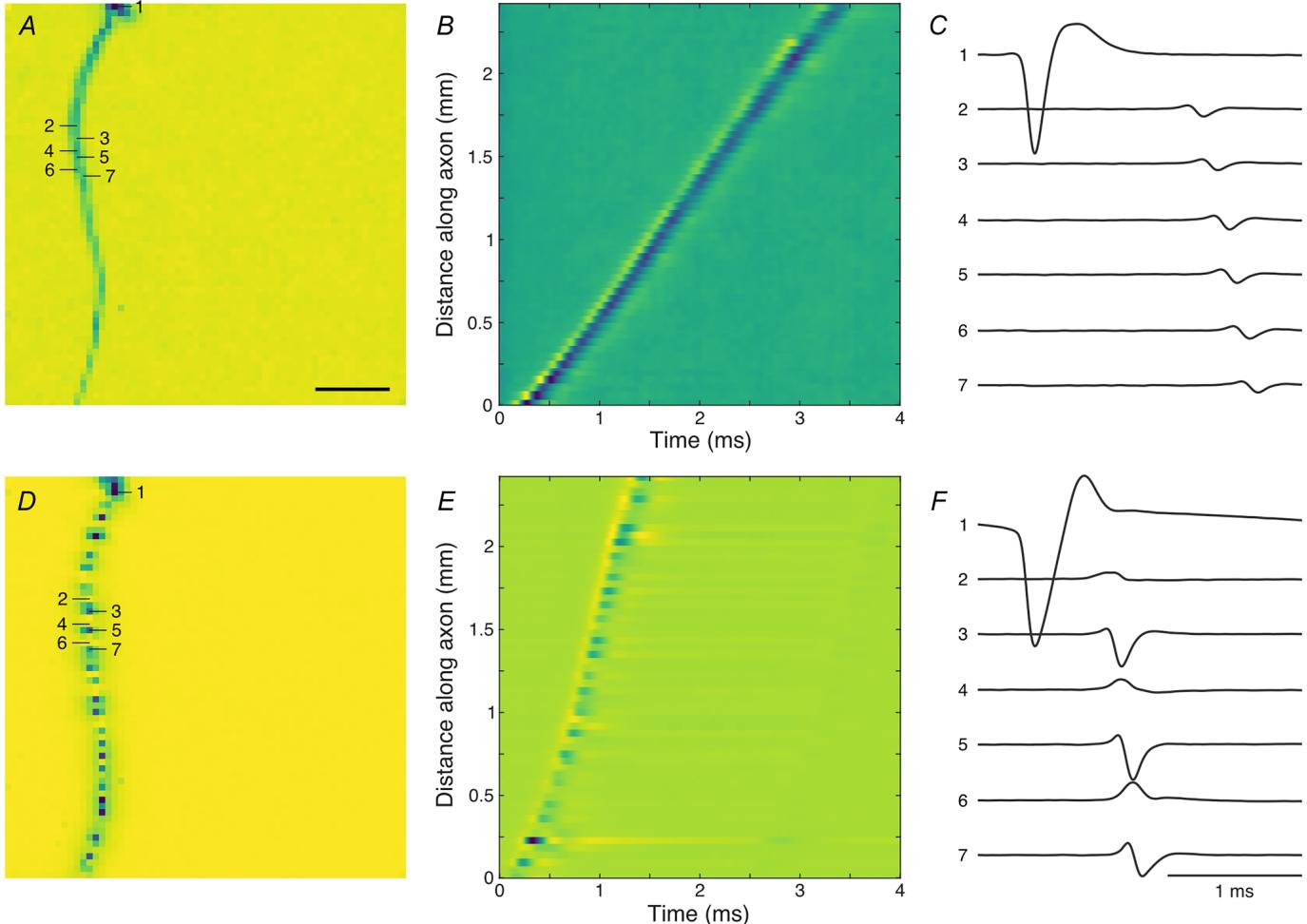
图1. 欧洲鹌鹑视网膜神经节细胞的电图像显示了具有和不具有跳跃传导的轴突
A,非跳跃式视网膜神经节细胞(RGC)的电图像,传导速度v = 0.79 m/s。沿尖峰触发的平均电活动时间维度的最小电压投影。冷色调表示负电位。为视觉清晰起见,胞体振幅已饱和。64×64电极,比例尺:500 µm。B,沿轴突的信号波形。冷色调表示负电位。C,A中所示七个选定电极的信号波形。比例尺:1 ms。y轴为任意单位,C和F中的y刻度相同。D-F,与A-C相同,但为跳跃式RGC,v = 2.02 m/s。
在欧洲鹌鹑中,许多被记录的视网膜神经节细胞(RGCs)表现出连续的轴突 spike 传导(图1A-C),这在大多数哺乳动物物种的RGC轴突中很常见。然而,很大一部分被记录的鹌鹑RGCs表现出不连续的,即跳跃式的轴突传导(图1D-F)。在这些情况下,我们观察到高振幅信号的不同轴突区域与相反信号极性的低振幅区域交替出现,这与具有被动传导段的有髓轴突的预期一致,这些轴突周期性地被类似郎飞氏结的活动结构中断(图1D和F)。对轴突上 spike 传导随时间的分析显示,在这两种情况下都存在大致线性的距离-时间关系(图1B和E)。最大负偏转时间的线性拟合斜率以及沿轴突的相应距离被用作轴突传导速度的估计值。
我们通过计算每个轴突在电图像中轨迹上局部最大值与最小值的比值,量化了其信号连续性程度。该连续性指数的分布呈双峰分布(图2),反映了跳跃式传导和非跳跃式传导的轴突。为了进一步分析,我们排除了不太可能属于这两组中任何一组的神经元(图2,灰色簇)。正如预期的那样,跳跃式传导轴突的整体传导速度更高(跳跃式:1.25±0.35米/秒,n=337;非跳跃式:0.71±0.12米/秒,n=163;秩和检验P<0.001)。虽然高传导速度仅存在于跳跃式传导轴突中,但令人惊讶的是,低传导速度在非跳跃式和跳跃式传导轴突中均存在。
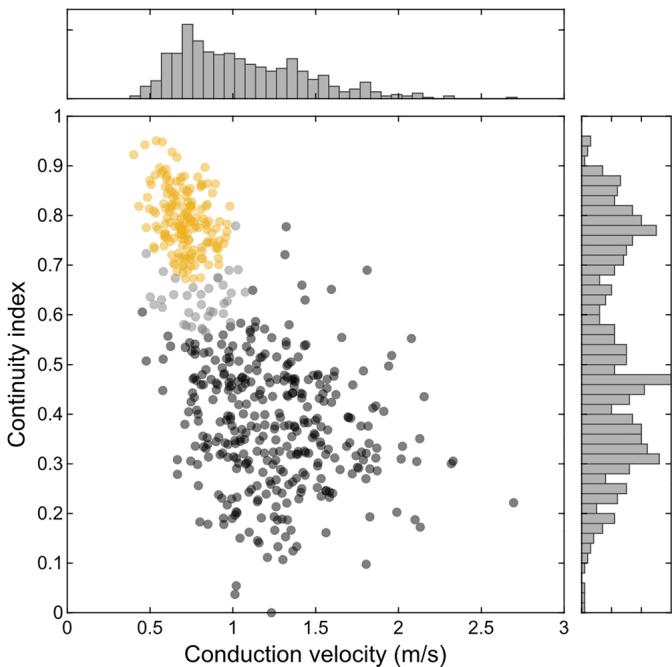
图2. 跳跃式传导轴突和非跳跃式传导轴突表现出不同的传导速度
来自一只欧洲鹌鹑视网膜、具有足够轴突长度的视网膜神经节细胞(RGCs)被分为337个跳跃式轴突(黑色)和163个非跳跃式轴突(黄色)。36个轴突(灰色)的重叠区域因进一步分析被排除(可能性<0.90,高斯混合)。连续性指数是沿轴突的稳健平均峰值振幅除以稳健平均谷值振幅。详见方法部分。图3和图4展示了来自相同细胞的数据。
¶ 生物物理参数的巨大变异性
多种生物物理参数决定了跳跃式锋电位传导的速度。通过对电图像的分析,可以估算鸟类视网膜内数百个细胞的视网膜内跳跃式传导的不同相关参数。最重要的是,信号在活动结之外的扩散有望在轴突传导速度中起主导作用。我们测量了活动结的范围,即同时活动的结(图3A-C)。这些数据表明,当前信号振幅最大的结上的信号扩散范围有多远。在鹌鹑视网膜中,同时活动的跳跃式结的总范围平均为311±114μm(n=335;观察到的最大值:722μm),并且确实与传导速度相关(图3D;相关系数:0.73,置信区间:0.67,0.77;P<0.001)。非跳跃式轴突上的平均信号范围更小(161±44μm;n=161;秩和检验:P<0.001),且与传导速度几乎不相关(相关系数:0.37,置信区间:0.23,0.50;P<0.001)。活动的逆向结(即激活后仍为负的结)的范围与活动的顺向结的范围相关(相关系数:0.58,置信区间:0.51,0.65;P<0.001),尽管逆向范围比顺向范围大1.97±1.07倍(秩和检验:P<0.001)。
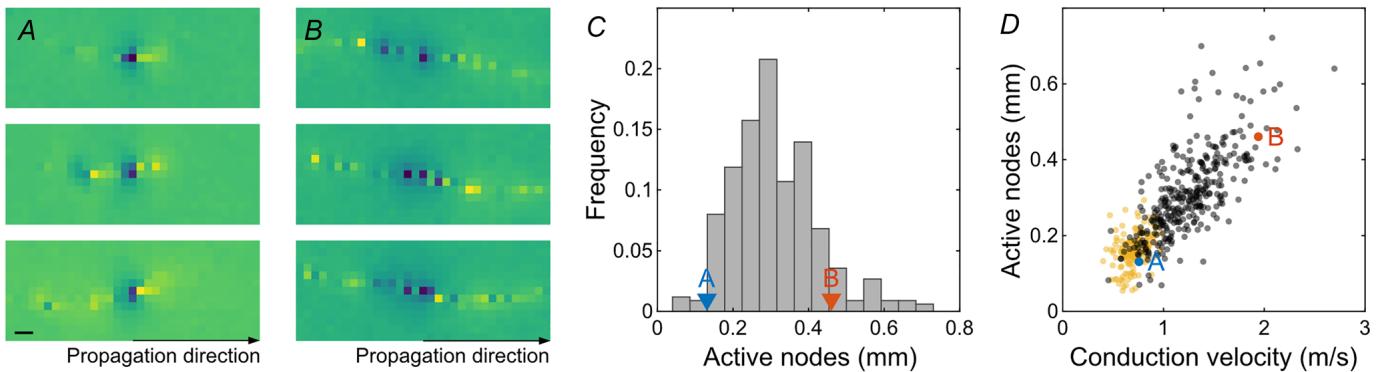
图3. 欧洲鹌鹑视网膜中活动节点的空间范围与传导速度相关
A,来自一个视网膜神经节细胞轴突的三个示例结的空间电活动放大图。电图像在空间和时间上与各自结的局部最小值对齐。蓝色表示负值。为了视觉清晰度,最大振幅已饱和。比例尺:100微米。B,与A相同,为具有大量同时活跃结的第二个视网膜神经节细胞。C,平均同时活跃结的直方图。标记了A和B的视网膜神经节细胞。D,跳跃式(黑色)和非跳跃式(黄色)轴突的活跃结空间范围与传导速度的关系。标记了A和B的视网膜神经节细胞。
正向激活节点的范围由多个参数决定,例如轴突的长度常数(它指示信号传播的范围)、节点的整体敏感性及其激活动力学。虽然在我们的记录中无法直接获取这些因素,但电信号的振幅和起始时间可以作为替代指标。平均节点振幅(图4A-D)比平均非跳跃式轴突的振幅高出2.33±1.18倍。在非跳跃式轴突中,轴突振幅与传导速度大致成比例(图4D;相关系数:-0.47,置信区间:-0.58,-0.34;P<0.001)。然而,对于跳跃式轴突,这种情况并不明显(相关系数:-0.24,置信区间:-0.34,-0.14;P<0.001)。此外,特定节点的信号起始(图4E-H)与传导速度无明显相关性(图4H;相关系数:-0.16,置信区间:-0.26,-0.06;P=0.003)。信号的起始时间和终止时间呈强相关性(相关系数:0.81,置信区间:0.76,0.84;P<0.001)。
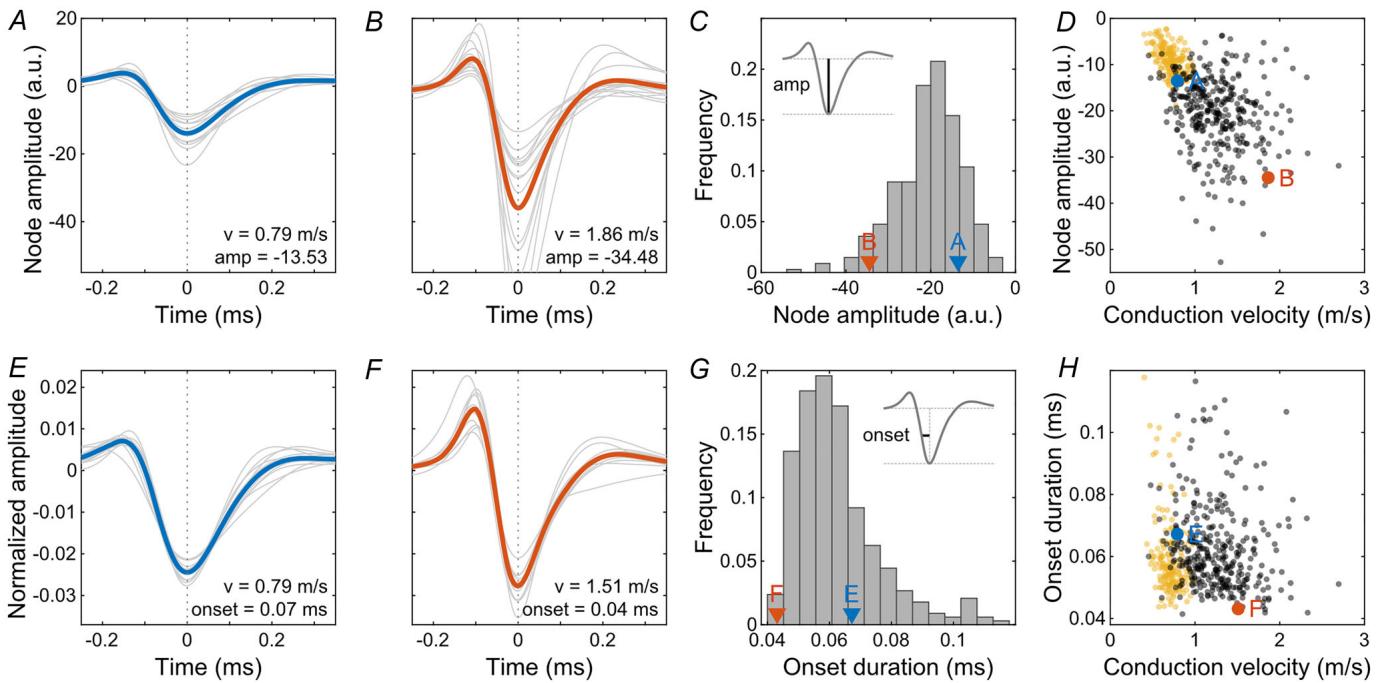
图4. 在欧洲鹌鹑视网膜中,不同轴突的节点振幅和起始持续时间存在较大差异。
A和B,两个视网膜神经节细胞(RGC)的跳跃式轴突的节点振幅。如C和D所示,为便于视觉区分,较慢的轴突(蓝色)和较快的轴突(红色)已做标记。灰色线条代表各个节点,粗线条代表它们的平均值。C,不同轴突的稳健平均节点振幅直方图。标记出了A和B中的视网膜神经节细胞。D,跳跃式轴突的节点振幅与传导速度的关系(黑色)。为便于比较,还显示了非跳跃式轴突的稳健平均振幅(黄色)。E和F,两个视网膜神经节细胞的跳跃式轴突的起始持续时间。灰色线条代表一根轴突上的各个节点(已标准化为绝对面积),粗线条代表它们的平均值。G,不同轴突的稳健平均起始持续时间直方图。标记出了E和F中的视网膜神经节细胞。H,跳跃式(黑色)和非跳跃式(黄色)轴突的起始持续时间与传导速度的关系。
¶ 电压门控钠通道聚集在结处
接下来,我们对鹌鹑视网膜颞区的髓鞘形成模式和钠通道分布进行了解剖学分析(图5A–C)。钠通道聚集在短管状结构中。这些聚集区没有髓鞘。无髓鞘轴突没有钠通道聚集,仅表现出弥漫性的泛钠通道免疫反应性,且这种反应性很少超过背景水平。因此,这些轴突未在图5C中呈现,因为它们通常对神经丝亚基呈阴性。不同轴突之间的神经丝表达水平存在差异。髓鞘形成及相应的钠通道聚集在神经丝强阳性和弱阳性的轴突上均会发生。钠通道聚集区的长度为1.4±0.3µm,宽度为1.1±0.3µm(n=52,1个视网膜)。对鸽子视网膜的实验结果与从鹌鹑中获得的结果一致,即泛钠通道免疫反应阳性的结位于神经丝阳性轴突上(图5D)。
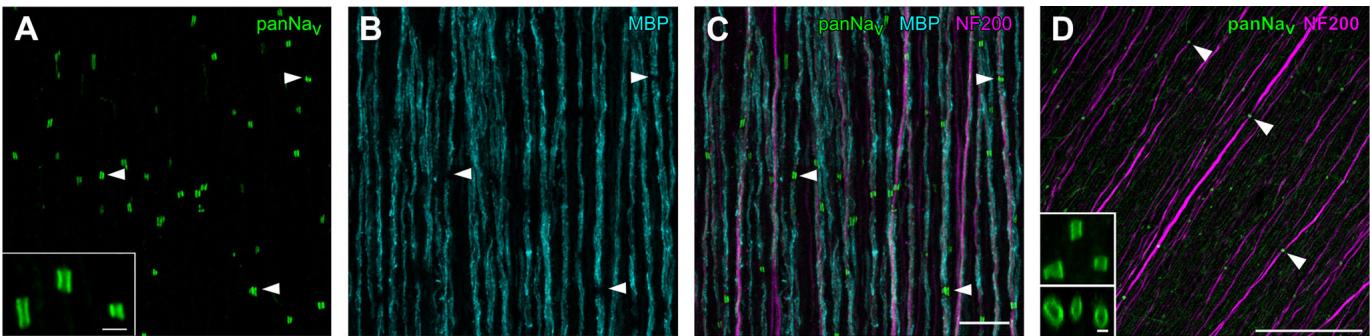
图5. 在欧洲鹌鹑和鸽子的视网膜中,电压门控钠通道聚集在有髓鞘的视网膜神经节细胞轴突的结处
A-C,鹌鹑视网膜神经纤维层的共聚焦图像,对电压门控钠通道(panNav)、髓鞘碱性蛋白(MBP)和神经丝(NF200)进行了免疫标记。在髓鞘化中断的部位,轴突上发现了密集的钠通道簇(箭头标记的示例位置)。A中的插图显示了更高放大倍数下的panNav簇。比例尺:A插图:2微米,C:10微米。D,鸽子视网膜中的钠通道簇。与鹌鹑视网膜一样,在轴突上发现了钠通道簇(箭头标记的示例位置)。插图显示了更高放大倍数下的panNav簇:顶部:图像堆栈的最大强度投影。底部:旋转图像堆栈的侧视图。比例尺:50微米,插图:1微米。
钠通道簇之间的距离是沿着神经丝强阳性轴突测量的(图6A)。这种结间长度(平均值:76.8±25.2µm,n=200)在单个轴突上的变化出人意料地大。然而,轴突之间的变异性明显更大(图6B;威尔科克森秩和检验:P<0.001),这表明结间长度具有细胞类型依赖性。结间长度与轴突直径呈正相关(平均值:0.9±0.2µm,n=200;相关系数:0.55,置信区间:0.44、0.64;P<0.001;图6C)这一发现进一步支持了上述观点,其中轴突直径通过每对结之间中部的神经丝标记宽度来估算。
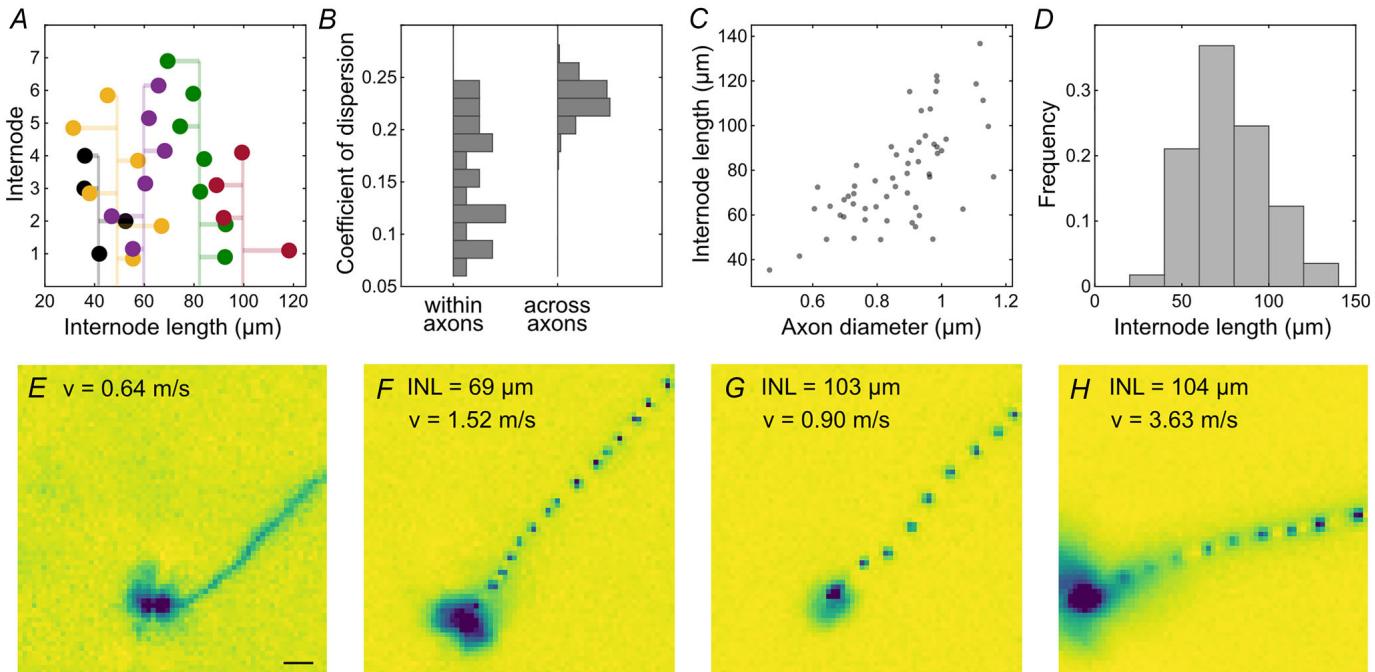
图6. 欧洲鹌鹑视网膜中轴突的结间长度存在很大差异
A,五条示例轴突的连续节间长度。垂直线代表特定轴突的平均节间长度。B,轴突内节间长度的变异显著小于轴突间的变异(四分位离散系数)。选取至少有五个测量节点的轴突(n = 22)。轴突间的方差采用 bootstrap 法计算。C,节点间距离随轴突直径的增大而增加。单个轴突的平均值(n = 57)。D,节间长度数量的直方图。E-H,使用电极间距为16µm的MEA(65×65电极)记录的电图像。INL表示平均节间长度,v表示传导速度。来自两个视网膜的示例。记录温度为36°C。比例尺:100µm。
节间长度有望成为轴突传导速度的主要决定因素(Brill等人,1977)。然而,从定性角度看,在我们的观察中这种依赖性似乎较弱(图6E–H)。
¶ 传导速度的种间差异很大
我们测量了来自不同生态位、有髓鞘和无髓鞘物种视网膜轴突的传导速度,以探索潜在的适应性(图7)。值得注意的是,鸽子(2.07±0.70米/秒;n=1135)和斑胸草雀(1.55±0.57米/秒,n=511)视网膜中的峰电位传导速度显著高于地面栖息的欧洲鹌鹑(1.29±0.71米/秒;n=1032)和原鸡(1.08±0.41米/秒;n=1219)。相比之下,无髓鞘的小鼠(0.65±0.15米/秒;n=398)和豚鼠(0.86±0.18米/秒;n=2700)视网膜的传导速度平均慢于鸟类物种,这与髓鞘的缺失相符(Kruskal-Wallis检验结合Tukey-Kramer两两比较检验:所有组合P<0.001)。
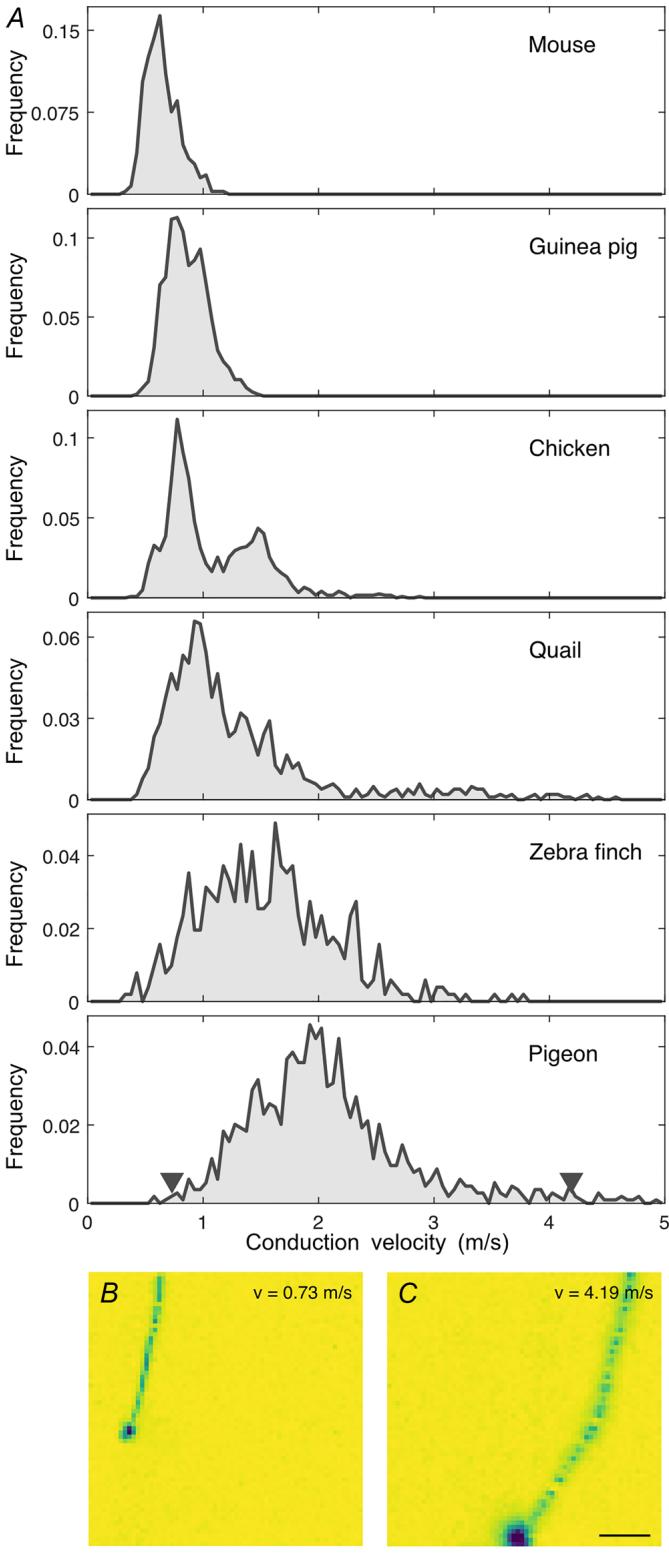
图7. 传导速度存在较大的种间差异
A,小鼠(2个视网膜,398个轴突)、豚鼠(2个视网膜,2700个轴突)、欧洲鹌鹑(2个视网膜,1032个轴突)、原鸡(2个视网膜,1219个轴突)、斑胸草雀(2个视网膜,511个轴突)和鸽子(2个视网膜,1135个轴突)的轴突传导速度直方图。排除长度不足的轴突。直方图已根据各物种分析的轴突总数进行标准化。最后一个面板中的箭头指示B和C中所示细胞的速度。请注意,记录是在低于动物体温的条件下进行的(见方法部分)。B和C,鸽子视网膜神经节细胞中慢速(B)和快速(C)轴突 spike 传导的示例电图像。比例尺:500微米。为清晰起见,B和C中的胞体振幅已饱和。
¶ 讨论
我们研究了视网膜神经节细胞轴突的跳跃式 spike 传导,并证实了视网膜内髓鞘形成和郎飞氏结的存在。平均而言,跳跃式传导的轴突比非跳跃式传导的轴突具有更高的传导速度,尽管两组之间的速度存在显著重叠。观察到的不同物种间轴突传导速度的差异似乎与其各自的生态位和行为相对应。
鹌鹑和鸽子视网膜轴突中panNav阳性钠通道簇的形态特征,包括其管状形状、大小、沿轴突的分布模式以及这些部位髓鞘的间隙,与在脊椎动物视神经和中枢神经系统其他部位的常规郎飞氏结中观察到的结构非常相似(图5)(Arancibia-Cárcamo等人,2017年;Boiko等人,2001年;Caldwell等人,2000年;O’Brien等人,2008年;Rasband等人,1999年)。我们使用了一种泛抗体,该抗体针对所有脊椎动物Nav1亚型中存在的高度保守序列(Rasband等人,1999年)。因此,在鹌鹑和鸽子视网膜神经节细胞(RGC)轴突的郎飞氏结处表达的确切钠通道亚基仍不清楚。在哺乳动物视网膜中,视网膜神经节细胞在轴突起始段表达Nav1.6,在神经纤维层内的无髓鞘轴突中表达Nav1.2。在那里,郎飞氏结仅在视神经中形成,并且在发育过程中,Nav1.6通常会取代Nav1.2。Nav1.8可能也存在于具有大口径轴突的α样细胞类型中(Van Hook等人综述,2019年)。因此,我们不禁推测,在鸟类中,在无髓鞘轴突中观察到的弥漫性panNav标记代表Nav1.2,而郎飞氏结处的簇状通道主要由Nav1.6形成,Nav1.8仅在一部分特别粗的轴突中表达。然而,还需要进一步的研究来确定鸟类视网膜神经节细胞轴突中特定的电压门控钠通道亚基及其动力学特性。
总体而言,我们关于视网膜的功能研究结果与神经系统其他部分的数据一致。然而,特定的限制因素对视网膜中的轴突传导有着独特的影响。神经纤维层需要具备良好的光学透明度,这限制了髓鞘的结构和数量。髓鞘起着电绝缘体的作用,它通过降低结间膜电容和膜电导,增加长度常数,减小时间常数,并最终提高轴突的传导速度。因此,传导速度与神经纤维层光学质量的保持之间可能存在一种平衡。事实上,只有一部分视网膜内视网膜神经节细胞(RGC)轴突是有髓鞘的(Imagawa等人,1999;Inoue等人,1980)。髓鞘化和快速传导速度可能更有利于那些传递与警觉性或运动处理相关信息的RGC类型。此外,所有离心轴突在视网膜内都被描述为有髓鞘的(Wilson和Lindstrom,2011)。
虽然最高的传导速度只在跳跃传导轴突中发现,最低的速度在非跳跃传导轴突中发现,但我们观察到跳跃传导轴突和非跳跃传导轴突的速度存在令人惊讶的大量重叠(图2)。有髓鞘轴突的传导速度似乎更能从轴突直径的增加中获益(Brill等人,1977年;Waxman,1980年;另见Hodes,1953年;Hoffmeister等人,1991年;Pumphrey和Young,1938年),并且对于直径大于0.2微米的轴突,有髓鞘轴突预计会比无髓鞘轴突达到更高的速度(Waxman和Bennett,1972年)。此外,无髓鞘轴突中更高的速度可能通过增加通道密度来实现(Schmidt和Knösche,2019年)。因此,所观察到的跳跃传导轴突(即有髓鞘轴突)的低速度,可能由同等直径的无髓鞘轴突实现,这可能提供更好的透明度。从简单的优化角度来看,人们可能会预期跳跃传导轴突和非跳跃传导轴突的速度之间存在清晰的界限。然而,观察到的显著重叠表明存在更复杂的优化过程。例如,增加有髓鞘细胞类型的数量可能会受到光学透明度需求的限制,尽管额外细胞类型所携带的信息可能需要更高的传导速度。相反,有髓鞘轴突可能具有额外的优势,但从进一步提高速度中获得的益处可能有限。髓鞘化的一个潜在优势可能是增加空间堆积密度。然而,在低传导速度下,有髓鞘轴突包括其鞘的总直径通常大于无髓鞘轴突的直径(Waxman,1980年)。此外,虽然髓鞘化的代谢优势对具有更高 firing 率的轴突特别有利(Perge等人,2009年),但我们发现速度相似的有髓鞘和无髓鞘轴突的 firing 率没有明显差异,这没有提供代谢优化的证据。尽管如此,髓鞘化可能为信息传递带来其他好处,例如减少 spike 定时抖动(Kim等人,2013年)。
测得的视网膜内传导速度与最近在鸡身上的研究结果基本一致(图7)(Seifert等人,2023年)。与中枢神经系统的其他部分相比,视网膜内传导速度相对较低。例如,皮质脊髓神经元的传导速度可达100米/秒(猫,Takahashi,1965年),丘脑-皮质传导速度在6-38米/秒之间(兔,Swadlow和Weyand,1985年),但也有研究描述过传导速度低至0.3米/秒的慢速皮质神经元(兔,Swadlow,1990年)。视网膜神经节细胞轴突的视网膜外传导速度确实高于视网膜内传导速度(Stanford,1987年;Stone和Freeman,1971年),这表明快速传导通常是有益的,并进一步证实了视网膜内髓鞘形成受限的观点。
虽然单个轴突上测量的结间长度变化(图6A)可能看起来出乎意料,但在不同脊椎动物的外周和中枢神经系统区域也描述过类似的变化(鸡听觉脑干:Seidl等人,2010年;斑马鱼脊髓:Auer等人,2018年;Vagionitis等人,2022年;兔脊髓:Hess和Young,1949年;兔外周神经:Vizoso和Young,1948年)。在我们的定性分析中,传导速度似乎仅与结间长度有微弱的相关性(图6E–H)。因此,理论研究预测结间长度对传导速度的影响很小(Moore等人,1978年;Schmidt和Knösche,2019年)。
一种方法学偏差与记录过程中视网膜的温度有关。尽管按照常规实验操作,该温度相对较高,但仍低于相应动物的体温。据推测,温度每升高10°C,传导速度大约会增加50%(Waxman,1980年综述)。因此,不应从绝对意义上看待传导速度。体温与离体记录温度之间的不匹配在鸟类物种中最为明显。在这些情况下,我们的结果可能最大程度地低估了传导速度。此外,生理数据中结的检测受到多电极阵列(MEA)电极间距的限制。根据采样定理,小于约90微米的结间长度无法被可靠检测到,这可能导致在我们的分析中,具有较小结间长度的视网膜神经节细胞(RGCs)的代表性不足。然而,使用更高分辨率MEA进行的对照测量(图6E–H)显示,观察到的跳跃传导模式没有明显差异。相反,解剖学分析可能倾向于偏小的结间长度,因为基于神经丝染色,视网膜神经节细胞轴突只能在相对较短的距离内被可靠追踪。另一个潜在的方法学偏差来源可能是,所有测试物种都在不同程度上被驯化,这可能影响了它们的视网膜内 spike 传导速度。例如,鸽子主要是为了定向能力和飞行速度而培育的,而斑胸草雀则是因其美观的羽毛而被选育的。相比之下,我们记录的是原鸡(家鸡的野生祖先)和欧洲鹌鹑的视网膜,其中欧洲鹌鹑与日本鹌鹑相比,作为家禽养殖的情况较少。
我们观察到,鸽子和斑胸草雀视网膜中的传导速度明显快于欧洲鹌鹑和班基瓦鸡。传导速度的这些种间差异与其各自的生态位和行为相符,特别是地面栖息、树栖和空中生活方式之间的区别。例如,欧洲鹌鹑主要是一种地面栖息的鸟类。虽然在迁徙季节,它会在夜间长途飞行,但它的大部分食物获取和巢穴建造都在地面附近进行。当受到威胁时,它通常会静止不动,依靠伪装保护自己,只有在万不得已时才会短途飞行,之后又回到地面并再次静止。另一方面,鸽子和斑胸草雀是飞行速度较快的鸟类,需要快速的视觉处理(Boström等人,2016;Potier等人,2020)。它们的集群行为要求它们对领头动物的方向变化做出快速反应,在栖息地等障碍物附近进行飞行机动时也是如此。此外,它们在飞行途中更有可能遭到捕食者的攻击,而灵活的飞行机动可能为它们提供关键的逃生机会。 此外,不同物种眼睛大小的差异可能也是导致视网膜内延迟不同的原因之一。虽然有证据表明,视网膜内的 spike 传导速度可以补偿延迟(Bucci等人,2024),但目前尚不清楚不同物种之间是否存在与眼睛大小相关的类似优化机制。似乎存在一种微弱的普遍趋势,即眼睛越大,传导速度越高。例如,在我们的数据中,鸽子的最大传导速度最高,而小鼠的最大传导速度最低。然而,由于鸽子的眼睛较大,且视神经位置偏移,最长轴突的 spike 到达时间差异大致被抵消了。同时,豚鼠的眼睛比斑胸草雀大,但最大传导速度却明显较慢。如果鸽子的最大轴突传导速度与小鼠相同,那么观察到的差异将对应约10毫秒的延迟。对于快速飞行的鸽子来说,这种延迟对应的飞行距离为27厘米。在鸽子视网膜中,最慢的非跳跃式轴突与最快的跳跃式轴突之间的传导延迟差异为24毫秒,对应的飞行距离为67厘米。
鸟类的视网膜是视网膜生理学适应物种生态的一个显著例子。鸟类视网膜内的轴突传导似乎代表了一种多方面的适应,这种适应精确地调整以满足它们的生态需求,平衡了对速度、时间精度、代谢效率和光学透明度的要求。
¶ 参考文献
Arancibia-Cárcamo, I. L., Ford, M. C., Cossell, L., Ishida, K., Tohyama, K., & Attwell, D. (2017). Node of Ranvier length as a potential regulator of myelinated axon conduction speed. eLife, 6, e23329.
Auer, F., Vagionitis, S., & Czopka, T. (2018). Evidence for myelin sheath remodeling in the CNS revealed by In vivo imaging. Current Biology, 28(4), 549–559.e3.
Blanke, N., Chang, S., Novoseltseva, A., Wang, H., Boas, D. A., & Bigio, I. J. (2023). Multiscale label-free imaging of myelin in human brain tissue with polarization-sensitive optical coherence tomography and birefringence microscopy. Biomedical Optics Express, 14(11), 5946.
Boiko, T., Rasband, M. N., Levinson, S. R., Caldwell, J. H., Mandel, G., Trimmer, J. S., & Matthews, G. (2001). Compact myelin dictates the differential targeting of two sodium channel isoforms in the same axon. Neuron, 30(1), 91–104.
Bonett, D. G. (2006). Confidence interval for a coefficient of quartile variation. Computational Statistics & Data Analysis, 50(11), 2953–2957.
Boström, J. E., Dimitrova, M., Canton, C., Håstad, O., Qvarnström, A., & Ödeen, A. (2016). Ultra-rapid vision in birds. PLoS ONE, 11(3), e0151099.
Brill, M. H., Waxman, S. G., Moore, J. W., & Joyner, R. W. (1977). Conduction velocity and spike configuration in myelinated fibres: Computed dependence on internode distance. Journal of Neurology, Neurosurgery, and Psychiatry, 40(8), 769–774.
Bucci, A., Büttner, M., Domdei, N., Rosselli, F. B., Znidaric, M., Diggelmann, R., Gennaro, M. D., Cowan, C. S., Harmening, W., Hierlemann, A., Roska, B., & Franke, F. (2024). Action potential propagation speed compensates for traveling distance in the human retina (p. 2024.04.30.591867). bioRxiv. https://doi.org/10.1101/2024. 04.30.591867
Caldwell, J. H., Schaller, K. L., Lasher, R. S., Peles, E., & Levinson, S. R. (2000). Sodium channel is localized at nodes of Ranvier, dendrites, and synapses. Proceedings of the National Academy of Sciences of the United States of America, 97(10), 5616–5620.
DePaoli, D., Gasecka, A., Bahdine, M., Deschenes, J. M., Goetz, L., Perez-Sanchez, J., Bonin, R. P., De Koninck, Y., Parent, M., & Côté, D. C. (2020). Anisotropic light scattering from myelinated axons in the spinal cord. Neurophotonics, 7(01), 015011.
Duda, S., Block, C. T., Pradhan, D. R., Arzhangnia, Y., Klaiber, A., Greschner, M., & Puller, C. (2025). Spatial distribution and functional integration of displaced retinal ganglion cells. Scientific Reports, 15(1), 7123.
Fujita, Y., Imagawa, T., & Uehara, M. (2000). Comparative study of the lamina cribrosa and the pial septa in the vertebrate optic nerve and their relationship to the myelinated axons. Tissue & Cell, 32(4), 293–301.
Fujita, Y., Imagawa, T., & Uehara, M. (2001). Fine structure of the retino-optic nerve junction in the chicken. Tissue & Cell, 33(2), 129–134.
Gao, L., Macklin, W., Gerson, J., & Miller, R. H. (2006). Intrinsic and extrinsic inhibition of oligodendrocyte development by rat retina. Developmental Biology, 290(2), 277–286.
Greschner, M., Field, G. D., Li, P. H., Schiff, M. L., Gauthier, J. L., Ahn, D., Sher, A., Litke, A. M., & Chichilnisky, E. J. (2014). A polyaxonal amacrine cell population in the primate retina. The Journal of Neuroscience, 34(10), 3597–3606.
Grundy, D. (2015). Principles and standards for reporting animal experiments in The Journal of Physiology and Experimental Physiology. The Journal of Physiology, 593(12), 2547–2549.
Grzybowski, A., & Winiarczyk, I. (2015). Myelinated retinal nerve fibers (MRNF) – Dilemmas related to their influence on visual function. Saudi Journal of Ophthalmology, 29(1), 85–88.
Hess, A., & Young, J. Z. (1949). Correlation of internodal length and fibre diameter in the central nervous system. Nature, 164(4168), 490–491.
Hodes, R. (1953). Linear relationship between fiber diameter and velocity of conduction in giant axon of squid. Journal of Neurophysiology, 16(2), 145–154.
Hoffmeister, B., Jänig, W., & Lisney, S. J. W. (1991). A proposed relationship between circumference and conduction velocity of unmyelinated axons from normal and regenerated cat hindlimb cutaneous nerves. Neuroscience, 42(2), 603–611.
Howlett, M. H. C., & McFadden, S. A. (2007). Emmetropization and schematic eye models in developing pigmented guinea pigs. Vision Research, 47(9), 1178– 1190.
Hughes, A. (1971). Topographical relationships between the anatomy and physiology of the rabbit visual system. Documenta Ophthalmologica Advances in Ophthalmology, 30(1), 33–159.
Imagawa, T., Fujita, Y., Kitagawa, H., & Uehara, M. (1999). Quantitative studies of the optic nerve fiber layer in the chicken retina. The Journal of Veterinary Medical Science, 61(8), 883–889.
Inoue, Y., Sugihara, Y., Nishimura, Y., & Shimai, K. (1980). Atypical neural sheaths formed by Müller cells in chicken retina. Okajimas Folia Anatomica Japonica, 57(2–3), 79–87.
Kainulainen, M., Spengler, J., Welch, S., Coleman, J., Harmon, J., Klena, J., Nichol, S., Albariño, C., & Spiropoulou, C. (2018). Protection against lethal Lassa virus infection induced with a scalable replicon particle vaccine in the guinea pig model. The Journal of Infectious Diseases, 217(12), 1957–1966.
Kim, J. H., Renden, R., & von Gersdorff, H. (2013). Dysmyelination of auditory afferent axons increases the jitter of action potential timing during high-frequency firing. The Journal of Neuroscience, 33(22), 9402–9407.
Kohsaka, S., Takamatsu, K., Nishimura, Y., Mikoshiba, K., & Tsukada, Y. (1980). Neurochemical characteristics of myelin-like structure in the chick retina. Journal of Neurochemistry, 34(3), 662–668.
Lee, K. H., Kim, S. W., Kwon, S. S., Oh, J., & Huh, K. (2015). Microperimetry and spectral domain optical coherence tomography in myelinated retinal nerve fibers. International Journal of Ophthalmology, 9(1), 170–172.
Laurila, M., Pilto, T., & Hohtola, E. (2005). Testing the flexibility of fasting-induced hypometabolism in birds: Effect of photoperiod and repeated food deprivations. Journal of Thermal Biology, 30(2), 131–138.
Leary, S., Underwood, W., Anthony, R., Cartner, S., Grandin, T., Greenacre, C., Gwaltney-Brant, S., McCrackin, M. A., Meyer, R., Miller, D., Shearer, J., Turner, T., & Yanong, R. (2020). AVMA Guidelines for the Euthanasia of Animals: 2020 Edition. American Veterinary Medical Association. https://www.avma.org/resources-tools/avma-policies/avmaguidelines-euthanasia-animals
Litke, A. M., Bezayiff, N., Chichilnisky, E. J., Cunningham, W., Dabrowski, W., Grillo, A. A., Grivich, M., Grybos, P., Hottowy, P., Kachiguine, S., Kalmar, R. S., Mathieson, K., Petrusca, D., Rahman, M., & Sher, A. (2004). What does the eye tell the brain?: Development of a system for the large-scale recording of retinal output activity. Institute of Electrical and Electronics Engineers Transactions on Nuclear Science, 51(4), 1434–1440.
Liu, Y., Jiang, Y., Xu, J., & Liao, W. (2023). Evolution of Avian eye size is associated with habitat openness, food type and brain size. Animals, 13(10), 1675.
Marshall, J., Mellerio, J., & Palmer, D. A. (1973). A schematic eye for the pigeon. Vision Research, 13(12), 2449–2453.
Moore, J. W., Joyner, R. W., Brill, M. H., Waxman, S. D., & Najar-Joa, M. (1978). Simulations of conduction in uniform myelinated fibers. Relative sensitivity to changes in nodal and internodal parameters. Biophysical Journal, 21(2), 147–160.
Nakazawa, T., Tachi, S., Aikawa, E., & Ihnuma, M. (1993). Formation of the myelinated nerve fiber layer in the chicken retina. Glia, 8(2), 114–121.
O’Brien, B. J., Caldwell, J. H., Ehring, G. R., Bumsted O’Brien, K. M., Luo, S., & Levinson, S. R. (2008). Tetrodotoxin-resistant voltage-gated sodium channels and are expressed in the retina. The Journal of Comparative Neurology, 508(6), 940–951.
O’Halloran, K. D. (2024). Update on requirements for ethics and welfare reporting in The Journal of Physiology. The Journal of Physiology, 602(10), 2149–2151.
Perge, J. A., Koch, K., Miller, R., Sterling, P., & Balasubramanian, V. (2009). How the optic nerve allocates space, energy capacity, and information. The Journal of Neuroscience, 29(24), 7917–7928.
Potier, S., Mitkus, M., & Kelber, A. (2020). Visual adaptations of diurnal and nocturnal raptors. Seminars in Cell & Developmental Biology, 106, 116–126.
Prinzinger, R., Preßmar, A., & Schleucher, E. (1991). Body temperature in birds. Comparative Biochemistry and Physiology Part A: Physiology, 99(4), 499–506.
Pumphrey, R., & Young, J. (1938). The rates of conduction of nerve fibres of various diameters in cephalopods. The Journal of Experimental Biology, 15(4), 453–466.
Radivojevic, M., Franke, F., Altermatt, M., Müller, J., Hierlemann, A., & Bakkum, D. J. (2017). Tracking individual action potentials throughout mammalian axonal arbors. eLife, 6, e30198.
Rasband, M. N., Peles, E., Trimmer, J. S., Levinson, S. R., Lux, S. E., & Shrager, P. (1999). Dependence of nodal sodium channel clustering on paranodal axoglial contact in the developing CNS. The Journal of Neuroscience, 19(17), 7516–7528.
Rashotte, M. E., Basco, P. S., & Henderson, R. P. (1995). Daily cycles in body temperature, metabolic rate, and substrate utilization in pigeons: Influence of amount and timing of food consumption. Physiology & Behavior, 57(4), 731–746.
Rashotte, M. E., Saarela, S., Henderson, R. P., & Hohtola, E. (1999). Shivering and digestion-related thermogenesis in pigeons during dark phase. American Journal of Physiology-Regulatory, Integrative and Comparative Physiology, 277(6), R1579–R1587.
Savory, C. J., Kostal, L., & Nevison, I. M. (2006). Circadian variation in heart rate, blood pressure, body temperature and EEG of immature broiler breeder chickens in restricted-fed and ad libitum-fed states. British Poultry Science, 47(5), 599–606.
Schmidt, H., & Knösche, T. R. (2019). Action potential propagation and synchronisation in myelinated axons. PLoS Computational Biology, 15(10), e1007004.
Schnitzer, J. (1985). Distribution and immunoreactivity of glia in the retina of the rabbit. The Journal of Comparative Neurology, 240(2), 128–142.
Seidl, A. H., Rubel, E. W., & Harris, D. M. (2010). Mechanisms for adjusting interaural time differences to achieve binaural coincidence detection. The Journal of Neuroscience, 30(1), 70–80.
Seifert, M., Roberts, P. A., Kafetzis, G., Osorio, D., & Baden, T. (2023). Birds multiplex spectral and temporal visual information via retinal on- and off-channels. Nature Communications, 14(1), 5308.
Seo, J. H., Haam, Y. G., Park, S. W., Kim, D. W., Jeon, G. S., Lee, C., Hwang, D. H., Kim, Y. S., & Cho, S. S. (2001). Oligodendroglia in the avian retina: Immunocytochemical demonstration in the adult bird. Journal of Neuroscience Research, 65(2), 173–183.
Shimmura, T., Ohashi, S., & Yoshimura, T. (2015). The highest-ranking rooster has priority to announce the break of dawn. Scientific Reports, 5(1), 11683.
Sköld-Chiriac, S., Nord, A., Tobler, M., Nilsson, J.-Å., & Hasselquist, D. (2015). Body temperature changes during simulated bacterial infection in a songbird: Fever at night and hypothermia during the day. Journal of Experimental Biology, 218(18), 2961–2969.
Stanford, L. R. (1987). Conduction velocity variations minimize conduction time differences among retinal ganglion cell axons. Science, 238(4825), 358–360.
Stett, A., Barth, W., Weiss, S., Haemmerle, H., & Zrenner, E. (2000). Electrical multisite stimulation of the isolated chicken retina. Vision Research, 40(13), 1785–1795.
Stone, J., & Freeman, R. B. (1971). Conduction velocity groups in the cat’s optic nerve classified according to their retinal origin. Experimental Brain Research, 13(5), 489–497.
Swadlow, H. A. (1990). Efferent neurons and suspected interneurons in S-1 forelimb representation of the awake rabbit: Receptive fields and axonal properties. Journal of Neurophysiology, 63(6), 1477–1498.
Swadlow, H. A., & Weyand, T. G. (1985). Receptive-field and axonal properties of neurons in the dorsal lateral geniculate nucleus of awake unparalyzed rabbits. Journal of Neurophysiology, 54(1), 168–183.
Takahashi, K. (1965). Slow and fast groups of pyramidal tract cells and their respective membrane properties. Journal of Neurophysiology, 28(5), 908–924.
Thorne, P. S., Yeske, C. P., & Karol, M. H. (1987). Monitoring guinea pig core temperature by telemetry during inhalation exposures. Fundamental and Applied Toxicology, 9(3), 398–408.
Underwood, H., Steele, C. T., & Zivkovic, B. (1999). Effects of fasting on the circadian body temperature rhythm of Japanese quail. Physiology & Behavior, 66(1), 137–143.
Vagionitis, S., Auer, F., Xiao, Y., Almeida, R. G., Lyons, D. A., & Czopka, T. (2022). Clusters of neuronal neurofascin prefigure the position of a subset of nodes of Ranvier along individual central nervous system axons in vivo. Cell Reports, 38(7), 110366.
van der Vinne, V., Pothecary, C. A., Wilcox, S. L., McKillop, L. E., Benson, L. A., Kolpakova, J., Tam, S. K. E., Krone, L. B., Fisk, A. S., Wilson, T. S., Yamagata, T., Cantley, J., Vyazovskiy, V. V., & Peirson, S. N. (2020). Continuous and non-invasive thermography of mouse skin accurately describes core body temperature patterns, but not absolute core temperature. Scientific Reports, 10(1), 20680.
Van Hook, M. J., Nawy, S., & Thoreson, W. B. (2019). Voltageand calcium-gated ion channels of neurons in the vertebrate retina. Progress in Retinal and Eye Research, 72, 100760.
Vaney, D. I. (1980). A quantitative comparison between the ganglion cell populations and axonal outflows of the visual streak and periphery of the rabbit retina. The Journal of Comparative Neurology, 189(2), 215–233.
Vizoso, A. D., & Young, J. Z. (1948). Internode length and fibre diameter in developing and regenerating nerves. Journal of Anatomy, 82(Pt 1–2), 110–134.
Waxman, S. G. (1980). Determinants of conduction velocity in myelinated nerve fibers. Muscle & Nerve, 3(2), 141–150.
Waxman, S. G., & Bennett, M. V. (1972). Relative conduction velocities of small myelinated and non-myelinated fibres in the central nervous system. Nature: New Biology, 238(85), 217–219.
Wilson, M., & Lindstrom, S. H. (2011). What the bird’s brain tells the bird’s eye: The function of descending input to the avian retina. Visual Neuroscience, 28(4), 337–350.
Witkovsky, P. (1971). Synapses made by myelinated fibers running to teleost and elasmobranch retinas. The Journal of Comparative Neurology, 142(2), 205–221.
Wolburg, H. (1980). Myelinated axons of ganglion cells in the retinae of teleosts. Cell and Tissue Research, 210(3), 517–520.
Won, M. H., Kang, T.-C., & Cho, S. S. (2000). Glial cells in the bird retina. Microscopy Research and Technique, 50(2), 151–160.
Yasumoto, Y., Nakao, R., & Oishi, K. (2015). Free access to a running-wheel advances the phase of behavioral and physiological circadian rhythms and peripheral molecular clocks in mice. PLoS ONE, 10(1), e0116476.
Zagkle, E., Grosiak, M., Bauchinger, U., & Sadowska, E. T. (2020). Rest-phase hypothermia reveals a link between aging and oxidative stress: A novel hypothesis. Frontiers in Physiology, 11, 575060.
Zeck, G., Lambacher, A., & Fromherz, P. (2011). Axonal transmission in the retina introduces a small dispersion of relative timing in the ganglion cell population response. PLoS ONE, 6(6), e20810.