¶ 神经元
¶ CXCR4相关原发性免疫缺陷中结构和精神运动缺陷的神经发育起源
¶ 原文下载:25415oa_origin.pdf
¶ 亮点
• IEI基因在人类发育中的大脑中表现出区域和阶段特异性表达
• WHIM突变改变小脑祖细胞动态,导致行为缺陷
• 早期靶向脑部的CXCR4抑制可挽救形态和功能结果
¶ 简而言之
Demenego等人表明,免疫缺陷先天错误(IEI)可独立于免疫功能障碍直接影响神经发育。在WHIM综合征中,CXCR4的过度激活通过细胞内在机制破坏小脑的组装和功能。早期以大脑为靶点的CXCR4拮抗剂可挽救结构和精神运动缺陷。这项研究重新定义了IEI相关症状的神经发育起源。
¶ CXCR4相关原发性免疫缺陷中结构和精神运动缺陷的神经发育起源
朱利亚·德梅涅戈、1,2萨拉·曼奇内利、1,2安东内拉·博雷卡、3,4罗萨尔巴·奥尔加·普罗塞、2,5a、1,2马特奥·米奥托、2马尔科·克雷莫内西、6劳拉·祖切利、1艾琳·科拉迪尼、4,5尤金·金、7卡塔琳娜·伊利奇、7爱德华多·弗拉维加、1,4卢卡·佩莱格里诺、1,8拉斐尔·巴多拉托、9罗伯托·鲁斯科尼、1,8达维德·波齐、1,4马里诺斯·卡利库尔迪斯、1,6戴安娜·卡什、7米凯拉·马特奥利、1,4和西蒙娜·洛达多1,2,10,*
1 意大利罗扎诺市,人道主义大学,生物医学科学系
2 神经发育生物学实验室,IRCCS Humanitas研究医院,意大利罗扎诺
3 意大利罗马国家研究委员会神经科学研究所
4 药理学与脑病理学实验室,IRCCS 胡马尼塔斯研究医院,意大利罗扎诺
5 德国柏林亥姆霍兹联合会马克斯·德尔布吕克分子医学中心
6 意大利罗扎诺IRCCS Humanitas研究医院适应性免疫实验室
7 英国伦敦国王学院精神病学、心理学与神经科学研究所神经影像科
8 应用物理、生物物理与微流控实验室,IRCCS 胡马尼塔斯研究医院,意大利罗扎诺
9 儿科诊所与A.诺奇韦利分子医学研究所,布雷西亚大学布雷西亚市民医院临床与实验科学系,意大利布雷西亚
10 主要联系人
* 通信:simona.lodato@hunimed.eu
https://doi.org/10.1016/j.neuron.2025.05.016
¶ 摘要
免疫缺陷先天性疾病(IEI)作为先天性慢性疾病,常与神经行为症状相关,传统上认为这些症状是患者负担的继发性表现。然而,其起源尚未得到阐明。本研究发现,IEI相关基因在人类大脑发育过程中会在神经谱系中表达,且在没有免疫挑战的情况下,IEI突变会直接损害神经发育轨迹,导致精神运动缺陷。带有导致Cxcr4过度激活突变的疣-低丙种球蛋白血症-免疫缺陷-髓系细胞滞留(WHIM)小鼠,表现出小脑发育性叶形成缺陷,这与感觉运动和情感功能障碍相关,重现了患者中描述的异常。对WHIM小鼠小脑的单细胞分析显示,颗粒细胞前体存在主要的转录失调,其异常增殖和迁移会引发叶形成和回路缺陷。脑室内注射AMD3100可挽救形态和行为缺陷,表明这些缺陷源于大脑特异性且依赖Cxcr4的机制。总之,我们的研究结果强调了精神运动性IEI表现背后神经发育影响的相关性,将我们对这些疾病的理解从免疫功能障碍扩展到了更广泛的层面。
¶ 引言
神经系统和免疫系统之间的相互作用是相互的、受到严格调控的,并且对维持生理稳态至关重要。1,2 越来越多的证据表明,在正常情况下,免疫系统会影响大脑的发育和功能,3 而神经免疫通讯的中断则会导致一系列疾病,包括神经发育障碍、4–9 精神疾病、4,6,10,11 以及神经退行性疾病。12–15 此外,患有慢性炎症性疾病(如炎症性肠病、16,1 银屑病、18,19 和类风湿关节炎20–23)的个体,常常会出现焦虑和抑郁等共病症状——这些症状通常被认为是其潜在免疫功能障碍的继发表现。
免疫缺陷先天错误(IEI)是一类遗传性疾病,其特征是免疫系统组成部分出现部分或完全功能障碍。24-26 这类患者对感染和恶性肿瘤的易感性增高,常伴有复杂的合并症。27,28 重要的是,IEI患者还表现出更高的神经精神症状发生率,尤其是焦虑和抑郁。26,29-32 这些表现是慢性免疫失调的间接后果,还是直接由影响大脑发育的潜在基因突变导致,目前尚未明确,这在很大程度上是由于建模方面的挑战以及跨学科研究的有限性。
在免疫缺陷性肠病(IEI)中,疣、低丙种球蛋白血症、免疫缺陷、骨髓粒细胞滞留(WHIM)综合征的特征是反复感染、骨质疏松和心脏缺陷。33-39 最近对一小群WHIM患者进行的神经影像学和神经精神病学评估显示,患者在运动协调方面存在细微但持续的缺陷,包括精细和粗大运动功能障碍以及共济失调,同时还伴有焦虑、抑郁和社交退缩。40 值得注意的是,磁共振成像(MRI)显示66%的病例存在非典型小脑 foliation,尤其影响下半球,伴有异常的层状方向。40 虽然这些观察结果表明小脑参与了WHIM的病理过程,但两者之间的机械联系尚未建立。
WHIM综合征由CXC趋化因子受体4(CXCR4)的常染色体显性突变引起,具体是该基因的C端胞质域发生突变(OMIM:#193670)。35,41 CXCR4会被其配体CXC趋化因子配体12(CXCL12)特异性激活,42 结合后会发生构象变化,启动下游信号级联反应,调控细胞迁移和增殖。在正常情况下,β-抑制蛋白介导的受体内吞确保CXCR4信号传导受到控制。43 而在WHIM综合征中,这种内吞作用受损,导致受体在细胞表面的暴露时间延长,即CXCR4过度激活,39,42 并导致造血干细胞41 以及骨髓中的成熟中性粒细胞出现滞留缺陷。35
目前用于WHIM综合征的治疗方法范围广泛且费用高昂,这凸显了迫切的医疗需求。CXCR4拮抗剂普乐沙福(AMD3100)的III期试验已显示出在增加循环白细胞亚群方面的疗效。44-46然而,这些试验仅纳入了10岁以上的个体,尽管有证据表明WHIM症状从出生时就存在,且早期干预的潜在益处(尤其是对非免疫表现)仍不明确。
在本研究中,我们揭示了与免疫缺陷性疾病(IEI)相关的精神运动障碍存在神经发育学起源,将这些表型与全身性免疫功能障碍区分开来。我们发现,IEI相关基因在早期大脑发育过程中会在小脑神经谱系中活跃表达。通过利用WHIM小鼠模型,我们证明Cxcr4的过度激活会直接损害小脑细胞结构,引发持久的行为和功能缺陷,这些缺陷与临床观察结果相符。最后,我们发现早期脑室内注射普乐沙福能够挽救WHIM小鼠的结构和行为缺陷,确立了脑内源性Cxcr4功能障碍与神经行为症状之间的直接联系。
¶ 结果
¶ 与免疫失调性肠病相关的基因在人类发育中的大脑中呈现出时间和区域特异性的表达模式
IEI患者会出现早发性损伤,且不仅限于免疫系统功能障碍。47尽管许多神经学改变都与IEI相关,32,48-50但人们对其程度仍缺乏全面的了解。通过利用经过验证的IEI相关基因分类,27,28我们整理出了517种IEI病症、其446个致病基因(呈现出独特的病理变异)以及相关的临床特征,包括在有资料的情况下对所报道的神经症状的详细描述(表S1)。这种方法使我们能够系统地绘制与IEI相关的神经缺陷的发生频率和范围。我们发现,41.6%的IEI与智力障碍、51-53神经发育迟缓与小头畸形、54-56焦虑57-60以及复发性脑病等相关,即便没有明显的病毒感染表现也是如此61-64(图1A),这表明IEI基因可能会影响神经发育。因此,我们利用BrainSpan数据集65来研究IEI基因在人类大脑中的表达,该数据集是一个全面的资源,提供了不同脑区和发育阶段的基因表达模式。通过对IEI基因进行层次聚类(数据集中存在446个致病基因中的444个,图S1A),我们在所有被分析的区域中确定了三个基因子集,它们表现出IEI基因的时间特异性表达模式(图1B和图S1A)。有趣的是,一个子集在产前和婴儿早期阶段富集(早期);另一个子集在婴儿晚期达到峰值(中期);最后一个子集从儿童期到成年期富集(晚期)(图1B和图S1A;表S2)。在不同脑区中,小脑(CB)和thalamus(TH)的IEI基因表达量最高。CB中富集的IEI基因数量是TH中观察到的两倍多(图1C、图S1A和图S1B),这表明CB可能特别容易受到IEI突变的影响。
因此,我们利用了最近发表的人类小脑单核RNA测序数据集66,以单细胞分辨率研究免疫缺陷(IEI)基因的表达模式。我们分析了来自健康供体小脑 的143,390个细胞核,涵盖从受孕后7周(pcw)到幼儿期(2.8-3.5岁)的9个发育阶段,并检查了IEI基因的表达(图1D-1F和S1C-S1E)。单核分析证实了人类小脑成熟过程中不同时间点和谱系的细胞异质性(图1E和1F)。67-70 86%的IEI相关基因在该数据集中表达,并具有特定的表达动态(表S2):23%属于BrainSpan小脑(CB)簇,22%属于早期簇,22%属于中期簇,8%属于TH簇,7%属于晚期簇。这一结果进一步证实了之前观察到的在早期、中期和CB簇中的富集现象。IEI基因在实质内的常驻免疫细胞类型和脑血管中循环的免疫细胞类型中均有表达(图1G、40个变异最大的基因和S1F)。然而,只有一小部分基因是免疫谱系所特有的(例如PTPRC和IKZF1),并且我们在神经细胞中也检测到了IEI基因(图1G)。我们发现了一些在大脑发育和成熟过程中具有已知表达和作用的基因,例如核因子κB亚基1(NFKB1)、71,72 B细胞淋巴瘤/白血病转录因子11B(BCL11B)73-75 和CXC趋化因子受体4(CXCR4),76,77 它们分别与NfkB1缺陷、Bcl11b缺陷和WHIM综合征相关,这些疾病均表现出神经系统症状(表S1和S2)。有趣的是,一些IEI基因(25个基因,例如BCL11B、PRKDC和CARD11B)也存在于西蒙斯基金会自闭症研究计划(SFARI)数据库中,并具有较高的置信度评分78(表S2),这凸显了它们在神经发育障碍中的作用。总体而言,这种模式表明IEI相关基因在人类发育中大脑的不同细胞类型中具有更广泛的作用。
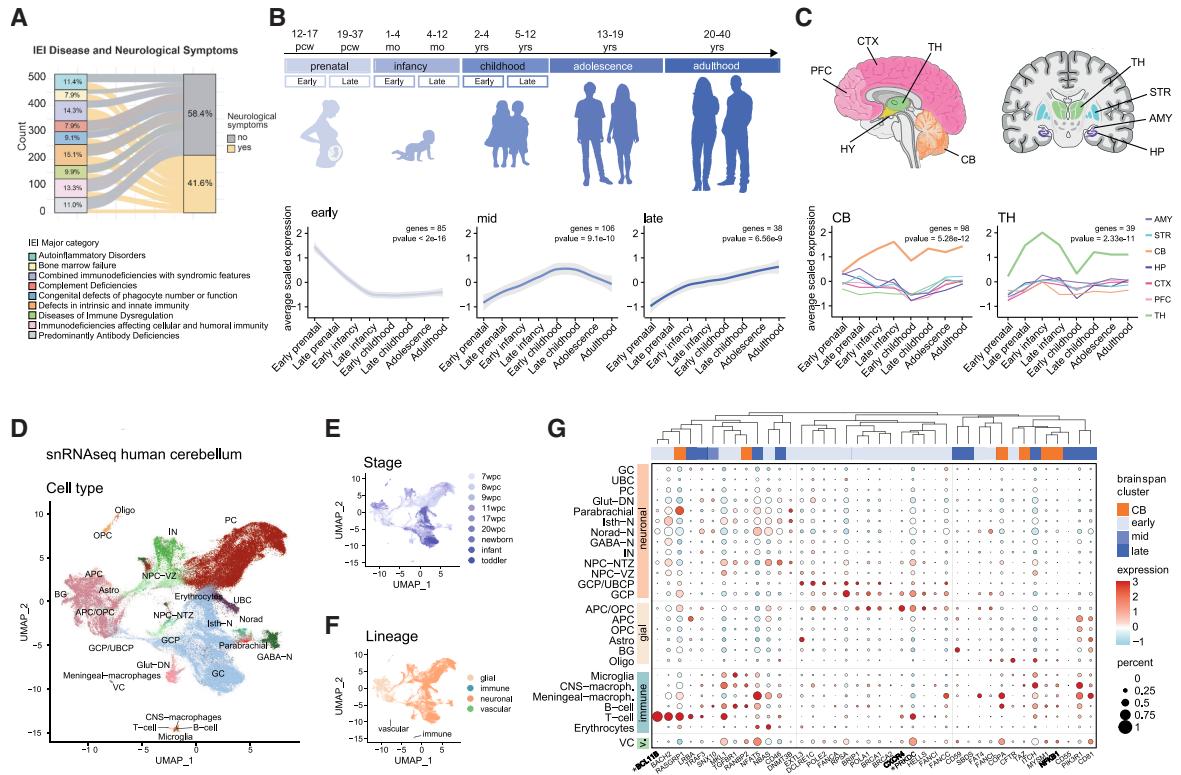
图1. 与免疫缺陷相关的基因在人类发育中的大脑中表现出时间和区域特异性表达模式
(A) 冲积图显示了各临床主要免疫缺陷病(IEI)类别中伴有神经系统症状的IEI的百分比。
(B) 人类发育时间点的示意图以及显示时间特异性表达模式的基因平均标准化表达的线图(早期,85个基因,p < 2e−16;中期,106个基因,p = 9.1e−10;晚期,38个基因,p = 6.56e−9)。
© 人类大脑切片示意图,显示组织定位以及具有组织特异性表达模式的基因的平均缩放表达折线图(CB,98个基因,p = 5.28e−12;TH,39个基因,p = 2.33e−11)。
(D) 按细胞类型着色的UMAP,展示来自健康供体小脑的单个细胞核。66
(E和F)UMAP显示单个细胞核按发育阶段和谱系着色。
(G) 显示选定IEI基因亚型特异性表达的点阵图。
*表示SFARI数据库中存在的基因。
¶ 磁共振成像显示WHIM小鼠小脑结构存在选择性改变
为了研究免疫缺陷(IEI)的遗传改变如何影响大脑组装,我们利用了成熟的小鼠模型,该模型携带与WHIM综合征相关的杂合CXCR4S338X突变(Cxcr4+/1013或WHIM),已被广泛用于表征免疫和骨骼缺陷。33,36,38,39,79–82
鉴于在WHIM患者中观察到的结构改变,我们对出生后第45天的WHIM小鼠和对照小鼠的大脑进行了MRI检查(图2A和图S2A)。离体MRI体素分析显示,WHIM小鼠的小脑存在选择性结构改变(图2A和图S2A;表S3和表S4)。最明显的缺陷出现在蚓部,我们观察到分隔LIV-V和LVI的原裂(fpr)处体积显著增加,而分隔LIV-V和LIII的前顶裂(fpc)处体积显著减少(图2A和图S2A)。由小脑传入和传出投射组成的白质树突状分支长度在LIII和LIX中减少(图2B),这表明Cxcr4+/1013小鼠中往返于小脑的感觉运动信息传导通路发生了变化。
随后,我们通过对P45动物进行尼氏染色来评估小脑的细胞结构。当测量浦肯野细胞层(PCL)的长度时(浦肯野细胞层由沿小脑小叶排成一行的浦肯野细胞(PCs)定义67),我们观察到在蚓部水平的LIII、LVIII和LIX区域,WHIM小鼠的小脑出现了缩短(图2C和图S2B)。我们还评估了不同耳间平面的半球中的浦肯野细胞层,发现多个小叶存在显著缩短,包括旁正中小叶(PML,图2C和图S2B)。值得注意的是,啮齿动物的旁正中小叶在解剖学上被认为与人类的薄小叶相匹配83,而薄小叶是WHIM患者中小脑改变最明显的区域40。
这些数据共同表明,WHIM小鼠存在区域性小脑异常和选择性分叶缺陷,这与WHIM患者中报道的情况极为相似。
¶ WHIM突变体表现出早发性行为改变,并对焦虑相关表型产生持久影响
因此,我们研究了WHIM突变体中异常的形态缺陷是否会导致行为改变。首先,我们在旷场实验箱中评估了WHIM小鼠的活动情况(图2D)。它们表现出更强的趋壁性(倾向于停留在靠近墙壁的地方,图2D),并且在周边区域的移动时间显著增加(图S2C),同时减少了在中央区域的休息时间(图S2C)。与对照组相比,它们的垂直活动次数更少(图2D),移动距离更短,速度也更慢(图S2C)。
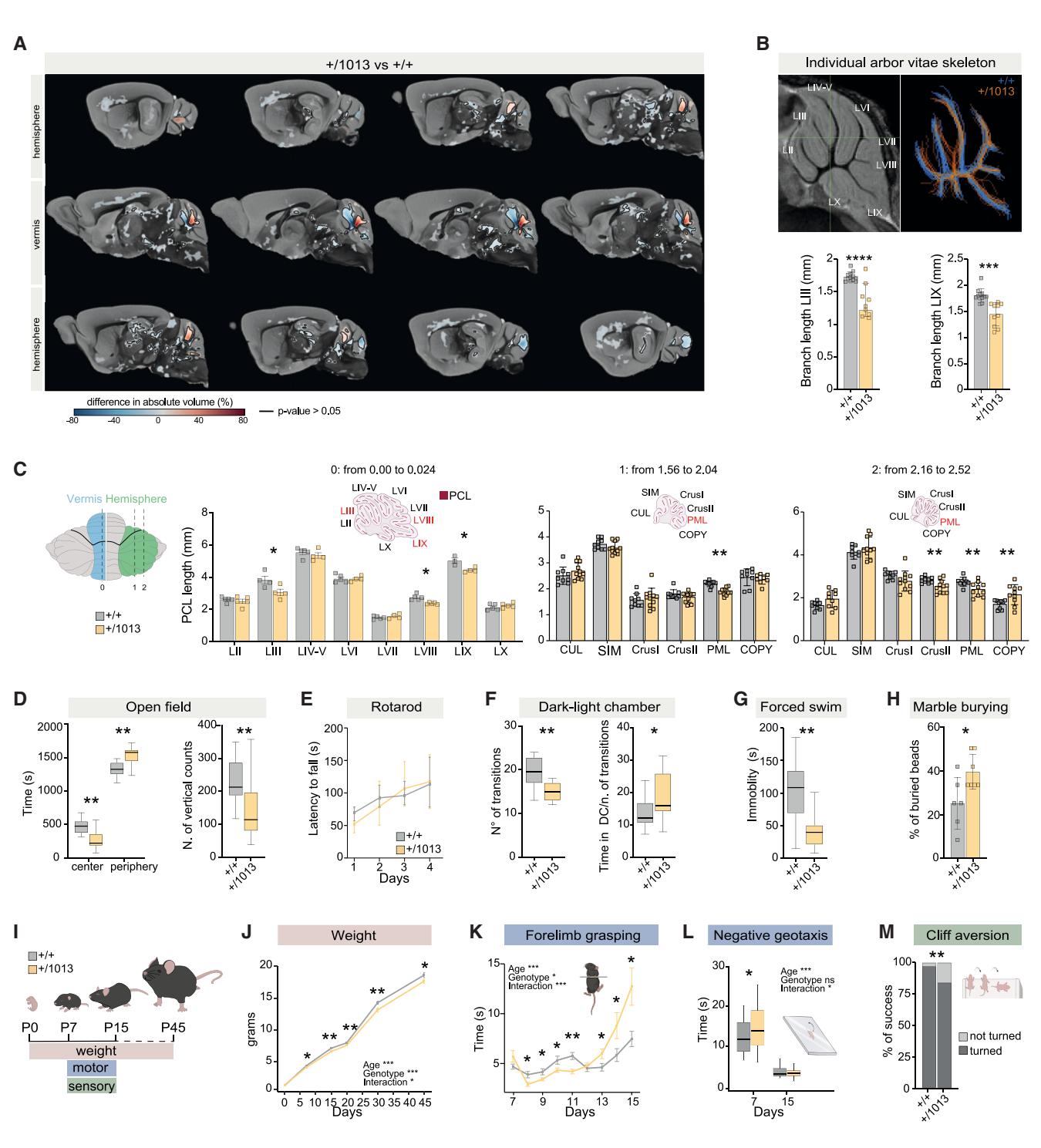
图2. WHIM突变体表现出小脑形态改变和类焦虑行为表型
(A)小脑脑容量的体素级比较显示,P45 WHIM小鼠存在明显的形态异常。红色:WHIM小鼠大于对照组;蓝色:WHIM小鼠小于对照组;黑色轮廓:经FWE校正后*p < 0.05的区域;每组n > 9只动物。
(B) 白质活树的二维骨架分析。**p < 0.01;每组n > 9只动物。
(C)小鼠小脑背侧示意图。 vermis和半球不同耳间水平的柱状图和矢状位小脑切片。多重t检验,*p < 0.05,**p < 0.01;n > 4只动物/条件。
(D)箱线图显示WHIM小鼠在竞技场中花费的时间和垂直计数的数量。Student’s t检验,**p < 0.01;n = 16只动物/条件。
(E)线图显示从加速转棒上跌落的潜伏期(秒)。双向方差分析,*p < 0.05;n = 11只动物/条件。
(F) 箱线图显示转换次数、暗箱停留时间与转换次数的比值。采用Student t检验,*p < 0.05,**p < 0.01;n = 16只动物/条件。
(G) 箱线图显示不动时间(秒)。Student t检验,**p < 0.01;n = 16只动物/条件。
(H) 柱状图显示被掩埋珠子的百分比。Student’s t检验,*p < 0.05;n > 6只动物/条件。
(I) 实验计划示意图。
(J) 折线图显示从P0到P45的体重。多重t检验,*p < 0.05,**p < 0.01;每个条件下n > 17只动物。
(K) 线图显示幼崽抓住棍子的时间。多重t检验,*p < 0.05;n > 14只动物/条件。
(L) 箱线图量化幼崽转身并面向上方所需的时间。多重t检验,*p < 0.05;每个条件下n > 30只动物。
(M) 柱状图显示转身离开悬崖的幼崽百分比。多重t检验,**p < 0.01;n > 30只动物/条件。
为了具体评估Cxcr4+/1013小鼠是否表现出运动表型的改变,我们进行了加速旋转棒测试。我们观察到WHIM小鼠和对照小鼠之间的跌落潜伏期没有显著差异(图2E和图S2D),这表明Cxcr4+/1013小鼠在旷场试验中表现出的活动异常并非由运动缺陷引起,而是提示存在类焦虑表型。事实上,在明暗箱试验中,Cxcr4+/1013小鼠的探索行为减少,表现为箱间过渡次数减少以及在暗箱中停留时间增加(图2F)。此外,在强迫游泳试验中,它们的不动时间缩短(图2G),这提示存在与焦虑相关的应对策略功能障碍。84在自我修饰试验中未发现差异(图S2E);然而,观察到埋大理石行为显著增加(图2H)。总体而言,这些数据表明Cxcr4+/1013小鼠存在类焦虑行为。
为了了解Cxcr4过度激活对感觉和运动发育的影响,我们采用了一套从Fox量表改编而来的标准化测试组合(图2I-2M和图S3)。与同窝对照幼鼠相比,WHIM幼鼠从出生后第7天起体重更低(图2J)。它们在移动能力测试(图S3B)和空中翻正测试(图S3E)中未表现出运动缺陷。然而,它们在旷场穿越测试(图S3C)和地面翻正测试(图S3D)中表现出短暂的显著差异。此外,WHIM幼鼠在前肢抓握测试中表现出行为受损(图2K),这表明其神经肌肉发育存在延迟。通过负趋地性测试测量发现,它们对重力前庭线索的运动反应较慢,这证实了其协调性和方向性存在损伤(图2L)。另外,在耳颤测试(图S3F)和听觉惊跳测试(图S3G)中发现,它们对感觉和听觉刺激的反应存在延迟。同样,用于评估由感觉刺激驱动的运动输出整合能力的悬崖回避测试显示,WHIM幼鼠的反应存在缺陷(图2M)。总之,我们的研究结果表明,Cxcr4+/1013幼鼠的身体、感觉和运动发育轨迹异于正常。
总体而言,我们的分析表明,WHIM小鼠表现出类似焦虑的表型,与WHIM患者中报告的表型相似。40我们的研究结果还表明,Cxcr4的过度激活会破坏新出现的神经回路的发育,导致出生后早期发育阶段的运动协调和感觉整合出现缺陷。这些发现为Cxcr4在神经发育障碍中的作用提供了新的见解。
¶ WHIM小脑结构损伤起源于产前早期阶段
小脑神经元回路对复杂功能的正常执行至关重要,它源于出生后长期的神经发生和高度协调的迁移过程。我们随后试图研究在WHIM突变体中观察到的小叶形成缺陷是否反映了小脑组装早期的改变。我们测量了成年(P45)、出生后早期(P7)和新生(P0)小鼠小脑蚓部水平上划分不同小叶的小脑裂长度(图3A)。在每个阶段,我们都观察到一致的大体形态改变,与同窝小鼠相比,WHIM小鼠的原裂(fpc)、次裂(fpr)和次级裂(fsec,分隔第Ⅷ小叶和第Ⅸ小叶)长度显著缩短(图3B和图S4A),这表明Cxcr4突变严重影响小脑结构。
在发育中的小脑中,外颗粒层(EGL)和内核区的生长速率不同,导致细胞密度存在差异。这一过程会驱动锚定中心(ACs)的形成以及随后的沟回延长。91为了深入了解小脑异常叶形成的潜在机制92,93,我们评估了WHIM突变体中EGL和核心区的正常差异性扩张情况。我们使用真正的标志物Pax6来评估Cxcr4+/1013小脑中颗粒细胞祖细胞(GCPs)和颗粒细胞(GCs)的密度与数量。研究发现,在叶形成之前(E16.5、E17.5;图3C-3E),WHIM小鼠小脑中Pax6+细胞的密度显著增加,而细胞总数未发生改变(图S4B)。值得注意的是,在E17.5时,这种变化可归因于小脑核心区Pax6+细胞密度的增加(图3F和S4C)。我们的结果与先前提出的解释发育中小脑折叠动态的表面褶皱模型一致,该模型表明EGL和核心区之间存在差异性扩张91,94。因此,我们利用一个用于软双层材料的数学模型95来解释E17.5和P0时小脑切片的形态测量数据,并描述褶皱不稳定性的演变(图3G)。在E17.5时,核心区细胞密度的增加会降低新生叶的振幅(图3H),这源于EGL和核心区之间刚度比的降低(图3I和S4D)。尽管在P0时观察到明显的形态变化(图3A和3C),但Pax6+细胞密度(图3C和3E)和褶皱分析(图S4E)均未出现差异。这些机械性改变导致了在WHIM突变体中观察到的异常折叠模式,并突显了颗粒细胞祖细胞行为在产前的关键动态变化。
¶ 单细胞测序分析揭示小脑前体细胞中过度活跃的Cxcr4信号传导
为了研究Cxcr4+/1013小鼠中观察到的异常叶片形成所涉及的细胞和分子基础,我们对P0期Cxcr4+/1013小鼠和对照组的显微切割小叶LIII-VI-V进行了单细胞RNA测序(图4A)。通过对10742个细胞进行分析(这些细胞在不同基因型间呈比例分布,图S5A-S5C),我们进行了无监督聚类,发现了26个聚类,它们被归为19种不同的细胞类型(图4B和图S5A-S5C)。与最近发表的数据集一致,我们识别出了颗粒前体细胞(GPC,标志物:Top2a、Mki67和Cxcr4)、双能前体细胞(BP,标志物:Glis3、Sox2和Pax3)、神经胶质生成前体(GP,标志物:Tnc、Slc4a4、Apoe和Aldh1l1)以及室管膜前体(epy,标志物:Spag17、Foxj1和Tmem212)。 我们还描绘了不同的兴奋性小脑神经元类型,包括单极刷细胞(UBC,富含Kirrel3、Eomes、Lmx1a)和颗粒细胞(GC,表达Reln、Neurod1、Eps8、St18)。发现了分子水平上不同的颗粒细胞前体亚群(GCP-A Top2a+和GCP-B Mfap4+)以及颗粒细胞亚群(GCI Neurod1+和GCII Cadps2+)。至于抑制性细胞类型,我们识别出了浦肯野细胞(PC,由Pcp2、Calb1标记)和中间神经元(IN,Gad1/2、Pax2、Slc6a5),包括表达生长抑素(Sst)的中间神经元亚群。此外,还识别出了峡部的神经元群体(峡部是小脑 和中脑之间的边界区域,峡部神经元,isth-N,富含Lhx9、Otx2和Asic4)以及小脑深部核团的γ-氨基丁酸能神经元(γ-aminobutyric acid [GABA] DN,富含Sox14、Gad1/2)。同时,还捕获到了非神经元细胞群体和中胚层衍生的细胞类型,包括小胶质细胞(Cx3cr1、Trem2)、血管细胞(Cldn5、Flt1、Cdh5和Pecam1)、脑膜内皮细胞(Cxcl12和Vtn)以及间充质细胞(Col1a1、Col3a1和Dcn)。
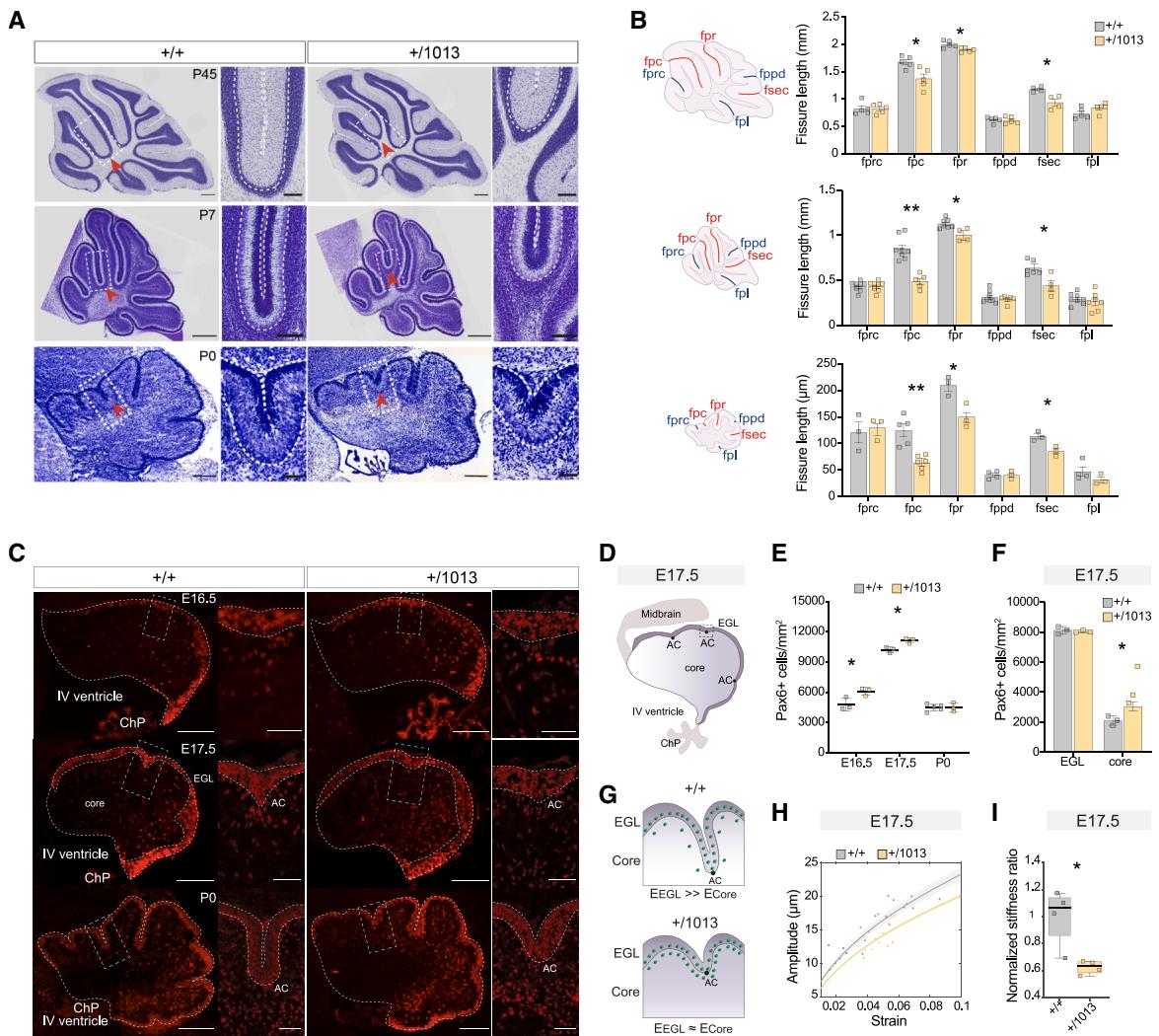
图3. WHIM突变体的小脑结构损伤起源于产前早期阶段
(A) P45、P7和P0时Cxcr4+/1013小鼠与对照小鼠的代表性矢状面尼氏染色切片。P45的标尺为500μm;局部放大图的标尺为120μm;P7和P0的标尺为200μm;局部放大图的标尺为50μm。
(B)P45、P7和P0时小鼠小脑矢状切片示意图,标注了脑沟名称,柱状图显示脑沟长度。多重t检验,*p < 0.05,**p < 0.01;n > 3只动物/条件。
(C)E16.5、E17.5和P0时期Cxcr4+/1013小鼠及对照小鼠小脑的代表性切片,用抗Pax6抗体染色。比例尺:200 μm;局部放大图比例尺:50 μm。
(D) E17.5小脑示意图,突出显示了外颗粒层(EGL)、核心和前联合(AC)。
(E) 点图显示E16.5、E17.5和P0时每平方毫米Pax6+细胞的数量。多重t检验,*p < 0.05;每组n > 3只动物。
(F) 柱状图显示E17.5时核心区和外颗粒层(EGL)中Pax6+细胞的数量(个/平方毫米)。多重t检验,*p < 0.05;每个条件下n > 3只动物。
(G) E17.5小脑叶片形成过程示意图。
(H) 在E17.5时折叠幅度减小,采用低变形起皱模型(实线)进行模拟。
(I)箱线图显示,E17.5时WHIM小鼠小脑的标准化刚度比降低。Student t检验,*p < 0.05;每组n > 3只动物。
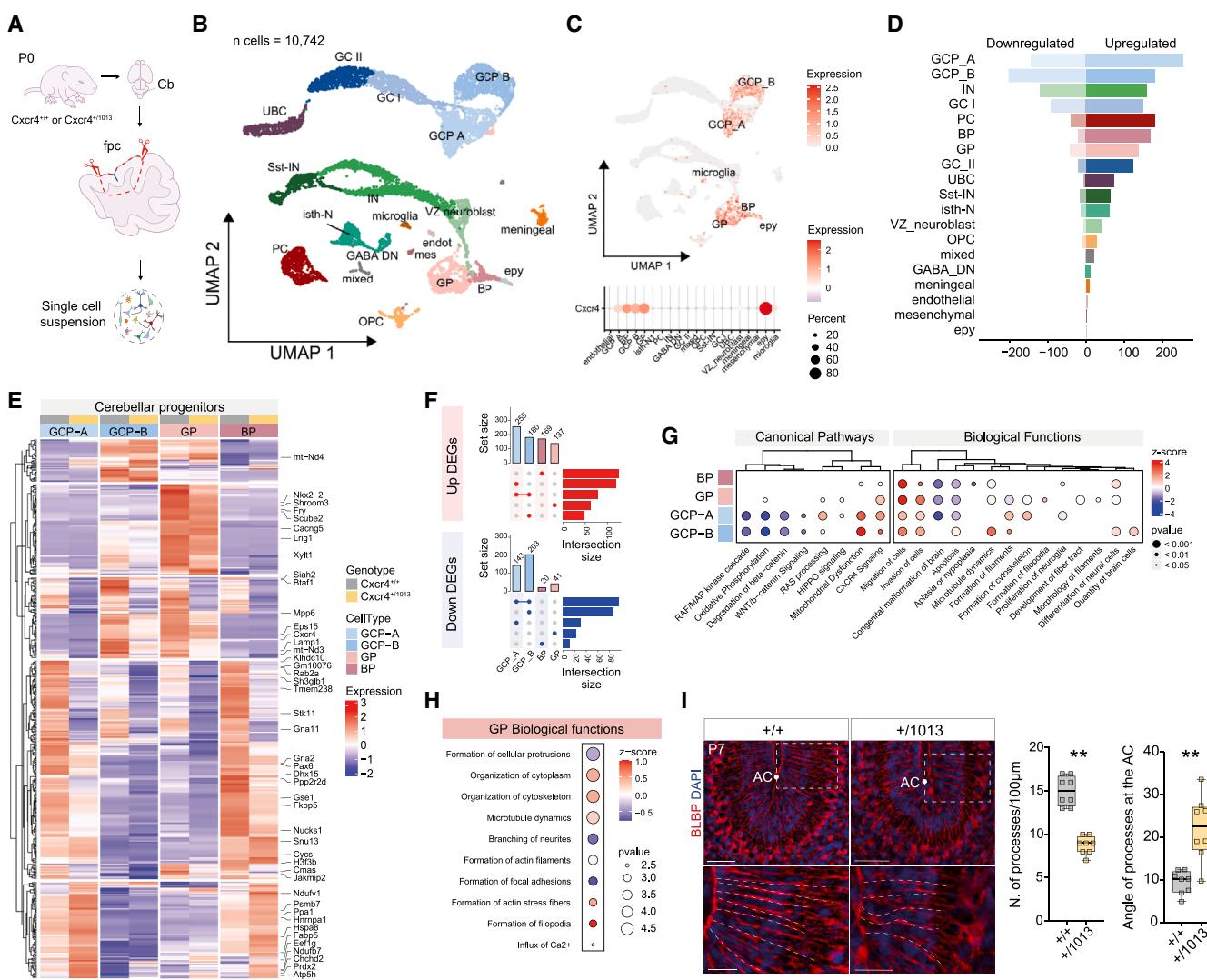
图4. 发育中小脑小叶的单细胞测序显示,颗粒细胞前体的Cxcr4信号过度活跃会导致异常迁移
(A) 实验方案。
(B) 按细胞类型着色的对照组和Cxcr4+/1013小脑的均匀流形逼近与投影(UMAP)测序。
(C)显示不同细胞类型中Cxcr4表达的特征图和点图。
(D) 条形图显示WHIM突变体中失调基因的数量,按细胞类型着色。MAST,*p < 0.05,平均log2倍变化 > 0.1。
(E) 热图显示具有代表性的最显著差异表达基因的标准化表达情况。
(F) upset图显示祖细胞中上调基因和下调基因之间的重叠程度。
(G和H)(G)小脑前体细胞中选定的失调经典通路和生物学功能的点阵图,以及(H)神经胶质生成祖细胞中的相关点阵图。
(I) P7小脑的代表性免疫荧光染色显示BLBP+纤维(红色)的方向,箱线图显示每100μm的突起数量以及在AC处突起的角度。学生t检验,*p < 0.05;n > 3只动物/条件。比例尺,50μm;裁剪图比例尺,25μm。
我们概述了Cxcr4的表达,并在GCPs、GPs、BPs、小胶质细胞和epy中对其进行了确认(图4C)。通过进行差异基因表达分析(图4D和4E),我们发现神经元和神经胶质祖细胞的转录足迹存在显著差异(表S5),同时伴随着神经元分子特征的改变。GCPs表现出最多数量的差异表达基因(DEGs);相比之下,isth-N、GABA-DN以及包括小胶质细胞在内的非神经细胞类型,尽管数量较少,但在WHIM小脑中显示出可忽略不计或无转录变化(图4D和4E)。在BP、GP和GCPs中观察到了不同的转录失调模式,而GCPs A和B共享多个失调基因(图4F),这表明WHIM小脑祖细胞中触发了谱系特异性反应。
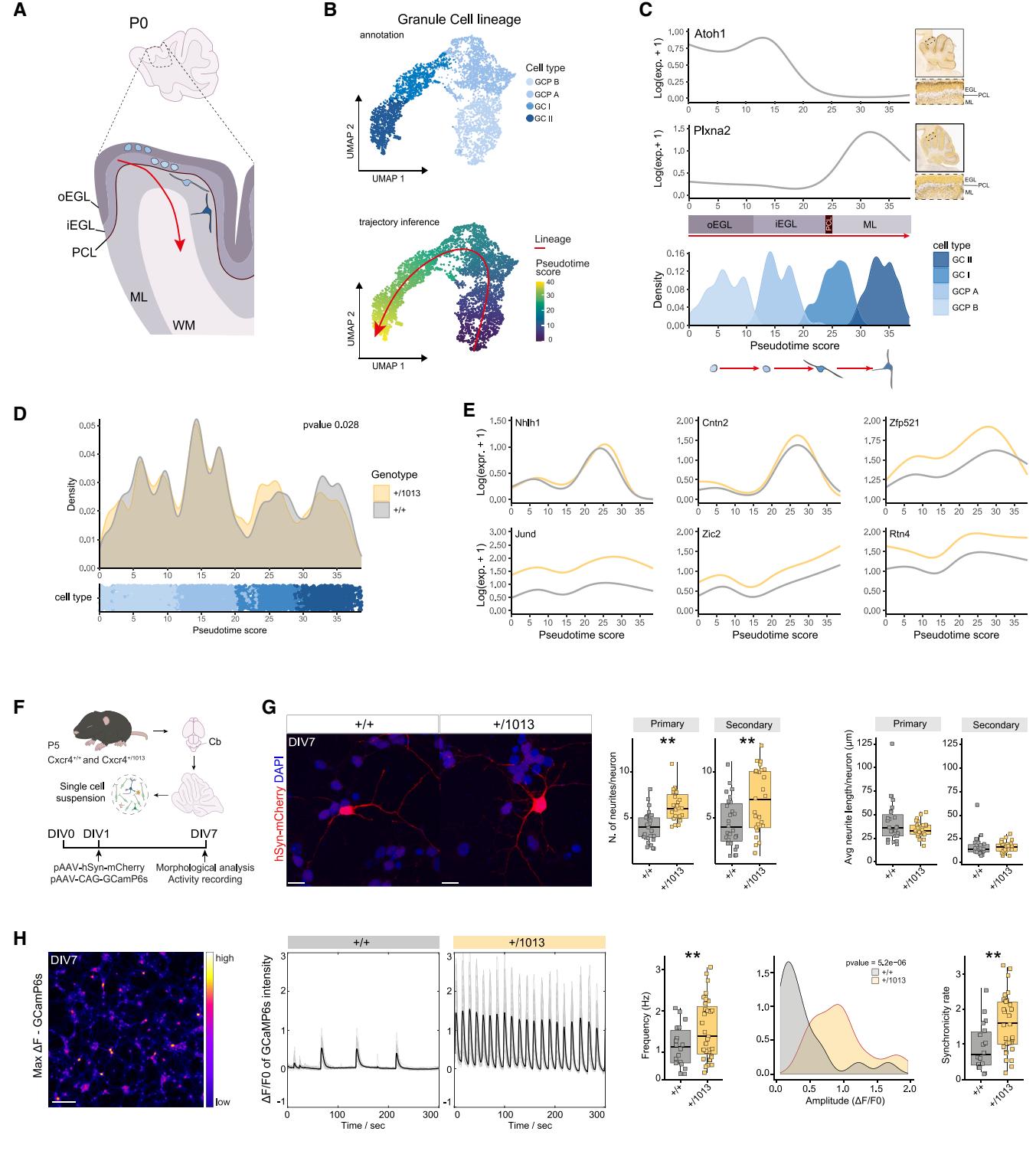
图5. 生发中心缺陷的产生与免疫表型无关
(A) 生发中心谱系发育示意图。
(B) 生发中心谱系的UMAP图,按细胞类型和伪时间评分着色,突出显示推断的轨迹(红色)。
(C)线图显示选定位置基因(Atoh1和Plxna2)在对照小脑中的表达,附带来自艾伦脑图谱的P4原位杂交(ISH)相关图像,以及密度图显示细胞沿假时间的分布,按细胞类型着色。
(D) 细胞分布图显示了沿假时间分数的细胞密度,按基因型(上图,密度图,柯尔莫哥洛夫-斯米尔诺夫检验,p = 0.028)和细胞类型(下图,点图)着色。
(E) 线图显示Cxcr4+/1013小脑假时间内选定的上调基因的表达。
(F) 实验计划示意图。
(G) DIV7时Cxcr4+/1013和对照mCherry阳性GCs的代表性图像,箱线图显示神经突数量和长度的量化结果。Student t检验,*p < 0.05,**p < 0.01;n > 10个细胞/条件。比例尺,10 μm。
(H) DIV7时GCamP6s荧光的最大强度投影图像及代表性归一化轨迹(ΔF/F0)。箱线图显示了颗粒细胞(GCs)中单个神经元的尖峰频率和同步率的量化结果,密度图显示了不同基因型之间振幅值的分布。采用Student t检验,*p < 0.05,**p < 0.01;每个条件下n > 10个细胞。数据以平均值±标准误(SEM)表示。比例尺,100μm。
对祖细胞集群的富集分析揭示了Cxcr4信号通路广泛且协调的激活(图4G和图S5D;表S6),这凸显了其在增强细胞迁移和存活方面的潜在影响。为验证这一假设,我们对生物学功能进行了全面分析(使用 Ingenuity 通路分析),结果显示与增强迁移、侵袭和细胞骨架动态相关的术语显著富集(图4G;表S7),这为了解Cxcr4过度激活对小脑祖细胞的多方面影响提供了宝贵见解。
有趣的是,颗粒细胞前体(GPs)是伯格曼神经胶质细胞(BG)的前体——伯格曼神经胶质细胞是一种神经胶质亚型,在小脑表面形成小叶的过程中,其纤维会沿着每个裂隙(AC)的底部排列,充当向内迁移的颗粒细胞(GCs)的轨道94——它们显示出Cxcr4通路的上调,同时与细胞突起形成和细胞骨架组织相关的术语表达失调(图4G和4H)。为了验证在颗粒细胞前体中观察到的分子变化,我们使用脑脂质结合蛋白(BLBP)标志物进行免疫染色,以选择性标记伯格曼神经胶质细胞96。对BLBP+纤维的追踪分析显示,在出生后第7天(P7),Cxcr4+/1013突变体中伯格曼神经胶质细胞纤维的排列发生了改变:与对照组相比,WHIM小鼠分子层中BLBP+突起的数量显著减少,同时这些纤维在第三叶(LIII)和第四叶(LIV)之间的裂隙处形成的角度增大(图4H和4I)。伯格曼神经胶质细胞纤维这种非典型的扇形模式可能导致了小脑小叶发育的异常。
总体而言,我们的单细胞分析表明,Cxcr4突变在发育过程中会影响多种小脑祖细胞的情况,这支持其对不同谱系的分化存在直接作用。
¶ 过度活跃的Cxcr4信号传导影响颗粒细胞的分化和自发活动
鉴于在GCP中观察到的转录变化,我们研究了GCP衍生物(即成熟GCs,图5A)的分化和成熟是否在WHIM小鼠中受到影响。我们通过推断轨迹拓扑结构并进行伪时间分析,研究了颗粒细胞谱系的发育路径(图5B)。我们确定了GCP-B是一个共同的起点(根)——该集群的熵值最高,意味着分化水平最低97(图S5E)——轨迹从这里经过GCP-A和GCI,最终终止于GCII(图5B、5C和S5F)。在Cxcr4+/1013小鼠和对照组之间,未观察到谱系拓扑结构的变化(图5B)。
值得注意的是,GCPs起源于菱形唇,迁移至外颗粒层(EGL),随后向内移动至内颗粒层(IGL),并在此过程中分化为成熟的颗粒细胞(GCs)92(示意图见图5A)。已知这一发育轨迹与基因表达的动态变化相关,这些变化标志着沿小脑皮质层迁移的GCs所处的分化阶段98。我们的拟时序分析证实,位置特异性标志物(如Atoh1和Plxna2)的表达模式遵循一定的分化序列,该序列与GCs沿其发育轨迹的分布相对应(图5C和图S5F)。这使我们能够计算拟时序评分,将其作为分化和GC迁移的替代指标,同时评估不同基因型中的这两个过程。我们观察到细胞分布存在显著差异,其中与GCI状态相关的频率存在分歧(拟时序评分20-30,图5D)。尽管Cxcr4仅在祖细胞中表达,但我们发现整个拟时序轨迹中都存在转录变化(图5D和图5E)。这些发现证实了我们之前关于WHIM小鼠中GCs迁移受损的观察结果(图3),同时还揭示了影响该谱系的更广泛的分化缺陷。
然而,目前尚不清楚迁移受阻是否会干扰分化进程,或者这两种损伤是否作为Cxcr4信号过度活跃的结果而独立发生。
为了开始厘清Cxcr4失调对颗粒细胞(GCs)的内在影响,我们从P5代Cxcr4+/1013小鼠和对照组小鼠的小脑中分离出颗粒细胞,并进行体外培养,从而排除了局部迁移信号的影响。在体外培养第1天(DIV1),我们用pAAV-hSyn-mCherry病毒感染颗粒细胞,以稀疏标记神经元用于形态学分析(图5F和5G),同时用pAAV-hSyn-GCaMP6s病毒感染,以观察其自发性电活动(图5F-5H)。在体外培养第7天(DIV7),我们观察到与对照组相比,Cxcr4+/1013神经元的初级和次级分支数量显著增加,而神经突长度保持不变(图5G),这表明Cxcr4失调对小脑神经元的形态复杂性有直接影响。在同一阶段,我们发现与对照组相比,WHIM综合征小鼠的颗粒细胞在多个神经元中的 spike频率和 spike同步率显著提高(图5H)。这些发现与先前的研究一致,即Cxcr4/Cxcl12信号通路的改变(如在Cxcr4敲除模型中)不仅影响神经元的定位,还影响其内在特性,如兴奋性、树突生长和突触可塑性。99
总的来说,我们的研究结果表明,Cxcr4的过度激活直接影响颗粒细胞(GC)的发育和成熟。尽管神经元分化轨迹和迁移行为是紧密交织的过程,但我们的体外数据显示,WHIM所改变的形态和功能表型源于颗粒细胞谱系的细胞自主性缺陷,与发育中小脑的三维细胞结构以及任何外周改变均无关。
¶ WHIM小鼠中颗粒细胞谱系发育缺陷影响浆细胞分化及功能特性
颗粒细胞(GCs)的正常发育是浦肯野细胞(PCs)成熟所必需的。浦肯野细胞具有特征性的树突 Arbor(图6A),并且是小脑皮质的唯一输出神经元。在我们的转录分析中,浦肯野细胞以及其他Cxcr4阴性细胞在基因表达方面出现了显著的失调(图4D)。富集分析显示,与树突分支形成、轴突发生以及突触神经传递和长时程增强(LTP)相关的基因表达下调(图6B),这表明浦肯野细胞的发育和突触成熟存在障碍。一致地,我们观察到在P30时,受影响的小叶内浦肯野细胞的总数量有所减少(图6C)。此外,我们发现,在距胞体特定距离(40-70μm)处,浦肯野细胞的树突复杂性显著降低(图6D和图S6A),尽管交叉点的总数没有显著变化(数据未显示)。这表明Cxcr4的过度激活以非细胞自主性的方式选择性地调控浦肯野细胞的数量及其近端树突分支,可能会破坏回路的组装。
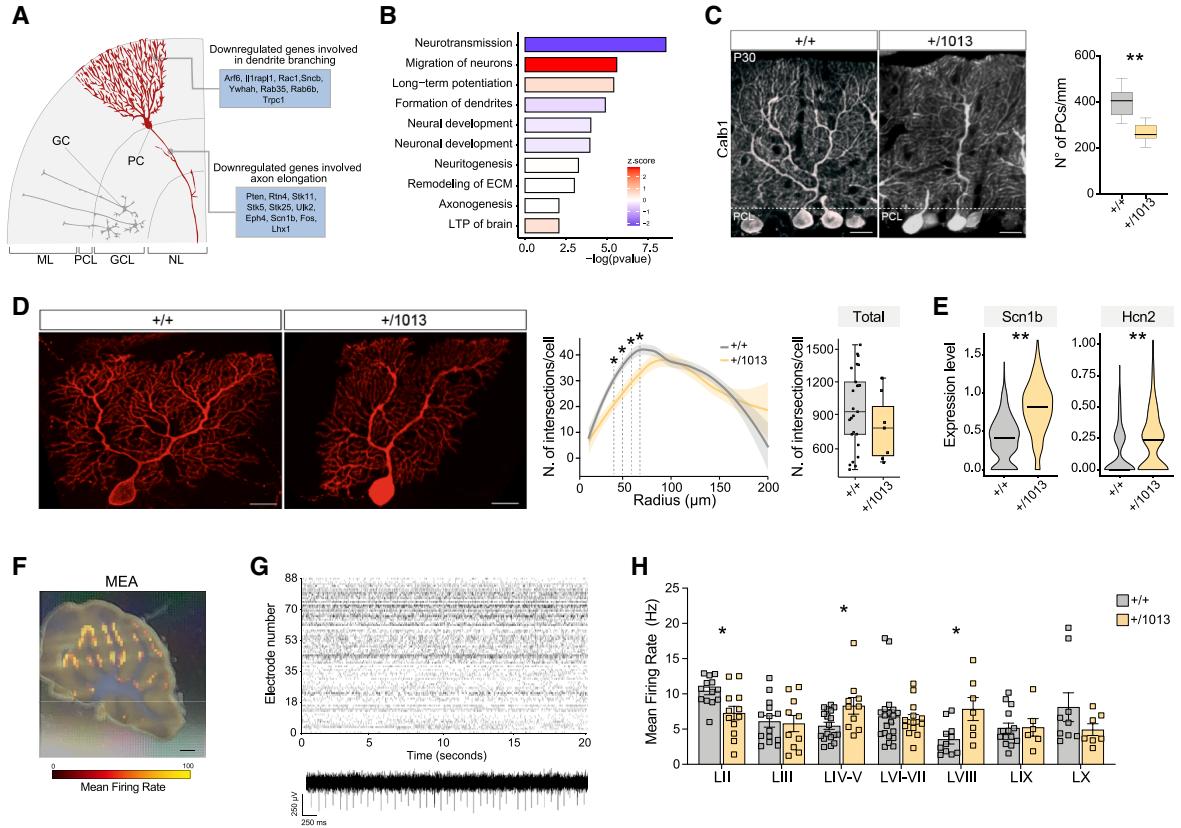
图6. Cxcr4突变的非细胞自主性效应
(A) 显示浦肯野细胞(PC)定位和选定下调基因的小脑层示意图。
(B) 柱状图显示浦肯野细胞(PCs)中显著失调的主要生物学功能,按激活Z分数着色。
© P30小脑的免疫荧光染色显示Cxcr4+/1013中Calb1+浦肯野细胞(红色),箱线图显示浦肯野细胞密度。Student t检验,**p < 0.01;n > 7只动物/条件。比例尺,20 μm。
(D) 对照小鼠和WHIM小鼠在P21时的单个浦肯野细胞(PC)。线图显示浦肯野细胞树突的半径(微米)和交叉点数,箱线图显示交叉点总数。采用Student t检验,*p < 0.05;每个条件下n > 7个细胞。比例尺,20微米。
(E) 小提琴图显示 PCs 中 Scn1b 和 Hcn2 的表达,**p < 0.01。
(F) 叠加了活动图的小脑切片光学图像。比例尺,2毫米。
(G)代表性光栅图(上方)记录的是对照组小脑 活动,下方记录的是单个活性电极随时间变化的动作电位。
(H) 柱状图显示每个脑叶记录的平均放电率(MFR)的定量分析。点表示被分析切片的数量。Mann-Whitney检验,*p < 0.05;
每个条件下n > 6只动物。
转录组学分析显示,WHIM浦肯野细胞(PCs)中多个离子通道基因的表达增加,包括钠电压门控通道β1亚基(Scn1b)和超极化激活环核苷酸门控通道2(Hcn2)(图6E)。为了研究观察到的WHIM小脑异常特征的潜在功能后果,我们使用高密度多电极阵列(HDMEA;图6F-6H和S6B-S6E)监测了Cxcr4+/1013和对照小脑切片的自发活动,该阵列在基础条件下记录浦肯野细胞的活动。WHIM切片的总体平均 firing rate(MFR)和活性单位数量与对照组无显著差异(图S6C),而不同特定小叶的MFR存在显著差异(图6H和S6E)。在WHIM小脑中,与改变的脑沟相邻的小叶LIV-V和LVIII的MFR显著增加,并且一致地,LVIII中的尖峰信号幅度也增加(图S6D)。
总体而言,这些数据证明了在小脑发育过程中,兴奋性神经元和抑制性神经元之间存在密切的相互作用,这导致了特定小叶的网络活动异常,并可能损害WHIM小脑皮质的整体输出。
¶ WHIM突变体表现出先天性白细胞减少症,但小脑的免疫状态未发生改变
虽然WHIM小鼠成年后的免疫表型已得到广泛研究36,38,但它们在发育过程中的免疫表型尚未被探索过。这是一个关键的研究空白,尤其是考虑到在WHIM患者中观察到免疫缺陷的早发性102,103,以及我们在Cxcr4+/1013幼鼠中关于神经发育的研究发现。为解决这一问题,我们对WHIM小鼠从胚胎第16.5天(E16.5)到出生后第45天(P45)进行了纵向免疫表型分析,采用多参数流式细胞术对肝脏、脾脏、血液和小脑组织进行检测(图7A)。
正如预期的那样,在E16.5时的WHIM胎肝中,所研究的任何免疫群体均未发现差异(图7B),胎肝造血不依赖于Cxcr4-Cxcl12轴104–106。因此,在同一阶段的脾脏免疫群体数量中未观察到变化(图S7E和S7F)。
有趣的是,早在P0时期,携带WHIM突变的动物就表现出明显的中性粒细胞减少和淋巴细胞减少(图7C、7D、S7A和S7B)。在WHIM小鼠的血液中观察到CD45+细胞数量普遍减少(图7C、7D、S7A和S7B),而在WHIM新生小鼠的脾脏中,CD11b+免疫细胞、中性粒细胞和B细胞显著减少,其他被分析的细胞类型也有普遍减少的趋势(图S7E和S7G)。
在研究的任何免疫群体中(图7E、7F和S7C),包括驻留小胶质细胞,均未在WHIM小鼠的小脑中检测到差异。此外,小胶质细胞的丰度以及作为激活标志物的CD86平均荧光强度(MFI)均保持不变(图7E和7F)。一致地,Iba1免疫染色显示Cxcr4+/1013新生小鼠与对照新生小鼠之间的小胶质细胞密度无差异(图7G),且在出生后第21天,通过分支和连接计数/细胞来衡量的小胶质细胞形态未受影响(图7H)。值得注意的是,WHIM小鼠是在特定无病原体(SPF)条件下饲养的,从未接触过任何免疫挑战。此外,与焦虑样行为相关的γδ T细胞介导的白细胞介素(IL)-17信号通路的组成部分——Il17及其受体Il17ra的表达水平在WHIM小鼠的小脑中未发生改变(图S7D)。
总之,这些研究结果表明,在基础条件下,WHIM小鼠的小脑并未表现出免疫失调的迹象,这支持了所观察到的形态和行为表型具有细胞自主性起源。
¶ 早期发育干预可改善WHIM的行为和结构缺陷
AMD3100是一种CXCR4拮抗剂,是目前正在评估的一种很有前景的疗法,用于治疗WHIM综合征的免疫相关症状。然而,迄今为止的临床试验仅纳入了10岁以上的患者44–46,尽管该疾病的临床表现在出生时就已出现。102,103
为了评估早期、大脑特异性的CXCR4抑制是否能挽救WHIM表型,我们在胚胎第12.5天(E12.5)向脑室注射AMD3100,并在出生后第7天(P7)和第45天(P45)分析行为和小脑结果(图8A)。与野生型对照组相比,接受治疗的Cxcr4+/1013幼鼠体重显著增加(图8B),这表明AMD3100会影响关键的发育轨迹。在悬崖回避测试中,几乎所有接受AMD3100治疗的幼鼠都表现出适当的回避反应,这与接受溶媒治疗的突变同窝幼鼠的不佳表现形成对比(图8C)。形态学评估显示,P7时小脑沟长度显著恢复(图8D和图S8A),P45时也观察到沟长度的部分改善(图S8B)。为了研究具有潜在临床相关性的早期产后治疗干预,我们在出生后第1天(P1)重复进行了脑室AMD3100注射(图8E)。与宫内给药类似,接受AMD3100治疗的Cxcr4+/1013幼鼠在P7时体重显著增加,与野生型水平相当(图8F),且在悬崖回避测试中的表现明显优于接受溶媒治疗的突变同窝幼鼠(图8G)。在P45时,接受治疗的小鼠在旷场中央停留的时间更长,垂直活动次数更多(图8H),表明其探索行为有所改善。此阶段的形态学分析还显示沟长度增加(图S8C),与胚胎期AMD3100给药的结果一致。
总之,这些研究结果提供了有力的证据,表明在WHIM小鼠中观察到的结构和行为异常源于发育中大脑内Cxcr4的内在功能障碍,并且可以通过早期的靶向干预来挽救。
¶ 讨论
我们的研究结果为慢性免疫疾病中神经行为症状背后复杂的神经免疫相互作用提供了新的见解。通过发现免疫缺陷(IEI)基因在小脑谱系中的发育富集,我们提出,内在的、大脑特异性的作用可能是IEI患者神经行为特征的基础。基于对WHIM小鼠模型的全面表征——该模型忠实地再现了人类的遗传和免疫表型33,36,38,39——我们发现,即使在没有免疫挑战的情况下,颗粒细胞前体(GCPs)也是所观察到的小脑叶片形成缺陷和回路连接错误的关键介导者。它们在分子、形态和功能上的破坏会损害浦肯野细胞(PC)的发育和小脑输出,导致与患者中描述的一致的持续性行为表型。
¶ 绘制与IEI相关的基因在人类大脑发育中的图谱
虽然免疫缺陷性疾病(IEI)和其他慢性炎症性疾病中经常报告行为改变,尤其是焦虑和抑郁,但这些症状通常被认为是全身性疾病的次要表现,在儿科患者中尤为如此。然而,未确诊或未治疗的神经精神症状可能会产生深远的长期影响。尽管先前的研究已通过非细胞自主性通路将免疫信号与大脑功能联系起来,但IEI基因对神经发育过程的直接作用尚未得到系统研究。
在此,我们首次对免疫缺陷性疾病(IEI)及其遗传结构和相关临床特征进行了全面分析。我们发现,超过40%的IEI基因与神经行为表型相关,而由于对患者的神经学特征描述有限,这一比例可能仍被低估。通过确定特定的发育窗口期和小脑易损性,我们为深入理解免疫相关遗传变异如何塑造大脑结构和功能奠定了基础。
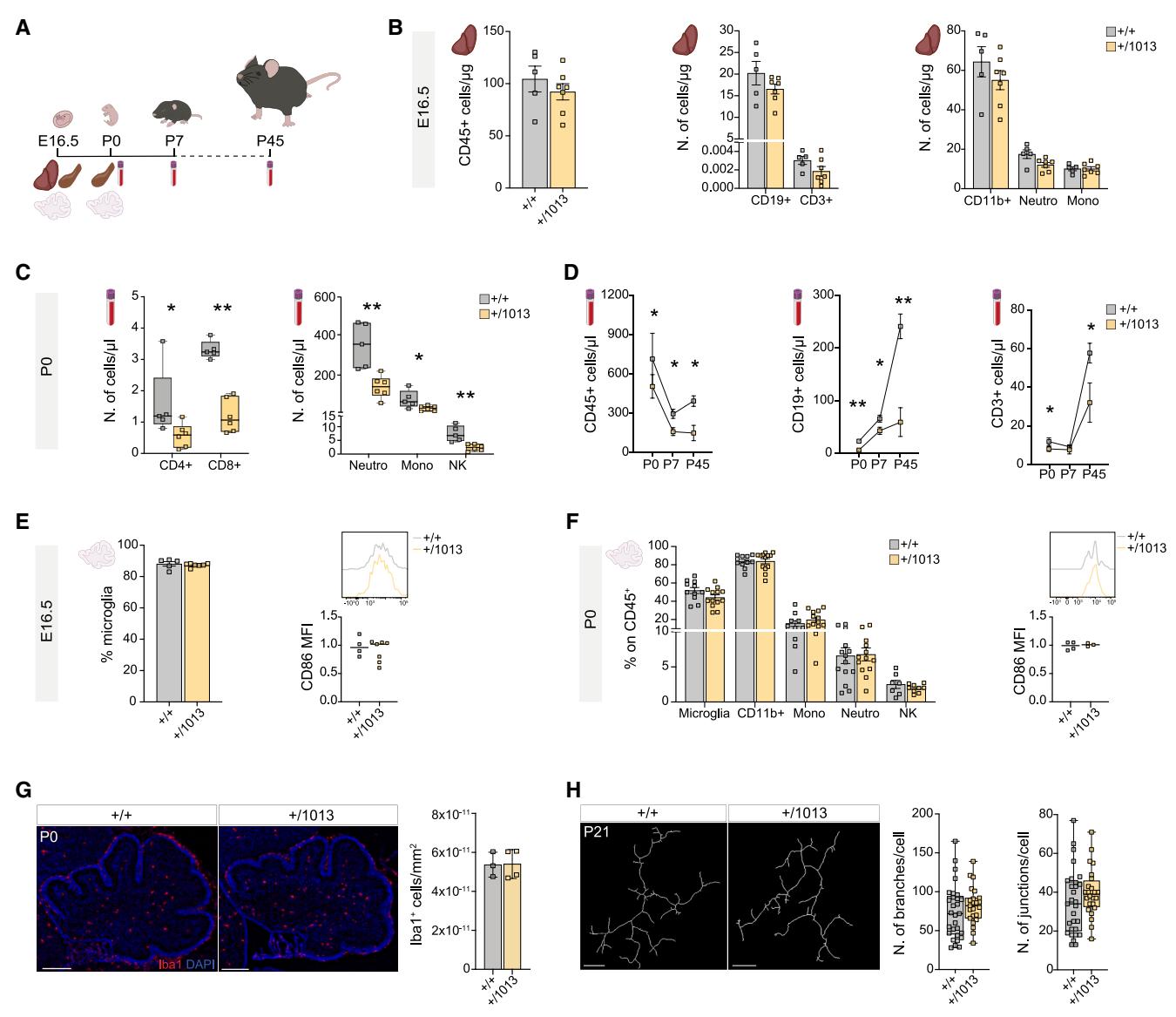
图7. WHIM突变体表现出先天性白细胞减少,但小脑的免疫状态未发生改变
(A) 实验方案。
(B)柱状图显示通过荧光激活细胞分选(FACS)分析的E16.5 WHIM肝脏中的免疫细胞亚群。采用Student’s t检验,*p < 0.05;每组n > 4只动物。数据以平均值±标准误(SEM)表示。
(C) 箱线图显示通过流式细胞术(FACS)分析的P0 WHIM血液中循环免疫细胞亚群。采用Student t检验,*p < 0.05;每组n > 4只动物。数据以平均值±标准误(SEM)表示。
(D) 线图显示通过流式细胞术(FACS)分析的P0至P45期间Cxcr4+/1013血液中循环的CD45+、CD19+和CD3+细胞。采用Student’s t检验,*p < 0.05,**p < 0.01;每个条件下n > 4只动物。
(E) 图表显示通过流式细胞术(FACS)分析的E16.5 WHIM小鼠小脑中,小胶质细胞在CD45+细胞中的百分比、CD86的平均荧光强度(MFI)以及相对定量结果。采用Student’s t检验,*p < 0.05;每组样本数n > 4只动物。
(F) 图表显示通过流式细胞术分析的P0 WHIM小鼠小脑的免疫学特征、CD86的平均荧光强度(MFI)和相对定量。采用Student t检验,*p < 0.05;每组n > 3只动物。数据以平均值±标准误(SEM)表示。
(G) P0时Cxcr4+/1013和对照组的代表性小脑切片,用小胶质细胞标志物Iba1染色及密度柱状图。比例尺,200 μm。多重t检验,*p < 0.05;每组n > 3只动物。
(H) P21时WHIM和对照组小脑内Iba1+小胶质细胞的3D重建及相对定量分析。比例尺,10 μm。多重t检验,*p < 0.05;每组n > 3只动物。
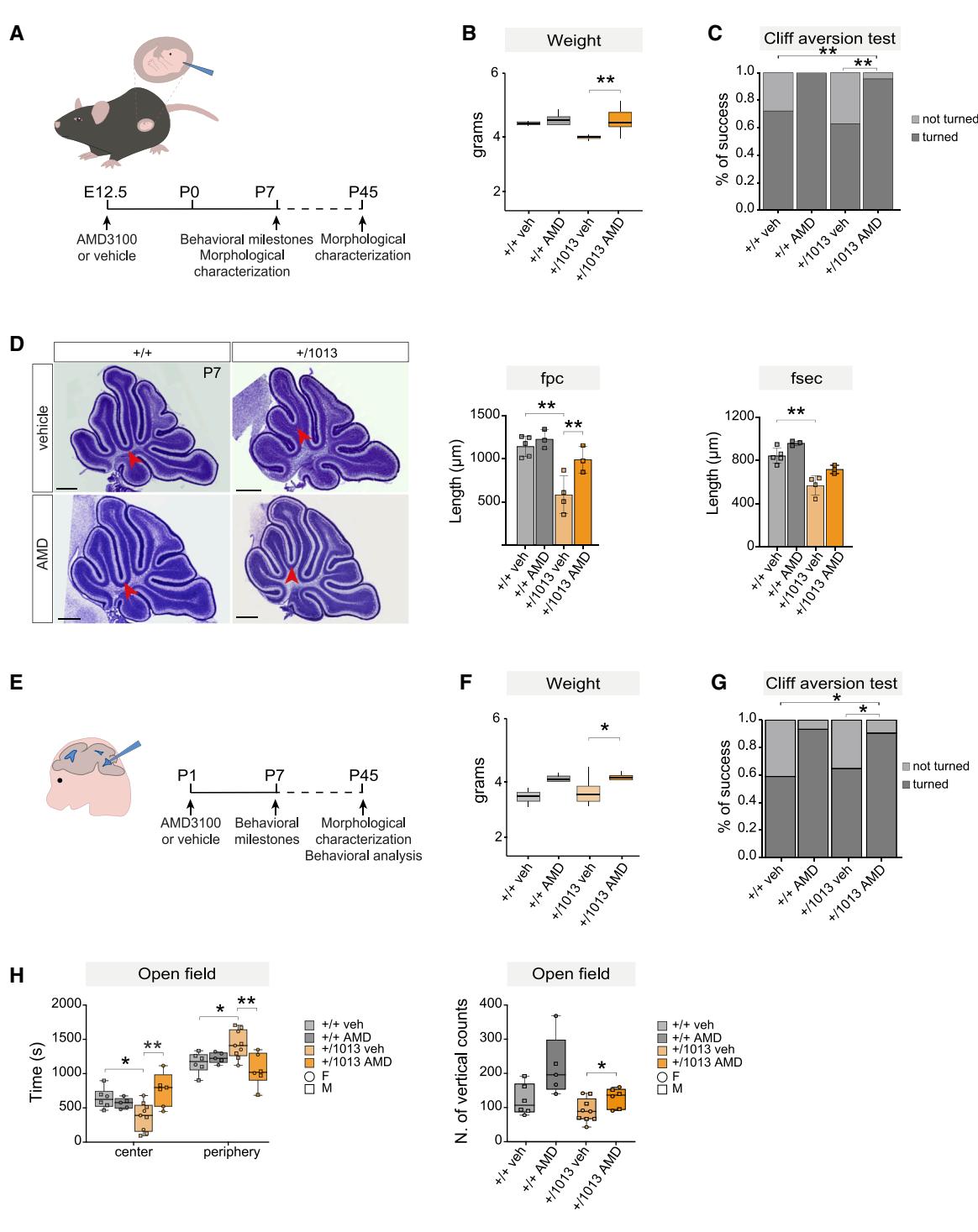
图8. WHIM的行为和结构改变可在发育早期阶段得到挽救
(A) 显示子宫内注射AMD3100或溶媒的实验方案。
(B) 箱线图显示在E12.5时注射AMD3100或溶媒后P7幼鼠的体重。多重t检验,**p < 0.01;每组n > 4只动物。
(C) 柱状图显示在E12.5时接受AMD3100或溶媒处理的P7幼鼠在悬崖回避测试中转身的百分比。多重t检验,**p < 0.01;每个条件下n > 4只动物。
(D) 在E12.5时注射AMD3100或溶媒后,P7时WHIM和对照小鼠小脑的代表性矢状尼氏染色切片,以及显示裂隙长度的柱状图。
比例尺,200 μm。多重t检验,**p < 0.01;每组n > 3只动物。
(E) 出生后注射AMD3100或溶媒的实验方案。
(F) 箱线图显示P1注射AMD3100或溶媒后P7幼鼠的体重。多重t检验,*p < 0.05;每组n > 4只动物。
G) 柱状图显示在P1时接受AMD3100或溶媒处理的P7幼鼠在悬崖回避测试中转身的百分比。多重t检验,*p < 0.05;每个条件下n > 4只动物。
(H)箱线图显示P1时注射AMD3100或溶媒的P45小鼠在旷场中的时间。单因素方差分析。箱线图显示旷场试验中的垂直计数次数。Student t检验,*p < 0.05;**p < 0.01;每个条件下n > 5只动物。
¶ 与WHIM相关的突变直接控制颗粒细胞的时空动态
在免疫功能异常的小鼠模型(例如,IL-6、IL-10和IL-18缺陷小鼠)中进行的磁共振成像(MRI)研究表明,免疫失调与脑结构改变有关,特别是在小脑和外侧隔区。109 我们的研究结果通过揭示一种直接的、基因特异性机制扩展了这项工作:Cxcr4的过度激活会破坏GCP的行为,损害小脑的叶片形成(通过MRI和组织学评估)以及GC回路的组装。考虑到它们的树突所接收的密集且高度特异性的输入,有理由认为胚胎期WHIM小脑中GC的功能行为受到其精确空间定位的强烈影响。110
我们关于Cxcr4依赖性的基底神经节突起扇形模式改变的研究结果,影响了WHIM小鼠小叶中成熟颗粒细胞的最终排列,这可能会影响细胞间接触信号以及它们沿小叶迁移的支架。总之,这支持存在一个明确的产前发育窗口,该窗口控制着叶片形成的起始和进展,而后这种形成在机械上会受到过度活跃的Cxcr4通路的维持和影响。
生发中心细胞跨层的协同迁移与其分化密切相关,这建立了成熟状态与空间定位之间的明确关系——这种关联可以通过单细胞假时间/假空间分析有效捕捉。这种耦合并非生发中心细胞谱系所独有,其他神经元群体——小脑的抑制性中间神经元以及大脑皮层的抑制性中间神经元——在迁移至最终位置的同时,也会逐步确定其身份。
我们的体外培养实验表明,即使在没有迁移信号的情况下,WHIM粒细胞也会呈现出独特的形态和电生理特征。先前对分离出的粒细胞的研究显示,它们的迁移遵循一个内在的程序性顺序形态变化,不受外部信号影响,最终进入以树突分支增加为特征的静止期。99,113因此,在体外观察到的WHIM粒细胞分支增加,可能源于过早的迁移停滞和提前的神经突发生。
考虑到免疫学纵向数据,研究发现WHIM小鼠中观察到的结构缺陷源于生发中心迁移和分化的内在改变。
¶ WHIM突变影响小脑回路的组装和行为
小脑在情感调节中的作用日益受到关注,小脑连接的改变与焦虑和情绪障碍有关。在细胞层面,颗粒细胞(GCs)是全脑数量最多的神经元群体,它们编码多种感觉和运动信息,其活动模式反映了感觉运动背景。WHIM幼鼠行为的广泛改变支持了小脑颗粒细胞在整合感觉和运动信号中的作用。事实上,颗粒细胞接收来自 mossy 纤维的输入,并将信息传递给浦肯野细胞(PCs),而浦肯野细胞又投射到小脑核团。这种复杂的结构最终将小脑 与中枢神经系统的其他部分连接起来。在此,我们表明,与 Cxcr4 相关的改变不仅影响颗粒细胞,还以非细胞自主性的方式影响浦肯野细胞,改变它们的转录谱,减少它们的树突延伸和分支,最终导致微电路活动的变化。兴奋性和抑制性神经元亚型之间的动态相互作用已被证明在大脑发育中至关重要,但精确的分子密码是否调控不同小叶中颗粒细胞 - 浦肯野细胞连接的细胞类型特异性和空间组装,仍有待阐明。
尽管WHIM幼崽的早期发育行为受到干扰,但部分行为在出生后第二周有所改善,这表明存在补偿机制的可能性。不过,类焦虑表型会持续到成年期,且可通过CXCR4拮抗作用逆转,这凸显了小脑情感回路的可塑性有限,并证实了发育敏感窗口期的存在。118未来的研究应探索这些影响是否为小脑特异性的,或是反映了长距离连接的更广泛破坏。
¶ 早期AMD3100治疗可恢复WHIM小鼠的小脑叶片形成,并对其行为产生持久影响
CXCR4拮抗剂AMD3100已获国际药品机构批准用于儿童造血干细胞动员,但仅在10岁以上的WHIM患者中进行过测试。在此,我们证明,在小鼠的胚胎期和出生后早期阶段脑室内注射AMD3100,可挽救小脑形态和行为缺陷。这些发现表明,针对中枢神经系统的早期干预在CXCR4相关疾病中具有此前未被认识到的潜力。虽然先前的研究表明,在小鼠子宫内脑室内注射AMD3100可调节表达Cxcr4的γ-氨基丁酸能中间神经元进入皮质板,但据我们所知,这是AMD3100直接作用于小脑发育过程的首个证据。
虽然我们的研究结果为Cxcr4-Cxcl12轴在小脑中的发育作用提供了有趣的见解,并支持了早期干预的可行性,但还需要进一步的研究来评估这些发现如何转化为人类病理学。因此,大型患者队列、年龄匹配的对照组以及综合的形态计量-行为分析至关重要。
我们的研究结果支持这样一种可能性:那些因突变的直接影响而发育已受到启动的大脑结构,在面临免疫损伤时,可能会更容易发生功能变化。进一步的研究将阐明,在WHIM综合征中,甚至在其他涉及神经行为缺陷的原发性免疫缺陷病(IEI)中,反复的免疫挑战是否会引发神经免疫交叉对话的改变,最终加剧现有的表型。
我们的研究总体上揭示了中枢神经系统发育,特别是小脑的发育,在神经免疫相互作用中以及其对免疫缺陷性疾病患者行为影响方面的重要作用。对免疫缺陷性疾病中神经行为症状的准确诊断,对于全面的患者护理至关重要,这也将为这些复杂疾病的临床评估带来重大转变。
¶ 资源可用性
¶ 主要联系人
更多信息以及对资源和试剂的请求应直接联系主要联系人Simona Lodato(simona. lodato@hunimed.eu),她将予以回应。
¶ 材料可用性
本研究未生成任何新的独特试剂。
¶ 数据和代码可用性
• P1 WHIM和对照小脑的单细胞基因表达数据集已存入GEO,自发表之日起可公开获取。GEO:GSE266671。
• P45 WHIM和对照组小脑的MRI数据已存放在OpenNeuro上,自发表之日起可公开获取。OpenNeuro:ds005137。
• BrainSpan图谱可在https://www.brainspan.org/获取。
• 人类单核数据集可在https://cellxgene.cziscience.com/collections/72d37bc9-76cc-442d-9131-da0e273862db/获取。
• 本文未报告原创代码。
• 如需重新分析本工作论文中报告的数据,所需的任何额外信息均可向主要联系人索取。
¶ 致谢
我们感谢A. Fontanesi和D. Uralov提供的技术支持,以及C. Saulle在流式细胞术(FACS)分析设置方面给予的帮助。我们要感谢巴斯德研究所的Arenzana-Seisdedos教授慷慨地与我们机构分享Cxcr4+/1013小鼠品系。感谢D. Kim博士和GENIE项目提供的pAAV-hSyn-GCaMP6s-WPRE质粒,以及K. Deisseroth教授提供的pAAV-hSyn-mCherry质粒。我们感谢基因组学、成像和流式细胞术Humanitas设施提供的技术支持。感谢Lodato实验室的所有成员进行富有成效的讨论并提出宝贵建议。本研究得到以下项目的支持:ERC启动基金IMPACT(编号101043003)、Cariplo Giovani 2019(编号1785)和意大利卫生部2019年最终研究基金(资助S.L.);ERC高级基金MATILDA(编号101055323)和EraNET Neuron JTC2021 InflASD项目(资助M. Matteoli);Cariplo Giovani 2019(编号1973)(资助I.C.);Cariplo-Telethon GJC21044A和PRIN-2022(编号2022JLA3EA)(资助D.P.);以及FRAXA 2021(资助A.B.)。
¶ 作者贡献
S.L.和G.D.构思了本研究,设计了实验并分析了数据。G.D.执行了所有实验和菌落维持工作;G.D.和L.Z.进行了基因分型、样本收集和组织学染色;S.M.开展了单细胞测序实验并分析了批量转录数据;S.M.和M. Miotto分析并解读了单细胞/细胞核测序数据;R.O.P.进行了尼氏分析并设定了里程碑测试;A.B、I.C.和M. Matteoli执行并分析了行为实验;V.A.、M.C.和M.K.执行并分析了流式细胞术实验;E. K.、K.I.和D.C.执行并分析了磁共振成像实验;E.F.和D.P.执行并分析了微电极阵列记录;L.P.和R.R.设计并分析了叶状模型;S.L.、G.D.和S.M.撰写了初稿;所有作者均对 manuscript 进行了修订。
¶ 利益声明
作者声明不存在利益冲突。
¶ STAR★方法
详细方法见本文的在线版本,包括以下内容:
• KEY RESOURCES TABLE • 关键资源表
• EXPERIMENTAL MODEL AND STUDY PARTICIPANT DETAILS
• 实验模型和研究参与者详情
○ 动物
○ 原代颗粒细胞培养
• 方法详情
○ 人类大脑中IEI相关基因的数据集及分析
○ 体外磁共振成像
○ 成年小鼠的行为测试
○ 发育里程碑测试
○ 尼氏染色
○ 实时定量聚合酶链式反应
○ 脑回分析
○ 单细胞RNA测序与分析
○ 多电极阵列分析
○ 源自肝脏、脾脏、血液和小脑 的免疫细胞集合
○ 细胞培养物免疫染色
○ 切片免疫染色
○ 脑室内注射AMD3100
○ 成像
○ 图像分析
• 量化与统计分析
¶ 补充信息
补充信息可在网上查阅:https://doi.org/10.1016/j.neuron.2025.05.016。
发布时间:2025年6月6日
¶ 参考文献
- Ben-Shaanan, T.L., Azulay-Debby, H., Dubovik, T., Starosvetsky, E., Korin, B., Schiller, M., Green, N.L., Admon, Y., Hakim, F., Shen-Orr, S. S. 等(2016)。奖励系统的激活可增强先天性和适应性免疫。《自然·医学》,22,940-944。https://doi.org/10.1038/nm.4133
- 海金(H.)和劳斯(A.)(2021)。压力期间的神经免疫反应:生理学视角。《免疫》54,1933-1947。https://doi.org/10.1016/j.immuni.2021.08.023
- 巴甫洛夫(V.A.)、查万(S.S.)和特雷西(K.J.)(2018)。《免疫学中的分子与功能神经科学》。《免疫学年度评论》36,783-812。https://doi.org/10.1146/annurev-immunol-042617-053158
- Al-Haddad, B.J.S., Jacobsson, B., Chabra, S., Modzelewska, D., Olson, E.M., Bernier, R., Enquobahrie, D.A., Hagberg, H., O¨stling, S., Rajagopal, L., 等. (2019). 宫内感染暴露后神经精神疾病的长期风险. 《美国医学会杂志·精神病学》76, 594–602. https://doi.org/10.1001/jamapsychiatry.2019.0029
- 崔(G.B.)、任(Y.S.)、王(H.)、金(S.)、金(H.)、金(S.V.)、霍弗(C.A.)、利特曼(D.R.)和许(J.R.)(2016)。小鼠中的母体白细胞介素-17a通路会促使后代出现类自闭症表型。《科学》351,933-939。https://doi.org/10.1126/science.aad0314
- Khandaker, G.M., Zimbron, J., Lewis, G., 和 Jones, P.B.(2013)。产前母体感染、神经发育与成人精神分裂症:基于人群研究的系统综述。《心理医学》,43,239-257。https://doi.org/10.1017/S0033291712000736
- Kim, S.、Kim, H.、Yim, Y.S.、Ha, S.、Atarashi, K.、Tan, T.G.、Longman, R.S.、Honda, K.、Littman, D.R.、Choi, G.B. 等人(2017)。母体肠道细菌促进小鼠后代的神经发育异常。《自然》549,528-532。https://doi.org/10.1038/nature23910
- Mirabella, F., Desiato, G., Mancinelli, S., Fossati, G., Rasile, M., Morini, R., Markicevic, M., Grimm, C., Amegandjin, C., Termanini, A. 等人(2021)。产前白细胞介素6水平升高会增加后代的谷氨酸能突触密度并破坏海马连接。《免疫》54,2611–2631.e8。https://doi.org/10.1016/j.immuni.2021.10.006
- Reed, M.D.、Yim, Y.S.、Wimmer, R.D.、Kim, H.、Ryu, C.、Welch, G.M.、Andina, M.、King, H.O.、Waisman, A.、Halassa, M.M. 等人(2020)。IL17a促进神经发育障碍小鼠模型的社交能力。《自然》577,249-253。https://doi.org/10.1038/s41586-019-1843-6
- 弗拉瓜斯(D. Fraguas)、迪亚斯-卡内哈(C.M. Dı´az-Caneja)、阿约拉(M. Ayora)、埃尔南德斯-阿尔瓦雷斯(F. Herna´ndez-A´lvarez)、罗德里格斯-基罗加(A. Rodrı´guez-Quiroga)、雷西奥(S. Recio)、莱萨(J.C. Leza)和阿朗戈(C. Arango)(2019)。首发精神病中的氧化应激与炎症:一项系统综述和荟萃分析。《精神分裂症通报》,45,742-751。https://doi.org/10.1093/schbul/sby125
- 亚昆奇科娃(O.)、伦纳森(E.H.)和王(Y.)(2024)。《免疫功能障碍对精神疾病因果影响的遗传证据:我们目前的研究进展如何?》,《转化精神病学》,14,63。https://doi.org/10.1038/s41398-024-02778-2
- Berriat, F.、Lobsiger, C.S. 和 Boille´ e, S.(2023)。外周免疫系统对神经退行性变的作用。《自然·神经科学》,26,942-954。https://doi.org/10.1038/s41593-023-01323-6
- 米肖(M. Michaud)、巴拉尔迪(L. Balardy)、穆利斯(G. Moulis)、高丹(C. Gaudin)、佩罗(C. Peyrot)、韦拉斯(B. Vellas)、塞萨里(M. Cesari)和努尔哈什米(F. Nourhashemi)(2013)。促炎细胞因子、衰老与年龄相关疾病。《美国老年病学会杂志》,14,877-882。https://doi.org/10.1016/j.jamda.2013.05.009
- Mildner, A., Schlevogt, B., Kierdorf, K., Bo¨ ttcher, C., Erny, D., Kummer, M.P., Quinn, M., Bru¨ ck, W., Bechmann, I., Heneka, M.T. 等人(2011)。小胶质细胞和髓系细胞亚群在阿尔茨海默病小鼠模型中具有独特且非冗余的作用。《神经科学杂志》,31,11159-11171。https://doi.org/10.1523/JNEUROSCI.6209-10.2011
- 彼得(I.)、杜宾斯基(M.)、布雷斯曼(S.)、帕克(A.)、卢(C.)、陈(N.)和王(A.)(2018)。《抗肿瘤坏死因子治疗与炎症性肠病患者帕金森病发病率》。《美国医学会杂志·神经病学》,75,939-946。https://doi.org/10.1001/jamaneurol.2018.0605
- Bannaga, A.S.和Selinger, C.P.(2015)。炎症性肠病与焦虑:关联、风险及面临的挑战。《临床与实验胃肠病学》,8,111-117。https://doi.org/10.2147/CEG.S57982
- Carloni, S., Bertocchi, A., Mancinelli, S., Bellini, M., Erreni, M., Borreca, A., Braga, D., Giugliano, S., Mozzarelli, A.M., Manganaro, D. 等人(2021)。肠炎症期间脉络丛血管屏障关闭的识别。《科学》374,439-448。https://doi.org/10.1126/science.abc6108
- Hedemann, T.L., Liu, X., Kang, C.N., 和 Husain, M.I.(2022)。银屑病与精神疾病之间的关联:给临床医生的最新进展。《综合医院精神病学》75,30-37。https://doi.org/10.1016/j.genhosppsych.2022.01.006
- Martínez-Ortega, J.M., Nogueras, P., Mun˜ oz-Negro, J.E., Gutie´ rrezRojas, L., Gonza´ lez-Domenech, P., 和 Gurpegui, M.(2019)。银屑病患者的生活质量、焦虑和抑郁症状:一项病例对照研究。《心身医学研究杂志》,124,109780。https://doi.org/10.1016/j.jpsychores.2019.109780
- 琼斯·阿马奥韦(E.E.)、安瓦尔(S.)、卡瓦努尔·斯里达尔(K.)、沙比尔(K.)、穆罕默德(E.H.)、巴哈尔(A.R.)、塔尔普尔(A.S.)、巴特(S.)、扎法尔(S.)和卡达尔(L.T.)(2022)。抑郁症和焦虑症与类风湿性关节炎的相关性。《Cureus》14,e23137。https://doi.org/10.7759/cureus.23137
- Machin, A.R.、Babatunde, O.、Haththotuwa, R.、Scott, I.、BlagojevicBucknall, M.、Corp, N.、Chew-Graham, C.A. 和 Hider, S.L.(2020)。类风湿关节炎患者焦虑与疾病活动度及生活质量的相关性:一项系统综述和荟萃分析。《临床风湿病学》,39,1471-1482。https://doi.org/10.1007/s10067-019-04900-y
- Marrie, R.A.、Hitchon, C.A.、Walld, R.、Patten, S.B.、Bolton, J.M.、Sareen, J.、Walker, J.R.、Singer, A.、Lix, L.M.、El-Gabalawy, R. 等(2018)。类风湿关节炎患者中精神疾病负担增加。《关节炎护理与研究》,70,970-978。https://doi.org/10.1002/acr.23539
- 宇田(M.)、桥本(M.)、鱼住(R.)、鸟居(M.)、藤井(T.)、田中(M.)、古(M.)、伊藤(H.)、寺尾(C.)、山本(W.)等(2021)。类风湿关节炎患者焦虑和抑郁的相关因素:一项横断面研究。《风湿病学进展》,61,65。https://doi.org/10.1186/s42358-021-00223-2
- Amaya-Uribe, L.、Rojas, M.、Azizi, G.、Anaya, J.-M. 和 Gershwin, M.E.(2019)。原发性免疫缺陷与自身免疫:综合综述。《自身免疫杂志》,99,52-72。https://doi.org/10.1016/j.jaut.2019.01.011
- 麦卡斯基尔(C.)、厄普顿(J.)和沃林顿(R.)(2018)。原发性免疫缺陷。《变态反应、哮喘与临床免疫学》,14,61。https://doi.org/10.1186/s13223-018-0290-5
- 皮卡德(C.)、博比·加斯帕尔(H.)、阿尔-赫兹(W.)、布斯菲亚(A.)、卡萨诺瓦(J.-L.)、沙提拉(T.)、克罗(Y.J.)、坎宁安-朗德尔(C.)、埃齐奥尼(A.)、佛朗哥(J.L.)等(2018)。国际免疫学会联合会:2017年原发性免疫缺陷病委员会关于先天性免疫缺陷的报告。《临床免疫学杂志》,38,96-128。https://doi.org/10.1007/s10875-017-0464-9
- Tangye, S.G., Al-Herz, W., Bousfiha, A., Chatila, T., CunninghamRundles, C., Etzioni, A., Franco, J.L., Holland, S.M., Klein, C., Morio, T. 等 (2020). 人类先天性免疫缺陷:国际免疫学会联合会专家委员会2019年分类更新。《临床免疫学杂志》,40,24-64。https://doi.org/10.1007/s10875-019-00737-x
- Tangye, S.G., Al-Herz, W., Bousfiha, A., Cunningham-Rundles, C., Franco, J.L., Holland, S.M., Klein, C., Morio, T., Oksenhendler, E., Picard, C.等(2022)。人类先天性免疫缺陷:国际免疫学会联合会专家委员会2022年分类更新。《临床免疫学杂志》,42,1473-1507。https://doi.org/10.1007/s10875-022-01289-3
- Isung, J.、Williams, K.、Isomura, K.、Gromark, C.、Hesselmark, E.、Lichtenstein, P.、Larsson, H.、Ferna´ndez de la Cruz, L.F.、Sidorchuk, A. 和 Mataix-Cols, D.(2020)。原发性体液免疫缺陷与精神疾病及自杀行为的关联以及自身免疫性疾病的作用。《美国医学会杂志·精神病学》77,1147-1154。https://doi.org/10.1001/jamapsychiatry.2020.1260
- Rider, N.L., Kutac, C., Hajjar, J., Scalchunes, C., Seeborg, F.O., Boyle, M., 和 Orange, J.S.(2017)。普通变异型免疫缺陷病成年患者的健康相关生活质量及治疗影响。《临床免疫学杂志》,37,461-475。https://doi.org/10.1007/s10875-017-0404-8
- Titman, P.、Allwood, Z.、Gilmour, C.、Malcolmson, C.、Duran-Persson, C.、Cale, C.、Davies, G.、Gaspar, H. 和 Jones, A.(2014)。原发性抗体缺乏症儿童的生活质量。《临床免疫学杂志》,34,844-852。https://doi.org/10.1007/s10875-014-0072-x
- 马努萨马(O.R.)、范·贝弗伦(N.J.M.)、范·哈根(P.M.)、德雷克斯哈格(H.A.)和达尔姆(V.A.S.H.)(2022)。原发性免疫缺陷中的心理症状:一种常见的合并症?《临床免疫学杂志》,42,695-698。https://doi.org/10.1007/s10875-022-01207-7
- Anginot, A., Nguyen, J., Abou Nader, Z., Rondeau, V., Bonaud, A., Kalogeraki, M., Boutin, A., Lemos, J.P., Bisio, V., Koenen, J. 等人(2023)。WHIM综合征相关的CXCR4突变会导致骨质疏松症。《自然·通讯》,14,2058。https://doi.org/10.1038/s41467-023-37791-4
- Dotta, L.、Notarangelo, L.D.、Moratto, D.、Kumar, R.、Porta, F.、Soresina, A.、Lougaris, V.、Plebani, A.、Smith, C.I.E.、Norlin, A.-C. 等(2019)。18 例 WHIM 综合征患者的长期结局:肺部疾病和 HPV 相关恶性肿瘤的高风险。《变态反应与临床免疫学实践杂志》,7,1568-1577。https://doi.org/10.1016/j.jaip.2019.01.045
- Hernandez, P.A., Gorlin, R.J., Lukens, J.N., Taniuchi, S., Bohinjec, J., Francois, F., Klotman, M.E., 和 Diaz, G.A. (2003). 趋化因子受体基因CXCR4的突变与WHIM综合征(一种联合免疫缺陷病)相关。《自然·遗传学》,34,70-74。https://doi.org/10.1038/ng1149
- Kallikourdis, M., Trovato, A.E., Anselmi, F., Sarukhan, A., Roselli, G., Tassone, L., Badolato, R., 和 Viola, A. (2013). WHIM综合征中的CXCR4突变会损害T细胞免疫突触的稳定性。《血液》122, 666–673。https://doi.org/10.1182/blood-2012-10-461830
- Kawai, T.和Malech, H.L.(2009)。WHIM综合征:先天性免疫缺陷病。《当代血液学观点》,16,20-26。https://doi.org/10.1097/MOH.0b013e32831ac557
- Balabanian, K.、Brotin, E.、Biajoux, V.、Bouchet-Delbos, L.、Lainey, E.、Fenneteau, O.、Bonnet, D.、Fiette, L.、Emilie, D.和Bachelerie, F.(2012)。CXCR4的适当脱敏对小鼠淋巴细胞发育和外周区室化是必需的。《血液》119,5722-5730。https://doi.org/10.1182/blood-2012-01-403378
- Balabanian, K.、Lagane, B.、Pablos, J.L.、Laurent, L.、Planchenault, T.、Verola, O.、Lebbe, C.、Kerob, D.、Dupuy, A.、Hermine, O. 等人(2005)。具有不同遗传异常的WHIM综合征是由CXCR4对CXCL12的脱敏受损引起的。《血液》105,2449-2457。https://doi.org/10.1182/blood-2004-06-2289
- Galli, J.、Pinelli, L.、Micheletti, S.、Palumbo, G.、Notarangelo, L.D.、Lougaris, V.、Dotta, L.、Fazzi, E. 和 Badolato, R.(2019)。疣-低丙种球蛋白血症-免疫缺陷-骨髓细胞滞留患者的小脑受累情况:神经影像学和临床发现。《罕见病杂志》,14,61。https://doi.org/10.1186/s13023-019-1030-8
- Heusinkveld, L.E., Yim, E., Yang, A., Azani, A.B., Liu, Q., Gao, J.-L., McDermott, D.H., 和 Murphy, P.M.(2017)。WHIM综合征免疫缺陷的发病机制、诊断和治疗策略。《孤儿药专家观点》5,813-825。https://doi.org/10.1080/21678707.2017.1375403
- Milanesi, S.、Locati, M. 和 Borroni, E.M.(2020)。异常CXCR4信号在WHIM综合征与华氏巨球蛋白血症的交叉点。《国际分子科学杂志》,21,5696。https://doi.org/10.3390/ijms21165696
- 比安奇(M.E.)和梅扎佩莱(R.)(2020)。趋化因子受体CXCR4在细胞增殖和组织再生中的作用。《免疫学前沿》,11,2109。https://doi.org/10.3389/fimmu.2020.02109
- 麦克德莫特(D.H.)、刘(Q.)、贝莱斯(D.)、洛佩兹(L.)、安纳亚-奥布莱恩(S.)、乌尔里克(J.)、夸特马(N.)、斯塔林(J.)、弗莱舍(T.A.)、普里尔(D.A.L.)等人(2014)。CXCR4拮抗剂普乐沙福长期低剂量治疗WHIM综合征的1期临床试验。《血液》123,2308-2316。https://doi.org/10.1182/blood-2013-09-527226
- 麦克德莫特(D.H.)、贝莱斯(D.)、赵(E.)、考恩(E.W.)、迪乔瓦纳(J.J.)、帕斯特拉纳(D.V.)、巴克(C.B.)、卡尔沃(K.R.)、加德纳(P.J.)、罗森茨威格(S.D.)等(2023)。普乐沙福与G-CSF治疗WHIM综合征的III期随机交叉试验。《临床研究杂志》,133,e164918。https://doi.org/10.1172/JCI164918
- 利维(A. Levy)、蒙迪尼(M. Mondini)和多伊奇(E. Deutsch)(2019)。普乐沙福治疗WHIM综合征。《新英格兰医学杂志》,380,e25。https://doi.org/10.1056/NEJMc1901646
- O¨ zdemir, E.(2022)。成人原发性免疫缺陷病的回顾性评估。《皮肤病与变态反应进展》,39,976-979。https://doi.org/10.5114/ada.2022.120887
- Dehkordy, S.F.、Aghamohammadi, A.、Ochs, H.D.和Rezaei, N.(2012)。与神经系统表现相关的原发性免疫缺陷病。《临床免疫学杂志》,32,1-24。https://doi.org/10.1007/s10875-011-9593-8
- 索尔斯(K.L.)、盖达-切尔德(C.A.)和加兰蒂诺(M.L.)(2020)。原发性免疫缺陷病患者自我报告的认知障碍。《大脑、行为与免疫健康》,9,100170。https://doi.org/10.1016/j.bbih.2020.100170
- Yildirim, M.、Ayvaz, D.C.、Konuskan, B.、Gocmen, R.、Tezcan, I.、Topcu, M.、Topaloglu, H.和Anlar, B.(2018)。原发性免疫缺陷病的神经系统受累。《儿童神经病学杂志》,33,320-328。https://doi.org/10.1177/0883073817754176
- Grossfeld, P.D., Mattina, T., Lai, Z., Favier, R., Jones, K.L., Cotter, F., 和 Jones, C.(2004)。11q末端缺失 disorder:110例前瞻性研究。《美国医学遗传学杂志A辑》129A,51-61。https://doi.org/10.1002/ajmg.a.30090
- Sauer, A.V., Hernandez, R.J., Fumagalli, F., Bianchi, V., Poliani, P.L., Dallatomasina, C., Riboni, E., Politi, L.S., Tabucchi, A., Carlucci, F. 等人(2017)。脑内腺苷代谢的改变导致ADA缺陷小鼠和患者出现行为和神经功能障碍。《科学报告》7,40136。https://doi.org/10.1038/srep40136
- 张宇、余晓、市川M.、莱昂斯J.J.、达塔S.、兰伯恩I.T.、景H.、金E.S.、比安卡拉纳M.、沃尔夫L.A.等(2014)。常染色体隐性磷酸葡萄糖变位酶3(PGM3)突变将糖基化缺陷与特应性、免疫缺陷、自身免疫和神经认知障碍联系起来。《变态反应与临床免疫学杂志》,133,1400–1409,1409.e1–5。https://doi.org/10.1016/j.jaci.2014.02.013
- Ammann, S., Schulz, A., Kra¨ geloh-Mann, I., Dieckmann, N.M.G., Niethammer, K., Fuchs, S., Eckl, K.M., Plank, R., Werner, R., Altmu¨ ller, J., 等. (2016). 与免疫缺陷和癫痫相关的AP3D1基因突变定义了一种新型Hermansky-Pudlak综合征。《血液》127, 997–1006. https://doi.org/10.1182/blood-2015-09-671636
- Bhala, S.、Best, A.F.、Giri, N.、Alter, B.P.、Pao, M.、Gropman, A.、Baker, E. H. 和 Savage, S.A.(2019)。端粒生物学障碍患者的中枢神经系统表现。《神经遗传学》,5,370。https://doi.org/10.1212/NXG.0000000000000370
- Oud, M.M., Tuijnenburg, P., Hempel, M., van Vlies, N., Ren, Z., Ferdinandusse, S., Jansen, M.H., Santer, R., Johannsen, J., Bacchelli, C.等(2017)。EXTL3基因突变导致神经-免疫-骨骼发育异常综合征。《美国人类遗传学杂志》,100,281-296。https://doi.org/10.1016/j.ajhg.2017.01.013
- Versteegh, J.J., Dulfer, K., Stuvel, K., Pasmans, S.G., 和 Utens, E.M.(2020)。Netherton综合征:儿童和成人患者及其父母的神经心理和社会心理功能。《健康心理学杂志》,25,2296-2316。https://doi.org/10.1177/1359105318790052
- Fageeh, H.N.(2018)。帕皮隆-勒菲弗综合征:两兄弟的罕见病例报告及文献复习。《国际临床儿科牙科学杂志》,11,352-355。https://doi.org/10.5005/jp-journals-10005-1538
- Phull, T.、Jyoti, D.、Malhotra, R.、Nayak, S.、Modi, H.、Singla, I. 和 P, A.(2023)。帕皮隆-勒菲弗综合征的诊断与管理:一例罕见病例报告及文献简要回顾。《Cureus》15,e43335。https://doi.org/10.7759/cureus.43335
- 马扎尔(I.)、斯托克斯(J.)、奥利(S.)、洛夫(E.)、埃斯彭森(A.)、巴斯(P.G.)、鲍尔斯(J.H.,三世)和希尔兹(A.L.)(2019)。从成人视角理解巴斯综合征患者的生活经历:一项定性一对一访谈研究。《孤儿病期刊》,14,243。https://doi.org/10.1186/s13023-019-1200-8
- Bolze, A., Byun, M., McDonald, D., Morgan, N.V., Abhyankar, A., Premkumar, L., Puel, A., Bacon, C.M., Rieux-Laucat, F., Pang, K., 等. (2010). 基于全外显子组测序发现人类FADD缺陷. 《美国人类遗传学杂志》, 87, 873-881. https://doi.org/10.1016/j.ajhg.2010.10.028
- Kotlarz, D., Marquardt, B., Barøy, T., Lee, W.S., Konnikova, L., Hollizeck, S., Magg, T., Lehle, A.S., Walz, C., Borggraefe, I., 等. (2018). 人类TGF-β1缺乏会导致严重的炎症性肠病和脑病。《自然·遗传学》,50,344-348。https://doi.org/10.1038/s41588-018-0063-6
- 拉斯(Russ, A.)、麦克(Mack, J.)、格林-墨菲(Green-Murphy, A.)、西方(Occidental, M.)和米安(Mian, A.)(2019)。《2型格里塞利综合征与噬血细胞性淋巴组织细胞增多症:具有相同突变但表现不同的姐妹》。《儿科血液学与肿瘤学杂志》,41,473-477。https://doi.org/10.1097/MPH.0000000000001522
- Savic, S., Parry, D., Carter, C., Johnson, C., Logan, C., Gutierrez, B.M., Thomas, J.E., Bacon, C.M., Cant, A., 和 Hambleton, S. (2015). 一例新的Fas相关死亡结构域蛋白缺乏症病例及治疗结果更新。《变态反应与临床免疫学杂志》,136,502-505.e4。https://doi.org/10.1016/j.jaci.2015.02.002
- 康,H.J.、川泽,Y.I.、程,F.、朱,Y.、徐,X.、李,M.、索萨,A.M. M.、普莱蒂科斯,M.、迈耶,K.A.、塞德马克,G.等(2011)。人类大脑的时空转录组。《自然》478,483-489。https://doi.org/10.1038/nature10523
- 塞普(M.)、莱斯(K.)、穆拉特(F.)、奥科涅奇尼科夫(K.)、乔希(P.)、莱ushkin(E.)、斯潘尼希(L.)、姆本盖(N.)、施耐德(C.)、施密特(J.)等人(2024)。哺乳动物小脑的细胞发育与进化。《自然》625,788-796。https://doi.org/10.1038/s41586-023-06884-x
- 赫尔(Hull, C.)和雷格尔(Regehr, W.G.)(2022)。小脑皮质。《神经科学年度评论》45,151–175。https://doi.org/10.1146/annurev-neuro-091421-125115
- Kozareva, V., Martin, C., Osorno, T., Rudolph, S., Guo, C., Vanderburg, C., Nadaf, N., Regev, A., Regehr, W.G., 和 Macosko, E. (2021). 小鼠小脑皮质转录组图谱全面定义细胞类型。《自然》598,214-219。https://doi.org/10.1038/s41586-021-03220-z
- 莱托(K.)、阿兰西略(M.)、贝克尔(E.B.E.)、布福(A.)、蒋(C.)、丁(B.)、多宾斯(W.B.)、杜萨特(I.)、哈尔迪普尔(P.)、哈滕(M.E.)等人(2016)。共识论文:小脑发育。《小脑》15,789-828。https://doi.org/10.1007/s12311-015-0724-2
- Voogd, J. 和 Glickstein, M.(1998)。小脑的解剖结构。《神经科学趋势》,21,370-375。https://doi.org/10.1016/s0166-2236(98)01318-6
- 德雷塞尔豪斯(E.C.)和梅弗特(M.K.)(2019)。神经系统中NF-κB功能的细胞特异性。《免疫学前沿》,10,1043。https://doi.org/10.3389/fimmu.2019.01043
- 卡尔奇施密特,B.,和卡尔奇施密特,C.(2009)。神经系统中的NF-κB。《冷泉港生物学展望》1,a001271。https://doi.org/10.1101/cshperspect.a001271
- 杜浩、王泽、郭锐、杨莉、刘刚、张哲、徐志、田宇、杨震、李雪等人(2022)。转录因子Bcl11a和Bcl11b是皮质投射神经元生成和分化所必需的。《大脑皮层》32,3611-3632。https://doi.org/10.1093/cercor/bhab437
- 西蒙(Simon, R.)、威格雷夫(Wiegreffe, C.)和布里奇(Britsch, S.)(2020)。Bcl11转录因子调节皮质发育和功能。《分子神经科学前沿》,13,51。https://doi.org/10.3389/fnmol.2020.00051
- 莫利诺(Molyneaux)、戈夫(Goff)、布雷特勒(Brettler)、陈(Chen)、赫尔瓦廷(Hrvatin)、林恩(Rinn)和阿洛塔(Arlotta)(2015)。DeCoN:新皮质锥体神经元命运选择过程中体内转录动态的全基因组分析。《神经元》85,275-288。https://doi.org/10.1016/j.neuron.2014.12.024
- 小泽(P.M.M.)、阿里扎(C.B.)、石桥(C.M.)、藤田(T.C.)、巴宁 - 平田(B.K.)、小田(J.M.M.)和渡边(M.A.E.)(2016)。CXCL12和CXCR4在正常小脑发育和髓母细胞瘤中的作用。《国际癌症杂志》,138,10 - 13。https://doi.org/10.1002/ijc.29333
- 王,Y.,李,G.,斯坦科,A.,朗,J.E.,克劳福德,D.,波特,G.B.,普莱热,S.J.,贝伦斯,T.和鲁宾斯坦,J.L.R.(2011)。CXCR4和CXCR7在调节中间神经元迁移中具有不同功能。《神经元》69,61-76。https://doi.org/10.1016/j.neuron.2010.12.005
- Arpi, M.N.T.和Simpson, T.I.(2022)。SFARI基因及其发现之处:利用RNA-seq数据模拟自闭症谱系障碍特定基因表达失调。《科学报告》12,10158。https://doi.org/10.1038/s41598-022-14077-1
- Alouche, N., Bonaud, A., Rondeau, V., Hussein-Agha, R., Nguyen, J., Bisio, V., Khamyath, M., Crickx, E., Setterblad, N., Dulphy, N. 等 (2021). 血液系统疾病相关的Cxcr4功能获得性突变导致不受控制的滤泡外免疫反应。《血液》137, 3050-3063。https://doi.org/10.1182/blood.2020007450
- Freitas, C., Wittner, M., Nguyen, J., Rondeau, V., Biajoux, V., Aknin, M.-L., Gaudin, F., Beaussant-Cohen, S., Bertrand, Y., Bellanne´-Chantelot, C. 等人(2017)。造血干细胞的淋巴分化需要有效的Cxcr4脱敏。《实验医学杂志》,214,2023-2040。https://doi.org/10.1084/jem.20160806
- Mayol, K., Biajoux, V., Marvel, J., Balabanian, K., 和 Walzer, T.(2011)。CXCR4和S1P5的序贯脱敏调控自然杀伤细胞的迁移。《血液》118,4863-4871。https://doi.org/10.1182/blood2011-06-362574
- Biajoux, V.、Natt, J.、Freitas, C.、Alouche, N.、Sacquin, A.、Hemon, P.、Gaudin, F.、Fazilleau, N.、Espe´li, M. 和 Balabanian, K.(2016)。有效的浆细胞分化和迁移需要Cxcr4脱敏。《细胞报告》,17,193-205。https://doi.org/10.1016/j.celrep.2016.08.068
- Apps, R. 和 Hawkes, R.(2009)。小脑皮质组织:单一图谱假说。《自然综述·神经科学》,10,670-681。https://doi.org/10.1038/nrn2698
- Anyan, J. 和 Amir, S.(2018)。是抑郁得无法游泳还是害怕停下来?将强迫游泳试验重新解读为衡量类焦虑行为的指标。《神经精神药理学》43,931-933。https://doi.org/10.1038/npp.2017.260
- 福克斯,W.M.(1965)。小鼠的反射发生与行为发展。《动物行为》,13,234-241。https://doi.org/10.1016/0003-3472(65)90041-2
- Feather-Schussler, D.N. 和 Ferguson, T.S.(2016)。脑瘫新生小鼠模型中的一系列运动测试。《视觉实验杂志》,117,53569。https://doi.org/10.3791/53569
- 鲍曼(O. Baumann)、博拉(R.J. Borra)、鲍尔(J.M. Bower)、卡伦(K.E. Cullen)、哈巴斯(C. Habas)、艾弗里(R.B. Ivry)、莱焦(M. Leggio)、马丁利(J.B. Mattingley)、莫利纳里(M. Molinari)、莫尔顿(E.A. Moulton)等人(2015)。共识论文:小脑在感知过程中的作用。《小脑》14,197-220。https://doi.org/10.1007/s12311-014-0627-7
- MacNeilage, P.R.和Glasauer, S.(2018)。重力感知:小脑的作用。《当代生物学》,28,R1296-R1298。https://doi.org/10.1016/j.cub.2018.09.053
- Therrien, A.S. 和 Bastian, A.J.(2015)。小脑损伤会损害感觉和运动功能的内部预测。《当代神经生物学观点》,33,127-133。https://doi.org/10.1016/j.conb.2015.03.013
- van der Heijden, M.E., Lackey, E.P., Perez, R., Ișleyen, F.S., Brown, A.M., Donofrio, S.G., Lin, T., Zoghbi, H.Y., 和 Sillitoe, R.V.(2021)。浦肯野细胞放电特性的成熟依赖于兴奋性神经元的神经发生。《eLife》10,e68045。https://doi.org/10.7554/eLife.68045
- 劳顿(A.K.)、恩斯特伦(T.)、罗尔巴赫(D.)、大村(M.)、特恩布尔(D.H.)、马穆(J.)、张(T.)、施瓦茨(J.M.)和乔伊纳(A.L.)(2019)。小脑折叠是由类流体层上的机械约束引发的,不存在细胞预模式。《eLife》8,e45019。https://doi.org/10.7554/eLife.45019
- Consalez, G.G.、Goldowitz, D.、Casoni, F. 和 Hawkes, R.(2020)。小脑颗粒细胞的起源、发育和分区。《神经回路前沿》14,611841。https://doi.org/10.3389/fncir.2020.611841
- Yeung, J.、Ha, T.J.、Swanson, D.J. 和 Goldowitz, D.(2016)。Pax6在小脑发育中的一种新型多价作用。《神经科学杂志》,36,9057-9069。https://doi.org/10.1523/JNEUROSCI.4385-15.2016
- Sudarov, A. 和 Joyner, A.L.(2007)。小脑形态发生:叶片模式由多细胞锚定中心协调。《神经发育》,2,26。https://doi.org/10.1186/1749-8104-2-26
- 佩莱格里诺(L.)、霍达帕拉斯特(S.)和卡布拉尔(J.T.)(2020)。褶皱、等离子体氧化的聚二甲基硅氧烷表面的正交波叠加。《软物质》16,595-603。https://doi.org/10.1039/C9SM02124H
- Oomman, S.、Strahlendorf, H.、Finckbone, V.和Strahlendorf, J.(2005)。出生后大鼠小脑伯格曼神经胶质中非致死性活性半胱天冬酶-3的表达。《脑研究·发育脑研究》,160,130-145。https://doi.org/10.1016/j.devbrainres.2005.07.010
- 古拉蒂(G.S.)、西坎达尔(S.S.)、韦舍(D.J.)、曼朱纳斯(A.)、巴拉德瓦杰(A.)、伯杰(M.J.)、伊拉甘(F.)、郭(A.H.)、谢(R.W.)、蔡(S.)等人(2020)。单细胞转录多样性是发育潜能的标志。《科学》367,405-411。https://doi.org/10.1126/science.aax0249
- 佐藤(M.)、铃木(K.)和中西(S.)(2006)。小脑颗粒细胞发育过程中BDNF应答基因的表达谱。《生物化学与生物物理研究通讯》,341,304-309。https://doi.org/10.1016/j.bbrc.2005.12.184
- Limatola, C.、Giovannelli, A.、Maggi, L.、Ragozzino, D.、Castellani, L.、Ciotti, M.T.、Vacca, F.、Mercanti, D.、Santoni, A.和Eusebi, F.(2000)。SDF-1alpha介导的大鼠小脑突触传递调节。《欧洲神经科学杂志》,12,2497-2504。https://doi.org/10.1046/j.1460-9568.2000.00139.x
- Witter, L.、Rudolph, S.、Pressler, R.T.、Lahlaf, S.I. 和 Regehr, W.G.(2016)。浦肯野细胞侧支使小脑皮层的输出信号能够反馈到浦肯野细胞和中间神经元。《神经元》91,312-319。https://doi.org/10.1016/j.neuron.2016.05.037
- Mapelli, L., Dubochet, O., Tedesco, M., Sciacca, G., Ottaviani, A., Monteverdi, A., Battaglia, C., Tritto, S., Cardot, F., Surbled, P. 等人(2022)。新一代微针3D高密度CMOS多电极阵列用于脑组织和类球体的设计、实现及功能验证。预印本发表于bioRxiv。https://doi.org/10.1101/2022.08.11.503595
- 盖尔(C.B.)、埃利森(M.)、克鲁兹(R.)、帕瓦尔(S.)、莱斯-皮勒(A.)、兹迈科维科娃(K.)、麦克纳尔蒂(S.M.)、伊尔马兹(M.)、埃文斯(M.O.)二世、戈登(S.)等(2022)。66名儿童和成人国际队列中WHIM综合征的疾病进展。《临床免疫学杂志》,42,1748-1765。https://doi.org/10.1007/s10875-022-01312-7
- 埃文斯(M.O.,二世)、麦克德莫特(D.H.)、墨菲(P.M.)和彼得森(M.M.)(2019)。WHIM综合征婴儿的异常新生儿筛查。《临床免疫学杂志》,39,839-841。https://doi.org/10.1007/s10875-019-00686-5
- Ara, T.、Tokoyoda, K.、Sugiyama, T.、Egawa, T.、Kawabata, K.和Nagasawa, T.(2003)。长期造血干细胞在个体发育过程中定植骨髓需要基质细胞衍生因子-1。《免疫》19,257-267。https://doi.org/10.1016/s1074-7613(03)00201-2
- 克里斯滕森(J.L.)、赖特(D.E.)、韦格斯(A.J.)和魏斯曼(I.L.)(2004)。胎儿造血干细胞的循环与趋化作用。《公共科学图书馆·生物学》,2,E75。https://doi.org/10.1371/journal.pbio.0020075
- 邹永仁、Kottmann, A.H.、黑田, M.、谷内, I. 和利特曼, D.R.(1998)。趋化因子受体CXCR4在造血和小脑发育中的功能。《自然》393,595-599。https://doi.org/10.1038/31269
- Alves de Lima, K., Rustenhoven, J., Da Mesquita, S., Wall, M., Salvador, A.F., Smirnov, I., Martelossi Cebinelli, G., Mamuladze, T., Baker, W., Papadopoulos, Z. 等. (2020). 脑膜 γδ T 细胞通过神经元中的 IL-17a 信号调节类焦虑行为. 《自然・免疫学》, 21, 1421-1429. https://doi.org/10.1038/s41590-020-0776-4.
- Goyal, M., Goyal, R., & Sanguinetti, J.L. (2024). 超声刺激迷走神经作为焦虑症的治疗方式. 《精神病学前沿》, 15, 1376140. https://doi.org/10.3389/fpsyt.2024.1376140.
- Fernandes, D.J., Spring, S., Corre, C., Tu, A., Qiu, L.R., Hammill, C., Vousden, D.A., Spencer Noakes, T.L., Nieman, B.J., Bowdish, D.M.E. 等. (2022). 免疫功能障碍的小鼠模型:其神经解剖学差异反映焦虑行为表型. 《分子精神病学》, 27, 3047-3055. https://doi.org/10.1038/s41380-022-01535-5.
- Sawtell, N.B. (2010). 颗粒细胞中的多模态整合作为类小脑回路中联想可塑性和感觉预测的基础. 《神经元》, 66, 573-584. https://doi.org/10.1016/j.neuron.2010.04.018.
- Wang, W.X., & Lefebvre, J.L. (2022). 形态假时间排序和命运图谱揭示小脑抑制性中间神经元的多样化. 《自然・通讯》, 13, 3433. https://doi.org/10.1038/s41467-022-30977-2.
- Silva, C.G., Peyre, E., & Nguyen, L. (2019). 细胞迁移促进动态细胞相互作用以调控大脑皮层形态发生. 《自然评论・神经科学》, 20, 318-329. https://doi.org/10.1038/s41583-019-0148-y.
- Komuro, H., & Yacubova, E. (2003). 小脑颗粒细胞迁移的最新研究进展. 《细胞与分子生命科学》, 60, 1084-1098. https://doi.org/10.1007/s00018-003-2248-z.
- Chin, P.W., & Augustine, G.J. (2023). 小脑与焦虑. 《细胞神经科学前沿》, 17, 1130505. https://doi.org/10.3389/fncel.2023.1130505.
- Moreno-Rius, J. (2018). 恐惧和焦虑相关障碍中的小脑. 《神经精神药理学与生物精神病学进展》, 85, 23-32. https://doi.org/10.1016/j.pnpbp.2018.04.002.
- Wester, J.C., Mahadevan, V., Rhodes, C.T., Calvigioni, D., Venkatesh, S., Maric, D., Hunt, S., Yuan, X., Zhang, Y., Petros, T.J. 等. (2019). 新皮质投射神经元以谱系依赖方式指导抑制性中间神经元回路发育. 《神经元》, 102, 960-975.e6. https://doi.org/10.1016/j.neuron.2019.03.036.
- Lodato, S., Rouaux, C., Quast, K.B., Jantrachotechatchawan, C., Studer, M., Hensch, T.K., & Arlotta, P. (2011). 兴奋性投射神经元亚型调控大脑皮层局部抑制性中间神经元的分布. 《神经元》, 69, 763-779. https://doi.org/10.1016/j.neuron.2011.01.015.
- Wang, S.S.-H., Kloth, A.D., & Badura, A. (2014). 小脑、敏感期与自闭症. 《神经元》, 83, 518-532. https://doi.org/10.1016/j.neuron.2014.07.016.
- Morland, B., Kepak, T., Dallorso, S., Sevilla, J., Murphy, D., Luksch, R., Yaniv, I., Bader, P., Roßler, J., Bisogno, G. 等. (2020). 普乐沙福联合标准方案用于符合自体移植条件的儿童实体瘤患者造血干细胞动员:一项两臂 Ⅰ/Ⅱ 期研究(MOZAIC). 《骨髓移植》, 55, 1744-1753. https://doi.org/10.1038/s41409-020-0836-2.
- Karres, D., Ali, S., van Hennik, P.B., Straus, S., Josephson, F., Thole, G., Glerum, P.J., Herberts, C., Babae, N., Herold, R. 等. (2020). 欧洲药品管理局关于普乐沙福(释倍灵)儿科适应症的建议 —— 用于增强淋巴瘤或恶性实体瘤儿童造血干细胞动员以采集并进行后续自体移植. 《肿瘤学家》, 25, e976-e981. https://doi.org/10.1634/theoncologist.2019-0898.
- López-Bendito, G., Sánchez-Alcañiz, J.A., Pla, R., Borrell, V., Picó, E., Valdeolmillos, M., & Marín, O. (2008). 趋化因子信号调控 γ- 氨基丁酸能中间神经元的皮质内迁移和最终分布. 《神经科学杂志》, 28, 1613-1624. https://doi.org/10.1523/JNEUROSCI.4651-07.2008.
- Chen, T.W., Wardill, T.J., Sun, Y., Pulver, S.R., Renninger, S.L., Baohan, A., Schreiter, E.R., Kerr, R.A., Orger, M.B., Jayaraman, V. 等. (2013). 用于神经元活动成像的超灵敏荧光蛋白. 《自然》, 499, 295-300. https://doi.org/10.1038/nature12354.
- Hao, Y., Hao, S., Andersen-Nissen, E., Mauck, W.M. Ⅲ, Zheng, S., Butler, A., Lee, M.J., Wilk, A.J., Darby, C., Zager, M. 等. (2021). 多模态单细胞数据的整合分析. 《细胞》, 184, 3573-3587.e29. https://doi.org/10.1016/j.cell.2021.04.048.
- Lee, H.Y., Greene, L.A., Mason, C.A., & Manzini, M.C. (2009). 出生后小鼠小脑颗粒神经元祖细胞和神经元的分离与培养. 《可视化实验杂志》, 23, 990. https://doi.org/10.3791/990.
- Krämer, D., & Minichiello, L. (2010). 原代小脑颗粒细胞的细胞培养. 《分子生物学方法》, 633, 233-239. https://doi.org/10.1007/978-1-59745-019-5_17.
- Losi, G., Prybylowski, K., Fu, Z., Luo, J.H., & Vicini, S. (2002). 发育中小脑颗粒神经元中的沉默突触. 《神经生理学杂志》, 87, 1263-1270. https://doi.org/10.1152/jn.00633.2001.
- Wood, T.C. (2018). QUIT:定量成像工具. 《开源软件杂志》, 3, 656. https://doi.org/10.21105/joss.00656.
- Avants, B.B., Tustison, N.J., Song, G., Cook, P.A., Klein, A., & Gee, J.C. (2011). ANTs 相似性度量在脑图像配准中性能的可重复评估. 《神经影像》, 54, 2033-2044. https://doi.org/10.1016/j.neuroimage.2010.09.025.
- Avants, B.B., Epstein, C.L., Grossman, M., & Gee, J.C. (2008). 基于互相关的对称微分同胚图像配准:评估老年人和神经退行性疾病大脑的自动标记. 《医学影像分析》, 12, 26-41. https://doi.org/10.1016/j.media.2007.06.004.
- Winkler, A.M., Ridgway, G.R., Webster, M.A., Smith, S.M., & Nichols, T.E. (2014). 一般线性模型的置换推断. 《神经影像》, 92, 381-397. https://doi.org/10.1016/j.neuroimage.2014.01.060.
- van der Walt, S., Schönberger, J.L., Nunez-Iglesias, J., Boulogne, F., Warner, J.D., Yager, N., Gouillart, E., Yu, T., 及 scikit-image 贡献者. (2014). scikit-image:Python 中的图像处理. 《PeerJ》, 2, e453. https://doi.org/10.7717/peerj.453.
- Nunez-Iglesias, J., Blanch, A.J., Looker, O., Dixon, M.W., & Tilley, L. (2018). 一种新型 Python 骨架图像分析库证实疟原虫对红细胞膜骨架的重塑. 《PeerJ》, 6, e4312. https://doi.org/10.7717/peerj.4312.
- Boitnott, A., Garcia-Forn, M., Ung, D.C., Niblo, K., Mendonca, D., Park, Y., Flores, M., Maxwell, S., Ellegood, J., Qiu, L.R. 等. (2021). DDX3X 综合征小鼠模型的发育和行为表型. 《生物精神病学》, 90, 742-755. https://doi.org/10.1016/j.biopsych.2021.05.027.
- Heyser, C.J. (2004). 啮齿类动物发育里程碑的评估. 《当代神经科学实验指南》, 第 8 章,第 8.18 单元. https://doi.org/10.1002/0471142301.ns0818s25.
- Livak, K.J., & Schmittgen, T.D. (2001). 利用实时定量 PCR 和 2 (-ΔΔC (T)) 法分析相对基因表达数据. 《方法学》, 25, 402-408. https://doi.org/10.1006/meth.2001.1262.
- Luo, W., Lin, G.N., Song, W., Zhang, Y., Lai, H., Zhang, M., Miao, J., Cheng, X., Wang, Y., Li, W. 等. (2021). 单细胞空间转录组分析揭示出生后小脑颗粒细胞与髓母细胞瘤的共同及差异特征. 《BMC 生物学》, 19, 135. https://doi.org/10.1186/s12915-021-01071-8.
- Sun, Z., & Südhof, T.C. (2021). 一种用于培养神经元神经网络分析的简单钙成像方法. 《神经科学方法杂志》, 349, 109041. https://doi.org/10.1016/j.jneumeth.2020.109041.
- Pilpel, N., Landeck, N., Klugmann, M., Seeburg, P.H., & Schwarz, M.K. (2009). 靶向重组病毒注射新生小鼠大脑实现特定前脑区域的快速可重复转导. 《神经科学方法杂志》, 182, 55-63. https://doi.org/10.1016/j.jneumeth.2009.05.020.
- Kaneko, M., Yamaguchi, K., Eiraku, M., Sato, M., Takata, N., Kiyohara, Y., Mishina, M., Hirase, H., Hashikawa, T., & Kengaku, M. (2011). 小脑回路形成过程中单层浦肯野细胞树突的重塑. 《公共科学图书馆・综合》, 6, e20108. https://doi.org/10.1371/journal.pone.0020108.
- Fujishima, K., Horie, R., Mochizuki, A., & Kengaku, M. (2012). 调控小脑浦肯野细胞树突形态特征的分支动力学原理. 《发育》, 139, 3442-3455. https://doi.org/10.1242/dev.081315.
- Gibson, D.A., & Ma, L. (2011). 利用病毒介导的 Cre 重组技术对出生后小鼠脑发育中基因功能的嵌合体分析. 《可视化实验杂志》, 54, 2823. https://doi.org/10.3791/2823.
- Arganda-Carreras, I., Fernández-González, R., Muñoz-Barrutia, A., & Ortiz-de-Solorzano, C. (2010). 组织切片的三维重建:在乳腺组织中的应用. 《显微镜研究与技术》, 73, 1019-1029. https://doi.org/10.1002/jemt.20829.
¶ STAR★方法
¶ 关键资源表
| REAGENT or RESOURCE | SOURCE | IDENTIFIER |
|---|---|---|
| Antibodies | ||
| Anti-Calbindin (mouse monoclonal) | Swant | Cat#300; RRID: AB_10000347 |
| Anti-Pax6 (rabbit polyclonal) | Sigma-Aldrich | Cat#AB2237; RRID: AB_1587367 |
| Anti-Iba1 (rabbit polyclonal) | Fujifilm | Cat#019-19741; RRID: AB_839504 |
| Anti-BLBP (rabbit polyclonal) | Merck Millipore | Cat#ABN14; RRID: AB_10000325 |
| Anti-RFP (rabbit polyclonal) | Rockland | Cat#600-401-379; RRID: AB_2209751 |
| Anti-CD45 | Biolegend / BD | Cat#103139/564225; RRID: AB_2716861 |
| Anti-CD19 | BD | Cat#562045/612971; RRID: AB_2870243 |
| Anti-CD3e | Invitrogen | Cat#15-0031-81; RRID: AB_157163 |
| Anti-Ly-6C | BD | Cat#560596; RRID: AB_1727555 |
| Anti-CCR2 | Biolegend | Cat#150605; RRID: AB_2571913 |
| Anti-CX3CR1 | Biolegend | Cat#149027 RRID: AB_2565967 |
| Anti-CD49b | BD | Cat#740704; RRID: AB_2740388 |
| Anti-CD11b | BD | Cat#563553; RRID: AB_2738276 |
| Anti-CD4 | BD | Cat#612952; RRID: AB_2813886 |
| Anti-CD8 | BD | Cat#612898; RRID: AB_2870186 |
| Anti-Ly-6G | BD | Cat#560601; RRID: AB_1727562 |
| Anti-CD86 | Biolegend | Cat#567201/566513; RRID: AB_2734770 |
| Bacterial and virus strains | ||
| pAAV-hSyn-GCaMP6s-WPRE | Douglas Kim & GENIE Project; Chen et al.¹²² | Addgene, Cat#100843 |
| pAAV-hSyn-mCherry | Karl Deisseroth Lab | Addgene, Cat#114472 |
| Biological samples | ||
| Cerebellar tissue from Cxcr4+/fl13 and WT mice | This paper | N/A |
| Liver, spleen, blood from Cxcr4+/fl13 and WT mice | This paper | N/A |
| Chemicals, peptides, and recombinant proteins | ||
| Poly-L-lysine | Sigma-Aldrich | Cat#P2636 |
| Neurobasal medium | Life Technologies | Cat#21103049 |
| Fetal Bovine Serum (FBS) | Life Technologies | Cat#1600004 |
| B-27 Supplement | Life Technologies | Cat#17504001 |
| Penicillin-Streptomycin | Euroclone | Cat#ECB3001 |
| Cytosine arabinofuranoside (AraC) | Sigma-Aldrich | Cat#C1788 |
| Topoisomerase Dissociation System | Worthington Biochemical | Cat#LK003150 |
| AMD3100 (Plerixafor) | Sigma-Aldrich | Cat#239825 |
| Eukitt Mounting Medium | Sigma-Aldrich | Cat#3989 |
| Violet stain | Sigma-Aldrich | Cat#C1791 |
| Glacial Acetic Acid | Sigma-Aldrich | Cat#A6283 |
| Fluoromount | Thermo Fisher Scientific | Cat#F4680 |
| LIVE/DEAD Aqua Dead Cell Stain Kit | Thermo Fisher Scientific | Cat#L34957 |
| DAPI | Thermo Fisher Scientific | Cat#D1306 |
| Critical commercial assays | ||
| RNeasy Mini Kit | Qiagen | Cat#74106 |
| QuantiTec Reverse Transcription Kit | Qiagen | Cat#205313 |
| PowerTrack SYBR Green Master Mix | Thermo Fisher Scientific | Cat#A4611 |
| Deposited data | ||
| Single cell gene expression datasets | GEO | GSE266671 |
| fMRI data | OpenNeuro | doos05137 |
| Experimental models: Organisms/strains | ||
| Cxcr4fl13 Knock-in mice | Institut Pasteur; Balabanian et al.³⁸ | N/A |
| Wild type C57BL/6J mice | Jackson Laboratory | Cat#000664 |
| Oligonucleotides | ||
| IL17ra primer fw: CCTCATCACACTCCATCGCCA | This paper | N/A |
| IL17ra primer rev: GCCGAGTAGACGATCCAGAC | This paper | N/A |
| Software and algorithms | ||
| GraphPad Prism (v10.0.0) | GraphPad | www.graphpad.com |
| R (v.4.3.1) | R Project | www.r-project.org |
| Seurat (v.4.4.0) | Hao et al.¹²³ | https://satijalab.org/seurat/ |
| Fiji (ImageJ) | NIH | https://imagej.net/Fiji |
| FlowJo (v10.10.0) | BD | https://www.flowjo.com/ |
| MATLAB | MathWorks | www.mathworks.com |
¶ 实验模型和研究参与者详情
¶ 动物
所有实验均按照欧洲共同体理事会(2010年9月22日第2010/63/EU号指令)和意大利第26/2014号法令确立的指南进行。该研究已获得Humanitas研究医院的机构动物护理和使用委员会(IACUC)以及意大利卫生部的批准。小鼠被饲养在特定无病原体(SPF)设施中,环境温度恒定(22±1℃),湿度为50%,光照/黑暗周期为12小时,可自由获取食物和水。SPF条件确保动物从未接触过免疫挑战。WHIM相关突变体Cxcr4+/1013敲入小鼠由Arenzana-Seisdedos教授慷慨提供,最初在巴斯德研究所生成,并饲养在C57BL/6J背景下。实验组包括从胚胎第16.5天(E16.5)到出生后第45天(P45)的同窝小鼠。在所有测量参数中均未观察到基于性别的差异。除成年行为测试仅使用年龄匹配的同窝雄性小鼠外,所有实验的结果均汇总了不同性别的数据。
对于定时妊娠,将Cxcr4+/1013基因敲入雄性小鼠与最多3只C57BL/6J雌性小鼠(购自Charles River实验室) overnight同笼饲养,次日早晨通过观察到阴栓来确认交配成功。本研究中使用的所有动物均为无实验史动物,之前未接触过AMD3100或其他干预措施。
¶ 原代颗粒细胞培养物
颗粒细胞培养物按照先前报道的方法获得124–126。每个实验至少使用来自至少两个不同窝的每种基因型4只出生后第5天(P5)的幼鼠。将颗粒细胞以约600,000个细胞/mL的密度接种在涂有聚-L-赖氨酸(#P2636,Sigma-Aldrich)的盖玻片上,培养于Neurobasal培养基(#21103049,Life Technologies)中,该培养基添加了10%胎牛血清(FBS,#1600004,Life Technologies)、0.5%无血清补充剂B-27(#17504001,Thermo Fisher Scientific)和100国际单位/mL的青霉素-链霉素(#ECB3001,Euroclone)。培养物在37℃、5% CO₂条件下孵育。24小时后,更换为新鲜的Neurobasal培养基,其中添加10% FBS、0.5%无血清补充剂B-27、100国际单位/mL的青霉素-链霉素、10μM阿糖胞苷(以消除增殖的非神经细胞,如内皮细胞和小胶质细胞)以及25mM氯化钾(通过轻度去极化促进颗粒细胞存活)。
在体外培养第4天(DIV4),将培养基更换为新鲜的Neurobasal培养基,其中添加了10%的胎牛血清(FBS)、0.5%的无血清补充剂B-27、100国际单位/毫升的青霉素-链霉素(Pen-Strep)、10μM的阿糖胞苷以及5mM的氯化钾(KCl),以促进功能性突触的形成。
¶ 方法详情
¶ 人类大脑中与IEI相关基因的数据集及分析
为了探究人类大脑中与原发性免疫缺陷(IEI)相关的基因表达,我们首先利用一个经过验证的分类系统(https://www.niaid.nih.gov/diseases-conditions/types-IEI,来源:国际免疫学会联盟,IUIS),整理出了526种遗传性IEI及其对应的444个致病基因。27,28随后,我们利用BrainSpan发育转录组65和单核RNA测序66数据集来分析基因表达模式。
我们利用了BrainSpan数据集,该数据集包含标准化的表达数据(RPKM),这些数据汇总了25个脑结构和31个年龄段的基因,这些基因被系统地分为7种不同的区域类型(PFC,前额叶皮层;CTX,大脑皮层;HP,海马体;CB,小脑;STR,纹状体;AMY,杏仁核;以及TH,丘脑)和8个发育时期(产前早期、产前晚期、婴儿晚期、幼儿早期、儿童晚期、青春期和成年期)。我们提取了444个目标基因(GOI,表S2)的表达数据,并使用层次聚类分析进行基因聚类,将区域类型和发育时期均作为关键分组变量。为了确定最佳聚类数量(k),我们采用了轮廓系数,选择使该指标最大化的值。为了能够识别不同的基因表达模式,我们绘制了不同区域和发育阶段的平均标准化基因表达图。为了在单核分析中捕捉关键发育时期基因表达的动态变化,我们重点关注了一个子集,该子集包含10个时间点中的9个(排除成年阶段),且仅包含健康受试者。使用“SCTransform()”对每个时间点的数据进行标准化,然后对标准化数据使用“RunHarmony()”进行降维,以整合数据用于可视化,同时不改变原始注释。为了专门分析目标基因的表达模式,我们计算了不同细胞类型的平均基因表达。结果以点图形式展示在图1G中。
¶ 体外磁共振成像
动物首先经心脏灌注含肝素的生理盐水,随后灌注溶于PBS的4%多聚甲醛(PFA),之后进行断头处理。去除皮肤、耳朵和下颌,将大脑留在颅骨内,以最大限度减少因解剖造成的组织损伤和变形。然后,每个大脑在4% PFA溶液中孵育24小时,之后放入含有0.05%(重量/体积)叠氮化钠的0.1M PBS中。样本随后被送往伦敦国王学院,并在该溶液中于4℃下储存3-4个月,以实现组织再水化。在进行离体MRI采集前60天,将样本转移至含8mM钆布醇(Gadovist,拜耳公司)的0.1M PBS和0.05%叠氮化钠溶液中。MRI检查人员对实验组情况不知情。每次同时扫描4个样本,将其固定在定制的3D打印支架中,该支架置于50毫升Falcon管内,管中充满全氟聚醚(Galden SV80,Apollo Scientific),使用39毫米正交发射/接收容积线圈(RAPID Biomedical),在配备B-GA12SHP梯度系统(1000 mT/m)和由ParaVision 7.0.0控制的Avance™ III HD控制台的9.4T BioSpec 94/20(Bruker BioSpin)上进行扫描。使用3D FLASH序列获取40微米各向同性分辨率的图像,参数如下:回波时间=6毫秒,重复时间=20毫秒,翻转角=33°,读出带宽=100千赫兹,平均次数=7,矩阵大小=625×625×500,视野=25×25×20毫米,扫描时间=14小时。
在ParaVision 7.0.0中重建了幅度和相位图像,并使用BrkRaw将其转换为NIfTI格式。使用定量成像工具(QUIT)中的unwrap_path命令对相位图像进行解缠。127 所有22名受试者的幅度和相位图像用于通过高级归一化工具(ANTs)中的antsMultivariateTemplateConstruction2.sh脚本创建特定于多变量研究的模板。128 然后,使用antsRegistration通过连续的刚体、仿射和微分同胚(SyN算法)变换将所有受试者配准到模板。129 使用ANTs命令CreateJacobianDeterminantImage生成这些复合变换的对数转换雅可比行列式图。为了对WHIM和WT大脑的局部体积进行体素级比较,使用FSL randomize130对对数雅可比图像进行排列测试(5000次排列、无阈值聚类增强和家族式错误率控制)。
每张单独的幅值图像都使用antsRegistration与模板进行刚性对齐,并围绕小脑进行裁剪。在Fiji中,先应用半径为2个体素(80微米)的3D中值滤波,然后生成矢状面中央10个体素的最小强度投影,最后使用半径为3、掩模权重为0.7进行反锐化掩模处理。使用魔棒工具从这个滤波后的图像中半自动分割出小脑髓质。对模板图像执行相同的操作,再使用antsRegistration将每个受试者分割出的中央矢状面小脑髓质与模板的进行刚性配准。在python中,使用scikit-image 0.21.0(skimage.morphology.skeletonize)构建小脑髓质的骨架,131并使用Skan 0.11.1(skan.summarize)测量骨架的分支长度。132根据连接点/端点坐标将分支自动分配到小脑小叶,这些坐标也由skan.summarize返回。
¶ 成年小鼠的行为测试
行为测试在光照阶段进行,45日龄小鼠在开始前先在测试室适应30分钟。同一天对两种基因型的小鼠按随机顺序进行测试,数据记录和分析时对基因型设盲。
¶ 旷场试验方面
通过视频追踪记录小鼠在30分钟旷场实验中的活动情况。该区域被虚拟划分为外围和中心。针对这些区域中的每一个,分析了停留时间(秒)、移动距离(厘米)、直立次数(动物自由站立或触碰旷场边缘)、直立时间、移动时间、休息时间(秒)以及移动速度(厘米/秒)。
¶ 对于加速转棒实验
我们使用了加速旋转棒(Panlab,#76-0770)。从P45开始对小鼠进行测试。将它们放在旋转棒上,让它们熟悉环境。旋转棒电机最初以4转/分钟的速度启动,每8秒加速1转/分钟,最高达到40转/分钟,持续300秒。动物每天进行5次试验,共持续4天。以掉落潜伏期(秒)作为表现评分,并取平均值用于统计分析。
¶ 明暗箱实验
将小鼠置于光亮箱中央,允许其在两个箱室中探索10分钟并进行记录。分析的行为表现如下:在光亮箱中停留的时间(秒)、在黑暗箱中停留的时间(秒)、潜伏期(秒)以及箱室间的穿梭次数。
¶ 对于强迫游泳试验
动物被置于开放式水容器中,水温保持在23±2℃;经过两分钟的适应期后,在4分钟的测试时段内测量其活动时间和不动时间(秒)。
¶ 对于埋埋珠测试
在一个常规的干净笼子里对小鼠进行测试,笼子里有12颗玻璃弹珠,这些弹珠放在垫料下方,以3×4的排列方式等距分布,覆盖整个笼子区域。将实验对象放入测试笼中,让它们探索并掩埋弹珠,时长10分钟。实验结束时,统计被掩埋的弹珠数量(超过50%的弹珠被垫料覆盖即视为被掩埋)。
¶ 用于自我梳理测试
动物被置于一个空旷、干净的场地中,场地内铺有一层薄垫料,允许它们自由活动10分钟。实验过程中记录了每只小鼠自我梳理的时间。
¶ 发育里程碑测试
发育里程碑是按照既定协议进行评估的,并改编自Fox量表。来自独立窝的幼崽每天在固定时间接受处理,以评估其身体发育情况。所有评估均在对基因型不知情的情况下进行和评分。参数分为体重、运动技能和感觉反射,并按以下方式进行评估。在出生后第0天、第7天、第15天、第20天、第30天和第45天测量体重(克)。其他发育里程碑在出生后第7天至第15天之间进行测试。
¶ 运动技能
通过行走、负趋地性、表面翻正、空中翻正和开阔场地穿越测试来评估运动活动。在行走测试中,幼鼠在透明围栏中被观察3分钟,其活动情况按0到3分进行评分。负趋地性测试测量幼鼠在30秒的试验时间内,在倾斜平面上完成180度转身所花费的时间。表面翻正测试评估幼鼠被背朝下放置后,在30秒内翻转至俯卧姿势所需的时间。空中翻正测试衡量幼鼠从15厘米高度落下时四肢着地的能力。在开阔场地穿越测试中,我们测量小鼠从放置在纸张上的直径13厘米的圆圈内走出所花费的时间。
¶ 感觉反射
通过悬崖回避、前肢抓握、耳朵抽搐和听觉惊跳测试来评估反射能力的发育情况。在悬崖回避测试中,幼崽被放置在箱子边缘,在3次各30秒的试验中,测量其转身并爬开的潜伏时间。如果幼崽在规定时间内没有从悬崖边转身,则该测试被视为失败。
记录了用棉签轻触耳朵时耳抽动反射的发育情况。对于前肢抓握测试,将幼崽释放,使其前爪放在一根悬挂的棍子上,然后测量抓握的持续时间。听觉惊跳测试则记录了幼崽对记录仪拍手声的非自愿跳跃反应。
¶ 尼氏染色
组织用含4%多聚甲醛(PFA)的1x PBS固定,使用Leica VT1000S振动切片机获得50μm厚的切片,使用Histo-Line MC4000冷冻切片机获得15μm厚的切片。
尼氏染色剂在使用前一天制备,成分包括1%的紫药水(Sigma-Aldrich公司,货号#C1791)、1%的冰醋酸(Sigma-Aldrich公司,货号#A6283)以及双蒸水,并经过过滤处理。选取不同耳间水平的小脑矢状切片(蚓部:0.00至0.24;半球:1.56至2.04、2.16至2.52),将其干燥后,用双蒸水水合,再用尼氏染色剂染色10分钟,之后用双蒸水冲洗,经浓度递增的乙醇梯度脱水,二甲苯透明,最后用Eukitt快干封片剂(Sigma-Aldrich公司,货号#03989)封片。
¶ 实时定量聚合酶链式反应
取P45小鼠的小脑,用TRIzol(货号15596018,赛默飞世尔科技)裂解,然后按照制造商说明提取总RNA。使用Nanodrop(赛默飞世尔科技)通过分光光度法对纯化的RNA进行定量,取500 ng RNA,按照制造商的规格,使用QuantiTec逆转录试剂盒(货号205313,凯杰公司)逆转录为cDNA。实时定量聚合酶链反应(RT-qPCR)采用PowerTrack™ SYBR Green Master Mix(货号A4611,赛默飞世尔科技)进行,以GAPDH作为内参。使用Viia7实时PCR系统(赛默飞世尔科技)进行循环反应,采用2-ΔΔCt法(Livak和Schmittgen,2001135)分析相对基因表达量。对所有独立生物学重复的循环阈值取三个技术重复的平均值,并根据这些平均值进行进一步计算。每个RNA样本均使用以下引物分析IL17ra:IL17ra:正向引物=CCTCATCACACTCATCGCCA,反向引物=GCCGAGTAGACGATCCAGAC。
¶ 叶理分析
我们对胚胎第17.5天(E17.5)和出生后第0天(P0)小脑矢状切片的免疫荧光图像进行了形态计量分析。该分析包括测量切片的精确轮廓以获取外颗粒层(EGL)长度,以及代表外颗粒层平滑长度的凸长度(即EGL0)。此外,我们还测定了由外颗粒层边界界定的总面积,以及小脑切片外平滑边界和内平滑边界所围成的面积。这些参数有助于评估施加在小脑双层结构上的机械应变(ϵ)。
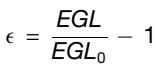
以及由此产生的褶皱幅度。具体而言,我们研究了在软双层材料中诱发正弦褶皱不稳定性时产生的应变(ϵ)与褶皱幅度(A)之间的关系。在低机械变形下(即E17.5时)出现的折叠模式的幅度与应变之间的关系采用以下方程建模(https://doi.org/10.1039/C9SM02124H):
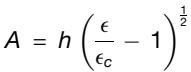
其中h是EGL层的厚度,εc是触发不稳定性必须超过的临界应变。临界应变通过以下关系取决于两层的刚度比
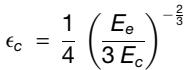
其中Ee和Ec分别是外层的面内弹性模量和芯层的面内弹性模量。超出低变形极限(ϵ > 10%)后出现的模式,即所谓的“高变形(HD)”状态(即在P0时),使用以下方程进行建模(https://doi.org/10.1039/C9SM02124H):
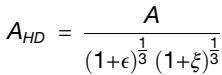
其中ξ = 5 ϵ (1 + ϵ)=32说明了应力-应变响应中的非线性(neo-Hookean行为)。高变形模型还能更好地体现褶皱模式向类折叠不稳定性的演变,这是发育完全的小脑褶皱的典型特征,与低变形模型所描述的纯正弦模式不同,后者更能体现褶皱的起始和初始阶段。
¶ 单细胞RNA测序与分析 样本制备
对照组和Cxcr4+/1013幼鼠(每窝每个样本n=8个胚胎)的P0小脑fpc周围区域(LIII和LIV-V)在无菌条件下,于显微镜控制下在冰冷的HBSS溶液中快速解剖。为减少性别影响,对照组和Cxcr4+/1013样本中均采用雌雄数量均衡的混合样本。按照制造商说明,使用木瓜蛋白酶解离系统试剂盒(#LK003150,Worthington)对解剖的组织进行解离。每个样本约10,000个细胞加载到Single Cell Chip G中,使用Single Cell 30 v2.1单细胞试剂试剂盒(10X Genomics)在Chromium系统中生成凝胶珠乳液。捕获和裂解后,按照制造商的方案(10X Genomics)进行cDNA合成并扩增14个循环。然后,每个样本取50 ng扩增的cDNA用于构建Illumina测序文库。按照10X Genomics的读数生成说明,在NovaSeq 6000 Illumina测序平台上进行测序。
¶ 单细胞RNA测序分析
使用Illumina bcl-convert工具将原始测序数据转换为fastq文件。使用CellRanger(10X Genomics,版本6.1.1.113)的count模块,采用默认设置,并将序列长度设为r1-length=28、r2-length=90,以预构建的小鼠基因组(版本mm10-1.2.0)为参考进行读数比对和计数。每个样本平均产生45,000个读数/细胞。使用Seurat R123包(版本4.4.0)在R(版本4.3.1)中导入原始数字基因表达矩阵(每个基因/细胞的UMI计数)。简要来说,样本质量控制通过以下方式进行评估:对每个样本,筛选掉符合以下任一标准的细胞:计算表达基因和UMI计数的log10(中位数绝对偏差,MAD),过滤掉偏离中位数2.5个MAD(上限和下限)的细胞,以及线粒体基因读数占比超过10.0%或核糖体基因读数占比低于5.0%的细胞。计算MAD后,进行基因筛选:去除在少于中位数-2.5个MADs的细胞中表达的基因,以及Y染色体上表达的基因、XIST和TSIX,以去除与性别相关的基因表达,同时也去除核糖体基因。
对于每个细胞,将特征计数除以该细胞的总计数,再乘以10000,然后使用log1p进行自然对数转换。之后,根据G2/M期和S期标志物的表达情况,为各个细胞分配细胞周期评分。
为了整合数据,使用了Seurat的SCT v2流程:样本通过“SCTransform(vst.flavor = “v2”,assay = “RNA”)”进行单独标准化,然后通过“SelectIntegrationFeatures”函数选择整合特征,接着进行“PrepSCTIntegration”“FindIntegrationAnchors”和“IntegrateData(normalization.method = “SCT”)”操作。
然后,我们对标准化数据进行了主成分分析(PCA),并使用基于图形的方法(肘部图)来选择要使用的主成分数量。随后,我们使用Louvain算法(在Seurat软件中)对细胞进行聚类,以迭代方式将细胞分组。通过分析聚类树图(clustree)来选择最佳分辨率。为了对聚类进行注释,我们使用Seurat中内置的FindAllMarkers函数确定差异表达基因(采用Wilcoxon秩和检验,并通过Bonferroni校正进行多重检验;校正后的P<0.05)。我们仅检测那些在聚类中至少40%的细胞中被发现,且在该聚类中的细胞与所有其余细胞之间平均显示出至少0.25倍差异(对数尺度)的基因。通过查阅所得的标志物,以及经典标志物基因的表达和文献中的其他标志物66,136,我们确定了细胞类型身份。
¶ 细胞类型特异性差异基因表达分析
为了确定差异表达基因,我们使用了Seurat软件包中的FindMarkers函数,该函数采用默认的两部分 hurdle模型(MAST),仅对在至少20%的簇内细胞中存在且在不同基因型间平均表现出至少0.10倍差异(对数尺度)的基因进行检验。差异表达基因列表通过Ingenuity Pathway Analysis(IPA——Qiagen Ingenuity Systems)的经典通路和生物学功能富集进行分析。
¶ 轨迹推断和伪时间评分
在轨迹推断和伪时间评分方面,我们首先对Seurat对象进行子集化,仅保留GCPs和GCs。在这个子集化对象上使用UMAP进行降维,以便在降维空间中可视化高维数据。为了确定轨迹的起点,我们采用了一种基于熵的方法,该方法使用TSCAN包1.40.0中的“perCellEntropy()”函数计算每个细胞的熵。为了推断轨迹并分配伪时间评分,我们使用了Slingshot 2.10.0算法。选择GCP-B簇作为起点(“根”),并基于UMAP降维后的维度进行伪时间评分。使用slingshot()函数拟合轨迹,并应用“slingCurves()”获取谱系曲线数据。为了评估不同基因型之间伪时间分布差异的显著性,我们使用“ks.test()”函数进行了柯尔莫哥洛夫-斯米尔诺夫(KS)检验。该检验比较了野生型和Cxcr4+/1013突变基因型之间伪时间评分的密度分布。
¶ 沿伪时间的差异表达分析
我们使用Tradeseq软件包1.16.0中的“fitGAM()”函数来模拟基因表达沿假时间以及在不同基因型间的变化,每个条件使用6个节点来拟合模型。利用“associationTest()”函数进行沿假时间的差异表达分析,以评估在轨迹上表达发生显著变化的基因。为了评估每个条件下通过错误发现率(FDR)阈值(FDR≤0.05)的基因,我们应用“p.adjust()”函数对p值进行校正。通过筛选符合FDR阈值的基因,生成了两种基因型的最终基因列表。
¶ 多电极阵列分析 体外急性小脑切片制备
P21的动物用异氟烷深度麻醉后断头。立即解剖大脑,将其置于冰冷的溶液中,该溶液的组成如下(mM):87氯化钠、21碳酸氢钠、1.25磷酸二氢钠、7氯化镁、0.5氯化钙、2.5氯化钾、25D-葡萄糖和7蔗糖,用95%氧气和5%二氧化碳平衡(pH7.4)。使用振动切片机(Leica VT1000S)切取小脑蚓部的旁矢状切片(300μm),然后在室温下于33℃的人工脑脊液(ACSF)中孵育至少1小时,人工脑脊液的组成如下(mM):129氯化钠、21碳酸氢钠、1.25磷酸二氢钠、1.8硫酸镁、1.6氯化钙、3氯化钾、10D-葡萄糖,用95%氧气和5%二氧化碳平衡(pH7.4)。记录期间,使用蠕动泵(申辰)以3.0 mL/min的速度向切片灌注ACSF溶液。
¶ 多电极阵列电生理记录
电生理记录采用二维高密度多电极阵列(HD-MEA,3Brain)进行,该阵列由4096个电极组成,电极间距为81μm,总记录面积为5.1×5.1 mm²(HD-Stimulo)。使用带有100μm宽导线的铂锚将切片固定在芯片上。平衡10分钟后,在标准ACSF溶液中以20kHz的采样率记录小脑切片的自发活动,持续5分钟,同时使用50Hz高通滤波器。每次记录结束时,使用高清数字显微镜(Bysameyee)拍摄切片的高清(HD)图像,随后将其与活动图叠加,以确保每个脑叶都有精确的电-解剖学关联。
¶ MEA数据分析
使用3Brain公司的BrainWave 4软件进行记录、尖峰检测和尖峰分类。为评估尖峰检测效果,我们采用了设置为-70μV的硬阈值算法(不应期=1ms,人工智能验证),而单个电极上的尖峰分类则通过具有3个特征的主成分分析(PCA)和标准k均值聚类算法计算得出。每个记录环节均包含对照组和Cxcr4+/1013基因型。仅将尖峰率高于0.8次/秒且每个脑叶活跃单位超过10个的记录纳入分析。若某一基因型的切片记录均未满足这两个标准,则整个实验不被纳入考量。已测量每个脑叶的平均放电率(MFR)和振幅的中值。此外,核密度估计(KDE)已被用于可视化和分析数据分布。数据分析采用非参数化的t检验(曼-惠特尼检验),以评估对照组和Cxcr4+/1013切片同一小脑 lobe内的频率和振幅指标。
¶ 肝、脾、血液和小脑来源的免疫细胞集合
取E16.5时期的胚胎进行解剖,收集肝脏、脾脏和小脑,在40μm细胞筛上研磨。将研磨后的组织置于1×裂解缓冲液(8.29g/L氯化铵#A9434、1g/L碳酸氢钾#60339、0.0372g/L乙二胺四乙酸二钠二水合物#ED2SS)中10分钟,清洗后,用活力标志物和直接偶联的一抗对细胞进行染色。用4%多聚甲醛固定细胞,在BD LSR Fortessa或FACSymphony细胞分析仪上获取样本。
对出生当天(P0)的幼鼠进行解剖,收集脾脏和小脑,在40 μm细胞滤网中研磨。研磨后的组织在1x裂解缓冲液中放置10分钟,然后洗涤,接着用活力标志物和直接偶联的一抗对细胞进行染色。用4%多聚甲醛固定细胞,样本在BD LSR Fortessa或FACSymphony细胞分析仪上进行采集。
在P0和P7时通过断头收集血液。在P45时,从侧尾静脉收集血液:用70%酒精清洁采集部位后,固定小鼠,轻轻划破侧尾静脉并获取样本。收集80-100μL后,用无菌纱布按压止血以停止出血。样本中的红细胞用1x裂解缓冲液去除,并用活力标记物和直接偶联的一抗染色。细胞用4%多聚甲醛固定,向样本中加入计数微球,然后在BD LSR Fortessa或FACSymphony细胞分析仪上进行检测。使用的活力标记物为LIVE/DEAD Fixable Aqua死细胞染色试剂盒(#L34957,赛默飞世尔科技),使用的一抗包括:抗CD45(#103139,Biolegend)、抗CD45(#564225,BD)、抗CD19(#560245,BD)、抗CD19(#612971,BD)、抗CD3e(#15-0031-81,eBioscience)、抗Ly-6C(#560596,BD)、抗CCR2(#150605,Biolegend)、抗CX3CR1(#149027,Biolegend)、抗CD49b(#740704,BD)、抗CD11b(#563553,BD)、抗CD4(#612952,BD)、抗CD8(#612898,BD)、抗Ly-6G(#560601,BD)、抗F4/80(#567201,BD)、抗F4/80(#565613,BD)、CD86(#105016,Biolegend)。数据通过FlowJo(版本10.10.0)进行分析。
¶ 小脑颗粒细胞培养
颗粒细胞培养物的获取方法如先前报道所述124-126。简而言之,将出生后第5天(P5)的幼鼠在冰上麻醉后处死。每个实验至少使用来自两个不同窝的每种基因型幼鼠各4只。从颅骨中快速取出大脑,小心剥去小脑 表面的脑膜。然后在无菌条件下,在立体显微镜引导下,于汉克平衡盐溶液(HBSS)中解剖小脑皮质。使用木瓜蛋白酶解离系统试剂盒(#LK003150,Worthington Biochemical)按照制造商说明进行组织解离。所得单细胞悬液随后通过70 μm细胞筛过滤,以去除大型非神经细胞,确保获得均一的神经细胞制剂。将小脑 细胞以约600,000个细胞/mL的密度接种在多聚-L-赖氨酸包被(#P2636,Sigma-Aldrich)的盖玻片上,培养基为神经基础培养基(#21103049,Life Technologies),并补充10%胎牛血清(FBS,#1600004,Life Technologies)、0.5%无血清补充剂B-27(#17504001,Thermo Fisher Scientific)和100 I.U./mL青霉素-链霉素(#ECB3001,Euroclone)。培养物在37℃、5% CO₂条件下孵育。24小时后,更换为新鲜的神经基础培养基,该培养基补充了10% FBS、0.5%无血清补充剂B-27、100 I.U./mL青霉素-链霉素、10μM阿糖胞苷(以消除增殖的非神经细胞,如内皮细胞和小胶质细胞)以及25mM氯化钾(通过轻度去极化促进颗粒细胞存活)。
为了可视化自发性GCs活动,将pAAV-hSyn-GCaMP6s-WPRE(1μL/mL,滴度2.2×10¹³ vg/mL)添加到培养基中。pAAV-hSyn-GCaMP6s-WPRE是Douglas Kim和GENIE项目赠送的(#100843,Addgene病毒制剂)。此外,还加入了pAAVhSyn-mCherry(1μL/ml,滴度10¹² vg/mL),以实现稀疏神经元标记,用于形态学分析。pAAV-hSyn-mCherry是Karl Deisseroth赠送的(#114472,Addgene病毒制剂)。
在体外培养第4天(DIV4),将培养基更换为新鲜的Neurobasal培养基,该培养基添加了10%的胎牛血清(FBS)、0.5%的无血清补充剂B-27、100国际单位/毫升的青霉素-链霉素(Pen-Strep)、10μM的阿糖胞苷以及5mM的氯化钾(KCl),以促进功能性突触的形成。在体外培养第7天(DIV7)对神经元进行钙成像和形态学分析。
¶ 颗粒细胞培养钙成像记录与分析
对表达GCaMP6s的第7天体外培养颗粒细胞(DIV7 GCs)进行钙(Ca²⁺)成像,实验在Leica公司的Thunder成像系统上进行,放大倍数为20倍。活细胞成像培养在记录室中进行,记录室维持在37℃、5% CO₂的环境,使用人工脑脊液(aCSF,成分以mM为单位:125氯化钠、5氯化钾、1.2磷酸二氢钾、25羟乙基哌嗪乙磺酸、6葡萄糖、2氯化钙;pH值7.4)。记录时长为5分钟,成像采样率为每帧300毫秒。每张载玻片随机选择3-4个视野进行成像和分析。 使用改编自Sun和Sudhof的MATLAB(MathWorks公司)脚本对延时图像文件进行分析。分析通过自定义函数(GCAMP_multiROI.m)进行,该函数用于从选定的感兴趣区域(ROIs)中提取荧光强度并量化钙活动。为确定感兴趣区域,从最初50帧中的第10至40帧生成中位强度投影以进行数据预览。利用impixel函数,根据荧光强度手动选择感兴趣区域。创建圆形感兴趣区域,并提取所有帧中每个感兴趣区域内的平均强度。然后将原始强度轨迹随时间绘图,以可视化荧光波动。 采用基于阈值的方法检测钙峰,阈值设为背景信号平均值加上1.5倍标准差。spike_detection函数通过检测高于该阈值的局部最大值来识别峰。同步钙峰定义为在特定时间窗口内多个感兴趣区域中出现的峰。在同步活动分析中,同步放电率计算为每分钟同步峰的数量。同步峰的振幅通过计算神经元间的平均ΔF/F₀来确定。基线荧光(F₀)估计为不同时间窗口内三个最低强度值的平均值。每个检测到的峰的相对荧光变化(ΔF/F₀)使用公式(F - F₀)/F₀计算,并确定ΔF/F₀的变异系数(CV)。
为便于可视化,使用稀疏矩阵随时间绘制了同步峰值,清晰呈现了同步活动。分析了各感兴趣区域内尖峰振幅和频率的分布,并叠加了ΔF/F₀轨迹,以比较单个细胞的反应与群体平均值。
¶ 细胞培养物的免疫染色
DIV7 GC用含4%多聚甲醛(PFA)和10%蔗糖的1×磷酸盐缓冲液(PBS)固定。细胞在含10%山羊血清、0.3% Triton X-100的1×PBS中封闭并透化处理,在室温(RT)下孵育1小时。随后,细胞与一抗在4℃下孵育过夜。用1×PBS洗涤后,细胞与二抗(1:750,Molecular Probes Alexa Fluor,Life Technologies)在室温下孵育2小时,再用1×PBS洗涤,用4’,6-二脒基-2-苯基吲哚(DAPI,Sigma-Aldrich,1×PBS中1:5000稀释)复染10分钟,最后用Fluoromount水性封片剂(#F4680,ThermoFisher Scientific)封片。所用的一抗为小鼠抗RFP(1:500,#600-401-379,Rockland)。
¶ 切片的免疫染色
对动物进行经心脏灌注,使用的是含4%多聚甲醛的磷酸盐缓冲液,随后将其断头。大脑用含4%多聚甲醛的1x磷酸盐缓冲液固定,之后在50微米厚的切片(由Leica VT1000S振动切片机切取)或15微米厚的切片(由Histo-Line MC4000冷冻切片机切取)上进行荧光免疫染色。
矢状面小脑切片在含10%山羊血清、0.3% Triton X-100的1x PBS中室温(RT)封闭并透化1小时,随后在4℃下与一抗孵育过夜。用1x PBS洗涤后,切片在室温下与二抗(1:750,Molecular Probes Alexa Fluor,Life Technologies)孵育2小时,洗涤后用4′,6-二脒基-2-苯基吲哚(DAPI,Sigma-Aldrich,1x PBS中1:5000)复染10分钟,并用Fluoromount水性封片剂(#F4680,ThermoFisher Scientific)封片。
使用的一抗包括小鼠抗钙结合蛋白(1:1000,#300,Swant)、兔抗Pax6(1:500,#AB2237,Sigma-Aldrich)、兔抗Iba1(1:2000,#019-19741,Fisher Scientific)、兔抗BLBP(1:200,#ABN14,Merck Millipore)、抗RFP(1:500,#600-401-379,Rockland)。
¶ 新生小鼠小脑的AAV注射
按照既定方案,对新生WHIM小鼠和对照小鼠的小脑进行了AAV注射。138–141对P0幼鼠进行低温麻醉并固定在操作台上。将微量注射器(Hamilton公司,#87930)的针头插入小脑蚓部分子层0.5毫米处,在60秒内注射1微升滴度为10¹²病毒基因组/毫升的AAV-hSyn-mCherry(Addgene公司,#114472)。幼鼠在37℃下复苏后放回母鼠身边。随后,在P21时通过心脏灌流收集注射幼鼠的脑组织。对100微米的小脑切片进行荧光免疫染色。
¶ AMD3100的脑室内注射
AMD3100(目前用于WHIM患者的临床试验:临床试验.gov:NCT02231879;NCT00967785;NCT01058993)或生理盐水被注射到WHIM和对照胚胎(E12.5)或幼鼠(P1)的第四脑室。
具体来说,将1微升AMD3100(1毫克/毫升,Sigma-Aldrich公司,货号239825)与含0.005%固绿的无菌盐溶液混合,并在胚胎发育第12.5天(E12.5)注射到WHIM胚胎和对照胚胎中。
P1幼鼠通过低温麻醉。向WHIM幼鼠和对照幼鼠注射2μL AMD3100(5mg/ml)与0.005%固绿在无菌盐水中的混合液。幼鼠在37℃下复苏后放回窝中。
注射后的胚胎在出生后第7天(P7)进行行为分析,随后在出生后第7天(P7)或第45天(P45)收集样本用于灌注和组织学表征。
¶ 成像
荧光图像是在Axioscan 7切片扫描仪(蔡司)上以10倍和20倍放大倍数获取的,或者在Thunder成像系统(徕卡)上以40倍放大倍数获取的。共聚焦图像是在SP8共聚焦显微镜(徕卡)上以40倍或63倍放大倍数获取的。
放大倍数。明场图像在Axioscan 7切片扫描仪(蔡司)上以20倍放大倍数获取,或在DotSlide显微镜(奥林巴斯)上以20倍放大倍数获取。
¶ 图像分析
¶ PCL长度测量
在P45脑矢状切片上,采用Nissl染色法对包含蚓部和半球的不同耳间水平的矢状小脑切片进行PCL长度评估,使用的是QuPath(0.4.4版本)。在脑沟起始处划定小叶,并用QuPath沿每个小叶的PCL绘制一条线。所有实验均在至少3个生物学重复样本上进行,每个动物考虑至少5个不同耳间水平的切片。
¶ 裂隙长度测量
使用QuPath在包含蚓部和半球的不同耳间水平的P0、P7和P45尼氏染色矢状小脑切片上测量裂隙长度。从切片表面相邻小叶的连接处开始,沿着每个裂隙绘制一条线。所有实验均在至少3个生物学重复上进行,每个动物考虑至少5个不同耳间水平的切片。
¶ 细胞计数
使用QuPath中的阳性细胞检测功能对细胞计数进行半自动处理。简而言之,手动定义感兴趣区域(ROI),并手动调整强度阈值以准确分割每个标记物。仅考虑与DAPI共染色的标记物阳性细胞,以确保其细胞身份。然后将所得计数归一化到ROI面积,以获得细胞密度。所有实验均在至少三个生物学重复样本上进行,每只动物至少考虑6个切片。手动定义感兴趣区域并设置阈值,以区分阳性细胞和阴性细胞。在整个实验分析过程中保持相同的阈值。
¶ 小胶质细胞形态分析
对P21动物小脑蚓部水平的矢状切片进行抗Iba1抗体染色。使用Fiji(v2.14)对小胶质细胞标志物Iba1阳性的单个细胞进行二值化和分割。使用Fiji的Skeletonize插件对所得图像进行骨架化处理,并通过Analyze Skeleton功能进行分析。从结果表格中获取每个细胞的分支数和连接点数。
¶ 伯格曼胶质纤维分析
对P7幼鼠小脑蚓部水平的矢状切面进行抗BLBP抗体染色。使用Fiji软件中的多点工具对分子层100微米长度内的突起数量进行计数。使用Fiji软件中的角度工具计算裂隙线与最近的BLBP+纤维之间的角度。所有实验均至少使用3个生物学重复样本,每只动物至少考虑6个切片。
¶ 肯野细胞形态分析
取P21动物小脑蚓部水平的矢状切片,用抗RFP抗体进行染色,以增强AAV-hSyn-mCherry的信号。选取Calb1和RFP标记均为阳性的单个细胞,使用Fiji软件中的Threshold功能创建掩膜。利用Fiji软件的神经解剖学插件,通过Sholl函数对所得图像进行分析。从结果表格中获取每个细胞的分支数量和树突延伸情况。
¶ 颗粒细胞形态分析
在DIV7,使用Fiji插件NeuronJ(8位图像)选择表达mCherry的单个GC进行分析。对每个选定的神经元进行半自动追踪,以量化神经突形态,包括总神经突长度和每个细胞的神经突数量。
¶ 量化和统计分析
数据收集和数据分析以盲法方式进行。所有使用的统计检验均已标明。整篇手稿中的统计检验均使用Prism 8(GraphPad Prism 10.0.0版本,适用于Windows系统,GraphPad Software公司,美国马萨诸塞州波士顿,www.graphpad.com)和R(4.3.1版本)完成。去除离群值并进行正态性检验(Shapiro–Wilk检验)后,组间差异的分析根据图例说明,采用未配对、双尾Student t检验或Mann–Whitney U检验进行单一比较,或采用单因素或双因素方差分析(ANOVA)结合Bonferroni多重比较检验。统计显著性根据图例说明标注为*p < 0.05,**p < 0.01,无显著性(n.s.)为p > 0.05。除非另有说明,所有数据均以均值±标准差(SD)表示。n的具体数值以及n所代表的含义(如动物数量、细胞数量等)在图例中注明。