¶ 《细胞与分子神经生物学》
¶ 丙泊酚间断暴露诱导人脑类器官神经发育改变
Sudena Wang1·克洛伊·霍尔·王永1,3·莱奥妮·林克1·张艺1·亚历山大·施拉格尔4·科拉·旺德4·克里斯托弗·帕茨克5·马蒂亚斯·克莱因6·托马斯·米特曼²7·迈克尔·K.E.舍费尔1,7,8
1 迈克尔·K.E.·舍费尔 michael.schaefer@unimedizin-mainz.de 德国美因茨约翰内斯·谷登堡大学医学中心麻醉科
2 德国美因茨约翰内斯·古腾堡大学医学中心生理学研究所,美因茨,德国
3 武汉大学人民医院整形外科,中国湖北省武汉市,430060
4 美因茨约翰内斯-古腾堡大学法医学研究所,德国美因茨55131
5 美国印第安纳州圣母市圣母大学生物科学系
6 德国美因茨约翰内斯·谷登堡大学医学中心免疫学研究所,朗根贝克街1号,55131 美因茨
7 德国美因茨市朗根贝克大街1号,美因茨约翰内斯·古腾堡大学7重点项目转化神经科学(FTN),邮编55131
8 约翰内斯·古腾堡大学美因茨免疫治疗研究中心(FZI),德国美因茨市朗根贝克街1号,邮编55131
¶ 摘要
妊娠期麻醉管理可能会对胎儿大脑发育产生影响。本研究使用H1胚胎干细胞衍生的人脑类器官(HBOs)来探究间歇性丙泊酚暴露(IPE)的影响。将HBOs在体外培养47至50天(div)时进行早期IPE处理,或在77至80天时进行晚期IPE处理,使用的丙泊酚浓度为50μM,这一浓度高于临床麻醉浓度。之后在无丙泊酚的条件下额外培养10天,随后在60天或90天时对HBOs进行分析。对HBOs生长情况和乳酸释放量的测定未发现神经毒性证据。多电极阵列记录显示,早期IPE处理后,60天时的神经元活动增强,而晚期IPE处理后90天时未观察到这一效应。RNA测序结果表明,60天时IPE上调了与神经发育和突触功能相关的基因,这些基因与HBOs从60天到90天发育过程中自然上调的基因存在重叠。这些发现表明,早期IPE会加速HBOs的大脑成熟,提示胎儿大脑的正常发育轨迹可能会出现偏差。
¶ 图形摘要
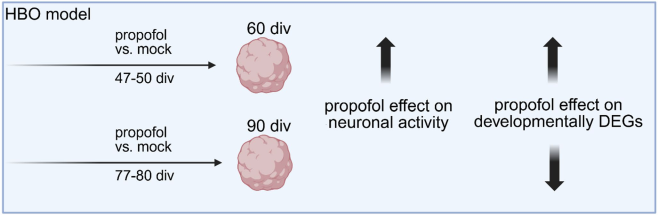
¶ 关键词:
人脑类器官·人类大脑类器官·麻醉剂·丙泊酚·神经发育
¶ 引言
大脑发育是一个多方面的过程,涉及神经发生、神经元迁移与分化、突触形成以及突触可塑性,所有这些对于建立和维持神经网络都至关重要(Budday 等人,2015 年)。发育中的大脑可能会遇到各种环境挑战,包括麻醉剂,这些挑战会影响神经网络并迫使大脑发生适应性变化(Sen,2016 年)。发育中的大脑对麻醉剂的易感性所带来的挑战,在孕期以及早产儿和新生儿中尤为重要(Paulus,2005 年;Ruggiero 等人,2019 年)。全球每年有数百万婴儿和儿童接触麻醉剂,0.75%至 2%的孕妇因非产科手术而接受麻醉(Reitman 和 Flood,2011 年;Zhou 等人,2023 年)。
丙泊酚是一种广泛使用的静脉全身麻醉药,用于诱导和维持麻醉,以及重症监护中的镇静,包括孕妇(Bosnjak等人,2016年;Malhotra等人,2017年;Zhang和Li,2023年)。有报道称,丙泊酚通过胎盘的速度较快,母胎静脉血药浓度比在0.7至0.8之间(Dailland等人,1989年;Sahinovic等人,2018年),这表明它可能对大脑发育产生影响。尽管丙泊酚或其他麻醉剂对人类胎儿的危害尚未得到明确证实,但有证据表明,接触麻醉剂可能会对神经发育和认知结果产生不利影响(Ing和Vutskits,2023年;Reighard等人,2022年),并且在人类以及各种浓度和依赖环境条件下的体内外实验研究中,均发现了神经毒性作用(Bosnjak等人,2016年;Zhang和Li,2023年)。伦理限制使得无法在孕妇患者中进行随机试验,而且没有动物模型能充分复制人类的妊娠过程(Reitman和Flood,2011年)。尽管如此,研究人员已在啮齿类动物模型中研究了产前和新生儿麻醉的病理影响。幼年时接触麻醉剂,尤其是丙泊酚,可能会导致行为改变和认知功能障碍(Aksenov等人,2020年;Chen等人,2016年;Sen和Sen,2016年)。实验研究表明,不同大脑结构中存在神经发生受损、神经元迁移异常以及神经毒性和神经凋亡作用(Gascoigne等人,2021年;Gluncic等人,2019年;Hirotsu等人,2019年;Yan等人,2017年)。此外,在一系列针对出生后第7天大鼠的研究中,对丙泊酚的作用进行了检测,发现了细胞死亡以及细胞死亡相关通路的激活。这一点可以通过钙蛋白酶、半胱天冬酶、FasL的上调,以及抗凋亡蛋白Bcl2的mRNA和蛋白表达的抑制来证明(Milanovic等人,2010年,2016年)。而且,丙泊酚的使用还导致突触蛋白表达减少,以及突触结构和连接性的改变。同时,轴突生长和可塑性标志物GAP-43以及树突微管稳定蛋白MAP-2的上调,表明机体激活了补偿机制以应对丙泊酚诱导的神经毒性(Milanovic等人,2017年)。某些过程似乎局限于特定的脑区,例如额叶皮质的突触发生增加和丘脑的突触消除。这些发现表明,在大脑发育的关键阶段使用丙泊酚会产生即时和持久的影响(Pesic等人,2015年)。在孕期母鼠使用丙泊酚后对其后代进行研究的实验中,也发现了类似的结果,包括海马神经元细胞密度和突触素表达降低(Xiong等人,2014年)。研究还表明,新生猕猴早期使用丙泊酚以及母猴接触丙泊酚会导致其脑部细胞死亡(Creeley等人,2013年),并且与大鼠的长期行为改变相关(Chen等人,2016年;Li等人,2014年;Milanovic等人,2016年,2017年;Pesic等人,2015年;Wan等人,2021年;Xiong等人,2014年;Zhong等人,2016年)。
源自人类胚胎干细胞(hESC)或诱导多能干细胞(iPSC)系的人脑类器官(HBOs)被认为是研究人类胎儿脑发育各方面的合适模型,包括神经网络的成熟(BenitoKwiecinski和Lancaster,2020;Qian等人,2019;Zafeiriou等人,2020)。HBO这一术语是所有三维神经类器官培养物的统称,既包括定向诱导的脑区特异性类器官,也包括自发形成的自组织三维神经类器官培养物,后者常被互换称为大脑类器官(Qian等人,2019)。
尽管麻醉可能会对胎儿的大脑发育产生不利影响,但针对胚胎干细胞(ESC)或诱导多能干细胞(iPSC)衍生的脑类器官(HBOs)中麻醉剂的研究却为数不多。研究结果表明,短期暴露于七氟醚会导致神经元过早分化(Lee等人,2022年;Shang等人,2022年),而长期暴露于氯胺酮(Du等人,2023年)和高剂量丙泊酚(Saglam-Metiner等人,2024年)则会产生神经毒性作用。不过,也有研究显示丙泊酚能在脑类器官中引发功能性电生理反应(Logan等人,2020年)。总体而言,关于麻醉剂对脑类器官影响的相关知识仍较为匮乏。特别是丙泊酚——一种在长期手术中常用的麻醉剂,其在不同发育阶段对模拟胎儿大脑发育的脑类器官模型产生的影响尚未得到研究。该模型或许能为评估孕期长期麻醉可能带来的潜在不良影响风险提供新的见解。为了通过实验解决这一问题,我们研究了在脑类器官发育的两个不同时间点(即培养2个月和3个月的脑类器官,这两个阶段被认为分别模拟了体内胎儿早期至中期的大脑发育阶段)进行长期间歇性丙泊酚暴露(IPE)所产生的影响(Zhao和Haddad,2024年)。通过结合多电极阵列(MEAs)的电生理记录、批量RNA测序、后续差异表达基因(DEGs)及通路的鉴定,以及基因集富集分析(GSEA),我们发现证据表明,长期间歇性丙泊酚暴露会在脑类器官中诱导出具有发育阶段特异性的神经元活动及突触相关基因表达的改变。
¶ 方法
¶ 研究设计
在两个发育阶段(图1),即60天和90天(推测会表现出神经元活性),我们对四个实验组的共68个脑类器官(HBOs)进行了研究(Fair等人,2020;Trujillo等人,2019),其中包括作为对照的模拟处理组和丙泊酚处理组,在丙泊酚处理组中,脑类器官间歇性暴露于50μM的丙泊酚中3天(从47天到50天,或从77天到80天)。选择该浓度是基于临床人脑组织浓度的研究结果(Van Hese等人,2020)以及对人诱导多能干细胞衍生的神经祖细胞(NPCs)的研究,这些研究表明,暴露于50μM丙泊酚6小时后,没有即时或延迟毒性(Long等人,2017)。我们研究了不同发育阶段间歇性丙泊酚暴露(IPE)对脑类器官的影响,测定了脑类器官中的丙泊酚浓度(n=8,来自一个批次的技术重复),并研究了脑类器官的大小和生长情况(n=10,来自两个批次的技术重复)、能量代谢物乳酸的释放(n=8,来自一个批次的技术重复)、通过多电极阵列(MEAs)检测的神经元活性(n=32,来自两个批次的技术重复),以及在批量RNA测序后鉴定差异表达基因(DEGs)及相关通路和基因集富集分析(GSEA)(n=20,来自两个批次的技术重复)。
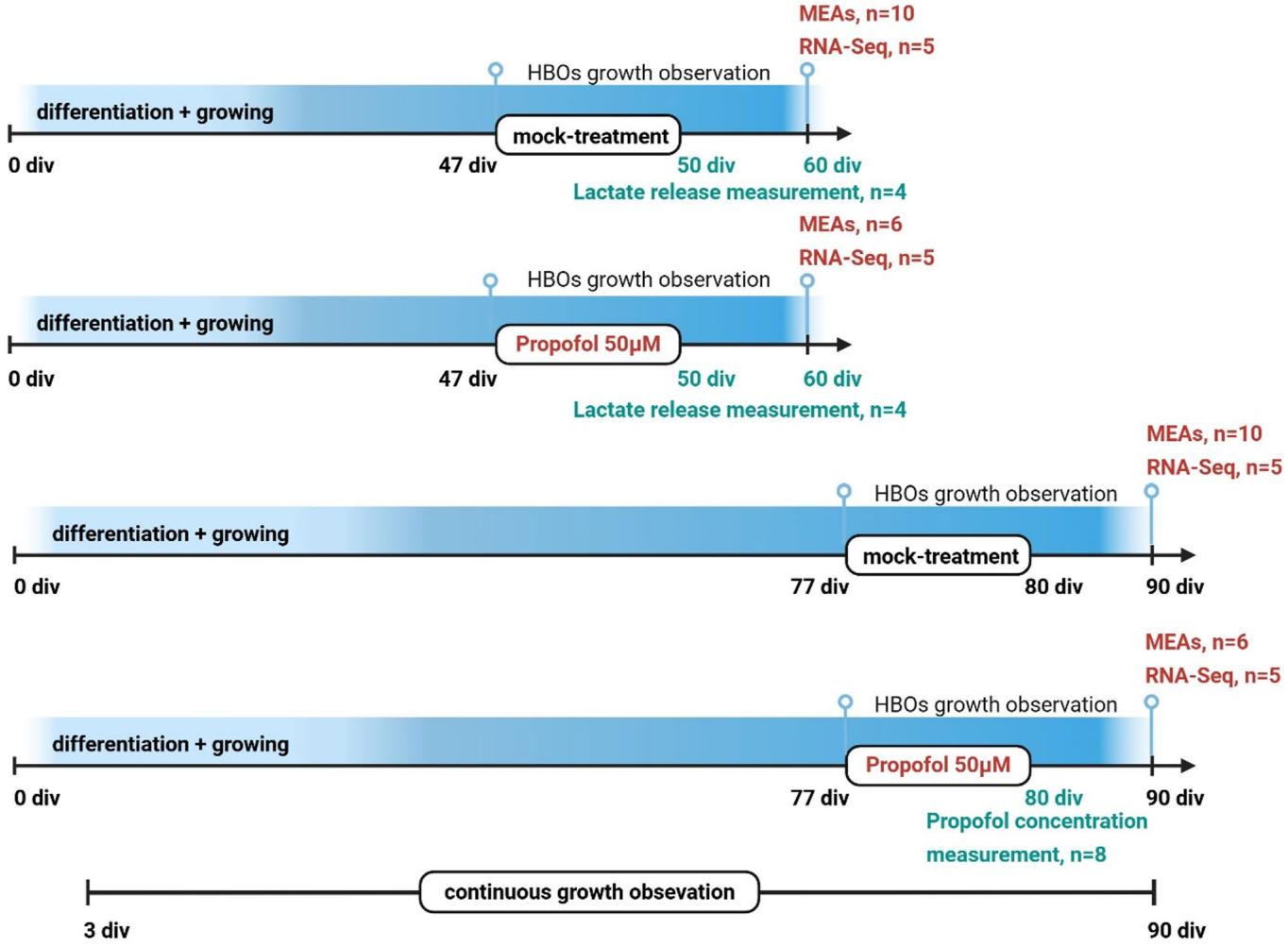
图1 研究设计。在两个发育阶段(60天和90天),对四个实验组共68个HBO进行了研究,包括作为对照的模拟处理组和丙泊酚处理组,其中HBO间歇性暴露于50μM丙泊酚中3天(从47-50天,或从77-80天)。使用微电极阵列(MEAs)对HBO进行分析(n=32,两批),进行RNA测序处理(n=20,两批),测量丙泊酚浓度(n=8,两批),并测定HBO培养基中的乳酸浓度(n=8,一批)。
¶ 人类脑类器官的生成
脑类器官由男性人类胚胎干细胞系H1(H1-hESC,WA01,WiCell研究 institute,NIH注册/批准号:0043/NIHhESC-10-0043)按照先前的方案稍作修改生成(Sutcliffe和Lancaster,2019)。简而言之,将第45代的H1-hESC在由基质胶/ MEM和mTeSR1(StemCell)组成的凝固培养基上培养,直至在6孔板中达到约70-80%的汇合度。第0天,使用Accutase(Sigma-Aldrich)分离细胞,并将其接种到96孔超低吸附板(ULA,Corning)中,每孔9000个细胞,加入150μL mTeSR1,并补充4 ng/ml碱性成纤维细胞生长因子(Peprotech)和1μM噻唑维因(Sigma-Aldrich)。体外培养第3天(3 div),更换75μL培养基为150μL不含碱性成纤维细胞生长因子或噻唑维因的新鲜mTeSR1。第6天(6 div),类胚体已形成,并转移到24孔ULA板中,该板含有500μL神经诱导培养基(补充材料,表1)。根据其形态和大小,在第12天(12 div),将类器官用基质胶(Corning)包被,并在60 mm培养皿(Greiner)中用不含视黄酸的分化培养基(补充材料,表1)在轨道摇床(Edmund Bühler)上进一步培养,直至实验结束(第60天或第90天)。第16天(16 div),轻轻去除基质胶包被,将类器官在含有视黄酸的分化培养基(补充材料,表1)中培养。所有培养阶段均在37°C、5% CO₂的条件下进行。
¶ 人类脑类器官(HBOs)对丙泊酚的间歇性暴露
丙泊酚(LGC,德国威塞尔)被稀释到二甲基亚砜(DMSO)中,得到10 mM的储备液。在47天或77天时,从该储备液中取浓度为50μM的丙泊酚加入培养基中,维持72小时(3天),随后更换为不含丙泊酚的新鲜培养基,持续10天。在对照条件下,加入等量的二甲基亚砜(终浓度:0.5%二甲基亚砜),作为模拟处理(图1)。
¶ 人类脑类器官中丙泊酚浓度分析
制备了丙泊酚储备液(1mg/ml,LGC,德国韦塞尔),其最终浓度为2ng/μl。其他校准品均由该溶液稀释而成。校准包括7个校准品,浓度分别为1、2、3、4、5、10和20ng/mg。每个校准品的制备过程为:将10μl相应的标准溶液转移至10mg脑组织(人脑空白基质)中。随后,加入10μl浓度为5ng/μl的内标(ISTD)丙泊酚-D17(LGC,德国韦塞尔)。
将人类脑类器官(HBOs)在80天龄时用50μM丙泊酚孵育1小时,或从77天龄到80天龄连续孵育3天。总共准备了8个HBOs(4个用丙泊酚处理,4个用模拟处理)用于分析,这些HBOs来自两个独立的培养批次,并在两个独立实验中进行了重复测量。样品制备时,称取2至4毫克的HBOs并进行匀浆处理。随后,像校准品一样加入10μl内标物(ISTD)。校准品和HBOs的提取过程为:加入100μl己烷(VWR,德国达姆施塔特),在搅拌器上剧烈振荡5分钟。然后将校准品和样品在15,000转/分钟的条件下离心10分钟,并将上清液转移至样品瓶中。提取物无需衍生化,可直接用于气相色谱-质谱联用(GC-MS)进一步分析(图S1)。
分析在安捷伦(德国瓦尔德布龙)气相色谱-质谱联用(GC-MS)系统上进行,该系统由8890气相色谱仪(GC)和5977B单四极杆质谱仪(MS)组成。进样口和传输线温度分别为250℃和280℃。进样量为1μl,采用不分流模式。氦气用作载气,隔垫吹扫流量为3ml/min。初始柱温为60℃,保持3分钟,随后以10℃/分钟的速率升温至120℃,接着以30℃/分钟的速率升温至最终温度300℃,并保持8分钟。每个样品的总运行时间为23分钟。采用70eV的电子轰击电离(EI)。离子源和四极杆的温度分别设定为230℃和150℃。为进行定量分析,质谱仪采用选择离子监测(SIM)模式,总驻留时间为120ms。用于丙泊酚和丙泊酚-D17定量分析的目标离子和定性离子的质荷比(m/z)数据分别为163.1、178.1、91.1和177.2、195.2、98.1。定量分析使用MassHunter Quantitative Analysis 12.1版软件进行。所得浓度已根据HBOs的重量进行校正。
¶ 类脑器官的生长和大小测量
在HBO生长和大小测量中,使用Evos显微镜(AMG,赛默飞世尔)从第3天开始至实验结束,捕获单个类器官的明场图像。使用ImageJ软件(RRID:SCR_003070),包括“多边形选择”工具和“测量”插件,对二维横截面积进行分析。
¶ 乳酸浓度的测定
使用L-乳酸检测试剂盒(MAK329,Sigma-Aldrich)按照制造商的说明在HBO培养基中测量乳酸。按照上述方法培养另一批HBO,在47天龄时将单个HBO转移至24孔板,从47天龄到50天龄用丙泊酚或模拟处理(每组n=4),并培养至60天龄。分别在47天龄(作为基线)、50天龄和60天龄时测定培养基中的乳酸含量,将其归一化至HBO重量,并以摩尔/克表示。
¶ 免疫荧光染色
在60小时(div)收集海马脑片(HBOs),用冰冷的磷酸盐缓冲盐水(PBS)洗涤一次,然后在含4%多聚甲醛(PFA)的PBS中固定15分钟,接着用PBS洗涤三次,并转移至4°C的30%蔗糖溶液中。次日,将标本用Epredia Neg-50 Blue(赛默飞世尔科技)包埋,使用冷冻切片机(HM 560 Cryo-Star,赛默飞世尔科技)切成12μm的冷冻切片。切片收集在Superfrost Plus黏附载玻片(New Erie Scientific LLC)上,于-20°C保存。 对于双重免疫荧光染色,切片在室温(RT)下风干30分钟,再用4%多聚甲醛固定10分钟。用PBS洗涤后,将切片在封闭液(含5%山羊血清、0.5%牛血清白蛋白、0.1% Triton X-100的PBS)中于室温孵育1小时。随后,将切片在含NeuN特异性一抗(稀释比例1:500,RRID:AB_2924930)或GFAP特异性一抗(稀释比例1:500,RRID:AB_10641162)的封闭液中于4°C孵育过夜。 次日,用PBS洗涤切片,然后在含二抗(山羊抗兔Alexa 568,RRID:AB_2534121;山羊抗豚鼠Alexa 488,AB_2534117,各稀释1:1000)的封闭液中于室温孵育1.5小时,再用PBS洗涤,并用4’,6-二脒基-2-苯基吲哚二盐酸盐(DAPI,1:10000;Sigma-Aldrich)复染5分钟,最后用PBS洗涤,使用荧光显微镜(BZ-X800,基恩士)在20倍物镜和适当的滤光片设置下进行成像。
¶ 高密度微电极阵列记录
在60天或90天的类器官被放置在Accura HDMEA芯片(3Brain公司,瑞士)上,并使用附带网格的铂锚固定到位。在37°C的DMEM环境中记录其活动。在多个通道中观察到自发活动,而在特定电压门控钠通道阻滞剂河豚毒素(TTX,2μM,Biozol公司)存在的情况下,这种自发活动消失,这证实了人类脑类器官(HBOs)会产生动作电位。使用Brainwave 5软件(3Brain公司,瑞士)在每种条件下记录活动5分钟,采用100Hz的高通滤波器,在黑暗环境中进行,采样频率为19754Hz。数据文件被导出、分段,并通过Julia/Jupyter笔记本中的代码将模拟电压转换为数字电压。
已确定Accura HD-MEA芯片重新校准的时间戳,这些时间戳在我们的记录中产生了人工尖峰,并且时间戳两侧各100个数据点被剔除,相当于每400毫秒剔除约10毫秒。该程序可防止这些重新校准伪影被纳入神经元信号分析中。我们还观察到“活动闪现”的情况,即大多数通道都处于饱和状态。这些也从分析中移除了。对数据应用了150-3000赫兹的带通雷米兹滤波器。在5毫秒的移动窗口内计算事件阈值,当尖峰与平均值的偏差达到5倍标准差时,即被检测到。我们从记录中选择了30个最活跃的通道,比较了这些通道在不同实验条件下的活动,并确保这些通道的平均频率高于0.5赫兹的最低活动水平(两个90天龄的模拟类器官因平均频率<0.4赫兹而被排除)。
¶ bulk RNA测序
使用RNAeasy试剂盒(Qiagen)纯化总RNA,通过Qubit 2.0评估其数量,并使用安捷伦生物分析仪上的RNA 6000 Nano芯片检查质量。使用NEBNext® Poly(A) mRNA磁分离模块和NEBNext® Ultra™ II RNA文库制备试剂盒(适用于Illumina®),从400 ng总RNA中制备带条形码的mRNA测序文库,最终进行12个循环的扩增。使用Invitrogen的Qubit HS DNA检测定量文库浓度,并使用安捷伦2100生物分析仪上的HS DNA芯片分析平均文库大小。测序在诺禾致源(英国剑桥)进行,使用Illumina NovaSeq 6000测序系统,每个样本的测序深度为3000万对末端(150个循环)读数(150个循环)。通过解复用的fastq.gz文件评估样本质量。对测序读数进行适配器序列修剪,并使用Qiagen的CLC Genomics workbench软件(v21.0.5)按照CLC的RNA测序分析默认设置进行处理。读数与GRCm38基因组(Waterston等人,2002年)比对,最小读数长度为50 bp。表达值单位为TPM。结果通过ArrayStar 17(Lasergene)展示,包括映射读数数量、目标长度、来源长度和位置、链、基因和基因ID,并根据mm10组装进行注释。对基因进行过滤,仅保留20个样本中至少有7个有效值且标准化读数>0.1的基因,以排除低表达基因。
数据的分析基本如前所述(Wang等人,2022)。简要来说,使用对数转换数据识别差异表达基因(DEGs),并使用GraphPad Prism生成火山图以可视化DEGs,标准如下:绝对差值>4、折叠变化(FC)>2且p<0.05。使用STRING数据库(https://string-db.org/)对选定的DEGs进行基因本体论(GO)富集分析。为了基于所有注释转录本评估功能意义,使用GSEA软件(http://www.gsea-msigdb.org)进行基因集富集分析(GSEA)(Subramanian等人,2005),并展示基因本体论生物学过程(GOBP)的富集图。基于与单个GO术语相关的基因,使用GraphPad Prism生成热图。此外,为了研究两组比较(60天龄HBOs±丙泊酚,以及90天龄HBOs±丙泊酚)之间共有的GO术语,使用在线工具(https://bioinformatics.psb.ugent.be/webtools/Venn/)生成维恩图,并对所有GOBP、GOCC、GOMF和标志基因集进行分析。GSEA排名基因列表基于折叠差异和P值。RNA-seq数据已作为GEO数据集存入,临时登录号为GSE294524:https://www.ncbi.nlm.nih.gov/geo/query/acc.cgi?acc=GSE294524。
¶ 统计方法
使用GraphPad Prism(10版)进行统计计算。数据以箱线图(中位数、第25至第75百分位数)呈现,包含单个数据点,须线延伸至最小值和最大值。为检验HBO生长和乳酸释放的差异(图2),采用Student非配对双尾t检验对呈参数分布的值进行两两比较。为检验HBOs的尖峰频率差异(图3),使用单因素方差分析(One-Way-ANOVA),随后采用Sidak多重比较法对四个实验组(60天HBO±丙泊酚、90天HBO±丙泊酚)中频率最高的前30个通道记录进行比较。排除无活动的HBOs(活动通道的平均活动<0.5Hz,n=2,90天对照组)或在不同HBOs中表现出异常高活动的单个记录通道(>5Hz,每个HBO有0-3个通道)。使用ROUT离群值检验对数据进行统计学显著离群值检验,并使用Shapiro-Wilk检验进行参数分布检验。p<0.05被认为具有统计学显著性。
¶ 结果
¶ 丙泊酚在人类脑组织类器官(HBOs)中迅速积累至超临床浓度,随后下降至临床相关水平
据报道,在接受癫痫病灶切除术的患者中,人脑组织中丙泊酚的浓度可达7.68纳克/毫克(假设密度与水相近,相当于43微摩尔)(Van Hese等人,2020年)。我们通过气相色谱-质谱联用技术(GC-MS)测定了在培养基中加入50微摩尔丙泊酚(相当于8.9微克/毫升)后,人脑类器官(HBOs)中丙泊酚的浓度。分析显示,1小时后,人脑类器官中丙泊酚的初始浓度为172.9±43纳克/毫克(平均值±标准差);暴露于丙泊酚72小时后,人脑类器官中丙泊酚的浓度为6.1±1.2纳克/毫克(平均值±标准差)。因此,丙泊酚暴露会使人脑类器官中丙泊酚迅速积累,达到超临床水平,而长期暴露则会使其浓度降至临床相关水平。
¶ IPE不影响HBO的生长速率或乳酸代谢
通过显微镜图像分析评估,在模拟条件下,人类脑类器官(HBOs)在90天体外培养(div)的最终观察时间点前均呈现持续生长(图2A、B)。接下来,研究人员检查了异丙酚(IPE)可能造成的生长干扰(图2C)。测定了从47至50天体外培养期间暴露于丙泊酚(50μM)或模拟处理的人类脑类器官在47至60天体外培养期间的大小,以及从77至80天体外培养期间接受处理的人类脑类器官在77至90天体外培养期间的大小。这使我们能够计算人类脑类器官随时间的生长倍数变化,但丙泊酚处理组与模拟处理组之间未发现差异(图2C及47-60天体外培养:模拟处理组1.19±0.16,丙泊酚处理组1.27±0.17,p=0.738;77-90天体外培养:模拟处理组1.09±0.05,丙泊酚处理组1.01±0.09,p=0.492,非配对t检验)。
HBOs表现出高糖酵解活性和乳酸释放(Castilla Bolanos等人,2024年),且有报道称丙泊酚可抑制急性大鼠脑切片中的糖酵解和乳酸释放(Hadjihambi等人,2020年)。因此,我们比较了在47至50天体外培养(div)期间,经IPE处理或模拟处理的HBOs的乳酸释放情况(图2D)。然而,在50天体外培养或60天体外培养时,细胞培养基中测定的乳酸浓度在各实验组之间无显著差异(图2D和50天体外培养:丙泊酚组0.41±0.09 SEM,模拟处理组0.29±0.03 SEM,p=0.274;60天体外培养:丙泊酚组0.44±0.1 SEM,模拟处理组0.4±0.04 SEM,p=0.769;非配对t检验)。这些结果表明,经IPE处理后的HBOs生长和代谢正常,且没有明显的神经毒性(即不可逆的灾难性代谢衰竭)。
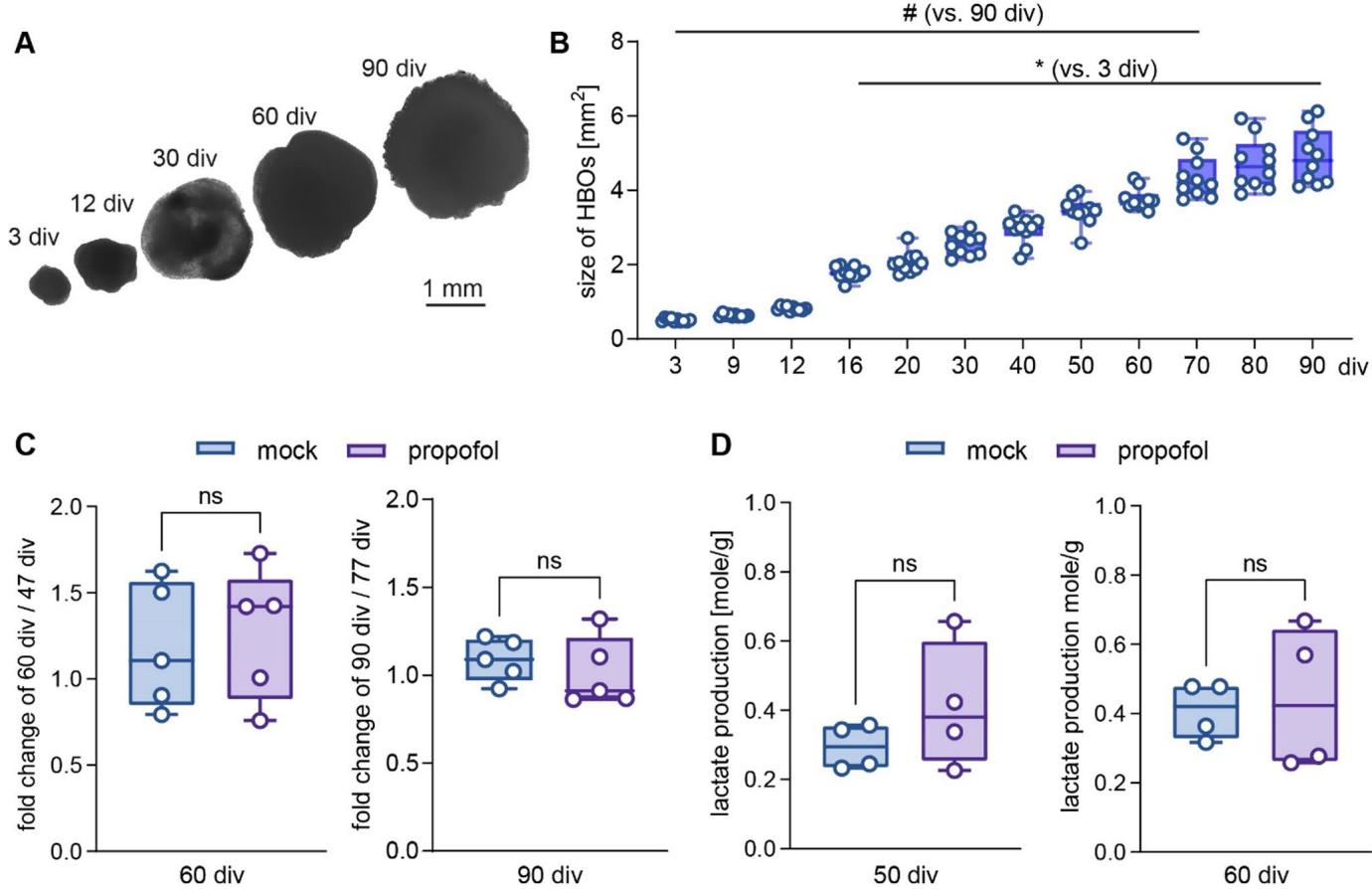
图2 HBO的生长速率和代谢不受丙泊酚间歇暴露的影响。A 明场显微镜图像显示了不同培养时间点的单个HBO(比例尺:1毫米)。B 从3天到90天的HBO大小评估显示其持续生长(n=10),与3天时相比,16-90天时的大小显著增加(*p<0.05),与90天时相比,3-70天时的大小有所减小(#p<0.05)。数据采用单因素方差分析(One-Way-ANOVA),随后进行Sidak多重比较分析。C 经模拟处理或50μM丙泊酚单次处理后,HBO在60天时相对于47天、80天时相对于77天的生长倍数变化(每组n=5)。D 从47天到50天经模拟处理或丙泊酚处理后,在50天和60天时测定的乳酸生成量(以HBO重量标准化,每组n=4)。数据采用Student非配对双尾t检验分析。数据以箱线图表示(中位数、第25至第75百分位数),须线范围为最小值到最大值。
¶ IPE对人类脑类器官(HBOs)的作用诱导对神经元活动的发育阶段特异性影响
在60天的分化阶段,双免疫荧光染色识别出表达星形胶质细胞标志物GFAP和成熟神经元标志物NeuN的细胞(图3A),这表明HBOs处于具有神经元活性的成熟阶段(Fair等人,2020年;Trujillo等人,2019年)。通过MEA记录来确认HBOs的电生理活性。实际上,HBOs在MEA记录中表现出多单位活动,表明存在尖峰活动,即动作电位的自发发放。在存在TTX(一种电压依赖性钠通道的选择性阻滞剂)的情况下,这种活动消失(图3B),从而证实了HBOs中神经元动作电位的发放。
为了研究丙泊酚对神经元活动的发育成熟影响及可能的阶段特异性作用,共记录了32个HBO(图1,60天龄时n=16,90天龄时n=16,丙泊酚处理组和模拟处理组的样本量相同)。实验组中绝大多数HBO表现出尖峰活动(成功率为93.75%,90天龄模拟处理组中有2个HBO无活动)(图2C、D)。对四个实验组的尖峰频率进行分析和多重比较后发现,在未进行丙泊酚处理的情况下,从60天龄到90天龄尖峰频率有所增加,这与HBO的发育成熟相符(图3E)。在60天龄时,与模拟处理相比,47至50天龄时进行IPE处理导致HBO的尖峰频率显著增加。在90天龄时,77至80天龄时进行IPE处理的HBO,其尖峰频率与模拟处理组相比无差异(图3E)。这些发现表明,IPE可使60天龄HBO的神经元活动持续增加,但对90天龄HBO无此作用,这提示其作用方式具有发育阶段特异性。
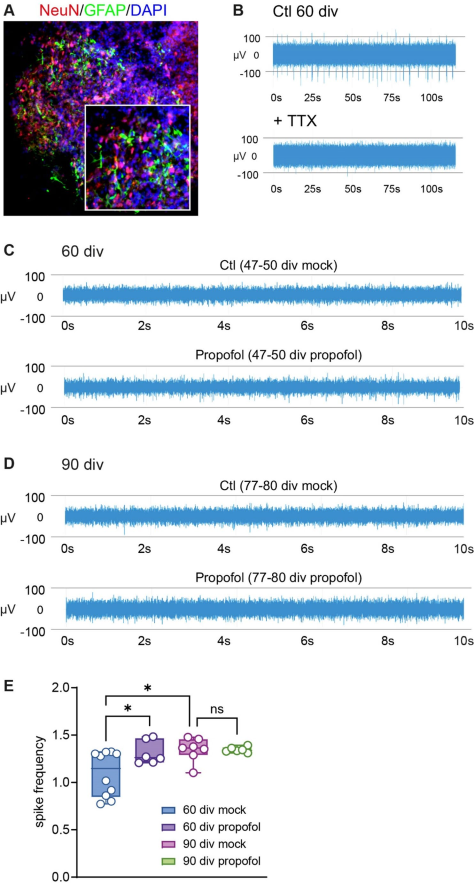
图3 间歇性丙泊酚暴露于HBOs对神经元活动产生发育阶段特异性影响。A 利用抗NeuN、抗GFAP进行免疫荧光染色,并对60天龄HBOs进行核染色(DAPI),显示存在有丝分裂后神经元和星形胶质细胞。B 在对照条件下和存在TTX的情况下,对60天龄HBOs进行高密度微电极阵列(HD-MEA)记录,表明HBOs中 spikes活动的神经元来源。注意在TTX处理条件下,多单位活动(spikes)消失。C、D 微电极阵列(MEA)记录显示,与模拟处理相比,间歇性丙泊酚暴露(IPE)后,60天龄HBOs的spikes频率增加(C),而90天龄HBOs则未出现这种情况(D)。E 间歇性丙泊酚暴露(IPE)或模拟处理后,60天龄和90天龄HBOs中spikes频率的汇总图(每组n=6-10),结果显示丙泊酚在60天龄时诱导spikes频率增加,而在90天龄时未观察到这种效应。*p<0.05,单因素方差分析(OneWay-ANOVA)后进行Sidak多重比较。
¶ IPE选择性地增加了HBOs中发育调控基因的表达
MEA记录的结果表明,IPE会改变HBOs的神经发育成熟过程。因此,我们进行了 bulk RNA测序及后续数据分析,以比较在IPE或模拟处理后,60天和90天时HBOs的转录组谱(图1)。
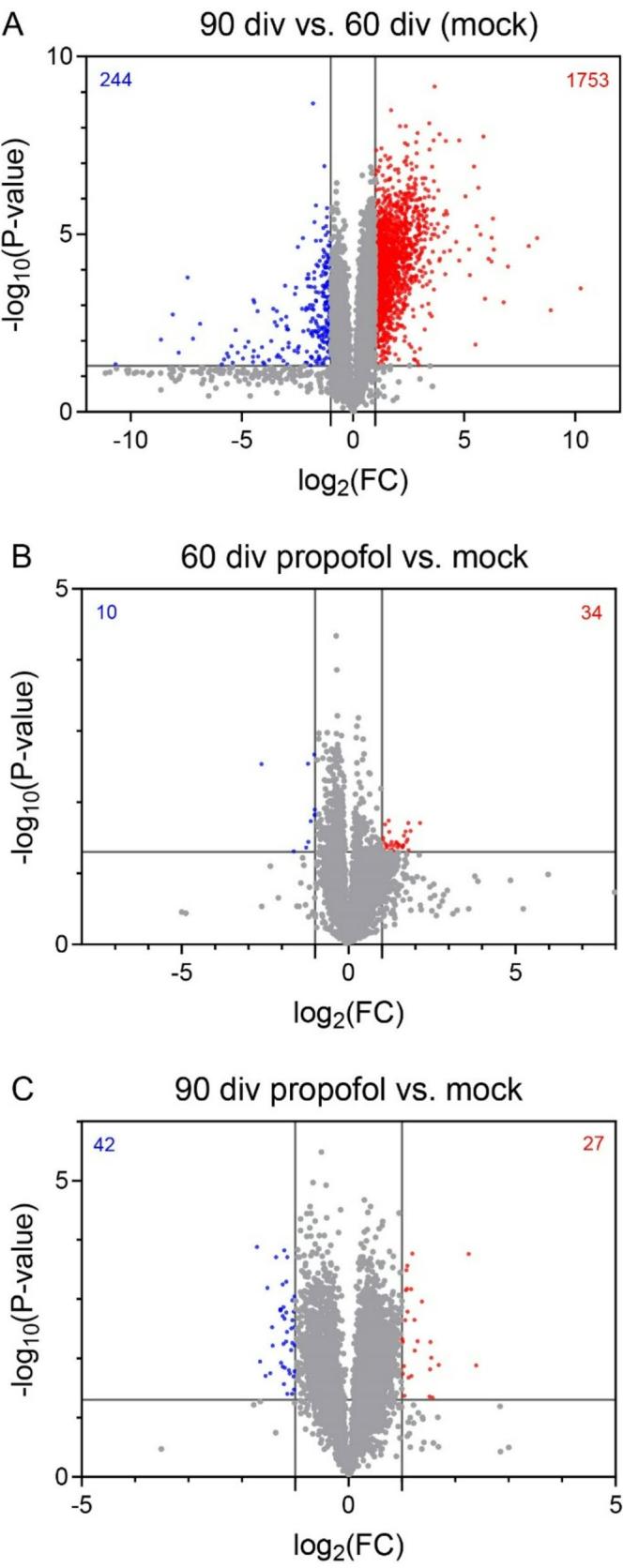
首先,我们在60天和90天的HBOs之间,通过严格的数据筛选(绝对差值>4,倍数变化>2,p<0.05)揭示了差异表达基因(DEGs),预期会有大量在发育过程中上调的基因。正如预期的那样,该分析显示,与60天时相比,90天时的HBOs中有1997个差异表达基因,其中1753个基因上调,244个基因下调(图4A)。
接下来,我们使用相同的数据排序标准,比较了60天龄的人类脑类器官(HBOs)在47至50天龄期间接受或未接受异丙酚暴露(IPE)的情况。结果显示,经异丙酚处理的HBOs中有44个差异表达基因(DEGs),其中34个基因上调,10个基因下调(图4B)。值得注意的是,在60天龄HBOs中,所有因异丙酚暴露而上调的基因,在90天龄与60天龄的模拟处理(mock)HBOs对比中也均上调。相反,在异丙酚暴露后HBOs中下调的10个差异表达基因中,有2个在90天龄与60天龄的模拟处理HBOs对比中也出现下调(图4C)。
为了评估各组间重叠差异表达基因(DEGs)的显著性,计算了一个表征因子(RF,http://nemates.org/MA/progs/overlap_stats.html)(Cho等人,2021)(图4D)。该计算显示,在60天与90天对比组中上调的差异表达基因,与丙泊酚处理60天与对照组60天对比组中上调的差异表达基因之间,存在特别显著的重叠(RF=15.0,p<7.17e41)。对90天时的人类脑类器官(HBOs)进行比较,无论是否在77至80天时进行丙泊酚暴露(IPE),结果显示丙泊酚处理的人类脑类器官中有69个差异表达基因,其中27个基因上调,42个基因下调。同样,在77至80天经丙泊酚处理后上调的27个基因中,有19个在90天对照组人类脑类器官与60天对照组人类脑类器官的对比中也出现上调(RF=10.6,p<5.27e-17)。相比之下,在77至80天经丙泊酚处理的90天人类脑类器官与未处理的90天人类脑类器官对比中下调的42个基因,以及在未暴露于丙泊酚的情况下90天与60天人类脑类器官对比中下调的基因,两者仅1个基因重叠(RF=2.4,p<0.341)。这些结果表明,丙泊酚暴露(IPE)选择性地增加了人类脑类器官中从60天到90天受发育调控的基因的表达。
¶ IPE对HBOs的作用导致差异表达基因在特定阶段的GO富集
如前所述,对间歇性暴露于丙泊酚或模拟处理的HBOs进行比较后发现,在60天龄时差异表达基因(DEGs)数量相对较少(44个),在90天龄时为69个。因此,在所有类别中均未发现差异表达基因的基因本体(GO)富集。然而,在60天龄时,IPE处理与模拟处理的比较显示,差异表达基因与GO细胞组分(GO_CC)术语“突触”和“轴突”相关(图5D)。与60天龄相比,在90天龄时,差异表达基因与GO分子功能(GO_MF)术语相关,如“跨膜转运蛋白活性”和“离子通道活性”(图5E)。
¶ GSEA揭示IPE的相反发育阶段特异性效应
与模拟处理组相比,丙泊酚间歇处理的HBOs中差异表达基因(DEGs)数量较少,使用STRING-DB未发现生物过程(GOBP)、分子功能(GOMF)和/或细胞组分(GOCC)的富集。因此,我们采用了基因集富集分析(GSEA),该方法基于所有注释的转录本计算富集情况,从而提供生物过程(BP)、分子功能(MF)和细胞组分(CC)的基因本体(GO)关联以及标记基因的扩展概述(Subramanian等人,2005年)。
基因集富集分析(GSEA)显示,从第47天到第50天进行异丙酚处理(IPE)后,在第60天时,与多种神经发育和突触相关的基因本体论生物学过程(GOBP)术语的关联增强,例如突触小泡胞吐(图6A-C)、轴突发生调控、树突发育和突触组装(图S2);而在第77天到第80天进行异丙酚处理后,第90天时观察到了相反的效果(图6A-C、图S2)。相反,GSEA未显示“Hallmark_凋亡”基因集中存在显著差异,这支持了异丙酚没有明显神经毒性作用的结论(图S2)。
根据GSEA富集图(图6A-C)(依据FDR和p值),实验组间各项比较(60天 vs. 90天(对照组)、60天丙泊酚 vs. 对照组、90天丙泊酚 vs. 对照组)的前3个GOBP术语均与突触功能相关。从60天到90天上调基因的富集分数略高,但与60天丙泊酚组和对照组之间计算出的富集分数相近(图6A、B)。然而,在90天丙泊酚组与对照组的比较中观察到了相反的效应(图6C)。值得注意的是,GOBP_突触小泡胞吐(GO:0016079)在所有实验组间比较的前3个GOBP中均有出现(图6A)。与丙泊酚对神经元活动和差异表达基因的发育阶段特异性效应一致,属于GOBP_突触小泡胞吐的人脑类器官中各个基因的表达热图(图6B)显示,与对照组处理相比,丙泊酚在60天和90天的发育阶段对这些基因的调控整体上呈相反趋势(以Z分数和log2倍变化表示,图S3)。
D
| 重叠差异表达基因(DEGs)分组 | 表征因子(RF) | p值 | |
|---|---|---|---|
| 上调DEGs | 60 div vs. 90 div (mock) <> 60 div 丙泊酚组 vs. mock | 15.0 | p<7.17e-41 |
| 60 div vs. 90 div (mock) <> 90 div 丙泊酚组 vs. mock | 10.6 | p<5.27e-17 | |
| 下调DEGs | 90 div vs. 60 div (mock) <> 90 div 丙泊酚组 vs. mock | 2.4 | p<0.341 |
图4 丙泊酚间歇性暴露选择性增强人脑类器官(HBOs)中发育调控基因的表达。A-C 火山图分别显示了模拟处理90天 vs 模拟处理60天、模拟处理60天 vs 丙泊酚处理60天、模拟处理90天 vs 丙泊酚处理90天的差异表达基因(DEGs)(标准:绝对差值>4,折叠变化>2,p<0.05)(n=5)。X轴代表经log2转换的折叠变化(log2 FC),Y轴代表经负log10转换的p值。图中显示了显著上调(红点)或下调(蓝点)的差异表达基因以及非显著调控基因(灰点)。D 计算不同实验组和发育阶段间上调及下调差异表达基因重叠的表征因子和p值(http://nemates.org/MA/progs/overlap_stats.html)(Cho等人,2021年)
接下来,我们测试了丙泊酚相反的发育阶段特异性效应是否在不同类别的基因本体(GO)术语中的各种基因集里可见(图7)。我们生成了显著调控的GO术语(生物过程GO术语、细胞组分GO术语、分子功能GO术语,错误发现率<0.05,p值<0.05)的维恩图,这些术语在60天龄人类脑类器官+丙泊酚组中上调,在90天龄人类脑类器官+丙泊酚组中下调。该分析显示了在每个发育阶段与丙泊酚处理相关的独特或共有的GO术语。特别是,发现135个生物过程GO术语、51个细胞组分GO术语、1个分子功能GO术语和4个标志GO术语会根据发育阶段受到丙泊酚的相反调控(图7)。因此,丙泊酚在不同类别的GO术语中的各种基因集里诱导了发育阶段特异性改变。
¶ 讨论
神经元活动是神经元结构发育、神经元分化和突触连接的关键决定因素。例如,在大脑发育的关键阶段,神经元活动的短暂改变会影响网络连接,并导致与神经精神疾病相关的认知症状(Bitzenhofer等人,2021年;Kirischuk等人,2017年;Marin,2016年)。因此,怀孕期间麻醉对神经元活动的抑制可能会影响胎儿大脑的神经元分化和突触连接(Rizzi等人,2008年)。
多项研究表明,人类脑类器官(HBOs)适用于模拟健康和疾病状态下的胎儿人脑发育(Bai,2024;Coronel等人,2026;Logan等人,2020;Sidhaye和Knoblich,2021)。在本研究中,从第47到50天(div)对人类脑类器官进行异丙酚暴露(IPE),导致其在第60天时神经元活性增强,而从第77到80天暴露后,在第90天时未观察到这种效应。RNA测序(RNA-seq)已识别出具有差异表达基因(DEGs)的发育阶段特异性转录组谱,这些基因反映了从第60到90天的神经元分化和突触形成。值得注意的是,在异丙酚暴露后的第60天,观察到与突触功能相关的同一组差异表达基因,这表明成熟过程加速。相比之下,在第90天时,异丙酚暴露后与突触功能相关的差异表达基因被下调,这表明异丙酚在人类脑类器官成熟过程中具有阶段特异性效应。多电极阵列(MEA)记录显示,经异丙酚处理的人类脑类器官在第60天时神经元活性增强,这与同期突触相关基因表达增加一致,但在第90天时未观察到这种功能相关性。未来的研究需要进一步开展工作,包括对神经元成熟和亚群标志物以及突触前和突触后蛋白的免疫荧光分析。本研究的一个局限性是,基因表达的变化未在蛋白质水平上得到验证。
我们选择在细胞培养基中单次施用50μM丙泊酚的间歇性治疗方案,依据是临床人体脑组织中的丙泊酚浓度可达43μM(Van Hese等人,2020年),且诱导多能干细胞衍生的神经祖细胞在50μM丙泊酚中暴露6小时后未出现毒性作用(Long等人,2017年)。施用后1小时,我们观察到浓度超过临床水平,这可能是由于丙泊酚具有高脂溶性,而在施用72小时后,其浓度降至临床相关水平。然而,需要注意的是,正如之前在大鼠脑片培养中所证实的(Gredell等人,2004年),丙泊酚的亲脂性导致其平衡速率较慢,这可能会产生浓度梯度。因此,位于脑类器官表面附近的神经元可能比位于较深处的神经元暴露于更高的浓度中。但本研究并未探究我们的脑类器官模型中此类浓度梯度的形成,以及它们对不同培养时长的脑类器官的神经元活动和转录组可能产生的影响。
给药后1小时至72小时丙泊酚浓度的下降表明,人脑类器官(HBOs)中存在降解丙泊酚的代谢途径。细胞色素P450(CYP)和尿苷二磷酸葡萄糖醛酸转移酶(UGT)的人类基因变异与不良临床结局相关,如丙泊酚相关输注综合征(Budic等人,2022年;Dinis-Oliveira,2018年)。在编码CYP的57个基因中,有12个CYP家族成员的表达水平被认为具有相关性(绝对表达值>3)。在90天龄时,16个CYP基因的绝对表达值>3。相比之下,在编码UGT的22个基因中,只有UGT8在60天龄和90天龄的人脑类器官中以相关水平表达。基于这些表达数据,似乎涉及CYP的代谢途径可能导致了丙泊酚水平的下降。
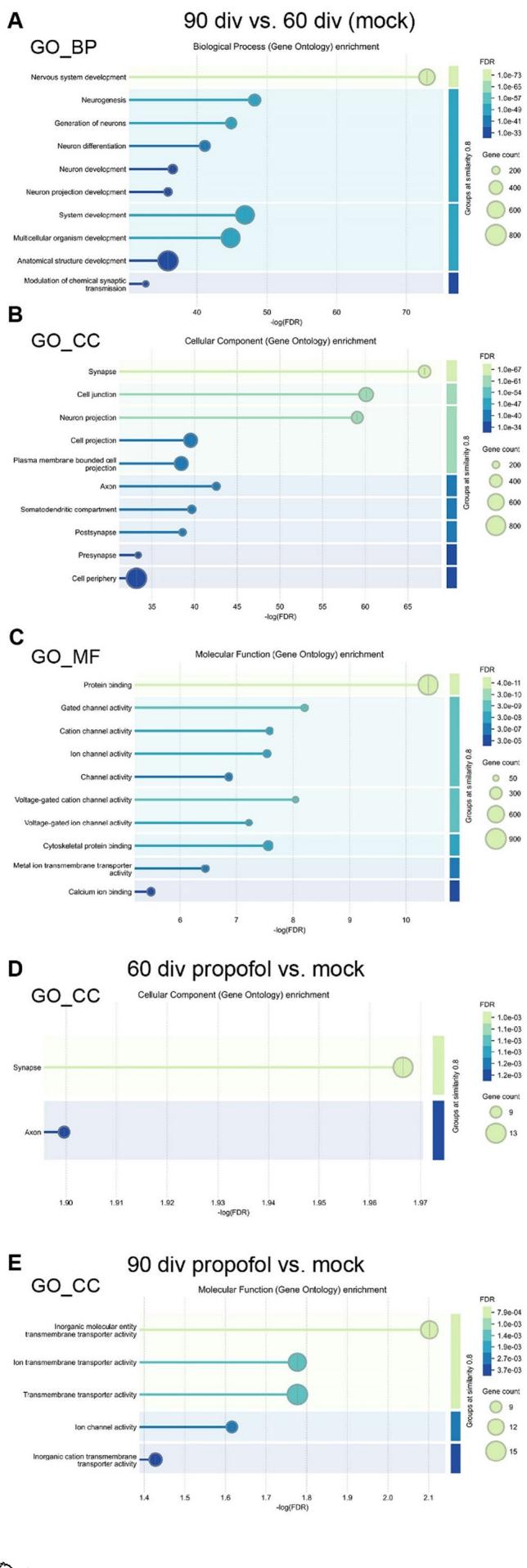
图5 丙泊酚诱导的差异表达基因在神经发育和突触相关的基因本体论术语中富集。A-E 使用STRING-DB进行基因本体论富集分析,揭示显著富集的基因本体论术语。X轴表示富集的负对数10转换统计显著性,即-log10(错误发现率),数值越大表明显著性越强。每个圆圈代表一个基因本体论术语,圆圈大小与该术语相关的基因数量成正比,颜色表示错误发现率,如右侧图例所示。分组的强度阈值设为0.8。
由于丙泊酚具有高脂质溶解度,人们假设血浆和脑组织之间会快速达到平衡(Sahinovic等人,2018年),且母胎静脉血药浓度比在0.7至0.8之间(Dailland等人,1989年;Sahinovic等人,2018年)。据我们所知,关于母亲长期使用镇静剂量期间胎儿脑中丙泊酚浓度的数据尚未有报道,目前尚不清楚本研究中人类脑细胞类器官(HBOs)中的丙泊酚浓度与临床环境中的浓度在多大程度上具有可比性。为回答这一问题,有必要通过使用大范围的丙泊酚浓度、改变治疗持续时间以及治疗后的观察时间点,并结合胎儿脑组织中临床浓度的数据,开展更多关于剂量-反应关系的研究。
尽管如此,人类脑类器官(HBOs)中初始较高的丙泊酚浓度可能引发了神经毒性效应。事实上,在新生大鼠中已观察到丙泊酚的短暂神经毒性效应,其证据包括活化的半胱天冬酶-3水平短暂升高、神经营养因子和突触蛋白的下调(Chen等人,2016年;Karen等人,2013年;Milanovic等人,2010年;Pesic等人,2015年),以及区域特异性的突触形成或消除(Karen等人,2013年;Milanovic等人,2010年;Pesic等人,2015年)。同时,已观察到针对丙泊酚诱导的神经毒性的补偿机制被激活(即GAP-43和MAP2的上调)(Milanovic等人,2017年)。这些研究结果共同表明,丙泊酚可诱导活动依赖过程、突触功能和可塑性发生即时变化。因此,人类脑类器官在60天龄时神经元活动增强,可能是由于异丙酚暴露(IPE)初始的短暂神经毒性效应,随后是与可塑性相关的过程所致。
为了全面了解IPE期间及之后的过程,有必要在47至50天和77至80天的丙泊酚治疗期间,以及直至60天和90天终点的后续治疗后间隔时间点,评估细胞凋亡、氧化应激和线粒体功能障碍的特定标志物(即裂解的半胱天冬酶3、活性氧和线粒体膜电位),以及神经元的成熟和可塑性。
先前的研究使用原代神经元培养物或人类诱导多能干细胞衍生的神经前体细胞,结果显示,分别给予10至100μM或20至300μM浓度的丙泊酚后,会产生神经毒性作用或线粒体功能损伤(Berndt等人,2018年;Long等人,2017年)。最近,研究发现用20μM丙泊酚处理人类胎儿前额叶皮层培养物6小时,会导致多种细胞类型(包括兴奋性和抑制性神经元、星形胶质细胞、少突胶质细胞祖细胞和小胶质细胞)的单细胞转录组谱发生瞬时变化。然而,这些变化并未改变单细胞轨迹,且去除丙泊酚后,这些影响得以逆转(Chang等人,2023年)。丙泊酚处理是否会产生更持久的影响仍未可知。我们基于延长处理时间的研究结果确实表明,这种持久影响可能会发生。在脑类器官中,35.6 ng/ml(200μM)的培养基浓度会导致细胞死亡,这通过TUNEL染色得到证实(Saglam-Metiner等人,2024年)。然而,通过评估人类脑类器官(HBO)的大小、生长速率以及代谢标志物乳酸的释放,我们并未观察到丙泊酚明显的神经毒性作用。鉴于乳酸释放可作为人类脑类器官中线粒体功能的指标(Cho等人,2021年),这些结果进一步表明,丙泊酚不会导致能量代谢的持续抑制。
此外,针对基因本体论(GO)术语“神经元凋亡过程调控”(GO:0043523)的RNA测序数据分析,并未显示出广泛神经元凋亡的典型特征(补充材料)。然而,在60天(326个基因中有18个)和90天(326个基因中有102个)时,观察到IPE组与对照组之间该GO术语对应的差异表达基因(DEGs),这表明存在阶段依赖性的适应性应激反应。
尽管如此,除了已提及的对神经元标志物进行免疫荧光分析的要求外,我们研究的一个局限性是缺乏对活化的半胱天冬酶-3、活性氧以及线粒体膜电位标志物的检测,而这些标志物此前已被证实与丙泊酚的神经毒性作用相关(Liang等人,2022年;Milanovic等人,2010年、2016年)。
丙泊酚在急性治疗期间的主要作用方式是减缓GABAA受体通道的关闭,从而增强抑制活性并减少神经元放电(Bai等人,1999年)。然而,我们的实验研究了其对神经发育的长期影响,需要注意的是,我们的治疗方案采用了“两阶段法”,首先让其暴露于丙泊酚中3天,以模拟丙泊酚的长期给药效果,随后在无丙泊酚的环境中持续10天。因此,神经元活动和基因表达谱的改变是丙泊酚暴露期间产生的影响与停药后适应性变化共同作用的结果。RNA测序结果表明,丙泊酚可促进人类脑类器官(HBO)的成熟。这一假设得到了以下事实的支持:在60天时,丙泊酚组与对照组之间,以及在无丙泊酚的情况下,60天与90天之间,观察到与突触功能相关的差异表达基因(DEGs)存在显著重叠。与这些发现一致的是,早期研究表明丙泊酚在体外可促进神经干细胞(NSC)的神经元分化(Sall等人,2012年)。此外,我们观察到在60天时,经丙泊酚早期暴露(IPE)后,自发尖峰活动增加。先前的研究表明,人类脑类器官在类似时期会出现神经元网络的成熟(Fair等人,2020年;Zafeiriou等人,2020年)。因此,我们提出,丙泊酚早期暴露于人类脑类器官后会促进神经元成熟,本研究的一个重要发现是,这种效应仅限于发育早期,而在人类脑类器官更高级的成熟阶段则未观察到。
这就引发了关于丙泊酚(及其他麻醉剂)在关键发育时期的影响、兴奋/抑制平衡(包括γ-氨基丁酸(GABA)从去极化作用向超极化作用的发育转变)以及稳态可塑性的疑问。事实上,有研究报道,幼鼠注射丙泊酚后树突棘密度迅速增加(De Roo等人,2009年),且这与GABA的发育转变相关(Puskarjov等人,2017年)。GABA转变对GABA能突触形成和神经回路发育至关重要(BenAri等人,2012年;Chudotvorova等人,2005年),并且研究表明,在人诱导多能干细胞(iPSC)衍生的生物工程化神经类器官(BENOs)中,这一转变大约发生在40天体外培养(div)时(Zafeiriou等人,2020年)。鉴于丙泊酚作为GABAA受体阳性变构调节剂的作用(Olsen,2018年),当47至50天体外培养的人类脑类器官(HBOs)暴露于丙泊酚时,它可能会调节这一过程,从而导致60天体外培养时神经元活性和突触相关基因表达增强。在未来的研究中,有必要在不同发育阶段的人类脑类器官中,通过膜片钳记录神经元对GABA和丙泊酚的反应,以验证这一假设。本研究中观察到的丙泊酚的阶段特异性效应进一步强调,在未来的发育、神经毒性或化合物筛选研究中,必须仔细考虑人类脑类器官的成熟状态。
总体而言,将HBO模型与2D高清微电极阵列(HD-MEA)记录相结合,能够充分获取组织的电生理参数。然而,2D微电极阵列(MEA)有限的接触面积可以通过使用3D微电极阵列系统来解决(Huang等人,2022年;Sharf等人,2022年)。与HBO切片结合使用时,这将有助于增加与电极接触的神经元数量(Sharf等人,2022年)。正如所报道的那样,培养90天的HBO可能因类器官内部的扩散限制而形成坏死核心(Sharf等人,2022年)。这可能会干扰HBO的功能特性,并可能解释为什么丙泊酚在培养90天的HBO中没有产生效果。 应采用更先进复杂的HBO模型,包括源自多能干细胞(PSCs)的血管化混合谱系组织(Adlakha,2023年),来研究丙泊酚的作用。最近,一种“芯片上ICU患者模型”被用于研究连续4天施用丙泊酚对血脑屏障、肥大细胞和脑类器官的影响。尽管这项研究没有探究丙泊酚对神经元活动的影响,但它表明促炎细胞因子和神经递质受体亚基的表达增加之间存在关联(Saglam-Metiner等人,2024年)。
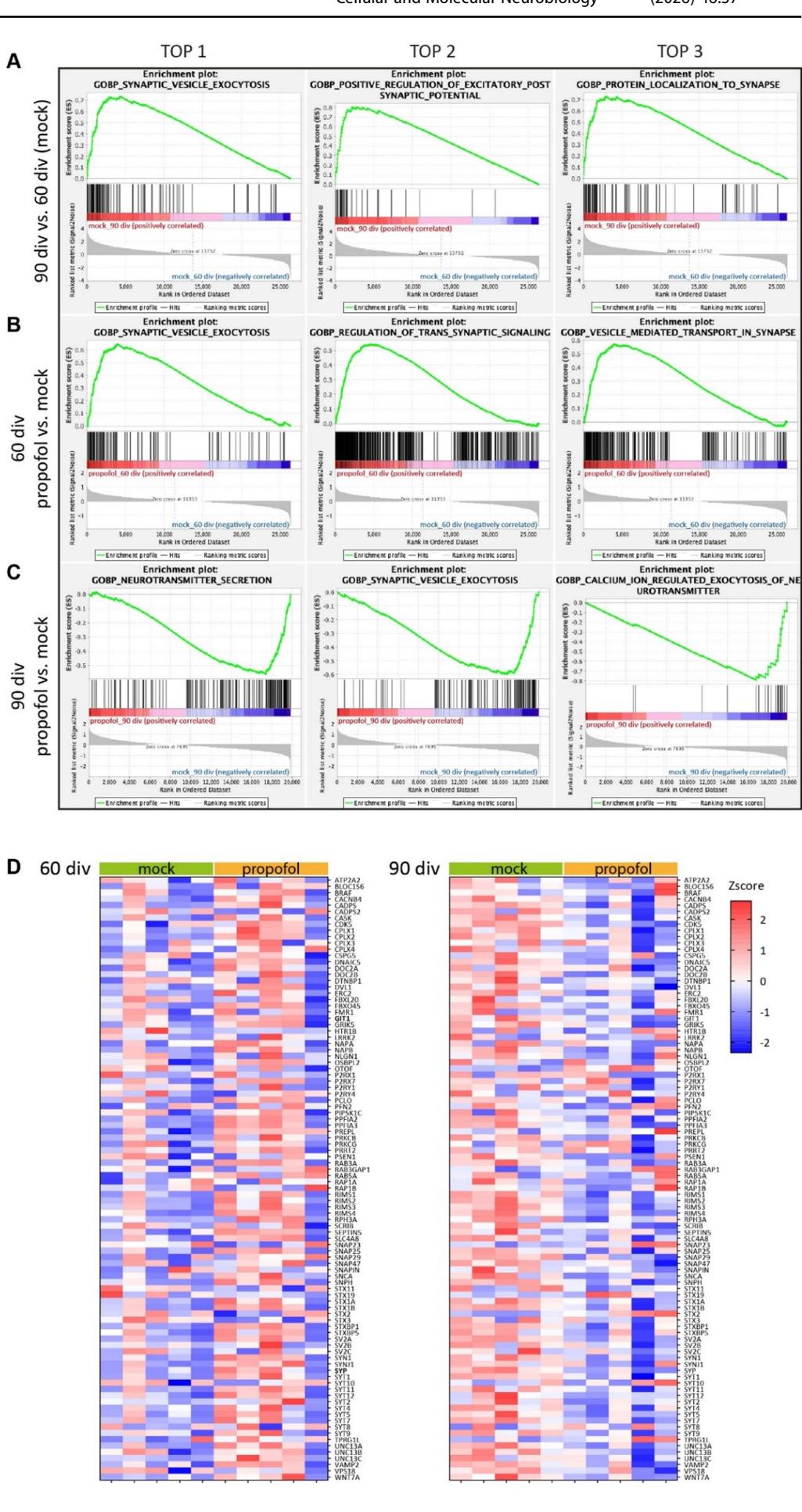
图6 GSEA揭示了丙泊酚在不同发育阶段的相反特异性作用。A-C 使用GSEA 4.1.0生成的富集图,显示了组间比较的前3个GOBP关联:A 90天 vs. 60天(对照组),B 60天丙泊酚组 vs. 对照组,以及C 90天丙泊酚组 vs. 对照组。绿色线图表示基因富集分数(ES),峰值代表最大富集。垂直黑色条表示属于该基因集的单个基因。底部部分显示所有基因的变化,红色表示高表达,蓝色表示低表达。D 属于GOBP_突触小泡胞吐(GO:0016079)的HBO中表达的单个基因在60天丙泊酚组 vs. 对照组以及90天丙泊酚组 vs. 对照组比较中的热图。显示了96个基因的相对表达水平(Z分数),红到蓝的颜色代表从高到低的表达。
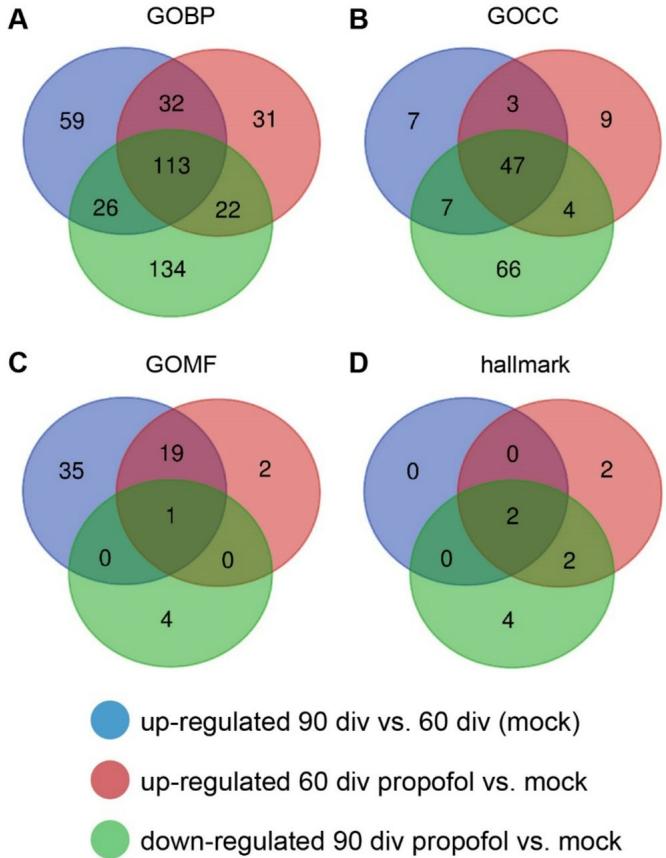
图7 丙泊酚诱导发育阶段特异性基因集调控。显著调控的GOBP、GOCC、GOMF和标志基因集的VENN图(标准:FDR值<0.05,标准化p值<0.05),蓝色圆圈代表模拟处理90天与模拟处理60天的上调,红色圆圈代表丙泊酚处理60天与模拟处理60天的上调,绿色圆圈代表丙泊酚处理90天与模拟处理90天的下调。重叠区域显示了每个发育阶段与丙泊酚处理相关的共享基因集数量。
总之,我们确定了异丙酚(IPE)对人类脑类器官(HBOs)中神经元活动和成熟的阶段特异性影响,从而为关键发育时期的麻醉机制提供了新见解。未来的研究应关注更先进的人类脑类器官模型,探索阶段特异性影响的潜在机制及其长期后果,这可能有助于提高孕期和生命早期的麻醉安全性。
¶ 补充信息
在线版本包含补充材料,可在https://doi.org/10.1007/s10571-026-01673-2获取。
¶ 致谢
手稿中纳入了BioRender插图。SW和YW获得了中国国家留学基金管理委员会的奖学金。
¶ 作者贡献
S.W.:数据整理、形式分析、调查、方法、撰写初稿。C.H.:形式分析、调查、方法。Y.W.、L.L.、Y.Z.:调查、方法。A.S.:形式分析、调查、方法。C.W.:形式分析、调查、方法、撰写初稿。C.P.:方法。M.K.:形式分析、方法。T.M.:概念化、数据整理、撰写初稿。M.K.E.S.:概念化、数据整理、形式分析、调查、方法、撰写初稿。
¶ 资金
开放获取资金由Projekt DEAL支持和组织。作者未披露任何资金信息。
¶ 数据可用性
RNA-seq数据已作为GEO数据集存档,临时登录号为GSE294524:https://www.ncbi.nlm.nih.gov/geo/query/acc.cgi?acc=GSE294524。
¶ 声明
¶ 利益冲突
作者声明不存在利益冲突。
¶ 开放获取
本文采用知识共享署名4.0国际许可协议授权,允许在任何媒介或格式中使用、分享、改编、分发和复制,前提是适当标注原作者和来源,提供知识共享许可协议的链接,并说明是否进行了修改。本文中的图片或其他第三方材料已纳入本文的知识共享许可协议,除非在材料的信用标注中另有说明。如果材料未纳入本文的知识共享许可协议,且您的预期使用未获得法定规定的许可或超出了允许的使用范围,您需要直接从版权持有人处获得许可。如需查看本许可协议的副本,请访问http://reativecommons.org/licenses/by/4.0/。
¶ 参考文献
- Adlakha YK. 人类3D脑类器官:引领脑和神经系统疾病的去分子化研究。《细胞死亡发现》,2023,9:221. 198
- Aksenov DP, Miller MJ, Dixon CJ, Drobyshevsky A. 发育早期接触麻醉剂对学习和感觉功能的影响。《发育心理生物学》,2020,62:559-572. 199
- Bai X. 诱导多能干细胞来源的脑细胞、类器官、组装体和血脑屏障模型在理解酒精和麻醉剂诱导的脑损伤中的应用:一个新兴视角。《神经再生研究》,2024,19:953-954. 200
- Bai D, Pennefather PS, MacDonald JF, Orser BA. 全身麻醉药丙泊酚减缓GABAA受体的失活和脱敏。《神经科学杂志》,1999,19:10635. 201
- Ben-Ari Y, Khalilov I, Kahle KT, Cherubini E. 脑成熟过程中GABA的兴奋/抑制转换与神经系统疾病。《神经科学家》,2012,18:467-486. 202
- Benito-Kwiecinski S, Lancaster MA. 脑类器官:培养皿中的人类神经发育。《冷泉港生物学展望》,2020. https://doi.org/10.1101/cshperspect.a035709. 203
- Berndt N, Rosner J, Haq RU, Kann O, Kovacs R, Holzhuitter HG, Spies C, Liotta A. 麻醉剂丙泊酚可能的神经毒性:对大鼠海马CA3区呼吸链复合体I抑制的证据。《毒理学档案》,2018,92:3191-3205. 204
- Bitzenhofer SH, Popplau JA, Chini M, Marquardt A, Hanganu-Opatz IL. 前额叶活动在发育过程中的短暂增强改变网络成熟并导致成年小鼠认知功能障碍。《神经元》,2021,109:1350-1364.e1356. 205
- Bosnjak ZJ, Logan S, Liu Y, Bai X. 丙泊酚诱导的发育神经毒性分子机制的最新见解:对保护策略的启示。《麻醉与镇痛》,2016,123:1286-1296. 206
- Budday S, Steinmann P, Kuhl E. 人类脑发育的物理生物学。《细胞神经科学前沿》,2015,9:257. 207
- Budic I, Jevtovic Stoimenov TJ, Pavlovic D, Marjanovic V, Djordjevic I, Stevic M, Simic D. 影响丙泊酚药代动力学和药效学的潜在遗传决定因素的临床重要性。《前沿医学(洛桑)》,2022,9:809393. 208
- Castilla Bolanos MA, Chinchalongporn V, Biswas RG, Bailey C, Wu M, Soong R, Saleh F, Simpson A, Schuurmans C, Near J. 通过高分辨率魔角旋转核磁共振波谱对完整人类来源脑类器官进行代谢分析。《生物预印本》,2024:2024.2006.2021.599412. 209
- Chang E, Wang Y, Zhu R, Wu L, Yang Y, Zeng S, Li N, Ruan X, Sun M, Zhang W, Zhou J, Miao M, Zhi H, Zhao H, Chen Q, Sun Q, Chang A, Zhang T, He X, Liu K, Ma S, Zhu W, Zhang Y, Magnani L, Ma D, Zhang J. 通过全面的单细胞RNA测序分析全身麻醉药对人类前额叶皮质细胞的作用谱。《交叉科学》,2023,26:106534. 210
- Chen B, Deng X, Wang B, Liu H. 多次而非单次接触丙泊酚诱导的持续性神经元凋亡和突触丢失导致新生大鼠长期认知功能障碍。《毒理学杂志》,2016,41:627-636. 211
- Cho A-N, Jin Y, An Y, Kim J, Choi YS, Le JS, Kim J, Choi W, K D-J, Yu W, Chang G-E, Kim D-Y, Jo S-H, Kim J, Kim S-Y, Kim Y-G, Kim JY, Choi N, Cheong E, Kim Y-J, Je HS, Kang H-C, Cho S-W. 具有脑 extracellular基质的微流控装置促进人类脑类器官的结构和功能成熟。《自然通讯》,2021,12:4730. 212
- Chudotvorova I, Ivanov A, Rama S, Hubner CA, Pellegrino C, Ben-Ari Y, Medina I. 大鼠海马培养物中KCC2的早期表达增加功能性GABA突触的表达。《生理学杂志》,2005,566:671-679. 213
- Coronel R, Gonzalez-Sastre R, Mateos-Martinez P, Maeso L, Llorente-Beneyto E, Martin-Benito S, Costa Gagosian VS, Foti L, Gonzalez-Caballero MC, López-Alonso V, Liste I. 人类脑类器官:神经发育和脑疾病的复杂、多功能且与人类相关的模型。《神经再生研究》,2026,21:837-854. 214
- Creeley C, Dikranian K, Dissen G, Martin L, Olney J, Brambrink A. 丙泊酚诱导的胎猴和新生猴脑中神经元和少突胶质细胞凋亡。《英国麻醉学杂志》,2013,110(增刊1):i29-i38. 215
- Dailland P, Cockshott ID, Lrin JD, Jacqnot P, Jorrot JC, Eve J, Harmey JL, Conseiler C. 剖宫产期间静脉注射丙泊酚:胎盘转运、母乳中的浓度:一项初步研究。《麻醉学》,1989,71:827-834. 216
- De Roo M, Klauser P, Briner A, Nikonenko I, Mendez P, Dayer A, Kiss JZ, Muller D, Vutskits L. 麻醉剂在脑发育的关键时期快速促进突触形成。《公共科学图书馆·综合》,2009,4:e7043.
- 迪尼斯-奥利维拉 RJ. 丙泊酚和磷丙泊酚的代谢谱:临床和法医解释方面. 《国际生物医学研究》,2018:6852857. 218
- 杜 Z、臧 Z、罗 J、刘 T、杨 L、蔡 Y、王 L、张 D、赵 J、高 J、吕 K、王 L、李 H、龚 H、范 X. 长期暴露于(2R,6R)-羟基去甲氯胺酮对人胚胎干细胞来源的脑类器官产生发育神经毒性. 《危险材料杂志》,2023,453:131379. 219
- 费尔 SR、朱利安 D、哈特劳布 AM、普苏鲁里 ST、马利克 G、萨默菲尔德 TL、赵 G、赫斯特 AB、阿克曼 W、霍林斯沃思 EW、阿里 M、麦克尔罗伊 CA、布希姆希 IA、伊米托拉 J、迈特雷 NL、贝德罗西安 TA、赫斯特 ME. 脑类器官的电生理成熟与动态形态和细胞发育相关. 《干细胞报告》,2020,15:855-868. 220
- 加斯科因 DA、谢尔久科娃 NA、阿克谢诺夫 DP. γ-氨基丁酸能系统的早期发育与新生儿麻醉相关风险. 《国际分子科学杂志》,2021,22(23):12951. https://doi.org/10.3390/ijms222312951. 221
- 格伦契奇 V、莫里奇 M、楚 Y、汉科 V、李 J、卢基奇 IK、卢基奇 A、埃达瑟里 SL、克罗因 JS、珀森斯 AL、佩里 P、凯利 L、夏夫利 TJ、尼斯 K、内皮尔 TC、科多沃尔 JH、图曼 KJ. 宫内暴露于麻醉剂改变发育中大脑皮层的神经元迁移模式并导致大鼠出生后行为缺陷. 《大脑皮层》,2019,29:5285-5301. 222
- 格雷德尔 JA、特恩奎斯特 PA、麦基弗 MB、皮尔斯 RA. 丙泊酚在大鼠脑组织中的扩散系数和分配系数测定:对体外药物作用研究的意义. 《英国麻醉学杂志》,2004,93:810-817. 223
- 哈季汉比 A、卡拉吉安尼斯 A、塞帕兰比尔 SM、阿克兰 GL、古林 AV. 全身麻醉剂对脑乳酸释放的影响. 《欧洲药理学杂志》,2020,881:173188. 224
- 广津 A、岩田 Y、辰巳 K、宫井 Y、松山 T、田中 T. 母体暴露于挥发性麻醉剂诱导胎脑白细胞介素-6并影响神经元发育. 《欧洲药理学杂志》,2019,863:172682. 225
- 黄 Q、唐 B、罗梅罗 JC、杨 Y、埃尔赛义德 SK、帕哈帕莱 G、李 TJ、莫拉莱斯·潘托哈 IE、韩 F、伯林基 C、向 T、索拉佐 M、哈通 T、秦 Z、卡福 BS、斯米尔诺娃 L、格拉西亚斯 DH. 用于脑类器官的壳式微电极阵列(MEAs). 《科学进展》,2022,8:eabq5031. 226
- 英 C、武茨基斯 L. 发育中大脑麻醉神经毒性的未解问题. 《当代麻醉学观点》,2023,36:510-515. 227
- 卡伦 T、施拉格 GW、本迪克斯 I、西夫林格 M、赫尔曼 R、潘塔齐斯 C、埃诺特 D、凯勒 M、克纳 T、费尔德霍夫-穆泽 U. 丙泊酚对未成熟大鼠大脑的短期和长期神经发育结局的影响. 《公共科学图书馆·综合》,2013,8:e64480. 228
- 基里舒克 S、辛宁 A、布兰基 O、杨 J-W、卢曼 HJ、基尔布 W. 早期神经元活动对新皮层发育的调节:生理学和病理生理学. 《细胞神经科学前沿》,2017,11:2017. 229
- 李 JA、裴 DH、崔 WH、赵 CH、邦 YS、柳 J. 七氟醚暴露对脑类器官中胎儿脑发育的影响. 《分子神经科学杂志》,2022,72:2440-2450. 230
- 李 J、熊 M、阿尔哈谢姆 HM、张 Y、蒂拉克 V、帕特尔 A、西格尔 A、叶 JH、贝克 A. 产前丙泊酚暴露对大鼠出生后发育的影响. 《神经毒理学与致畸学》,2014,43:51-58. 231
- 梁 Y、黄 Y、邵 R、肖 F、林 F、戴 H、潘 L. 丙泊酚通过诱导线粒体凋亡产生神经毒性. 《实验与治疗医学》,2022,24:630.
- Logan S, Arzua T, Yan Y, Jiang C, Liu X, Yu LK, Liu QS, Bai X. 人诱导多能干细胞来源大脑类器官的结构、分子和电生理表型动态表征及与胎儿和成人基因谱的比较[J]. Cells, 2020. https://doi.org/10.3390/cells9051301.
- Long B, Li S, Xue H, Sun L, Kim DH, Liu Y. 丙泊酚对人诱导多能干细胞来源神经前体细胞的影响[J]. Neural Plasticity, 2017: 9182748.
- Malhotra A, Yosh E, Xiong M. 丙泊酚在非产科手术中对胎儿大脑的影响[J]. Brain Sci, 2017, 7(8): 107. https://doi.org/10.3390/brainsci7080107.
- Marin O. 精神疾病治疗的发育时机与关键窗口期[J]. Nat Med, 2016, 22: 1229-1238.
- Milanovic D, Popic J, Pesic V, Loncarevic-Vasiljkovic N, Kanazir S, Jevtovic-Todorovic V, Ruzdijic S. 反复给予丙泊酚后新生大鼠大脑中钙蛋白酶和半胱天冬酶-3活性的区域和时间分布特征[J]. Dev Neurosci, 2010, 32: 288-301.
- Milanovic D, Pesic V, Loncarevic-Vasiljkovic N, Pavkovic Z, Popic J, Kanazir S, Jevtovic-Todorovic V, Ruzdijic S. Fas配体/Fas死亡受体通路参与丙泊酚诱导的新生大鼠大脑凋亡和神经炎症[J]. Neurotox Res, 2016, 30: 434-452.
- Milanovic D, Pesic V, Loncarevic-Vasiljkovic N, Avramovic V, Tesic V, Jevtovic-Todorovic V, Kanazir S, Ruzdijic S. 新生期丙泊酚麻醉改变成年大鼠突触可塑性蛋白表达并增加刻板行为和抗焦虑行为[J]. Neurotox Res, 2017, 32: 247-263.
- Olsen RW. γ-氨基丁酸A型受体:正向和反向变构调节剂[J]. Neuropharmacology, 2018, 136: 10-22.
- Paulus W. 妊娠期用药[J]. MMW Fortschr Med, 2005, 147: 37-40.
- Pesic V, Milanovic D, Popic J, Smiljanic K, Tesic V, Kanazir S, Jevtovic-Todorovic V, Ruzdijic S. 新生期丙泊酚麻醉改变活性依赖过程并诱导大鼠青春期对右旋苯丙胺的短暂运动亢进反应[J]. Int J Dev Neurosci, 2015, 47: 266-277.
- Puskarjov M, Fiumelli H, Briner A, Bodogan T, Demeter K, Lacoh CM, Mavrovic M, Blaesse P, Kaila K, Vutskits L. 钾-氯共转运体2介导的氯离子外流决定丙泊酚麻醉对树突棘的发育阶段依赖性影响[J]. Anesthesiology, 2017, 126: 855-867.
- Qian X, Song H, Ming GL. 大脑类器官:进展、应用与挑战[J]. Development, 2019. https://doi.org/10.1242/dev.166074.
- Reighard C, Junaid S, Jackson WM, Arif A, Waddington H, Whitehouse AJO, Ing C. 儿童期麻醉暴露与神经发育结局:系统评价与荟萃分析[J]. JAMA Netw Open, 2022, 5: e2217427.
- Reitman E, Flood P. 妊娠期非产科手术的麻醉考量[J]. Br J Anaesth, 2011, 107(Suppl 1): i72-i78.
- Rizzi S, Carter LB, Ori C, Jevtovic-Todorovic V. 临床麻醉对豚鼠胎儿大脑造成永久性损伤[J]. Brain Pathol, 2008, 18: 198-210.
- Ruggiero A, Ariano A, Triarico S, Capozza MA, Ferrara P, Attina G. 新生儿药理学及临床意义[J]. Drugs Context, 2019, 8: 212608.
- Saglam-Metiner P, Yanasik S, Odabasi YC, Modamio J, Negwer M, Biray-Avci C, Guler A, Erturk A, Yildirim E, Yesil-Celiktas O. 模拟肥大细胞与大脑类器官在神经炎症中协同作用的ICU芯片模型[J]. Commun Biol, 2024, 7: 1627.
- Sahinovic MM, Struys MMRF, Absalom AR. 丙泊酚的临床药代动力学与药效学[J]. Clin Pharmacokinet, 2018, 57: 1539-1558.
- Sall JW, Stratmann G, Leong J, Woodward E, Bickler PE. 临床相关浓度的丙泊酚可增加神经元分化但对体外海马神经前体细胞无毒性[J]. Anesthesiology, 2012, 117: 1080-1090.
- Sen T, Sen N. 异氟醚通过组蛋白脱乙酰酶4抑制CREB活性导致发育中大脑认知障碍[J]. Neurobiol Dis, 2016, 96: 12-21.
- Shang J, Li B, Fan H, Liu P, Zhao W, Chen T, Chen P, Yang L. 七氟醚促进人诱导多能干细胞来源中脑类器官多巴胺能神经元过早分化[J]. Front Cell Dev Biol, 2022, 10: 941984.
- Sharf T, van der Molen T, Glasauer SMK, Guzman E, Buccino AP, Luna G, Cheng Z, Audouard M, Ranasinghe KG, Kudo K, Nagarajan SS, Tovar KR, Petzold LR, Hierlemann A, Hansma PK, Kosik KS. 人类大脑类器官中的功能性神经元环路和振荡动力学[J]. Nat Commun, 2022, 13: 4403.
- Sidhaye J, Knoblich JA. 大脑类器官:研究人类神经发育与疾病的综合生物检测体系[J]. Cell Death Differ, 2021, 28: 52-67.
- Subramanian A, Tamayo P, Mootha VK, Mukherjee S, Ebert BL, Gillette MA, Paulovich A, Pomeroy SL, Golub TR, Lander ES, Mesirov JP. 基因集富集分析:一种基于知识的基因组表达谱解读方法[J]. Proc Natl Acad Sci U S A, 2005, 102: 15545-15550.
- Sutcliffe M, Lancaster MA. 利用标准实验室设备生成三维大脑类器官的简易方法[J]. Methods Mol Biol, 2019, 1576: 1-12.
- Trujillo CA, Gao R, Negraes PD, Gu J, Buchanan J, Preissl S, Wang A, Wu W, Haddad GG, Chaim IA, Domissy A, Vandenberghe M, Devor A, Yeo GW, Voytek B, Muotri AR. 皮质类器官中出现的复杂振荡波模拟人类早期大脑网络发育[J]. Cell Stem Cell, 2019, 25: 558-569.e557.
- Van Hese L, Theys T, Absalom AR, Rex S, Cuypers E. 靶控输注期间丙泊酚和瑞芬太尼在血浆与脑组织中预测浓度与实际浓度的比较:一项前瞻性观察研究[J]. Anaesthesia, 2020, 75: 1626-1634.
- Wan J, Shen CM, Wang Y, Wu QZ, Wang YL, Liu Q, Sun YM, Cao JP, Wu YQ. 新生期反复暴露于丙泊酚损害大鼠成年后海马突触可塑性和识别功能[J]. Brain Res Bull, 2021, 169: 63-72.
- Wang Y, Wernersbach I, Strehle J, Li S, Appel D, Klein R, Rier K, Hummel R, Tegeder I, Schäfer MKE. 创伤后早期通过PLX3397抑制CSF1R对小鼠创伤性脑损伤后炎症和神经元维持产生时间依赖性和性别依赖性影响[J]. Brain Behav Immun, 2022, 106: 49-66.
- Waterston RH, Lindblad-Toh K, Birney E, Rogers J, Abril JF, Agarwal P, Agarwala R, Ainscough R, Alexandersson M, An P, Antonarakis SE, Attwood J, Baertsch R, Bailey J, Barlow K, Beck S, Berry E, Birren B, Bloom T, Bork P, Botcherby M, Bray N, Brent MR, Brown DG, Brown SD, Bult C, Burton J, Butler J, Campbell RD, Carninci P, Cawley S, Chiaromonte F, Chinwalla AT, Church DM, Clamp M, Clee C, Collins FS, Cook LL, Copley RR, Coulson A, Couronne O, Cuff J, Curwen V, Cutts T, Daly M, David R, Davies J, Delehaunty KD, Deri J, Dermitzakis ET, Dewey C, Dickens NJ, Diekhans M, Dodge S, Dubchak I, Dunn DM, Eddy SR, Elnitski L, Emes RD, Eswara P, Eyras E, Felsenfeld A, Fewell GA, Flicek P, Foley K, Frankel WN, Fulton LA, Fulton RS, Furey TS, Gage D, Gibbs RA, Glusman G, Gnerre S, Goldman N, Goodstadt L, Grafham D, Graves TA, Green ED, Gregory S, Guigó R, Guyer M, Hardison RC, Haussler D, Hayashizaki Y, Hillier LW, Hinrichs A, Hlavina W, Holzer T, Hsu F, Hua A, Hubbard T, Hunt A, Jackson I, Jaffe DB, Johnson LS, Jones M, 等. 小鼠基因组的初步测序与比较分析[J]. Nature, 2002, 420: 520-562.
- Xiong M, Li J, Alhashem HM, Tilak V, Patel A, Pisklakov S, Siegel A, Ye JH, Bekker A. 妊娠大鼠暴露于丙泊酚诱导子代神经毒性和持续性学习缺陷[J]. Brain Sci, 2014, 4: 356-375.
- Yan Y, Qiao S, Kikuchi C, Zaja I, Logan S, Jiang C, Arzua T, Bai X. 丙泊酚诱导新生小鼠海马神经元凋亡但不影响星形胶质细胞、少突胶质细胞或神经干细胞[J]. Brain Sci, 2017, 7(10): 130. https://doi.org/10.3390/brainsci7100130.
- Zafeiriou MP, Bao G, Hudson J, Halder R, Blenkle A, Schreiber MK, Fischer A, Schild D, Zimmermann WH. 生物工程神经元类器官中γ-氨基丁酸极性转换与神经元可塑性[J]. Nat Commun, 2020, 11: 3791.
- Zhang J, Li Y. 丙泊酚诱导的发育性神经毒性:从机制到治疗策略[J]. ACS Chem Neurosci, 2023, 14: 1017-1032.
- Zhao HH, Haddad G. 大脑类器官的实验方案与局限性[J]. Front Cell Neurosci, 2024, 18: 2024.
- Zhong L, Luo F, Zhao W, Feng Y, Wu L, Lin J, Liu T, Wang S, You X, Zhang W. 妊娠晚期暴露于丙泊酚通过BDNF-TrkB信号通路损害大鼠子代的学习记忆功能[J]. J Cell Mol Med, 2016, 20: 1920-1931.
- Zhou N, Liang S, Yue X, Zou W. 产前麻醉暴露与子代神经发育结局:叙述性综述[J]. Front Neurol, 2023, 14: 1146569.
出版商说明:施普林格·自然对于已发表地图中的管辖权声明以及机构隶属关系保持中立。