¶ 《细胞神经科学前沿》
¶ 明视觉条件下含黑视蛋白的视网膜神经节细胞在瞳孔光反射中的关键作用
¶ 原文下载32b25b3eb8acd0a33778d11f2b937cafeb81_origin.pdf
Jeremy Matthew Bohl †, Abdul Rhman Hassan †, Zachary J. Sharpe, Zachary J. Sharpe †, Megi Kola, Angela Shehu, Deborah Langrill Beaudoin, Tomomi Ichinose *
美国密歇根州底特律市韦恩州立大学医学院眼科、视觉与解剖科学系
¶ 摘要
瞳孔光反射(PLR)对于保护视网膜免受过量光线损伤至关重要。视网膜中的内在光敏视网膜神经节细胞(ipRGCs)是一类神经元,它们在PLR的产生中起着关键作用,既能接收视杆/视锥光感受器的信号,又能通过黑视蛋白直接感知光线。以往的研究通过基因修饰的小鼠模型,探究了光感受器和ipRGCs在PLR中的作用。在本研究中,我们使用N-亚硝基-N-甲基脲(MNU)急性消融光感受器,以考察ipRGCs在PLR中的作用。我们利用C57BL6/J野生型(WT)小鼠,在腹腔注射MNU前以及注射后5天,通过三种不同强度的光刺激,进行了PLR和多电极阵列(MEA)记录。我们还对视杆和视锥功能缺陷小鼠(Gnat1–/–和Cnga3–/–:双敲除小鼠,dKO)进行了相同的测量,以便与已发表的、利用突变小鼠研究光感受器和ipRGCs在PLR中作用的研究结果进行比较。 在野生型小鼠中,随着光刺激强度的增加,PLR引起的瞳孔收缩程度也随之增大。在MNU处理的小鼠中,低强度光刺激无法诱发PLR,这表明在此光强度下,PLR是由光感受器引发的。相比之下,高强度光刺激能完全诱发PLR,与野生型小鼠的反应相似。在双敲除小鼠中,低强度光刺激无法诱发PLR,而高强度光刺激会诱发迟发性PLR,这与以往的报道一致。对MNU处理小鼠的视网膜组织进行的离体MEA记录显示,存在一群ipRGCs,它们的反应起始快、达峰时间短,这表明它们可能驱动了快速的PLR反应。 这些结果表明,ipRGCs主要在高强度光线下对PLR起作用,这与以往利用突变小鼠模型得出的结果不一致。我们的研究结果显示,当受到高强度光刺激时,ipRGCs中的黑视蛋白反应会产生快速且强烈的PLR。
¶ 引言
瞳孔光反射(PLR)在眼睛受到光照时被诱发,可保护视网膜免受过量光线照射。诱发瞳孔光反射的神经通路始于视网膜光感受器和内在光敏视网膜神经节细胞(ipRGCs),这些细胞将信号传递至中脑的橄榄顶盖前核(OPN)和动眼神经副核,最终信号传回到眼眶内的睫状神经节,使瞳孔收缩。由于瞳孔光反射易于检查,它在临床上被广泛用于诊断眼部和脑部疾病,如青光眼和脑损伤(La Morgia等人,2018年;Pinheiro和Da Costa,2021年)。
内在光敏视网膜神经节细胞(ipRGCs)是最近才被发现的。Lucas等人(2001,2003)报告称,具有视杆/视锥细胞退化(rd/rd)的小鼠在高辐照度下仍保留强烈的瞳孔光反射(PLR)。在这些小鼠中进一步敲除黑视蛋白基因会减弱瞳孔光反射(Lucas等人,2003),这表明表达黑视蛋白的细胞可直接感知光线并诱发瞳孔光反射。表达黑视蛋白的细胞被归类为内在光敏视网膜神经节细胞,并且已被证明在非成像视觉中至关重要,包括瞳孔光反射和昼夜光同步(Hattar等人,2003;Guler等人,2008;Aranda和Schmidt,2021)。rd/rd小鼠在暗视到间视光线下不会表现出瞳孔光反射(Lucas等人,2001;Lucas等人,2003),这表明在较低光照条件下,视杆/视锥光感受器输入到内在光敏视网膜神经节细胞会诱发瞳孔光反射,而黑视蛋白则在较高辐照度下负责瞳孔光反射。
除了具有黑视蛋白光敏性外,内在光敏视网膜神经节细胞(ipRGCs)还接收视杆/视锥光感受器的输入。研究人员利用突变小鼠模型,探究了视杆/视锥细胞以及黑视蛋白反应在瞳孔光反射(PLR)中的作用。在视杆/视锥细胞功能异常的小鼠和人类模型中,高辐照度下可诱发瞳孔光反射,但其起始速度明显慢于对照组(Gooley 等人,2012;Kostic 等人,2016)。在代谢型谷氨酸受体6敲除(mGluR6-KO)小鼠中也观察到了瞳孔光反射起始延迟的现象,这些小鼠的视杆/视锥信号无法正常传递至ON型双极细胞及下游的神经节细胞(Beier 等人,2022)。相反,在因opn4基因缺失(opn4–/–)而缺乏黑视蛋白的小鼠中,多种辐照度下均可诱导出瞳孔光反射;然而,在光照期间,瞳孔收缩仅为短暂现象(Zhu 等人,2007)。这些研究表明,在所有刺激强度下,视杆/视锥光感受器对瞳孔光反射的快速起始至关重要,而内在光敏视网膜神经节细胞中的黑视蛋白反应仅在高辐照度下诱发瞳孔光反射,并参与形成瞳孔光反射的持续成分。
大多数关于瞳孔光反射(PLR)的研究都是利用转基因小鼠模型进行的,我们想知道这些小鼠的视网膜是否可能通过重塑产生代偿效应或变化。我们使用N-亚硝基-N-甲基脲(MNU)在5-7天的短时间内选择性地消融视杆/视锥光感受器(Smith和Yielding,1986;Smith等人,1988),这种方法将可塑性变化的可能性降到了最低。这种方法使我们能够研究视杆/视锥光感受器和内在光敏视网膜神经节细胞(ipRGCs)在瞳孔光反射中的作用,揭示了迄今为止未知的内在光敏视网膜神经节细胞的特征。
¶ 材料与方法
¶ 动物模型建立
所有动物实验程序均获得韦恩州立大学机构动物护理和使用委员会的批准(IACUC 20-10-2909 和 23-11-6310)。实验是按照《ARVO眼科学和视觉研究动物使用声明》进行的。本研究使用了野生型(WT)小鼠(C57BL/6J;#000664,美国缅因州杰克逊实验室),年龄为1至6个月,雌雄均有。
N-亚硝基-N-甲基脲(MNU)小鼠的制备方法如下:将MNU溶液(HY-34758,MedChem Express公司,美国新泽西州)以62.5–93.75 mg/kg的单剂量腹腔注射到野生型小鼠体内。注射后5–7天进行瞳孔测量和多电极阵列记录。作为对照,向野生型小鼠腹腔注射生理盐水。
视杆/视锥双敲除(Cnga3–/–,Gnat1–/–;dKO)小鼠(由Samar Hattar博士馈赠)缺乏视锥细胞环核苷酸门控通道(Cnga3)和视杆细胞转导蛋白α亚基(Gnat1),这些是光感受器视觉循环中的关键分子。对dKO小鼠进行了瞳孔光反射(PLR)、多电极阵列(MEA)和免疫组织化学(IHC)染色评估。杂合同窝小鼠被用作对照(Cnga3+/–,Gnat1+/–;dKO+/–)。
¶ 瞳孔测量法
在进行瞳孔光反射(PLR)测量前,小鼠需经过1小时以上的暗适应。记录在 Zeitgeber 时间3点至6点之间进行。所有记录过程中,实验人员用手对小鼠进行机械固定,固定时间为数分钟,期间不使用麻醉剂。每只小鼠从一只或两只眼睛进行瞳孔测量。若测量两只眼睛,在完成第一只眼睛的测量后,需让小鼠暗适应30分钟,再测量第二只眼睛。每只小鼠仅进行一次瞳孔测量。所有操作均在昏暗的红光条件下进行。
瞳孔测量是使用配备定焦摄像机(Lumenara 400;Teledyne Technologies,美国加利福尼亚州)的体视显微镜,在850纳米红外LED(M850L3;ThorLabs,美国新泽西州)照明下进行的。瞳孔光反射(PLR)由500纳米(绿色)光诱导10秒,采用三种刺激强度:低(中间视觉,5.34×10⁴光子/μm²/s)、中(明视觉,2.95×10⁵光子/μm²/s)和高(高明视觉,3.72×10⁶光子/μm²/s)。这些强度是使用光度计(International Light Technologies,美国马萨诸塞州皮博迪)在小鼠头部置于LED下方的位置测量的。瞳孔光反射记录以约25帧/秒(FPS)的速度进行视频录制(NorPix 9;NorPix,加拿大魁北克)。
¶ 视网膜制备
实验技术与先前描述的相似(Ichinose等人,2014;Ichinose和Hellmer,2016)。简要来说,对28-60日龄的小鼠实施安乐死,在黑暗条件下,使用含氧的HEPES缓冲溶液制备全视网膜标本或250μm厚的切片标本,该缓冲溶液的成分如下(单位:mM):115氯化钠、2.5氯化钾、2.5氯化钙、1.0氯化镁、10 HEPES和28葡萄糖,并用氢氧化钠将pH值调节至7.37。
¶ 免疫组织化学
我们采用了标准的免疫组织化学程序(Farshi等人,2016年)。视网膜全铺片用4%多聚甲醛固定,并用含10%正常驴血清(NDS)和0.5%曲拉通-X的PBS(PBS-T)封闭。将黑视蛋白抗体(1:5000,AB-N39,Advanced Targeting Systems公司,美国加利福尼亚州)在PBS-T中于4°C孵育3天,随后用Alexa568驴抗兔抗体(Invitrogen公司;A10042)孵育2小时。Gnat1抗体(1:1000,PA5-28336,赛默飞世尔科技公司)在室温下孵育过夜。DAPI(1:10000,西格玛公司)与二抗一起孵育20分钟。用共聚焦显微镜(TCS SP8;徕卡公司,德国)观察染色组织。使用40倍物镜,以0.3μm的数字步长对光感受器层或神经节细胞层进行完整扫描。在视网膜所有四个象限的周边视网膜中部采集共聚焦图像。
¶ 多电极阵列(MEA)
野生型(WT)、MNU处理和双敲除(dKO)小鼠经过 overnight 暗适应后,在红外光下使用夜视设备制备视网膜全铺片。随后将视网膜标本分为4个象限。每个视网膜象限连同一片透明滤纸一起放置在用于BioCAM DupleX系统(3Brain公司,瑞士)的Accura HD-MEA芯片(4096个记录电极排列在3.8毫米×3.8毫米区域的多电极阵列)上,并用方形铂锚固定。标本持续灌注含氧的AMES培养基,流速为3–7毫升/分钟,并通过温度控制器(Warner TC-324C,ALA Scientific公司,美国纽约)维持在33–34°C。在部分记录中,使用谷氨酸受体阻滞剂混合液来阻断光感受器向视网膜神经网络的突触输入,其中包括:mGluR6激动剂L-2-氨基-4-膦酰基丁酸(L-AP4,10μM)、离子型谷氨酸拮抗剂6-氰基-7-硝基喹喔啉-2,3-二酮(CNQX,15μM)、红藻氨酸拮抗剂(S)-1-(2-氨基-2-羧乙基)-3-(2-羧基-5-苯基噻吩-3-基-甲基)-5-甲基嘧啶-2,4-二酮(ACET,1μM)以及N-甲基-D-天冬氨酸(NMDA)拮抗剂D-(-)-2-氨基-5-膦酰基戊酸(D-AP5,50μM)。所有谷氨酸阻滞剂均购自Tocris公司(R&D Systems Inc.,美国明尼苏达州明尼阿波利斯)。使用与瞳孔光反射测量相同的三种强度的绿光刺激,诱导神经节细胞的光诱发锋电位反应。
¶ 数据分析
使用AIVIA软件(徕卡)分析瞳孔光反射(PLR)视频,以测量记录过程中每一帧的瞳孔直径。使用SigmaPlot15(美国加利福尼亚州Grafitti公司)通过单组分指数函数拟合PLR收缩曲线(拟合曲线的R2>0.90),并采用单因素方差分析(ANOVA)结合Tukey事后检验法比较野生型(WT)、MNU注射组和双敲除(dKO)小鼠的潜伏期、曲率(tau)和峰值收缩。所有统计测量中,n等于眼睛的数量,p值<0.05被认为具有统计学意义。
对于免疫组织化学图像,使用ImageJ(美国马里兰州国立卫生研究院)对黑视蛋白和DAPI阳性细胞进行计数。使用AIVIA软件分析Gnat1和DAPI染色的光感受器。在每种条件下,对视网膜每个象限中140×140μm大小图像内的细胞进行分析。采用单因素方差分析(ANOVA)结合Tukey事后检验法,比较生理盐水组、MNU注射组和双敲除(dKO)小鼠的DAPI和黑视蛋白阳性细胞计数。所有分析中,p<0.05被认为具有统计学显著性。
多电极阵列(MEA)分析使用Brainwave 5软件(3Brain公司,瑞士)以及定制的Python和MATLAB代码(由Benjamin Sivyer博士慷慨提供)进行。采用自动 spike 分选器1,根据位置以及Hilgen等人(2017年)所述的波形的两个成分来检测并聚类峰电位。每个组织的多个试验分别进行分选,且每个案例都发现了相似的聚类数量。使用MATLAB(MathWorks公司,美国马萨诸塞州纳蒂克)对峰电位序列和放电率(FR)进行进一步分析。对于每个试验,所有检测到的单位都经过相同的无偏滤波。基于以往研究(Qiu等人,2005年)、(Prigge等人,2016年)、(Mure等人,2019年)、(Berry等人,2023年),ipRGC单位由三个参数定义:刺激开始后,平均放电率(mFR)达到基线mFR + 2×标准差(SD)(反应潜伏期);达到该阈值后20秒内的mFR保持在基线mFR + SD;刺激结束后的一段时间内的mFR大于基线mFR + SD。从未达到基线mFR + 2×SD或基线mFR为零的细胞单位被舍弃。我们将快速起始的ipRGC单位定义为在刺激开始后0至2秒内出现反应潜伏期的单位。
使用SigmaPlot15.0(Grafitti)进行曲线拟合,以计算上升相速率。应用了指数上升函数:y = aebt
其中(a)是基线mFR,(b)是增长率(若b>0表示指数增长,b<0表示指数衰减),(e)是自然对数的底数,(t)表示时间。我们计算了每种视网膜组织对光的反应中的放电率增加量(b值)。这一过程针对每种小鼠类型进行,并进行了后续比较。此外,我们还测量了从光刺激开始到达到速率峰值63%时的潜伏期。使用Prism 8(GraphPad Software Inc.,加利福尼亚州)中的方差分析(ANOVA)对这些值进行比较。本分析中,p值<0.05被认为具有显著性。
¶ 结果
C57野生型、MNU处理及视杆-视锥细胞功能障碍小鼠的瞳孔光反射(PLR)
我们在野生型小鼠中进行了瞳孔光反射(PLR)实验,以研究视网膜细胞的作用。在光照前,暗适应使瞳孔完全散大。在10秒的弱光闪烁刺激下,瞳孔轻微收缩后恢复(图1A、B,弱光组)。随着辐照度增加,瞳孔收缩更快且更明显(图1A、B,中光组和强光组)。
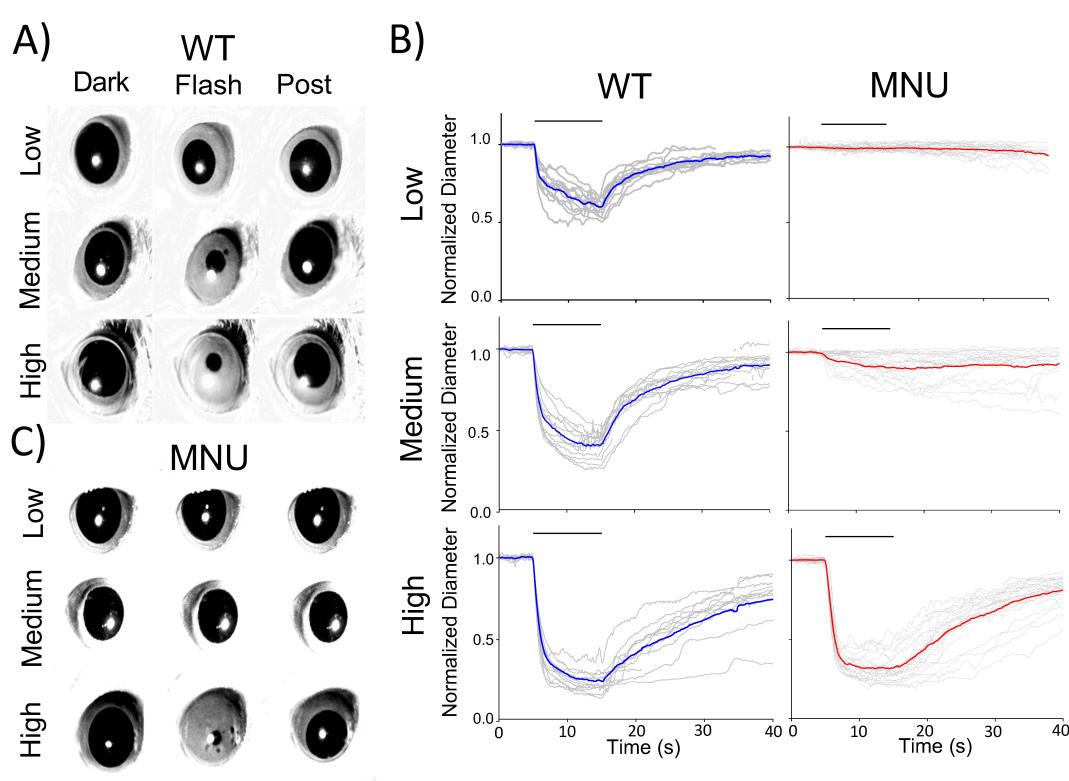
图1 野生型(WT)和N-亚硝基-N-甲基脲(MNU)注射小鼠的瞳孔光反射(PLR):(A)WT小鼠PLR记录的单帧图像。展示了每种光强度下光刺激前(黑暗)、光刺激期间(闪光)和恢复阶段(之后)的瞳孔图像。(B)将标准化瞳孔直径作为时间的函数绘图。叠加了单个眼睛(灰色轨迹)以及WT(蓝色)和MNU(红色)的平均瞳孔收缩情况。(C)MNU注射小鼠的一组代表性瞳孔图像。在低光和中光刺激下,几乎检测不到PLR。相比之下,高光可诱发PLR,其动力学和水平与WT的PLR相似。
瞳孔光反射(PLR)由内在光敏视网膜神经节细胞(ipRGCs)介导(Guler 等人,2008),这些细胞通过视黑质直接感知光线(Lucas 等人,2003),同时也接收来自光感受器的突触输入。为了研究视黑质和光感受器在瞳孔光反射中的作用,我们向野生型(WT)小鼠腹腔注射了甲基亚硝基脲(MNU),研究表明这种物质能在几天内清除光感受器,因此,此时的瞳孔光反射仅由视黑质的反应引起(Smith 和 Yielding,1986;Smith 等人,1988;Wang 等人,2021)。注射 MNU 后 5 至 7 天,我们对瞳孔光反射进行了测量(图 1B、C)。弱光刺激未能在 MNU 处理的小鼠中诱发瞳孔光反射,这表明在这种光照条件下,视杆细胞和视锥细胞对瞳孔光反射至关重要。中等强度的光刺激能在 MNU 处理的小鼠中诱发瞳孔光反射,但与野生型小鼠相比,其收缩幅度更小,时程更慢(图 1B、C,中等强度)。这些结果与之前的观察一致,即内在光敏视网膜神经节细胞的敏感性较低,且视黑质反应较迟缓(Gooley 等人,2012;Kostic 等人,2016;Beier 等人,2022)。随后,我们将刺激强度提高到高辐照度。此时瞳孔光反射被充分且快速地诱发,与野生型小鼠的瞳孔光反射相同(图 1B,高强度)。这一结果出乎意料,因为之前的研究认为,在所有辐照度下,光感受器都会影响瞳孔光反射的起始(Gooley 等人,2012;Kostic 等人,2016;Beier 等人,2022)。
我们分析了野生型(WT)和甲基亚硝基脲(MNU)处理眼的强光诱发瞳孔光反射(PLR)起始情况(图2)。我们发现,野生型眼的瞳孔光反射潜伏期显著短于甲基亚硝基脲处理眼(图2A、B,野生型n=5,甲基亚硝基脲处理组n=5,p<0.05,非配对Student t检验)。然而,甲基亚硝基脲处理眼的瞳孔光反射收缩速度快于野生型眼(图2C、D,p<0.05,配对t检验,n=21只眼),且达到最大收缩的时间相近(图1,强光)。野生型眼和甲基亚硝基脲处理眼的收缩程度相同(图2E,p=0.94)。这些分析证实,甲基亚硝基脲处理小鼠的强光诱发瞳孔光反射上升阶段与野生型眼相当。由于甲基亚硝基脲处理眼仅含有内在光敏视网膜神经节细胞(ipRGCs),我们的结果表明,在此光刺激下,内在光敏视网膜神经节细胞对瞳孔光反射有完全的贡献。
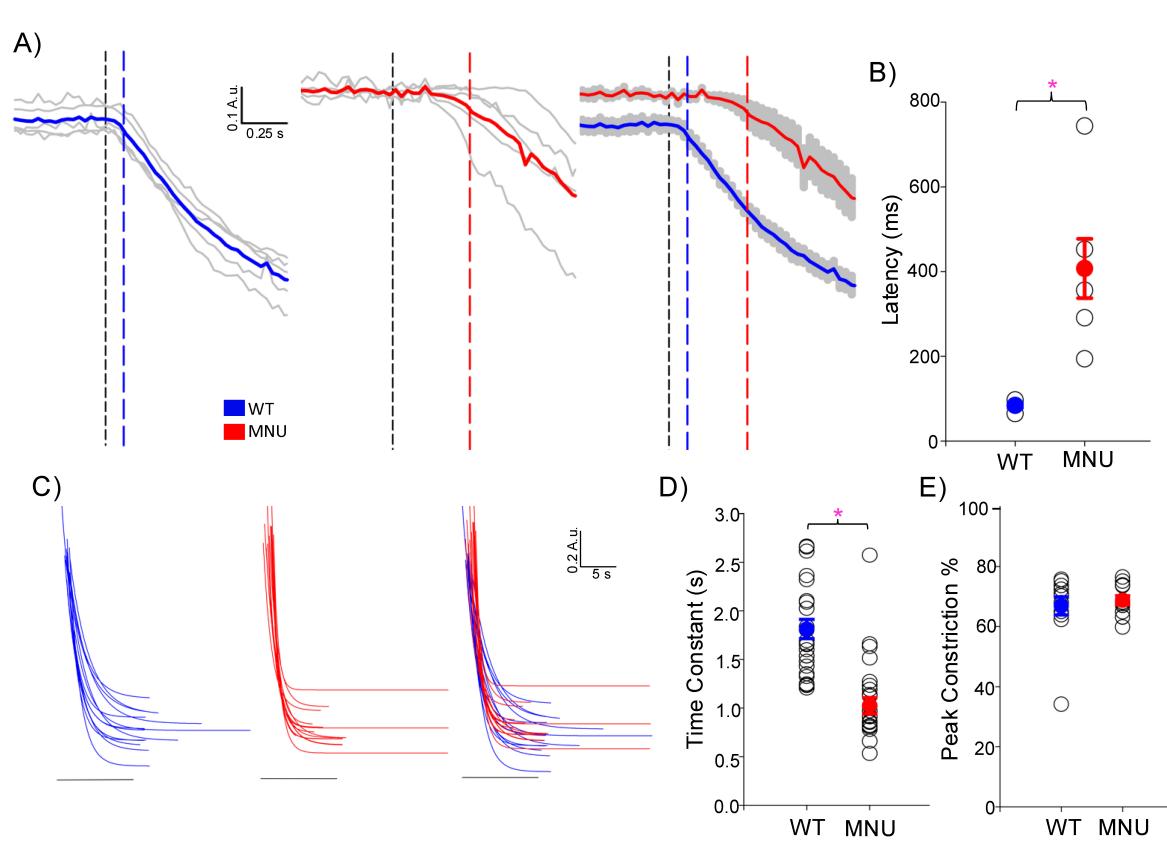
图2 强光诱发的瞳孔光反射(PLRs)初始阶段在野生型(WT)和N-亚硝基-N-甲基脲(MNU)处理的眼睛之间是相当的:(A)在短时间尺度上展示了WT(蓝色)和MNU处理眼睛(红色)的初始阶段。黑色虚线垂直线表示光刺激开始,蓝色或红色线表示瞳孔光反射的起始点。从光开始到瞳孔光反射开始的潜伏期,WT短于MNU处理的眼睛。(B)汇总图表显示了WT和MNU处理眼睛的潜伏期,MNU处理的眼睛表现出显著延迟(p < 0.05,Student非配对t检验)。WT和MNU的平均值及标准误分别以蓝色和红色呈现。(C)强光诱发的瞳孔光反射初始阶段用单组分指数衰减曲线对WT(蓝色)和MNU(红色)小鼠的眼睛进行拟合(R2> 0.90)。(D)显示各曲线拟合时间常数(tau)的图表。MNU表现出较低的tau,表明其瞳孔光反射比WT更快(p < 0.05,n = 12只小鼠)。(E)显示峰值收缩的图表表明,WT和MNU小鼠之间没有差异(p = 0.07,n = 12只小鼠)。*p < 0.05。
先前的研究报告使用突变小鼠模型来研究内在光敏视网膜神经节细胞(ipRGCs)在瞳孔光反射(PLR)中的作用,结果表明,在任何刺激光强度下,这些小鼠的瞳孔光反射都更慢且幅度更小(Gooley等人,2012年;Kostic等人,2016年;Beier等人,2022年)。我们的甲基亚硝基脲(MNU)实验结果与这些报告相矛盾(图1)。为了比较我们的MNU模型与突变小鼠模型的瞳孔光反射,我们在视杆-视锥光感受器功能异常的小鼠模型(Cnga3–/–和Gnat1–/–:双敲除小鼠)中测量了瞳孔光反射。暗适应后,它们的瞳孔完全扩张,这与野生型(WT)小鼠没有差异(单因素方差分析,p > 0.5)。
在双敲除(dKO)小鼠中,弱光刺激仅能微弱诱发瞳孔光反射(PLR),中等光刺激诱发的PLR幅度小且反应缓慢(图3B,弱光和中等光),这与我们的MNU小鼠类似。强光刺激能诱发更强的反应(图3B,强光);然而,其瞳孔收缩程度小于野生型(WT)小鼠的PLR,且PLR起始更慢(p < 0.0001,图3C,强光)。我们将结果与其同窝对照小鼠(Cnga3+/–和Gnat1+/–;dKO+/–,n = 3只小鼠)进行了比较。在弱光和中等光条件下,它们的PLR与野生型小鼠相似(图3C,绿色)。但强光刺激下,其PLR无法完全达到野生型小鼠的水平,这表明在dKO小鼠中观察到的幅度更小、反应更慢的PLR是由该小鼠品系本身导致的。尽管MNU小鼠和dKO小鼠都仅通过内在光敏视网膜神经节细胞(ipRGCs)对光产生反应,但MNU小鼠在强光刺激下的收缩速度快得多,与野生型小鼠相当。
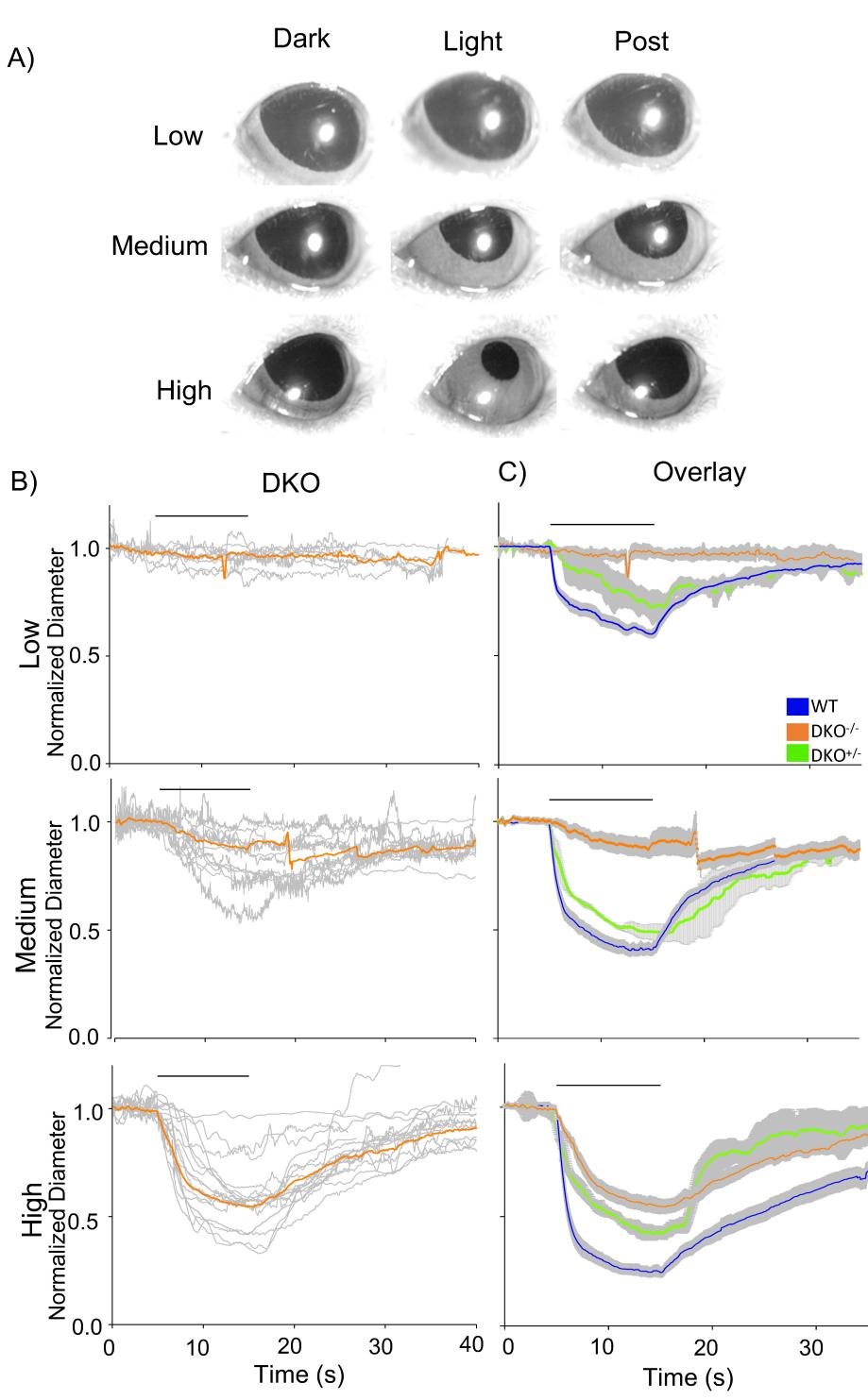
图3 双基因敲除(dKO)小鼠的瞳孔光反射(PLR)。(A)一组显示dKO小鼠瞳孔光反射的瞳孔图像。弱光未诱发瞳孔光反射,中至高强度光刺激可引起轻微的瞳孔收缩。(B)绘制了dKO小鼠(n=10)的标准化瞳孔直径随时间的变化。单个dKO小鼠眼睛的数据以灰色表示,所有眼睛的平均反应以橙色表示。(C)dKO小鼠眼睛(橙色)、dKO同窝对照小鼠(dKO+/–:绿色)和野生型(WT)小鼠(蓝色)的平均瞳孔光反射叠加了标准误(灰色)。
¶ MNU视网膜组织中的光感受器功能异常
先前的研究表明,MNU注射后光感受器仍然存在(Jain等人,2016年;Tao等人,2015年),这可能诱发了我们的MNU小鼠出现快速的内在光敏视网膜神经节细胞(ipRGC)反应。我们进行了组织分析,以检查MNU注射是否去除了光感受器。我们首先对比了垂直的视网膜切片(图4A)。MNU注射消除了视网膜外层,从外丛状层(OPL)到光感受器外节(图4A,生理盐水组6只小鼠,MNU组12只小鼠)。视网膜切片取自视网膜中央和周边区域;MNU注射后,整个视网膜的光感受器丢失情况是一致的。
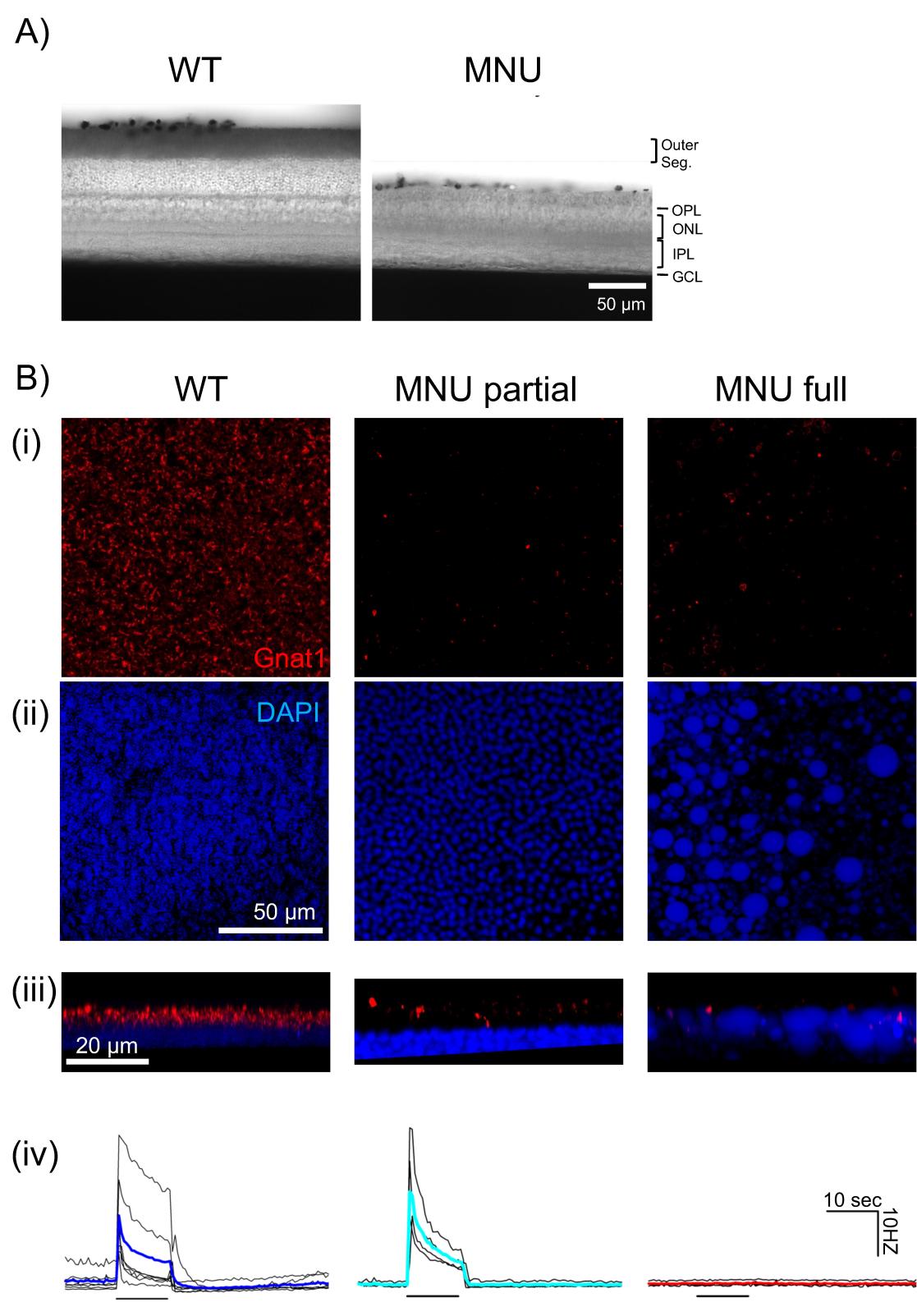
图4 N-亚硝基-N-甲基脲(MNU)可选择性消融视杆/视锥光感受器:(A)微分干涉相差图像显示野生型(WT)(左)和MNU处理眼(右)的视网膜垂直切片。注射MNU的视网膜显示光感受器层缺失,包括外节和外核层。视网膜内层保持完整。(B)整装组织中光感受器层的免疫组织化学图像(i-iii)。(左列)未接受MNU处理的WT小鼠显示大量Gnat1标记的视杆外节(红色)和DAPI标记的光感受器胞体(蓝色)。下方面板(iii)显示侧视图的数字渲染图像。最下方面板(iv)的单个轨迹(黑色)和平均值(蓝色)显示神经节细胞对弱光刺激的MEA记录。(中列)MNU部分处理的组织显示Gnat1斑点减少,而胞体几乎完整。MEA记录[单个轨迹(黑色)和平均值(青色)]显示弱光诱发的光反应(iv)。(右列)总体而言,MNU注射几乎完全消除了Gnat1标记的外节(i),这些外节位于DAPI标记的胞体层中(iii)。胞体肿胀并呈现鹅卵石样不规则结构(ii)。侧视图显示肿胀的胞体与混杂的Gnat1斑点。对于这些眼,MEA记录的单个轨迹(黑色)和平均值(红色)显示弱光未诱发神经节细胞峰电位(iv)。
然而,在大多数视杆细胞和视锥细胞已被清除的rd10小鼠中,退化的光感受器仍能对光做出反应(Ellis等人,2023年)。我们使用抗Gnat1抗体和DAPI染色对MNU处理的组织进行了检查[图4B(i-iii)]。在野生型(WT)组织中,Gnat1标记视杆细胞的外段,DAPI标记光感受器的胞体[图4B(i),“WT”]。光感受器层的侧面观显示,胞体和外段呈极性分布[图4B(iii),“WT”]。我们使用同一眼的视网膜组织进行了多电极阵列(MEA)检测,发现许多神经节细胞对弱光刺激有反应[图4B(iv),“WT”]。
注射MNU后,Gnat1染色显著减少(野生型:185,460±31,900个视杆细胞/平方毫米,n=3;部分MNU处理组:16,980±46,300个视杆细胞/平方毫米,n=7,p<0.05,非配对Student t检验)。然而,在某些情况下,弱光刺激仍能诱发与野生型组织相似的MEA光反应[图4B(iv),“MNU部分”]。在这些情况下,尽管Gnat1染色显著减少,但其胞体以及胞体-外段的极性得以保留[图4B(iii),“MNU部分”]。
然而,在大多数情况下,MNU注射消除了MEA记录中的弱光诱发反应[图4B第(iv)组,“MNU完全”]。与野生型(WT)和MNU部分组相比,Gnat1染色显著减少(1190±700个视杆细胞/mm²,n=4,与对照组相比p<0.05,非配对Student t检验)。此外,光感受器胞体肿胀,胞体外段的极性消失[图4B第(ii)组,“MNU完全”]。
基于这些观察结果,我们认为当弱光诱发反应消失时,MNU完全有效。如果在注射MNU后,MEA记录或瞳孔光反射(PLR)中仍能被弱光诱发光反应,我们则认为MNU部分有效,并将这些小鼠从我们的MNU组中排除。
我们还研究了MNU是否会影响神经节细胞层细胞(GCL)(图5A)。通过DAPI和opn4抗体的免疫组织化学方法对GCL结构进行了检查,这两种物质分别对GCL细胞核和内在光敏视网膜神经节细胞(ipRGCs)进行了染色。我们发现,野生型(WT)和MNU处理的组织中,GCL内的细胞数量相近(图5A、B,p = 0.29,野生型样本数n = 10,MNU处理样本数n = 11)。不同视网膜中ipRGCs的数量存在差异。尽管野生型、MNU处理和双敲除(dKO)视网膜组织中ipRGCs的平均数量相同,但dKO+/-小鼠的ipRGCs数量比dKO小鼠多(图5A、C,p = 0.022,单因素方差分析,野生型样本数n = 12,dKO+/-样本数n = 9,MNU处理样本数n = 13,dKO样本数n = 10)。这表明这些小鼠存在轻微的重塑现象。尽管如此,在不同实验条件下,GCL细胞的数量保持一致(图5B,p = 0.56,单因素方差分析)。这些结果表明,这些小鼠的GCL重塑程度极小,且MNU小鼠中强光诱导的瞳孔光反射(PLRs)的快速发作并非由ipRGCs的代偿性增加所致。
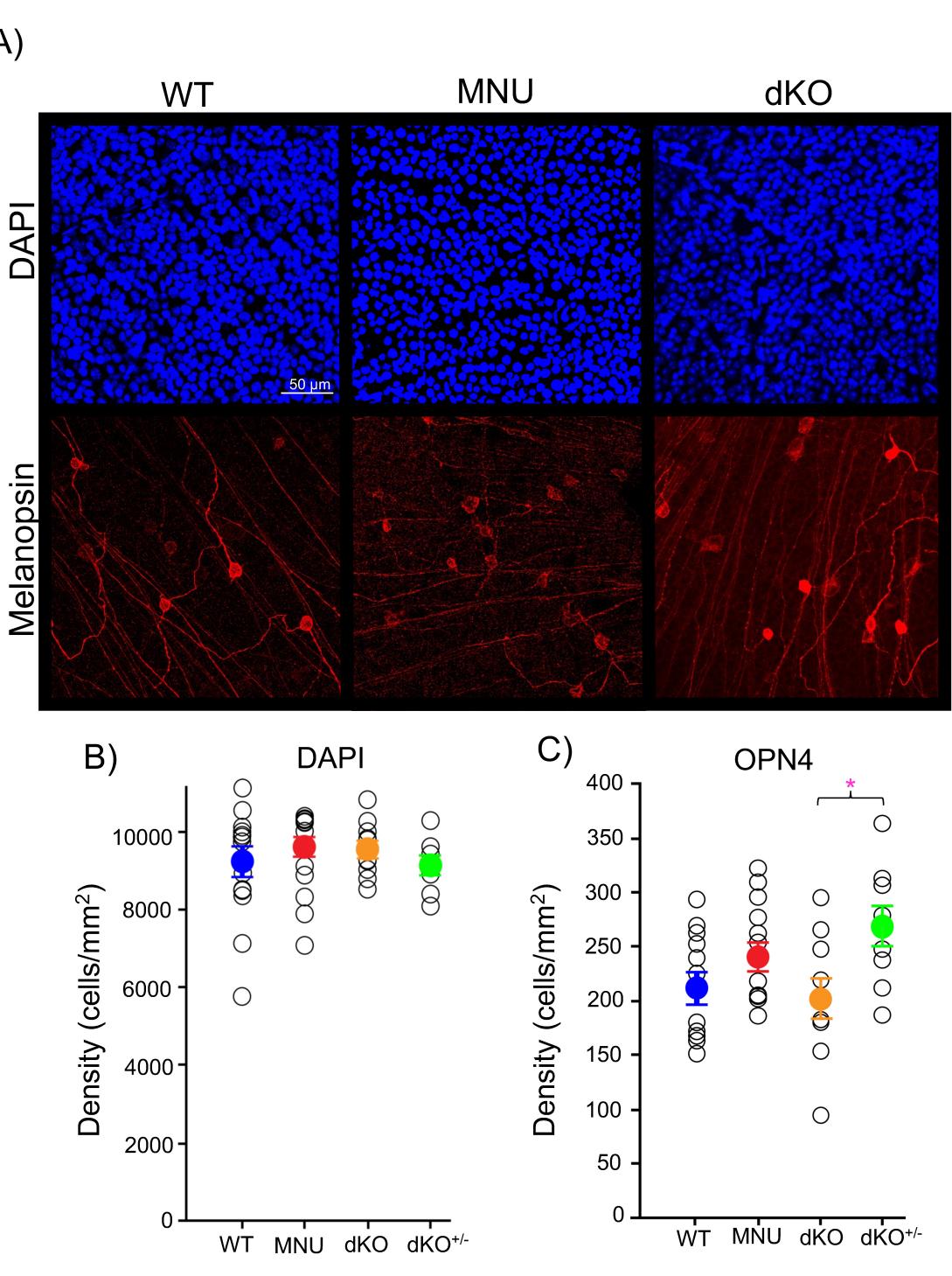
图5 N-亚硝基-N-甲基脲(MNU)和双敲除(dKO)小鼠的神经节细胞完好无损:(A)野生型(WT)、MNU和dKO视网膜组织中,经DAPI(蓝色)和OPN4内在光敏感性视网膜神经节细胞(ipRGCs,红色)免疫染色后的代表性神经节细胞层图像。(B)通过DAPI染色计数的神经节细胞层(GCL)细胞体数量在WT(蓝色)、MNU(红色)、dKO(橙色)和dKO+/-(绿色)视网膜之间保持相似(p = 0.385,n = 15只WT小鼠、n = 17只MNU小鼠、n = 9只dKO+/-小鼠和n = 10只dKO小鼠,采用单因素方差分析及Tukey法事后比较)。(C)WT、MNU和dKO+/-小鼠的ipRGCs数量也保持稳定;然而,与杂合同窝小鼠相比,dKO小鼠的ipRGCs数量有所减少(p = 0.022,n = 12只WT小鼠、n = 13只MNU小鼠、n = 9只dKO+/-小鼠和n = 10只dKO小鼠,采用单因素方差分析及Tukey事后比较)。*p < 0.05。
¶ 通过MEA记录ipRGC的光诱发反应
为了探究野生型(WT)、甲基亚硝基脲(MNU)处理和双敲除(dKO)小鼠瞳孔光反射(PLR)反应存在差异的生理机制,我们使用多电极阵列(MEA)记录了内在光敏视网膜神经节细胞(ipRGCs)的光诱发反应。我们采用强光刺激——与瞳孔光反射记录中使用的相同“强光”强度,来诱发内在光敏视网膜神经节细胞的放电率反应。每个组织中检测到数百至数千个单位,我们根据方法部分描述的标准分离出内在光敏视网膜神经节细胞单位。在野生型组织中,内在光敏视网膜神经节细胞单位的定义是在光开始时产生放电且具有持久反应(图6A,下图)。这些单位在光刺激后立即显示出光诱发反应,表明野生型小鼠存在光感受器输入(图6A,n = 4只野生型小鼠)。
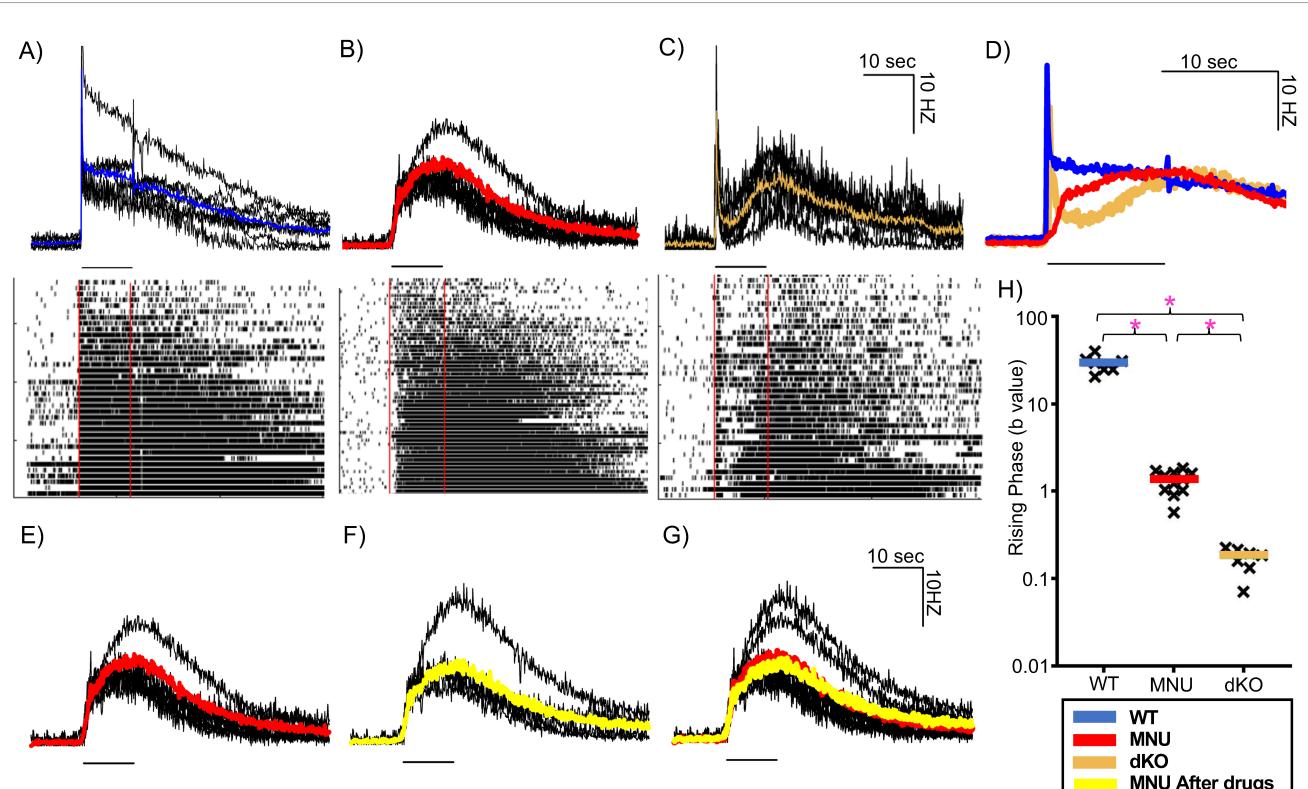
图6 三种小鼠在强光刺激下内在光敏视网膜神经节细胞(ipRGCs)的MEA记录。(A–C)黑色单独轨迹表示野生型(WT)(A)、N-亚硝基-N-甲基脲(MNU)(B)和双敲除(dKO)(C)小鼠中的ipRGC单元,彩色线条表示平均轨迹(WT:蓝色,n=7个组织;MNU:红色,n=11个组织;dKO:橙色,n=7个组织)。每条轨迹下方的黑线表示10秒光刺激的时间。下方面板显示的光栅图包含来自每个相应组织的代表性ipRGC群体的单个尖峰。(D)三种不同小鼠的ipRGC平均尖峰率轨迹叠加显示。三种颜色分别对应(A–C)中的三种小鼠品系。(E–G)MNU注射小鼠在强光强度下的平均尖峰率(红色)(E)以及在存在谷氨酸受体阻滞剂(L-AP4、D-AP5、ACET和CNQX)时的平均尖峰率(黄色)(F)。(G)这些轨迹的叠加图显示ipRGC尖峰无变化。(H)柱状图显示三种不同小鼠ipRGC尖峰率初始阶段的曲率(b)。黑色十字表示单个轨迹,彩色柱表示每种类型所有轨迹的平均值。*p < 0.05。
在注射MNU的视网膜组织中(n=11个组织,来自8只小鼠),弱光刺激未引发光反应[图4B第(iv)组]。相比之下,强光刺激引发了具有持久尖峰的光反应,这提示存在内在光敏视网膜神经节细胞(ipRGCs)。我们发现,一部分ipRGC单元在光照开始后立即做出反应。在每个MNU组织中均有发现(平均值:15.6%,范围为ipRGC单元的6.7–23.3%,图6B)。光照开始至达到峰值反应63%时的潜伏期为1.57±0.07秒(n=4个MNU组织),这与图2中瞳孔光反射(PLR)的时间相当(潜伏期+时间常数:1.5–2秒)。
我们记录了双敲除(dKO)小鼠组织的多电极阵列(MEA),以检查在强光下MNU组织中发现的快速反应性内在光敏视网膜神经节细胞(ipRGCs)群体是否存在(图6C,n = 4只dKO小鼠)。在光刺激下,会诱发初始的瞬态反应,该反应迅速消退,随后出现缓慢起始、持续时间较长的反应(图6C)。初始反应最有可能是由视杆光感受器中残留的Gnat2诱导的,而非由ipRGCs诱导(Allen等人,2010)。ipRGCs会诱导缓慢起始、持续时间较长的反应。我们没有发现任何快速起始的ipRGC单元,其动力学特征与MNU视网膜中的ipRGC单元相匹配(图6B、C)。图6D叠加了野生型(WT)、MNU和dKO组织的平均ipRGC反应,表明dKO的放电反应中ipRGC成分的起始明显慢于WT和MNU组织。为了分析这些组织中ipRGC反应的起始情况,我们利用曲线拟合特性获得了(b)值,该值代表上升阶段的曲率(详情请参见方法部分)。这些(b)值的图表(图6H)显示,WT组织的上升阶段比MNU和dKO组织更快(p < 0.0001,单因素方差分析),且MNU组织的上升阶段比dKO组织更快(p < 0.0001,单因素方差分析)。这些时间结果与我们的瞳孔光反射(PLR)结果一致(图1、3),表明某些ipRGCs对光的反应较快,从而塑造了MNU组织中PLR的初始成分,而这种成分在突变小鼠中是缺失的。
为了进一步排除光感受器输入参与MNU小鼠的快速反应,我们应用了一种谷氨酸受体阻滞剂混合物来抑制从光感受器到内在光敏视网膜神经节细胞(ipRGCs)的突触传递(n = 5个组织,来自4只小鼠)。我们记录了灌注谷氨酸受体阻滞剂前后的 spike 率(图6E、F)。叠加后,达到峰值10%的时间(之前:0.55 ± 0.03秒,之后:0.525 ± 0.09秒,n = 5,p = 0.9,非配对 Student t检验)和峰值 spike 率(之前:16 ± 1.6赫兹,之后:13.8 ± 2.3赫兹,n = 5,p = 0.4,非配对 Student t检验)均未检测到差异(图6G),这表明光感受器诱发的输入对该反应没有贡献。这一结果,连同低光刺激未引起反应的证据(图4B),证实了MNU小鼠的光感受器输入已被消除。
¶ 讨论
我们通过MNU注射在5-7天内消除光感受器,研究了视杆细胞、视锥细胞光感受器和黑视蛋白在瞳孔光反射(PLR)中的作用。尽管MNU小鼠在低强度和中等强度光刺激下的瞳孔光反射减弱,但高强度光刺激却出人意料地引发了快速且强烈的瞳孔光反射,与野生型(WT)小鼠眼睛的反应相当。在双敲除(dKO)突变小鼠中,我们未观察到强烈的瞳孔光反射。随后,我们使用视网膜离体标本,通过多电极阵列(MEA)检测内在光敏视网膜神经节细胞(ipRGCs)的电活动,结果显示MNU处理的组织中约15%的内在光敏视网膜神经节细胞具有快速起始的反应。我们的活体小鼠实验和离体多电极阵列结果表明,内在光敏视网膜神经节细胞的内在光反应能够在高强度光刺激下诱导瞳孔光反射,这与之前关于光感受器在高强度光诱导的瞳孔光反射中起关键作用的报道相矛盾。
¶ MNU注射与光感受器/内在感光视网膜神经节细胞
N-亚硝基-N-甲基脲(MNU)是一种DNA烷化剂,作为强效致癌物广泛存在于环境中(Smith等人,1988),并已被用于构建视网膜变性小鼠模型,该模型可清除光感受器而不影响视网膜内层神经元(Kiuchi等人,2002;Wang等人,2021)。DNA烷化缺陷以及随后的糖基化酶(AAG)和聚(ADP-核糖)聚合酶(PARP1)激活以启动凋亡通路的过程仅发生在光感受器中,而视网膜内层神经元不受影响(Calvo等人,2013;Meira等人,2009;Uehara等人,2006)。
与这些先前的报告一致,我们观察到在所有受试小鼠中,MNU注射后仅5-7天,视网膜光感受器层就被消除了(图4A)。尽管我们观察到光感受器外段从中央区域到周边区域都被消除了,但残留的光感受器可能仍对强光刺激有反应。Jain等人(2016年)使用s-视蛋白、m-视蛋白和视紫红质进行了免疫染色,并在MNU注射7天后观察到了残留的光感受器。Tao等人(2015年)观察到,MNU在7天内消除了视杆细胞,但视锥细胞的消除需要10天。此外,在rd10小鼠中,即使外段缩短,正在退化的光感受器仍继续对光产生反应(Ellis等人,2023年)。因此,我们检查了MNU处理组织中的残留光感受器。
MNU注射后5-7天,光感受器层和Gnat1染色的点状结构显著减少(图4)。在一些MNU处理的组织中,仍能观察到光感受器胞体,且在相同的眼睛中,弱光刺激仍能诱发光感受器介导的反应(图4B,“MNU部分损伤”)。然而,在大多数MNU处理的组织中,未观察到弱光诱发的反应(图4B,“MNU完全损伤”)。此外,强光刺激可诱发内在光敏视网膜神经节细胞(ipRGC)的反应,但在光刺激结束时从未诱发视锥细胞的信号传导(n=11个组织)。在这些相同的组织中,我们观察到外丛状层(OPL)附近有肿胀的胞体,且有少量Gnat1点状结构存在。这些结果表明,MNU注射后5-7天,这些视网膜中的视杆细胞和视锥细胞均已失去功能。我们将后者用作进行瞳孔光反射(PLR)和多电极阵列(MEA)记录的MNU小鼠,以确保MNU小鼠中快速且强烈的PLR和ipRGC反应并非源于光感受器的反应。
尽管MNU小鼠的光感受器被消除,dKO小鼠的光感受器功能失调,但神经节细胞是完整的(图5)。Jain等人(2016年)观察到MNU组织中的内在光敏视网膜神经节细胞(ipRGCs)数量增加。内在光敏视网膜神经节细胞的数量范围相对较大(图5C),在某些情况下,注射MNU后其数量可能会增加。然而,MNU处理的眼睛中内在光敏视网膜神经节细胞数量的增加不太可能在几天内与突触后靶标建立新的连接以增强瞳孔光反射(PLR)。综上所述,我们证实注射MNU能在5-7天内消除光感受器,且不会影响内在光敏视网膜神经节细胞。
¶ 视杆/视锥光感受器和内在光敏视网膜神经节细胞(ipRGCs)对瞳孔光反射(PLR)的作用
内在光敏视网膜神经节细胞(ipRGCs)是非成像视觉的关键神经元,它们也接收来自视杆/视锥光感受器的突触输入。这些光敏细胞在瞳孔光反射(PLR)中的作用主要是在光感受器退化的小鼠模型中进行研究的。由于视杆光感受器比视锥和ipRGCs对光更敏感(Field和Rieke,2002;Pang等人,2004;Qiu等人,2005Berson等人,2002),因此视杆细胞对弱光诱发的瞳孔光反射至关重要。一种光感受器退化模型——rd/rd cl小鼠——仅在高辐照度下表现出瞳孔光反射,而在中低辐照度下则没有(Lucas等人,2001;Lucas等人,2003)。在这些小鼠中,瞳孔光反射是由强度相当于ipRGCs工作范围的光刺激诱发的(Lucas等人,2001)。在我们的实验中,MNU小鼠和双敲除(dKO)小鼠的瞳孔光反射与rd/rd小鼠一致,即在辐照度达到10⁴光子/μm²/s(或10¹²光子/cm²/s)时均未表现出瞳孔光反射,这也是我们的弱光刺激强度(图1–3)。
内在光敏视网膜神经节细胞(ipRGCs)对光刺激的敏感性较低,反应迟缓且持续时间长(Berson 等人,2002;Dacey 等人,2005)。由于这种缓慢的特性,人们对这些感光细胞的不同时间作用进行了研究。Lucas 等人(2001)比较了野生型小鼠和 rd/rd cl 小鼠在强光诱发下的瞳孔光反射(PLR),发现与野生型相比,rd/rd cl 小鼠的瞳孔光反射起始明显延迟。Kostic 等人(2016)使用视杆细胞/视锥细胞功能障碍的小鼠(Cnga3–/–;Rho–/– 或 Gnat1–/–),发现了一种微弱且缓慢的瞳孔光反射。同样,Beier 等人(2022)使用 mGluR6 敲除、Elfn1 敲除和视锥细胞 Cx36 敲除的小鼠(这些小鼠的光感受器与三级神经元的传递被阻断),得出结论:内在光敏视网膜神经节细胞塑造了瞳孔光反射的持续阶段。一项针对盲人的研究也显示了类似的结果,这些盲人的光感受器功能异常,但昼夜节律正常(Gooley 等人,2012)。另一方面,opn4–/– 小鼠表现出持续时间较短的瞳孔光反射(Zhu 等人,2007)。所有这些结果表明,即使在强光刺激下,光感受器对于瞳孔光反射的启动也至关重要,而黑视蛋白则在光照期间负责维持反应。我们的双敲除小鼠(Cnga3–/–;Gnat1–/–)也显示出一致的结果(图 3)。
然而,我们的MNU小鼠并未显示出相同的结果。尽管MNU小鼠的瞳孔光反射(PLR)起始时间延迟(图2A、B),这可能是由于光感受器被清除所致,但MNU小鼠眼睛的收缩速度比野生型(WT)小鼠更快(图2C、D),且两种情况下达到峰值收缩的时间相近(图1)。根据图2中的测量结果,两种情况下PLR达到63%峰值的总时间约为1.5–2.0秒(潜伏期+时间常数)。我们的多电极阵列(MEA)记录结果支持了PLR的研究结果。在MNU小鼠中,我们发现约15%的内在光敏视网膜神经节细胞(ipRGCs)产生具有快速起始的峰电位:MNU组织达到63%峰值的时间平均为1.5秒。这种快速的ipRGC光反应不太可能归因于重塑,因为在野生型(WT)、MNU和双敲除(dKO)小鼠中,DAPI染色的神经节细胞层细胞数量以及表达视蛋白4(OPN4)的神经节细胞数量是相同的(图5)。
我们的研究与先前研究的主要区别在于小鼠模型的使用。先前的研究大多采用突变小鼠模型,包括光感受器退化模型(rd/rd)、光感受器功能障碍模型(Cnga3-KO、Gnat1-KO)以及视网膜网络突变模型(mGluR6-KO)。例如,尽管双敲除(dKO)组织因残留的视杆细胞活动而出现初始的放电增加,但这种增加是短暂的,并未加快内在光敏感视网膜神经节细胞(ipRGCs)的整体反应。相比之下,我们通过注射甲基亚硝基脲(MNU)在数天内清除光感受器,从而降低了视网膜重塑和代偿效应的风险。通过这种方式,我们发现,在没有光感受器的情况下,内在光敏感视网膜神经节细胞(ipRGCs)的反应速度足以形成强光诱发的瞳孔光反射(PLR)。我们关于内在光敏感视网膜神经节细胞(ipRGCs)对瞳孔光反射(PLR)贡献的新发现,可能对临床眼科疾病的诊断具有重要意义。此外,我们认为这一发现将有助于更全面地理解从光转导到行为结果的视网膜环路机制。
¶ 研究的局限性
Jain等人(2016年)使用MNU来研究细胞对瞳孔光反射(PLR)的作用。尽管我们采用了类似的实验步骤,但我们的结果和结论与他们的并不一致。在他们注射了MNU的小鼠中,与野生型(WT)小鼠相比,对强光刺激的瞳孔收缩仅达到一半程度,尽管他们观察到在注射MNU 7天后内在光敏感视网膜神经节细胞(ipRGCs)的数量有所增加。虽然他们实验中使用的MNU浓度、小鼠品系和刺激光强度与我们的相似,但其他条件存在差异,例如麻醉情况(我们:未使用麻醉;Jain等人:轻度麻醉)以及PLR刺激前的暗适应时间[我们:>30分钟,Jain等人(2016年):60–100秒],这些可能是导致结果不同的原因。
我们进行了体内瞳孔光反射(PLR)测量和体外内在光敏视网膜神经节细胞(ipRGC)记录,以研究ipRGC的光反应是否能解释MNU小鼠的瞳孔光反射。我们在这些测量中统一了光刺激强度和温度等条件。然而,体内和体外实验的这些条件无法完全相同。在体内实验中,小鼠眼睛视网膜处的光强度可能比体外研究中MEA培养室的光强度弱,这是由于角膜和晶状体的光衍射所致。小鼠的体温(38°C)高于MEA记录室的温度(33–34°C),这可能是这些研究中快速反应的ipRGC比例较低的原因。尽管某些条件存在差异,但我们发现,在MNU组织中,两种记录都显示出相似的结果,这表明ipRGC的直接光反应可以解释MNU小鼠中强烈的瞳孔光反射(PRL)。
¶ 声明
¶ 数据可用性声明
本研究中提出的原创成果已包含在本文及补充材料中,更多疑问可向通讯作者咨询。
¶ 伦理声明
该动物研究已获得韦恩州立大学机构动物护理和使用委员会的批准。这项研究是按照当地法规和机构要求进行的。
¶ 作者贡献
JB:数据整理、形式分析、资金获取、调查、方法学、验证、软件、写作——审阅与编辑、可视化。AH:概念化、数据整理、形式分析、调查、方法学、写作——审阅与编辑、软件、验证、可视化。ZS:概念化、数据整理、调查、方法学、写作——审阅与编辑。MK:数据整理、形式分析、调查、方法学、软件、验证、写作——审阅与编辑。AS:数据整理、形式分析、调查、软件、写作——审阅与编辑。DB:数据整理、形式分析、验证、可视化、写作——审阅与编辑。TI:概念化、形式分析、资金获取、调查、方法学、软件、监督、验证、可视化、写作——原始稿件、写作——审阅与编辑。
¶ 资助
作者声明本研究、论文撰写和/或发表获得了资金支持。本研究得到了美国国立卫生研究院EY028915(TI)、美国国立卫生研究院EY032917(TI)、美国国立卫生研究院EY004068(视觉核心)、朗布尔奖学金(JB)以及RPB grant的支持。
¶ 致谢
我们要感谢张道琪博士在使用黑视蛋白抗体进行免疫组织化学方面提供的建议,感谢Benjamin Sivyer博士慷慨提供多电极阵列分析的Python和MATLAB代码并给予指导,还要感谢Bashir Khatib-Shahidi先生和Goichi Suganuma先生提供的技术支持。
¶ 利益冲突
作者声明,本研究是在不存在任何可能被视为潜在利益冲突的商业或财务关系的情况下进行的。
¶ 生成式人工智能声明
作者声明,本手稿的创作未使用生成式人工智能。
¶ 出版商说明
本文中表达的所有观点均仅为作者个人观点,不一定代表其所属机构、出版商、编辑和审稿人的观点。本文中可能对任何产品的评价,或其制造商可能提出的任何声明,出版商均不提供保证或背书。
¶ 参考文献
- Allen A. E., Cameron M. A., Brown T. M., Vugler A. A., Lucas R. J. (2010). 缺失所有已知视网膜光转导级联关键组分的小鼠的视觉应答. 《公共科学图书馆·综合》, 5: e15063. DOI: 10.1371/journal.pone.0015063
- Aranda M. L., Schmidt T. M. (2021). 内在光敏性视网膜神经节细胞的多样性:环路与功能. 《细胞与分子生命科学》, 78: 889-907.
- Beier C., Bocchero U., Levy L., Zhang Z., Jin N., Massey S. C., 等. (2022). 不同的视网膜外环路驱动成像与非成像视觉行为. 《细胞报告》, 39: 111003.
- Berry M. H., Leffler J., Allen C. N., Sivyer B. (2023). 啮齿类黑视蛋白神经节细胞功能亚型在昼夜光照下的角色转换. bioRxiv [预印本]. DOI: 10.1101/2023.08.26.554902
- Berson D. M., Dunn F. A., Takao M. (2002). 调控生物钟的视网膜神经节细胞的光转导作用. 《科学》, 295: 1070-1073.
- Calvo J. A., Moroski-Erkul C. A., Lake A., Eichinger L. W., Shah D., Jhun I., 等. (2013). Aag DNA糖基化酶可促进Parp1介导的烷基化诱导组织损伤. 《公共科学图书馆·遗传学》, 9: e1003413. DOI: 10.1371/journal.pgen.1003413
- Dacey D. M., Liao H. W., Peterson B. B., Robinson F. R., Smith V. C., Pokorny J., 等. (2005). 灵长类视网膜中表达黑视蛋白的神经节细胞可编码颜色与辐照度信号并投射至外侧膝状体核. 《自然》, 433: 749-754.
- Ellis E. M., Paniagua A. E., Scalabrino M. L., Thapa M., Rathinavelu J., Jiao Y., 等. (2023). 视锥细胞及视锥通路在晚期视网膜变性中仍保持功能. 《当代生物学》, 33: 1513-1522.e4.
- Farshi P., Fyk-Kolodziej B., Krolewski D. M., Walker P. D., Ichinose T. (2016). 小鼠视网膜中多巴胺D1受体的表达具有双极细胞类型特异性. 《比较神经学杂志》, 524: 2059-2079.
- Field G. D., Rieke F. (2002). 小鼠视杆细胞到双极细胞的非线性信号传递及其对视觉敏感度的意义. 《神经元》, 34: 773-785.
- Gooley J. J., Ho Mien I., St Hilaire M. A., Yeo S. C., Chua E. C., Van Reen E., 等. (2012). 人类持续光照下,黑视蛋白与视杆-视锥光感受器在介导瞳孔对光反应中发挥不同作用. 《神经科学杂志》, 32: 14242-14253.
- Guler A. D., Ecker J. L., Lall G. S., Haq S., Altimus C. M., Liao H. W., 等. (2008). 黑视蛋白细胞是视杆-视锥信号输入非成像视觉的主要通路. 《自然》, 453: 102-105.
- Hattar S., Lucas R. J., Mrosovsky N., Thompson S., Douglas R. H., Hankins M. W., 等. (2003). 黑视蛋白与视杆-视锥感光系统介导了小鼠所有主要的附属视觉功能. 《自然》, 424: 76-81.
- Hilgen G., Sorbaro M., Pirmoradian S., Muthmann J. O., Kepiro I. E., Ulloa S., 等. (2017). 适用于大规模高密度多电极阵列的无监督锋电位分类方法. 《细胞报告》, 18: 2521-2532.
- Ichinose T., Hellmer C. B. (2016). 小鼠视网膜OFF型双极细胞亚型的差异化信号传递与谷氨酸受体组成. 《生理学杂志》, 594: 883-894.
- Ichinose T., Fyk-Kolodziej B., Cohn J. (2014). 小鼠视网膜ON型视锥双极细胞亚型在时间编码中的作用. 《神经科学杂志》, 34: 8761-8771.
- Jain V., Srivastava I., Palchaudhuri S., Goel M., Sinha-Mahapatra S. K., Dhingra N. K. (2016). 经典光感受器是小鼠瞳孔对光反射的主要介导者. 《公共科学图书馆·综合》, 11: e0157226. DOI: 10.1371/journal.pone.0157226
- Kiuchi K., Yoshizawa K., Shikata N., Matsumura M., Tsubura A. (2002). 烟酰胺可抑制N-甲基-N-亚硝基脲诱导的SD大鼠与C57BL小鼠光感受器细胞凋亡. 《实验眼研究》, 74: 383-392.
- Kostic C., Crippa S. V., Martin C., Kardon R. H., Biel M., Arsenijevic Y., 等. (2016). 视杆与视锥细胞对瞳孔对光反射早、晚动态过程的影响作用分析. 《眼科研究与视力学》, 57: 2501-2508.
- La Morgia C., Carelli V., Carbonelli M. (2018). 黑视蛋白视网膜神经节细胞与瞳孔:对神经眼科学的临床意义. 《神经科学前沿》, 9: 1047. DOI: 10.3389/fneur.2018.01047
- Lucas R. J., Douglas R. H., Foster R. G. (2001). 小鼠体内一种可介导瞳孔收缩的眼部光色素的特性研究. 《自然·神经科学》, 4: 621-626.
- Lucas R. J., Hattar S., Takao M., Berson D. M., Foster R. G., Yau K. W. (2003). 黑视蛋白敲除小鼠在高辐照度下瞳孔对光反射减弱. 《科学》, 299: 245-247.
- Meira L. B., Moroski-Erkul C. A., Green S. L., Calvo J. A., Bronson R. T., Shah D., 等. (2009). Aag启动的碱基切除修复可驱动烷基化诱导的小鼠视网膜变性. 《美国国家科学院院刊》, 106: 888-893.
- Mure L. S., Vinberg F., Hanneken A., Panda S. (2019). 人类内在光敏性视网膜神经节细胞的功能多样性. 《科学》, 366: 1251-1255.
- Pang J. J., Gao F., Wu S. M. (2004). 暗适应小鼠视网膜中视杆双极细胞、视锥去极化双极细胞与AII无长突细胞的光诱发电流反应. 《生理学杂志》, 558: 897-912.
- Pinheiro H. M., Da Costa R. M. (2021). 计算视角下瞳孔对光反射作为诊断辅助工具的系统文献综述. 《生物医学信息学杂志》, 117: 103757.
- Prigge C. L., Yeh P. T., Liou N. F., Lee C. C., You S. F., Liu L. L., 等. (2016). M1型内在光敏性视网膜神经节细胞通过视网膜内逆行信号调控视觉功能. 《神经科学杂志》, 36: 7184-7197.
- Qiu X., Kumbalasiri T., Carlson S. M., Wong K. Y., Krishna V., Provencio I., 等. (2005). 异源表达黑视蛋白可诱导细胞产生光敏性. 《自然》, 433: 745-749.
- Smith S. B., Yielding K. L. (1986). 甲基亚硝基脲经胎盘诱导的小鼠视网膜变性模型. 《实验眼研究》, 43: 791-801.
- Smith S. B., Hashimi W., Yielding K. L. (1988). N-甲基-N-亚硝基脲经胎盘诱导的小鼠视网膜变性:持续光照与全黑暗环境的影响. 《实验眼研究》, 47: 347-359.
- Tao Y., Chen T., Fang W., Peng G., Wang L., Qin L., 等. (2015). N-甲基-N-亚硝基脲诱导的小鼠视网膜光感受器变性的时间拓扑特征. 《科学报告》, 5: 18612.
- Uehara N., Miki K., Tsukamoto R., Matsuoka Y., Tsubura A. (2006). 烟酰胺通过抑制聚ADP核糖聚合酶活性与JNK/AP-1信号通路,阻断N-甲基-N-亚硝基脲诱导的大鼠光感受器细胞凋亡. 《实验眼研究》, 82: 488-495.
- Wang F., Li E., De L., Wu Q., Zhang Y. (2021). OFF-瞬态型α视网膜神经节细胞介导逼近刺激触发的先天防御反应. 《当代生物学》, 31: 2263-2273.e3.
- Zhu Y., Tu D. C., Denner D., Shane T., Fitzgerald C. M., Van Gelder R. N. (2007). 小鼠瞳孔对光反应中依赖黑视蛋白的持续性与光增强效应. 《眼科研究与视力学》, 48: 1268-1275.