¶ 《自然·通讯》
¶ 一种膜靶向光开关可恢复退化视网膜对光的生理性ON/OFF反应
¶ 原文下载:s41467-025-55882-2_origin.pdf
Published online: 11 January 2025 在线发表:2025年1月11日
Gaia Ziraldo1、Sara Cupini 1,2、Valentina Sesti3,4、Emanuela Delfino 1,2、Guglielmo Lanzani 4、Chiara Bertarelli3,4、Fabio Benfenati 1,5,6,7和Stefano Di Marco 1,5,6,7
1 意大利热那亚意大利理工学院突触神经科学中心。
2 意大利热那亚大学实验医学系,热那亚,意大利。
3 米兰理工大学“朱利奥·纳塔”化学、材料与化学工程系,米兰,意大利。
4 意大利米兰意大利理工学院纳米科学与技术中心。
5 意大利热那亚IRCCS圣马蒂诺综合医院。
6 以下作者贡献相同:法比奥·本费纳蒂、斯特凡诺·迪·马尔科。
7 以下作者共同指导了这项工作:法比奥·本费纳蒂、斯特凡诺·迪·马尔科。电子邮箱:fabio.benfenati@iit.it;stafano.dimarco@iit.it
¶ 引言
色素性视网膜炎和黄斑变性缺乏有效的视觉恢复疗法,这促使了光遗传学和视网膜假体等新策略的发展。然而,由于视网膜神经元受到大量光诱发激活,且不考虑视觉信息在ON通道和OFF通道中的分离(这对对比度敏感度和空间分辨率至关重要),视觉恢复效果不佳。在此,我们发现Ziapin2(一种以光依赖方式调节神经元电容和兴奋性的膜光开关)能够在小鼠和大鼠的光感受器退化遗传模型中,恢复视网膜神经节细胞对全视野刺激产生的快速和缓慢的ON、OFF及ON-OFF反应,并重新激活其兴奋性和抑制性电导。向完全失明的rd10小鼠玻璃体内注射Ziapin2可恢复其光驱动行为和视觉运动反射。研究结果表明,Ziapin2是在视网膜退化晚期恢复生理性视觉反应的一种极具潜力的分子。
视觉依赖于从环境中提取和识别形状。视网膜处理视觉信息的能力远超当今最先进的相机。这种出色的表现源于视网膜网络能够将视觉信息分离到不同的平行通道中,分别在ON通路和OFF通路中同时处理正对比度或负对比度,从而能够分离和提取视觉特征,如空间组织或运动。因此,在啮齿动物的视网膜中,可以识别出30多种功能类型的视网膜神经节细胞(RGCs),它们对明暗有着不同的反应1–3。视觉信息的分离和对比度编码最初是在光感受器带状突触处产生的,这得益于水平细胞产生的抑制性环绕,以及三种主要双极细胞(BCs)中正负对比度的物理分离——视杆和视锥ON型双极细胞表达超极化的代谢型谷氨酸受体6(mGluR6),而视锥OFF型双极细胞则表达去极化的AMPA/红藻氨酸谷氨酸受体。周边视网膜的视杆双极细胞以相反的方式调节视锥ON和OFF通路,从而有助于对比度敏感性:它们通过缝隙连接直接兴奋视锥ON型双极细胞,并通过AII无长突细胞的甘氨酸能突触抑制视锥OFF型双极细胞。从这一点开始,视觉信息在这两个平行的信息流中保持分离状态,直到到达更高层级的整合中心4–8。
视网膜光感受器的进行性退化是导致严重视力障碍的最常见原因之一。视网膜色素变性(RP)是一组导致视杆细胞死亡,并继而导致视锥细胞死亡的遗传性疾病的统称,全球每3500至4000人中就有1人受其影响,是最常见的遗传性视网膜退化疾病9,10。另一方面,年龄相关性黄斑变性(AMD)累及黄斑中心凹负责敏锐中心视力的视锥细胞4,影响着全球约8%的普通人群以及约25%的70岁以上人群11。尽管AMD和RP较为常见,但治疗方法尚未取得成功,目前尚无获批的药物治疗方案12,13。
除了旨在对抗或减缓光感受器死亡的基因和细胞疗法14-23外,其他策略还指向由光依赖性重新激活未受变性影响的视网膜内层网络。光遗传学已在临床前模型中广泛测试,最近在一项正在进行的临床试验中,有1名视网膜色素变性患者的相关情况被报道24,25。尽管光遗传学适用于任何视网膜色素变性突变及疾病的任何阶段,但异源视蛋白固有的低光敏感性需要增强光线,且由此产生的视力相对有限。有研究提出,视网膜假体可产生光诱导的电信号,激活视网膜内层,并在营养不良的视网膜中恢复一定程度的光敏感性26-35。在眼内,假体芯片可植入视网膜前或视网膜下位置。视网膜前装置更靠近视网膜神经节细胞,其优势在于能刺激视网膜的最终共同通路。同时,视网膜下植入物可充分利用视网膜内层的计算处理功能。然而,不考虑平面装置的固有局限性(视野小,空间分辨率比黄斑视锥细胞低1-2个数量级),包括基于光伏纳米颗粒的装置36-38在内的所有假体方法,都会诱导视网膜内层产生光诱发的非选择性激活,将所有视觉信息压缩到ON通路中,无法产生负对比度信息和高空间分辨率。
新一代基于偶氮苯的光开关最近被证实能够光敏感化内源性蛋白质,且无需基因工程[39,40]。最新的光开关对可见光敏感,通过在细胞内作用于通道位点,触发视网膜神经节细胞(RGCs)的电压门控或配体门控离子通道的光可逆性阻断[41-48]。然而,这些化合物也无法产生负对比度信息,它们仅能在光照时调节视网膜网络,引发ON通路的大规模激活。
我们最近设计并从生物学角度表征了一种新型两亲性偶氮苯基光开关,命名为Ziapin2,它作用于膜的被动特性,不会直接干扰离子通道或神经递质受体。Ziapin2由一个偶氮苯核心组成,其一侧有两个吡啶𬭩封端的分支,另一侧有一个疏水性氮杂环庚烷环。Ziapin2通过使其极性末端与磷脂头部基团对齐,其疏水核心与膜的疏水脂质链对齐,自发地分配到两个膜小叶中48。在黑暗中,相反的Ziapin2分子的两个氮杂环庚烷发生反式相互作用,减少膜厚度,从而增加电容并降低神经元的兴奋性。由毫秒级青色光脉冲(450-500 nm;峰值在470 nm;图1a,左)触发的反式到顺式异构化,通过从膜核心移除疏水端基导致膜松弛,从而使电容急剧下降。这会导致神经元膜快速超极化,随后出现反弹去极化。由于阳极断裂机制,这些变化增加了内在兴奋性,并触发动作电位(AP)发放49-51。神经元兴奋性的双向明暗调节使这种分子成为一种很有前景的工具,可用于在视网膜的ON/OFF通路中区分放电区域与抑制性周围区域。
在此,我们测试了Ziapin2在体外和体内恢复退化视网膜生理光反应的能力,所用视网膜来自rd10小鼠和皇家外科医学院(RCS)大鼠。rd10小鼠的Pde6b基因存在隐性R560C突变,而该基因对视杆细胞的正常功能至关重要;RCS大鼠的Mertk基因存在隐性突变,这会损害视网膜色素上皮(RPE)吞噬脱落的视杆和视锥细胞外段的能力。由于Ziapin2对内在兴奋性具有双重作用,它通过作用于双极细胞(BC)水平,恢复了视网膜神经节细胞(RGCs)中多种光诱发的ON/OFF反应,并伴随其兴奋性和抑制性电导的重新激活。此外,对失明的6月龄rd10小鼠进行单次玻璃体内注射Ziapin2后,通过重新激活不同的ON和OFF视网膜神经节细胞群,恢复了其光驱动行为和视觉运动反应。结果表明,Ziapin2是一种很有前景的分子,可通过生理性重新激活视网膜内层处理过程,在视网膜变性晚期恢复视觉反应。
¶ 结果
¶ Ziapin2调节视力正常动物中单个视网膜神经节细胞的光诱发活动
Ziapin2对神经元兴奋性的双向调节促使我们测试其在视网膜中的作用。我们首先对从有视力的野生型(WT)C56BL6/J小鼠分离出的全视网膜外植体中单个视网膜神经节细胞(RGC)的光诱发活动进行膜片钳记录(图1a)。我们记录了在功率密度为2至20 mW/mm²的条件下,全视野500毫秒的青色光(图1b)或绿色光(图S1)刺激下的基础反应。然后,我们用第二个玻璃吸管靠近被膜片钳记录的视网膜神经节细胞,进行局部给药(2分钟吹入),药物为溶媒(Ames培养基中含10%二甲基亚砜)或Ziapin2(200 µM)。与基础状态相比,Ziapin2融入视网膜神经节细胞膜后,在青色光刺激下会促进动作电位(AP)的发放,而溶媒吹入的视网膜神经节细胞在光刺激下则无此效应(图1b)。如各自的 raster 图所示(图1b),Ziapin2对青色光诱发的放电活动的调节与刺激时间同步,且在15次刺激方案中保持一致。有趣的是,当用处于Ziapin2吸收光谱之外的绿色光刺激同一视网膜神经节细胞时,未检测到放电模式的变化(图S1a、b)。
刺激时间直方图(PSTH)分析和放电率计算证实,应用Ziapin2后,蓝光刺激能可靠地诱导视网膜神经节细胞(RGC)放电率增加,而在溶媒处理的视网膜神经节细胞(图1c、d)或经Ziapin2处理并接受绿光刺激的视网膜神经节细胞中则无此现象(图S1c、d)。对光诱发的动作电位(AP)计数和放电率变化的计算表明,在所有测试的光功率密度(2、10和20 mW/mm²)下,与溶媒处理(图1e、f)或绿光刺激(图S1e、f)相比,蓝光刺激经Ziapin2处理的视网膜神经节细胞的效果均极为显著。
¶ 视网膜神经节细胞(RGC)动作电位动态的变化反映了Ziapin2的光依赖性电容效应
为了确认视网膜神经元中Ziapin2的光激发机制,我们利用相平面图分析,研究了在黑暗中或经蓝光刺激后,用溶媒或Ziapin2处理的视网膜神经节细胞(RGCs)中产生的动作电位(AP)的动态变化(图2a和图S2)。与黑暗中Ziapin2引起的电容增加一致,首次光诱发的动作电位相对于基础状态表现出较慢的动态变化,其最大去极化斜率、最大复极化斜率和动作电位振幅均显著降低(图2a、b)。蓝光刺激通过阶段性地降低电容,引起了动作电位动态变化的相反加速,使最大去极化斜率、最大复极化斜率和动作电位振幅显著增加(图2a、b)。在经溶媒处理并接受相同光刺激方案的视网膜神经节细胞中,未观察到动作电位动态变化。同样,在经Ziapin2处理但接受绿光刺激的视网膜神经节细胞中,也未观察到光诱发的动作电位动态变化(图S3)。
然后,我们使用低通滤波器对记录进行滤波,以提取光刺激开始后1.5秒时间窗口内缓慢的阈下膜电位振荡(图2c)。我们观察到,在所有测试的功率密度下,光反应期间的峰值膜去极化显著增加,而超极化后峰值未受影响(图2d)。Ziapin2将去极化的开始和恢复至基础Vm水平的时间精确地聚焦在光刺激的开启/关闭时刻,而处于基础状态或经溶媒处理的视网膜神经节细胞(RGCs)在Vm变化中表现出大得多的时间变异性。为了定量评估这种效应,我们为每个记录的视网膜神经节细胞计算了15次扫描中最大Vm变化所在区间的标准差。结果表明,视网膜神经节细胞膜中Ziapin2的存在确实能显著同步阈下光诱发的膜电位振荡,降低反应变异性(图2e)。
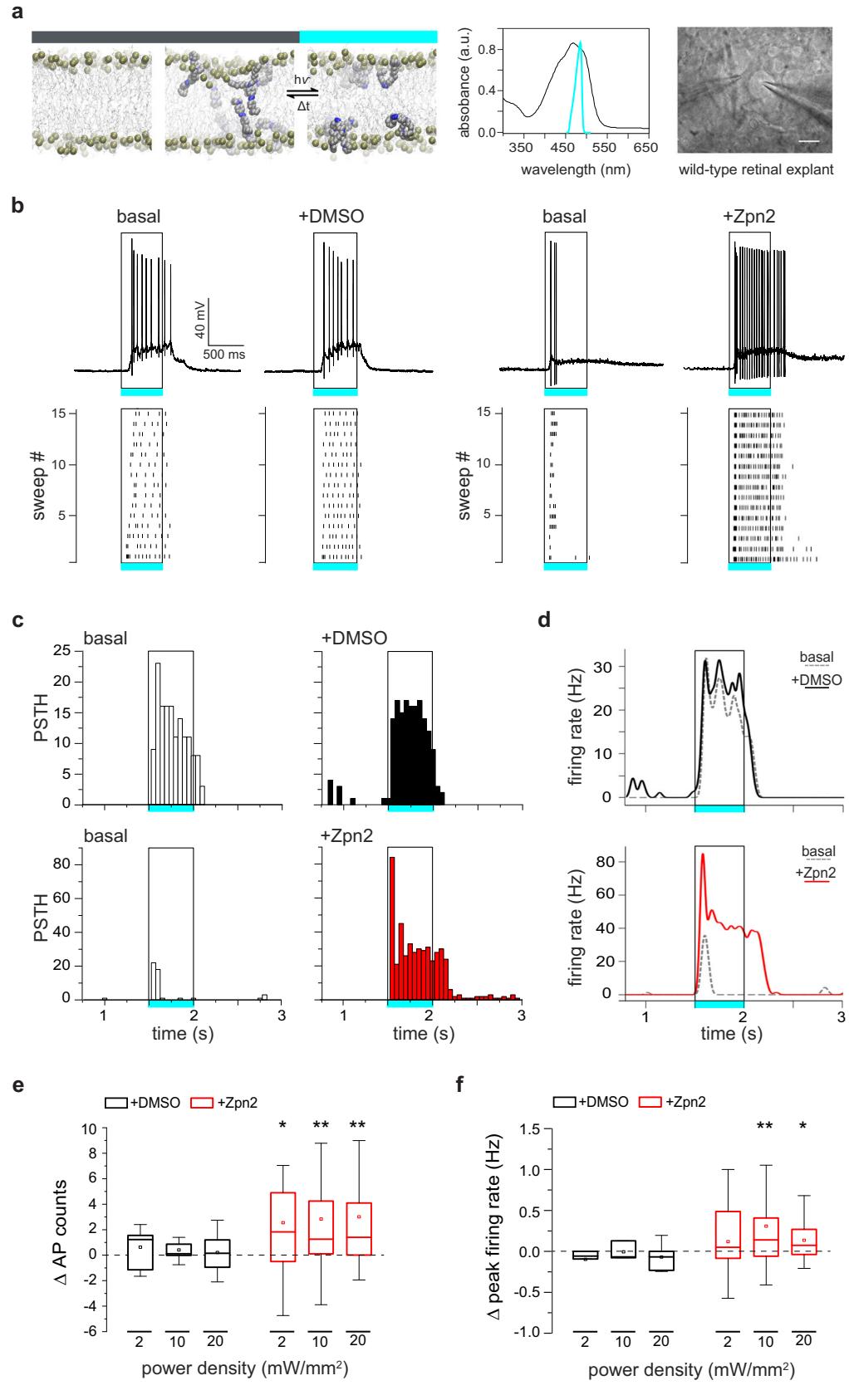
图1 | Ziapin2增强野生型视网膜中光诱发的视网膜神经节细胞(RGC)放电活动。a 左图:Ziapin2的分子结构及其自发膜插入后的拓扑结构:在黑暗中,Ziapin2整合到磷脂双分子层中(左),并以反式异构体的形式在相对的膜小叶上自缔合(中),导致膜收缩,而蓝光诱导其转化为顺式构象可逆转这种收缩(右)。改编自49。中图:Ziapin2在二甲基亚砜(DMSO)中的紫外-可见吸收光谱(黑色轨迹;吸收峰为470 nm),与本研究中使用的蓝色LED的光谱输出叠加。右图:视网膜神经节细胞的图像,左侧为用于施加Ziapin2的吹管,右侧为膜片钳电极。比例尺,20 µm。b 代表性的电流钳记录轨迹(上)和相应的光栅图(下;15次扫描),记录自野生型小鼠视网膜外植体中的两个不同视网膜神经节细胞,分别在给予溶媒(10% v/v DMSO)或Ziapin2(200 µM)之前(基础状态)和之后,显示经Ziapin2处理的神经元在蓝光刺激(500 ms,20 mW/mm²;空心矩形)下,光诱发的动作电位(AP)放电增强。c 如(b)中两个视网膜神经节细胞的代表性刺激时间直方图(PSTH),显示在给予DMSO(上排,黑色柱)或Ziapin2(下排,红色柱)之前(基础状态,空心柱)和之后,对蓝光刺激的动作电位计数(50 ms bins)。矩形框住了蓝光刺激期间(500 ms,20 mW/mm²)的反应。d (b)中所示的两个视网膜神经节细胞在基础条件下(灰色虚线)以及随后施加DMSO(上,黑线)或Ziapin2(下,红线)后的放电率变化。蓝光刺激(500 ms,20 mW/mm²)的时间由空心矩形表示。e、f 箱线图分别表示在施加DMSO(黑色箱)或Ziapin2(红色箱)后,在不同功率密度(2、10和20 mW/mm²)下,相对于基础状态的蓝光诱发动作电位计数(e)和峰值放电率(f)的变化。变化表示为Ziapin2/DMSO吹管施加后与基础状态之间的差值(Δ)。箱线图的中线代表平均值,内部的方块表示中位数,箱体边界显示第一和第三四分位数,须线显示最小值和最大值。*p < 0.05,**p < 0.01;与基础状态相比的双尾配对Wilcoxon符号秩检验(DMSO组和Ziapin2组分别有12个和34个视网膜神经节细胞)。确切的p值和源数据见源数据文件。
¶ Ziapin2恢复了失明rd10小鼠视网膜外植体中视网膜神经节细胞(RGCs)的自然编码能力
鉴于Ziapin2在有视力视网膜的 spike RGC 中表现出的暗/光双功能活性,我们试图测试它是否能恢复对光不敏感的退化视网膜的光敏感性以及视网膜网络的复杂处理能力。为了验证这一假设,我们对取自6月龄 rd10 小鼠的失明视网膜进行了膜片钳实验。在首次尝试中,我们像处理正常有视力的视网膜外植体一样,将 Ziapin2(200 µM)直接吹到记录的 RGC 上(图 S4a)。然而,在来自营养不良视网膜的 RGC 中,蓝光刺激并未诱发动作电位(APs),仅引发了依赖光的阈下去极化,而绿光刺激则无此现象(图 S4b、c)。这表明,在对光不敏感的视网膜中,当缺乏来自二级视网膜神经元的伴随光诱发突触输入时,Ziapin2 无法使 RGC 达到放电阈值。因此,为了让 Ziapin2 渗透到所有未因退化而受损的视网膜神经元中,我们先将视网膜外植体浸入含有 Ziapin2(10 µM,30分钟)的溶液中,然后将其转移到记录室,并评估 Ziapin2 对蓝光与绿光刺激的特异性效应。在这些条件下,RGC 对蓝光刺激会发放动作电位序列,而对绿光刺激则不会(图 S4d)。
事实上,在全视网膜治疗后,Ziapin2重新激活了多种视网膜神经节细胞(RGC)反应,包括对青色光的ON和OFF反应,这些反应具有不同的动态特征,从短暂到持续再到受抑制(图3a-d)。在2至30 mW/mm²的所有测试功率密度下,对青色光的总动作电位(AP)计数和峰值瞬时发放率均显著增加,而对绿色光则无此现象(图3e)。正如之前所描述的55,当我们通过共聚焦显微镜回顾性研究经AlexaFluor-633标记的记录到的视网膜神经节细胞的三维形态时,发现青色光诱发的反应始终与所有记录到的视网膜神经节细胞在视网膜内丛状层中的树突分层一致(图3a)。
为了探究经Ziapin2处理的失明视网膜中可能出现的视网膜神经节细胞(RGC)反应的复杂性,我们使用高密度多电极阵列(HD-MEA)记录了光诱发反应,该阵列能够同时追踪数百个视网膜神经节细胞56,57。绿光刺激并未显著影响视网膜神经节细胞的整体放电(图4a、b),仅少数内在光敏性视网膜神经节细胞出现典型的缓慢、持续性反应(如图4b左侧光栅图所示)。相反,蓝光刺激重现了在正常视力视网膜中通常记录到的多种反应:可以识别出从快速到迟缓的ON-持续性和ON-瞬时性细胞、ON-OFF细胞以及OFF-抑制性或OFF-瞬时性细胞(图4c)。值得注意的是,细胞4显示出明显的适应迹象,这意味着Ziapin2恢复了细微但重要的网络机制。
我们使用高密度微电极阵列(HD-MEA),通过将那些表现出光诱发放电率变化大于平均自发放电率加2倍标准差的视网膜神经节细胞(RGCs)视为有反应的细胞,评估了在退化视网膜中经Ziapin2重新激活的光反应性视网膜神经节细胞的百分比。在所有记录的视网膜中,仅有3%的视网膜神经节细胞对绿光刺激有反应,而在经Ziapin2处理的视网膜中,对蓝光有反应的细胞比例显著更高(63%)(Fisher精确检验,p < 0.0001;图4d)。对各个高密度微电极阵列实验的结果进行分析时,我们观察到,与实际上无效的绿光相比,Ziapin2能够显著恢复多种视网膜神经节细胞亚类对蓝光的反应(图4d、e)。
由于Ziapin2效应本质上是电容变化的瞬态过程,因此它有可能对高频刺激做出响应。于是,我们研究了光诱导的Ziapin2刺激能够以多高的频率重复进行以增强细胞兴奋性。通过让失明的rd10外植体接受频率逐渐增加、时长逐渐缩短的蓝光闪烁(相比之下,对照组为0.25赫兹的单次250毫秒光闪烁),我们发现,在10赫兹的光刺激下,Ziapin2诱导的视网膜神经节细胞(RCG) firing率增加不受影响;在15赫兹时,这种增加有所减弱但仍然存在;而在30赫兹时,这种增加几乎消失(图S5)。
尽管主要目的是表征Ziapin2对去神经支配BCs的影响,但我们想知道Ziapin2的作用是否特定于退化视网膜,还是在野生型(WT)视网膜的整个回路中也存在。我们将野生型视网膜外植体分别在溶媒(0.5%二甲基亚砜)或Ziapin2(10微摩尔)溶液中孵育,并通过高密度微电极阵列(HD-MEAs)记录视网膜神经节细胞(RGC)群体对蓝光的反应。我们发现,经Ziapin2处理的视网膜中,具有持续或瞬态放电模式的反应性ON型、OFF型、ON/OFF型视网膜神经节细胞的数量与对照组相似(图S6a、b),但与溶媒处理的野生型视网膜相比,持续型ON型和OFF型视网膜神经节细胞对蓝光的放电率显著提高(图S6c)。
¶ Ziapin2加快了退化rd10视网膜中视网膜神经节细胞(RGCs)的动作电位动态变化
随着光感受器的丧失,失明的视网膜在解剖和功能网络组织方面发生了显著而深刻的变化,导致视网膜神经节细胞(RGCs)接收光诱发的突触输入并触发动作电位(AP)发放以处理视觉信息的能力受损。
我们首先验证了退化视网膜中诱发的放电确实是由Ziapin2反式到顺式异构化引起的膜电容突然下降所触发的。为此,我们向单个视网膜神经节细胞局部施加Ziapin2(200微摩尔),并用青色或绿色光进行刺激(图S7a)。与我们之前在原代海马神经元中的观察结果一致,青色光(而非绿色光)刺激显著降低了视网膜神经节细胞的电容,且不影响膜电阻,导致膜时间常数出现光依赖性下降(图S7b、c)。
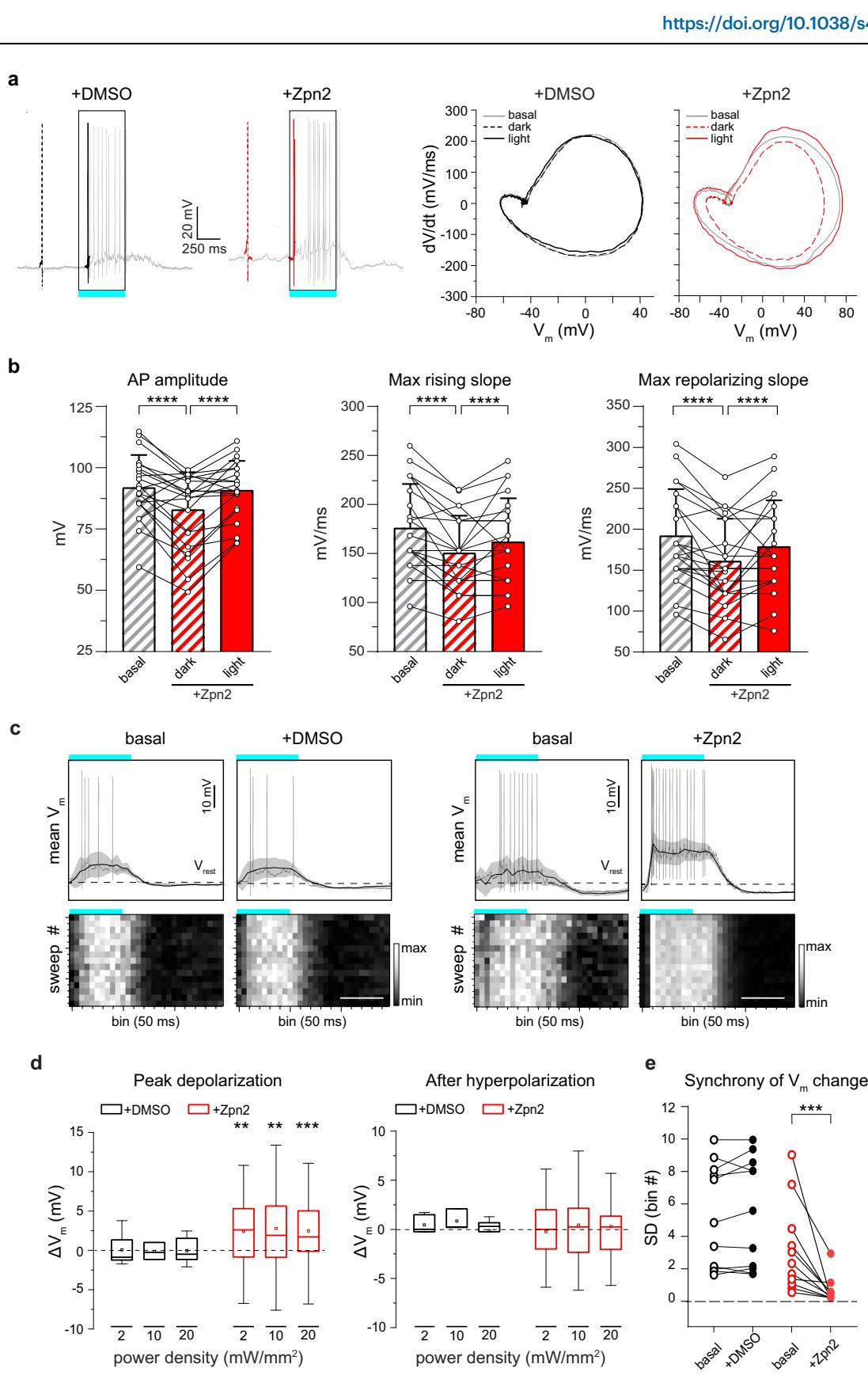
图2 | Ziapin2引起的光诱发电容变化在野生型视网膜中诱导更快的动作电位动力学和膜去极化。a左图:在溶媒(10%体积/体积二甲基亚砜;左图,黑色)或Ziapin2(200μM;右图,红色)存在下,两个视网膜神经节细胞(RGC)的代表性全细胞电流钳记录轨迹,显示暗环境中的第一个尖峰(虚线)和第一个光诱发尖峰(实线)。右图:与基础条件下暗环境中的动作电位波形(灰色线)相比,在局部施加二甲基亚砜(黑色)或Ziapin2(红色)后,暗环境中(虚线)和青色光刺激期间(实线;20mW/mm²,500ms)第一个动作电位波形的相平面图分析。b从每个记录的RGC在暗环境和青色光刺激下施加Ziapin2之前(基础状态)和之后的相平面图分析中得出的动作电位振幅(左图)、最大上升斜率(中图)和最大复极化斜率(右图)的变化。柱状图表示平均值±标准误,叠加有单个数据点(n=22个RGC)。c上图:从光刺激开始(500ms,青色水平条)的1.5s时间窗口内,在基础状态下以及用溶媒(10%体积/体积二甲基亚砜;左图)或Ziapin2(200μM;右图)处理后,从RGC记录的代表性低通滤波电压轨迹。图中显示了在15次扫描的相同时间窗口内计算的平均膜电位(±标准差,灰色区域)。静息膜电位(虚线),即暗环境中的膜电位。动作电位叠加在电压轨迹上。下图:15次扫描期间膜电位变化的灰度表示(50ms bins)。比例尺,500ms。d箱线图显示在用溶媒(10%体积/体积二甲基亚砜;黑色)或Ziapin2(200μM;红色)处理并以递增功率密度(2、10和20mW/mm²;二甲基亚砜和Ziapin2局部施加分别为n=12和34)的青色光刺激的RGC中,相对于静息膜电位计算的峰值去极化(左图)和峰值超极化后电位(右图)(见图c)。箱线图的中线代表平均值,箱内的方块代表中位数,箱体边界显示第一和第三四分位数,须线显示最小值和最大值。e青色光响应中电压变化同步性的评估,在Ziapin2或二甲基亚砜局部施加之前(基础状态)和之后(二甲基亚砜和Ziapin2局部施加分别为n=10和11个RGC)。**p<0.01,***p<0.001,****p<0.0001;与基础状态相比的双尾配对Wilcoxon符号秩检验。确切的p值和源数据作为源数据文件提供。
为了进一步了解Ziapin2对rd10视网膜外植体中视网膜神经节细胞(RGCs)被动特性的电容效应,我们通过相平面图分析研究了动作电位(AP)动力学的变化。视网膜用Ziapin2(10μM,处理30分钟)孵育,并用蓝光激活Ziapin2,或用绿光作为阴性对照进行刺激。在黑暗中或对绿光的反应中,放电模式和动作电位波形(最大动作电位峰值以及最大上升斜率和复极化斜率)未观察到差异(图5a、b)。相反,与相同细胞对绿光刺激产生的动作电位相比,蓝光刺激显著加快了动作电位的动力学过程,峰值振幅显著增加,上升期和复极化期也更快(图5c)。当我们应用低通滤波器去除动作电位并检测缓慢的电压振荡时(图5d),发现在所有测试的功率密度(2-30 mW/mm²)下,蓝光刺激能显著增加去极化峰值和超极化后电位的振幅,而绿光刺激则无此效应(图5e)。
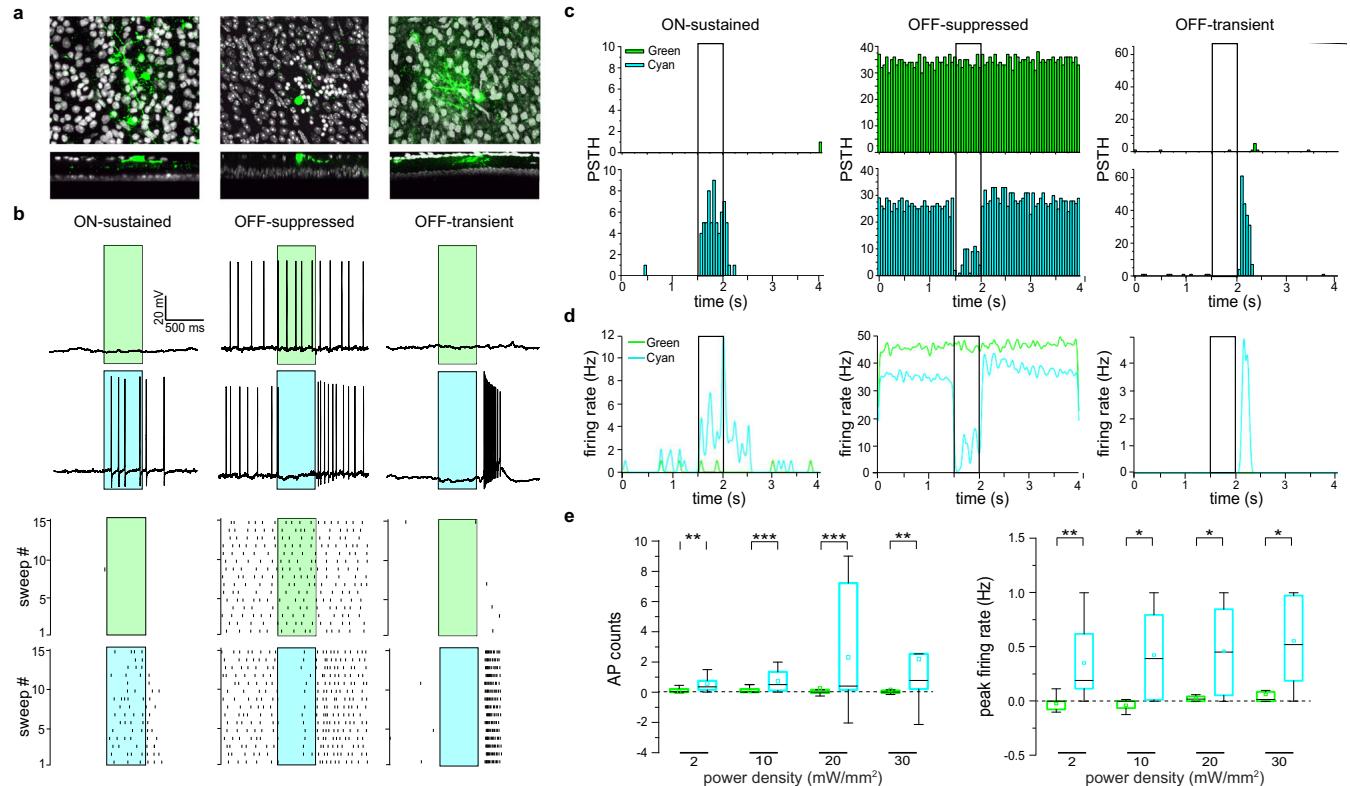
图3 | Ziapin2可恢复退化rd10视网膜中视网膜神经节细胞(RGCs)对光的生理反应。a上图:(b)中记录的视网膜神经节细胞的形态重建,用Alexa Fluor 633(绿色)标记。下图:相同Z投影的横向切片,显示记录的视网膜神经节细胞的树突在不同内网层(IPL)亚层中的分布。这三个视网膜神经节细胞的形态和树突分层与其对光的ON-持续型(左)、OFF-抑制型(中)和OFF-瞬变型(右)生理反应相对应。b上图:在存在Ziapin2(10μM)的情况下孵育失明视网膜外植体后,(a)中所示的视网膜神经节细胞对绿光或青光(500毫秒;20毫瓦/平方毫米)全视野照明的代表性反应。在绿光照射下未检测到光依赖性放电活动,而青光刺激则诱导出类似有视力动物的各种反应。下图:光栅图显示相同视网膜神经节细胞在15次连续扫描中的放电活动。光刺激以青色或绿色阴影区域表示。c、d(b)中记录的视网膜神经节细胞的代表性刺激后时间直方图(c)和瞬时放电率(d)。柱形图表示响应绿光(上图)或青光(下图)刺激记录的动作电位(AP)计数(50毫秒 bins)。光刺激(500毫秒)以开放矩形表示。绿光未引起放电活动的调制。e箱线图显示在从光刺激开始到结束后1秒的时间窗口内,响应500毫秒绿光或青光(彩色框)刺激的光诱发动作电位计数(左)和峰值放电率(右),并归一化为黑暗中记录的自发活动。光刺激以递增的功率密度(2、10、20和30毫瓦/平方毫米)施加。箱线图的中线代表平均值,箱内的正方形代表中位数,箱的边界代表第一和第三四分位数,须线代表最小值和最大值。*p<0.05,**p<0.01,***p<0.001;双尾配对样本Wilcoxon符号秩检验(n=14)。确切的p值和源数据见源数据文件。
¶ Ziapin2可恢复退化rd10视网膜中视网膜神经节细胞(RGCs)的光诱发兴奋性和抑制性突触输入
我们发现,Ziapin2能够恢复退化视网膜重新激活视觉信息处理的分离通道的能力,但这只有在将光开关应用于所有视网膜神经元而非仅单个视网膜神经节细胞(RGC)时才会发生(见图S4)。这些发现引发了一个问题:光诱发的多种视网膜神经节细胞反应,是源于整个视网膜网络功能的恢复,还是源于对视网膜神经节细胞内在兴奋性的直接影响。 为回答这一问题,我们采用电压钳配置进行膜片钳实验,以测量在经Ziapin2(10µM,孵育30分钟)处理的失明rd10小鼠视网膜中,光诱发的对视网膜神经节细胞的突触输入。在进入细胞内区室之前,我们通过在细胞贴附式配置下记录蓝光诱发的放电活动来评估视网膜神经节细胞的极性,并以绿光作为阴性对照(见图6a中的代表性OFF型视网膜神经节细胞)。 有趣的是,一旦达到全细胞配置,我们发现动作电位(APs)是由视网膜神经节细胞中光诱发的突触电导激活产生的,而在绿光刺激下,这种突触电导可忽略不计(图6b)。实际上,Ziapin2恢复了兴奋性和抑制性电导(图6c),细胞极性和动作电位的产生正是源于这两种电导之间精细的时间相互作用。 总体而言,在失明视网膜外植体的视网膜神经元中激活Ziapin2后,在2和20 mW/mm²两种功率密度下,均能显著重新激活对视网膜神经节细胞的生理性兴奋性(ge)和抑制性(gi)突触输入(图6d)。
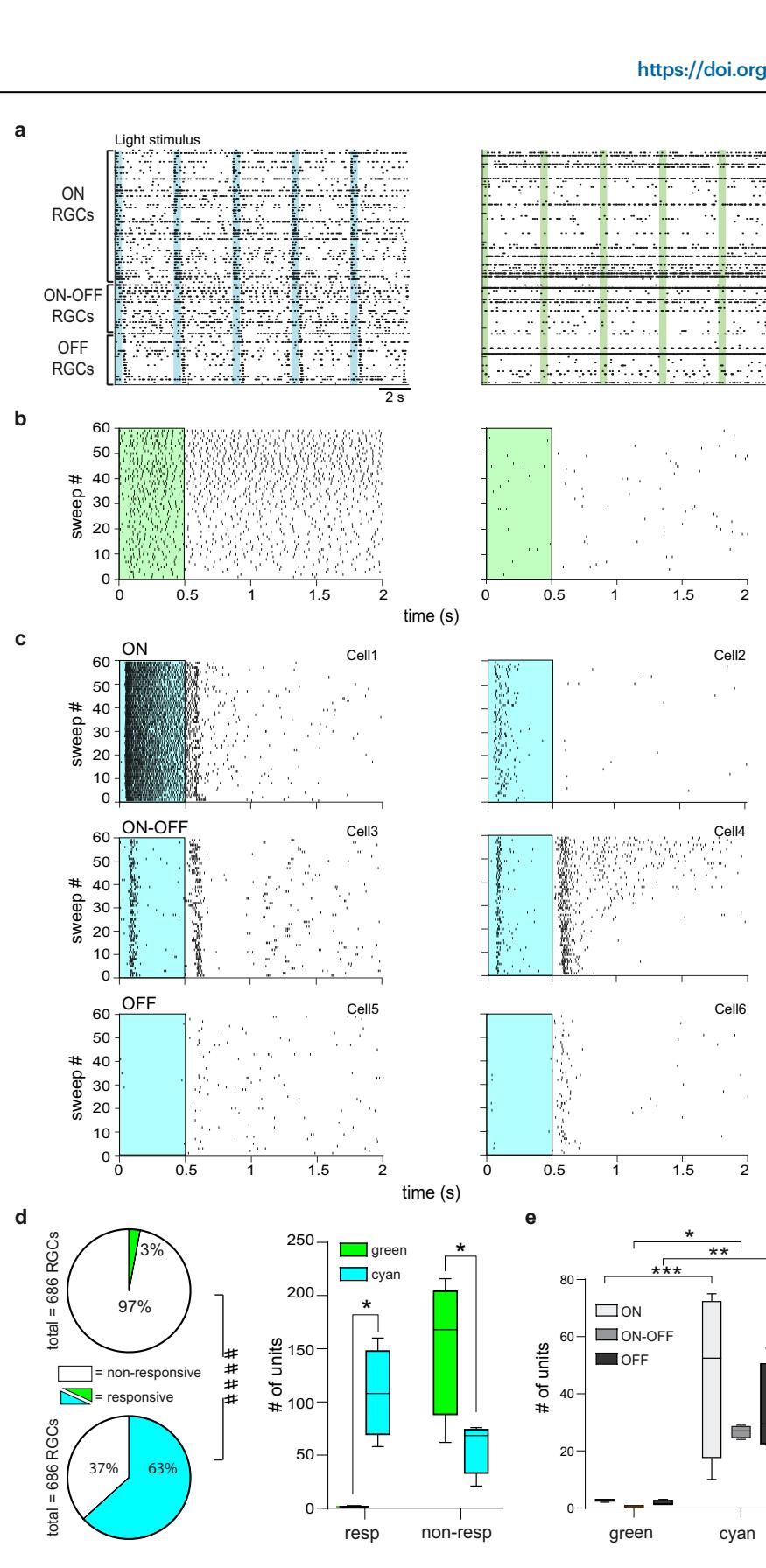
图4 | Ziapin2恢复退化rd10视网膜在分离通道中分析视觉信息的能力。a 用10 µM Ziapin2孵育后的同一只rd10盲视网膜外植体在高清微电极阵列(HD-MEA)记录中获得的代表性动作电位(AP)光栅图,分别用青色光(左)或绿色光(右)刺激(500毫秒;2毫瓦/平方毫米)。每行代表经极性分类的单个视网膜神经节细胞(RGC)的放电活动。仅在全视野青色光刺激下恢复了光依赖性放电活动,绿色光刺激则未恢复。光脉冲用垂直彩色编码条表示。b 两个具有显著不同自发活动的RGC在60次扫描中产生的AP代表性光栅图。在这两个细胞中,绿色光刺激(绿色矩形)均无法调节放电活动。c 不同类型RGC对全视野青色光刺激(青色矩形)产生AP放电的代表性光栅图。青色刺激引发了持续ON型(细胞1)、瞬态ON型(细胞2)、ON-OFF型(细胞3、细胞4)、OFF抑制型(细胞5)和瞬态OFF型(细胞6)反应。d 左图:饼图表示对绿色光(上)和青色光(下)刺激有反应的RGC占HD-MEA记录的RGC总数的百分比(括号中为具体数量)。***p < 0.001,双侧Fisher精确检验;对绿色光和青色光有反应/无反应的RGC比较。右图:箱线图显示4只rd10小鼠视网膜中对青色光或绿色光刺激有反应和无反应的RGC数量。箱线图中线代表平均值,箱内方块代表中位数,箱体边界为第一和第三四分位数,须线为数据的最小值和最大值。e 箱线图显示4只rd10小鼠视网膜中对青色光或绿色光刺激有反应的ON型、ON-OFF型和OFF型RGC数量。箱线图中线代表平均值,箱内方块代表中位数,箱体边界为第一和第三四分位数,须线为数据的最小值和最大值。####p < 0.0001,Fisher精确检验;对绿色光和青色光有反应/无反应的RGC比较;*p < 0.05,**p < 0.01,***p < 0.001,双因素方差分析/霍尔姆-希达克检验(n = 4)。确切的p值和源数据见源数据文件。
为了进一步研究突触传递在Ziapin2介导的反应产生中的作用,我们用mGluR6激动剂L-AP4灌流野生型(WT)和rd10视网膜外植体,以阻止光感受器介导的信号传递至二阶神经元,并通过高密度微电极阵列(HD-MEA)记录分析视网膜神经节细胞(RGC)对蓝光的放电反应。值得注意的是,在具有代表性的视网膜神经节细胞中,L-AP4完全消除了野生型视网膜中250毫秒蓝光刺激引起的放电反应,而在经Ziapin2处理的rd10视网膜中,该药物对放电反应几乎没有影响(图6e)。对独立实验中获得的视网膜神经节细胞群体对100毫秒和250毫秒蓝光刺激的放电反应进行统计分析,证实L-AP4能显著抑制野生型视网膜中ON型放电反应,但在经Ziapin2处理的rd10视网膜中则无此作用(图6f)。这一结果排除了残余光感受器的激活介导rd10视网膜神经节细胞中记录到的光诱发电流和动作电位(APs)的可能性,表明Ziapin2主要作用于双极细胞(BCs)水平。
为了验证在Ziapin2处理的rd10视网膜中,氰刺激后OFF反应的重新激活是否也涉及视杆双极细胞(rod BCs)和AII无长突细胞,我们用甘氨酸受体阻滞剂士的宁(10μM;图S8a)灌流视网膜外植体。结果发现,士的宁使OFF型和ON/OFF型视网膜神经节细胞(RGCs)的比例显著降低了约25%,而对ON型视网膜神经节细胞的比例(图S8b)以及反应性视网膜神经节细胞亚型的相对占比(图S8c)没有显著影响。
¶ Ziapin2对退化视网膜中视网膜处理功能的重新激活与物种和基因突变无关
视网膜色素变性是一种单基因疾病,由超过100种不同的突变引起,这些突变会影响在光感受器或视网膜色素上皮(RPE)细胞中表达的基因。为了评估Ziapin2在退化视网膜中的重新激活潜力是否与特定突变和功能失调的细胞类型无关,我们研究了Ziapin2对10月龄失明的RCS大鼠视网膜的影响,RCS大鼠是一种因Mertk基因突变导致RPE功能障碍而引发视杆-视锥细胞退化的动物模型。从RCS大鼠身上取出完全退化的视网膜,用Ziapin2(10μM,处理30分钟)孵育,通过膜片钳记录视网膜神经节细胞(RGCs)对蓝光或作为阴性对照的绿光的反应,来评估其光敏感性。
尽管动物物种和基因突变存在差异,但我们能够诱导出与Ziapin2处理的失明rd10视网膜中观察到的相似的光诱发反应,包括ON-持续性、OFF-抑制性和OFF-瞬态反应,而当用绿光刺激相同的视网膜神经节细胞(RGCs)时,这些反应无法检测到(图S9a)。刺激后时间直方图(PSTH)分析清楚地表明,仅在蓝光照射时,从光刺激开始后的1.5秒时间窗口内可检测到动作电位(AP)发放的增加,而绿光照射时则无此现象,这证明Ziapin2是这些效应的原因(图S9b)。动作电位发放的峰值速率在蓝光刺激期间或刺激结束后立即被测量,这与野生型(WT)视网膜神经节细胞已知的ON和OFF反应相似(图S9c)。最后,我们发现,在所有测试的功率密度(2–30毫瓦/平方毫米)下,所有记录的视网膜神经节细胞在蓝光刺激下,光诱发的动作电位计数和峰值发放率均显著增加,而对绿光无反应(图S9d、e)。
接下来,我们使用AMPA/红藻氨酸受体拮抗剂CNQX(10 µM)59和代谢型谷氨酸受体6激动剂L-AP4(20 µM)58对视网膜神经节细胞(RGCs)的这些反应进行了表征。CNQX完全消除了经Ziapin2处理的RCS视网膜中由蓝光诱发的OFF反应,而L-AP4对蓝光诱发的ON反应没有影响(图S10a)。我们还分析了图2所示的视网膜神经节细胞阈下膜电压振荡,观察到Ziapin2依赖的蓝光诱发去极化几乎不受L-AP4影响,而CNQX会使其减弱但不会完全消除(图S10b)。这些结果进一步证实,在失明视网膜中,突触隔离的视网膜神经节细胞经Ziapin2诱发的去极化不足以达到放电阈值,而失明视网膜中光诱发的视网膜神经节细胞放电是由于恢复了视网膜内层二阶神经元和中间神经元之间的精细相互作用。
接下来,我们重点研究了CNQX和L-AP4的应用对RCS盲视网膜中视网膜神经节细胞(RGCs)的光诱发突触输入的影响。CNQX显著消除了RGC的光诱发突触输入,这支持了Ziapin2通过作用于整个视网膜网络来恢复盲视网膜光诱发反应的假设(图S10c,左图)。氰光刺激在RGC中产生的突触电流在应用L-AP4前后可叠加,这一事实进一步证实了这一点,表明信号传递不依赖于光感受器的激活(图S10c,右图)。
值得注意的是,在用绿光刺激同一视网膜神经节细胞(RGC)期间进行的记录显示,没有光诱发反应,且这两种药物对RGC放电活动的影响可忽略不计(图S11a)。此外,在光刺激期间测量的膜电压和基础RGC电导方面,CNQX和L-AP4未引起任何可检测到的影响(图S11b、c)。
为了验证这一假设,研究人员在应用L-AP4前后,通过高清微电极阵列(HD-MEA)对年龄匹配的同基因RDY大鼠的健康视网膜以及经Ziapin2处理的营养不良型RCS大鼠的退化视网膜进行了平行记录(图S12)。在视力正常的RDY大鼠视网膜中,光诱发的ON型和ON-OFF型视网膜神经节细胞(RGC)的ON反应被完全消除,而ON-OFF型RGC的OFF反应未受影响(图S12a、c)。相反,在经Ziapin2孵育的营养不良型RCS大鼠视网膜中,应用L-AP4后,ON型和ON-OFF型RGC的蓝光诱发放电模式均未出现任何改变(图S12b、d)。对独立实验中获得的RGC对蓝光刺激的放电反应进行统计分析证实,L-AP4仅能显著消除有视力的RDY大鼠RGC的放电反应,而对失明的RCS大鼠RGC完全无效(图S12e)。
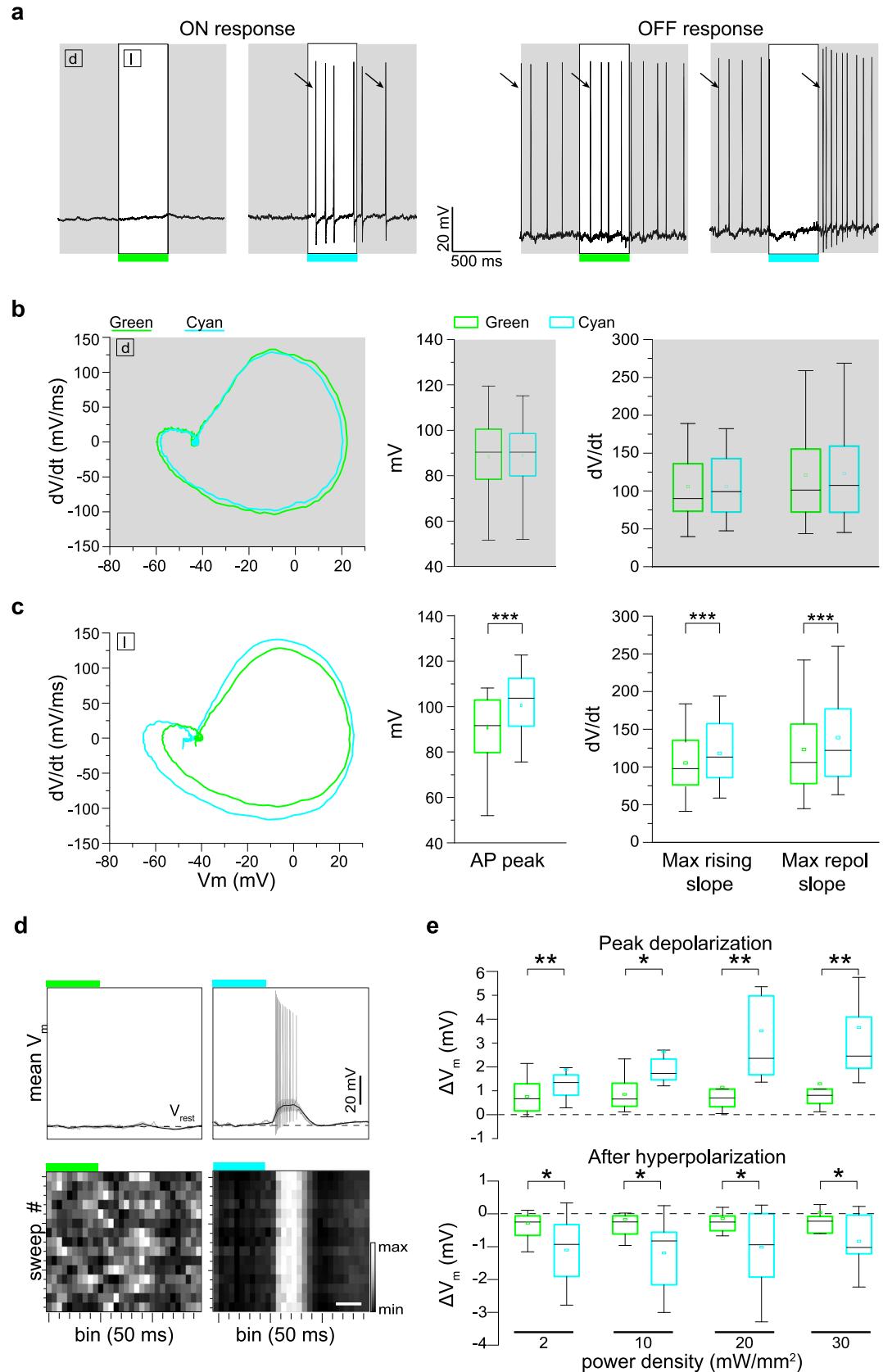
图5 | Ziapin2引起的光诱发电容变化在退化的rd10视网膜中诱导更快的动作电位动力学和膜(变化)。a 来自经Ziapin2(10μM)孵育的失明rd10视网膜的两个视网膜神经节细胞(RGC)的代表性电流钳记录轨迹,显示对青色光(右侧轨迹)有ON(左侧)和OFF(右侧)反应,但对绿色光(左侧轨迹)无反应。开放矩形代表光刺激的时间(500毫秒,20毫瓦/平方毫米)。箭头指示用于进行(b)中所示波形分析的黑暗中(d)和光反应中(l)的第一个动作电位。b 左图:光刺激前,在(a)中所示的相同RGC中,黑暗中(d)产生的第一个动作电位的代表性相平面 plot分析。右图:箱线图显示从所有记录的RGC(n=28个RGC)的相平面分析计算出的黑暗中的动作电位峰值、最大上升斜率和最大复极化斜率。c 左图:在绿色或青色光刺激(l)期间,(a)中所示的相同RGC中产生的第一个动作电位的代表性相平面 plot分析。右图:绿色或青色光刺激后的动作电位峰值、最大上升斜率和最大复极化斜率的箱线图。***p<0.001;双尾配对Wilcoxon符号秩检验(n=28个RGC)。d 上图:在1.5秒的时间窗口内,从绿色(左侧)或青色(右侧)光刺激(500毫秒,20毫瓦/平方毫米)开始,记录的经Ziapin2(10μM)孵育的RGC的代表性低通滤波电压轨迹。这些图显示了在15次扫描的相同时间窗口内计算的平均(±标准差,灰色区域)膜电位(Vm)。静息膜电位(Vrest,虚线),即黑暗中的膜电位。青色光诱发的动作电位叠加在电压轨迹上。下图:15次扫描期间膜电位变化的灰度表示(50毫秒区间)。比例尺,250毫秒。e 箱线图显示在用Ziapin2处理并在不同功率密度(2、10、20和30毫瓦/平方毫米)下接受绿色或青色光刺激(彩色框)的RGC中,相对于静息膜电位计算的峰值去极化(上图)和峰值超极化后电位(下图)(参见d)(n=14个RGC)。箱线图的中线代表平均值,箱内的正方形代表中位数,箱体边界显示第一和第三四分位数,须线显示最小值和最大值。*p<0.05;**p<0.01;青色光与绿色光刺激的双尾配对Wilcoxon符号秩检验。确切的p值和源数据作为源数据文件提供。
¶ 在体内对年老失明的rd10小鼠进行玻璃体内注射Ziapin2可恢复其视觉驱动行为
为了探究Ziapin2能否作为体内视觉恢复的潜在治疗工具,我们向6月龄的失明rd10小鼠玻璃体内注射了Ziapin2(200µM,二甲基亚砜的最终玻璃体内浓度为10%)。同龄的野生型(WT)小鼠和失明rd10小鼠均注射了溶媒,并作为对照组。在注射后的两周内,我们通过光驱动行为测试来研究小鼠的表现(图7a)。我们利用明暗箱对失明小鼠的视觉恢复情况进行评估,该装置的原理是啮齿类动物天生厌恶有光照的开阔空间,这种厌恶会引发焦虑情绪60(详见方法部分)。小鼠可在整个装置内自由活动,先在黑暗条件下记录其在每个舱室的停留时间,持续3分钟,随后在左侧舱室用5勒克斯的白色弱光照射,同样记录3分钟。在完全黑暗的测试中,野生型小鼠、溶媒处理的失明rd10小鼠以及Ziapin2处理的失明rd10小鼠表现极为相似,这从它们在左侧舱室及其开阔中心区域的停留时间均可得到验证(图7b、c)。相反,当开启光照后,玻璃体内注射Ziapin2的小鼠恢复了避光行为,与注射溶媒的失明对照组相比,它们在光照舱室及其开阔中心区域的停留时间均显著减少,且表现接近野生型小鼠(图7d、e)。值得注意的是,对注射后长达两周内效果的时间进程分析显示,Ziapin2诱导的光驱动行为改善具有持续性,这一点也可从个体动物的表现得到证实(图S13a、b)。
¶ 在体内对年老的失明rd10小鼠进行玻璃体内注射Ziapin2,可恢复其视觉运动反应和视网膜神经节细胞的生理性放电。
为了研究玻璃体内注射Ziapin2对失明rd10小鼠模式感知的影响,我们评估了小鼠对以随机顺序呈现的不同空间频率移动光栅模式的视动反应(OMR)。对移动模式的感知会引发与刺激同步的先天性头部运动,这些运动被追踪并量化为OMR评分,当评分超过1.2的阈值时,表明视觉功能正常61,62。正如预期的那样,未接受治疗的野生型(WT)小鼠在0.05至0.3周/度的空间频率范围内,OMR指数>1.2,且玻璃体内注射溶媒对此没有影响(图8a和图S13c)。相反,老年rd10小鼠表现出较差的OMR反应(评分<1),且注射溶媒对此没有影响。值得注意的是,年龄匹配的rd10小鼠在玻璃体内注射Ziapin2后,视觉功能显著提高,OMR评分显著高于1.2,且在整个2周的观察期内均保持这一水平(图8a),三个实验组中小鼠的个体表现也证实了这一点(图S13c)。
为了验证盲鼠体内视觉恢复是否依赖于体外观察到的Ziapin2的作用,我们对玻璃体内注射两天后接受溶媒或Ziapin2处理的rd10小鼠的视网膜进行了高密度微电极阵列(HD-MEA)记录。与行为学上观察到的视觉恢复一致,全视野蓝光刺激能够在接受Ziapin2体内处理的rd10小鼠的16.6%的记录视网膜神经节细胞(RGCs)中触发动作电位(AP)发放,而接受溶媒处理的rd10小鼠的这一比例为1.7%(Fisher精确检验,p < 0.0001;图8b左)。对视网膜神经节细胞亚类发放反应的统计分析显示,与溶媒处理的rd10小鼠相比,Ziapin2处理的小鼠中,有反应的ON型和ON-OFF型视网膜神经节细胞显著增加,而有反应的OFF型视网膜神经节细胞增加幅度较小且不显著(图8b右)。
在进行HD-MEA记录的同时,研究人员对视网膜横切面进行了免疫组织化学分析,以评估视杆细胞和视锥细胞的损耗情况,以及Ziapin2注射可能产生的促炎效应。由于该化合物在异构化过程中会发生能量光转化,且在玻璃体内注射后到达视网膜各层时会被大量稀释,导致其本身荧光较弱,因此无法可靠地检测到Ziapin2的荧光。对视锥 Arrestin(图S14a)和视紫红质(图S14b)的定量形态学分析显示,视杆细胞完全消失,外视网膜中仅存极少数缺乏外节的视锥细胞胞体(图S14d、e),这与光反应缺失的情况一致。尽管之前的研究已证实Ziapin2具有高度的生物相容性,在体外和体内均不影响神经元的存活能力,但我们仍分析了GFAP和Iba1的免疫反应性,它们分别作为 Müller细胞/星形胶质细胞和小胶质细胞活化的标志物,对野生型(WT)和rd10小鼠玻璃体内注射溶剂或Ziapin2后的情况进行了检测(图S14c)。与之前的结果一致,在营养不良的rd10小鼠中,未观察到Ziapin2引起的GFAP或Iba1免疫反应性增强以及小胶质细胞数量增加,这表明Ziapin2的施用没有明显的促炎活性(图S14f、g)。
¶ 讨论
使用膜靶向光致变色分子治疗视觉障碍是现有视网膜假体的一种很有前景的替代策略。我们利用了Ziapin2有趣的双面特性,这是一种膜靶向光致变色化合物,它通过单纯作用于膜的被动特性,使神经元在黑暗中兴奋性降低,在光刺激下则阶段性地更易兴奋,且不会干扰离子通道或神经递质受体。将这种化合物应用于受光感受器退化影响的光不敏感视网膜,其灵感来源于该分子的双功能行为,这种行为似乎非常适合模拟神经视网膜的ON/OFF处理机制。目前,有几种材料和人工视网膜装置可以替代退化光感受器的光转导过程。然而,使用这些材料和装置的主要挑战在于,难以重现正常视网膜中存在的自然编码多样性,并且会不加区分地将ON(光)信号施加于ON型和OFF型视锥双极细胞。

图6 | Ziapin2恢复退化rd10视网膜中视网膜神经节细胞(RGCs)的光诱发兴奋性和抑制性突触输入。a上图:用10µM Ziapin2孵育30分钟后,来自失明rd10视网膜的OFF型RGC在细胞贴附式构型下的代表性电压钳记录,分别接受绿色(左)或青色(右)光的全视野刺激(500毫秒,20毫瓦/平方毫米)。下图:在达到全细胞构型并施加从-86到34毫伏的电压阶跃后,在同一RGC中记录到光诱导电流。光刺激在底部轨迹中以彩色编码条显示。b根据电流轨迹计算出,在(a)中所示的经Ziapin2孵育的同一RGC中,对绿色或青色光刺激产生的总电导。c从电压钳记录中推断出,在(a)中所示的同一RGC中,由绿色(左)或青色(右)光刺激诱发的兴奋性(ge)和抑制性(gi)电导。d所有RGC在2毫瓦/平方毫米和20毫瓦/平方毫米功率密度下接受绿色(绿色框)和青色(青色框)光刺激时,计算出的兴奋性(ge;左)和抑制性(gi;右)电导最大值的箱线图(n=12个RGC)。*p<0.05;双尾配对Wilcoxon符号秩检验,青色光与绿色光刺激对比。e左:在基础状态下以及应用mGluR6激动剂L-AP4(可消除视杆和视锥ON型双极细胞(BCs)的光诱发激活)后,来自健康野生型(WT)视网膜的ON型RGC接受青色光(2毫瓦/平方毫米;250毫秒;矩形)刺激的代表性高密度微电极阵列(HD-MEA)记录(20次扫描的光栅图及下方相应的peri-stimulus time histogram,PSTH)。右:对经Ziapin2(10µM)孵育的失明rd10视网膜的代表性RGC应用相同方案,在应用L-AP4之前(基础状态)和之后接受青色光刺激。f健康WT视网膜(左)和经Ziapin2处理的失明rd10视网膜(右)中的RGC在有无L-AP4存在时,接受青色光(2毫瓦/平方毫米)刺激100毫秒和250毫秒后的放电活动箱线图(WT和rd10视网膜分别有322个和266个RGC,均来自2只WT小鼠和2只rd10小鼠)。箱线图的中线代表平均值,箱内的方块代表中位数,箱体边界表示第一和第三四分位数,须线显示最小值和最大值。
***p < 0.001,双尾配对Wilcoxon符号秩检验,基础状态与L-AP4对比。确切的p值和源数据详见源数据文件。
在本文中,我们发现Ziapin2作用于视网膜神经元的分子机制与在人工膜、细胞系和原代神经元中所描述的相同,即根据黑暗/光照条件,以相反的方向改变膜电容。当将Ziapin2直接吹送到野生型视网膜的视网膜神经节细胞(RGCs)上时,它会增强RGCs对光的兴奋性,诱导RGCs放电,且相对于生理性光转导机制具有叠加效应。然而,在完全退化的视网膜中,由于RGCs的突触输入对光不敏感,单个RGC的刺激不足以达到放电阈值,因此Ziapin2必须作用于视网膜二级神经元。当整个视网膜用Ziapin2孵育时,蓝光会激活多个不同的RGC亚群(持续型ON、瞬变型ON、ON-OFF型、抑制型OFF、瞬变型OFF的RGCs),同时RGCs上的兴奋性和抑制性突触输入也会恢复,这表明Ziapin2的关键作用在于视网膜二级神经元。这些反应始终与RGC树突在视网膜内丛状层的分层情况一致,且使用特定突触阻滞剂获得的数据表明,Ziapin2作用于双极细胞(BCs),并对视锥细胞的ON型和OFF型双极细胞有差异性激活6–8。尽管Ziapin2刺激能够使RGCs恢复多种不同的功能性反应,但无法识别健康视网膜中存在的所有众多RGC功能亚型1,这可能是因为本研究中使用的rd10小鼠和RCS大鼠的视网膜退化程度较深,且视网膜内层存在明显的重连接现象。
Ziapin2的作用机制非常适合重新激活视网膜的处理过程。作为一种靶向膜的光开关,它能在单细胞分辨率下发挥作用。在黑暗中,细胞膜电容会出现持续性增加,而在蓝光刺激下,这种增加会阶段性消失,这是一种作用于膜被动特性的高速机制,它会根据光线的有无使神经元要么不易兴奋,要么易于兴奋。在后一种情况下,光诱导的膜电容突然降低会增强任何离子电流改变膜电位的能力。与电容的瞬时变化一致,Ziapin2的作用在相对较高频率的光刺激下仍然有效,在15赫兹时仍可检测到,而15赫兹被视为“运动”视觉的黄金标准。Ziapin2的另一个作用是抑制退化视网膜特有的强烈自发性振荡66–68,从而降低背景噪声,提高信噪比,进而增强信号识别能力。Ziapin2的电容机制在双极细胞(BCs)中可能非常有效,因为双极细胞主要通过膜电位的阈下振荡来工作,而不会产生动作电位(APs)。此外,双极细胞沿着入射光呈放射状分布,而除光感受器外的其他视网膜神经元则与光轴呈垂直排列。因此,由于这种结构差异,双极细胞每单位面积会吸收更多的光。
在视网膜网络水平上,Ziapin2对视网膜神经节细胞(RGCs)的兴奋性/抑制性输入的作用以及生理性RGC亚群的出现,意味着ON型和OFF型双极细胞(BCs)会被差异性激活。Ziapin2以高亲和力嵌入富含胆固醇的脂筏质膜中,在光刺激下,膜电容相对于暗环境值迅速下降约10–15%49。已知视杆/视锥-ON型双极细胞具有较长的轴突,可延伸至内网状层(IPL)最内侧部分(3–5层),而视锥-OFF型双极细胞的轴突则短得多,与内网状层1、2外层的OFF型视网膜神经节细胞相接触6–8,69,70。由于仅约50%的细胞电容来自胞体71,视杆/视锥-ON型双极细胞可能因整体细胞电容更高且膜上捕获的Ziapin2数量更多,而对Ziapin2的作用更敏感。视杆/视锥-ON型双极细胞经历的电容绝对降幅更大,这会引发更快的电压变化和更快的激活。即使视杆/视锥-ON型双极细胞与OFF型双极细胞的电容变化百分比可能没有显著差异,光诱发的膜时间常数减小也会影响电紧张性递减传导沿双极细胞轴突的速度,而这一速度与轴突长度相关。这可以解释为何具有较长轴突的ON型双极细胞会受到更显著的影响,而轴突较短的OFF型双极细胞则不会受到明显影响。ON型双极细胞选择性受影响的其他机制可能包括脂筏的差异性富集(Ziapin2对脂筏具有高亲和力49),或是视网膜神经元中表达的机械敏感通道72。事实上,最近的一项研究表明,Ziapin2通过引起膜变形,可调节HEK293细胞中过表达的TRAAK机械敏感钾通道73。
ON型和OFF型双极细胞(BCs)以及相关视网膜神经节细胞(RGCs)的特异性激活,其潜在机制之一可能涉及光诱导的视杆双极细胞和AII无长突细胞的激活,这些细胞通过甘氨酸能突触与OFF型双极细胞相连。此前有研究表明,该通路可通过光遗传学恢复ON-OFF反应74,75。使用士的宁拮抗AII无长突细胞抑制作用的实验显示,在Ziapin2的作用下,该机制仅占视网膜神经节细胞OFF反应的约三分之一,且可能存在其他依赖Ziapin2的抑制机制来实现ON/OFF信号分离。这些观察结果对于潜在的临床应用具有重要意义。事实上,位于视网膜周边的视杆双极细胞和AII无长突细胞的参与,能够扩大接受治疗患者的潜在视野,而其他抑制性连接的存在可能有助于在黄斑水平恢复生理性ON/OFF信号传导。最后,我们不能排除视杆/视锥-ON型和视锥-OFF型双极细胞中电压门控通道的差异表达,以及/或者在缺乏光感受器输入的情况下,视杆/视锥-ON型双极细胞的静息膜电位更去极化49。ON型双极细胞受光诱导的优先调制,可能会重新构建视网膜神经节细胞上兴奋性和抑制性输入的时间调谐,从而产生不同视网膜神经节细胞亚群的特定活动模式。值得注意的是,在退化视网膜中被Ziapin2激活的所有不同类型的视网膜神经节细胞,均与其在视网膜内丛状层(IPL)中的树突分层形态特征相符。
视网膜色素变性可由编码光感受器或视网膜色素上皮(RPE)细胞所表达蛋白的不同基因发生大量致病性突变引起,其变性进程各不相同,这使得通过基因治疗来彻底纠正基因病变极具挑战性。我们已证实,在光感受器表达基因Pde6B存在突变的rd10视网膜中,光诱发的视网膜回路活动可得到恢复52,53。6月龄时,这些小鼠的视杆细胞完全缺失,残留的视锥细胞胞体极少且缺乏外节,研究表明其反应性至少比野生型(WT)视锥细胞低两个数量级76,这与在高亮度下也缺乏光反应的情况一致。为了证明Ziapin2能够重新激活退化的视网膜,且不受引发光感受器退化的致病突变影响,我们还在RCS退化视网膜中测试了Ziapin2,该视网膜中RPE表达的Mertk基因存在突变54,这种突变会损害光感受器的维持和存活,并在人类中引发视杆-视锥细胞退化77。为此,我们使用了10月龄的粉红眼RCS大鼠,其视杆/视锥细胞在6月龄时已完全退化38,78。值得注意的是,我们完全复现了在rd10退化模型中获得的结果,包括对视网膜神经节细胞(RGC)放电的影响、不同RGC亚群的激活、突触电导的激活以及对突触阻滞剂的反应,这表明Ziapin2对任何失去光感受器和光敏感性的视网膜回路都具有活性。
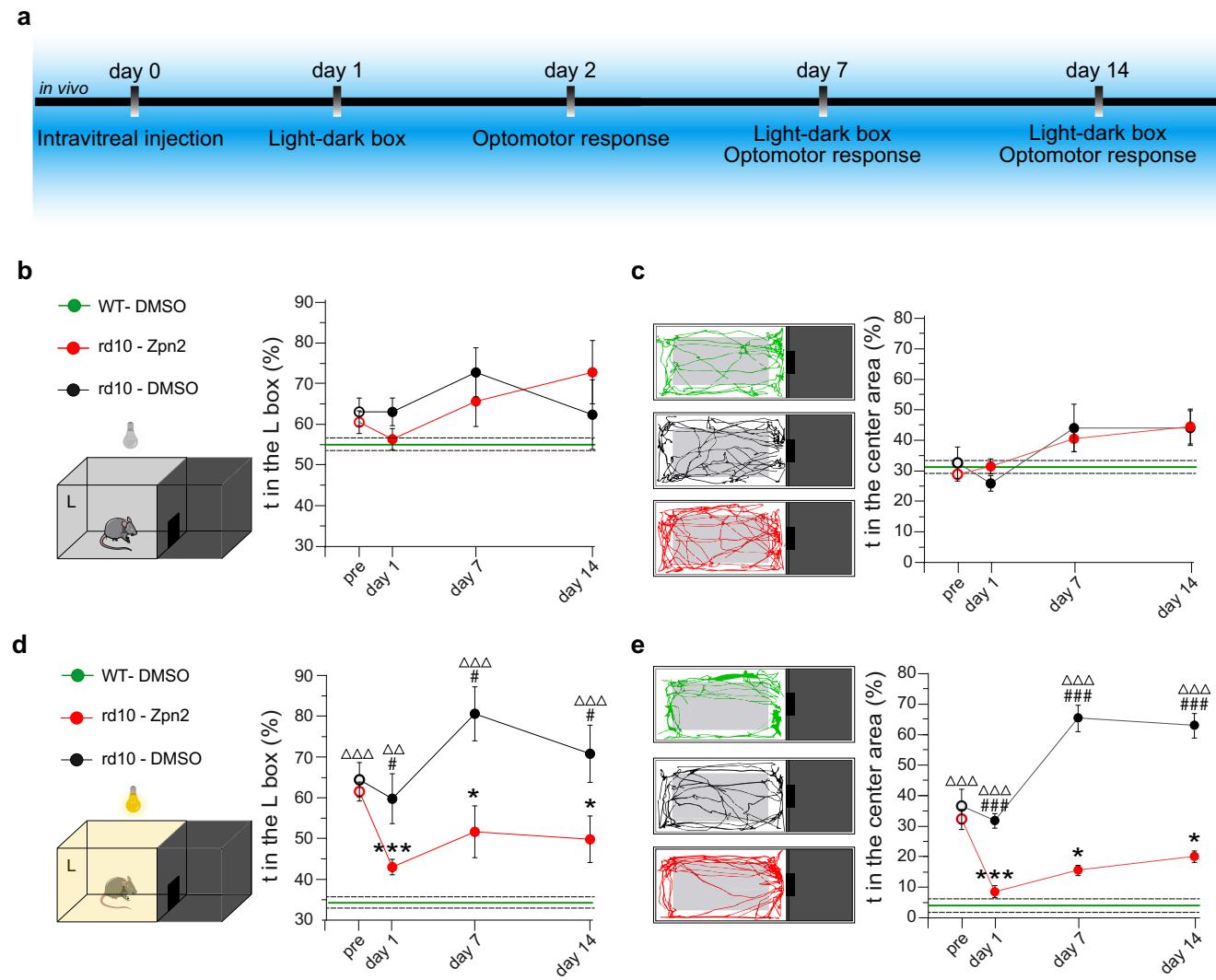
图7 | 在体内施用Ziapin2后,失明的rd10小鼠的光敏感性得以恢复。a 实验时间线,显示了对6月龄失明的rd10小鼠和年龄匹配的野生型(WT)小鼠进行的体内操作,这些小鼠接受了双侧玻璃体内注射溶媒或生理盐水配制的Ziapin2。b 完全置于黑暗中的明暗箱装置示意图。右侧的时间曲线显示了注射溶媒(二甲基亚砜;黑色)或Ziapin2(红色)的失明rd10小鼠在测试总时长内于左侧隔间(L)所花费时间的平均百分比(±标准误)。为便于比较,还显示了注射溶媒的WT小鼠(绿色;平均值±标准误)(平均值:实心水平线;标准误:虚线)。c (b)中所述三个实验组的小鼠在左侧隔间的代表性活动轨迹。右侧的时间曲线显示了在3分钟观察期内,小鼠在左侧隔间中心区域(灰色矩形)所花费时间的平均百分比(±标准误)。为便于比较,显示了注射溶媒的WT小鼠(绿色;平均值±标准误)。d 光照条件下(左侧隔间为5勒克斯白光)的装置示意图。右侧的时间曲线显示了三个实验组在3分钟测试内于光照隔间所花费时间的平均百分比(±标准误)。为便于比较,显示了注射溶媒的WT小鼠(绿色;平均值±标准误)。e (d)中所述三个实验组的小鼠在有光照的左侧隔间的代表性活动轨迹。右侧的时间曲线显示了小鼠在左侧隔间中心区域所花费时间的平均百分比(±标准误)。为便于比较,显示了注射溶媒的WT小鼠(绿色;平均值±标准误)。p < 0.05,p < 0.001,组内与“处理前”相比,单因素方差分析/邓尼特检验;#p < 0.05,##p < 0.01,###p < 0.001,与rd10/Ziapin2组相比,单因素方差分析/图基检验;ΔΔp < 0.01,ΔΔΔp < 0.001,与WT/二甲基亚砜组相比,单因素方差分析/图基检验(WT/二甲基亚砜,n = 7;rd10/二甲基亚砜,n = 14;rd10/Ziapin2,n = 18)。gp < 0.0001,双侧费希尔精确检验;##p < 0.01,###p < 0.001,双因素方差分析/霍尔姆-希达科检验(rd10小鼠/二甲基亚砜组和rd10小鼠/Ziapin2组均n = 3)。确切的p值和源数据见源数据文件。使用BioRender制作。Benfenati, F. (2024) https://BioRender.com/o06m024。
在完全失明的rd10小鼠体内进行给药后,单次玻璃体内注射Ziapin2能通过重新激活大量视网膜神经节细胞,在长达两周的时间里稳定恢复其光驱动行为和空间辨别能力。此外,我们证实Ziapin2无毒性,且不会在视网膜中引发促炎效应,这与我们之前在原代神经元和大脑皮层中的研究结果一致。在给药方式上,我们采用了在患者中广泛使用的微创玻璃体内注射,这表明Ziapin2能够轻松穿透内界膜到达视网膜内层神经元并发挥其生理作用。
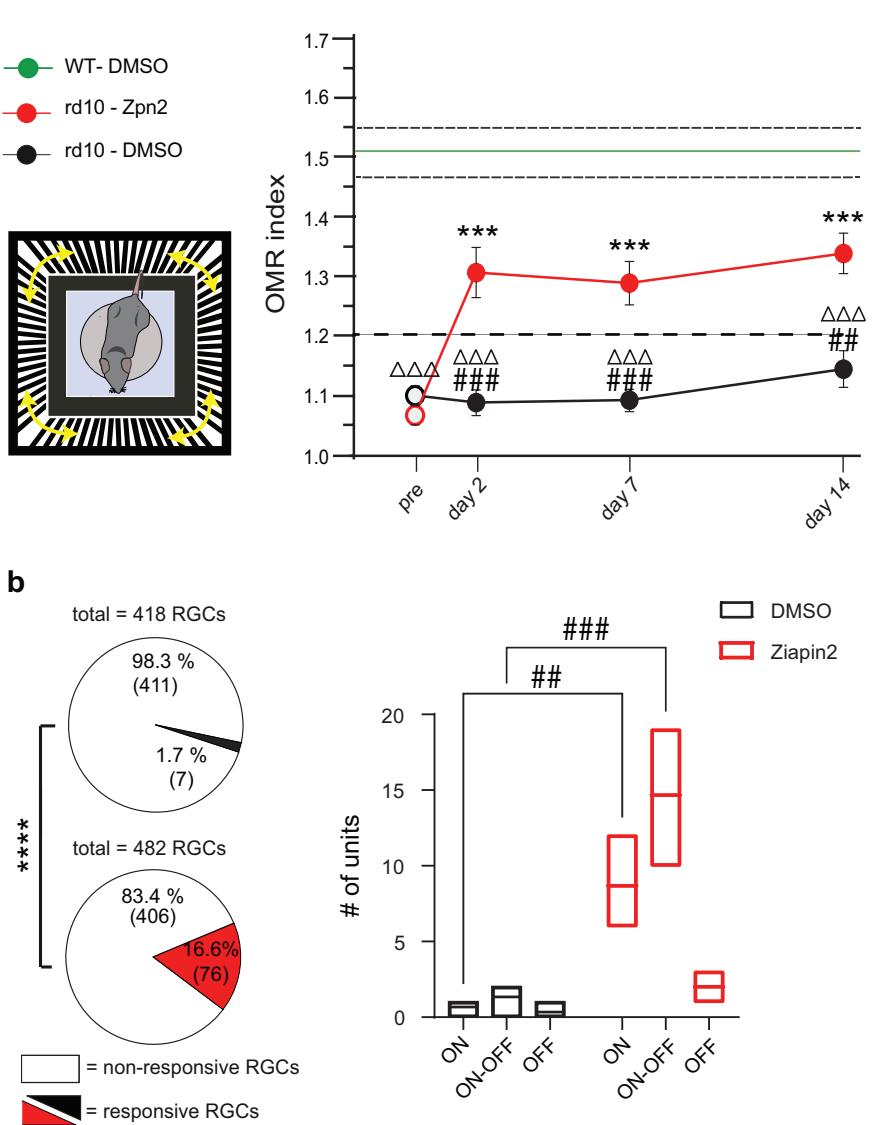
图8 | 在失明的rd10小鼠体内注射Ziapin2后,其视觉运动反应和视网膜神经节细胞的生理放电得以恢复。a左侧:视觉运动反应(OMR)装置的示意图。右侧:右侧的时间曲线显示了三个实验组在注射前(pre)和注射后的平均(±标准误)OMR峰值指数。OMR指数可区分可感知(>1.2)和不可感知(<1.2)的模式。为便于比较,还显示了注射溶媒的野生型(WT)小鼠(绿色;均值±标准误)。b在玻璃体内注射二甲基亚砜(DMSO)或Ziapin2两天后,使用高密度微电极阵列(HD-MEA)对rd10小鼠的视网膜外植体进行视网膜神经节细胞(RGCs)的细胞外记录。饼图显示了在记录的所有视网膜神经节细胞中,对全视野蓝光刺激(2毫瓦/平方毫米,500毫秒;上方为DMSO组,黑色部分;下方为Ziapin2组,红色部分)有反应的视网膜神经节细胞所占百分比。括号中为细胞的绝对数量。右侧的箱线图显示了根据对光的反应分类的有反应的ON型、ON-OFF型和OFF型视网膜神经节细胞的数量。箱线图的中线代表均值,箱内的方块代表中位数,箱体的边界代表第一和第三四分位数,须线代表最小值和最大值。a *p < 0.05,***p < 0.001,组内与“注射前”相比,采用单因素方差分析/邓尼特检验;#p < 0.05,##p < 0.01,###p < 0.001,与rd10/Ziapin2组相比,采用单因素方差分析/图基检验;ΔΔp < 0.01,ΔΔΔp < 0.001,与WT/DMSO组相比,采用单因素方差分析/图基检验(WT/DMSO组,n = 7;rd10/DMSO组,n = 14;rd10/Ziapin2组,n = 18)。b ****p < 0.0001,采用双侧费希尔精确检验;##p < 0.01,###p < 0.001,采用双因素方差分析/霍尔姆-希达科检验(rd10小鼠/DMSO组和rd10小鼠/Ziapin2组均为n = 3)。确切的p值和源数据见源数据文件。使用BioRender制作。Benfenati, F. (2024) https://BioRender. com/i45t231。
另一种靶向唯一的视杆/视锥-ON双极细胞的策略是光遗传学,其使用特定的Grm6启动子79,80(综述参见81)。然而,视杆/视锥-ON双极细胞的基因靶向远非理想,尤其是在退化的视网膜中82。因此,在视杆/视锥-ON双极细胞的基因靶向与视网膜神经节细胞中不依赖其表型的通用视蛋白表达之间,视觉恢复方面并未出现显著差异65,83。作为一种光致变色分子,Ziapin2可以与其他用于神经元刺激的光药理学工具进行基准比较。Isacoff团队率先研发的那些工具使谷氨酸受体可被紫外光光切换,但需要对通道进行基因修饰,以使其能与偶氮苯-谷氨酸激活剂形成共价键(综述参见参考文献84)。最近,Kramer及其合作者率先研发的一系列衍生偶氮苯类化合物(包括AAQ、DENAQ、BENA Q、DAD)——目前处于Ⅰ/Ⅱ期临床试验阶段85——被发现可进入视网膜神经节细胞,并通过从细胞内侧阻断钾离子通道来介导其光诱导激活(综述参见参考文献86)。虽然这些分子大多靶向视网膜的最终输出,而不考虑生理性ON/OFF处理,但有报道称DAD至少在一定程度上可调节双极细胞的活动,主要引发ON反应,极少引发OFF反应87。相反,Ziapin2不影响内源性离子通道,主要靶向双极细胞,并能重新激活视网膜神经节细胞中的兴奋性和抑制性突触电流,促进生理性视网膜神经节细胞亚群的重新出现,这可能对诱导功能性视力的持续恢复至关重要83。考虑到其潜在的治疗用途,Ziapin2治疗仍存在一些局限性,例如在光谱的绿/红区域缺乏光谱敏感性(这可能需要使用护目镜)、在生理溶液中的部分溶解性,以及由于膜更新导致的生理效应时间限制49。目前正在进行进一步研究,以生成水溶性和红移的Ziapin2衍生物,并对该分子进行封装,以实现安全且持久的递送。
总之,我们已经证明,Ziapin2凭借其两亲性,能够嵌入所有视网膜神经元,并在视网膜色素变性(RP)临床前模型的退化视网膜中恢复视觉信息的生理复杂网络处理。Ziapin2不仅恢复了具有不同病理机制的完全退化视网膜的光敏感性,还重新激活了负责对比度敏感性和空间分辨的生理性ON/OFF处理,使得多种类似于正常视网膜的视网膜神经节细胞(RGC)反应得以出现。Ziapin2恢复视网膜神经节细胞亚群选择性激活的显著能力表明,这种以创新光转导机制为特征的分子,有望优于目前正在进行视网膜色素变性治疗临床试验的现有假体、光遗传学或光药理学疗法。
¶ 方法
¶ 伦理审批和动物处理
所有动物处理和实验方案均符合欧洲共同体制定的指南(2014年3月4日第2014/26/EU号指令),并获得了意大利卫生部的批准(批准号:357/2019-PR)。本研究使用了野生型C57Bl6/J小鼠以及C57Bl6/J背景的纯合rd10小鼠。种鼠购自杰克逊实验室(美国缅因州巴尔港)。粉红眼RCS营养不良大鼠和非营养不良的正常视力对照大鼠(RDY)由M.M. La Vail博士(美国加利福尼亚大学旧金山分校贝克曼视觉中心)友好提供。动物饲养于标准条件下,采用12/12小时光暗循环,食物和水自由摄取。通过随机选择实验组,使6月龄小鼠和10月龄大鼠的雌雄比例保持平衡。
¶ 视网膜外植体的制备
小鼠视网膜外植体取自6月龄、背景为C57Bl6/J的野生型(WT)和纯合rd10小鼠。大鼠视网膜外植体取自10月龄的RDY大鼠和RCS大鼠。实验动物先进行至少60分钟的暗适应,随后通过吸入二氧化碳处死后进行颈椎脱臼。为保持暗适应状态,在昏暗红光下摘除眼球,并将其转移至含有经碳氧混合气体处理的Ames培养基(美国生物公司,产品编号A1372-25)的培养皿中。移除角膜后,将眼杯切成两半,使视网膜与巩膜分离。进行膜片钳记录时,将视网膜感光细胞面朝下放置在记录室中,并转移至Eclipse FN1显微镜载物台(尼康欧洲公司,荷兰阿姆斯特丹),用红外光照明,通过连接电荷耦合器件(CCD)相机的监视器进行观察。视网膜持续用经碳氧混合气体处理的Ames培养基灌注。为暴露目标视网膜神经节细胞(RGC),用膜片钳电极移除上方的内界膜。
¶ 膜片钳记录和视觉刺激方案
使用Axopatch 200B放大器(Molecular Devices公司,美国加利福尼亚州圣何塞)对视网膜神经节细胞(RGCs,胞体直径≥20μm)进行全细胞和细胞贴附式膜片钳记录。在对正常视力对照组和失明视网膜外植体进行电流钳记录(I=0)时,硼硅酸盐膜片钳电极(最终电阻4.5–6.0 MΩ)内填充的溶液成分(单位:mM)为:126葡萄糖酸钾、4氯化钠、0.02氯化钙、0.1 BAPTA、0.1 EGTA-氢氧化钾、1硫酸镁、15葡萄糖、3三磷酸腺苷二钠、0.1三磷酸鸟苷钠、5 HEPES,pH 7.3。为记录光诱发的突触电流(失明视网膜外植体),将细胞电压钳制在-86 mV至+34 mV的范围内,电压阶跃为24 mV。对于这些记录,膜片钳电极(最终电阻5.0–7.0 MΩ)内填充的细胞内溶液成分(单位:mM)为:120甲烷磺酸铯、4氯化钠、0.02氯化钙、1硫酸镁、0.1 EGTA-氢氧化铯、10磷酸肌酸、3三磷酸腺苷二钠、0.1三磷酸鸟苷钠、10 HEPES,用氢氧化铯调节pH至7.3。通过向细胞内溶液中添加5 mM QX-314来阻断电压门控钠电流。根据先前描述的方法88–91,将总光诱发电导分解为兴奋性和抑制性成分。
在从视力正常的C57Bl6/J小鼠分离出的视网膜外植体上进行膜片钳实验时,记录了基础光诱发的视网膜神经节细胞(RGC)对青色和绿色闪光的放电活动,并将其与通过一根置于被膜片钳记录的RGC胞体附近的第二根硼硅酸盐玻璃电极(最终电阻1.0-1.2兆欧)在Ames培养基中施加200微摩尔Ziapin2或10%二甲基亚砜(DMSO)2分钟后,相同刺激方案下的光诱发反应进行比较。对于从纯合rd10小鼠和RCS大鼠分离出的失明视网膜外植体中RGC的膜片钳记录,视网膜从巩膜分离后,立即在含10微摩尔Ziapin2/0.5% DMSO的2毫升离心管中,用含碳氧合的Ames培养基孵育30分钟。
在急性 puff 施加 200 µM Ziapin2 后,通过施加 -5 mV 的电压阶跃,测量了 Ziapin2 和光诱导的视网膜神经节细胞(RGCs)膜电容(Cm)和膜电阻(Rm)的变化。电极输入电阻始终进行补偿。使用 Origin 软件计算电容电流面积(Q)。膜电容(Cm)的计算公式为 Cm = Q/ΔV。在施加 5 mV 电压阶跃期间,通过绿色或青色光(200 ms)照射来测量细胞膜电容的光依赖性变化,并与在黑暗中施加相同 5 mV 电压阶跃所获得的膜电容(Cm)进行比较。采用相同的实验方案测量膜电阻(Rm),其计算公式为 Rm = ΔV/I。
视觉刺激由500毫秒的彩色圆形光点闪烁组成(直径50微米),这些光点由SPECTRA X光源引擎产生,并通过显微镜光学系统聚焦到被膜片钳记录的视网膜神经节细胞上。记录了对不同光谱输出(青色,波长=470纳米;绿色,544纳米)在功率密度依次增加(2、10、20和30毫瓦/平方毫米)时的刺激诱发活动。将Alexa Fluor 633(50微米)添加到两种细胞内溶液中,用于细胞识别和形态重建。
¶ 电生理记录分析
刺激时间直方图(PSTHs)的构建方法是:记录光诱发的放电活动(50毫秒 bins:动作电位计数),时间窗口为从光刺激开始到光刺激结束后500毫秒(ON细胞),或者从光刺激结束到之后1秒(OFF细胞)。光诱发的动作电位计数在15次扫描中取平均值,并以光刺激前1.5秒内的自发动作电位计数(50毫秒 bins)进行标准化。放电率采用核平滑法计算,使用高斯核(σ=25毫秒),通过Python 3编写的自制程序实现。峰值放电率定义为(A1−A2)/(A1+A2),其中A1是在黑暗中测得的最大反应振幅,A2是在500毫秒光刺激期间(ON细胞)或光刺激结束后1秒时间窗口内(OFF细胞)测得的最大反应振幅。在动作电位波形分析中,使用给予Ziapin2/二甲基亚砜后出现的第一个自发动作电位和第一个光诱发动作电位,构建电压时间导数(dV/dt)与电压的关系图(相平面图),并与基础状态下(即给予Ziapin2/二甲基亚砜前)第一个自发动作电位的相平面图进行比较。通过该图提取最大上升斜率、最大复极化斜率和动作电位峰值。在膜电位调制分析中,对全细胞电流钳记录的轨迹进行分析:在500毫秒光刺激开始后的1.5秒时间窗口内应用低通滤波器;对于15次扫描中的每一次,在50毫秒的 bins 内计算滤波后的平均膜电位值,并以最小值(黑色方块,min)和最大值(白色方块,max)进行标准化。
¶ 视网膜神经节细胞的形态重建
膜片钳实验结束后,将视网膜在含4%多聚甲醛的磷酸盐缓冲盐水(PBS)中于室温(RT)固定30分钟,然后用0.1M PBS洗涤3次,每次10分钟。如前所述55,固定后的视网膜随后在双苯甲亚胺(Hoechst 33342,1:300;Sigma-Aldrich)存在下于室温孵育30分钟,并再次洗涤(3次,每次10分钟)。组织样本用Mowiol(Sigma-Aldrich)封片于两个玻璃盖玻片之间。使用配备超分辨率LAS-X Lightning去卷积软件的SP8/HyD共聚焦显微镜(徕卡显微系统,德国韦茨拉尔)对整装视网膜进行成像。
¶ 高密度微电极阵列记录和视觉刺激方案
使用基于CMOS的高密度微电极阵列(HD-MEA)对视网膜神经节细胞(RGCs)的光诱发动作电位(APs)进行胞外记录,该设备可同时从4096个电极(BioCam X,3Brain公司,瑞士瓦登斯维尔)进行记录。在离体实验中,视网膜在记录前先在含有10μM Ziapin2的埃姆斯培养基中孵育;对于经眼内注射Ziapin2处理的视网膜,在手术后两天取出组织,直接用于胞外记录。将新鲜分离的视网膜(参见视网膜外植体制备)切成两半,将半视网膜感光细胞面朝上放置在预先涂有多聚-DL-鸟氨酸氢溴酸盐(5mg/ml;Sigma-Aldrich公司)的HD-MEA(Arena Chip,3Brain公司)表面,以改善视网膜神经节细胞与记录电极的接触。所有实验均在暗室中于室温下进行。光刺激由Lumencor Spectra-X光源(Optoprim公司,意大利维梅卡泰)产生的全视野青色或绿色闪光(250和500毫秒)组成,闪光频率为0.25Hz。通过Z16 APO显微镜(徕卡显微系统)将光斑聚焦在组织样本上,最终功率密度范围为0.003至2mW/mm²。在相同实验条件(即刺激持续时间和功率密度)下,通过重复20-60次扫描记录视网膜神经节细胞的光诱发反应。采集的数据通过3Brain程序提供的基于Henning排序的算法92进行 spike 分选和峰值检测。通过对处理后数据的后续人工监督,排除噪声信号的错误采样。当神经元在光刺激下的放电活动增加到超过“平均自发放电率加2×标准差”这一放电阈值时,被归类为“反应性视网膜神经节细胞”;其余神经元被视为“无反应性”,并排除在分析之外。
ON、ON-OFF和OFF反应分别被计算为光刺激期间或刺激结束后500毫秒内放电活动的增加,其极性通过人工监督确认。为了阻断向视网膜神经节细胞(RGCs)的突触输入并研究光诱发放电活动的起源,分别通过含氧的Ames培养基灌注应用10μM的6-氰基-7-硝基喹喔啉-2,3-二酮(CNQX;Tocris,英国布里斯托尔)、20μM的L-(+)-2-氨基-4-膦酰基丁酸(L-AP4,Tocris)或10μM的盐酸士的宁(Sigma-Aldrich),持续时间分别为15分钟、5分钟和10分钟。开发了自定义的Matlab(MathWorks,美国马萨诸塞州纳蒂克)代码,用于对采集的数据进行进一步的离线分析。
¶ 眼内注射
6月龄的rd10盲鼠和年龄匹配的野生型(WT)小鼠(雌雄不限)在手术显微镜下通过鼻锥吸入1.5%异氟烷进行麻醉。注射前,用1%托吡卡胺滴眼液(VISUfarma SpA,意大利罗马)扩瞳,并用4%盐酸奥布卡因滴眼液(Alfa Intes,意大利卡索里亚)进行局部麻醉。使用10μl NanoFil注射器(NANOFIL,World Precision Instruments,美国佛罗里达州萨拉索塔)装入800μM Ziapin2或溶媒(40%二甲基亚砜生理盐水溶液),并连接到带有34号钝针的眼内注射套件(IO-KIT,World Precision Instruments)。注射前,用30号针头刺穿结膜,以更好地进入玻璃体腔。在手术显微镜(M651 Leica Microsystems)载物台下方,使用微量注射器(UMP3T-1,World Precision Instruments)以200 nl/s的控制流速向每只小鼠的双眼玻璃体内各注射1μl上述溶液,最终玻璃体中Ziapin2的浓度为200μM(含10%二甲基亚砜)。注射后立即向眼内滴入妥布霉素地塞米松(0.3% + 0.1%,TobraDex®,爱尔康,意大利米兰)和0.2%卡波姆(Lacrigel®,Dompè,意大利米兰)溶液,分别用于预防手术相关感染和角膜脱水。眼部手术后,将动物单独置于黑暗环境中1小时,以避免应激和不适,并让其从麻醉中恢复。
¶ 明暗箱实验
眼内注射后,研究人员使用一种由两个相连腔室组成的装置测试小鼠的光敏感性:一个是“光箱”,其壁为透明的;另一个是“暗箱”,其壁为黑色的,以此营造一个受保护的隐蔽空间。该测试基于小鼠躲避强光区域的本能行为,而对黑暗区域的偏好是生理光感知的一个指标。实验装置被放置在一个黑暗的实验室中,在测试前,小鼠需适应黑暗环境1小时。测试开始时,先将小鼠放在“光室”中央,在黑暗环境中放置3分钟,然后在箱子上方开启5勒克斯强度的受控光源。在两种光照条件下进行的视频记录,使我们能够监测小鼠在整个光室及其中心区域所花费的时间。为了评估Ziapin2在恢复个体光敏感性方面的功效,研究人员在注射前15天对小鼠进行了该测试,以比较眼内手术前后的表现。
¶ 视动反应(OMR)
为了研究失明小鼠和野生型注射小鼠的空间/模式感知能力,我们研究了它们对不同空间频率移动模式的眼动反应(OMR)。眼动反应装置(PhenoSys GmbH,德国柏林)由一个立方体盒子组成,盒子中央有一个升高的圆形平台,不受约束的小鼠被放置在该平台上,周围有四个液晶显示屏。视觉刺激包括在四个屏幕上投射具有不同空间频率的黑白条纹的移动光栅图案,以创建一个虚拟圆柱体。盒子底部的镜子营造出无限深度的光学错觉。在中心位置,视力正常的动物会随着视觉刺激同步移动头部。一台摄像机放置在动物上方,用于自动追踪其身体/头部对移动光栅图案的反应运动,同时软件利用这些信息确定视觉阈值(眼动反应评分61,62)。我们设计了一个虚拟刺激方案来评估注射Ziapin2后rd10小鼠的表现,该方案包括随机呈现的0.05、0.1、0.15、0.2、0.25、0.3、0.35、0.375、0.4、0.45和0.5周/度的空间频率。每个空间频率以12°/秒的速度呈现60秒,中间穿插3秒的全视野灰色刺激。注射载体的年龄匹配rd10小鼠和野生型小鼠被用作对照组。1.2分被用作定量识别失明和光敏感动物的临界值:眼动反应指数低于该值的动物被认为无法感知特定的空间频率。将每只实验动物和对照动物玻璃体内注射后的最高眼动反应指数与其注射前的最佳表现进行了比较。
¶ 视网膜组织化学
对小鼠进行体内处理,通过眼内注射Ziapin2或溶媒,两天后取出视网膜并在含4%多聚甲醛(Sigma-Aldrich)的0.1M PBS中固定过夜,随后用0.1M PBS冲洗,经15–30%蔗糖梯度进行冷冻保护,包埋于OCT冷冻介质(Tissue-Tek;Qiagen,米兰,意大利)中,使用MC5050低温切片机(Histo-Line Laboratories)将其冷冻切片为25μm厚。横向切片被装片于明胶包被的载玻片上,在处理前储存于-20°C。切片首先在室温下用10%正常山羊血清(NGS,Sigma-Aldrich)孵育1小时,以阻断非特异性抗体结合,然后在4°C下与以下一抗孵育过夜:兔抗视紫红质(1:500;Abcam,货号ab221664)、兔抗视锥细胞抑制蛋白(1:500;Merck-Millipore,货号AB15282)、豚鼠抗GFAP(1:500;Synaptic Systems,货号173011)和兔抗Iba1(1:250;Wako,货号01919741)。Alexa Fluor 488和568偶联的二抗(Alexa 488山羊抗豚鼠和Alexa 568山羊抗兔;ThermoFisher)稀释1:100后,在室温下孵育1小时。切片用0.1M PBS冲洗三次以去除多余抗体,并用Mowiol(Sigma-Aldrich)封片。使用SP8/HyD共聚焦显微镜(Leica Microsystems)对视网膜切片进行成像。为便于比较,整个成像过程中的采集参数保持一致。定量分析采用ImageJ软件(NIH,贝塞斯达,马里兰州)进行,对锥细胞抑制蛋白、视紫红质和Iba1进行细胞计数,对GFAP进行整合免疫反应性分析。
¶ 统计分析
计划实验所需的样本量(n)是通过G*power软件针对方差分析(ANOVA)预先确定的。确定时参考了类似实验和初步数据,设定效应量为0.25–0.40,I类错误(α)为0.05,1-ß(即检验效能,其中ß为II类错误)为0.9。实验数据以均值±标准误(SEM)表示,或用箱线图表示(中线代表中位数,方形符号代表均值,箱体范围为第25–75百分位数,须线长度代表最小/最大数据点),其中n表示神经元数量(体外实验)或个体动物数量(体内实验)。实验数据的正态分布通过D’Agostino–Pearson正态性检验或Shapiro–Wilk正态性检验进行评估。根据样本的配对情况和正态分布与否,采用双尾配对Student t检验或Wilcoxon符号秩检验比较两组样本。对于两组以上的正态分布样本组,采用单因素或双因素方差分析(ANOVA),随后进行Dunnett、Tukey或Holm-Šídák事后多重比较检验。对于两组以上的非正态分布样本组,采用单因素Kruskal–Wallis方差分析,随后进行Dunn多重比较检验。列联表的统计分析采用Fisher精确检验。统计学显著性标准为p < 0.05。统计分析使用OriginPro2020 SR1和GraphPad Prism 8.3.0软件进行。
¶ 报告摘要
有关研究设计的更多信息,请参见本文所链接的《自然》系列期刊报告摘要。
¶ 数据可用性
本研究中生成的数据已在源数据文件中提供。源数据随本文一同提供。
¶ 代码可用性
在Matlab环境中定制的代码托管于意大利理工学院,并可在公共的IIT“gitlab”代码库中获取,地址为[https://gitlab.iit.it/nbt008-public/retina-hd-mea-public]。
¶ 参考文献
- Goetz, J. 等人. 利用功能、形态和基因表达对小鼠视网膜神经节细胞进行统一分类. 《细胞报告》, 40, 111040 (2022).
- 马斯兰, R. H. 视网膜的细胞群:普罗克特演讲. 《眼科研究与视力学》, 52, 4581 (2011).
- Baden, T. 等人. 小鼠视网膜神经节细胞的功能多样性. 《自然》, 529, 345–350 (2016).
- 马斯兰, R. H. 视网膜的神经元组织. 《神经元》, 76, 266–280 (2012).
- Rossi, E. A., Roorda, A. 人类中央凹视觉分辨率与视锥细胞间距的关系. 《自然·神经科学》, 13, 156-157 (2009).
- Wässle, H. 哺乳动物视网膜中的并行处理. 《自然综述·神经科学》, 5, 747–757 (2004).
- Wässle, H. 等人. 哺乳动物视网膜中的甘氨酸能传递. 《分子神经科学前沿》, 2, 6 (2009).
- Euler, T., Haverkamp, S., Schubert, T., Baden, T. 视网膜双极细胞:视觉的基本组成单元. 《自然综述·神经科学》, 15, 507-519 (2014).
- Pascolini, D., Mariotti, S. P. 全球视力障碍估计:2010年. 《英国眼科学杂志》, 96, 614-618 (2012).
- Parmeggiani, F. 等人. 视网膜色素变性:基因与疾病机制. 《当代基因组学》, 12, 238-249 (2011).
- Provis, J. M., Penfold, P. L., Cornish, E. E., Sandercoe, T. M., Madigan, M. C. 黄斑的解剖与发育:特殊性及对黄斑变性的易感性. 《临床与实验眼科学》, 88, 269-281 (2005).
- 米川由香里, 金一奎. 与年龄相关的黄斑变性的临床特征和当前治疗. 《冷泉港医学展望》, 5, a017178 (2014).
- 米内川洋, Miller J.W., 金I.K. 年龄相关性黄斑变性:管理与诊断的进展. 《临床医学杂志》, 4, 343-359 (2015).
- Trapani, I., Banfi, S., Simonelli, F., Surace, E. M., Auricchio, A. 遗传性视网膜变性的基因治疗:前景与挑战. 《人类基因治疗》, 26, 193-200 (2015).
- Maguire, A. M. 等人. 基因转移治疗利伯先天性黑矇的安全性和有效性. 《新英格兰医学杂志》, 358, 2240-2248 (2008).
- Bennett, J., Chung, D. C., Maguire, A. 视网膜的基因递送:从小鼠到人类. 《酶学方法》, 507, 255-274 (2012).
- Ziccardi, L. 等人. 视网膜营养不良的基因治疗. 《国际分子科学杂志》, 20, 5722 (2019).
- Scholl, H. P. N. 等人. 遗传性视网膜变性的新兴疗法. 《科学·转化医学》, 8, 368rv6 (2016).
- Zarbin, M. 基于细胞的退行性视网膜疾病治疗. 《分子医学趋势》, 22, 115–134 (2016).
- Morizur, L., Herardot, E., Monville, C., Ben M’Barek, K. 人类多能干细胞:理解和治疗视网膜变性的工具箱. 《分子细胞神经科学》, 107, 103523 (2020).
- Nair, D. S. R., Thomas, B. B. 基于干细胞的视网膜退行性疾病治疗策略. 《当代干细胞研究与治疗》, 17, 214-225 (2022).
- Maeda, A., Mandai, M., Takahashi, M. 视网膜疾病的基因与诱导多能干细胞治疗. 《基因组学与人类遗传学年度综述》, 20, 201-216 (2019).
- Mandai, M. 等人. 用于黄斑变性的自体诱导干细胞来源视网膜细胞. 《新英格兰医学杂志》, 376, 1038–1046 (2017).
- Simunovic, M. P. 等人. 视觉恢复的光遗传学方法. 《实验眼科学研究》, 178, 15-26 (2019).
- Sahel, J. A. 等人. 光遗传学治疗后失明患者视觉功能的部分恢复. 《自然-医学》, 27, 1223-1229 (2021).
- Dagnelie, G. 视网膜植入物:一个多学科领域的兴起. 《当代神经病学观点》, 25, 67–75 (2012).
- Bloch, E., Luo, Y., da Cruz, L. 视网膜假体系统的进展. 《眼科治疗进展》, 11, 251584141881750 (2019).
- Weiland, J. D., Cho, A. K., Humayun, M. S. 视网膜假体:当前临床结果与未来需求. 《眼科学》, 118, 2227-2237 (2011).
- Stingl, K. 等人. 新型电子视网膜下植入物alpha AMS在15例遗传性视网膜变性致盲患者中的多中心试验中期结果. 《神经科学前沿》, 11, 445 (2017).
- Maya-Vetencourt, J. F. 等人. 一种全有机视网膜假体可恢复退行性失明大鼠模型的视力. 《自然·材料》, 16, 681-689 (2017).
- Ghezzi, D. 等人. 一种聚合物光电子接口恢复了失明大鼠视网膜的光敏感性. 《自然·光子学》, 7, 400–406 (2013).
- Benfenati, F., Lanzani, G. 用于开发第二代视网膜假体的新技术. 《实验动物》, 47, 71–75 (2018).
- Ghezzi, D. 等人. 一种用于神经元光激活的混合生物有机界面. 《自然·通讯》, 2, 166 (2011).
- Manfredi, G., Colombo, E., Bassotti, J., Benfenati, F., Lanzani, G. 有机视网膜假体的光化学. 《物理化学年度评论》, 70, 99–121 (2019).
- Lorach, H. 等人. 具有高视敏度的光伏视觉恢复. 《自然·医学》, 21, 476–482 (2015).
- Benfenati, F., Lanzani, G. 纳米颗粒用于神经刺激的临床转化. 《自然综述·材料》, 6, 1–4 (2020).
- Maya-Vetencourt, J. F. 等人. 视网膜下注射半导体聚合物纳米颗粒可恢复视网膜营养不良大鼠模型的视力. 《自然·纳米技术》, 15, 698–708 (2020).
- Francia, S. 等人. 光诱导的聚合物纳米颗粒中的电荷产生可恢复晚期视网膜色素变性大鼠的视力. 《自然·通讯》, 13, 3677 (2022).
- Bianco, A., Perissinotto, S., Garbugli, M., Lanzani, G., Bertarelli, C. 通过光致变色控制光学特性:一种很有前景的光子学方法. 《激光与光子学评论》, 5, 711-736 (2011).
- Zhang, J., Wang, J., Tian, H. 听从光的指令:光致变色生物材料的研究进展. 《材料展望》, 1, 169–184 (2014).
- Mourot, A. 等人. 光致变色离子通道阻滞剂的调节. 《ACS化学神经科学》, 2, 536–543 (2011).
- Bléger, D., Hecht, S. 可见光激活分子开关. 《德国应用化学(国际版)》, 54, 11338–11349 (2015).
- Tochitsky, I. 等人. 偶氮苯光开关如何恢复失明视网膜的视觉反应. 《神经元》, 92, 100–113 (2016).
- Laprell, L. 等人. 使用光致变色AMPA受体激动剂恢复失明视网膜的光敏感性. 《ACS化学神经科学》, 7, 15–20 (2016).
- Polosukhina, A. 等人. 盲鼠视觉反应的光化学恢复. 《神经元》, 75, 271–282 (2012).
- Kramer, R. H., Mourot, A., Adesnik, H. 用于控制天然神经元信号蛋白的光遗传药理学. 《自然·神经科学》, 16, 816-823 (2013).
- Fortin, D. L. 等人. 内源性离子通道和细胞兴奋性的光化学控制. 《自然·方法》, 5, 331–338 (2008).
- Tochitsky, I., Trautman, J., Gallerani, N., Malis, J. G., Kramer, R. H. 利用一种高效、安全且持久的光开关恢复失明视网膜的视觉功能. 《科学报告》, 7, 45487 (2017).
- DiFrancesco, M. L. 等人. 膜靶向光开关对神经元放电的调节. 《自然·纳米技术》, 15, 296–306 (2020).
- Paterno, G. M. 等人. 膜内光致动器对模型膜和完整细胞中磷脂动力学的影响. 《Langmuir》, 36, 11517–11527 (2020).
- Paternò, G. M. 等人. 膜环境使两亲性偶氮苯能够超快速异构化. 《先进科学》, 7, 1903241 (2020).
- Wert, K. J., Lin, J. H., Tsang, S. H. 视网膜变性的一般病理生理学. 《发育眼科学》, 53, 33-43 (2014).
- LaVail, M. M., Battelle, B. A. 眼色素沉着和光剥夺对大鼠遗传性视网膜营养不良的影响. 《实验眼科学研究》, 21, 167-192 (1975).
- Roska, B., Werblin, F. S. 哺乳动物视网膜中十个平行堆叠表征间的垂直相互作用. 《自然》, 410, 583–587 (2001).
- Ferrea, E. 等人. 利用微电子多电极阵列对脑切片中场电位进行大规模、高分辨率电生理成像. 《神经电路前沿》, 6, 80 (2012).
- Volpi, R. 等人. 使用受限玻尔兹曼机对视网膜神经节细胞群进行建模. 《科学报告》, 10, 16549 (2020).
- Sabharwal, J., Seilheimer, R. L., Cowan, C. S., Wu, S. M. ON交叉电路塑造小鼠OFF视网膜神经节细胞中心和周围的时空分布. 《神经回路前沿》, 10, 231391 (2016).
- Borghuis, B. G., Looger, L. L., Tomita, S., Demb, J. B. kainate受体介导小鼠视网膜中瞬时和持续性OFF双极细胞通路的信号传导. 《神经科学杂志》, 34, 6128-6139 (2014).
- Bourin, M., Hascoët, M. 小鼠明暗箱实验. 《欧洲药理学杂志》, 463, 55–65 (2003).
- Kretschmer, F., Kretschmer, V., Kunze, V. P., Kretzberg, J. OMRarena:基于视觉运动反应确定小鼠视觉阈值的自动化测量和刺激系统. 《公共科学图书馆·综合》, 8, e78058 (2013).
- Kretschmer, F., Sajgo, S., Kretschmer, V., Badea, T. C. 一种测量小鼠视动反应和视觉运动反应的系统. 《神经科学方法杂志》, 256, 91-105 (2015).
- Bassetto, C. A. Z. 等人. 光脂质激发触发去极化光电容电流和动作电位. 《自然·通讯》, 15, 1139 (2024).
- Cehajic-Kapetanovic, J., Singh, M. S., Zrenner, E., MacLaren, R. E. 修复视力的生物工程策略. 《自然-生物医学工程》, 7, 387-404 (2023).
- Gilhooley, M. J. 等人. 视觉恢复的光遗传学方法的系统比较. 《分子治疗:方法与临床开发》, 25, 111-123 (2022).
- Denlinger, B. 等人. 局部光感受器退化导致视网膜神经元的局部病理生理重塑. 《JCI洞察》, 5, e132114 (2020).
- Biswas, S. 等人. rd10视网膜内在神经元振荡的药理学分析. 《公共科学图书馆·综合》, 9, e99075 (2014).
- 屠汉阳, 陈盈君, McQuiston, A. R., 乔超群, 陈正光. 一种常染色体显性遗传性光感受器变性小鼠模型中的新型视网膜振荡机制. 《细胞神经科学前沿》, 9, 513 (2016).
- Tsukamoto, Y., Omi, N. 小鼠视网膜双极细胞的分类:与视杆驱动的aII无长突细胞通路相关的类型特异性连接. 《神经解剖学前沿》, 11, 1-25 (2017).
- Werginz, P., Benav, H., Zrenner, E., Rattay, F. 模拟ON型和OFF型视网膜双极细胞在电刺激下的反应. 《视觉研究》, 111, 170-181 (2015).
- Oltedal, L., Veruki, M. L., Hartveit, E. 视网膜视杆双极细胞的被动膜特性和电紧张信号处理. 《生理学杂志》, 587, 829–849 (2009).
- 庞晶晶. 视网膜神经元中机械敏感离子通道的多样性. 《国际分子科学杂志》, 25, 4877 (2024).
- Moschetta, M. 等人. 膜靶向非遗传性光开关对机械敏感钾通道的调控. 《物理化学杂志B》, 127, 8869–8878 (2023).
- Macé, E. 等人. 通过玻璃体内注射AAV将视紫红质通道蛋白-2靶向到ON双极细胞可恢复失明小鼠的ON和OFF视觉反应. 《分子治疗》, 23, 7-16 (2015).
- Khabou, H. 等人. 光遗传学靶向aII无长突细胞可恢复内视网膜执行的视网膜计算. https://doi.org/10.1016/j.omtm.2023.09.003 (2023).
- Ellis, E. M. 等人. 圆锥细胞和圆锥细胞通路在晚期视网膜变性中仍保持功能. 《当代生物学》, 33, 1513–1522.e4 (2023).
- Yang, S., Zhou, J., Li, D. 视网膜色素上皮的功能与疾病. 《药理学前沿》, 12, 727870 (2021).
- Lorach, H. 等人. 在与MERTK突变相关的视网膜色素变性啮齿动物模型中,感光细胞的长期挽救. 《科学报告》, 8, 1–10 (2018).
- Cronin, T. 等人. 一种合成腺相关病毒衣壳和启动子对视网膜双极细胞的高效转导和光遗传刺激. 《欧洲分子生物学组织分子医学》, 6, 1175-1190 (2014).
- van Wyk, M., Pielecka-Fortuna, J., Löwel, S., Kleinlogel, S. 恢复失明视网膜中的开启开关:光敏感型mGluR6,一种下一代、细胞定制的光遗传学工具. 《公共科学图书馆·生物学》, 13, e1002143 (2015).
- McClements, M. E., Stollenga, F., MacLaren, R. E., Cehajic-Kapetanovic, J. 退化视网膜的光遗传学基因治疗:最新进展. 《神经科学前沿》, 14, 570909 (2020).
- van Wyk, M., Hulliger, E. C., Girod, L., Ebneter, A., Kleinlogel, S. ON双极细胞靶向基因治疗当前的分子局限性. 《神经科学前沿》, 11, 161 (2017).
- Lindner, M., Gilhooley, M. J., Hughes, S., Hankins, M. W. 用于视觉恢复的光遗传学:从原理验证到转化挑战. 《视网膜与眼研究进展》, 91, 01089 (2022).
- Gorostiza, P., Isacoff, E. 用于操控离子通道和孔隙的光学开关与触发器. 《分子生物系统》, 3, 686–704 (2007).
- Kiora Pharmaceuticals, Inc. AAO最新消息:Kiora的小分子光开关在患有视网膜色素变性的失明患者中显示出显著的视力改善. https://www.newsfilecorp.com/release/186265 (2023).
- Berry, M. H. 等人. 用于视力恢复的光药理学. 《当代药理学观点》, 65, 102259 (2022).
- Laprell, L. 等人. 双极细胞的光药理学控制可恢复失明小鼠的视觉功能. 《临床研究杂志》, 127, 2598–2611 (2017).
- Taylor, W. R., Vaney, D. I. 不同的突触机制在兔视网膜中产生方向选择性. 《神经科学杂志》, 22, 7712–7720 (2002).
- Borg-Graham, L. J. 视网膜中方向选择性的计算发生在神经节细胞的突触前. 《自然·神经科学》, 4, 176–183 (2001).
- Di Marco, S. 等人. 小鼠α样视网膜神经节细胞感受野的兴奋性和抑制性作用. 《神经生理学杂志》, 110, 1426–1440 (2013).
- Di Marco, S., Nguyen, V. A., Bisti, S., Protti, D. A. 早期长期视觉剥夺引起的视网膜回路永久性功能重组. 《神经科学杂志》, 29, 13691-13701 (2009).
- Muthmann, J. O. 等人. 利用高密度多电极阵列检测大型神经群体的尖峰信号. 《神经信息学前沿》, 9, 1–21 (2015).
¶ 致谢
作者感谢M.M. La Vail博士(加州大学旧金山分校贝克曼视觉中心,加利福尼亚州)慷慨提供非营养不良型RDY大鼠和营养不良型RCS大鼠;感谢Luca Maragliano(意大利安科纳理工大学和意大利理工学院)提供图1a所示的分子动力学快照;感谢M. Cilli和L. Emionite(圣马蒂诺综合医院IRCCS)。
意大利热那亚的相关人员为外科手术提供了协助;意大利热那亚意大利理工学院的R.钱乔、I.多尔托、A.梅希利、R.纳沃内和D.莫鲁佐提供了技术支持。本研究得到了意大利Telethon(项目编号GMR22T2013)、意大利卫生部(最终研究项目编号GR-2021-12374630)、2019年欧盟“地平线2020”玛丽·居里行动计划创新培训网络“Entrain Vision”(项目编号861423)、意大利大学与研究部(2020年国家研究项目编号2020XBFEMS)以及圣马蒂诺综合医院IRCCS(当前研究和5×1000赠款)的支持。
¶ 作者贡献
G.Z.和S.D.M.进行了体外膜片钳实验;C.B.、V.S.和G.L.设计并表征了Ziapin2;G.Z.和S.C.进行并分析了体内实验。E.D.编写了算法并分析了高密度微电极阵列数据。F.B.和S.D.M.构思了这项研究,规划了实验,分析了数据,并撰写了手稿。
¶ 利益冲突
C.B.、V.S.、G.L.和F.B.是专利申请“光致变色化合物”(PCT/IB2019/054530)的发明人之一。其余作者声明无利益冲突。
¶ 包容性与伦理规范
作者在设计、实施和报告其研究时遵循了《全球行为准则》的建议。
¶ 补充信息
补充信息 在线版本包含可在https://doi.org/10.1038/s41467-025-55882-2获取的补充材料。
通信往来及材料索取请联系法比奥·本费纳蒂或斯特凡诺·迪·马尔科。
《自然·通讯》感谢达里奥·普罗蒂、若昂·卡瓦略-德-索萨以及其他匿名评审人对本研究同行评审所做的贡献。同行评审文件已提供。
重印和许可信息请见 http://www.nature.com/reprints
出版商说明:施普林格·自然对于已出版地图中的管辖权声明以及机构隶属关系保持中立。
开放获取 本文采用知识共享署名-非商业性使用-禁止演绎4.0国际许可协议进行许可。根据该协议,允许以任何媒介或格式进行任何非商业性使用、共享、分发和复制,但需适当注明原作者及出处,提供知识共享许可协议的链接,并说明是否对授权材料进行了修改。根据本许可协议,您无权共享改编自本文或其部分内容的改编材料。本文中的图片或其他第三方材料均包含在本文的知识共享许可协议中,除非在材料的信用说明中另有注明。如果材料未包含在本文的知识共享许可协议中,且您的预期使用未获得法定规定的许可或超出了允许的使用范围,您需要直接从版权持有人处获得许可。如需查看本许可协议的副本,请访问http://creativecommons.org/licenses/by-nc-nd/4.0/。
© 作者(们)2025年