¶ 细胞报告方法
¶ 人类神经肌肉类器官模拟癌症诱导的肌肉恶病质
¶ 原文下载:人类神经肌肉类器官模拟癌症诱导的肌肉恶病质.pdf
¶ 图形摘要
¶ 作者
皮埃特罗·基奥利奥、比阿特丽斯·奥莱塔、卡米拉·佩齐尼、…、马可·桑德里、罗伯塔·萨托里、安娜·乌尔西奥洛
¶ 通讯作者
roberta.sartori@unipd.it (R.S.), anna.urciuolo@unipd.it (A.U.)
¶ 简介
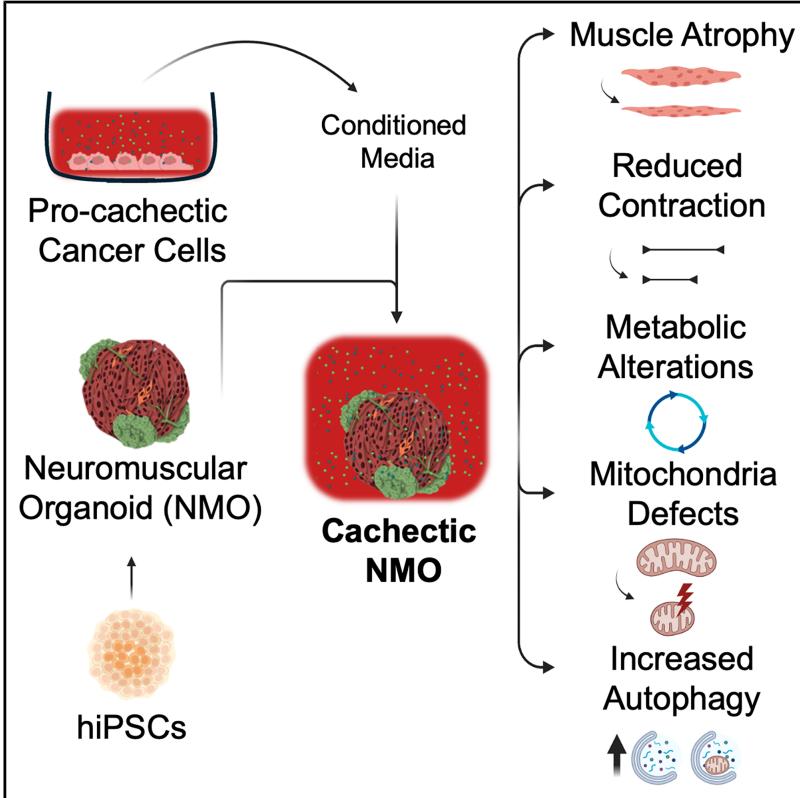
Chiolerio等人介绍了源自人诱导多能干细胞的神经肌肉类器官,将其作为一种创新的体外平台,用于模拟癌症诱导的肌肉萎缩。这些类器官重现了肌肉恶病质的关键特征,为研究潜在机制和开发潜在疗法提供了一个多细胞、具有生理相关性的人类模型。
¶ 亮点
• 人诱导多能干细胞衍生的神经肌肉类器官会成熟并对基因诱导的肌肉萎缩做出反应
• 在促恶病质因子作用下,神经肌肉类器官(NMOs)可模拟恶病质肌肉的形态和功能
• 恶病质神经肌肉类器官(NMOs)表现出癌症恶病质的代谢、线粒体和分子特征
• 神经肌肉类器官(NMOs)为研究机制和测试潜在的恶病质疗法提供了一个平台
¶ 人类神经肌肉类器官模拟癌症诱导的肌肉恶病质
皮埃特罗·奇奥利奥,1,2,13比阿特丽斯·奥莱塔,1,2,3,13卡米拉·佩齐尼,4,5路易吉·萨尔托雷,1,2乔治亚·格雷戈隆,1,2奥尼利亚·加利亚诺,3,5拉特萨,4,5瓦莱里娅·罗克珊娜·巴尔马塞达·瓦尔迪兹,4,5戴维德·卡奇亚雷利,6,7,8卡米拉·卢尼,9卡洛·维斯科米,4,5梅兰妮·普兰克,10萨拉-玛丽亚·芬特,11,12马可·桑德里,4,5罗伯塔·萨托里,4,5,14,和安娜·乌尔乔洛洛1,2,14,15,
1 帕多瓦大学分子医学系,意大利帕多瓦市G. Colombo街3号,邮编35131
2 神经肌肉工程实验室,儿科研究所,Citta’黛拉Speranza,Corso USA 4/F,35127米兰,意大利
3 帕多瓦大学工业工程系,意大利帕多瓦市格拉德尼戈街6/a号,邮编35131
4 帕多瓦大学生物医学科学系,意大利帕多瓦市乌戈·巴奇大街58/B号,邮编35131
5 威尼托分子医学研究所,奥鲁斯街2号,35129 帕多瓦,意大利
6 意大利波佐利市弗莱格雷营地街34号,哈佛-阿尔梅尼斯综合基因组学实验室,Telethon遗传学与医学研究所(TIGEM)
7 意大利那不勒斯“费德里科二世”大学转化医学系,那不勒斯,意大利
8 意大利那不勒斯,南部高等研究院(SSM,高等研究学院),基因组学与实验医学项目8组
9 博洛尼亚大学土木、化学、环境与材料工程系(DICAM),意大利博洛尼亚市泰拉奇尼街28号,邮编40131
10 空间代谢组学专业知识中心,VIB癌症生物学中心,VIB,鲁汶,比利时
11 比利时鲁汶VIB癌症生物学中心细胞代谢与代谢调控实验室,VIB
12 比利时鲁汶市鲁汶大学肿瘤学系细胞代谢与代谢调节实验室及鲁汶癌症研究所(LKI)
13 这些作者贡献相同
14 这些作者贡献相同
15 主要联系人
- 通讯作者:roberta.sartori@unipd.it(R.S.)、anna.urciuolo@unipd.it(A.U.)
https://doi.org/10.1016/j.crmeth.2026.101331
动机 癌症诱发的肌肉恶病质背后机制的研究是一项重大挑战。目前可用的体内和体外模型存在局限性,无法在与患者相关的背景下研究恶病质。因此,我们试图开发一种源自人类细胞的多细胞三维(3D)体外模型,该模型能够重现恶病质肌肉中观察到的表型,包括肌肉收缩受损以及细胞和分子层面的改变。
¶ 摘要
癌症恶病质是一种毁灭性的代谢消耗综合征,影响高达80%的实体癌患者,尽管对肿瘤生物学的理解有所进步,但该病仍无法治愈。本研究引入源自人诱导多能干细胞(hiPSCs)的神经肌肉类器官(NMOs),将其作为研究癌症驱动的肌肉恶病质的平台。我们发现,NMOs对萎缩刺激反应良好,在用源自诱导恶病质的癌细胞的条件培养基处理时,能重现癌症恶病质的关键特征。具体而言,恶病质性NMOs表现出肌肉质量减少、肌肉收缩功能受损、细胞内钙稳态改变、线粒体功能障碍(伴随代谢转变)以及自噬增强。基于这些结果,我们提出源自hiPSCs的NMOs可作为研究人类肌肉恶病质的体外工具,未来有望用于患者特异性建模和治疗筛选。
¶ 引言
尽管过去十年在理解肿瘤生物学方面取得了重大进展,但癌症恶病质——一种导致体重下降和组织消耗的代谢综合征——仍然是一种无法治愈的疾病。它影响着80%的实体癌患者1-4,并占癌症死亡病例的高达30%2,5。尽管被认为是晚期事件,但许多患者在确诊时就已经出现了体重下降2,5。骨骼肌质量和力量的丧失是癌症恶病质中一个相关的临床事件,并预示着不良结局1,6。营养补充无法逆转恶病质,目前也没有有效的治疗方法1,2。
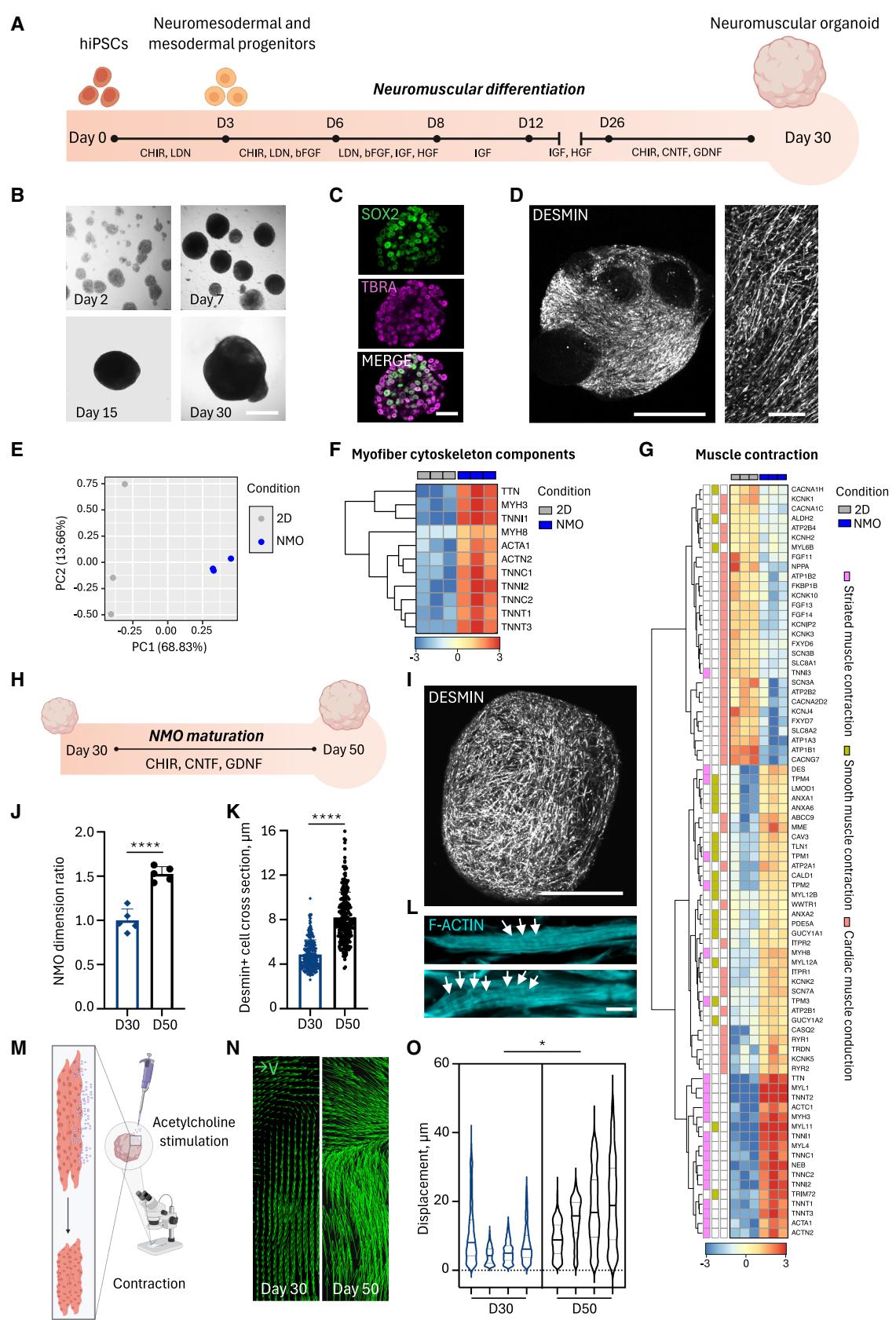
图1. 源自人诱导多能干细胞的神经肌肉类器官在分化50天后显示出功能性肌肉改善
(A) 用于在第30天前获得人诱导多能干细胞衍生神经中胚层器官(hiPSC-derived NMOs)的分化方案示意图;标注了关键的培养基更换时间点。
(B) 代表性明场图像显示了第2天(D2)、第7天(D7)、第15天(D15)和第30天(D30)的形态进展。比例尺为500微米。
© 共聚焦免疫荧光显示第2天时祖细胞中SOX2和TBRA的表达。比例尺,30 μm。
(D) 30天NMOs的z-stack共聚焦图像,对结蛋白(白色)进行染色。比例尺:左侧750 μm,右侧200 μm。
(E) 二维样本与NMO样本的主成分分析(PCA),每个点代表一个样本。扩展数据详见数据S1。
(F和G)与肌纤维细胞骨架成分相关的差异表达基因(F)以及与Reactome肌肉收缩相关的差异表达基因(G)的层次聚类及热图可视化。扩展数据详见数据S1。
(H) 神经肌肉类器官从30天到50天成熟过程的示意图。
(I) 50天NMO的z堆叠共聚焦图像,对结蛋白(白色)进行染色。比例尺:750 μm。
(J) 30天(D30)和50天(D50)神经类器官(NMOs)之间的类器官面积比。数据以每种条件下5个独立神经类器官的平均值±标准差表示。采用异方差Student t检验;****p < 0.0001。
(K) 结蛋白阳性横截面积的量化。数据以8个NMO的≥3张图像的平均值±标准差表示(每个条件240个肌管)。采用异方差Student t检验;****p < 0.0001)。
(L) F-肌动蛋白染色显示第50天的肌节结构(箭头所示)。比例尺为5μm。
(M) 乙酰胆碱诱导的收缩性测试示意图。
(N)乙酰胆碱刺激后D30和D50神经肌肉接点最大位移的代表性矢量图。所示感兴趣区域的尺寸相同。
(O)乙酰胆碱刺激后D30和D50 NMO最大位移的小提琴图。每个小提琴代表单个NMO中最大位移大小的平均值(每个条件4个NMO;每个NMO≥650个事件)。嵌套双尾t检验;*p = 0.0222)。
另见数据S1、S2和视频S1。
对小鼠模型的研究表明,癌症恶病质是由通过泛素-蛋白酶体(UPS)和自噬-溶酶体系统增加的肌肉蛋白质分解所驱动的。7-9然而,目前尚不清楚是什么引发了患者的恶病质,为什么有些癌症会导致恶病质而其他癌症则不会,以及为什么有些恶病质前期患者会发展为明显的恶病质。1癌症诱导的分泌性全身因子,包括那些转运到细胞外囊泡中的因子,10可以通过损害宿主代谢、11诱导肌肉分解代谢和抑制蛋白质合成来触发和维持肌肉萎缩。2,4重要的是,在荷瘤小鼠中保持肌肉质量可独立于肿瘤生长延长生存期,12这凸显了骨骼肌是对抗恶病质发生的关键治疗靶点。
为癌症驱动的患者肌肉恶病质制定有效的治疗策略,需要解决一些尚未解答的基本问题。当前的研究方法存在局限性,一方面难以在患者体内直接研究这些机制,另一方面使用动物模型时存在物种特异性差异。13,14
多能干细胞和类器官技术的进步使人们能够利用人类诱导多能干细胞(hiPSCs)生成三维骨骼肌模型,其中包括能够再现骨骼肌结构和功能的患者特异性类器官。包含功能性人类神经元和肌肉部分的类器官(以下简称神经肌肉类器官[NMOs])已被用于模拟重症肌无力、肌萎缩侧索硬化症和杜氏肌营养不良等疾病。尽管源自人类诱导多能干细胞,但神经肌肉类器官中的肌管仍达到了较高的成熟度,这可能是由于三维结构结合了多细胞复杂性以及其他细胞类型释放的营养因子。
在此,我们提出将人诱导多能干细胞衍生的自组装神经肌肉类器官(NMOs)作为一种体外工具,用于研究恶病质肌肉中的代谢变化以及肌肉重塑/可塑性。我们的研究表明,在NMOs中,肌管会对基因诱导的萎缩刺激做出反应。当用来自恶病质诱导性(而非非恶病质诱导性)癌细胞的条件培养基(CM)处理时,NMOs重现了恶病质肌肉的关键特征,如肌肉质量减少、收缩功能受损、细胞内钙调节异常、线粒体功能障碍以及自噬增强。这些发现表明,NMOs为研究恶病质提供了一种创新的体外人类肌肉模型。这种方法为揭示恶病质的致病机制(可能以个性化方式)以及评估治疗干预措施开辟了新途径。
¶ 结果
¶ 神经肌肉类器官重现了功能性骨骼肌
为了生成神经肌肉类器官(NMOs),将人诱导多能干细胞(hiPSCs)以单细胞形式接种到基质胶微滴上,并根据已发表的分化方案直接分化为自组装的球体(图1A和1B)。接种后两天且分化开始前,人诱导多能干细胞表达多能性标志物,如八聚体结合转录因子4(OCT4)、同源盒蛋白NANOG以及SRY盒转录因子2(SOX2;图S1A和S1B)。分化开始两天后,细胞失去OCT4和NANOG的表达(图S1C和S1D),但共表达神经中胚层祖细胞的关键决定性转录因子SOX2和中胚层诱导性T盒转录因子brachyury(TBRA,即TBRA+SOX2+),或仅表达中胚层祖细胞标志物TBRA16,19,27-32(即TBRA+SOX2-;图1C和S1D)。分化30天后,神经肌肉类器官中可见神经元细胞簇以及大片细长的、结蛋白阳性的肌细胞(图1D和S1E)。为了评估分化30天后神经肌肉类器官中终末分化的肌源性细胞,我们将其转录谱与在二维(2D)条件下进行神经肌肉分化的体外模型进行了比较16。转录组数据的主成分分析(PCA)显示,二维样本和神经肌肉类器官样本明显分离(图1E和数据S1)。两种样本均表达肌纤维/骨骼肌收缩相关基因,但与二维样本相比,神经肌肉类器官中与肌纤维细胞骨架成分和骨骼肌收缩相关的基因上调,而心肌传导相关基因未上调(Reactome数据集;图1F和1G;数据S1),这证实了三维系统中骨骼肌分化得到改善。
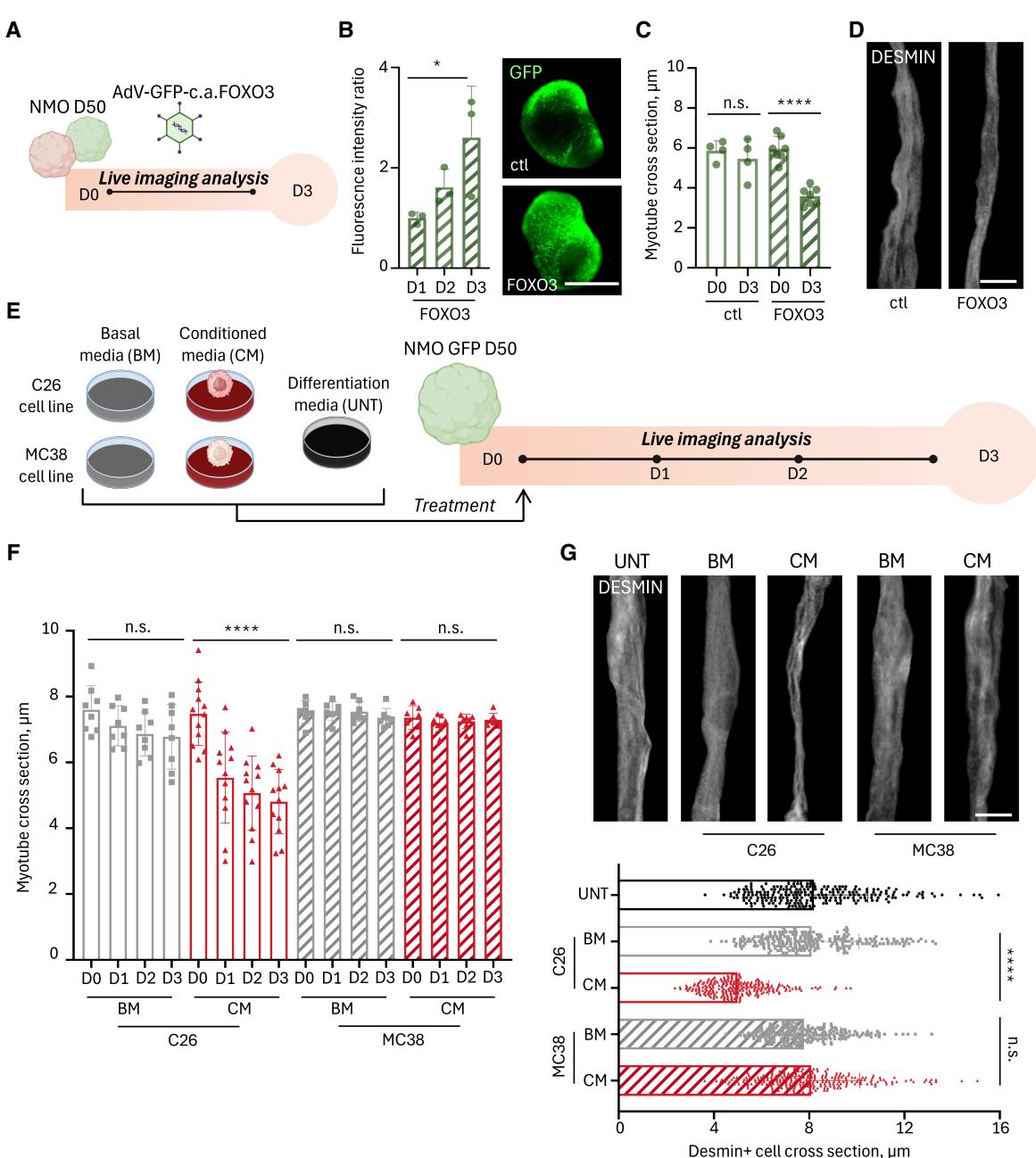
图2. 神经肌肉类器官(NMOs)对遗传性和可溶性恶病质刺激会产生肌肉萎缩反应
(A)示意图时间线显示了用AdV-GFP-c.a.FOXO3或对照AdV-GFP处理源自hiPSC或GFP+ hiPSC的50天神经球(NMO)的过程。、
(B)左图,源自hiPSC的神经球在感染后第1、2和3天(D1-D3)的GFP荧光强度比。数据以每个神经球≥3张图像的平均值±标准差表示;每个点代表一个单独的神经球。采用普通单因素方差分析;*p=0.0477。右图,感染AdV-GFP(上)和AdV-GFP-c.a.FOXO3(下)的神经球在D3的代表性体视显微镜图像。比例尺,1毫米。
(C) 感染AdV-GFP-c.a.FOXO3或对照病毒前(D0)和感染3天后(D3)GFP+肌管横截面的量化。数据以每个NMO的平均肌管直径的平均值±标准差表示(≥20个横截面,每个NMO 3张图像,每个条件≥4个NMO)。采用普通单因素方差分析;****p < 0.0001,另见数据S2。
(D) 感染AdV-GFP-c.a.FOXO3或对照病毒3天后,神经肌肉器官(NMOs)中结蛋白阳性(灰色)肌管的代表性免疫荧光图像。掩码突出显示单个肌管。比例尺,7微米。
(E) 使用基础培养基(BM)以及来自C26(恶病质)和MC38(非恶病质)小鼠结肠癌细胞系的条件培养基(CM)对50天龄GFP+神经肌肉器官(NMO)进行处理的示意图。在分化培养基中培养的未处理(UNT)NMO用作对照。处理持续3天(第50-53天),并在指定时间点进行时间序列成像。
(F) 在使用C26或MC38条件培养基/骨髓培养基处理前(D0)和处理的3天内(D1-D3),对GFP+肌管直径进行定量分析。数据以每个条件下≥7个神经肌肉器官(NMO)的平均值±标准差表示(每个NMO≥20个横截面和3张图像)。采用普通单因素方差分析;****p < 0.0001,另见数据S2。C26骨髓培养基/条件培养基的定量结果与未处理组(UNT)的定量结果在图S2E中进行比较。
(G)上图:经C26和MC38条件培养基/骨髓培养基或UNT处理的GFP+神经肌肉器官中结蛋白阳性(灰色)肌管的代表性免疫荧光图像。掩膜突出显示单个纤维。比例尺,7μm。下图:结蛋白阳性横截面的定量分析。数据以≥3张图像/神经肌肉器官的平均值±标准差表示(每个条件8个神经肌肉器官,每个条件240个肌管)。采用普通单因素方差分析;****p < 0.0001,另见数据S2。
基于培养时间延长可促进类器官成熟这一发现,我们将NMO的培养时间延长至50天分化期(图1H、1I和S1F)。与30天的NMO相比,50天的NMO在大小(图1J)、肌肉区面积(图S1G)和肌管横截面(图1K)方面均显著增加,且存在肌节结构(图1L和S1H),这表明骨骼肌的成熟度有所提高。与先前的研究以及之前的分析(图S1E和S1F)一致,通过TUBB3和MAP2的基因表达(图S1I和数据S2)、神经元功能活性(图S1J和视频S1)以及对神经肌肉接头(NMJ)并列的突触前和突触后元件的检测(图S1K),证实了50天NMO中存在神经元。最后,为了确认30天和50天NMO之间的形态计量学差异能否在功能水平上体现,我们对骨骼肌进行了功能分析。我们用乙酰胆碱(ACh)处理NMO以刺激肌管收缩(图1M;视频S1)。通过粒子测速分析(PIVlab)进行的成像分析显示,50天的NMO比30天的NMO收缩更强,矢量图、平均最大位移(图1N、1O、S1L、S1M和S1N)以及位移空间分布(图S1L、S1M和S1N)均能体现这一点。
.gif)
视频S1. 未处理的D30和D50神经肌肉器官以及经处理的D50神经肌肉器官的功能活动,与图1、3、S1和S3相关
通过微电极阵列(MEA)分析评估了D50神经肌肉类器官(NMO)的神经功能,同时通过实时成像分析观察了给予乙酰胆碱(Ach)后神经肌肉类器官的实时收缩情况。
这些数据共同表明,50天的神经肌肉器官(NMOs)在体外模拟了功能性人类骨骼肌,这提示它们在研究肌肉可塑性和病理生理学方面具有潜在应用价值。
¶ NMOs具有遗传可操作性,并且对恶病质刺激有反应
为了开发一个成熟的骨骼肌模型来研究恶病质状态下的肌肉反应,我们重点研究了50天龄神经肌肉类器官(NMOs)中的肌肉部分。我们首先通过腺病毒(AdV)感染过表达组成型活性(c.a.)叉头框O3转录因子(FOXO333),研究了NMO骨骼肌是否能对已知的萎缩刺激做出适当反应(图2A)。我们优化了用于NMO感染的腺病毒剂量和时间,使用空病毒(AdV-ctl)作为阴性对照。AdV-ctl和AdV c.a.FOXO3均能驱动GFP表达,这通过GFP随时间的增加证实了感染成功(图2B和图S2A)。为了通过活体成像评估处理期间肌管的形态参数,我们还加入了GFP+诱导多能干细胞(hiPSCs)来生成GFP-NMOs(图S2B)。值得注意的是,在处理后的NMOs中,与AdV-ctl相比,c.a.FOXO3的过表达显著减小了肌管大小(图2C、2D和图S2C;数据S2),模拟了FOXO3依赖的成人骨骼肌萎缩。这些结果支持将50天龄NMOs用作体外模型,以研究骨骼肌对萎缩刺激的适应,正如在肌肉恶病质背景下预期观察到的那样。
为了验证这一假设,我们将神经肌肉类器官(NMOs)暴露于致恶病质的C26结肠癌细胞系的条件培养基(CM)中3天,同时以非致恶病质的MC38结肠癌细胞的条件培养基作为对照(图2E)。此外,我们还设置了两组对照:一组是在最佳分化培养基中培养的神经肌肉类器官(未处理组,UNT),另一组是用癌细胞生长培养基(基础培养基,BM)处理的神经肌肉类器官(图2E)。我们未观察到类器官在处理前后的宏观差异(图S2D)。然而,与MC38条件培养基组、基础培养基组和未处理对照组相比,C26条件培养基处理组的肌管大小随时间显著减小(图2F、S2E;数据S2)。重要的是,在两种不同的人诱导多能干细胞(hiPSC)系生成的神经肌肉类器官中,均观察到了C26条件培养基介导的萎缩表型(图S2F;数据S2)。处理3天后,我们通过结蛋白(desmin)免疫荧光成像分析进一步量化了C26条件培养基处理的神经肌肉类器官中肌管的横截面,结果与活细胞成像数据一致(图2G、S2G、S2H;数据S2)。C26条件培养基还增加了细胞死亡事件(图S2I;数据S2),并减少了恶病质性神经肌肉类器官的总肌肉面积(图S2J;数据S2)。用非致恶病质的MC38条件培养基处理的神经肌肉类器官未出现萎缩,这表明C26条件培养基的表型与其致恶病质的分泌组相关,而非肿瘤分泌组本身。
总之,这些数据表明,人诱导多能干细胞衍生的肌管能对萎缩/促恶病质刺激做出适当反应,这提示它们可用于体外研究癌症恶病质中人类骨骼肌的生理病理学。
¶ 经C26条件培养基处理后,神经肌肉类器官(NMOs)表现出功能损伤
由于在给予乙酰胆碱(ACh)后神经肌肉类器官(NMOs)会发生收缩(图1N和1O),我们测试了C26细胞条件培养基(C26-CM)处理的功能效应(图3A)。虽然所有样本在ACh诱导下都会发生收缩(视频S1),但与对照组相比,C26-CM处理显著减弱了NMO的收缩,这可通过向量图、平均最大位移的减小(图3B、3C和3D;数据S2)、小位移事件(<5μm)百分比的增加以及大位移事件(>15μm)百分比的减少体现(图3E和S3A;数据S2)。极坐标图通过同时评估位移幅度和方向,也显示经C26-CM处理的NMOs其收缩协调性发生了改变(图3F和S3B)。接下来,我们监测了钙稳态——这对肌肉收缩至关重要38——在ACh刺激期间,未处理(UNT)、C26细胞骨髓(C26-BM)处理和C26-CM处理的非绿色荧光蛋白(GFP)表达NMOs的肌管中加载Fluo-4钙染料后的情况。通过Fluo-4活体成像对ACh诱导收缩时的钙流进行量化,结果显示钙处理功能发生改变,证实了恶病质类器官存在功能损伤(图3G、3H和S3C;数据S2)。
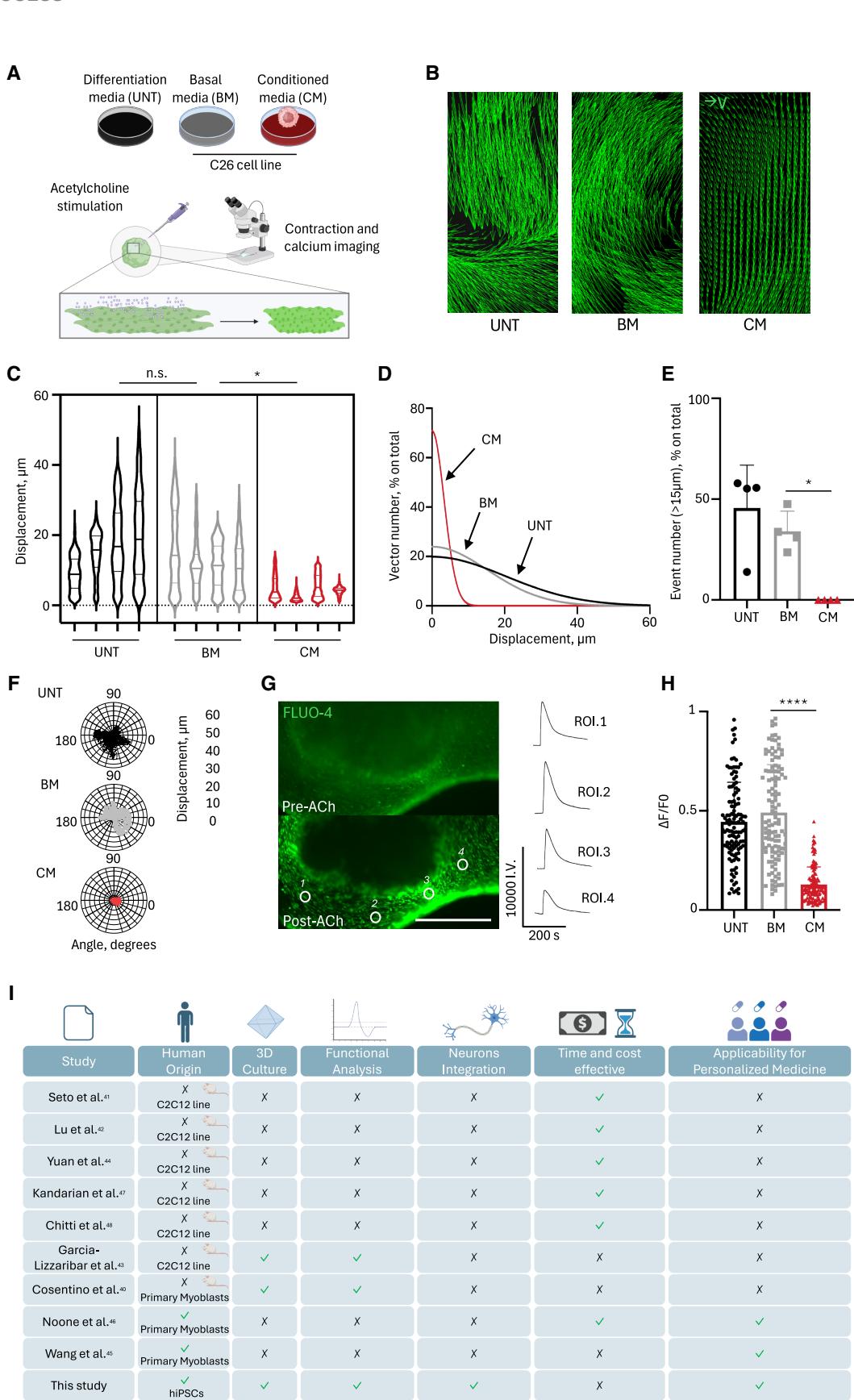
图3. 恶病质神经肌肉器官(NMOs)显示出肌肉功能下降
(A)通过C26来源的BM和CM处理后,通过直接ACh刺激来测试GFP+ NMOs肌肉功能的策略示意图。UNT条件被纳入作为对照。
(B) 在C26-BM/CM处理后以及未处理(UNT)条件下,GFP+神经肌肉器官收缩期间记录的乙酰胆碱(ACh)诱导位移的代表性向量图。样本间考虑了相同的感兴趣区域。
(C)小提琴图显示了经C26-BM/CM处理后的GFP+神经运动单位(NMOs)以及未处理(UNT)的NMOs中,乙酰胆碱(ACh)诱导的最大位移。每个小提琴代表单个NMO中最大位移大小的平均值(每种条件4个NMO;每个NMO≥655个事件)。采用嵌套单因素方差分析(nested one-way ANOVA);*p = 0.0173,另见数据S2。
(D) 在乙酰胆碱刺激下,GFP+神经运动器官(UNT)或经C26-BM/CM处理的神经运动器官中,位移频率分布(0–60 μm和5 μm区间)的高斯插值。
(E) C26来源的BM/CM处理后以及UNT样本中,GFP+神经运动器官(NMOs)中位移>15μm的频率分布。数据以4个NMOs/条件的平均值±标准差表示,每个点代表单个NMO。普通单因素方差分析;**p=0.0011;*p=0.0124,另见数据S2。
(F)在C26 BM/CM处理后以及UNT样本中,GFP+神经运动单位在乙酰胆碱(ACh)刺激下的最大位移(微米)和方向性(度)的代表性极坐标图。
(G)左图:ACh刺激前后GFP+ NMO的单个实时成像帧(Fluo-4)。比例尺,500 μm。右图:显示不同独立感兴趣区域(ROI)钙瞬变幅度的代表性轨迹。
(H)在经过C26来源的BM/CM处理后的GFP+神经运动细胞(NMOs)以及未处理(UNT)的神经运动细胞中,通过Fluo-4成像对钙峰值幅度(ΔF/F0)进行量化。数据以均值±标准差表示,每个条件下从4个神经运动细胞中获取120次测量结果。采用普通单因素方差分析(ordinary one-way ANOVA);****p < 0.0001,另见数据S2。
(I)比较方案总结了NMOs和其他癌症诱导的肌肉恶病质体外模型,强调了相对优势和局限性(绿色对勾=存在;黑色叉号=不存在)。
另请参见数据S2和视频S1。
总之,这些数据证明,神经肌肉类器官(NMOs)在暴露于恶病质分泌因子时能够模拟人类骨骼肌的(功能异常)情况。尽管成本较高且细胞培养时间更长,但在评估体外模拟和研究癌症诱导的肌肉恶病质的关键标准(如起源物种、空间组织、功能分析能力、神经元整合以及个性化医疗应用潜力)时,与目前可用的体外模型相比,我们的NMO平台满足所有这些要求(图3I)。
¶ 经C26条件培养基处理的神经肌肉类器官(NMOs)表现出代谢改变和线粒体功能障碍
由于能量代谢紊乱、线粒体形态和功能改变以及自噬增强是恶病质的关键特征,我们监测了神经肌肉类器官(NMOs)中的这些特征。空间代谢组学显示,与对照组相比,经C26细胞条件培养基(C26-CM)处理的恶病质性NMOs中三羧酸循环(TCA循环)中间产物(如柠檬酸/异柠檬酸和苹果酸)富集(图4A、4B和S4A;数据S3),这支持了生物能量学受损的观点。接下来,我们研究了线粒体的形态和功能。电子显微镜显示,对照组NMOs(即未处理组(UNT)和C26细胞骨髓培养基(C26-BM)处理组)中的线粒体呈细长状,嵴结构规则;而恶病质性NMOs中的线粒体则体积小、呈碎片化且电子密度高,其嵴结构难以辨认(图4C)。通过对线粒体输入受体亚基(TOM20)和肌球蛋白的免疫荧光共染色进行成像分析,并使用线粒体分析插件进行量化,证实了恶病质性肌管中的线粒体碎片化程度增加(图4D、S4B和S4C;数据S2)。利用Oroboros O2k对单个类器官的氧通量分析表明,在基础条件下以及给予复合体I/II底物后,恶病质性NMOs中经线粒体DNA含量校正的线粒体呼吸作用均减弱(图4E、4F、S4D和S4E;数据S2)。与UNT组和C26-BM组样本相比,这还与肌管中线粒体含量减少以及TOM20荧光强度降低相关(图S4E和S4F;数据S2)。
由于自噬增加可能导致线粒体内容物碎片化、减少以及萎缩,54,55我们对这一蛋白水解系统进行了监测。C26-CM肌管中溶酶体相关膜蛋白1(LAMP1)与TOM20共定位增加,表明线粒体自噬增强(图4G和图S4G;数据S2),电子显微镜显示恶病质神经肌肉标本(NMOs)的囊泡内存在线粒体,也印证了这一点(图4H)。与对照组相比,恶病质肌管中自噬标志物泛素结合蛋白p62(sequestosome 1)或微管相关蛋白1轻链3β(LC3B)的点状结构也显著增多,4,54,55表明自噬增强(图4I和图4J;数据S2)。
总之,这些数据表明,神经肌肉器官型模型(NMOs)再现了癌症恶病质诱导的肌肉萎缩的关键特征,包括肌纤维萎缩、收缩能力下降、线粒体功能障碍以及自噬增强。因此,NMOs代表了一种人体骨骼肌体外模型,可用于研究与恶病质患者相关的发病机制假说和治疗方法。
¶ 讨论
癌症恶病质以肌肉减少为特征,可能伴随或不伴随脂肪减少,它会严重影响生活质量、降低化疗反应并缩短总生存期,但目前缺乏有效的治疗方法,部分原因是动物模型在重现人类病理生理学方面存在局限性。因此,迫切需要3D体外人体模型来研究肌肉恶病质的机制、开发转化方法,并减少动物的使用。已有报道称,神经肌肉类器官(NMOs)能够模拟健康和疾病状态下的人类骨骼肌,但迄今为止,尚未有研究使用神经肌肉类器官来模拟癌症诱导的肌肉恶病质。
我们将人诱导多能干细胞衍生的神经肌肉类器官作为人类骨骼肌的三维体外模型,用于研究癌症驱动的肌肉恶病质。
人诱导多能干细胞衍生的神经肌肉类器官(NMOs)展现出功能性骨骼肌部分。与二维培养物相比,这种三维结构促进了肌肉的成熟。此外,与第30天的NMOs相比,第50天的NMOs在乙酰胆碱(ACh)刺激下显示出肌管大小增加和肌肉收缩增强,表明其随时间逐渐成熟。NMOs的多细胞复杂性(包括神经元成分)提供了生理相关的环境,能更好地重现关键的稳态肌肉反应。
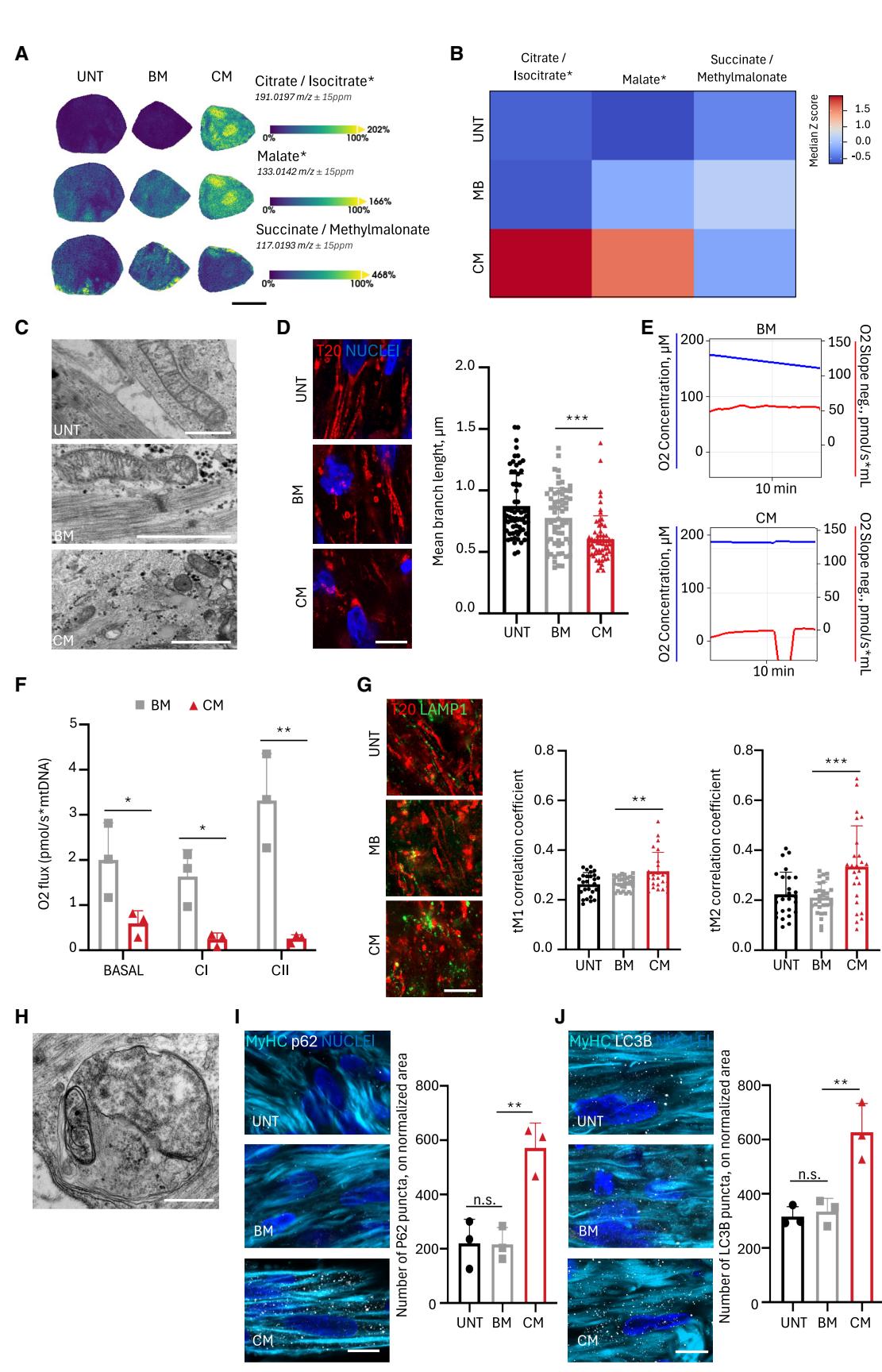
图4. 恶病质神经肌肉器官(NMOs)表现出典型的肌肉恶病质的分子和线粒体改变
(A)空间代谢组学图谱显示了经C26源BM和CM处理后,NMO切片中三羧酸循环(TCA)相关代谢物的分布。未处理(UNT)条件被纳入作为对照。比例尺为500μm。扩展数据详见数据S3。
(B)经C26源BM/CM处理后的NMO以及未处理(UNT)NMO中,三羧酸循环(TCA)相关代谢物的热图定量分析。扩展数据详见数据S3。
(C)经C26 BM/CM处理后的NMO和未处理NMO中线粒体形态的代表性电子显微镜图像。比例尺为1μm。
(D)左图:共聚焦免疫荧光图像显示经C26 BM/CM处理后的NMO和未处理NMO肌管中的TOM20(T20)。比例尺为8.5μm。右图:肌管内线粒体分支长度的定量分析。图S2B中展示了与MyHC+共染色以识别肌管的代表性图像。数据以平均值±标准差表示,每个条件下来自3个NMO的≥10张图像。采用普通单因素方差分析;****p < 0.0001,另见数据S2。
(E)代表性Oroboros轨迹显示经C26 BM/CM处理后的NMO在基础呼吸期间的氧气浓度和消耗速率。
(F)暴露于BM和CM的NMO中的特定氧气通量测量。在底物特异性条件下评估复合体I和II的呼吸作用。数据为三次独立实验的平均值±标准差(n = 3)。采用异方差Student t检验:*p < 0.05,**p < 0.01;另见数据S2。
(G)左图:经C26 BM/CM处理的神经肌肉器官(NMOs)以及未处理(UNT)的神经肌肉器官中TOM20(T20)和LAMP1的共聚焦免疫荧光图像。比例尺为8.5μm。中间为T20上共定位系数tMCC1的定量分析,右图为LAMP1上共定位系数tMCC2的定量分析。数据以平均值±标准差表示,每个条件下来自3个神经肌肉器官的≥8张图像。单因素方差分析:中间,**p=0.0049;右图,***p=0.0003),另见数据S2。
(H) 电子显微镜显示,经C26条件培养基处理的NMO中,囊泡内有线粒体。比例尺为500纳米。
(I)左图:共聚焦免疫荧光显示,经C26 BM/CM处理和UNT后的神经肌肉器官(NMOs)中的肌球蛋白重链(MyHC,青色)和p62(灰色)。比例尺,7.5μm。右图:肌球蛋白重链阳性区域(MyHC+ROIs)内p62斑点的定量分析。数据以平均值±标准差表示,每个条件下3个神经肌肉器官(NMOs),每个神经肌肉器官至少8张图像。单因素方差分析;**p=0.0042,另见数据S2。
(J)左图:共聚焦免疫荧光显示,经C26 BM/CM处理和UNT处理后的NMO中MyHC(青色)和LC3B(灰色)的表达。比例尺,7.5 μm。右图:MyHC+感兴趣区域内LC3B斑点的定量分析(每个条件3个NMO)。数据以每个条件3个NMO的≥8张图像的平均值±标准差表示。单因素方差分析;**p = 0.0055,另见数据S2。
另请参见数据S2和S3。
NMOs对先前在成年小鼠肌肉中测试过的萎缩刺激做出了预期反应,这证实了它们模拟与动态病理相关的分解代谢状态的能力。关键的是,当用来自诱导恶病质的癌细胞(而非非诱导恶病质的癌细胞)的条件培养基处理时,NMOs表现出恶病质中肌肉萎缩的所有特征,例如肌肉质量和收缩能力下降、细胞内钙稳态改变、线粒体碎片化和功能障碍的出现以及自噬增加。尤其值得注意的是,NMOs能够捕捉恶病质肌肉中自噬增加与线粒体功能障碍之间的复杂相互作用,这与体内癌症恶病质研究的结果一致。这包括自噬标志物(p62和LC3B)增加、线粒体自噬的证据(LAMP1和TOM20共定位),以及在用诱导恶病质的癌细胞培养基处理后线粒体形态/功能的改变。这表明我们的模型可能在研究参与肌肉萎缩的特定通路的作用方面特别有用,有可能促成新治疗靶点的发现。事实上,NMOs的遗传可操作性使其能够研究功能获得和功能丧失方法,这不仅为机制研究,也为对抗肌肉萎缩的靶向干预开辟了可能性。
由于肌肉无力是癌症进展过程中患者出现的关键临床事件,2 其功能缺陷以及神经元成分的存在使得神经肌肉类器官(NMOs)在模拟恶病质中的神经肌肉交叉对话 37 和评估治疗方法方面具有特别重要的意义。与其他由人类诱导多能干细胞(hiPSC)衍生的神经肌肉类器官相比,20,21,23,25,26 本研究中生成的神经肌肉类器官提供了一种操作简便、省时省力且成本效益高的方法,无需预分化步骤,能够在分化的初始阶段实现神经肌肉类器官的扩增。研究其他方案衍生的神经肌肉类器官是否能重现我们平台中观察到的特征将具有重要价值,这也将为科学界研究肌肉恶病质开辟广泛的机会。
虽然神经肌肉类器官(NMO)复制了癌症恶病质的许多特征,但必须承认,它在完全重现活生物体中存在的复杂系统相互作用方面存在局限性。未来的研究应着重于将神经肌肉类器官与其他相关细胞类型/类器官整合,以创建一个更全面的体外模型,捕捉恶病质发病机制中涉及的器官间交叉对话。
总之,我们的人类诱导多能干细胞衍生的神经肌肉器官平台为癌症恶病质研究带来了重大进展。它提供了一个极具前景的人类肌肉模型,可用于研究恶病质机制以及开发/测试潜在疗法,并能够以患者特异性的方式研究这些过程。随着该模型的进一步完善和扩展,我们预计它将在克服小鼠模型的局限性方面发挥关键作用,从而增进我们对癌症患者这种毁灭性肌肉萎缩病症的理解和治疗。
¶ 研究的局限性
NMO分化和成熟不完全可能会影响特定恶病质表型的建模。作为一种体外模型,NMO缺乏来自其他器官系统、肿瘤微环境以及可能影响恶病质发病机制的患者特异性信号异质性的作用。
¶ 资源可用性
¶ 主要联系人
如需更多信息和资源,请联系主要联系人安娜·乌尔乔洛(anna.urciuolo@unipd.it),相关需求将由其处理。
¶ 材料可获得性
本研究未生成新的独特试剂。
¶ 数据和代码可用性
• bulk RNA测序(RNA-seq)数据可在NCBI基因表达综合数据库(GEO:GSE226477)获取。2D样本(GSM7076294–GSM7076296)和NMO样本(GSM7076297–GSM7076299)。
• 生物信息学分析是使用公开可用的工具按照开发者的说明进行的。
• 如需重新分析本文所报告的数据,任何所需的额外信息均可通过主要联系人获取。
¶ 致谢
我们感谢Nicola Elvassore教授在人类诱导多能干细胞方面提供的支持。本研究得到了Bando Direzione Scientifica IRP Citta della Speranza(编号21/05)、分子医学系的部门研究综合预算(BIRD2022)、意大利抗癌研究协会2023年MFAG项目(编号:29118)以及Panciera基金会对A.U.的支持;得到了帕多瓦大学生物医学系的部门研究综合预算(BIRD 2023)对R.S.的支持。O.G.得到了ERC-2023-STG OriSha项目(编号101117759)的支持。C. Laterza得到了ERC-2022-STG COnNect项目(编号101077714)的支持。D.C.由Telethon基金会核心资助、Armenise哈佛基金会职业发展奖、意大利卫生部(卫生行动计划轨迹3,T3-AN-09,“Genomed”;2021年专项研究,“genOMICA”;2023年MCNT2,“EUCARDIS”)、意大利大学和研究部以及欧盟(下一代欧盟计划——MUR-PRIN-2022,编号2022T7XP29,PNC 0000001 D3-4-Health项目)资助。A.U.、M.S.和C.V.得到了Telethon/Cariparo VIMM计划项目(编号:GSP24003)的支持。M.S.得到了下一代欧盟计划(国家复苏和韧性计划框架下,项目编号CN00000041,CUP编号C93C22002780006,第4部分“代谢和心血管疾病”)以及意大利抗癌研究协会-IG项目(编号:23257和30366)的支持。S.-M.F.感谢Stichting Tegen Kanker(STK)、FWO和鲁汶大学提供的资金支持。图文摘要中的示意图(许可证编号#CE28ZKZ5M3)以及图1A、1H、1M、2A、2E、3A、3I、S2A和S2B(许可证编号#HZ28ZKYR0Y)均通过BioRender.com制作。
¶ 作者贡献
A.U.和R.S.设计了本研究,且贡献均等;P.C.和B.A.开展了分化实验并进行了所有分析;C.P.为癌细胞培养基制备和数据解读提供了帮助;L.S.在RNA测序分析、肌肉收缩量化及图形呈现方面做出了贡献;G.G.参与了钙分析和线粒体形态量化工作;O.G.进行了细胞重编程;C. Laterza构建了GFP-人诱导多能干细胞;D.C.开展了RNA测序;C. Luni进行了批量RNA测序数据分析与解读;B.A.为空间代谢实验提供了支持;M.P.开展了空间代谢实验、代谢组学分析及数据解读;V.R.B.V.进行了Oroboros分析;C.V.、S.-M.F.和M.S.在数据解读方面提供了重要意见。所有作者都参与了手稿的修订。A.U.负责监督类器官的生成、表征以及处理后的分析;A.U.和R.S.分析解读了数据,撰写了手稿,并监督了整个项目。
¶ 利益声明
作者声明不存在利益冲突。
¶ STAR★方法
详细方法见本文的在线版本,包括以下内容:
• 关键资源表
• 实验模型和研究参与者详情
○ 人诱导多能干细胞的衍生与培养
○ 人诱导多能干细胞的分化与培养
○ 小鼠结肠腺癌细胞系的培养
• 方法详情
○ 用C26和MC38条件培养基处理NMO
○ 免疫荧光分析及图像制备
○ 收缩和钙动力学的实时成像分析
○ 多电极阵列(MEA)测定
○ 活死分析
○ 腺病毒感染
○ RNA纯化和逆转录定量聚合酶链反应
○ 批量测序分析
○ 空间代谢组学分析
○ 高分辨率呼吸测定法
• 定量与统计分析
¶ 补充信息
补充信息可在网上查阅:https://doi.org/10.1016/j。
crmeth.2026.101331.
收到日期:2025年10月1日
修订日期:2025年11月13日
接受日期:2026年1月22日
发表时间:2026年2月17日
¶ 参考文献
- Fearon, K., Strasser, F., Anker, S.D., Bosaeus, I., Bruera, E., Fainsinger, R.L., Jatoi, A., Loprinzi, C., MacDonald, N., Mantovani, G., et al. (2011). Definition and classification of cancer cachexia: An international consensus. Lancet Oncol. 12, 489–495. https://doi.org/10.1016/S1470- 2045(10)70218-7.
- Baracos, V.E., Martin, L., Korc, M., Guttridge, D.C., and Fearon, K.C.H. (2018). Cancer-associated cachexia. Nat. Rev. Dis. Primers 4, 17105. https://doi.org/10.1038/nrdp.2017.105.
- Martin, A., and Freyssenet, D. (2021). Phenotypic features of cancer cachexia-related loss of skeletal muscle mass and function: lessons from human and animal studies. J. Cachexia Sarcopenia Muscle 12, 252–273. https://doi.org/10.1002/jcsm.12678.
- Sartori, R., Romanello, V., and Sandri, M. (2021). Mechanisms of muscle atrophy and hypertrophy: implications in health and disease. Nat. Commun. 12, 330. https://doi.org/10.1038/s41467-020-20123-1.
- von Haehling, S., Morley, J.E., and Anker, S.D. (2010). An overview of sarcopenia: facts and numbers on prevalence and clinical impact. J. Cachexia Sarcopenia Muscle 1, 129–133. https://doi.org/10.1007/ s13539-010-0014-2.
- Wesseltoft-Rao, N., Hjermstad, M.J., Ikdahl, T., Dajani, O., Ulven, S.M., Iversen, P.O., and Bye, A. (2015). Comparing two classifications of cancer cachexia and their association with survival in patients with unresected pancreatic cancer. Nutr. Cancer 67, 472–480. https://doi.org/10.1080/ 01635581.2015.1004728.
- Sandri, M. (2016). Protein breakdown in cancer cachexia. Semin. Cell Dev. Biol. 54, 11–19. https://doi.org/10.1016/j.semcdb.2015.11.002.
- Mitch, W.E., and Goldberg, A.L. (1996). Mechanisms of Muscle Wasting — The Role of the Ubiquitin–Proteasome Pathway. N. Engl. J. Med. 335, 1897–1905. https://doi.org/10.1056/nejm199612193352507.
- Cohen, S., Nathan, J.A., and Goldberg, A.L. (2015). Muscle wasting in disease: Molecular mechanisms and promising therapies. Nat. Rev. Drug Discov. 14, 58–74. https://doi.org/10.1038/nrd4467.
- Marceca, G.P., Londhe, P., and Calore, F. (2020). Management of Cancer Cachexia: Attempting to Develop New Pharmacological Agents for New Effective Therapeutic Options. Front. Oncol. 10, 298. https://doi.org/10. 3389/fonc.2020.00298.
- Wyart, E., Carra` , G., Angelino, E., Penna, F., and Porporato, P.E. (2025). Systemic metabolic crosstalk as driver of cancer cachexia. Trends Endocrinol. Metab. xx, 1–12. https://doi.org/10.1016/j.tem.2024.12.005.
- Zhou, X., Wang, J.L., Lu, J., Song, Y., Kwak, K.S., Jiao, Q., Rosenfeld, R., Chen, Q., Boone, T., Simonet, W.S., et al. (2010). Reversal of cancer cachexia and muscle wasting by ActRIIB antagonism leads to prolonged survival. Cell 142, 531–543. https://doi.org/10.1016/j.cell.2010.07.011.
- Baracos, V.E. (2018). Bridging the gap: Are animal models consistent with clinical cancer cachexia? Nat. Rev. Clin. Oncol. 15, 197–198. https://doi. org/10.1038/nrclinonc.2018.14.
- Argile´ s, J.M., Busquets, S., Stemmler, B., and Lo´ pez-Soriano, F.J. (2014). Cancer cachexia: Understanding the molecular basis. Nat. Rev. Cancer 14. https://doi.org/10.1038/nrc3829.
- Kim, J., Koo, B.K., and Knoblich, J.A. (2020). Human organoids: model systems for human biology and medicine. Nat. Rev. Mol. Cell Biol. 21, 571–584. https://doi.org/10.1038/s41580-020-0259-3.
- Auletta, B., Chiolerio, P., Cecconi, G., Rossi, L., Sartore, L., Cecchinato, F., Barbato, G., Lauroja, A., Maghin, E., Easler, M., et al. (2025). Tissue-engineered neuromuscular organoids. Commun. Biol. 8, 1074. https://doi. org/10.1038/s42003-025-08484-z.
- Urzi, A., Lahmann, I., Nguyen, L.V.N., Rost, B.R., Garcı´a-Pe´ rez, A., Lelievre, N., Merritt-Garza, M.E., Phan, H.C., Bassell, G.J., Rossoll, W., et al. (2023). Efficient generation of a self-organizing neuromuscular junction model from human pluripotent stem cells. Nat. Commun. 14, 8043. https://doi.org/10.1038/s41467-023-43781-3.
- Shin, M.K., Bang, J.S., Lee, J.E., Tran, H.D., Park, G., Lee, D.R., and Jo, J. (2022). Generation of Skeletal Muscle Organoids from Human Pluripotent Stem Cells to Model Myogenesis and Muscle Regeneration. Int. J. Mol. Sci. 23, 5108. https://doi.org/10.3390/ijms23095108.
- Rossi, L., Auletta, B., Sartore, L., La Placa, M., Cecconi, G., Chiolerio, P., Maghin, E., Angiolillo, S., Carraro, E., Gagliano, O., et al. (2025). Engineering Assembloids to Mimic Graft-Host Skeletal Muscle Interaction. Adv. Healthc. Mater. 14, e2404111. https://doi.org/10.1002/adhm.202404111.
- Pereira, J.D., DuBreuil, D.M., Devlin, A.C., Held, A., Sapir, Y., Berezovski, E., Hawrot, J., Dorfman, K., Chander, V., and Wainger, B.J. (2021). Human sensorimotor organoids derived from healthy and amyotrophic lateral sclerosis stem cells form neuromuscular junctions. Nat. Commun. 12, 4744. https://doi.org/10.1038/s41467-021-24776-4.
- Yin, Y., Zhou, W., Zhu, J., Chen, Z., Jiang, L., Zhuang, X., Chen, J., Wei, J., Lu, X., Liu, Y., et al. (2025). Generation of self-organized neuromusculoskeletal tri-tissue organoids from human pluripotent stem cells. Cell Stem Cell 32, 157–171.e8. https://doi.org/10.1016/j.stem.2024.11.005.
- Maffioletti, S.M., Gerli, M.F.M., Ragazzi, M., Dastidar, S., Benedetti, S., Loperfido, M., Vandendriessche, T., Chuah, M.K., and Tedesco, F.S. (2015). Efficient derivation and inducible differentiation of expandable skeletal myogenic cells from human ES and patient-specific iPS cells. Nat. Protoc. 10, 941–958. https://doi.org/10.1038/nprot.2015.057.
- Gao, C., Shi, Q., Pan, X., Chen, J., Zhang, Y., Lang, J., Wen, S., Liu, X., Cheng, T.L., and Lei, K. (2024). Neuromuscular organoids model spinal neuromuscular pathologies in C9orf72 amyotrophic lateral sclerosis. Cell Rep. 43, 113892. https://doi.org/10.1016/j.celrep.2024.113892.
- Chal, J., Tanoury, Z.A., Hestin, M., Gobert, B., Aivio, S., Hick, A., Cherrier, T., Nesmith, A.P., Parker, K.K., and Pourquie´ , O. (2016). Generation of human muscle fibers and satellite-like cells from human pluripotent stem cells in vitro. Nat. Protoc. 11, 1833. https://doi.org/10.1038/nprot. 2016-110.
- Mavrommatis, L., Jeong, H.W., Kindler, U., Gomez-Giro, G., Kienitz, M.C., Stehling, M., Psathaki, O.E., Zeuschner, D., Bixel, M.G., Han, D., et al. (2023). Human skeletal muscle organoids model fetal myogenesis and sustain uncommitted PAX7 myogenic progenitors. eLife 12, RP87081. https://doi.org/10.7554/eLife.87081.
- Faustino Martins, J.M., Fischer, C., Urzi, A., Vidal, R., Kunz, S., Ruffault, P.L., Kabuss, L., Hube, I., Gazzerro, E., Birchmeier, C., et al. (2020). Self-Organizing 3D Human Trunk Neuromuscular Organoids. Cell Stem Cell 26, 172–186.e6. https://doi.org/10.1016/j.stem.2019.12.007.
- Sambasivan, R., and Steventon, B. (2020). Neuromesodermal Progenitors: A Basis for Robust Axial Patterning in Development and Evolution. Front. Cell Dev. Biol. 8, 607516–607519. https://doi.org/10.3389/fcell. 2020.607516.
- Henrique, D., Abranches, E., Verrier, L., and Storey, K.G. (2015). Neuromesodermal progenitors and the making of the spinal cord. Dev 142, 2864– 2875. https://doi.org/10.1242/dev.119768.
- Guibentif, C., Griffiths, J.A., Imaz-Rosshandler, I., Ghazanfar, S., Nichols, J., Wilson, V., Go¨ ttgens, B., and Marioni, J.C. (2021). Diverse Routes toward Early Somites in the Mouse Embryo. Dev. Cell 56, 141–153.e6. https://doi.org/10.1016/j.devcel.2020.11.013.
- Gouti, M., Delile, J., Stamataki, D., Wymeersch, F.J., Huang, Y., Kleinjung, J., Wilson, V., and Briscoe, J. (2017). A Gene Regulatory Network Balances Neural and Mesoderm Specification during Vertebrate Trunk Development. Dev. Cell 41, 243–261.e7. https://doi.org/10.1016/j.devcel.2017. 04.002.
- Edri, S., Hayward, P., Baillie-Johnson, P., Steventon, B.J., and Martinez Arias, A. (2019). An epiblast stem cell-derived multipotent progenitor population for axial extension. Dev 146, dev168187. https://doi.org/10.1242/ dev.168187.
- Edri, S., Hayward, P., Jawaid, W., and Martinez Arias, A. (2019). Neuromesodermal progenitors (NMPs): A comparative study between pluripotent stem cells and embryo-derived populations. Dev 146, dev180190. https://doi.org/10.1242/dev.180190.
- Sandri, M., Sandri, C., Gilbert, A., Skurk, C., Calabria, E., Picard, A., Walsh, K., Schiaffino, S., Lecker, S.H., and Goldberg, A.L. (2004). Foxo Transcription Factors Induce the Atrophy-Related Ubiquitin Ligase Atrogin-1 and Cause Skeletal Muscle Atrophy. Cell 117, 399–412. https://doi.org/10. 1016/S0092-8674(04)00400-3.
- Zhang, W., Sun, W., Gu, X., Miao, C., Feng, L., Shen, Q., Liu, X., and Zhang, X. (2022). GDF-15 in tumor-derived exosomes promotes muscle atrophy via Bcl-2/caspase-3 pathway. Cell Death Discov. 8, 162. https:// doi.org/10.1038/s41420-022-00972-z.
- Schmidt, M., Poser, C., and von Maltzahn, J. (2020). Wnt7a Counteracts Cancer Cachexia. Mol. Ther. Oncolytics 16, 134–146. https://doi.org/10. 1016/j.omto.2019.12.011.
- Rohm, M., Scha¨ fer, M., Laurent, V., U¨ stu¨ nel, B.E., Niopek, K., Algire, C., Hautzinger, O., Sijmonsma, T.P., Zota, A., Medrikova, D., et al. (2016). An AMP-activated protein kinase-stabilizing peptide ameliorates adipose tissue wasting in cancer cachexia in mice. Nat. Med. 22, 1120–1130. https://doi.org/10.1038/nm.4171.
- Sartori, R., Hagg, A., Zampieri, S., Armani, A., Winbanks, C.E., Viana, L.R., Haidar, M., Watt, K.I., Qian, H., Pezzini, C., et al. (2021). Perturbed BMP signaling and denervation promote muscle wasting in cancer cachexia. Sci. Transl. Med. 13, eaay9592. https://doi.org/10.1126/scitranslmed. aay9592.
- Rall, J.A. (2022). Discovery of the regulatory role of calcium ion in muscle contraction and relaxation: Setsuro Ebashi and the international emergence of Japanese muscle research. Adv. Physiol. Educ. 46, 481–490. https://doi.org/10.1152/ADVAN.00108.2022.
- Cosentino, M., Forcina, L., Zouhair, M., Apa, L., Genovese, D., Boccia, C., Rizzuto, E., and Musaro` , A. (2023). Modelling three-dimensional cancerassociated cachexia and therapy: The molecular basis and therapeutic potential of interleukin-6 transignalling blockade. J. Cachexia Sarcopenia Muscle 14, 2550–2568. https://doi.org/10.1002/jcsm.13329.
- Seto, D.N., Kandarian, S.C., and Jackman, R.W. (2015). A key role for leukemia inhibitory factor in C26 cancer cachexia. J. Biol. Chem. 290, 19976– 19986. https://doi.org/10.1074/jbc.M115.638411.
- Lu, S., Li, Y., Shen, Q., Zhang, W., Gu, X., Ma, M., Li, Y., Zhang, L., Liu, X., and Zhang, X. (2021). Carnosol and its analogues attenuate muscle atrophy and fat lipolysis induced by cancer cachexia. J. Cachexia Sarcopenia Muscle 12, 779–795. https://doi.org/10.1002/jcsm.12710.
- Garcı´a-Lizarribar, A., Villasante, A., Lopez-Martin, J.A., Flandez, M., SolerVa´ zquez, M.C., Serra, D., Herrero, L., Sagrera, A., Efeyan, A., and Samitier, J. (2023). 3D bioprinted functional skeletal muscle models have potential applications for studies of muscle wasting in cancer cachexia. Biomater. Adv. 150. https://doi.org/10.1016/j.bioadv.2023.213426.
- Yuan, L., Han, J., Meng, Q., Xi, Q., Zhuang, Q., Jiang, Y., Han, Y., Zhang, B., Fang, J., and Wu, G. (2015). Muscle-specific E3 ubiquitin ligases are involved in muscle atrophy of cancer cachexia: An in vitro and in vivo study. Oncol. Rep. 33, 2261–2268. https://doi.org/10.3892/or.2015.3845.
- Wang, R., Kumar, B., Bhat-Nakshatri, P., Khatpe, A.S., Murphy, M.P., Wanczyk, K.E., Simpson, E., Chen, D., Gao, H., Liu, Y., et al. (2023). A human skeletal muscle stem/myotube model reveals multiple signaling targets of cancer secretome in skeletal muscle. iScience 26, 106541. https://doi.org/10.1016/j.isci.2023.106541.
- Noone, J., Rooney, M.F., Karavyraki, M., Yates, A., O’Sullivan, S.E., and Porter, R.K. (2023). Cancer-Cachexia-Induced Human Skeletal Muscle Myotube Degeneration Is Prevented via Cannabinoid Receptor 2 Agonism In Vitro. Pharmaceuticals 16, 1580. https://doi.org/10.3390/ph16111580.
- Kandarian, S.C., Nosacka, R.L., Delitto, A.E., Judge, A.R., Judge, S.M., Ganey, J.D., Moreira, J.D., and Jackman, R.W. (2018). Tumour-derived leukaemia inhibitory factor is a major driver of cancer cachexia and morbidity in C26 tumour-bearing mice. J. Cachexia Sarcopenia Muscle 9, 1109–1120. https://doi.org/10.1002/jcsm.12346.
- Chitti, S.V., Kang, T., Fonseka, P., Marzan, A.L., Stewart, S., Shahi, S., Bramich, K., Ang, C.S., Pathan, M., Gummadi, S., and Mathivanan, S. (2023). Proteomic analysis of the small extracellular vesicles and soluble secretory proteins from cachexia inducing and non-inducing cancer cells. Proteomics 23, e2100314. https://doi.org/10.1002/pmic.202100314.
- Pin, F., Barreto, R., Couch, M.E., Bonetto, A., and O’Connell, T.M. (2019). Cachexia induced by cancer and chemotherapy yield distinct perturbations to energy metabolism. J. Cachexia Sarcopenia Muscle 10, 140–154. https://doi.org/10.1002/jcsm.12360.
- Sun, N., Krauss, T., Seeliger, C., Kunzke, T., Sto¨ ckl, B., Feuchtinger, A., Zhang, C., Voss, A., Heisz, S., Prokopchuk, O., et al. (2024). Inter-organ cross-talk in human cancer cachexia revealed by spatial metabolomics. Metabolism 161, 156034. https://doi.org/10.1016/j.metabol.2024. 156034.
- Fonseca, G.W.P.d., Farkas, J., Dora, E., von Haehling, S., and Lainscak, M. (2020). Cancer cachexia and related metabolic dysfunction. Int. J. Mol. Sci. 21, 2321. https://doi.org/10.3390/ijms21072321.
- Beltra` , M., Pin, F., Ballaro` , R., Costelli, P., and Penna, F. (2021). Mitochondrial dysfunction in cancer cachexia: Impact on muscle health and regeneration. Cells 10, 1–18. https://doi.org/10.3390/cells10113150.
- Kubat, G.B., Bouhamida, E., Ulger, O., Turkel, I., Pedriali, G., Ramaccini, D., Ekinci, O., Ozerklig, B., Atalay, O., Patergnani, S., et al. (2023). Mitochondrial dysfunction and skeletal muscle atrophy: Causes, mechanisms, and treatment strategies. Mitochondrion 72, 33–58. https://doi.org/10. 1016/j.mito.2023.07.003.
- van der Ende, M., Grefte, S., Plas, R., Meijerink, J., Witkamp, R.F., Keijer, J., and van Norren, K. (2018). Mitochondrial dynamics in cancer-induced cachexia. Biochim. Biophys. Acta. Rev. Cancer 1870, 137–150. https:// doi.org/10.1016/j.bbcan.2018.07.008.
- Aversa, Z., Pin, F., Lucia, S., Penna, F., Verzaro, R., Fazi, M., Colasante, G., Tirone, A., Rossi Fanelli, F., Ramaccini, C., et al. (2016). Autophagy is induced in the skeletal muscle of cachectic cancer patients. Sci. Rep. 6, 30340. https://doi.org/10.1038/srep30340.
- Penna, F., Ballaro` , R., Martinez-Cristobal, P., Sala, D., Sebastian, D., Busquets, S., Muscaritoli, M., Argile´ s, J.M., Costelli, P., and Zorzano, A. (2019). Autophagy Exacerbates Muscle Wasting in Cancer Cachexia and Impairs Mitochondrial Function. J. Mol. Biol. 431, 2674–2686. https:// doi.org/10.1016/j.jmb.2019.05.032.
- Hemel, I.M.G.M., Engelen, B.P.H., Luber, N., and Gerards, M. (2021). A hitchhiker’s guide to mitochondrial quantification. Mitochondrion 59, 216–224. https://doi.org/10.1016/j.mito.2021.06.005.
- Biswas, A.K., and Acharyya, S. (2020). Cancer-Associated Cachexia: A Systemic Consequence of Cancer Progression. Annu. Rev. Cancer Biol. 4, 391–411. https://doi.org/10.1146/annurev-cancerbio-030419-033642.
- Law, M.L. (2022). Cancer cachexia: Pathophysiology and association with cancer-related pain. Front. Pain Res. 3, 971295. https://doi.org/10.3389/ fpain.2022.971295.
- Waning, D.L., and Guise, T.A. (2015). Cancer-associated muscle weakness: What’s bone got to do with it? BoneKEy Rep. 4, 691. https://doi. org/10.1038/bonekey.2015.59.
- Penna, F., Busquets, S., and Argile´ s, J.M. (2016). Experimental cancer cachexia: Evolving strategies for getting closer to the human scenario. Semin. Cell Dev. Biol. 54. https://doi.org/10.1016/j.semcdb.2015.09.002.
- Jalal, S., Dastidar, S., and Tedesco, F.S. (2021). Advanced models of human skeletal muscle differentiation, development and disease: Threedimensional cultures, organoids and beyond. Curr. Opin. Cell Biol. 73, 92–104. https://doi.org/10.1016/j.ceb.2021.06.004.
- Iberite, F., Gruppioni, E., and Ricotti, L. (2022). Skeletal muscle differentiation of human iPSCs meets bioengineering strategies: perspectives and challenges. NPJ Regen. Med. 7, 23–30. https://doi.org/10.1038/s41536- 022-00216-9.
- Beltra` , M., Po¨ lla¨ nen, N., Fornelli, C., Tonttila, K., Hsu, M.Y., Zampieri, S., Moletta, L., Corra` , S., Porporato, P.E., Kivela¨ , R., et al. (2023). NAD+ repletion with niacin counteracts cancer cachexia. Nat Comms 14, 1849. https://doi.org/10.1038/s41467-023-37595-6.
- Schindelin, J., Arganda-Carreras, I., Frise, E., Kaynig, V., Longair, M., Pietzsch, T., Preibisch, S., Rueden, C., Saalfeld, S., Schmid, B., et al. (2012). Fiji: an open-source platform for biological-image analysis. Nat Methods 9, 676–682. https://doi.org/10.1038/nmeth.2019.
- Thielicke, W., and Stamhuis, E.J. (2014). PIVlab – Towards User-friendly, Affordable and Accurate Digital Particle Image Velocimetry in MATLAB. J. Open. Res. Soft. 2, e30. https://doi.org/10.5334/jors.bl.
- Gagliano, O., Luni, C., Qin, W., Bertin, E., Torchio, E., Galvanin, S., Urciuolo, A., and Elvassore, N. (2019). Microfluidic reprogramming to pluripotency of human somatic cells. Nat. Protoc. 14, 722–737. https://doi.org/ 10.1038/s41596-018-0108-4.
- Maccione, A., Gandolfo, M., Massobrio, P., Novellino, A., Martinoia, S., and Chiappalone, M. (2009). A novel algorithm for precise identification of spikes in extracellularly recorded neuronal signals. J. Neurosci. Methods 177, 241–249. https://doi.org/10.1016/j.jneumeth.2008.09.026.
- Xiong, Y., Soumillon, M., Wu, J., Hansen, J., Hu, B., Van Hasselt, J.G.C., Jayaraman, G., Lim, R., Bouhaddou, M., Ornelas, L., et al. (2017). A Comparison of mRNA Sequencing with Random Primed and 3′ -Directed Libraries. Sci. Rep. 7, 14626. https://doi.org/10.1038/s41598-017-14892-x.
- Anders, S., Pyl, P.T., and Huber, W. (2015). HTSeq-A Python framework to work with high-throughput sequencing data. Bioinformatics 31, 166–169. https://doi.org/10.1093/bioinformatics/btu638.
- Dobin, A., Davis, C.A., Schlesinger, F., Drenkow, J., Zaleski, C., Jha, S., Batut, P., Chaisson, M., and Gingeras, T.R. (2013). STAR: Ultrafast universal RNA-seq aligner. Bioinformatics 29, 15–21. https://doi.org/10.1093/ bioinformatics/bts635.
- Huber, W., Carey, V.J., Gentleman, R., Anders, S., Carlson, M., Carvalho, B.S., Bravo, H.C., Davis, S., Gatto, L., Girke, T., et al. (2015). Orchestrating high-throughput genomic analysis with Bioconductor. Nat. Methods 12, 115–121. https://doi.org/10.1038/nmeth.3252.
- Love, M.I., Huber, W., and Anders, S. (2014). Moderated estimation of fold change and dispersion for RNA-seq data with DESeq2. Genome Biol. 15, 550. https://doi.org/10.1186/s13059-014-0550-8.
¶ STAR★方法
¶ 关键资源表
| REAGENT or RESOURCE | SOURCE | IDENTIFIER |
| Antibodies | ||
| Rabbit anti-NANOG (D73G4) XP | CellSignaling | Cat# 4903; RRID: AB_10559205 |
| Mouse anti-OCT4 (C30A3) | Cell Signaling | Cat# 2840; RRID: AB_2167691 |
| Rabbit anti-SOX2 | Milipore | Cat# AB5603; RRID: AB_2286686 |
| Goat anti-T/Bra | R&D System | Cat# AF2085; RRID: AB_2200235 |
| Rabbit anti-Desmin | Abcam | Cat# AB15200; RRID: AB_301744 |
| Mouse anti-β tubulin Il/Tuj1 | Biolegend | Cat# MMS-435P; RRID: AB_2313773 |
| Mouse anti-Myosin Heavy Chain | DSHB | Cat# MF-20; RRID: AB_2147781 |
| Rabbit anti-62 | Sigma Aldrich | Cat# P0067; RRID: AB_1841064 |
| Rabbit anti-C3 | Sigma Aldrich | Cat# L7543; RRID: AB_796155 |
| Rabbit anti-TOM20 (D8T4N) | Cel Signaling | Cat# mAb#42406; RRID: AB_2687663 |
| Rat anti-LAMP1 | DHSB | Cat# 1D4B; RRID: AB_2134500 |
| Chemicals,peptides,and recombinant proteins | ||
| StemMACS iPS-Brew XF | Miltenyi Biotec | Cat# 130-104-368 |
| DMEM 1× | Thermo Fisher | Cat# 41966029 |
| RPMI 1640 | Thermo Fisher | Cat# 11875093 |
| DMEM F-12 | Thermo Fisher | Cat# 11320074 |
| MiR05 | Oroboros Instruments | Cat# 60101-01 |
| Penilin-Streptomycin | Thermo Fisher | Cat# 15140122 |
| MEM Non-Essential Amino Acids | Thermo Fisher | Cat# 11140035 |
| Insulin-Transferring-Selenium | Thermo Fisher | Cat# 41400045 |
| 2-Mercaptoethanol | Thermo Fisher | Cat# 31350010 |
| KSR | Thermo Fisher | Cat# 10828028 |
| Matrigel | Corming | Cat# 354230 |
| TrypLE | Thermo Fisher | Cat# 12563029 |
| EDTA | Thermo Fisher | Cat# AM9260G |
| L-Glutamine | Thermo Fisher | Cat# 25030081 |
| FBS | Thermo Fisher | Cat# A5256701 |
| Sodium pyruvate | Thermo Fisher | Cat# 11360070 |
| Y-27632 | Miltenyi Biotec | Cat# 130-106-538 |
| CHIR 99021 | Bio-Techne | Cat# 4423/10 |
| LDN-193189 | Miltenyi Biotec | Cat# 130-103-925 |
| FGF-b/FGF-2 | ImmunoTools | Cat# 11343625 |
| IGF-1 | Miltenyi Biotec | Cat# 130-093-886 |
| HGF | ImmunoTools | Cat# 11343413 |
| CNTF | PeproTech | Cat# 450-13 |
| GDNF | PeproTech | Cat# 450-10 |
| Acetylcholine | Sigma Aldrich | Cat# A6625 |
| Fluo-4 | Thermo Fisher | Cat# F14201 |
| Pluronic F-127 | Thermo Fisher | Cat# P3000MP |
| Hoechst | Thermo Fisher | Cat# 33342 |
| ADP | Sigma Aldrich | Cat# 01897 |
| Digitonin | Sigma Aldrich | Cat# 300410 |
| Pyruvate | Sigma Aldrich | Cat# P2256 |
| REAGENT or RESOURCE | SOURCE | IDENTIFIER |
| Malate | Sigma Aldrich | Cat# M1000 |
| Succinate | Sigma Aldrich | Cat# S2378 |
| Rotenone | Sigma Aldrich | Cat# R8875 |
| CCCP | Sigma Aldrich | Cat# C2759 |
| Antimycin A | Sigma Aldrich | Cat# A8674 |
| OCT | Sakura | Cat# 4583 |
| Alexa 647 Conjugate α-bungarotoxin | Thermo Fisher | Cat# B35450 |
| Alexa 647 Conjugate biotinylated phalloidin | Thermo Fisher | Cat# A22287 |
| Critical commercial assays | ||
| RNA Extraction RNeasy Kit | QIAGEN | Cat# 74034 |
| High-capacity cDNA RT Kit | Thermo Fisher | Cat# 4368814 |
| RNASEOUT Recomb. RNASE Inhib. | Thermo Fisher | Cat# 10777019 |
| Powrup SYBR Master Mix | Thermo Fisher | Cat# A25776 |
| Live-dead cellviability kit | Sigma Aldrich | Cat# CBA415 |
| Deposited data | ||
| Bulk RNA-seq data (already published) | GEO: GSE226477 | https://www.ncbi.nlm.nih.gov/geo/query/ acc.cgi?acc=GSE226477 |
| Experimental models: Cellines | ||
| BJ15 cl44 | Elvassore N. Lab | DOl: https://doi.0rg/10.1002/adhm.202404111 |
| BJ15 cl21 | Elvassore N. Lab | DOl: https://doi.0rg/10.1038/s42003-025-08484-z |
| MC38 | Marigo I. Lab | DOl: https://doi.0rg/10.1038/s41422-019-0224-x |
| C26 | Costelli P. Lab | DOI: https:/doi.org/10.3390/cancers13133285 |
| Oligonucleotides | ||
| Primers used for qPCR | This study | Data S2 |
| Software and algorithms | ||
| Fij | Schindelin et al.64 | https://imagej.net/Fiji |
| GraphPad Prism | GraphPad | https://www.graphpad.com/scientific-software/prism/ |
| PIViab | Thielicke and Stamhuis65 | https://www.pivlab.de |
| Other | ||
| Biofloat 96-well plate | Sarstedt | Cat. No.: 83.3925.400 |
¶ 实验模型和研究参与者详情
¶ 人类诱导多能干细胞的诱导和培养
本研究中所有的人类诱导多能干细胞系(野生型或组成型表达绿色荧光蛋白)均已发表16,19,它们是通过微流体技术重编程包皮成纤维细胞系(BJ;男性)获得的66。人类诱导多能干细胞在无饲养层条件下培养,培养板(6孔板,Sarstedt)预先用0.5%基质胶(MRF,Corning)包被,培养基为StemMACS iPS-Brew XF(Miltenyi Biotec),并添加1%青霉素/链霉素(P/S;Gibco-Fisher Scientific),培养环境为37℃、5%二氧化碳的细胞培养箱。所有细胞系均经检测确认无支原体污染,且在用于分化实验前传代次数均控制在30代以内。对于绿色荧光蛋白阳性的人类诱导多能干细胞,在12代时用慢病毒载体进行转导,该载体编码绿色荧光蛋白和嘌呤霉素抗性基因,受PGK启动子调控19。
¶ 人诱导多能干细胞的分化与培养
二维分化方案和样本表征先前已有报道。16 为生成神经肌器官(NMO),我们采用了先前研究中的人诱导多能干细胞(hiPSC)分化为神经肌肉的方案。16,19 具体来说,将基质胶液滴接种在无菌玻璃盖玻片(Vetrotecnica)上,形成1平方厘米的液滴,然后放入24孔板(Sarstedt)中。将液滴在细胞培养箱中于37°C孵育20分钟,使基质胶聚合。分化前两天(第-2天),使用TryplE Select(Gibco)将人诱导多能干细胞酶解为单细胞。将40,000个细胞重悬于50μL添加了10μM StemMACS Y27632的StemMACS iPS-Brew XF中,接种到基质胶液滴上,在37°C和5% CO₂条件下孵育90分钟,之后再补充培养基。分化前一天(第-1天),更换培养基,将细胞在StemMACS iPS-Brew XF中培养。分化方案从第0天开始,根据我们已发表的方案,改编自使用小分子和生长因子的文献研究。24,16,19 值得注意的是,不同细胞培养设置中使用的细胞密度(每平方厘米的细胞数量)是相同的。简而言之,从第0天到第2天,培养基更换为杜尔贝科改良 eagle 培养基/营养混合物F-12(DMEM F-12,Gibco)基础培养基,并添加胰岛素-转铁蛋白-硒(ITS,Gibco)、1%青霉素-链霉素(Gibco)、3μM WNT激动剂CHIRON99021(Miltenyi Biotec)和0.5μM BMP拮抗剂LDN193189(Miltenyi Biotec)。从第3天到第5天,向培养基中补充20 ng/mL的成纤维细胞生长因子2(FGF-2,Immunotools)。第6天,将球状体从基质胶液滴上机械分离,并将4-6个球状体包埋到一个基质胶液滴中进行扩增。从第6天开始,培养基更换为DMEM F-12,并添加15% Knockout™血清替代物(KSR,Gibco)、10 ng/mL肝细胞生长因子(HGF,ImmunoTools)、2 ng/mL胰岛素样生长因子1(IGF-1,Miltenyi Biotec)、20 ng/mL FGF-2和0.5μM LDN193189。从分化的第8天到第11天,细胞在添加了15% KSR和2 ng/mL IGF-1的DMEM F-12中培养。从第12天开始,对之前的培养基进行调整,加入10 ng/mL HGF和2 ng/mL IGF-1。从第18天起,将神经肌器官转移到超低吸附96孔板中,在培养箱的轨道摇床上培养。从第22天开始,神经肌器官在肌源性次级分化培养基(最佳神经肌器官分化培养基,UNT)中培养,该培养基由DMEM F-12组成,并添加2% KSR、1×ITS、1%青霉素-链霉素、1μM CHIRON99021、10 ng/mL睫状神经营养因子(CNTF;PeproTech)和10 ng/mL胶质细胞源性神经营养因子(GDNF;PeproTech),直至第50天。
¶ 小鼠结肠腺癌细胞系的培养
我们使用了两种小鼠结肠癌细胞系,分别是源自BALB/c小鼠结肠腺癌的colon-26(C26)结肠癌细胞系和源自C57BL/6小鼠结肠腺癌的colon-38(MC38)结肠癌细胞系。C26细胞在高糖DMEM培养基(Gibco)中培养,该培养基添加了10%胎牛血清(FBS,Gibco)、1%青霉素/链霉素(100 U/mL青霉素、0.1 mg/mL链霉素)。MC38细胞在RPMI 1640培养基(Gibco)中培养,该培养基添加了10%胎牛血清、1%青霉素/链霉素、2 mM L-谷氨酰胺、1 mM丙酮酸钠和0.1 mM MEM非必需氨基酸。细胞在37°C、含5% CO₂的 humidified atmosphere中培养。所有实验均使用低传代细胞进行。
¶ 方法详情
¶ 用C26和MC38条件培养基处理NMO
为收集条件培养基,将C26细胞或MC38细胞接种并培养至汇合度约90%。随后,C26细胞的培养基更换为无血清DMEM,MC38细胞的培养基更换为无血清RPMI 1640,两种培养基均含有抗生素和谷氨酰胺,细胞继续培养24小时。之后收集条件培养基,在4℃下以4500转/分钟的速度离心15分钟,通过0.22μm滤器过滤后用于神经类器官(NMOs)。从第50天起,将神经类器官培养在200μL的条件培养基(C26-CM、MC38-CM)、基础培养基(C26-BM、MC38-BM)或最佳神经类器官分化培养基(UNT)中。基础培养基为C26或MC38细胞的常规生长培养基(不含细胞培养物)。处理持续72小时,直至类器官培养的第53天。在整个处理期间,使用LSM800倒置共聚焦显微镜(蔡司)监测GFP阳性神经类器官,以追踪其随时间发生的形态和荧光变化。
¶ 免疫荧光分析和图像制备
类器官在室温下用4%多聚甲醛固定1小时,然后用PBS洗涤5分钟。样本以整装形式进行分析,或包埋于OCT(樱花)中,冷冻切片成30微米的切片。样本在室温下用含1%牛血清白蛋白、0.5%曲拉通X-100(Sigma)的1×PBS溶液(PBST)封闭2小时。一抗稀释于1%牛血清白蛋白PBST溶液中,在4℃下振荡孵育48小时(整装样本)或过夜(冷冻切片)。之后,整装染色样本在振荡板上用1×PBST溶液洗涤3次,每次30分钟,然后与二抗在4℃下孵育48小时(整装样本)或在室温下孵育2小时(冷冻切片),随后用1×PBS洗涤两次,每次30分钟。细胞核用10μg/mL的Hoechst(赛默飞世尔)进行复染。使用LSM800倒置共聚焦显微镜(蔡司)获取图像。我们使用ImageJ软件进行图像的亮度和对比度调整以及通道合并。
¶ 收缩和钙动力学的实时成像分析
所有活体成像分析均按照已发表的实验方案,使用配备PLANAP0 1.0×物镜的Leica M205 FCA体视显微镜进行,采集速率为每秒16帧。16,19 必要时,用终工作浓度为10μM的乙酰胆碱(ACh)神经递质刺激样本。
在钙实验中,样本按照说明书和文献使用Fluo-4-AM(Invitrogen)进行处理。16,19简而言之,用PBS洗涤后,将样本与20μM Fluo-4-AM、5μL/mL PluronicTM F-127(赛默飞世尔科技)和12.5μL/mL磺吡酮(Sigma-Aldrich)在无血清细胞培养基中于37℃和5% CO₂条件下孵育30分钟。然后,用不含KSR的肌源性次级分化培养基精确洗涤样本,并进行活细胞成像分析。
¶ 多电极阵列(MEA)测定法
使用CorePlateTM 6W 38/60和BioCAM DupleX(3Brain公司)进行细胞外记录,其有效面积为14.44平方毫米。电极长度为25微米,在64×64的网格中以60微米的间距(节距)排列,便于记录瞬时细胞外电压信号。将D50神经微球(NMOs)加载到培养室中进行单个NMO分析。在急性模式下测量信号,并在稳定条件(37°C、5% CO₂)下记录2分钟的自发性电活动。数据以20 kHz的采样率收集并存储,用于离线分析。使用精确计时 spike 检测(PTSD)算法67进行 spike 检测,差分阈值设置为标准差的8倍。
¶ 活死分析
在活细胞和死细胞实验中,按照协议说明,使用适用于3D和2D细胞培养的活死细胞活力检测试剂盒(Millipore)处理神经运动单元。简要来说,将样本与0.4 μL/mL、1.6 μL/mL的碘化丙啶在1:1的细胞培养基和PBS溶液中混合,在37℃、5% CO₂的条件下孵育60分钟。然后用肌源性次级分化培养基精确洗涤样本,并进行活体成像分析。活体成像按照先前在整装样本中描述的方法进行。
¶ 腺病毒感染
AdV-c.a.FoxO3此前已在体内使用并得到验证。33 每个NMO都用添加到培养基中的107 vg的AdV-c.a.FoxO3或AdV-GFP(用作阴性对照)处理。
¶ RNA纯化和逆转录定量聚合酶链反应
按照制造商的说明和先前的研究,使用RNeasy Plus Mini Kit(Qiagen)分离和纯化总细胞RNA。16,19简而言之,通过在细胞培养孔中直接裂解收获神经微球(NMOs),并根据方案进一步处理。使用Nanodrop(赛默飞世尔科技)评估提取的RNA质量和浓度。使用高容量cDNA逆转录试剂盒(Applied Biosystems)在专用热循环仪(Mastercycler ×50a,Eppendorf)中获得第30天和第50天神经微球的互补DNA(cDNA)。根据制造商的说明,使用QuantStudioTM 5实时PCR(赛默飞世尔科技)和Platinum SYBR Green SuperMix试剂盒组件(Invitrogen,11733-038)对神经标志物的表达进行定量。所有使用的引物列于数据S2中。
¶ 批量测序分析
使用Qubit 4.0荧光测定法(赛默飞世尔科技公司)对总RNA进行定量。使用NEGEDIA数字mRNA-seq研究级测序服务(Next Generation Diagnostic srl),从125 ng总RNA中制备文库,该服务包括文库制备、质量评估以及在NovaSeq 6000测序系统上采用单端100循环策略(Illumina公司)进行测序。原始数据由Next Generation Diagnostic srl的专有NEGEDIA数字mRNAseq流程(v2.0)分析,该流程包括通过质量过滤和修剪进行的清洗步骤、与参考基因组的比对以及按基因计数。
¶ 空间代谢组学分析
收集神经运动性器官(NMOs)并包埋在2–3%的羧甲基纤维素中,随后进行冷冻(置于液氮中的异戊烷浴),并储存在密封容器中,温度为-80℃。切取10μm厚的冷冻切片,将其安装在导电的IntelliSlides(布鲁克道尔顿公司,德国不来梅)上,在施加基质前,于室温下在真空干燥器中干燥30分钟。1,5-二氨基萘盐酸盐基质的制备方法如先前所述(Liu等人,2014):将39.5mg的1,5-DAN溶解在500μL的1M盐酸和4mL的蒸馏水中,超声处理后加入4.5mL乙醇。
使用HTX M5-SprayerTM(HTX Technologies公司),其流速为0.08 mL/min,喷嘴温度为70℃,喷嘴速度为1300 mm/min。在timsTOF fleX MALDI-2质谱仪(德国不来梅市布鲁克道尔顿公司)上以负离子模式进行MALDI-MSI分析,m/z范围为70–850,空间分辨率为10 μm,激光频率为10 kHz。使用多种代谢物和基质峰的m/z比值进行在线校准,并使用红磷进行外部校准。
¶ 高分辨率呼吸测定法
使用NextGen-O2k(奥地利因斯布鲁克Oroboros仪器公司)测量BM和CM类器官的氧通量,并使用DatLab 8.0(Oroboros仪器公司)进行记录。通过极谱氧传感器(POS)随时间监测氧信号,并持续绘制神经中胚层类器官(NMOs)的氧消耗量。2毫升O2k chambers的极谱氧传感器(POS)每天在37℃的实验温度下进行校准(空气校准)。所有实验均在 mitochondrial respiration medium MiR05中进行。将神经中胚层类器官(NMO)加入0.5毫升 chambers后,加入1.25 mM ADP,并用0.1μg洋地黄皂苷进行通透处理。加入1.25 mM丙酮酸和0.5 mM苹果酸,随后加入2.5 mM琥珀酸。用0.125μM鱼藤酮阻断与复合体I(CI)相关的呼吸,通过解偶联剂三氟甲氧基苯基腙(CCCP)(0.25μM/步)滴定评估电子传递能力。加入0.25μM抗霉素A可完全抑制呼吸。对于所有轨迹,仅选择氧通量的稳态,排除因化学物质添加或孵育介质的间歇性复氧导致的不可避免的滴定伪影。氧消耗数据以线粒体DNA(mtDNA)的拷贝数进行标准化。
¶ 量化与统计分析
细胞类型百分比和肌隔比例的量化是根据文献进行的。16,19 对于NMO区域的量化,我们在ImageJ上应用了“Find Edges”功能,然后使用徒手选择工具对NMO进行分割,随后使用“Measure”功能。为了量化NANOG+OCT4+、NANOG-OCT4-、TBRA+SOX2+、TBRA+SOX2-和TBRA-SOX2+的数量,我们使用了ImageJ软件(Fiji,v.2.14.0/1.54f)的细胞计数工具。每种染色的阳性细胞数量以每个视野中计数的细胞核总数的百分比表示。对于肌管厚度的量化,使用Fiji软件中ImageJ的“measure”功能进行分析。我们在处理前和处理期间通过GFP+NMO的实时成像分析进行量化。具体而言,分析了6至13个独立的生物学重复(NMO),考虑每个NMO沿每个显示出典型肌管伸长形态的细胞量化的3个横截面的平均值,每个实验条件的每个时间点至少分析160个细胞。在实验结束时(处理后72小时),对整装结蛋白染色的类器官也进行了肌管横截面的量化。在这里,每个条件分析8个独立的生物学重复(NMO),每个NMO至少考虑30个肌管,每个实验条件总共分析≥240个肌管。每个肌管横截面的量化是通过沿每个单个肌管长度进行的3次横截面测量的平均值计算得出的。结蛋白阳性细胞的代表性图像是通过在ImageJ上使用“Find Edges”功能分离单个肌管,然后通过“Clear Outside”去除背景获得的。对于肌肉区域量化和碘化丙啶阳性区域量化,我们使用“Threshold”功能选择阳性区域,然后使用ImageJ的“Measure”功能。为了量化荧光强度,通过在没有任何可检测荧光信号的区域选择三个感兴趣区域(ROI)来估计背景荧光。使用ImageJ的“Measure”工具获取每个ROI的平均荧光强度,然后取平均值来定义相应图像的背景荧光水平。所报告的荧光强度量化是通过从每个图像的平均荧光强度中减去背景值计算得出的。对于线粒体形态分析,每个生物学重复至少获取8张图像,并通过ImageJ的“Mitochondria analyzer”插件进行分析。对于共定位分析,每个生物学重复至少获取8张图像,并通过ImageJ的“Colocalization threshold”插件进行分析。对于TOM20骨架图像,我们应用ImageJ的“Skeletonize”插件生成掩码。为了量化P62和LC3b斑点,每个生物学重复考虑至少8张图像,在ImageJ上使用“Threshold”功能选择后,通过“Particle analyze”插件进行分析。
在定量实时聚合酶链式反应中,基因表达的目标循环阈值(Ct值)以管家基因GAPDH或TUBB3的Ct值进行标准化。数据以相对于D30 NMO样本的基因表达相对倍数变化呈现,采用2−ΔΔCT法。使用R 4.3.3版本及Bioconductor 3.71版本进行生物信息学分析。通过R包org.Hs.e.g.,.db 3.18版本对基因进行注释。若基因在同一培养条件下至少2个重复样本的原始计数均不低于2,则将其过滤掉。随后使用R包DESeq2 1.42.72版本对原始计数进行标准化,并以每百万次计数(CPM)表示。为避免出现无穷大值,通过添加1个伪计数获得对数2尺度的CPM数据。主成分分析(PCA)通过R统计包中的prcomp函数进行,该函数在中心化后采用奇异值分解(SVD)。差异表达基因(DEGs)通过DESeq2从原始计数数据中计算得出,采用Benjamini-Hochberg法校正后的P值低于0.01的基因被视为差异表达基因。使用R包pheatmap 1.0.12版本,采用欧氏距离进行层次聚类及热图可视化。所示基因集来源于Reactome数据库(https://reactome.org/)。
在钙ΔF/F0计算中,根据文献,每个样本选择≥30个大小为20 μm²的感兴趣区域(ROI),以确定基线(神经递质刺激前,F0)和最大(神经递质刺激后,Fpeak)荧光强度值。16,19简而言之,我们对输出的LAS X.csv文件使用了MATLAB 2021软件(MathWorks)的最大值和平均值函数。ΔF/F0的计算将ΔF视为Fpeak减去F0,其中Fpeak是神经递质刺激时测得的最大荧光强度,F0为基线。对于钙瞬变分析,选择了4个用于钙ΔF/F0计算的代表性ROI。根据文献,使用LAS X徕卡软件和MATLAB 2021软件(MathWorks)分析ROI的荧光强度变化。16,19
在矢量图生成和位移测量方面,根据文献,使用了基于图形用户界面(GUI)的粒子图像测速软件(PIVlab)3.07版本。16,19 简而言之,在实时成像分析期间获取的选定帧对经过互相关处理,以生成矢量图和局部位移。具体而言,通过对收缩前获取的帧对和神经肌肉器官(NMOs)最大位移时获取的帧对进行互相关,来量化最大位移。使用自定义的R(4.3.1版本)脚本及ggplot2 3.5.1版本包,绘制了显示每个样本的位移与矢量方向之间关系的极坐标图。所有提及的MATLAB算法的源代码可在MATLAB文档、GraphPad Prism 6版本、根据开源GNU GPL 3.0许可授权的ImageJ插件中找到。所有脚本和自定义代码可向作者索取。
使用FlexImaging 7.0软件(布鲁克)获取质谱图像。使用SCiLS Lab 2025b(布鲁克)对数据进行分析,质量精度为±15 ppm,不进行去噪,并采用均方根归一化。将光谱数据和感兴趣区域导出至MetaboScape 2025(布鲁克),并使用MetaboScape自定义数据库对质荷比进行注释,质量精度为±10 ppm。随后使用shinyapps制作实验条件间的统计箱线图和热图。
为了进行线粒体DNA(mtDNA)定量分析,提取了总DNA,并通过SYBR Green实时聚合酶链式反应(PCR)分析了线粒体DNA的拷贝数。对样本的核DNA(nDNA)含量进行了校正。采用比较法(2ΔΔCT)确定相对线粒体DNA含量。线粒体DNA的寡核苷酸引物针对MT-ND4设计,而B2M的寡核苷酸引物用于核基因组的标准化。所有使用的引物均列于数据S2中。
所有统计分析均使用GraphPad prism 6进行。我们将数据表示为多个生物学重复的平均值±标准差(如图例所示)。我们通过方差不等的Student t检验、单因素方差分析(ANOVA)、双尾嵌套t检验和Tukey多重比较检验确定统计显著性,这些检验在图例和数据S2中均有显示。p值小于0.05被认为具有统计学显著性。
¶ 补充信息
¶ 人类神经肌肉类器官模拟
¶ 癌症诱导的肌肉恶病质
皮埃特罗·基奥利奥、比阿特丽斯·奥莱塔、卡米拉·佩齐尼、路易吉·萨尔托雷、乔治·格雷戈隆、奥尼利亚·加利亚诺、拉特萨、瓦莱里娅·罗克珊娜·巴尔马塞达·巴尔德斯、达维德·卡奇亚雷利、卡米拉·卢尼、卡洛·维斯科米、梅兰妮·普兰克、萨拉-玛丽亚·芬特、马尔科·桑德里、罗伯塔·萨托里和安娜·乌尔西奥洛
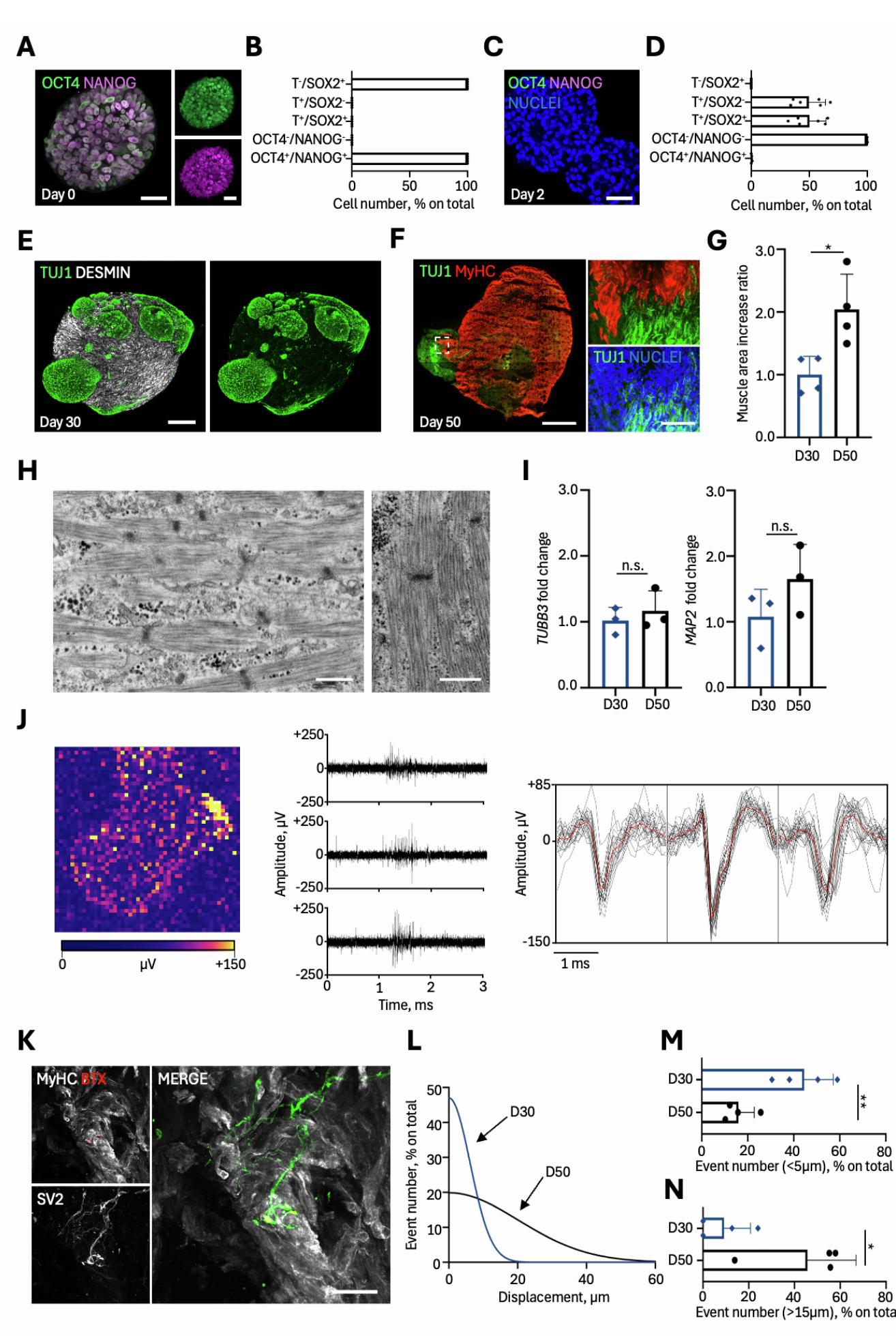
图S1. 图1中所报道的神经肌肉类器官(NMOs)的表征。A. 代表性共聚焦免疫荧光图像,显示人诱导多能干细胞(hiPSC)分化第0天时的多能细胞(共表达OCT4和NANOG)。比例尺,40 μm。B. 人诱导多能干细胞分化第0天时鉴定出的T-/SOX2+、T+/SOX2-、T+/SOX2+、NANOG-OCT4-、NANOG+OCT4+细胞的定量分析。定量结果以阳性细胞占总细胞核的百分比表示,数据为≥5次独立重复实验的平均值±标准差。C. 人诱导多能干细胞分化2天后OCT4和NANOG的代表性共聚焦免疫荧光图像。比例尺,40 μm。D. 人诱导多能干细胞分化2天后鉴定出的T-/SOX2+、T+/SOX2-、T+/SOX2+、NANOG-OCT4-、NANOG+OCT4+细胞的定量分析。定量结果以阳性细胞占总细胞核的百分比表示,数据为6次独立重复实验的平均值±标准差。E. 分化30天后神经肌肉类器官的代表性Z-stack共聚焦免疫荧光图像,整体 mounts 染色显示TUJ-1(绿色)和结蛋白(灰色)。仅显示结蛋白染色的图像见图1D。比例尺,320 μm。F. 分化50天后神经肌肉类器官的代表性Z-stack共聚焦免疫荧光图像,横截面染色显示TUJ-1(绿色)和肌球蛋白重链(MyHC,红色)。比例尺,600 μm(左图)和85 μm(右图)。G. 第30天(D30)和第50天(D50)神经肌肉类器官中肌肉阳性区域(μm²)的定量分析。数据为4次独立重复实验的平均值±标准差。采用异方差Student’s t检验确定统计学显著性;*p = 0.0168。H. 显示第50天神经肌肉类器官切片中肌节结构的代表性电子显微镜图像。比例尺,500 nm。I. 第30天(D30)和第50天(D50)神经肌肉类器官中TUBB3和MAP2基因的表达。数据分别以GAPDH和TUBB3基因表达为参照进行标准化,并以第50天相对于第30天神经肌肉类器官的倍数变化表示。数据为3次独立生物学重复实验的平均值±标准差。采用异方差Student’s t检验;n.s. 无显著性差异。平均CT值和相对标准偏差列于数据S2中。J. 左图,在基础条件下,使用3Brain多电极阵列(MEA)系统记录的第50天神经肌肉类器官的平均电压振幅代表性活动图。振幅强度根据电压刻度(µV)进行颜色编码。另见视频S1。中图,在3Brain多电极阵列系统基础活动记录期间,第50天神经肌肉类器官中的代表性尖峰事件。每条轨迹对应于单个电极的原始信号。右图,来自各个电极的代表性尖峰波形。每个图显示3个独立电极的尖峰振幅(µV)随时间(ms)的变化;红线表示平均波形。K. 分化50天后神经肌肉类器官的代表性Z-stack共聚焦免疫荧光图像,染色显示肌球蛋白重链(灰色)、SV2(左图:灰色,右图:绿色)和α-银环蛇毒素(BTX,红色)。比例尺,20 µm。L. 在第30天(D30,蓝线)和第50天(D50,黑线)GFP+神经肌肉类器官中,乙酰胆碱(ACh)刺激后记录的位移事件在0 μm至最大60 μm范围内、5 μm间隔的频率分布的高斯插值。M. 第30天和第50天神经肌肉类器官中,在0-5 μm范围内乙酰胆碱诱导的位移向量频率分布。数据为每种条件下4个神经肌肉类器官的平均值±标准差,每个点代表一个神经肌肉类器官。采用异方差Student’s t检验确定统计学显著性;**p = 0.0073。N. 第30天和第50天神经肌肉类器官中,在>15 μm范围内乙酰胆碱诱导的位移向量频率分布。数据为每种条件下4个神经肌肉类器官的平均值±标准差,每个点代表一个神经肌肉类器官。采用异方差Student’s t检验确定统计学显著性;*p = 0.0234。
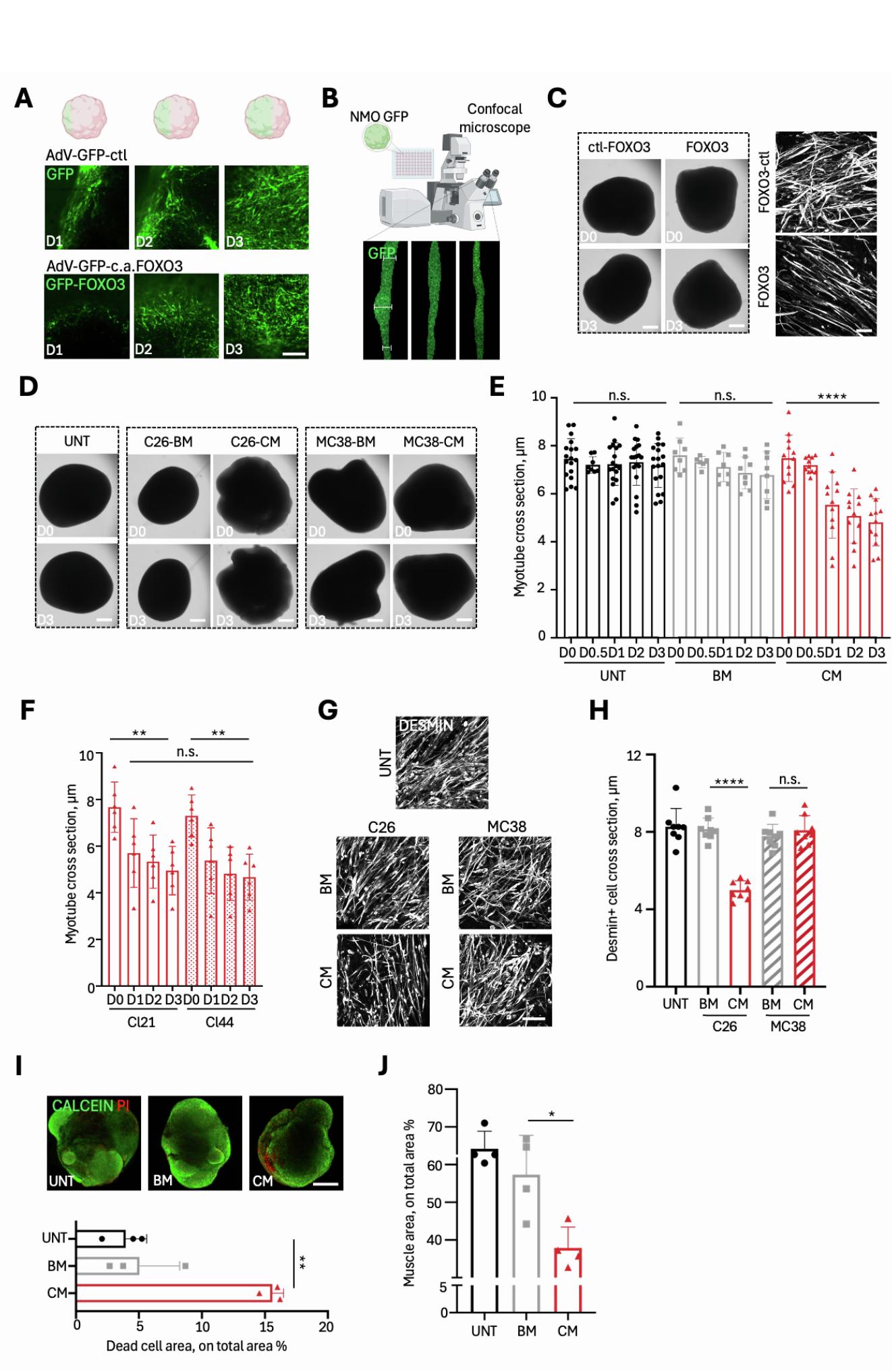
图S2. 图2中所报道的UNT、BM-C26、CM-C26、BM-MC38、CM-MC38神经肌肉类器官(NMOs)的表征。A. 感染后1、2和3天(D1、D2和D3),经AdV-GFP和AdV-GFP-c.a.FOXO3处理的NMOs的代表性共聚焦图像。比例尺,200 μm。B. 示意图展示了在时间进程活体成像分析中,用于量化处理后的NMOs和对照组中GFP+肌管横截面的策略。C. 左图,代表性明场(BF)图像显示了AdV-GFP-ctl(ctl-FOXO3)和AdV-GFP-c.a.FOXO3(FOXO3)处理前(D0)和处理72小时(D3)时NMOs的形态。比例尺,500 μm。右图,经D3 ctl-FOXO3和D3 FOXO3处理的NMOs的结蛋白(灰色)染色的代表性Z-stack共聚焦免疫荧光图像。比例尺,50 μm。D. 代表性明场图像显示了经C26和MC38的BM及CM处理前(D0)和处理72小时(D3)时NMOs的形态。作为对照,在UNT条件下平行进行实验。比例尺,500 μm。E. 与UNT条件相比,C26-BM和CM处理前(D0)及处理后12小时(D0.5)、24小时(D1)、48小时(D2)和72小时(D3)时GFP+肌管横截面的量化(图2F中报道)。数据以每个时间点每个NMO的平均肌管横截面直径的平均值±标准差表示。每个点代表从单个NMO获得的平均值,其中对≥20个肌管横截面进行了量化并取平均值。每个NMO测量3张图像。每个条件下共分析≥6个独立的NMOs。采用普通单因素方差分析确定统计学显著性;***p < 0.0001。统计结果详见数据S2。F. 从BJ来源的人诱导多能干细胞的两个不同克隆(cl21和cl44)生成的NMOs在C26-CM处理前(D0)及处理后24小时(D1)、48小时(D2)和72小时(D3)时GFP+肌管横截面的量化。每个点代表从单个NMO获得的平均值,其中对≥20个肌管横截面进行了量化并取平均值。此处报道的数据也包含在图2F分析的样本组中。每个NMO测量3张图像。每个条件下共分析≥6个独立的NMOs。采用普通单因素方差分析确定统计学显著性;cl21,**p = 0.0015;cl44,**p = 0.0051。统计结果详见数据S2。G. UNT NMOs以及经C26和MC38的BM/CM处理72小时的NMOs的结蛋白(灰色)代表性Z-stack共聚焦免疫荧光图像。比例尺,75 μm。H. 经C26和MC38来源的BM及CM处理72小时后,GFP+第50天NMOs中结蛋白+肌管横截面的量化。作为对照,在UNT条件下平行进行分析。数据以每个条件下240个肌管横截面的平均值±标准差表示,每个NMO测量≥3张图像,每个条件下分析8个独立的NMOs。数据来源于图2G中分析的样本。采用普通单因素方差分析确定统计学显著性;****p < 0.0001。统计结果详见数据S2。I. 经C26来源的BM及CM处理72小时后,NMOs的钙黄绿素和碘化丙啶(PI)染色的代表性共聚焦图像(上图),以及死细胞面积(碘化丙啶阳性面积)的量化(下图)。作为对照,在UNT条件下平行进行分析。比例尺,500 μm。数据以每个条件下3个独立NMOs的平均值±标准差表示。采用普通单因素方差分析确定统计学显著性;**p = 0.0023。统计结果详见数据S2。J. 经C26来源的BM及CM处理72小时后,NMOs肌肉面积的量化。作为对照,在UNT条件下平行进行分析。数据以每个NMO 2张整装图像的平均值±标准差表示,每个条件下分析4个独立的NMOs。采用普通单因素方差分析确定统计学显著性;*p = 0.0116。统计结果详见数据S2。
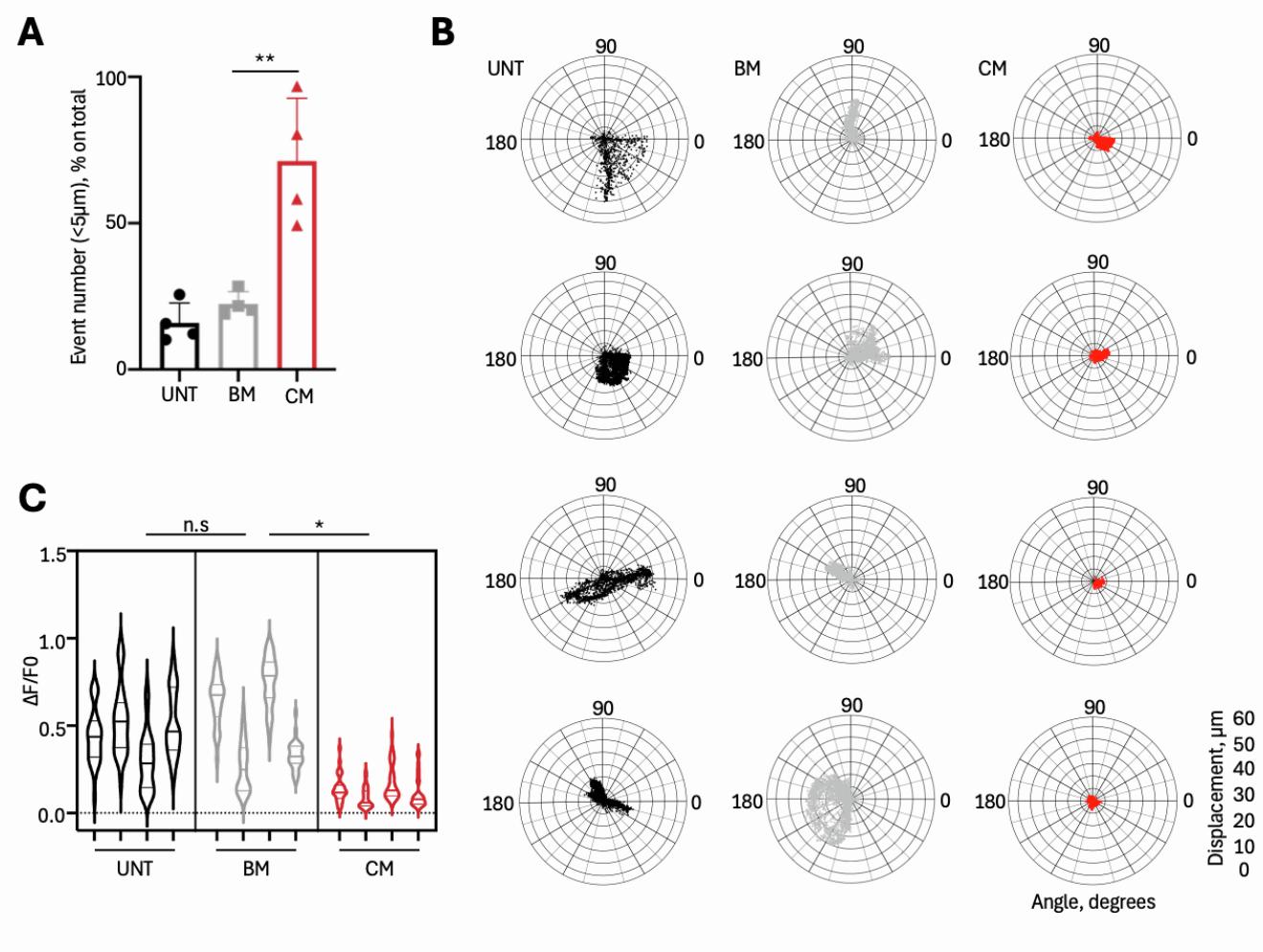
图S3. 图3中所报道的UNT、BM-C26、CM-C26、神经肌肉类器官(NMOs)的表征。A. 在经C26来源的BM和CM处理72小时后,用乙酰胆碱(ACh)刺激的GFP+第53天神经肌肉类器官中,1-5μm范围内乙酰胆碱诱导的位移向量频率分布。作为额外对照,对UNT条件进行了分析。数据以4个神经肌肉类器官/条件的平均值±标准差表示,每个点代表单个神经肌肉类器官。采用普通单因素方差分析(Ordinary One-way ANOVA)确定统计学显著性;**p=0.0014。统计结果详见数据S2。B. 代表性极坐标图显示,经C26来源的BM和CM处理72小时后,用PIVlab分析GFP+第53天神经肌肉类器官在乙酰胆碱刺激下的最大位移(μm)和位移方向性(角度,度)的量化结果。作为额外对照,对UNT条件进行了分析。图中显示了与图3F所报道数据相关的单个神经肌肉类器官。C. 小提琴图显示,经C26来源的BM和CM处理72小时后,与UNT条件相比,用Fluo-4活体成像分析GFP+第53天神经肌肉类器官在乙酰胆碱刺激下检测到的钙峰幅度(ΔF/F0)的量化结果。数据来自图3H中分析的样本。每个小提琴图代表单个神经肌肉类器官(4个神经肌肉类器官/条件)的钙峰平均值(n=30)。采用嵌套单因素方差分析(nested one-way ANOVA)确定统计学显著性;*p=0.0188。统计结果详见数据S2。
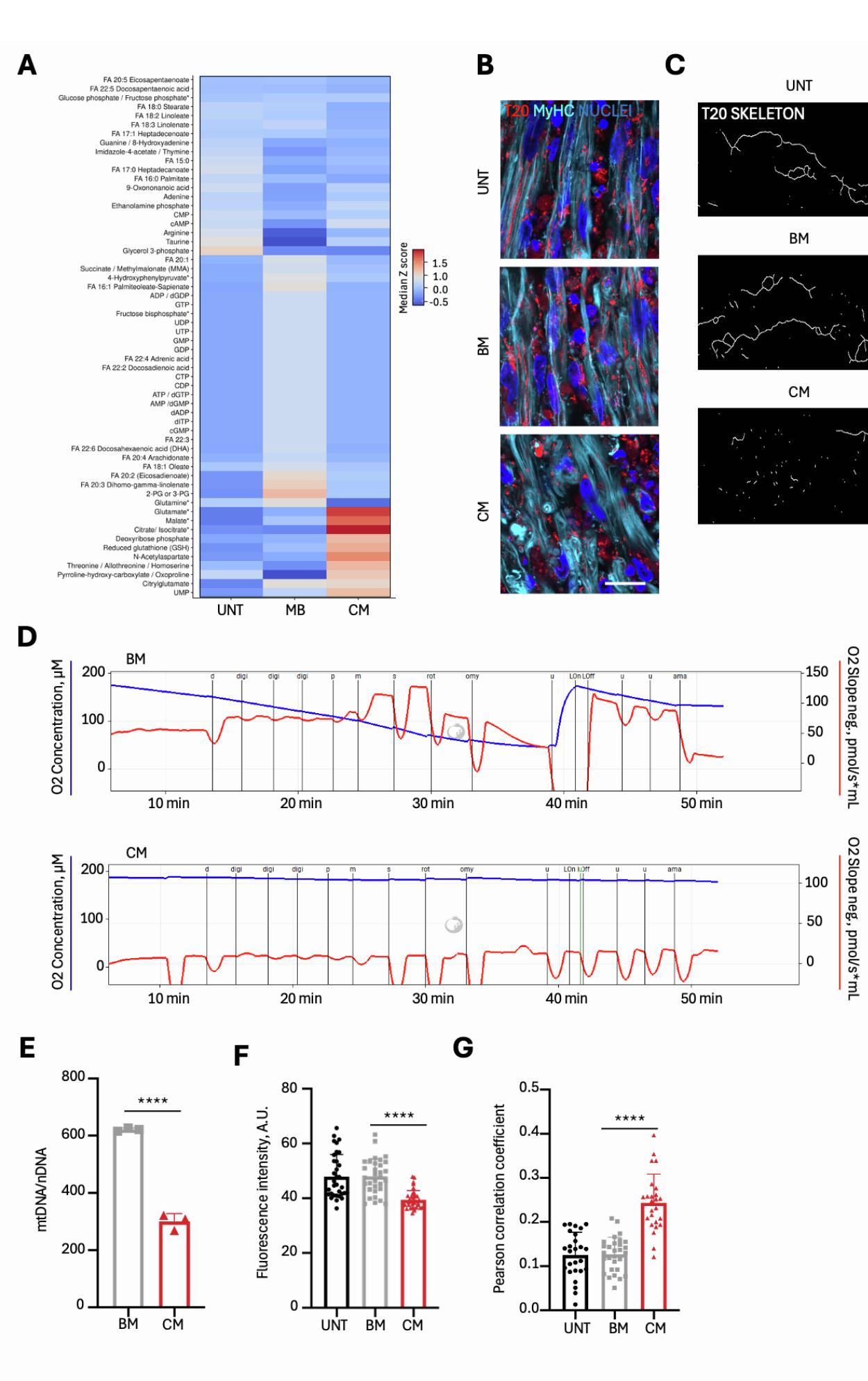
图S4. 图4中所报道的UNT、BM-C26、CM-C26、神经肌肉类器官(NMOs)的表征。A. 热图显示经C26来源的BM和CM处理72小时后,第53天神经肌肉类器官切片中代谢物的定量情况。作为额外对照,对UNT条件进行了分析。数据详见数据S3。B. 代表性共聚焦免疫荧光图像显示经C26来源的BM和CM处理72小时后,第53天神经肌肉类器官切片中的TOM20(T20)和肌球蛋白重链(MyHC)。作为额外对照,对UNT条件进行了分析。TOM20与细胞核的共染色图像见图4D。比例尺,15μm。C. 在不同实验条件下,对T20染色的神经肌肉类器官进行形态计量分析后生成的代表性骨架图。D. 代表性Oroboros轨迹显示经C26来源的BM和CM处理72小时后,第53天神经肌肉类器官切片中随时间变化的氧浓度(μM,左轴)和氧消耗率(负氧斜率,右轴)。作为额外对照,对UNT条件进行了分析。放大分析见图4E。E. 经C26-BM和C26-CM处理的神经肌肉类器官中的线粒体DNA(mtDNA)含量。数据以每个实验条件下3个独立神经肌肉类器官的平均值±标准差表示。采用方差不齐的Student t检验确定统计学显著性;****p < 0.0001。F. 在肌球蛋白重链阳性区域内选择相同尺寸的感兴趣区域(ROI),对T20的荧光强度进行定量。每个点代表每张图像的实测荧光强度;每个实验条件下,对3个独立神经肌肉类器官的至少10张图像进行了分析。采用普通单因素方差分析(Ordinary One-way ANOVA)确定统计学显著性;****p < 0.0001。统计结果详见数据S2。G. 对T20和LAMP1的阈值化皮尔逊相关系数(PCC)进行定量。每个点代表每张图像的实测皮尔逊相关系数;每个实验条件下,对3个独立神经肌肉类器官的至少8张图像进行了分析。采用普通单因素方差分析确定统计学显著性;****p < 0.0001。统计结果详见数据S2。