¶ 发表文献:ACS Nano(IF:17.1)
¶ 铂纳米酶在年龄相关性黄斑变性的光损伤模型中对抗光感受器退行性病变与视网膜炎症
¶ 原文下载:29铂纳米酶在光损伤模型中抑制年龄相关性黄斑变性的光感受器退行与视网膜炎症.pdf
萨拉·库皮尼,-斯特凡诺·迪马可,-卢卡·博塞利,亚历西奥·卡瓦利,朱利亚·塔里科内,瓦伦蒂娜·马斯特罗纳尔迪,瓦伦蒂娜·卡斯塔尼奥拉,伊丽莎贝塔·科伦坡,皮尔·保罗·蓬帕,*和法比
¶ 摘要:
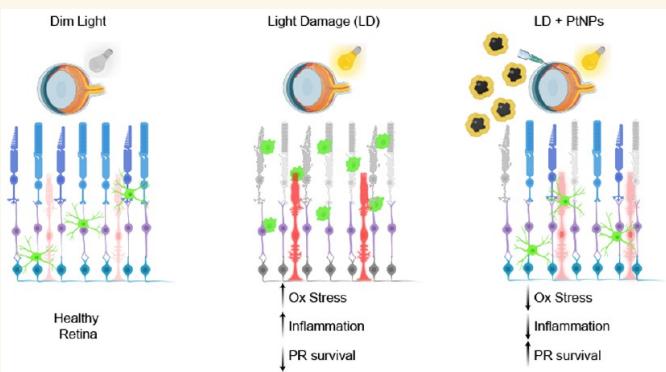
老年性黄斑变性(AMD)中感光细胞的退化与氧化应激相关,这是由于视杆细胞和视锥细胞剧烈的有氧代谢所致。若这种代谢不能通过内源性抗氧化机制得到适当平衡,则会加速感光细胞退化。尽管老年性黄斑变性因其在老年人中的高发病率而被列为重点眼病,但目前尚无有效治疗方法。虽然全身性施用抗氧化剂未能延缓退化,但局部施用的稀土纳米颗粒已被证明能有效预防视网膜光氧化损伤。然而,由于在生物介质中分散性存在固有问题、抗氧化能力有限以及寿命较短,这些纳米颗粒仍局限于临床前阶段。在此,我们提出将铂纳米颗粒(PtNPs)作为一种治疗年龄相关性黄斑变性(AMD)的治疗工具,PtNPs是一种强效的抗氧化纳米酶。PtNPs在极低浓度下仍表现出高催化活性,并能保护原代神经元免受氧化损伤及随之而来的细胞凋亡。我们通过玻璃体内注射PtNPs,采用in vivo视网膜电图(ERG)和ex vivo视网膜形态学及电生理学检测,评估其在预防或减轻暗饲养白化Sprague-Dawley大鼠光损伤方面的功效。研究发现,无论是预防性还是损伤后治疗,PtNPs均能增强ERG对光刺激的反应振幅。Ex vivo记录表明,在接受PtNPs治疗的受损视网膜中,ON型视网膜神经节细胞对光刺激的反应得到了选择性保留。光损伤后给予PtNPs能显著保护感光细胞数量,并抑制退化引发的炎症反应,而预防性治疗的效果相对温和。数据表明,PtNPs通过发挥抗氧化和抗炎作用,能有效打破氧化应激、退行性变和炎症之间的恶性循环。PtNPs能提高退化视网膜中感光细胞的存活率和视觉功能,同时具有高生物相容性,这使其成为治疗AMD的潜在策略。
¶ 关键词:
氧化应激,纳米颗粒,视细胞死亡,穆勒细胞,小胶质细胞,视网膜电图,高密度多电极阵列
¶ 引言
视网膜中的视杆和视锥光感受器(PRs)具有人体最高的氧化代谢率特征。它们处于极大的氧梯度环境中—一脉络膜中氧浓度最高,而在缺乏直接血液供应的视网膜外层则急剧下降。此外,光感受器持续暴露于光照下,超过特定光子功率密度时可能诱发光毒性。这些伴随终身的条件使光感受器极易受到氧化损伤及活性氧(ROS)的有害影响。当这些物质(主要是由线粒体中的电子传递链产生,超过低生理水平(<100nM)时1,渐进性细胞损伤便随之发生,伴随着DNA和细胞膜的改变,以及细胞内信号通路,触发细胞死亡程序和炎症过程。2-4 在生理条件下,氧化微环境的影响会被视网膜色素上皮细胞(RPE)和光感受器细胞(PRs)中的内源性抗氧化及细胞修复系统所中和。然而,当这些抗氧化活性关键基因发生突变,或衰老过程中长期暴露于氧化环境时,便会导致光感受器细胞退化,进而分别引发诸如视网膜色素变性(RP)和萎缩性年龄相关性黄斑变性(AMD)等疾病。视网膜色素变性作为一组导致视杆细胞死亡并继发视锥细胞死亡的罕见遗传性疾病的总称,全球患病率约为1/4000;而被世界卫生组织定义为“priority eyedisease”的年龄相关性黄斑变性,在70至90岁人群中发病率约为 。5-9AMD主要累及黄斑区负责敏锐中心视觉的{f4}区域中的旁中心凹视杆细胞及中心凹视锥细胞。10,11这种严重的功能损伤对老年群体具有毁灭性影响,可导致认知能力下降和抑郁状态。12除罕见遗传类型外,学界普遍认为慢性氧化应激及随之引发的炎症是萎缩性AMD发病机制和病程进展的关键环节13-16
。
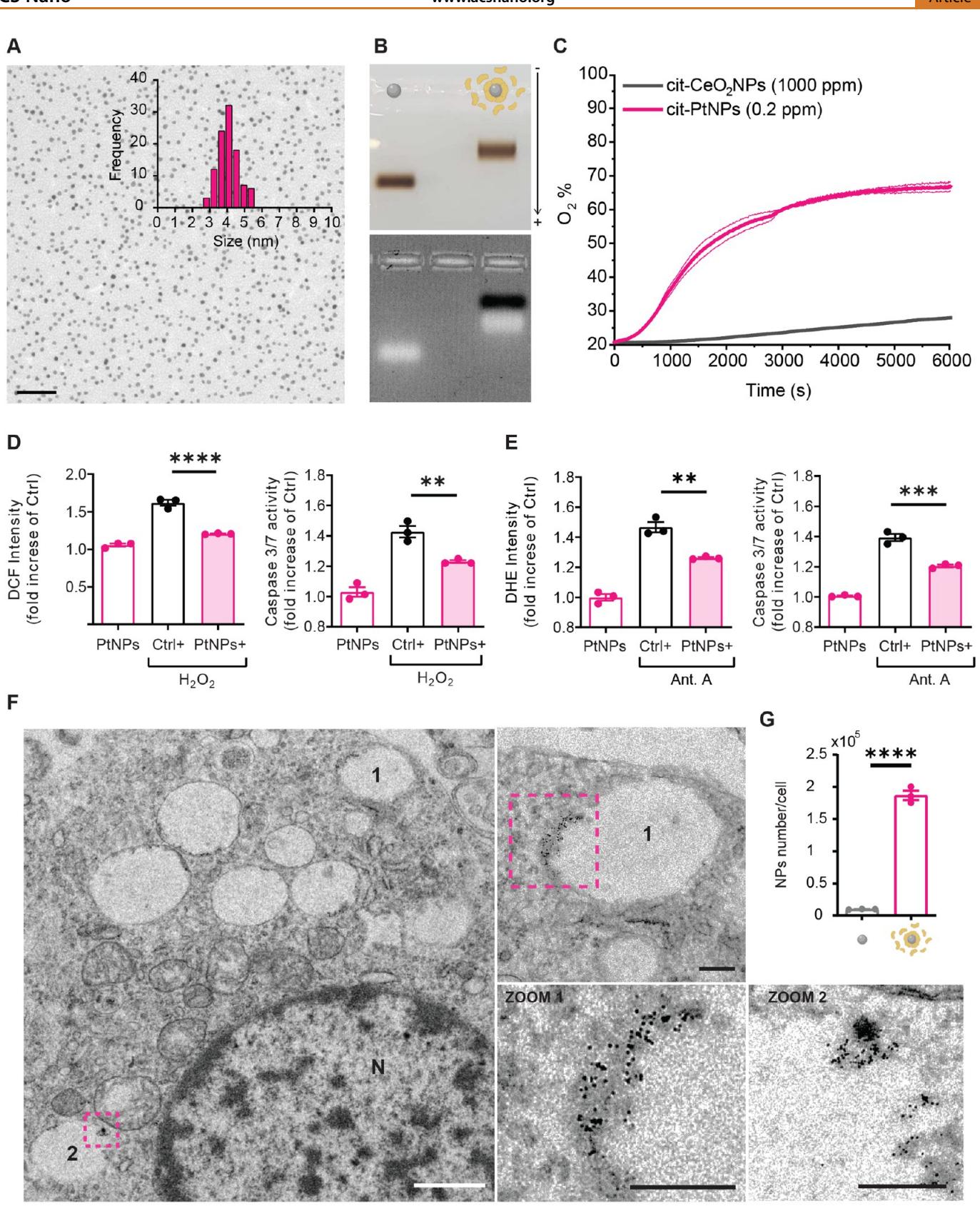
图1.铂纳米酶的物理-化学与生物学表征。(A)RSA包覆铂纳米颗粒的代表性TEM显微照片(比例尺:50纳米)及粒径统计分析(至少计数200个纳米颗粒)。(B) 琼脂糖凝胶中的凝胶迁移实验。凝胶显示为明场模式 (上图)和紫外透射模式(下图)。第一泳道显示柠檬酸盐稳定的铂纳米颗粒电泳迁移情况,第二泳道可观察到RSA包覆铂纳米颗粒的电泳迁移延迟。在透射模式下,可见未结合的过量RSA(黑色条带)。©通过反应生成氧气的实时监测评估类CAT活性(详见方法)。在含 (空气)的样品瓶中,将柠檬酸盐稳定的铂纳米颗粒胶体悬浮液(cit-PtNPs, )和柠檬酸盐稳定的CeO纳米颗粒胶体悬浮液(cit-C NPs, )暴露于 ()中。铂纳米颗粒的类CAT活性诱导的O2百分比达 ,而浓度高5000倍的 纳米颗粒在100分钟后仅诱导 (D,E)铂纳米颗粒对原代大鼠皮质神经元化学诱导活性氧与凋亡恢复的影响。分别采用1mM 处理5分钟(D)和5 抗霉素A处理24小时(E)用于诱导培养物中的ROS。ROS值通过使用相应的荧光探针(分别为 和DHE)进行测量。细胞凋亡通过caspase 3/7活性进行检测。结果以均值 标准差表示,来源于 次独立实验,并相对于未处理的对照组进行标准化。 、 、 ;单因素方差分析/Tukey检验。在所有情况下,用 RSA包被的PtNPs预处理48小时的神经元均显示出ROS水平和细胞凋亡的显著恢复。(F)RSA包被的PtNPs被原代大鼠皮层神经元内化后的代表性TEM图像(比例尺: )。两个含有PtNPs的细胞内囊泡用数字标出并放大显示。放大囊泡的比例尺为 N表示细胞核。(G)通过ICP-MS测量估算的每个细胞的纳米颗粒摄取量。RSA包被的PtNPs的摄取量显著高于柠檬酸盐稳定的
尽管年龄相关性黄斑变性(AMD)患病率极高,但治疗策略尚未被证明成功。17平面视网膜假体设备18,19或光遗传学技术20,21在恢复AMD患者丧失的高分辨率中央视力方面效果不佳。22,23通过干细胞实现视网膜细胞(包括RPE和感光细胞)分化的替代疗法前景广阔,但大多仍处于临床前阶段。24-26延缓疾病进展的药理学方法包括具有抗氧化特性的药物、补体级联反应抑制剂和神经保护剂。然而,目前尚无任何疗法能阻止或逆转干性AMD的任何阶段。27,28
基于纳米粒子(NP)的疗法作为神经退行性疾病的潜在治疗手段,近来引起了极大关注。相较于全身给药疗法,纳米粒子可轻易以胶体悬浮液形式局部注射至玻璃体,具备给药简便和扩散性高的优势。研究人员已探索使用二氧化钛、29二氧化硅、30金纳米粒子、31,32或氧化铈3等纳米材料来预防或延缓光感受器退化。在此背景下,下调有害氧化应激水平是一种前景广阔的治疗策略。纳米酶一一即能模拟天然酶(包括抗氧化酶)行为的催化性纳米粒子一一近年来在该领域展现出独特吸引力。34-37与天然酶相比,纳米酶具有合成工艺简便、规模化生产成本低、稳定性高、以及在广泛环境条件下耐久性强等多重优势。38其中,氧化铈纳米粒子等特定类型的稀土纳米粒子,多年来一直被视作眼部疾病的潜在治疗剂。33,39,40例如,纳米氧化铈被证明可以预防黑暗饲养的白化大鼠视网膜中由光损伤诱导的光感受器损伤,并在损伤发生后给药时减少变性和视力障碍的程度。41近年来,纳米氧化铈已广泛应用于各种基于氧化的变性模型,包括光损伤42,43或乌谢尔综合征(tubby小鼠)、视网膜色素变性(视紫红质P23H大鼠)或湿性年龄相关性黄斑变性44-47的遗传模型,并发现其在减轻变性诱导的炎症方面也有效果。尽管具有潜力,纳米氧化铈的临床应用仍受限于与其潜在毒性相关的一些担忧。33作为纳米氧化铈的替代方案,钇纳米颗粒也被提出具有相似性能。48
近年来,铂基纳米颗粒(PtNPs)作为强大的纳米酶崭露头角,展现出内在的多种酶活性,可模拟过氧化物酶(POD)、过氧化氢酶(CAT)和超氧化物歧化酶(SOD)等主要天然抗氧化酶。PtNPs的活性催化位点为其表面原子,这些原子具有显著且持续的活性氧清除活性invitro,无需特殊配体即可实现高性能表现。38,49-51完全生物相容性的生物蛋白冠包覆PtNPs能被细胞内吞,其溶酶体在酸性pH环境下将纳米颗粒从蛋白冠中释放,从而提升其纳米酶性能。51此外,PtNPs表现出优异的稳定性与生物相容性in vitroinvivos1,并因其强大的抗炎潜力而备受关注。+因此,虽然尚未在眼部疾病治疗领域进行测试in vivo,但将其作为基于纳米酶的抗氧化疗法应用于神经退行性疾病52,53等多种氧化应激诱导疾病的治疗具有极大吸引力。
本研究利用在暗光饲养的白色大鼠中通过光损伤诱导背侧视网膜PR退化热点生成的AMD大鼠模型54,55,通过invivo视网膜电图(ERG)和exvivo高密度多电极阵列(HD-MEA)记录的视网膜形态及视网膜上电位,研究玻璃体内注射铂纳米颗粒(PtNPs)在预防或改善光氧化视网膜损伤方面的效果。我们发现,在预防性和治疗性方案中,PtNPs均能保持视网膜ERG活性、PR细胞数量以及ON型视网膜神经节细胞(RGC)反应,并减轻退行性病变引发的炎症反应,其中病灶后治疗显示出更高疗效。数据表明,低浓度PtNPs能有效打破活性氧(ROS)、退行性病变和炎症之间的恶性循环,使其成为治疗AMD的潜在策略。
¶ 结果与讨论
铂纳米粒子作为纳米酶可诱导高效持久的活性氧清除作用。在本研究中,我们选择PtNPs凭借其无需表面壳工程即具备内在的类酶活性。38 使用4纳米尺寸的PtNPs能够实现最大化表面与体积比 (增加可用于反应的表面原子数),同时不损失尺寸且纳米结构的形状控制。柠檬酸盐封端的铂纳米颗粒的制备方法如先前报道所述,51得到了具有窄尺寸分布的可重现单分散产物,这通过透射电子显微镜(TEM;图1A)和动态光散射(DLS;图S1)得以展示。
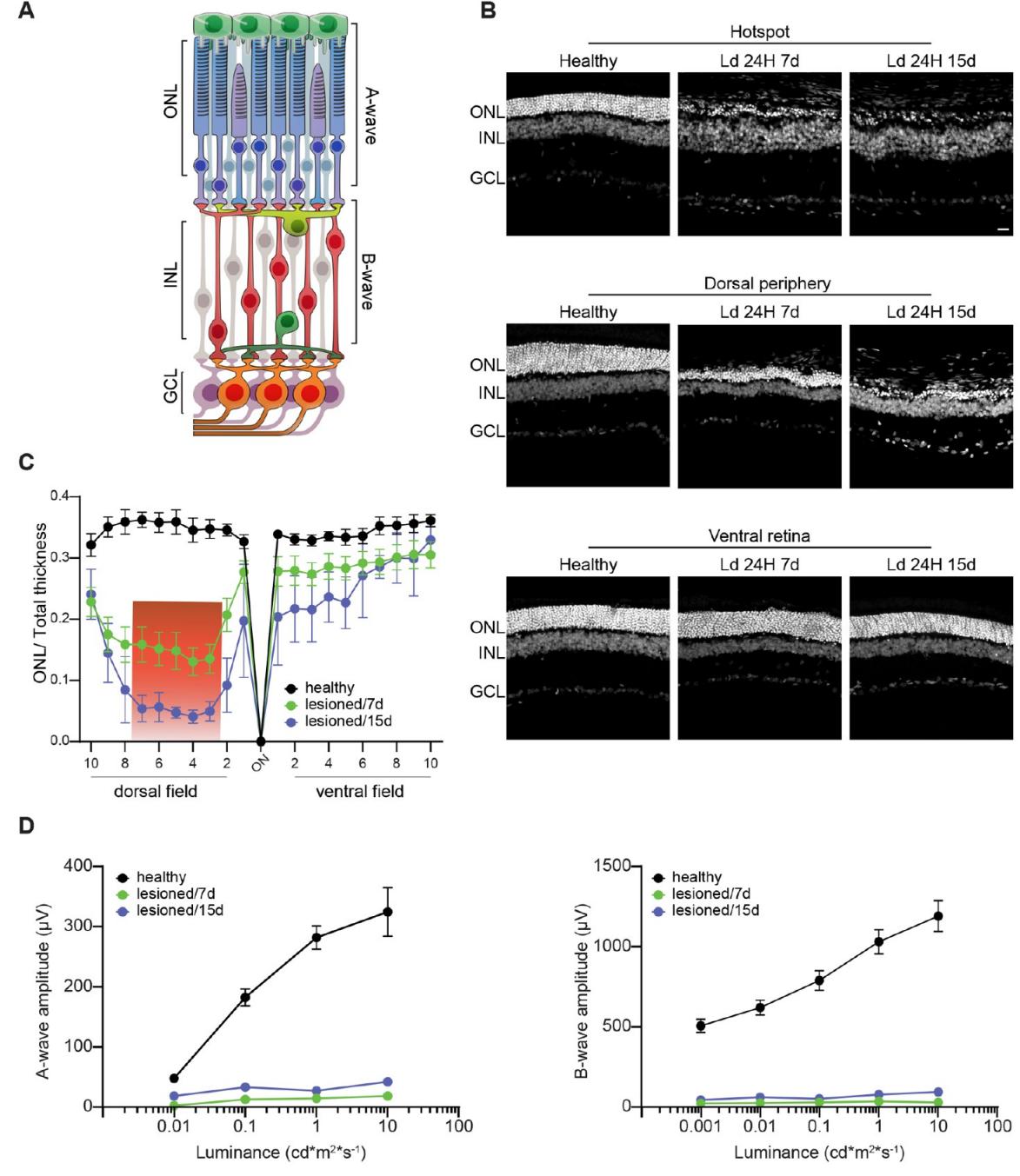
图2.萎缩性黄斑变性光损伤模型的形态功能表征。(A)视网膜回路及负责产生闪光视网膜电图(fERG)响应的神经元组分示意图。A波反映闪光后光感受器(PRs)的光活化,B波则与电刺激从PRs向二级神经元的传递相关。(B)白化SD大鼠在光诱导视网膜损伤(1000勒克斯光照24小时)后两个恢复时间点(7天和15天)的形态学改变和视网膜功能损伤评估,所有大鼠均饲养于弱光环境(5-10勒克斯)。健康大鼠与光损伤24小时后分别于损伤后7天(Ld24H7d)和15天(Ld24H15d)分析的大鼠,其背侧视网膜热点区(上行)、背侧周边区(中行)和腹侧视网膜(下行)的bisbenzimide标记(白色)代表性图像。值得注意的是,在两个损伤组中均发现Ld 24H15d组存在rosetts及光感受器损失,而腹侧视网膜未检测到显著变化。©外核层(ONL)厚度以总视网膜厚度归一化后(均值 标准误),从背侧周边经视神经(ON)至腹侧周边的20个等距视网膜位点进行计算。光损伤导致背侧中央视网膜(热点区)ONL严重变薄,该区域光感受器发生不可逆损伤,外围伴有可能逐步扩展的退化半影区(红框)。样本量:健康组 ;Ld 24H7d组n ; Ld 24H 15d组n ,(D)在刺激强度范围内(0.001至 ,A波(左)和B波(右)的振幅(均值 标准误)以半对数坐标绘制。1000勒克斯暴露24小时显著降低损伤动物两组fERG成分。样本量:健康组 ;Ld 24H7d组 ;Ld 24H15d组 。缩写:ONL,外核层;INL,内核层;GCL,神经节细胞层。比例尺: 2 0 \mu \mu \mathrm { m } _
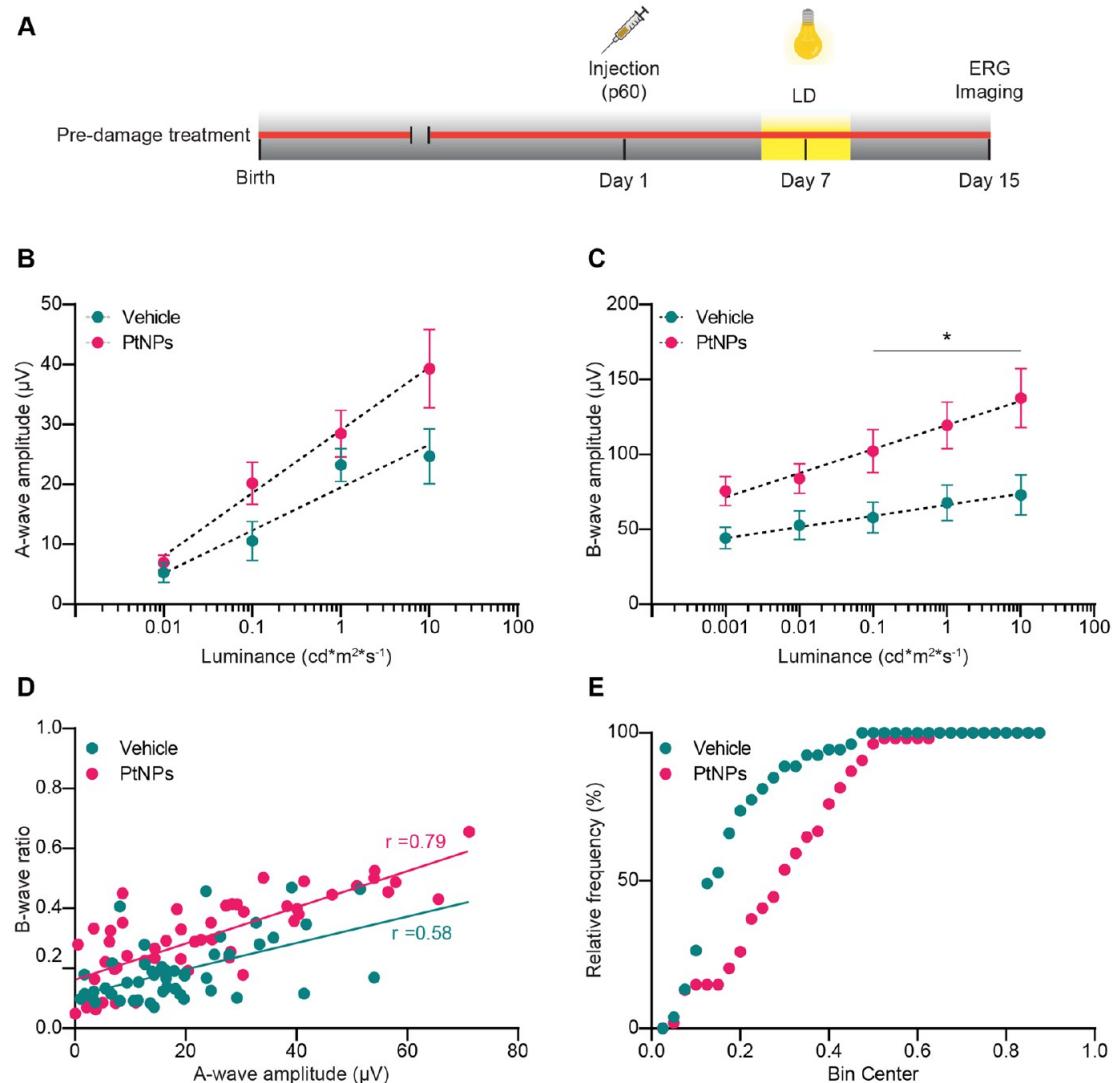
图3.PtNPs预防性治疗对光损伤视网膜电活动的影响。(A)实验时间线。在弱光环境下饲养的2月龄白化SD大鼠玻璃体内注射2 PtNPs或对照剂(RSA)。一周后,通过暴露于1000勒克斯光照24小时诱导光氧化损伤。注射后15天,进行视网膜电图记录,并采集视网膜组织进行形态学分析(成像)。(B,C)以半对数尺度绘制注射对照剂(蓝色)或PtNPs(红色)的动物在光损伤前A波(B)和B波©振幅(平均值 标准误)随刺激强度(0.001至10cd )变化的曲线。注射PtNPs的损伤动物表现优于注射对照剂的动物,尤其在较高亮度下的B波,表明PtNPs在光感受器/二级神经元突触层面产生作用。样本量:对照组与PtNPs组均为 。 ;采用双向混合方差分析/Holm-Sidak多重比较检验。(D)光损伤前注射对照剂(蓝色)或PtNPs(红色)的损伤动物中B波比值(即实验记录的B波振幅除以由A波振幅推导的健康B波振幅)与A波振幅的相关性。图中显示线性回归线的皮尔逊相关系数 (E)图(D)中B/A波比值的累积分布。 ,Kolmogorov-Smirnov检验。
考虑到白蛋白是玻璃体液中含量最丰富的蛋白质,我们用大鼠血清白蛋白(RSA)包覆铂纳米颗粒(PtNPs),以获得仿生包覆层,并在目标生物体液中实现良好的胶体稳定性。51此步骤还能去除溶液中过量的柠檬酸盐,从而最大程度地减少invivo注射后生物体液成分的渗透压和pH变化。对RSA包覆的PtNPs进行的凝胶迁移实验分析显示出一条清晰的条带,其特征是电泳迁移率较原始的PtNPs更慢,这是由于尺寸增大和表面电荷降低所致。
复合物的电荷(图1B)。通过RSA吸附形成的PtNP-RSA复合物极大地稳定了电解细胞外介质中的铂纳米颗粒,模拟了蛋白质冠的效应。这些纳米酶的抗氧化酶样特性已在其他文献中得到详细研究。49在此,我们以“金标准”纳米氧化铈(CeONPs)为参照,对PtNPs的过氧化氢酶样特性进行了基准测试—一后者是生物应用领域(尤其是视网膜保护)中被研究最广泛的纳米酶之一。 33,41-47,56-60利用氧传感器,我们比较了随时间推移由过氧化氢酶样反应产生的氧气量(参见方法部分)。本实验中,纳米颗粒的核尺寸与表面化学性质均经过标准化处理,并在溶酶体pH值(pH5)条件下进行测试。我们发现,即使在CeO₂纳米颗粒过量5000倍的情况下,Pt纳米颗粒仍显著优于后者(图1C)。尽管据报道柠檬酸盐有利于CeO 的活性和胶体稳定性,但使用不同配体或更单分散样品时可能产生差异( 倾向于聚集成更大的纳米组装体)。尽管如此,我们相信观察到的3个数量级的差异强烈表明PtNPs具有净优越的活性。
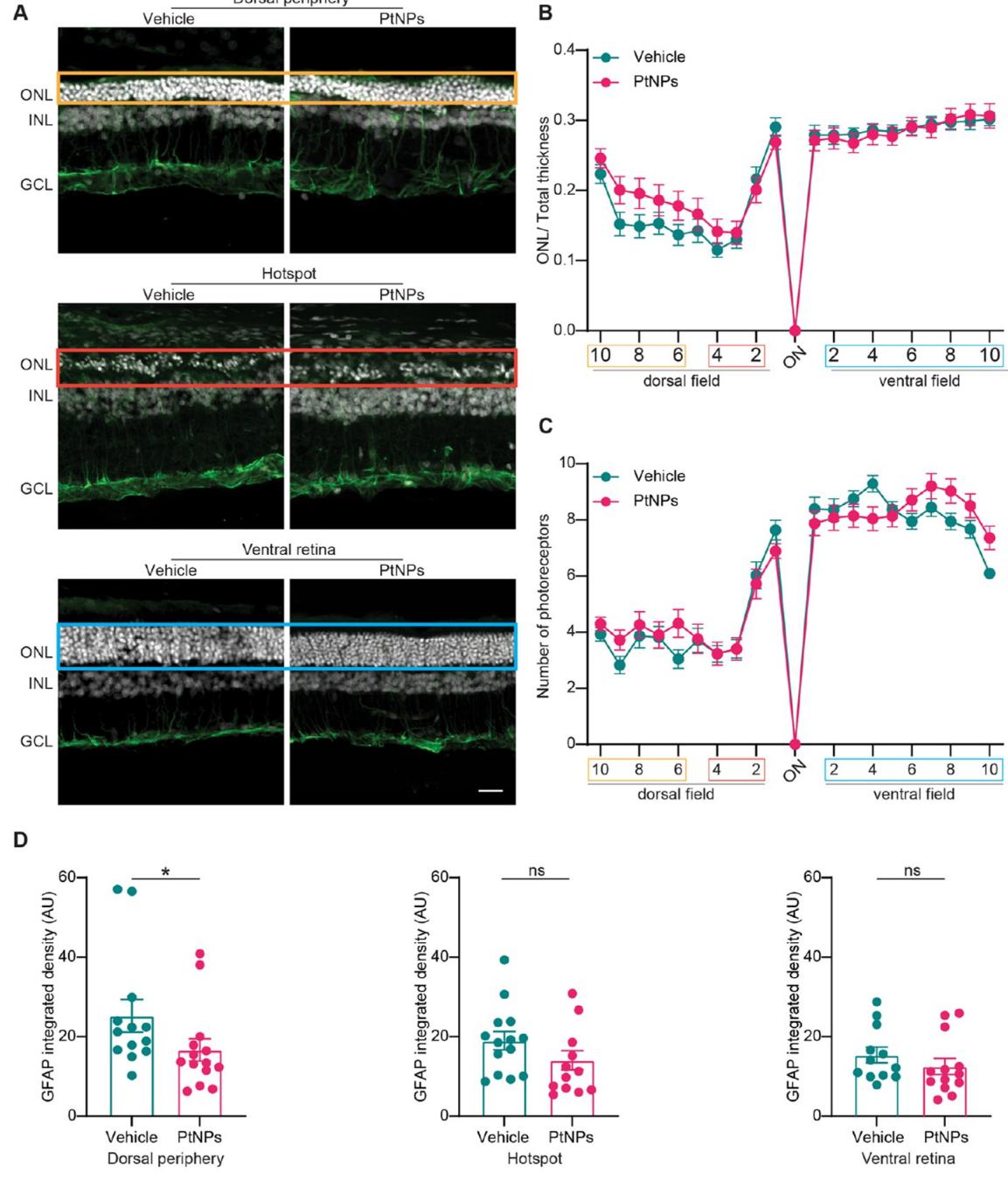
图4.PtNPs预防性治疗对光损伤视网膜形态的影响。(A)用双苯甲亚胺进行细胞核标记(白色)并针对Muler细胞标记物GFAP(绿色)进行免疫染色的背侧周边区、热点区和腹侧视网膜的代表性图像。图像显示与溶剂处理的同窝动物相比,PtNPs预处理动物仅对背侧视网膜的外核层厚度产生轻微影响。缩写:ONL,外核层;INL,内核层;GCL,神经节细胞层。比例尺: (B,C)对光损伤前注射溶剂(蓝色)或PtNPs(红色)的动物,将标准化至视网膜总厚度的ONL厚度(B)及光感受器核层行数©沿从背侧周边至腹侧周边、穿过视神经(ON)的20个等距视网膜位点进行绘制。数据以均值 sem表示。彩色框表示(A)中对应的分析区域。样本量:溶剂组与PtNPs组均为 。双因素混合方差分析/费希尔LSD检验。(D)对背侧周边区 (左图;溶剂组 4,PtNPs组12)、热点区(中图;两组均为 )和腹侧视网膜(右图;溶剂组 ,PtNPs组13)的GFAP表达积分光密度进行定量分析。柱状图表示均值 sem,并叠加显示各实验数据点。PtNPs能显著降低背侧周边区的GFAP表达。ns, 0.05;曼-惠特尼U检验/非配对学生t检验。
我们此前报道过,生物有效浓度的铂纳米颗粒与包括小鼠原代神经元在内的多种细胞类型完全生物相容,且不会实质上影响神经元活力。51在此,作为in vitro替代指标以in vivo研究,我们评估了铂基纳米制剂对原代大鼠皮层神经元的保护能力一一这些神经元分别受到过氧化氢或抗霉素A诱导的线粒体ROS产生的氧化损伤,该过程常参与炎症反应。61,62通过荧光探针 和DHE评估神经元培养物的ROS水平,并通过测定caspase3/7活性来评估细胞凋亡诱导情况(图1D,E)。两项实验均表明,使用铂纳米颗粒对神经元进行预防性处理能显著降低细胞内ROS水平,并逆转ROS诱导的细胞凋亡,证明其对氧化应激导致的细胞死亡具有强大抑制活性。
通过对经PtNPs处理的原代大鼠皮层神经元进行透射电子显微镜(TEM)观察,我们证实了纳米酶的主动内吞作用。正如先前在小鼠模型中所示,这些纳米酶存在于细胞内囊泡中,与其内吞及内溶酶体归宿一致(图1F)。51此外,我们通过质谱分析法对PtNPs的细胞摄取进行了定量评估,进一步证实蛋白质包覆对其有效内化的关键作用。事实上,与RSA稳定的PtNPs相比,原始PtNPs的内化程度显著偏低,这很可能归因于其在生物介质中胶体稳定性较低(图1G)。
轻度光损伤诱导白化大鼠视网膜背侧出现光感受器变性的热点区域。为探究PtNPs是否能预防或减轻视网膜中过度的氧化应激和炎症反应,我们采用白化大鼠一一一种研究啮齿类动物光感受器变性的成熟动物模型-诱导视网膜光损伤。该模型依赖于在弱光条件下饲养的白化大鼠天生对光敏感的特性 ,其主要特征是光感受器损伤始于并集中在一个称为“hotspot”的视网膜背侧局部区域。在光照暴露期间,热点区域的光感受器完全变性,随后数日内变性蔓延至背侧周边视网膜,而腹侧部分几乎保持完整(见图2A、B中对急性光损伤后第7天和第15天外核层厚度的分析结果)。事实上,仅在对光更敏感的背侧视网膜中,外核层厚度与视网膜总厚度的比值随时间推移逐渐下降,并在热点区域达到最低值。尽管受到相同的光照,腹侧视网膜因具有内在的光损伤抵抗性,其外核层厚度未出现变化 (图2C)
随后,我们通过暗适应动物(暗视条件下)的闪光视网膜电图(fERG)记录视网膜对短暂光刺激的电反应,以表征视网膜功能损伤。我们量化了与光感受器激活直接相关的早期"A波"超极化反应,以及随后由二级视网膜神经元突触后激活产生的"B波"去极化反应。在健康对照同窝小鼠中记录到的A波(图2D左)和B波(图2D右)振幅(黑色轨迹),在光损伤后第7天(绿色轨迹)和第15天(蓝色轨迹)出现严重损伤,这与外核层厚度的减少趋势一致。
铂纳米酶预处理可减轻光诱导的外视网膜功能损伤。从生物学角度来看,小于50纳米的颗粒预计能更高效地穿透玻璃体视网膜界面和内界膜,而尺寸 纳米的纳米颗粒则无法渗透至视网膜组织。若要评估玻璃体内为了验证注入的PtNPs是否能够通过视网膜扩散并到达光感受器细胞,我们对来自invivoPtNP注射眼的超薄视网膜切片进行了透射电镜观察。有趣的是,在光感受器细胞内,包括细胞体及外节层面,均发现了PtNPs的存在(图s2)。
考虑到PRs中存在PtNPs,我们首先分析了它们在防止光诱导氧化损伤方面是否具有活性。在预防性方案中(图3A),将2月龄暗室饲养的Sprague-Dawley白化大鼠在光损伤诱导前7天分别玻璃体内注射载体(RSA)或RSA包被的PtNPs胶体悬浮液,并于7天后进行视网膜电图和免疫组化分析。尽管光损伤7天后ERG信号仍显著减弱,我们观察到PtNPs治疗组的视网膜功能恢复有所改善,表现为全视野亮度刺激下A波和B波振幅增加。B波2倍的恢复幅度较A波更为显著,且具有统计学意义(图3B,C)。
为了推断光感受器与二级神经元之间的信号传递效能,我们计算了B波与A波振幅的比值(图S3和表S1)。66 若仅光感受器受损,将导致A波振幅降低而B/A波比值保持不变;相反,若光感受器与双极细胞间的突触传递功能异常,则在A波振幅正常的情况下B/A波比值会下降。因此,我们绘制了不同实验组的标准化B波比值图:将记录的B波振幅除以健康动物中相同A波所能产生的预期B波振幅,再与A波数值进行对比(图3D;参见方法)。可以注意到,注射PtNP的动物数据(红色)相较于注射溶剂的动物(蓝色)分布在图的上部区域,在A波振幅较大时尤为明显。此外,标准化B/A波振幅比值的累积分布显示两组数据存在显著差异 001;柯尔莫哥洛夫-斯米尔诺夫检验),这证实PtNP预防性治疗对维持光感受器与双极细胞间突触传递的效果更为突出,而非恢复光感受器的生理特性或存活率(图3E)。
铂纳米酶预处理可减轻星形胶质细胞对光损伤的反应。在功能分析之后,我们研究了铂纳米颗粒对视网膜形态和炎症反应程度的预防效果。视网膜各层厚度的形态学评估(图4A)显示,沿整个视网膜剖面,载体组与铂纳米颗粒处理组之间的外核层/视网膜总厚度比值(光损伤后光感受器保存情况的测量指标,图4B)以及外核层中光感受器数量(图4C)均无显著差异。虽然腹侧视网膜未受影响,但预防性给予铂纳米颗粒仅轻微缓解了背侧视网膜外核层厚度的急剧光诱导下降,这证实了图3B中观察到的A波振幅增加的趋势。随后,分别通过胶质纤维酸性蛋白和离子钙结合适配分子1的特异性标记物免疫组化,评估了穆勒细胞/星形胶质细胞和小胶质细胞对光损伤的促炎反应。在生理条件下,GFAP在穆勒细胞中表达水平在应激诱导下,内界膜中GFAP的表达会在整个米勒细胞过程中过度增加。PtNPs预处理显著降低了视网膜背侧周边区域GFAP的综合免疫荧光强度,但在热点区域未观察到这种效应,而在视网膜腹侧则未发现任何影响(图4D)。然而,根据载体组和PtNPs处理组视网膜中IBA1阳性细胞的数量和分布判断(图S4),PtNPs并未影响小胶质细胞在光损伤区域的募集。
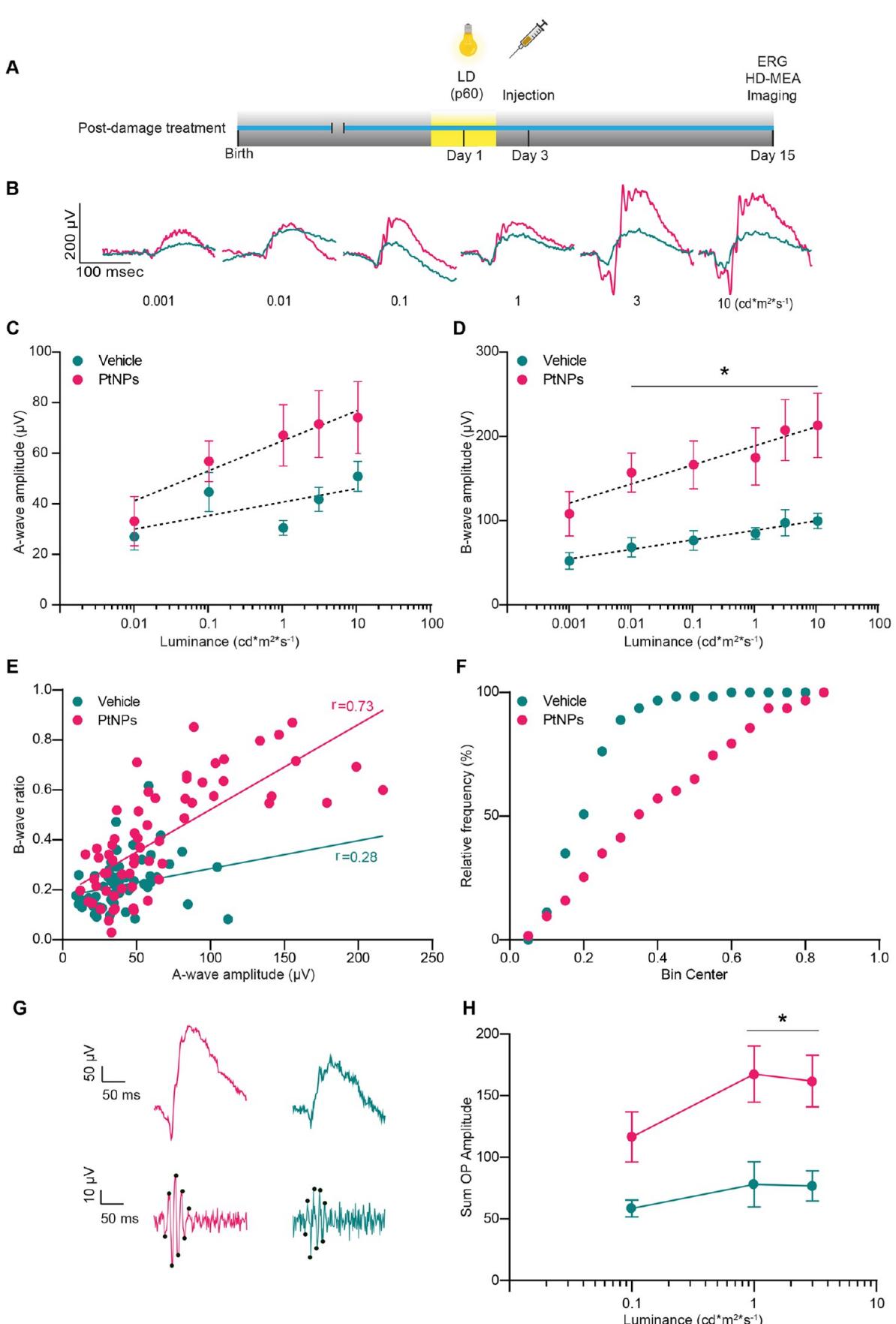
图5.光损伤视网膜后给予铂纳米颗粒(PtNPs)治疗对其电活动的影响。(A)实验时间线。将饲养于弱光条件下的两月龄SD白化大鼠暴露于1000勒克斯光照24小时引发光氧化损伤,48小时后分别向玻璃体内注射2微升! )PtNPs或载体(RSA)。光损伤后第15天进行闪光视网膜电图(fERG)记录,并采集视网膜组织用于电生理(高密度微电极阵列,HD-MEA)与形态学分析(成像)。(B) 通过光损伤24小时后,分别向动物注射溶媒(蓝色)或铂纳米颗粒(红色),在所有测试亮度下,由亮度递增的光闪诱发的代表性fERG轨迹突显了两组动物的差异。(C,D)A波©和B波(D)的振幅(均值 sem)以半对数尺度绘制为刺激强度(范围0.001至 )的函数,对应光损伤24小时后注射载体(蓝色)或PtNPs(红色)的动物。在所有测试亮度下,注射PtNPs的动物比注射载体的动物显示出更大的振幅,尤其是B波,表明PtNPs在保留视网膜功能方面具有积极作用,即使在严重光损伤后也是如此。E.光损伤后注射载体(蓝色)或PtNPs(红色)的损伤动物中,B波比值(即实验记录的B波振幅与通过A波振幅推导的健康B波振幅的比值)与A波振幅之间的相关性。图中显示了线性回归线的皮尔逊相关系数 。(F)(D)中绘制的B/A波比值的累积分布。两个实验组之间的差异表明PtNPs能够保持光感受器与次级神经元之间的高效突触传递,并增强光感受器活化。 ,柯尔莫哥洛夫-斯米尔诺夫检验。(G,H)PtNP处理与载体处理动物中,振荡电位随亮度(0.1、1和3cd s )变化的代表性记录(G)及振幅总和均值(±sem) OP峰值用黑点标出。样本量:载体组 ;PtNPs组 ;双因素混合方差分析/Holm-Sidak检验(C、D、H)。
综上所述,数据表明预防性玻璃体内注射PtNPs能在强烈光氧化应激后保护光感受器与二级视网膜神经元之间的突触传递,并减少神经胶质细胞活化。这表明其主要作用机制是通过影响炎症反应,从而调节视网膜信号传导。
光损伤后施用铂纳米酶可挽救视网膜的电生理活动。接下来我们分析了PtNPs在光损伤后给药时是否同样能有效对抗氧化应激/炎症/神经元死亡循环 (图5A) 。
在弱光环境下饲养的两个月大斯波rague-道利大鼠先接受光损伤处理,24小时后进行玻璃体内注射对照溶剂或铂纳米颗粒。随后留出2周手术恢复期,最后一天进行invivo闪光视网膜电图测量及exvivo电生理学与形态学分析。典型闪光视网膜电图记录如图5B所示。对A波(图5C)和B波(图5D)平均振幅的分析表明,相较于注射对照溶剂组,光损伤后给予铂纳米颗粒治疗能增强闪光视网膜电图反应。与预防性方案相比,A波恢复更为显著(在 以上光强时约 ),而同等光强范围内预防性方案的平均值仅为 (图5C)。损伤后铂纳米颗粒治疗显著提升了B波振幅,在整个光强范围内较对照组增强2倍(图5D)。健康视网膜中B波的光强响应曲线遵循类S型的Naka-Rushton函数(参见图2D),而在本实验的光损伤视网膜中,无论接受何种处理,该曲线均保持近似线性。鉴于B波比A波显示出更显著的治疗效应,我们进一步探究了铂纳米颗粒在损伤后治疗中是否能改善光感受器至双极细胞的视觉信息传递。通过绘制标准化B波比率与对应A波振幅的关系曲线,我们发现曲线呈现显著的上移趋势。
PtNP处理组相较于媒介物处理组的实验点分布情况(图5E)。此外,归一化B/A波振幅比的累积分布显示两组数据群体存在极显著差异 ; Kolmogorov-Smirnov检验;图5F)。我们最终探究了在外层视网膜观察到的PtNPs对突触传递的刺激效应是否会影响内层视网膜的神经信号传递。为解答这一问题,我们测量了振荡电位(OPs)的振幅—一这些叠加在B波上升相的小波簇反映了内层视网膜中双极细胞、无长突细胞与神经节细胞间的交互作用。观察到在PtNPs处理的病变组中,OP振幅较媒介物处理组显著增大,这与视网膜信息处理的整体再激活现象相一致 (图5G、H) 。
光损伤后用铂纳米酶体内治疗的损伤视网膜显示出ON型视网膜神经节细胞反应的选择性保护。在invivo记录结束时及组织化学分析前,视网膜被紧急摘取并以视网膜上配置方式放置于高清MEA芯片上进行exvivo电生理分析。每片视网膜的背侧和腹侧部分被分割并分别记录。记录的背侧半视网膜3D重建图像一一附有外核层、内核层和视网膜神经节细胞层的特写镜头显示:载体处理组的视网膜结构遭到严重破坏,而PtNP处理组则得到实质性保留(图6A)。
随后,我们采用两组刺激对半视网膜进行测试:(i)使用白色(开)或黑色(关)全视野刺激(持续时间50、100和250毫秒,频率0.25赫兹),以研究视网膜神经节细胞反应的极性和时间动态;(ii)采用1赫兹交替呈现、空间频率范围为0.03至0.80周期/度(cpd)的方形亮度光栅,以研究空间滤波和空间分辨率特性。由于个体差异以及视网膜与芯片之间电耦合的轻微变化,我们从每个样本中记录了不同数量的视网膜神经节细胞,其中载体注射组和PtNP注射组的背侧视网膜分别总计607个和213个视网膜神经节细胞,腹侧视网膜分别总计984个和193个视网膜神经节细胞,并按照方法部分所述将其分类为开型或关型细胞(图6B和图S5B)。在背侧视网膜中,开型视网膜神经节细胞是受PtNPs保护程度更高的细胞群。实际上,PtNP注射组的开型视网膜神经节细胞数量显著高于载体处理组(载体组和PtNPs组的活跃细胞占比分别为39.8%和61.5%)。随后,通过将ON或OFF刺激期间放电≤1次动作电位的视网膜神经节细胞视为“无反应”,放电>1次者视为“有反应”,计算出每种刺激极性对应的有反应视网膜神经节细胞百分比。分析还表明,PtNPs处理使得背侧视网膜中具有响应性的视网膜神经节细胞(RGC)数量相较于无响应性的RGC有所增加,而在同一区域的OFF-RGC群体中未观察到显著差异(图6C)。
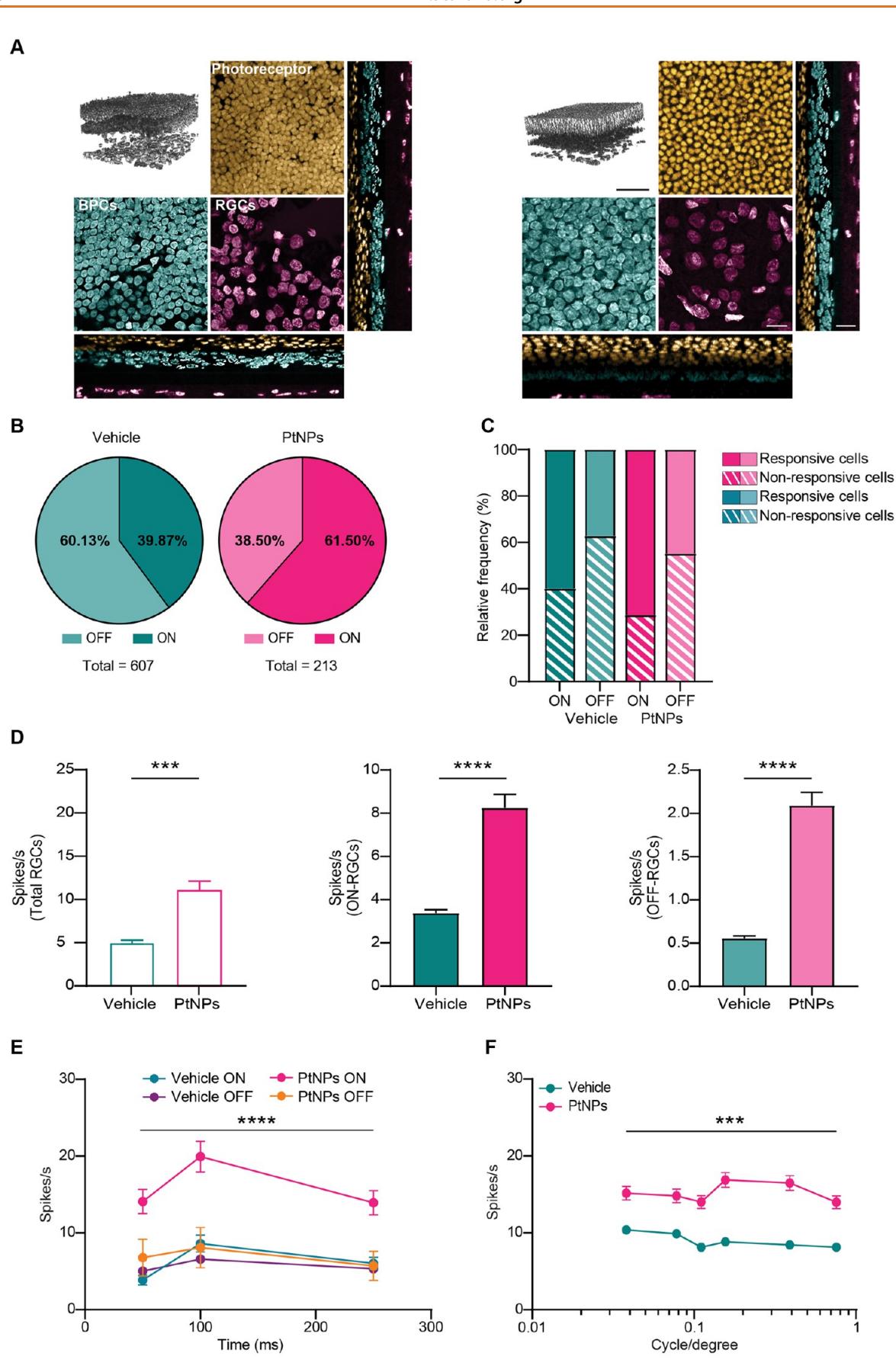
图6.铂纳米粒子损伤后处理对背侧光损伤视网膜中视网膜神经节细胞放电的影响。 (A)左上图:光损伤24小时后,载体(左)和铂纳米粒子(右)处理大鼠代表性背侧半视网膜的三维重建(比例尺: )。其他面板:各视网膜层的z轴放大图及正交XZ、YZ投影(比例尺: )。铂纳米粒子处理改善了视网膜结构,而载体处理视网膜因持续退化出现显著结构改变。(B) 饼图显示光损伤24小时后,在对照组(蓝色)和PtNP处理组(红色)大鼠的每个背侧半视网膜中,记录到的活跃细胞总数中,处于ON状态(深色)和OFF状态(浅色)的视网膜神经节细胞所占百分比。值得注意的是,PtNP处理的视网膜中活跃ON-RGCs的出现率更高 ,Fisher精确检验)。©各RGC极性响应细胞的百分比。两组中ON-RGCs的响应性均更高。PtNP处理进一步提高了ON-RGCs的响应比例,而OFF-RGCs未观察到差异。(D)在光损伤24小时后,经载体(蓝色)和PtNP(红色)处理的大鼠背侧半视网膜中,总RGCs(左图;载体和PtNP分别为 ${ \bf { \dot { n } } } = 6 0 7 $ 和213个细胞)、ON-RGCs(中图;载体和PtNP分别为 和131个细胞)和OFF-RGCs(右图;载体和PtNP分别为 和82个细胞)对250毫秒全场闪光刺激的放电活动柱状图(平均值 sem)。这些图表显示PtNP处理的视网膜RGC放电活动呈现整体性显著增强。(E)全场闪光刺激引发的RGC放电时间动态。OFF-RGCs未见差异,而PtNP处理(非载体处理)视网膜的ON-RGCs表现出显著更高的放电活性。(F)通过空间频率0.2至0.8 cpd的反转光栅评估空间分辨能力所诱发的RGC放电活动。经PtNP处理的光损伤视网膜在所有测试频率下均较载体处理视网膜表现出空间分辨率的显著提升。 , , ;曼-惠特尼U检验(D),双向混合方差分析/Holm-Sidak检验(E,PtNPON-RGCs对比载体ON-RGCs;F,PtNP对比载体)。
当我们分析总RGC放电响应(左图)以及ON型(中图)和OFF型(右图)RGC群体的独立放电率时(图6D),观察到PtNP处理组视网膜中所有RGC群体的放电活动较溶剂注射组均出现显著增强。通过对背侧视网膜ON-与OFF-RGC响应时间动态的分析,我们确认PtNP处理组的ON-RGC群体表现出显著高于溶剂注射组的动态响应,而OFF-RGC群体在PtNP处理后未显示任何显著改善(图6E)。
最后,当用不同空间频率的图案刺激背侧半视网膜时,PtNP处理组的视网膜神经节细胞诱发的放电活动显著高于溶剂处理组的平坦反应曲线(图6F),这证实了观察到的振荡电位增加(见图5)。通过模拟invivo视网膜空间辨别的过程,该ex vivo实验表明PtNP能够保持视网膜神经节细胞感受野的空间组织,从而更有效地编码图案刺激。此外,PtNP注射组的空间分辨曲线形态表明,其长程和短程的侧向抑制均得到保留,而这一现象在溶剂处理的视网膜中几乎完全消失。
从视网膜腹侧部分收集的相应结果总结于图S5中。无论处理方式如何,腹侧视网膜层的3D重建均未显示明显的结构改变(图S5A)。在载体注射组和PtNP注射组中,给光-和撤光-RGCs的数量未见显著差异(载体组和PtNP组的活跃细胞比例分别为 和 ;图S5B)。两种处理方式间,给光-RGCs的响应与非响应百分比(图S5C)以及RGC总峰电位响应(图S5D)亦无显著差异。对腹侧视网膜给光-和撤光-RGCs响应时间动态的分析(图S5E)显示,给光-RGCs的放电活动优势在载体组和PtNP处理组大鼠中相似。这一结果与背侧视网膜的相应记录形成对比一一在背侧视网膜中,给光-RGC群体对光损伤及PtNPs的保护作用均表现出更高的敏感性。
在光损伤后施用铂纳米酶可显著减轻光感受器变性和视网膜炎症。通过双苯甲亚胺核染色以及炎症标志物GFAP和IBA1的免疫组化检测,评估了损伤后PtNPs治疗对视网膜形态的影响。与预防性方案中观察到的结果相反,用PtNPs治疗光损伤视网膜显著保留了外核层中光感受器细胞核的数量(图7)。
尽管PtNPs未能保护热点区域的PR细胞群(但在该区域观察到了更好的形态保存和更少的rosettas;图7A),与对照组相比,外周背侧视网膜得到了显著保护(图7B)。如图2和图4所示,两个实验组在视网膜腹侧部分未观察到差异,该区域对光损伤具有较强抵抗力且形态未明显受影响(图7C,D)。通过对ONL/视网膜总厚度比值(图7E)和PR细胞层数(图7F)随视神经距离变化的定量分析,证实了PtNPs存在下外周背侧区域ONL中PR细胞群具有高度显著性的保护效果。
随后,我们通过评估穆勒细胞/星形胶质细胞中GFAP的表达以及小胶质细胞的数量和活化状态,分析了治疗对光损伤引发的炎症反应的影响。与功能恢复的结果一致,PtNPs治疗显著降低了GFAP表达,这不仅发生在背侧周边区域 (正如预防性方案中已观察到的,见图4),在光氧化损伤最严重的核心区域也同样明显(图8A,B,左图)。PtNPs的显著保护作用既体现在GFAP表达积分密度的定量分析中(中图),也体现在累积频率分布曲线上(右图)。正如预期,在两种实验条件下,腹侧视网膜几乎未受光损伤影响(图8C,D)。
我们最终分析了IBA1阳性小胶质细胞。在生理条件下,驻留小胶质细胞位于视网膜内层并呈现分枝状形态。应激诱导后,小胶质细胞失去突起,转变为阿米巴样形态,并迁移至视网膜外层,开始从脉络膜循环中招募巨噬细胞。PtNP处理组背侧视网膜热点区域的小胶质细胞数量未发生改变(图9A)。然而,为评估小胶质细胞的促炎激活状态,我们对每个IBA1-阳性细胞。热点小胶质细胞突起的肖尔分析显示,与溶剂处理的视网膜相比,PtNP处理的视网膜中交叉点数量增加2倍,表明其分支形态显著增多(图9B)。这种治疗依赖性变化通过圆度指数分析得到了证实,经铂纳米粒子处理的视网膜中的小胶质细胞保持了静息状态、分支状小胶质细胞特有的低圆度指数特征(图9C),而溶剂处理的视网膜中的小胶质细胞则呈现圆形。铂纳米粒子的抗炎作用同样明显体现在背侧周边区域的小胶质细胞数量显著减少了超过4倍(图9D),而在腹侧视网膜未观察到任何影响(图S6)。
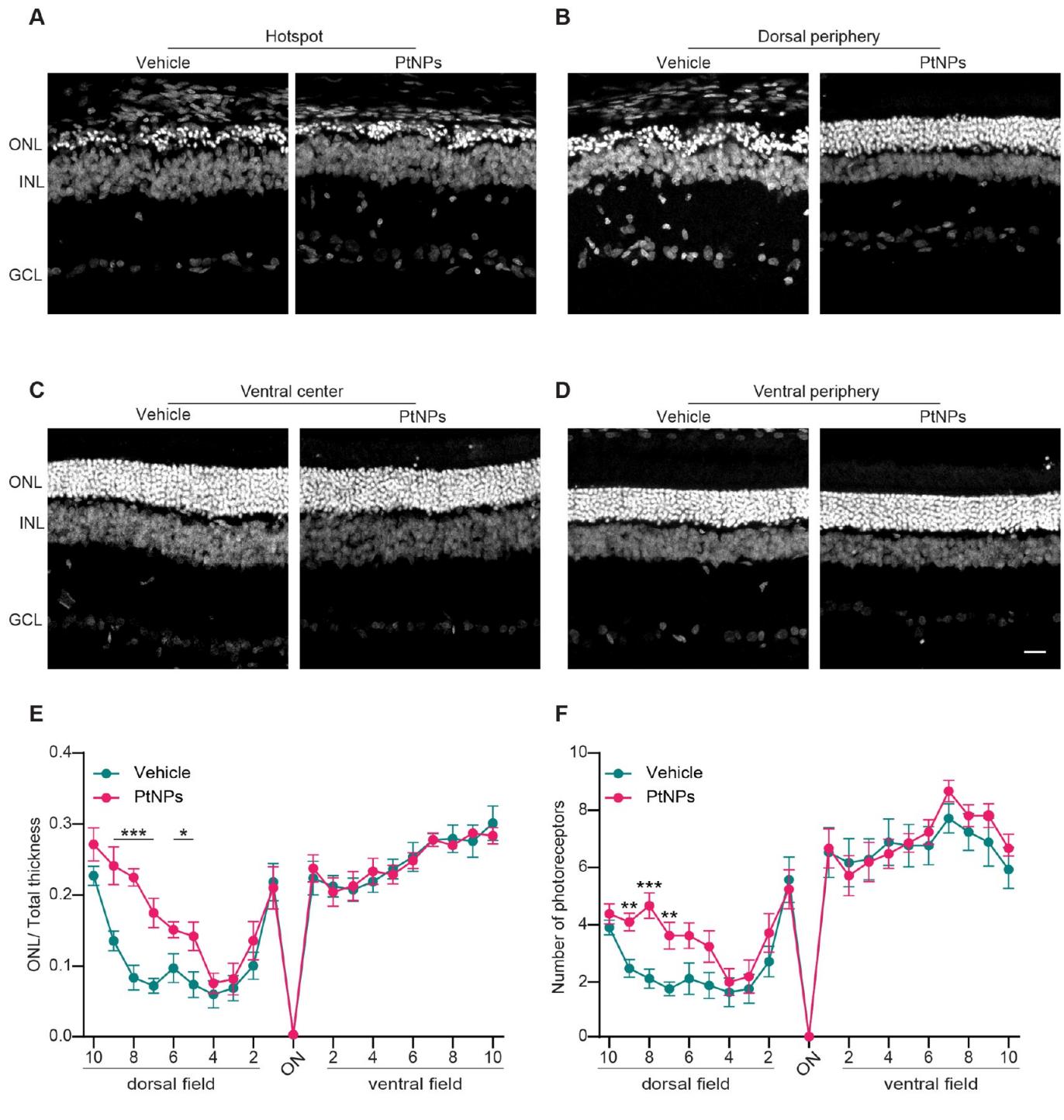
图7.光损伤视网膜后PtNPs治疗的形态学效应。(A-D)背侧周边区、热点区及腹侧视网膜的代表性横切面,采用bisbenzimide进行细胞核标记(白色)。缩写:ONL,外核层;INL,内核层;GCL,神经节细胞层。比例尺: (E、F)将ONL厚度标准化至视网膜总厚度(E)及光感受器核层行数(F),在从背侧周边至腹侧周边 (经过视神经)的20个等距视网膜位点进行统计,对象为光损伤24小时后注射载体(蓝色)或PtNPs(红色)的动物。数据以均值 标准误表示。样本量:载体组 ;PtNPs组 * , , ;双因素混合方差分析/费希尔LSD检验。PtNPs能显著维持背侧视网膜周边区的ONL厚度与光感受器数量,将损伤区域扩展仅限制在热点水平,并阻止变性向半影区蔓延。腹侧区域未受光损伤影响。
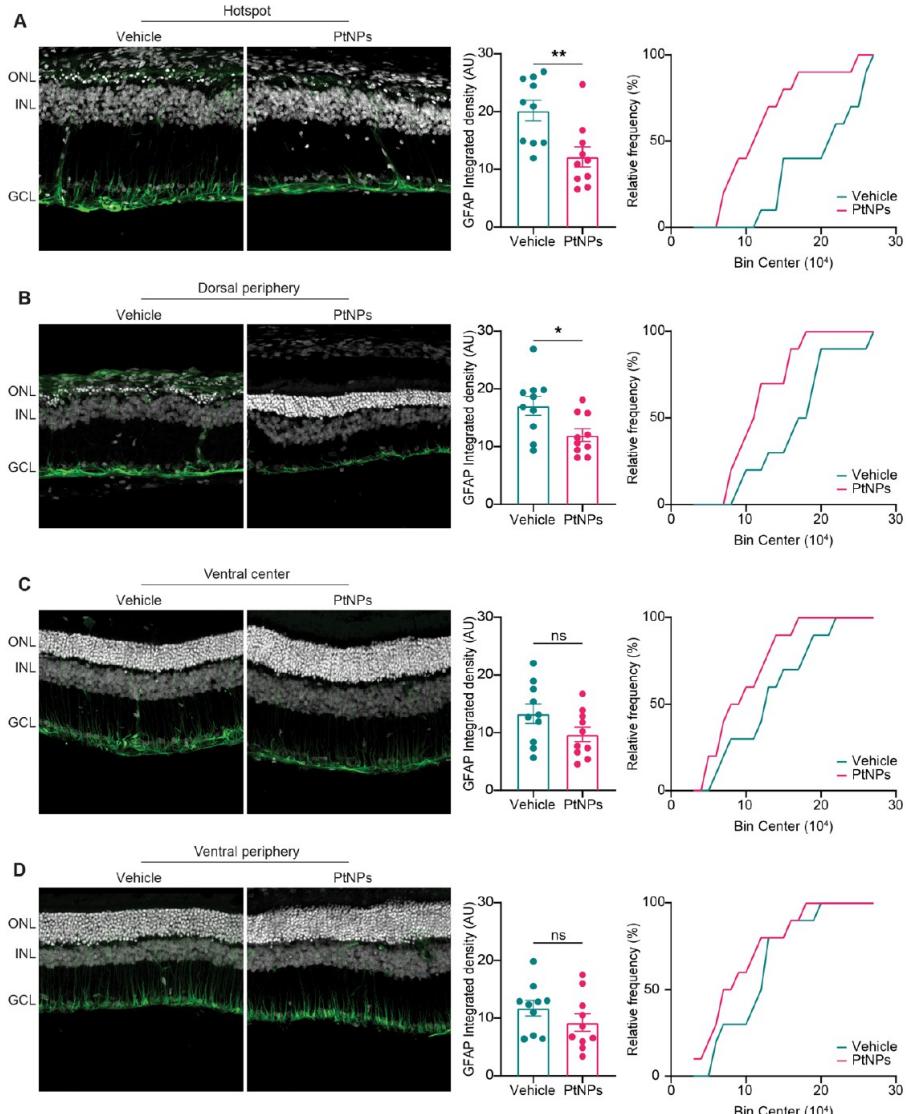
图8.PtNPs损伤后治疗对光损伤视网膜中星形胶质细胞活化的影响。(A-D)在光损伤后24小时注射载体(蓝色)或PtNPs(红色)的动物视网膜中,对背侧视网膜热点区(A)和周边区(B)以及腹侧视网膜中心区(C)和周边区(D)的GFAP表达进行分析。左侧面板:针对Muler细胞标记物GFAP(绿色)进行免疫标记的代表性视网膜横切面,与bisbenzimide核标记(白色)合并显示。缩写:ONL,外核层;INL,内核层;GCL,神经节细胞层。比例尺: 微米。中间面板:GFAP表达积分密度的定量分析。条形图表示平均值 标准误,并叠加显示各实验数据点。PtNPs显著降低背侧视网膜中GFAP的表达范围。样本量:载体组 ;PtNPs组 , ;Mann-WhitneyU检验/非配对Studentt检验。右侧面板:相应的累积频率分布曲线(分箱宽度:10000)。与载体处理的视网膜相比,PtNPs注射显著降低了Muller细胞在热点区及相邻背侧周边区中GFAP的上调(A, ;B, ;Kolmogorov-Smirnov检验)。在腹侧区域,两个实验组之间未见差异(C, ;D, ;Kolmogorov-Smirnov检验)。
综合来看,数据显示,与预防性方案相比,损伤后PtNP治疗在维持视杆细胞数量以及降低背侧视网膜穆勒细胞和小胶质细胞促炎反应方面更为有效。
¶ 结论
稀土纳米颗粒因其抗氧化和抗炎潜力已被广泛应用,以期缓解各种神经退行性疾病中的氧化应激。其中一种疾病是萎缩性年龄相关性黄斑变性(AMD),这是一种目前无法治愈的老年性黄斑病变,长期氧化应激是其致病因素之一。另一种氧化损伤可导致视网膜变性的情况是太空飞行相关神经眼综合征,这归因于持续暴露于微重力和宇宙辐射环境。68特别是,多次研究表明高剂量纳米氧化铈通过玻璃体内或局部给药,能有效预防最敏感视网膜区域(即通常不适应直接照射的背侧视网膜)的光诱导氧化损伤。41-47,56-60最近研究揭示了铂纳米颗粒具有内在的多种类酶特性,其高生物相容性和在生物介质中的稳定性使其成为增强和替代细胞内系统内源性抗氧化活性的多功能工具。38,49根据生物介质中蛋白质浓度的不同,铂纳米颗粒表面会形成蛋白质冠层,该层结构在细胞外环境中保护了PtNPs的催化活性。51然而,在细胞内部化及由于溶酶体积累,PtNPs的类抗氧化酶性质完全恢复并得到增强,这要归功于蛋白水解环境(电晕降解)与酸性pH值(增强铂纳米颗粒性能)$。在此我们于原代大鼠神经元中证实了这些特性及细胞内归宿,表明铂纳米颗粒能保护神经元免受活性氧生成和炎症诱导的细胞凋亡。此外,得益于其极小尺寸(4纳米)和RSA涂层,我们证明了它们能够穿越内界膜并渗透整个视网膜厚度,抵达光感受器细胞。
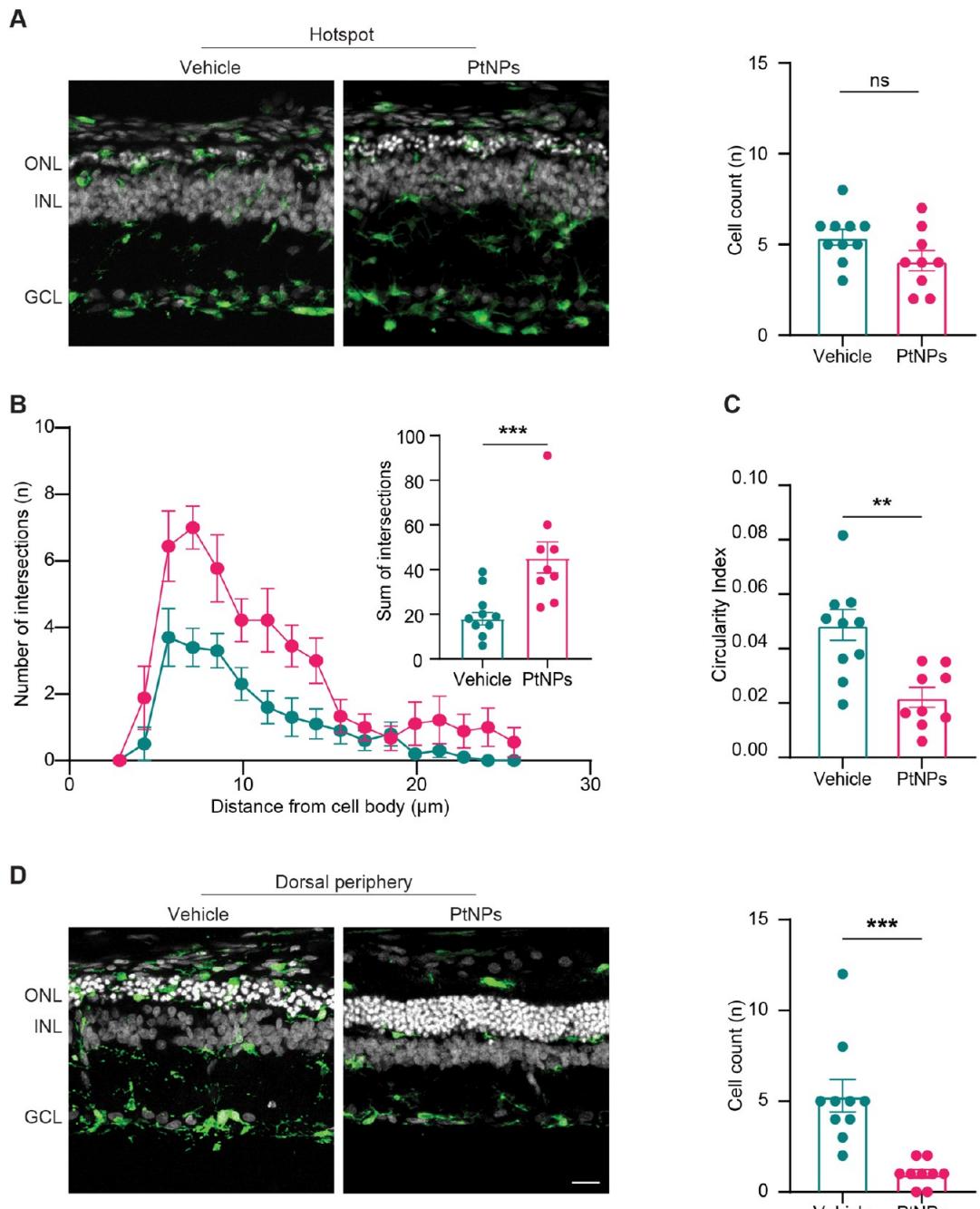
图9.PtNPs损伤后处理对光损伤视网膜中小胶质细胞活化的影响。在光损伤后24小时注射载体(蓝色)或PtNPs(红色)的动物视网膜,采用小胶质细胞标记物IBA1(绿色)进行免疫标记,并与bisbenzimide核标记(白色)合并显示。缩写:ONL,外核层;INL,内核层;GCL,神经节细胞层。比例尺: 微米。(A)背侧视网膜热点区。左侧为代表性的IBA1染色横截面,右侧条形图显示ONL中计数的IBA1阳性小胶质细胞平均数(±sem),并叠加个体实验点。(B)Sholl分析显示小胶质细胞突起与距胞体递增距离绘制同心壳的平均 ( )交点数量。插图条形图表示从胞体到最大分支延伸距离计算的交点总数均值( 。(C)背侧视网膜热点区ONL中小胶质细胞的圆形度指数。该指数通过Fiji软件插件计算,圆形度值1.0代表完美圆形,趋近零值表明多边形延伸程度增加。条形图显示均值 ( )并叠加个体实验点。PtNPs组观察到更延伸的多边形样形态,提示小胶质细胞活化程度降低。(D)背侧视网膜周边区。左侧为代表性IBA1染色横截面,右侧条形图显示ONL中计数的IBA1阳性小胶质细胞平均数( 并叠加个体实验点。小胶质细胞通常驻留于视网膜内层发挥监视作用。光损伤及光感受器变性后,小胶质细胞向视网膜外层迁移,收缩足突并呈现更类阿米巴形态。PtNPs能显著减少其在ONL的浸润。样本量:载体组 ;PtNPs组r 。 , ,非配对Student t检验(A-C),Mann-Whitney U检验(D)。
如既往使用稀土纳米颗粒的研究一样,我们在由暗光饲养白化大鼠的光氧化损伤所诱导的光感受器变性模型中评估了铂纳米颗粒的神经保护作用。这种光损伤白化大鼠模型在多个方面具有重要意义。首先,该模型是在健康成年动物中诱导建立的,减少了可能影响遗传基础模型的代偿效应。作为人类年龄相关性黄斑变性的替代模型,它具备非遗传性起源的特点,并急性复现了光感受器在生命周期中所经历的慢性氧化应激。该模型的特征是局限且渐进的光感受器变性,在无中央凹动物模型中模拟了人类萎缩性年龄相关性黄斑变性中发生的渐进性旁中心凹视杆细胞/中心凹视锥细胞死亡。第三,由于光感受器光损伤是通过氧化应激累积诱导产生的,这使其成为评估铂纳米颗粒等抗氧化疗法效能的理想模型。虽然光氧化损伤会直接且不可逆地引发热点区域的光感受器死亡,但氧化应激及随之产生的慢性炎症反应会导致外周背部视网膜区域的光感受器死亡持续扩展2,3,54,5,63,64,69,70。因此,热点区域的死亡光感受器难以恢复,而外周背部区域的光感受器尚未遭受不可逆损伤,这使其成为治疗的理想靶标。
我们通过玻璃体内注射的方式将RSA包被的铂纳米粒子(PtNPs)施用于眼部—一这是人类广泛使用的给药途径一一采用低剂量并按照两种策略进行:(i)预防性保护,即在光损伤前1周给予PtNPs;(ii)损伤后治疗,即在光损伤后1天注射PtNPs。与先前使用高浓度纳米铈的研究不同,在测试浓度下,预防性方案未能有效对抗光感受器(PR)死亡,但显著减轻了光损伤诱导的星形胶质细胞增生,并增强了视网膜电图(ERG)的B波,证明PR对二级视网膜神经元的激活功能有所改善。另一方面,在光损伤后24小时给予PtNPs(治疗性方案)一一这种在确诊疾病后使用纳米粒子的更佳策略—一效果更为显著。PtNPs显著保留了背侧视网膜周边区的外核层(ONL)厚度和PR数量,仅将损伤范围限制在热点区域,并阻止了变性向半影区扩散。这一效果在光损伤后2周对离体视网膜大量(数百个)视网膜神经节细胞(RGCs)的记录中尤为明显。PtNPs大幅增加了背侧视网膜中ON型RGCs的活跃数量,提升了它们对光刺激的放电活性,并增强了对不同空间频率图案刺激的空间分辨能力。后一种效应与PR和二级神经元之间增强的信号传递相一致,从而维持了对对比度和空间敏感性至关重要的侧向环路功能(在大鼠视网膜层面,1cpd约对应 )。
虽然抗氧化铂纳米颗粒的治疗方法有效,但不能使凋亡的光感受器再生。因此,其主要作用在于延缓退化进程,并挽救那些尚未遭受不可逆损伤、且位于热点区域(外周背侧视网膜)邻近半暗带区域的视网膜神经节细胞。在这方面,一个重要效果是背侧视网膜中星形胶质细胞增生和小胶质细胞增生的显著下调,这降低了视网膜炎症的程度并促进功能恢复。Muller细胞/星形胶质细胞标志物GFAP的表达在整个背侧视网膜中明显下调,而在炎症热点区被强烈激活的小胶质细胞则恢复至静息状态。虽然这些效应可能部分继发于变性程度的减轻,但它们很可能依赖于PtNPs直接的抗炎活性。活性氧(ROS)是关键的信号分子,主要参与炎症性疾病的调节和进展71。在这方面,PtNPs对小胶质细胞活化的抑制作用可能具有重要意义,因为最近有报道称,小胶质细胞-神经元轴可通过分泌趋化因子激活神经元mTORC通路,从而诱导神经元自噬功能障碍72,73。
多个因素可促使铂纳米颗粒(PtNPs)在损伤后治疗中表现出更高疗效。在预防性和治疗性方案中,眼内注射PtNPs与生理学分析的时间间隔均固定为15天,而两种方案的主要差异在于注射PtNPs时是否存在光诱导性炎症。在预防性方案中,PtNPs仅能在光损伤前“强化”正常视网膜的抗氧化能力;而在损伤后方案中,它们于光损伤导致视网膜炎症达到峰值时发挥作用。伴随免疫系统激活有助于PtNPs在内界膜层面的摄取,从而增强抗炎效果。事实上,PtNPs在低pH值环境下(最可能位于溶酶体区室1)展现最大催化效应,该区室在小胶质细胞炎症期间尤为活跃,且近期研究报道了纳米酶靶向小胶质细胞治疗神经退行性疾病的案例。数据表明PtNPs的主要作用在于减少炎症反应的恶性循环,而非预防光氧化损伤,当其应用于已处于炎症状态的组织时效果更为显著。确实,损伤后给予的PtNPs能同时减轻星形胶质细胞和小胶质细胞的炎症反应,而预防性给予的PtNPs仅轻微减弱星形胶质细胞对光损伤的反应。但我们不能排除以下可能性:预防性方案中PtNPs浓度可能在光损伤发生时已下降,或光损伤与生理评估之间的时间窗口较短,导致预防性治疗效果较低。
目前对铂纳米颗粒进行的生物和免疫相容性测试结果令人鼓舞,因为它们在生物/细胞环境中具有高化学稳定性(例如与银纳米颗粒不同)38,49,51,74。铂纳米颗粒已在某些国家(如日本)作为膳食补充剂、护肤霜和其他化妆品上市销售。然而,鉴于铂纳米颗粒制剂尚未获得临床批准,仍需考虑纳米材料在眼科疾病治疗中应用的普遍担忧和风险。必须承认,鉴于铂纳米颗粒卓越的催化性能,可在极低剂量下获得治疗效果,从而限制不良反应。关于PtNP给药途径,玻璃体腔注射的风险相对较低,因其已广泛应用于抗VEGF单克隆抗体治疗湿性黄斑变性,美国每年约有600万例治疗⁷⁵,且所有注射的并发症发生率仅为1.9%⁷⁶。此外,正如近期其他纳米颗粒研究所报道的,通过开发适合局部给药的眼药水制剂,未来眼内注射的风险可能进一步降低。59
综上所述,数据表明,在强烈的光氧化应激后,玻璃体内注射铂纳米颗粒(PtNPs)能够维持视网膜生理功能。通过保护光感受器与二级视网膜神经元之间的突触传递并减少胶质细胞的活化,视觉信息处理得以改善。这表明铂纳米颗粒的作用主要针对光氧化损伤引发的炎症反应,而该反应已知是视网膜退行性病变进展的主要环节之一。相应地,铂纳米颗粒的活性会影响视网膜信号传导,这意味着该疗法对多数视网膜退行性病变可能有效,并可作为预防电磁辐射所致高风险视网膜损伤(如航天飞行中)的手段。我们倾向于推测,铂纳米颗粒可通过发挥强大的抗氧化与抗炎协同作用,有效打破活性氧、退行性病变与炎症之间的恶性循环。尽管仍需在更可靠的萎缩性年龄相关性黄斑变性模型(如碘酸钠损伤的猪视网膜模型)77上进行进一步研究,但退行性视网膜中光感受器存活率提高、炎症减轻以及视觉功能改善的结果,使铂纳米颗粒成为治疗年龄相关性黄斑变性的潜在策略。
¶ 方法
伦理批准与动物处置。白化SD孕鼠购自查尔斯河公司(意大利卡尔科)。用于invivo研究的大鼠饲养于低光照环境(5-10勒克斯,12小时光照/12小时黑暗,早7点开灯),恒温( )恒湿( ),提供饮用水及全价颗粒饲料(意大利塞蒂莫米拉内塞Mucedola公司adlibitum),饲养于IRCCS圣马蒂诺医院动物中心的环境富集条件下。所有动物操作及程序均遵循欧盟委员会指导原则(2014年3月4日第2014/26/EU号指令)执行,并获意大利卫生部批准(分别针对invitro和in vivo实验的484/2021-PR号及357/2019-PR号许可)。本研究通过遵循3R原则全力减轻动物痛苦并减少使用数量。
纳米颗粒的合成、表征与稳定化。 PtNPs的合成与稳定化。PtNPs的制备遵循先前报道的方案49,51。所有试剂均使用超纯水配制用于反应。简言之,将 氯铂酸(H ,P7082,BioXtra级,Merck)与 柠檬酸三钠 ,71402,BioUltra级,Merck)在室温条件下连续加入 持续搅拌的超纯水中。随后,在搅拌下逐滴加入 硼氢化钠 ,213462,Merck),将温度升至 并维持30分钟。形成的棕黑色胶体悬浮液在室温冷却后,使用10kDaAmicon离心过滤器,以 柠檬酸钠多次洗涤以去除可能残留的未反应铂前体。最终PtNP浓缩液用NaOH调节至中性pH,并稀释于 大鼠血清白蛋白(RSA,Sigma-Aldrich)溶液中。进行额外洗涤以消除过量柠檬酸盐,并将NPs重新浓缩至约 浓度(含 RSA)。通过电感耦合等离子体质谱(ICP-MS)对RSA稳定化的PtNP进行浓度定量。用于玻璃体内注射的工作浓度为 PtNPs(含 RSA,接近生理玻璃体组成)。
制备柠檬酸盐稳定的 的TMAOH稳定CeONPs )购自AppliedNanoparticle(纳米技术工程公司)。
TMAOH稳定的 经过配体交换获得柠檬酸盐稳定的 配体交换过程包括:使用 柠檬酸三钠溶液通过离心对胶体悬浮液进行多次洗涤,且每次离心步骤前对悬浮液进行20分钟超声处理。为避免潜在团聚,将NPs重新悬浮并在数日内配置成 的溶液。所有测量前,柠檬酸盐稳定的 悬浮液均经20分钟超声处理。通过TEM和DLS对柠檬酸盐稳定的 悬浮液进行分析,结果显示其在生理pH值下相比TMAOH稳定的CeO具有更优的胶体稳定性和更小的流体动力学半径。 名词短语。
动态光散射。采用Nano ZS(英国马尔文仪器公司)通过动态光散射测定PtNPs的流体动力学直径。进行了三次独立测量,每次累计运行11次。
琼脂糖凝胶电泳实验。采用 琼脂糖凝胶、90V、25分钟的条件,通过电泳评估存在与不存在RSA蛋白冠的PtNP 电泳运行情况。
氧传感器测量。实验在8毫升玻璃瓶中进行,瓶口以隔膜塞密封。通过将细针插入隔膜,使系统内部压力与大气压保持平衡。瓶内气相氧浓度变化通过光纤针式传感器(Pyroscience公司FireSting-O2传感器)进行记录。
样品瓶中装有300μL的HO(2.5M)、800μL乙酸盐缓冲液(pH=5)和400μL纳米颗粒悬浮液,最终获得铂纳米颗粒浓度为0.2ppm,氧化铈纳米颗粒浓度为1000 ppm的混合溶液。反应混合物在整个实验过程中保持在室温(约25℃),空气对照(基线)显示约20%的
大鼠原代皮层神经元氧化应激检测方法。原代皮层细胞培养物取自野生型Sprague-Dawley大鼠(意大利卡尔科CharlesRiver公司),实验过程中尽一切努力减少动物痛苦并降低使用数量。简言之,通过CO吸入法处死孕鼠,经剖腹产取出18天胚胎(E18)。将酶解分离的皮层神经元以每孔80000个细胞的总密度接种于聚-D-赖氨酸包被(0.1mg/mL,Sigma公司)的玻片上。细胞在37℃、5%COz、90%湿度的条件下,使用Neurobasal培养基 (Gibco/Thermo-Fischer Scientific公司)进行培养,培养基添加物终浓度为: 谷氨酰胺、1%青霉素/链霉素及5%B27补充剂 (Gibco/Thermo-Fischer Scientific公司)。
2’,7’-二氯荧光素(DCFDA)检测法。将原代大鼠皮层神经元(每孔 个细胞)接种于12孔板中,在标准细胞培养条件下培养。细胞使用终浓度为 的RSA稳定化铂纳米颗粒进行处理。孵育48小时后,洗涤神经元以去除未内化的铂纳米颗粒,并通过 -二氯荧光素(DCFDA)检测法对细胞内活性氧(H2O2)水平进行定量分析。在FluoroBrite培养基(Gibco)中,神经元与DCFDA探针及 于 C共孵育15分钟。随后用新鲜FluoroBrite培养基洗涤神经元,并使用Infinite 200 Pro Tecan酶标仪测定DCF荧光强度。激发滤光片设置为 ,发射滤光片为 。实验结果以未经处理的细胞(阴性对照)为基准进行标准化。未添加铂纳米颗粒的H2O2处理组作为阳性对照。
二氢乙锭(DHE)检测。将原代大鼠皮层神经元以 的密度接种于96孔板(Falcon)中,终体积为 ,在标准细胞培养条件下培养。用浓度为 的RSA稳定化铂纳米粒子处理细胞48小时。随后洗涤神经元以去除未内化的铂纳米粒子,并与5μM的抗霉素A(ThermoFisher)孵育24小时。使用二氢乙锭检测试剂盒(Abcam)对细胞内活性氧(超氧阴离子)水平进行定量。DHE使用浓度为5μM,与细胞孵育1小时30分钟。 在使用Tecan Infinite 200 Pro微孔板阅读器测量DHE强度之前,添加了新鲜的FluoroBrite。激发滤光片设定为 ,发射滤光片设定为 。结果相对于未处理细胞(阴性对照)进行标准化处理。使用不含PtNPs的AntimycinA处理作为阳性对照。
细胞凋亡/Caspase3/7检测。将原代大鼠皮层神经元以 5个/孔的密度接种于96孔板中,每孔终体积为 ,并在标准细胞培养条件下培养。神经元使用浓度为 的RSA稳定化铂纳米颗粒进行处理。孵育48小时后,细胞分别与 MH202共同孵育15分钟,或与5 抗霉素A共同孵育24小时,随后加入CellEvent caspase 3/7检测试剂(赛默飞)孵育30分钟。在通过Infinite 20o Pro Tecan酶标仪测量caspase荧光强度前,需添加新鲜FluoroBrite培养基。激发滤光片设定为502nm,发射滤光片设定为 。结果以未处理细胞(阴性对照)为基准进行标准化。未添加铂纳米颗粒的H2O2和抗霉素A处理组作为阳性对照。
透射电子显微镜(TEM)成像观察铂纳米颗粒(PtNPs)。通过滴铸法将3μL胶体样品(经适当稀释)沉积在铜网(CF150-Cu-50-150目碳膜)上,真空干燥处理。使用ImageJ软件测量至少200个纳米颗粒的直径,构建纳米颗粒尺寸统计分布图。
原代神经元成像。将原代大鼠皮层神经元与RSA稳定的铂纳米颗粒(浓度 )共同孵育48小时,随后用胰蛋白酶-EDTA解离,离心后重悬于含 戊二醛的细胞培养基固定液中,室温缓慢搅拌条件下固定45分钟。神经元经离心后,在0.1MNa-二甲肿酸盐缓冲液配制的 戊二醛中室温轻柔搅拌孵育1小时,并用 -二甲肿酸盐缓冲液洗涤3次(每次10分钟)。随后将神经元置于 -二甲肿酸盐缓冲液配制的 四氧化俄中进行后固定90分钟。细胞在 条件下用 醋酸铀水溶液染色过夜。经Milli-Q水多次清洗后,样品通过梯度乙醇系列( , )脱水并包埋于EPON树脂中。未处理的细胞作为对照。使用莱卡EMUC6超薄切片机配备金刚石刀切割70纳米厚度的切片。
离体视网膜成像技术。在玻璃体内注射PtNPs24小时后解剖视网膜组织。将视网膜样本置于聚四氟乙烯多孔板支架中,用 二甲肿酸钠缓冲液快速漂洗,随后在室温条件下用含 戊二醛的 二甲肿酸钠缓冲液固定2小时,并用0.1M二甲肿酸钠缓冲液洗涤3次(每次10分钟)。接着用含 酸与 亚铁氰化钾的0.1M二甲肿酸钠缓冲液后固定90分钟,用PBS冲洗3次后再以去离子水清洗2次。随后在避光条件下用 醋酸铀酰替代物(溶于HO)室温染色45分钟。经Millipore 纯水多次清洗后,样品通过梯度乙醇(70%、90%、96%、100%v/v)进行脱水处理。环氧树脂包埋过程包括:先后在环氧丙烷中浸泡30分钟,EPON树脂与环氧丙烷混合液(1:1)中静置过夜,EPON树脂与环氧丙烷混合液(2:1)中处理3小时,最后在纯 EPON树脂中浸渍48小时。超薄切片使用LeicaEMUC6超薄切片机制备:先用玻璃刀切割 厚度切片并经甲苯胺蓝染色观察视网膜分层结构,确定目标区域后用金刚石刀切割 超薄切片。成像使用日本JEOL公司生产的JEM1011型透射电子显微镜完成,工作加速电压为 。
光氧化损伤程序。为诱导光氧化损伤,将SD大鼠单独置于透明有机玻璃笼中,笼内不铺设垫料或放置水瓶以避免任何阴影区域。将笼具放入光照柜(型号3-00001125-0,Tecniplast)中,持续接受1000勒克斯的双向光照24小时。光氧化程序结束后,恢复并维持低照度条件(5-10勒克斯),直至下一实验程序开始。
玻璃体内注射操作流程。在光氧化损伤前1周(损伤前处理)或损伤后2天(损伤后处理),通过异氟烷吸入麻醉动物(诱导浓度 ;维持浓度 )。使用东莨菪碱眼药水(10 mg/mL,Visumidriatic,VisuFarma)扩瞳,并用盐酸苯氧苄胺眼药水(4 mg/mL,Novesina,Alfa Intes)进行局部麻醉。保持 角度,使用30号针头进行两次连续穿刺以实现结膜的最佳穿透。这为后续注射所用的34号钝头汉密尔顿针开辟了更易操作的路径。通过聚四氟乙烯管连接汉密尔顿针的微量注射器(UMP3T-1,WPI)用于控制注射溶液的流速。流速设定为 ,总注射量为2 手术操作在手动外科显微镜(LeicaM651)下进行,术中持续使用无菌生理盐水保持角膜湿润。术后预防性处理中,角膜使用妥布霉素地塞米松( ,Tobradex,Alcon)进行局部治疗。
闪光视网膜电图(fERG)记录。动物暗适应1小时后,在暗室中进行记录。在微弱的红光下,通过异氟烷吸入麻醉动物(诱导浓度 ;维持浓度 ),并将其置于位于全视野球罩内的立体定位仪上。使用托吡卡胺滴眼液散瞳,并使用盐酸苯诺辛酯滴眼液进行局部麻醉。记录过程中使用无菌生理盐水保持角膜湿润。将主动环形铂电极置于角膜上,参考电极和接地铂电极分别皮下植入颊部和头皮。通过直肠探针监测体温,并使用加热垫维持在 左右。视网膜反应通过单眼记录获得,同时闭合对侧眼。fERG方案采用对数递增的光强度闪光刺激。每次记录3个反应,刺激间隔5秒,最后取平均值。记录过程中使用高通和低通滤波器。从记录中提取的参数包括A波、B波和振荡电位的振幅。A波振幅从基线测量到第一个负向波峰,B波振幅从A波负向波峰测量到最高正向波峰。振荡电位通过60Hz高通滤波器对波形进行滤波后测量,并对第1-4个波峰的振幅和潜伏期进行求和。
高密度多电极阵列(HD-MEA)记录。Exvivo视网膜记录采用高密度多电极阵列(HD-MEA)(BioCamX,3Brain)进行。光刺激由投影仪(E4500MKII,EKB Technologies Ltd.)提供,该投影仪与Z16APO显微镜 (Leica,德国韦茨拉尔)耦合,以将刺激聚焦并定位于视网膜中心。动物通过吸入 和颈椎脱位法实施安乐死。眼球被摘除并标记背侧-腹侧方位。视网膜在充氧( , )的Ames培养基(Sigma-Aldrich,圣路易斯,密苏里州)中快速解剖,并分为背侧和腹侧半视网膜。随后将样本置于基于CMOS的BioCamX高密度多电极阵列(Arena芯片;3Brain,瑞士普费菲孔)上。4096个电极直接与所记录半视网膜的视网膜神经节细胞接触。峰值排序和峰值检测使用3Brain提供的基于Henning排序算法的例程进行。排序结果经人工监督和调整,以消除被误采样为信号的噪声。在后续分析中,仅考虑整个记录期间发放率大于0.5 spike/s的通道。视网膜神经节细胞的极性通过全视野黑白闪光期间诱发的峰值数量进行评估。呈现了40次扫描,持续时间分别为10、50和250毫秒,其间穿插4秒灰色背景。我们还通过使用空间频率范围为0.3至0.8cpd、频率为2Hz的反转光栅刺激,并记录对光栅条纹的脉冲响应,分析了半视网膜的空间分辨率。cdp的计算以线性测量 微米为参考。78
视网膜免疫染色程序。通过吸入CO和颈椎脱位法对动物实施安乐死。摘除眼球,标记背腹方向,置于含4%多聚甲醛(Sigma-Aldrich,圣路易斯,密苏里州)的0.1M磷酸盐缓冲液(PBS,Sigma-Aldrich 公司,美国密苏里州圣路易斯)中固定中过夜,并在0.1MPBS中漂洗三次,每次10分钟。解剖眼球去除角膜、虹膜和晶状体。获得的眼杯经 和 蔗糖溶液平衡冷冻保护后,包埋于OCT冷冻培养基(Tissue-Tek;Qiagen)中,并于干冰中冷冻。使用 MC5050冷冻切片机(Histo-Line Laboratories)切割 的视网膜切片,收集于明胶和多聚赖氨酸包被的载玻片上,并在免疫染色前保存于 。所有免疫组织化学分析中,切片均用0.1MPBS 漂洗三次以去除多余OCT,随后在室温下用 正常山羊血清(NGS,Sigma-Aldrich,圣路易斯)封闭1小时以避免抗体非特异性结合。根据表1,将针对穆勒细胞/星形胶质细胞标记物GFAP 和小胶质细胞标记物IBA1的一抗用含 Triton X-100的0.1MPBS 稀释,并于 孵育过夜。切片经 PBS漂洗三次后,在室温下用bisbenzimide 核标记染料(1:300 Hoechst,Sigma-Aldrich,圣路易斯)及1:100 稀释的二抗共同孵育1小时。切片经 PBS 漂洗三次去除多余抗体,最后用Mowiol封片剂(Sigma-Aldrich,圣路易斯)和 mm 盖玻片封片。视网膜图像通过激光扫描共聚焦显微镜(Leica SP8;德国韦茨拉尔)搭配 倍油镜获取。半视网膜组织用bisbenzimide核标记染料(1:300)孵育30分钟,经0.1MPBS 洗涤三次后,夹在两片 盖玻片之间进行封片。
表1
| Primary antibody | Localization | Supplier | Cat. No. | Host | Type | Dilution | Secondary antibody | Dilution | Host |
| Anti-GFAP | Muiller cell | Sigma | G3893 | Mouse | Monoclonal | 1:250 | AlexaFluor 488 | 1:100 | Goat |
| Anti-IBA1 | Microglia | Wako | 019-19741 | Rabbit | Polyclonal | 1:500 | AlexaFluor 568 | 1:100 | Goat |
视网膜形态计量学分析。所有视网膜形态计量学分析均通过对经过视盘的眼背腹侧切片进行成像来完成,采用 微米的中央及外周 层扫描,分辨率 24像素,Z步进330纳米。对于视网膜半球,采集参数为129.2 微米,分辨率 像素。为便于比较,所有成像过程中采集参数保持恒定。所有图像均使用ImageJ软件(NIH,贝塞斯达,马里兰州)进行处理。
双苯甲酰胺核染色。为评估外核层厚度和光感受器数量,以视神经为参照将视网膜切片分为20个等距区域(10个背侧和10个腹侧)。外核层厚度以外核层与视网膜总厚度的比值进行测量,并同步计算光感受器行数。
GFAP与IBA1分析。为评估GFAP积分光密度,将各层(GCL、IPL、ONL)三个感兴趣区域(ROI; 像素)的平均值进行加和。
从外核层中分离出单个IBA1阳性细胞并进行二值化处理。使用ImageJFiji发行版中的Circularity插件计算圆形度指数(圆形度 (面积/周长))。圆形度值为1.0代表完美圆形,数值越接近零则表示多边形趋于细长。通过排除胞体进行Sholl分析并统计交点总数:以胞体为中心绘制直径步进 的同心圆,评估神经突延伸长度及其与各同心圆的交叉分支数量。外核层中的IBA1阳性细胞采用人工计数。
统计分析。计划实验所需样本量 是使用G*Power软件预先确定的,针对四组实验设计的方差分析,基于类似实验及预实验数据,设定效应值0.25-0.40、 (I类错误) 和1 (ⅡI类错误) 。实验数据均以均值 标准误表示,对应 样本量。采用D’Agostino-Pearson正态性检验评估数据分布形态。两组样本比较使用Studentt检验(正态分布)或Mann-Whitney U检验(非正态分布)。为比较两个以上的正态分布实验组,采用单向或双向混合方差分析,随后进行霍姆-希达克、图基或费希尔LSD多重比较检验。实验组间的累积分布采用Kolmogorov-Smirnov检验进行分析。列联分析使用Fisher精确检验进行。变量间的相关性检验基于皮尔逊相关系数进行。当p值 时视为具有统计学显著性。统计分析使用MATLAB R2022b和GraphPad Prism 9.5.1软件完成。
¶ 相关内容
*s支持信息
支持信息可在htps:/pubs.acs.org/doi/10.1021/acsnano.3c07517免费获取。
关于PtNPs表征、它们在外视网膜中的存在、健康大鼠与光损伤大鼠B/AERG波之间的相关性、PtNPs预防性治疗对光损伤视网膜中小胶质细胞活化的影响,以及PtNPs后损伤治疗对腹侧光损伤视网膜中神经节细胞放电和小胶质细胞活化的影响的补充结果 (PDF)
¶ 作者信息
通讯作者 Pier Paolo Pompa - Nanobiointeractions & Nanodiagnostics, Istituto Italiano di Tecnologia,l6l63 Genova,Italy; orcid.org /0000-0001-7549-0612;电子邮件:pierpaolo.pompa iit.it 法比奥·本费纳蒂- Center for Synaptic Neuroscience and Technology,Istituto Italiano di Tecnologia,6l32 Genova, Italy; IRCCS Ospedale Policlinico San Martino,16132 Genova, Italy;ORCID编号:0000-0002-0653-8368; 电子邮件:fabio.benfenati@iit.it
¶ 作者
萨拉·库皮尼 - 突触神经科学与技术中心,意大利理工学院,16132 热那亚,意大利;实验医学系,热那亚大学,16132 热那亚,意大利
斯蒂法诺·迪马尔科 - 突触神经科学与技术中心,意大利理工学院,16132 热那亚,意大利;IRCCS 圣马蒂诺综合医院,16132 热那亚,意大利;orcid.org/0000-0003-4847-6270
卢卡·博塞利 - 纳米生物相互作用与纳米诊断中心,意大利理工学院,16163 热那亚,意大利;orcid.org/0000-0002-2732-5484
亚历西奥·卡瓦利 - 突触神经科学与技术中心,意大利技术研究院,16132 热那亚,意大利;实验医学系,热那亚大学,16132 热那亚,意大利
朱莉娅·塔里科内 - 纳米生物相互作用与纳米诊断学,意大利技术研究院,16163 热那亚,意大利
瓦伦蒂娜·马斯特罗纳尔迪 - 纳米生物相互作用与纳米诊断中心,意大利理工学院,16163 热那亚,意大利
瓦伦蒂娜·卡斯塔尼奥拉 - 突触神经科学与技术中心,意大利理工学院,l6l32 热那亚,意大利;IRCCS 圣马蒂诺综合医院,16132 热那亚,意大利
伊丽莎白·科伦坡 - 突触神经科学与技术中心,意大利理工学院,16132 热那亚,意大利;IRCCS 圣马蒂诺综合医院,16132 热那亚,意大利
完整的联系信息请访问:https://pubs.acs.org/10.1021/acsnano.3c07517
作者贡献
-S.C.和S.D.M.共同贡献。
声明作者声明没有竞争性财务利益。
¶ 致谢
我们衷心感谢 Antonio De Fusco 博士和Doriana Debellis博士(意大利热那亚IIT电子显微镜中心)在电子显微镜技术上的协助,GiuliaMirra 和Lorenzo Cursi(意大利热那亚意大利技术研究院)在氧化铈纳米颗粒表征方面的帮助,以及Filippo Galluzzi(意大利热那亚意大利技术研究院)在图像处理方面的支持。同时,我们感谢R.Ciancio、I.Dallorto、A.Mehilli、R.Navone 和D.Moruzzo(意大利热那亚意大利技术研究院)提供的技术与行政协助。本研究获得了以下项目的资助:Euronanomed3(项目Nanolight 2019-132予F.B.)、意大利卫生部(最终研究项目RF-2021-12374404予F.B.)、意大利大学与研究部(PRIN2020WMSNBL予F.B.)以及IRCCS圣马蒂诺医院热那亚分院(常规研究及5×1000资助项目予F.B.、E.C.和 S.D.M.)。此外,我们亦感谢意大利航天局(ASI)和欧洲航天局(ESA)对P.P.P.和 F.B.的支持。
¶ 文献列表
- Sies H. 过氧化氢:作为生理性氧化应激核心氧化还原信号分子的氧化良性应激[J]. Redox Biology, 2017, 11: 613-619.
- Yu D-Y, Cringle S J. 视网膜变性与局部氧代谢[J]. Exp Eye Res, 2005, 80: 745-751.
- Kunchithapautham K, Rohrer B. 暴露于氧化应激的光感受器中的凋亡与自噬[J]. Autophagy, 2007, 3: 433-441.
- Bardi G, Boselli L, Pompa P P. 铂纳米酶的抗炎潜力:机制与展望[J]. Nanoscale, 2023, 15: 14284.
- Mariotti A, Pascolini D. 全球视力损伤估计[J]. Br J Ophthalmol, 2012, 96: 614-618.
- Ferrari S, et al. 视网膜色素变性:基因与疾病机制[J]. Current Genomics, 2011, 12: 238-249.
- Friedman D S, et al. 美国年龄相关性黄斑变性患病率[J]. Arch Ophthalmol, 2004, 122: 564-572.
- Yonekawa Y, Kim I K. 年龄相关性黄斑变性的临床特征及当前治疗[J]. Cold Spring Harbor Perspectives in Medicine, 2015, 5: a017178.
- Yonekawa Y, Miller J W, Kim I K. 年龄相关性黄斑变性:诊疗进展[J]. Journal of Clinical Medicine, 2015, 4: 343-359.
- Provis J M, Penfold P L, Cornish E E, et al. 黄斑的解剖与发育:专门化及其对黄斑变性的易感性[J]. Clinical and Experimental Optometry, 2005, 88: 269-281.
- de Morais Fabricio D, Chagas M H N, Diniz B S. 衰弱与认知衰退[J]. Translational Research, 2020, 221: 58-64.
- Berdeaux G H, Nordmann J-P, Colin E, Arnould B. 年龄相关性黄斑变性患者的视力相关生活质量[J]. American Journal Of Ophthalmology, 2005, 139: 271-279.
- Jarrett S G, Boulton M E. 氧化应激在年龄相关性黄斑变性中的后果[J]. Molecular Aspects of Medicine, 2012, 33: 399-417.
- Potilinski M C, Tate P S, Lorenc V E, Gallo J E. 新疗法揭示年龄相关性黄斑变性中氧化应激与免疫机制的新见解[J]. Neuropharmacology, 2021, 188: 108513.
- Chan T C, et al. 活性氧在视网膜疾病发病机制和治疗中的作用[J]. Exp Eye Res, 2020, 201: 108255.
- Ozawa Y. 光暴露视网膜中的氧化应激及其在年龄相关性黄斑变性中的意义[J]. Redox Biology, 2020, 37: 101779.
- Cabral de Guimaraes T A, Daich Varela M, Georgiou M, Michaelides M. 干性年龄相关性黄斑变性的治疗:治疗途径、临床试验与未来方向[J]. British Journal of Ophthalmology, 2022, 106: 297-304.
- Lorach H, et al. 通过光伏技术实现高视力视功能恢复[J]. Nature Medicine, 2015, 21: 476-482.
- Maya-Vetencourt J F, et al. 全有机视网膜假体在退行性失明大鼠模型中恢复视觉功能[J]. Nat Mater, 2017, 16: 681-689.
- Sahel J-A, et al. 光遗传学疗法后盲人患者视功能的部分恢复[J]. Nature Medicine, 2021, 27: 1223-1229.
- Harris A R, Gilbert F. 运用光遗传学恢复视功能时需正视风险[J]. Graefe’s Archive for Clinical and Experimental Ophthalmology, 2022, 260: 41-45.
- Abidi M, Karrer E, Csaky K, Handa J T. 干性年龄相关性黄斑变性临床试验的临床与临床前评估[J]. Ophthalmology Science, 2022, 2: 100213.
- Scholl H P, et al. 遗传性视网膜变性的新兴疗法[J]. Science Translational Medicine, 2016, 8: 368rv366.
- Maeda A, Mandai M, Takahashi M. 视网膜疾病的基因与诱导多能干细胞治疗[J]. Annual Review of Genomics and Human Genetics, 2019, 20: 201-216.
- Morizur L, Herardot E, Monville C, M’Barek K B. 人多能干细胞:理解与治疗视网膜变性的工具箱[J]. Molecular and Cellular Neuroscience, 2020, 107: 103523.
- Holan V, Palacka K, Hermankova B. 基于间充质干细胞的视网膜退行性疾病治疗:实验模型与临床试验[J]. Cells, 2021, 10: 588.
- Biswal M R, et al. 抗氧化基因治疗的时机:对治疗干性AMD的启示[J]. Investigative Ophthalmology & Visual Science, 2017, 58: 1237-1245.
- Cao Y, et al. 营养素、特定饮食模式及益生菌与年龄相关性黄斑变性的关联[J]. Curr Med Chem, 2022, 29: 6141-6158.
- Jo D H, et al. 裸露二氧化钛纳米颗粒对病理性新生血管形成的抗血管生成作用及其可控毒性[J]. Nanomedicine: Nanotechnology, Biology and Medicine, 2014, 10: e1109-e1117.
- Jo D H, Kim J H, Yu Y S, Lee T G, Kim J H. 硅酸盐纳米颗粒对血管内皮生长因子诱导的视网膜新生血管化的抗血管生成作用[J]. Nanomedicine: Nanotechnology, Biology and Medicine, 2012, 8: 784-791.
- Jo D H, et al. 金与二氧化硅纳米球对血管内皮生长因子介导血管生成的抑制活性取决于其尺寸[J]. Nano Research, 2014, 7: 844-852.
- Kim J H, et al. 金纳米颗粒通过抑制VEGFR-2激活抑制视网膜新生血管形成[J]. Biomaterials, 2011, 32: 1865-1871.
- Cui W, et al. 纳米氧化铈在眼病治疗中的应用:最新进展与未来展望[J]. Materials Today Nano, 2022, 18: 100218.
- 张蓉, 闫学海, 范克龙. 受天然酶启发的纳米酶[J]. Accounts of Materials Research, 2021, 2: 534-547.
- 梁敏, 闫学海. 纳米酶:从新概念、机制与标准到应用[J]. Acc Chem Res, 2019, 52: 2190-2200.
- Ghorbani M, et al. 纳米酶抗氧化剂作为天然抗氧化剂的新兴替代品:成就与挑战展望[J]. Nano Today, 2019, 29: 100775.
- 黄渊, 任劲松, 曲晓刚. 纳米酶:分类、催化机制、活性调控及应用[J]. Chem Rev, 2019, 119: 4357-4412.
- Pedone D, Moglianetti M, De Luca E, Bardi G, Pompa P P. 纳米生物医学中的铂纳米颗粒[J]. Chem Soc Rev, 2017, 46: 4951-4975.
- Lord M S, Berret J F, Singh S, Vinu A, Karakoti A S. 氧化还原活性氧化铈纳米颗粒:现状与紧迫问题[J]. Small, 2021, 17: 2102342.
- Rajeshkumar S, Naik P. 氧化铈纳米颗粒的合成及生物医学应用综述[J]. Biotechnology Reports, 2018, 17: 1-5.
- Chen J, Patil S, Seal S, McGinnis J F. 稀土纳米颗粒可防止细胞内过氧化物诱导的视网膜变性[J]. Nat Nanotechnol, 2006, 1: 142-150.
- Fiorani L, et al. 氧化铈纳米颗粒可减轻光损伤视网膜中的小胶质细胞激活与神经退行性事件[J]. PLoS One, 2015, 10: e0140387.
- Tisi A, et al. 氧化铈纳米颗粒在高强度光照诱导急性损伤后对视网膜的长期神经保护作用[J]. Exp Eye Res, 2019, 182: 30-38.
- Kong L, et al. 纳米氧化铈通过调控凋亡/生存信号通路延长Tubby小鼠光感受器细胞寿命[J]. Neurobiology of Disease, 2011, 42: 514-523.
- Cai X, Sezate S A, Seal S, McGinnis J F. 通过玻璃体内注射纳米氧化铈持续保护Tubby小鼠免受光感受器变性[J]. Biomaterials, 2012, 33: 8771-8781.
- Kyosseva S V, Chen L, Seal S, McGinnis J F. 纳米氧化铈抑制Vldlr基因敲除小鼠视网膜中炎症与血管生成相关基因的表达[J]. Exp Eye Res, 2013, 116: 63-74.
- Wong L L, Pye Q N, Chen L, Seal S, McGinnis J F. 在光感受器变性模型P23H-1大鼠中界定纳米氧化铈的催化活性[J]. PLoS One, 2015, 10: e0121977.
- Mitra R N, et al. 氧化钇纳米颗粒在光损伤视网膜变性模型中防止光感受器死亡[J]. Free Radical Biol Med, 2014, 75: 140-148.
- Moglianetti M, et al. 铂纳米酶在氧化应激介导的疾病模型中恢复细胞ROS稳态[J]. Nanoscale, 2016, 8: 3739-3752.
- Gatto F, Moglianetti M, Pompa P P, Bardi G. 铂纳米颗粒降低活性氧物种并调控基因表达而不改变THP-1单核细胞的免疫反应[J]. Nanomaterials, 2018, 8: 392.
- Tarricone G, et al. 铂纳米酶的催化生物转换:神经血管单元中活性氧清除的机制见解[J]. Nano Lett, 2023, 23: 4660-4668.
- Liu Y-Q, et al. 纳米酶清除ROS以预防帕金森病中病理性α-突触核蛋白传播[J]. Nano Today, 2021, 36: 101027.
- Zhang Y, Liu W, Wang X, Liu Y, Wei H. 纳米酶赋能的心脑血管疾病治疗[J]. Small, 2023, 19: 2204809.
- Grimm C, Remé C E. 光损伤作为视网膜变性的模型[J]. Retinal Degeneration: Methods and Protocols, 2012, 935: 87-97.
- Riccitelli S, Di Paolo M, Ashley J, Bisti S, Di Marco S. 光暴露触发视网膜功能形态和分子变化的时间过程[J]. Cells, 2021, 10: 1561.
- Wong L L, et al. 催化纳米氧化铈在大鼠视网膜中优先保留,且玻璃体内注射后无细胞毒性[J]. PLoS One, 2013, 8: e58431.
- Cai X, McGinnis J F. 纳米氧化铈:干性年龄相关性黄斑变性的潜在治疗剂[J]. Retinal Degenerative Diseases: Mechanisms and Experimental Therapy, 2016, 854: 111-118.
- Cai X, Seal S, McGinnis J F. 纳米氧化铈在小鼠眼中的无毒性滞留[J]. Molecular Vision, 2016, 22: 1176.
- Badia A, et al. 重复局部施用3 nm氧化铈纳米颗粒可逆转AMD小鼠模型的疾病萎缩表型并抑制新生血管性变性[J]. ACS Nano, 2023, 17: 910-926.
- Shin C S, et al. 无创递送自再生氧化铈纳米粒子以调节视网膜氧化应激[J]. ACS Applied Bio Materials, 2022, 5: 5816-5825.
- Mittal M, Siddiqui M R, Tran K, Reddy S P, Malik A B. 炎症和组织损伤中的活性氧[J]. Antioxidants & Redox Signaling, 2014, 20: 1126-1167.
- Patergnani S, Bouhamida E, Leo S, Pinton P, Rimessi A. 线粒体氧化应激与“线粒体炎症”:疾病中的参与者[J]. Biomedicines, 2021, 9: 216.
- Valter K, et al. 视神经切断后神经营养因子上调及光诱导损伤视网膜保护作用的时间进程[J]. Investigative Ophthalmology & Visual Science, 2005, 46: 1748-1754.
- Yu T Y, Acosta M L, Ready S, Cheong Y L, Kalloniatis M. 光暴露引起视网膜功能改变:光感受器阳离子通道通透性增加、光感受器凋亡及视网膜代谢功能改变[J]. Journal of Neurochemistry, 2007, 103: 714-724.
- Tavakoli S, et al. 玻璃体内脂质体视网膜递送的眼部屏障:玻璃体视网膜界面的影响[J]. J Controlled Release, 2020, 328: 952-961.
- Asi H, Perlman I. 视网膜电图a波、b波与振荡电位之间的关系及其在临床诊断中的应用[J]. Documenta Ophthalmologica, 1992, 79: 125-139.
- Johnson M A, Jeffrey B G, Messias A M, Robson A G. ISCEV暗适应全视野ERG b波刺激-反应序列扩展方案[J]. Documenta Ophthalmologica, 2019, 138: 217-227.
- Yang J-W, et al. 航天飞行相关神经眼综合征:潜在发病机制与干预措施综述[J]. International Journal of Ophthalmology, 2022, 15: 336.
- Stone J, et al. 哺乳动物视网膜光感受器死亡与存活的机制[J]. Progress in Retinal And Eye Research, 1999, 18: 689-735.
- Samardzija M, et al. 光应激通过视紫红质介导的机制影响视锥细胞与水平细胞[J]. Exp Eye Res, 2019, 186: 107719.
- Fokam D, Hoskin D. 活性氧在炎症反应中的工具性作用[J]. Frontiers in Bioscience-Landmark, 2020, 25: 1110-1119.
- Festa B P, et al. 小胶质细胞至神经元的CCR5信号通路调节神经变性中的自噬[J]. Neuron, 2023, 111: 2021-2037.
- Festa B P, Siddiqi F H, Jimenez-Sanchez M, Rubinsztein D C. 小胶质细胞因子通过CCR5毒害神经元自噬:一个可药物化靶点[J]. Autophagy, 2023, 23: 1-3.
- Voiry D, et al. 纳米材料电催化性能报告的最佳实践[J]. ACS Nano, 2018, 12: 9635-9638.
- Grzybowski A, et al. 玻璃体内注射更新:Euretina专家共识建议[J]. Ophthalmologica, 2018, 239: 181-193.
- Ramos M S, et al. 患者报告的玻璃体内注射后并发症及其预测因素[J]. Ophthalmology Retina, 2021, 5: 625-632.
- Monés J, et al. 模拟萎缩性AMD的外视网膜层选择性地图样萎缩猪模型:I期剂量递增研究视网膜下碘酸钠[J]. Investigative Ophthalmology & Visual Science, 2016, 57: 3974-3983.
- Hughes A. 大鼠示意图眼[J]. Vision Research, 1979, 19: 569-588.