¶ 水解阿拉伯木聚糖米糠对谷氨酸能爆发活动的调节作用:一项基于人诱导多能干细胞来源神经元与胶质细胞的多电极阵列研究
巴桑特·K·普里, 塞西莉亚·卡图尼奥-卡尔, 伊万·韦尔杜奇1、2、3、4
- 分子生物学,剑桥高级研究中心,剑桥,英国
- 心理学,帕福斯尼亚波利斯大学,帕福斯,塞浦路斯
- 电生理学,剑桥高级研究中心,剑桥,英国
- 电生理学,3Brain AG,热那亚,意大利
通讯作者:Basant K. Puri, bpuri@cantab.net
¶ 类别:营养学
¶ 关键词:星形胶质细胞、生物麸、谷氨酸、谷氨酸能神经元、诱导多能干细胞
¶ 摘要
天然产物MGN-3(Biobran)是一种脱脂、部分水解的米糠源半纤维素,经Lentinusedodes提取物酶法改性而成。其含有高比例的阿拉伯木聚糖。该物质对脑室内注射链脲佐菌素诱导的小鼠散发性阿尔茨海默病具有保护作用,并能逆转该疾病模型中的空间记忆缺陷。本研究旨在通过基于多电极阵列的体外微电生理实验,在培养的人谷氨酸能神经元与胶质细胞混合体系中验证以下假设:MGN-3可增强人神经细胞中谷氨酸能突发的活性。
神经元、GABA能神经元和星形胶质细胞。MGN-3在0.750gL-1和两种浓度下的作用,研究了在由人诱导多能干细胞(hiPSC)分化的GABA能神经元、谷氨酸能神经元和星形胶质细胞组成的三元培养体系中, 0.375gL-1及载体对照对谷氨酸能爆发活动的影响。采用正态(高斯)广义线性模型分析了以载体对照标准化的谷氨酸能爆发次数变化。该统计模型具有高度显著性( )。两种MGN-3浓度均与非常显著的主要效应相关。这些结果为拒绝“MGN-3不影响人类神经元和星形胶质细胞中谷氨酸能爆发活动”的零假设提供了有力证据。该研究的优势包括创新性使用hiPSC衍生神经元和星形胶质细胞,以及研究结果具有强统计显著性。局限性包括体外条件可能无法完全模拟体内环境、hiPSC衍生细胞制备可能存在变异性,以及需要测试其他神经元亚型或更多剂量以评估剂量依赖性效应。这些需要在未来的研究中加以解决。
¶ 引言
天然产物MGN-3,亦称Biobran、Lentin Plus、BRM4和Ribraxx,是一种脱脂、部分水解的米糠来源半纤维素,经Lentinus edodes提取物酶法修饰而成,含有高比例阿拉伯木聚糖[1,2]。在小鼠模型中,Ghoneum与El Sayed[3]近期证实MGN-3对脑室内注射链脲佐菌素诱导的散发性阿尔茨海默病具有保护作用;该疾病模型中MGN-3逆转了空间记忆缺陷。空间记忆缺陷是阿尔茨海默病的早期预测指标;事实上,空间导航障碍可能是临床前阿尔茨海默病的生物标志物[4,5]。
阿尔茨海默病中兴奋性与抑制性神经传递之间的电生理平衡发生改变,其中神经元与胶质细胞间的交互作用变化尤为关键[6]。突触前环节涉及谷氨酸能与GABA能神经元,并与星形胶质细胞相关联;而突触后环节同样涉及谷氨酸能与GABA能神经元,此次则与小胶质细胞相互作用[6]。多项证据表明谷氨酸在这一脑内稳态网络中具有重要作用。首先,大鼠实验中应用二氢红藻氨酸抑制中枢星形胶质细胞的谷氨酸摄取会损害空间记忆[7]。其次,哺乳动物的空间记忆提取受后嗅皮层谷氨酸能神经元调控[4]。此外,空间记忆提取需要后嗅皮层-腹外侧眶额皮层通路传递空间信息,该通路属于谷氨酸能通路[4]。空间记忆调节涉及乳头体上核与其支配的齿状回之间的同步活动,这种同步依赖于乳头体上核的谷氨酸释放[8]。在主动回避学习过程中,齿状回会出现增强的谷氨酸响应[9]。抑制海马齿状回的谷氨酸响应会导致空间学习记忆受损,而解除这种抑制则可恢复空间学习能力[10]。最后,尽管人类甲基苯丙胺成瘾与记忆缺陷相关[11],在甲基苯丙胺戒断破坏空间记忆的小鼠模型中,研究表明恢复海马背侧CA1区星形胶质细胞的谷氨酰胺清除功能能够挽救空间记忆[12]。总之,这些研究支持记忆功能与谷氨酸能网络之间存在紧密联系。
谷氨酸能N-甲基-D-天冬氨酸受体依赖性长时程增强作用与学习记忆的介导密切相关[13,14]。事实上,Collingridge及其同事40多年前发表的开创性研究表明,对大鼠海马CA1区神经元进行N-甲基-DL-天冬氨酸离子电泳给药可引发谷氨酸能爆发活动[15]。现已证实,介导LTP的CA1突触长时程可塑性可通过θ节律爆发模式的谷氨酸能活动,同时刺激突触后NMDAR与α-氨基-3-羟基-5-甲基-4-异恶唑丙酸受体而实现;此类谷氨酸能爆发活动与NMDAR钙离子内流相关[14,16]。θ节律爆发活动与记忆功能的关联不仅限于海马体,在海马-间脑-皮层网络的其他区域也同样存在[17]。
基于上述研究,我们假设MGN-3可增强人类神经元与胶质细胞中的谷氨酸能簇发活动。本研究旨在通过体外多电极阵列微电生理实验验证这一假设,实验采用与阿尔茨海默病相关的脑稳态网络[6]中的人类神经元与胶质细胞混合培养体系,具体包括谷氨酸能神经元、γ-氨基丁酸能神经元及星形胶质细胞。本体系未纳入小胶质细胞基于两点考量:实践层面在于其簇发活动难以被检测;理论层面在于,尽管小胶质细胞参与阿尔茨海默病稳态模型的突触后环节,但在支撑记忆学习功能的海马-间脑-皮质网络中并不发挥主要作用。
¶ 材料与方法
¶ 实验设计
MGN-3在两种浓度及零浓度条件下进行了测试。零浓度组由不含任何MGN-3的"载体溶液"构成,该溶液用于稀释非零浓度的MGN-3制剂。因此,单独的载体溶液作为对照组。本研究在英国剑桥的剑桥高级研究中心进行,探讨了两种浓度的MGN-3及载体溶液(对照组)对人工诱导多能干细胞来源的GABA能神经元、谷氨酸能神经元与星形胶质细胞三重培养体系中谷氨酸能爆发活动的影响。
¶ MEA平板制备
所有实验均使用六孔MEA板(CorePlate™;3Brain AG,瑞士普费菲孔)。在铺板前一天,向每个孔中加入无菌过滤的 聚乙烯亚胺(美国沃尔瑟姆Thermo Fisher Scientific Inc.)与1 硼酸盐缓冲液(Thermo Scientific)的混合溶液,静置一小时后,用无菌磷酸盐缓冲盐水冲洗两次,再用无菌水冲洗两次,最后在无菌微生物安全柜中干燥过夜。
¶ 细胞培养与维持
细胞在BrainPhys™神经元培养基(STEMCELL Technologies Inc., 加拿大温哥华)中培养,该培养基添加了100微克/毫升层粘连蛋白(天然,鼠源;Gibco, Thermo Fisher Scientific Inc.)、70微克/毫升庆大霉素(Gibco)、 iCell神经补充剂B(FUJIFILM Cellular Dynamics, Inc. (FCDI), 美国麦迪逊)、 iCell神经系统补充剂(FUJIFILM Cellular Dynamics)以及1 N-2补充剂(Gibco)。
冷冻保存的人源诱导多能干细胞分化GABA能神经元(iCell GABANeurons;富士胶片细胞动力学公司)、谷氨酸能神经元(iCell GlutaNeurons;富士胶片细胞动力学公司)及星形胶质细胞(iCell Astrocytes 2.0;富士胶片细胞动力学公司)于 C水浴中解冻150秒,在轻轻旋动50毫升离心管的同时逐滴加入1毫升培养基以防止渗透压冲击。随后补充添加2毫升(星形胶质细胞、谷氨酸能神经元)或6毫升(GABA能神经元)培养基。取20微升细胞悬液进行细胞计数。细胞悬液以400g离心5分钟,弃去上清液后用培养基重悬细胞至总体积1毫升。由两名研究人员分别使用血细胞计数板进行人工细胞计数。
神经元和星形胶质细胞预先混合成三重培养物,并以70微升液滴的形式直接接种到平板微芯片上,每个液滴包含78,000个谷氨酸能神经元( )、42,000个GABA能神经元( )和20,000个星形胶质细胞( )。将平板置于 、 CO2的湿润培养箱中一小时,随后加入300微升培养基。90分钟后再加入1毫升培养基。细胞维持期间每两到三天更换一半培养基。
¶ 微电极阵列记录
所有记录均使用HyperCam MEA系统(3Brain)采集,该系统维持恒定的 温度和5% CO2环境。实验采用六孔板配置,每孔配备2304个电极(电极间距60微米,电极尺寸25微米 微米,总记录区域2.9毫米 毫米)(见图1)。

图1:采用3Brain CorePlate™六孔培养板记录细胞培养物的电活动,每个孔内有2304个电极同时进行记录。
MEA板在每次记录前需在HyperCam上平衡10分钟。体外培养第22天(DIV 22),先记录五分钟基线自发活动,随后添加10微摩尔苦味宁(Thermo Scientific)诱导晕厥样癫痫发作。五至七分钟后,手动向每个孔添加测试化合物,并立即进行15分钟记录。
信号以10 kHz频率采样,经100 Hz高通滤波处理,并采用噪声消除压缩采集(高低阈值分别为3.5个标准差/4个标准差)。
¶ 化合物制备和处理
MGN-3(大和制药,东京)溶于乙醇,配制成浓度为0.375克/毫升的储备液。将MGN-3按1:500和1:1000比例稀释,分别对应0.750克/升和0.375克/升的浓度,直接加入培养基中。每个MEA板预留两个孔作为溶剂对照组(乙醇体积分数分别为 和 )。在HyperCam内保持培养板不动,通过移液器直接向孔中加入印防己毒素、MGN-3及溶剂对照液。为确保各孔条件一致,每孔总体积添加量为20微升,加入化合物或溶剂后由培养基补足剩余体积。
¶ 峰值与网络分析
所有检测分析均使用BrainWave 5.0(3Brain)进行。通过- 的硬阈值结合人工智能验证检测棘波。活跃单元少于30个(<0.05次/分钟)的孔板被排除在分析之外;24个孔板中共有4个被剔除。当同一电极检测到至少三个棘波且棘波间隔小于或等于100毫秒时,记录为爆发活动。算法参数根据每次记录进行定制。所有棘波与爆发结果均由两名研究人员手动核对,确保与视觉评估结果一致。
原始数据从软件中提取并经过手动处理。通过比较五分钟基线记录与给药后即刻最后五分钟记录及给药后一天的五分钟记录,分析了MGN-3的效果。
¶ 统计分析
进行的统计检验如下。首先,采用高斯广义线性建模。在此建模中,响应变量为谷氨酸能爆发次数相对于载体对照的归一化变化。由于神经元形成了同步网络,任一电极上的活动与其他活跃电极的活动密切相关,因此数据分组良好。因此,归一化的谷氨酸能爆发变量采用正态或高斯广义线性模型进行分析,
以化合物(载体和两种浓度的MGN-3)、时间(基线及两个随访时间)作为因素,并采用恒等典范连接函数进行建模。其次,计算了三个组中每组爆发次数的算术平均值,并附有相应的标准误和95%置信区间。这些统计分析及图形绘制均使用R v. 4.2.1(奥地利维也纳统计计算R基金会)和JASP 0.17.2.1(荷兰阿姆斯特丹JASP团队)[18,19]完成。
¶ 结果
特征性爆发模式,以及归因于单个谷氨酸能爆发的尖峰,如图2所示。
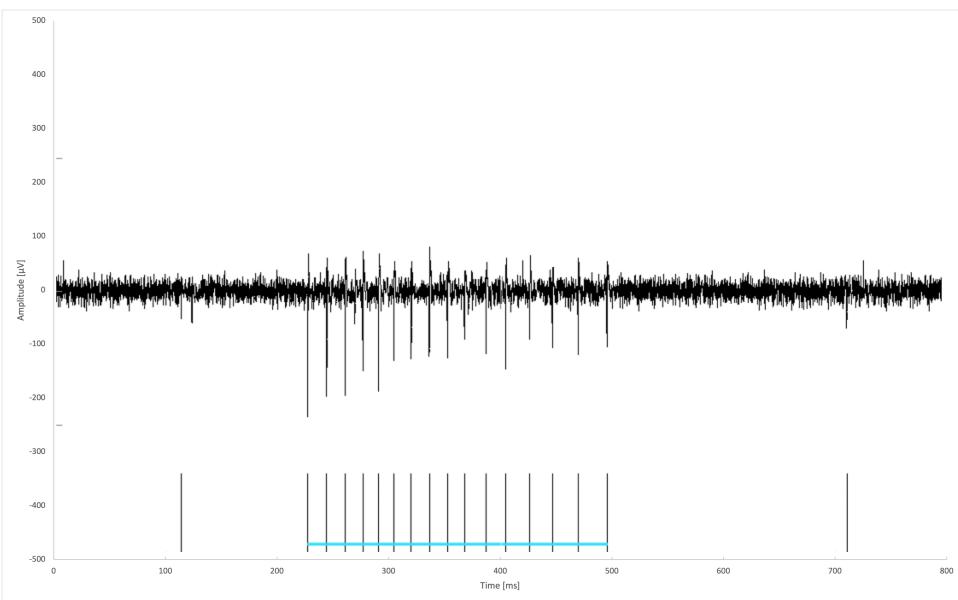
图2:电极记录示例轨迹,显示特征性爆发模式。蓝色水平线将归属于单次爆发的动作电位簇分组显示。
在所有孔中都记录到了自发电活动。在后续分析中,活性单元少于30个(尖峰频率低于 次/秒)的孔被排除。基线记录期间,所有孔均记录到自发尖峰活动、簇状放电及网络簇状放电活动。基线活动的特征表现为:每个孔的平均(标准误)放电频率为140(12.2)次/秒,平均簇状放电频率为9.3(1.3)次/秒,每个孔平均有73(4)个活跃的簇状放电单元。网络簇状放电活动呈间歇性,包含异步活动阶段和规律性网络簇状放电阶段(见图3)。
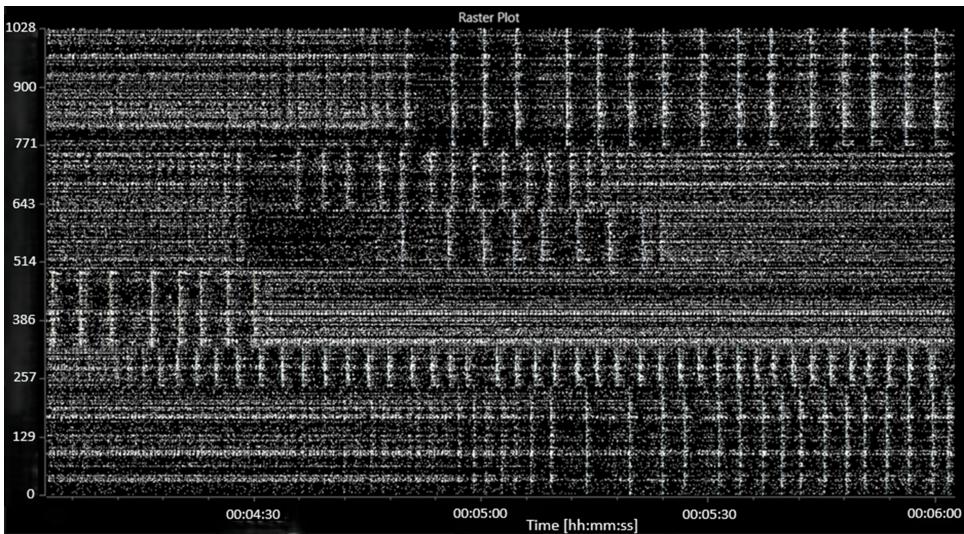
图3:显示特征性基线电活动(在加入印防己毒素或MGN-3之前)的光栅图。
横坐标(x轴)表示时间,格式为时:分:秒。纵坐标(y轴)显示电极编号。
添加苦味毒素后,平均放电频率和平均爆发频率持续下降,分别降至每孔62(8.4)次放电/秒和每孔4.3(1.0)次爆发/秒。活跃爆发单元数量也减少至每孔50(5)个活跃爆发单元。同时观察到网络爆发频率与同步性增强。图4展示了添加苦味毒素后的特征活动点阵图。
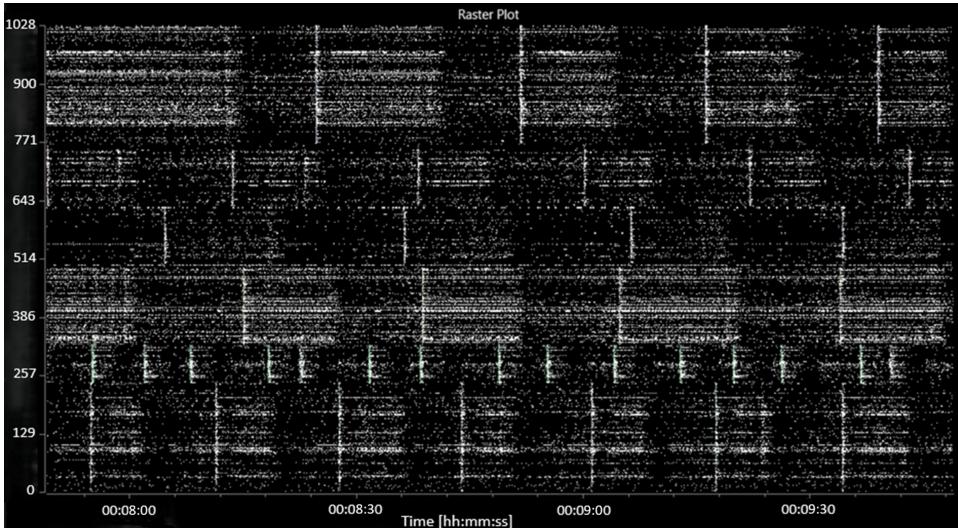
图4:添加印防己毒素后显示特征性活动的光栅图。
横坐标(x轴)表示时间,格式为时:分:秒。纵坐标(y轴)表示电极编号。
加入MGN-3后,平均放电频率进一步降低至每孔57(6)次/秒,活跃爆发单元数量强劲回升至每孔70(4)次/秒。爆发频率略微上升至每孔4.6(0.6)次/秒。网络活动未出现显著变化,其表现基本类似印防己毒素诱导的活动模式。图5展示了添加MGN-3后特征活动的栅格图。
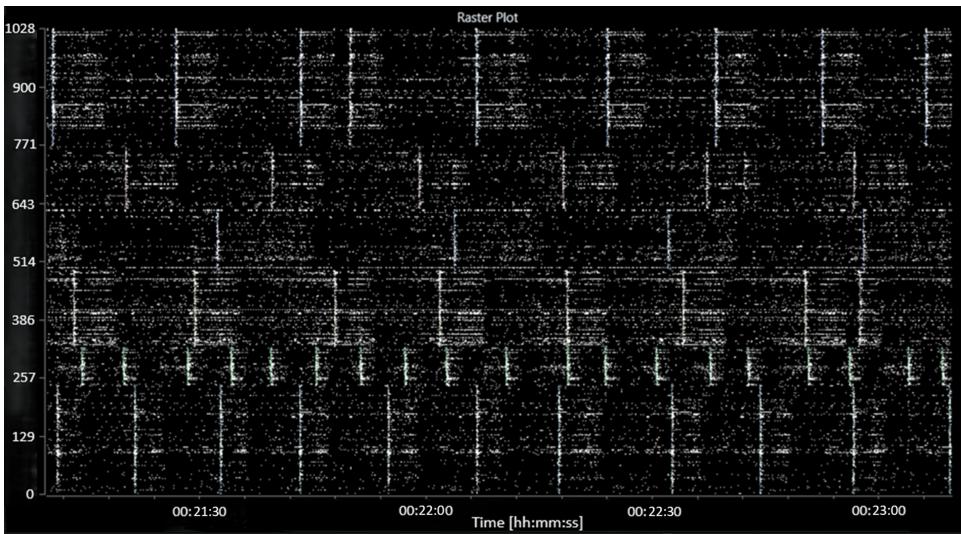
图5:显示添加MGN-3后特征活动的栅格图(在添加印防己毒素之后)。
横坐标(x轴)表示时间,格式为时:分:秒。纵坐标(y轴)表示电极编号。
在1:1000浓度下,MGN-3的平均爆发次数为15.561(0.999;五个孔;1634个电极);在1:500浓度下,MGN-3的平均爆发次数为15.252(0.692;八个孔;2892个电极);而溶媒组的平均爆发次数为13.443(0.662;七个孔;2924个电极)。图6展示了这些组平均值及其对应的 置信区间的分布图。
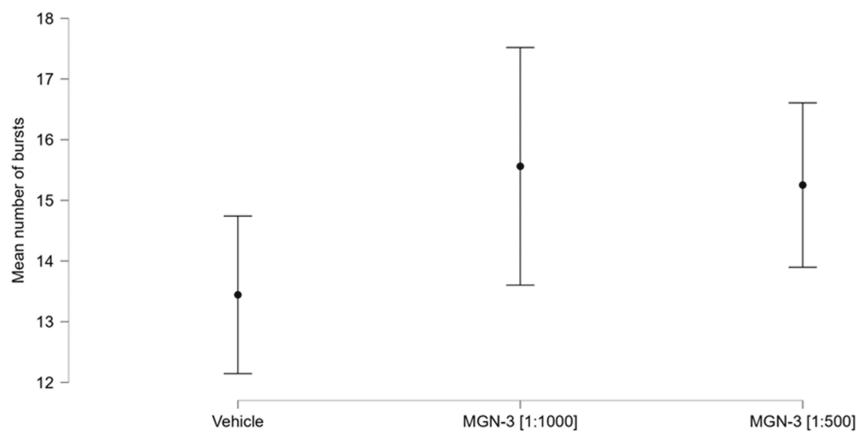
图6:组平均突发值及 置信区间。
统计模型具有高度显著性(卡方 , )。如表1所示,两种浓度的MGN-3均表现出高度显著效应。其中九个培养孔(三个对应较低MGN-3浓度,六个对应较高MGN-3浓度)也呈现显著效应,这些未在表1中展示。所有对照孔均未显示显著效应,模型截距亦不显著。时间因素未达显著水平。使用拟合差异(DFFITS)统计量表明,没有证据表明存在异常影响的观测值。
表 1:高斯广义线性模型系数。
| Estimate | Standard error | t | p | |
| MGN-3 (1 in 1000) | -0.684 | 0.156 | -4.389 | 8.103 × 10-5 |
| MGN-3 (1 in 500) | 1.291 | 0.156 | 8.278 | 3.330 × 10-10 |
¶ 讨论
该化合物两种浓度的高度显著主效应为拒绝零假设提供了有力证据。这些结果支持MGN-3能增强人类神经元和星形胶质细胞中谷氨酸能爆发活动的假设。大多数化合物孔也显示出显著的主效应,而所有载体对照孔均未呈现显著效应——鉴于这些是对照组,该结果符合预期。
关于这些结果的另一种解释可能是MGN-3通过作用于GABA能神经元的氯离子通道诱发了晕厥样癫痫发作。然而,这种可能性极低,原因有二:首先,细胞已预先用苦味毒处理,该物质会阻断GABAA受体氯离子通道的离子流动。
被GABA激活[20]。其次,没有证据表明MGN-3可作为印防己毒素的竞争性拮抗剂;事实上,由活化半纤维素与β1,3-葡聚糖构成的多糖结构并不直接提示此类作用[21]。
有人认为,皮卡毒素预处理意味着实验是在过度兴奋状态下进行的,这与阿尔茨海默病的表型无关。然而,多个研究团队指出,过度兴奋(或兴奋性毒性)状态与阿尔茨海默病存在关联[22-24]。事实上,在一项阿尔茨海默病相关的体外研究中,正是基于此原因采用了皮卡毒素预处理,以探讨牛磺酸能否阻止β-淀粉样蛋白和谷氨酸受体激动剂的神经毒性[24]。尽管如此,如果如本研究结果所示,MGN-3确实会诱发谷氨酸能活性增强,那么这一效应在未经皮卡毒素预刺激的细胞中应当更清晰、甚至更显著地显现;因此,未来有必要开展此类研究。
目前的结果表明MGN-3可能在阿尔茨海默病(包括早期阶段)中具有治疗作用,这一论断尚不成熟。一方面,这些结果与MGN-3在散发性阿尔茨海默病小鼠模型中具有保护作用的研究发现相一致[3]。另一方面,迄今为止尚未有已发表的证据表明这种营养补充剂对人类阿尔茨海默病具有益处。针对存在认知衰退的成年人群开展随机、安慰剂对照的试点研究将是适宜的。
关于本研究的优势,包括创新性地使用hiPSC来源的神经元和星形胶质细胞,以及研究结果具有稳健的统计学显著性。在研究局限性方面,其中一个问题涉及对苦味毒素的预处理。这一点已在上述讨论中说明。此外,体外条件可能无法完全复制体内环境。其他潜在局限性包括hiPSC来源细胞制备物的潜在变异性,以及需要测试其他神经元亚型或追加剂量以评估剂量依赖性效应。这些问题应在未来研究中予以解决。另一问题在于本研究仅在单层神经元和星形胶质细胞体系中进行,这与哺乳动物大脑中存在的三维几何结构存在明显差异。采用微针电极的三维高分辨率功能成像技术近期已实现应用,这种微针电极能够在不对细胞造成损伤的前提下,从三维神经胶质阵列内部获取电活动数据。在未来体外后续研究中采用此类新技术是适宜的。
¶ 结论
本研究支持以下假设:MGN-3能增强人类神经元与星形胶质细胞中的谷氨酸能爆发。需通过进一步研究阐明以下问题:第一,MGN-3增强谷氨酸能活性的潜在机制(例如通过受体调节或代谢途径);第二,当前研究发现如何转化应用于体内模型或临床场景;第三,实验所用特定浓度与治疗剂量的关联性。事实上,开展更详尽的体外剂量反应研究(无需印防己毒素预处理)将有助于确定最佳剂量。
附加信息作者贡献
所有作者均已审阅过即将发表的终稿,并同意对工作的所有方面负责。
概念与设计: 巴桑特·K·普里,伊万·韦尔杜奇数据获取、分析或解读:巴桑特·K·普里、塞西莉亚·卡图尼奥-卡尔、伊万·韦尔杜奇
手稿起草: Basant K. Puri
重要学术内容的手稿关键评审:塞西莉亚·卡图尼奥-卡尔,伊万·韦尔杜奇
¶ 披露
**受试者声明:** 所有作者均确认本研究未涉及人类参与者或组织。**动物受试者声明:** 所有作者均确认本研究未涉及动物受试者或组织。**利益冲突声明:** 为遵守国际医学期刊编辑委员会(ICMJE)的统一披露表格,所有作者声明如下:**付款/服务信息:** 所有作者声明,提交的工作未从任何组织获得财务支持。**财务关系:** I.V. 声明受雇于3Brain 。系该公司雇员。B.P. 声明获得Daiwa的资助。系一项MGN-3(不涉及阿尔茨海默病)人体试验的主要研究者。**其他关系:** 所有作者声明不存在任何其他可能影响所提交工作的关系或活动。
¶ 参考文献
- Ghoneum M. 米糠来源的活化阿拉伯木聚糖 MGN-3 的体外抗 HIV 活性[J]. 生物化学生物物理研究通讯, 1998, 243:25-29. https://doi.org/10.1006/bbrc.1997.8047
- Ooi SL, Pak SC, Micalos PS, Schupfer E, Lockley C, Park MH, Hwang SJ. 香菇酶修饰米糠阿拉伯木聚糖的健康促进特性及临床应用——叙述性综述[J]. 分子, 2021, 26:2539. https://doi.org/10.3390/molecules26092539
- Ghoneum MH, El Sayed NS. Biobran/MGN-3 对散发性阿尔茨海默病小鼠模型的保护作用:氧化应激和凋亡通路的可能作用[J]. 氧化医学与细胞寿命, 2021, 2021:8845064. https://doi.org/10.1155/2021/8845064
- Qi X, Du ZJ, Zhu L, et al. 谷氨酸能后嗅皮层-腹外侧眶额皮层通路调节空间记忆检索[J]. 神经科学通报, 2019, 35:447-460. https://doi.org/10.1007/s12264-018-0325-4
- Coughlan G, Laczó J, Hort J, Minihane AM, Hornberger M. 空间导航缺陷——临床前阿尔茨海默病被忽视的认知标志物?[J]. 自然评论神经病学, 2018, 14:496-506. https://doi.org/10.1038/s41582-018-0031-x
- Czapski GA, Strosznajder JB. 阿尔茨海默病中小胶质细胞-神经元串扰中的谷氨酸和 GABA[J]. 国际分子科学杂志, 2021, 22:11677. https://doi.org/10.3390/ijms222111677
- Bechtholt-Gompf AJ, Walther HV, Adams MA, Carlezon WA Jr, Ongür D, Cohen BM. 阻断大鼠星形胶质细胞谷氨酸摄取诱导快感缺失迹象和空间记忆受损[J]. 神经精神药理学, 2010, 35:2049-2059. https://doi.org/10.1038/npp.2010.74
- Li Y, Bao H, Luo Y, et al. 乳头上核通过释放谷氨酸与齿状回同步调节空间记忆检索[J]. 生命, 2020, 9:e53129. https://doi.org/10.7554/eLife.53129
- Wang S, Pan DX, Wang D, Wan P, Qiu DL, Jin QH. 一氧化氮通过增强海马齿状回谷氨酸水平促进主动回避学习[J]. 行为大脑研究, 2014, 271:177-183. https://doi.org/10.1016/j.bbr.2014.06.011
- Ren P, Xiao B, Wang LP, Li YS, Jin H, Jin QH. 一氧化氮通过干扰空间学习期间海马齿状回谷氨酸反应损害阿尔茨海默病大鼠模型的空间学习记忆[J]. 行为大脑研究, 2022, 422:113750. https://doi.org/10.1016/j.bbr.2022.113750
- Potvin S, Pelletier J, Grot S, Hébert C, Barr AM, Lecomte T. 甲基苯丙胺使用障碍患者的认知缺陷:一项荟萃分析[J]. 成瘾行为, 2018, 80:154-160. https://doi.org/10.1016/j.addbeh.2018.01.021
- Shi P, Li Z, He T, et al. 星形胶质细胞选择性 STAT3 敲低通过恢复 dCA1 区星形胶质细胞谷氨酸清除能力挽救甲基苯丙胺戒断破坏的小鼠空间记忆[J]. 胶质细胞, 2021, 69:2404-2418. https://doi.org/10.1002/glia.24046
- Morris RG. NMDA 受体与记忆编码[J]. 神经药理学, 2013, 74:32-40. https://doi.org/10.1016/j.neuropharm.2013.04.014
- Wu D, Bacaj T, Morishita W, et al. 突触后 synaptotagmin 介导 LTP 期间的 AMPA 受体胞吐[J]. 自然, 2017, 544:316-321. https://doi.org/10.1038/nature21720
- Collingridge GL, Kehl SJ, McLennan H. 体外拮抗氨基酸诱导的大鼠海马 CA1 神经元兴奋[J]. 生理学杂志, 1983, 334:19-31. https://doi.org/10.1113/jphysiol.1983.sp014477
- Larson J, Munkácsy E. θ 爆发 LTP[J]. 大脑研究, 2015, 1621:38-50. https://doi.org/10.1016/j.brainres.2014.10.034
- Barnett SC, Parr-Brownlie LC, Perry BA, et al. 前丘脑核神经元维持记忆[J]. 当前神经生物学研究, 2021, 2:100022. https://doi.org/10.1016/j.crneur.2021.100022
- R Core Team. R:统计计算的语言与环境[M]. 维也纳:R 统计计算基金会, 2022.
- JASP Team. JASP(版本 0.18.1)[CP/OL]. 2023-10-08. https://jasp-stats.org/.
- Olsen RW. GABAA 受体的印防己毒素样通道阻滞剂[J]. 美国国家科学院院刊, 2006, 103:6081-6082. https://doi.org/10.1073/pnas.0601121103
- Masiulis S, Desai R, Uchański T, et al. 结构药理学揭示的 GABA(A) 受体信号机制[J]. 自然, 2019, 565:454-459. https://doi.org/10.1038/s41586-018-0832-5
- Mattson MP. 兴奋毒性与兴奋保护机制:神经退行性疾病防治的丰富靶点[J]. 神经分子医学, 2003, 3:65-94. https://doi.org/10.1385/NMM:3:2:65
- Lipton SA, Rosenberg PA. 兴奋性氨基酸作为神经系统疾病的共同最终通路[J]. 新英格兰医学杂志, 1994, 330:613-622. https://doi.org/10.1056/NEJM199403033300907
- Louzada PR, Paula Lima AC, Mendonca-Silva DL, Noël F, De Mello FG, Ferreira ST. 牛磺酸可预防β-淀粉样蛋白及谷氨酸受体激动剂的神经毒性:GABA受体激活及其对阿尔茨海默病与其他神经系统疾病的潜在意义[J]. 美国实验生物学学会联合会杂志, 2004, 18:511-518. https://doi.org/10.1096/fj.03-0739com