¶ 基于聚二甲基硅氧烷微结构的高密度微电极阵列定制化体外神经元网络构建方案
¶ 原文下载:protocol_for_tailored_in_vitro_neuronal_networks.pdf
Haeb 等,《STAR Protocols》,第 7 卷,104349 页2026 年 3 月 20 日 © 2026 作者。由爱思唯尔公司(Elsevier Inc.)出版DOI:10.1016/j.xpro.2026.104349
¶ 摘要
基于互补金属氧化物半导体(CMOS)的高密度微电极阵列(HD-MEAs)能够以高时空分辨率记录神经元活动。然而,将聚二甲基硅氧烷(PDMS)微结构集成到 HD-MEA 表面以调控网络结构,目前仍面临挑战,且方案具有平台特异性。本文提出一套涵盖 PDMS 制备、HD-MEA 芯片准备、PDMS-HD-MEA 微结构对准及细胞培养的实验方案,并提供替代方法。研究结果表明,在不同系统中均可重复构建具有特征性活性模式的模块化网络。该方案支持构建特定结构的神经元网络,同时保持与多种 HD-MEA 系统的兼容性。
出版方说明:执行任何实验方案均需遵守当地机构的实验室安全与伦理准则。
作者:安娜 - 克里斯蒂娜・黑布(Anna-Christina Haeb)、山本秀明(Hideaki Yamamoto)、保罗・罗奇(Paul Roach)、丹尼尔・梅里韦瑟(Daniel Merryweather)、佐藤雄哉(Yuya Sato)、丹尼尔・托内罗(Daniel Tornero)、霍尔迪・索里亚诺(Jordi Soriano)联系方式:haeb.anna@web.de(A.-C.H.)、daniel.tornero@ub.edu(D.T.)、jordi.soriano@ub.edu(J.S.)
¶ 研究亮点
- 适用于不同 HD-MEA 芯片制造商的 PDMS 基模块化网络构建方案
- PDMS 制备、涂层及与 HD-MEA 表面贴合的详细步骤
- 延长 HD-MEA 芯片使用寿命、提升复用率的操作与清洗方案
- 方案优化细节、局限性及潜在解决方案说明
¶ 基于聚二甲基硅氧烷微结构的高密度微电极阵列定制化体外神经元网络构建方案
安娜 - 克里斯蒂娜・黑布 ¹,²,³,⁴,⁹,、山本秀明⁵,⁹、保罗・罗奇⁶,⁹、丹尼尔・梅里韦瑟⁶、佐藤雄哉⁵,⁷、丹尼尔・托内罗 ¹,⁸,、霍尔迪・索里亚诺 ²,³,¹⁰,*¹ 西班牙巴塞罗那大学医学院与健康科学学院生物医学系、神经科学研究所,巴塞罗那 08036² 西班牙巴塞罗那大学理学院凝聚态物理系,巴塞罗那 08028³ 西班牙巴塞罗那大学复杂系统研究所(UBICS),巴塞罗那 08028⁴ 西班牙奥古斯特・皮・苏涅尔生物医学研究所(IDIBAPS),巴塞罗那 08036⁵ 日本东北大学电气通信研究所,仙台 980-8577⁶ 英国拉夫堡大学理学院化学系,莱斯特郡 LE11 3TU⁷ 日本早稻田大学纳米与生命创新研究机构,东京 162-0041⁸ 西班牙马德里神经退行性疾病生物医学研究网络中心(CIBERNED),马德里 28029⁹ 技术联系人¹⁰ 主要联系人
- 通信作者:haeb.anna@web.de(A.-C.H.)、daniel.tornero@ub.edu(D.T.)、jordi.soriano@ub.edu(J.S.)DOI:10.1016/j.xpro.2026.104349
¶ 摘要
基于互补金属氧化物半导体(CMOS)的高密度微电极阵列(HD-MEAs)能够以高时空分辨率记录神经元活动。然而,将聚二甲基硅氧烷(PDMS)微结构集成到 HD-MEA 表面以调控网络结构,目前仍面临挑战,且方案具有平台特异性。本文提出一套涵盖 PDMS 制备、HD-MEA 芯片准备、PDMS-HD-MEA 微结构对准及细胞培养的实验方案,并提供替代方法。研究结果表明,在不同系统中均可重复构建具有特征性活性模式的模块化网络。该方案支持构建特定结构的神经元网络,同时保持与多种 HD-MEA 系统的兼容性。
有关本方案使用与执行的完整细节,请参考 Sato 等人的研究 ¹。
¶ 实验前准备
体外神经元网络为研究可控、可操作环境中的神经元动态提供了多功能模型,可应用于药物筛选、疾病建模及信息处理 ²。HD-MEA 系统是极具优势的平台,能够以高时空分辨率监测整个神经元网络的活动 ³。
体外网络通常在平面表面生长,神经元随机连接并形成高度互联的结构⁴,这与大脑中高度有序且复杂的结构形成鲜明对比⁵,⁶。为模拟这种类脑结构,可利用 PDMS 等生物工程微结构构建具有定制化连接性的模块化神经元网络⁷。这类被称为 “芯片上的大脑”(brain-on-a-chip)的微结构,可与 MEA 系统集成,形成先进的神经元研究平台⁸。然而,现有方案大多聚焦于低密度 MEA 适配的 PDMS,而非高密度 MEA¹,¹³。此外,不同 HD-MEA 系统的芯片设计、材料及布局存在差异,导致通用方案的开发难度增加 ¹⁴。目前商用的 HD-MEA 系统包括 3Brain 公司 ¹⁵、Maxwell Biosystems 公司 ¹⁶,¹⁷及 MultiChannel Systems 公司的产品 ¹⁸。
在 HD-MEA 技术出现之前,微加工 PDMS 器件已被有效用于调控 MEA 上培养神经元网络的黏附位点与轴突生长 ¹⁹⁻²¹。HD-MEA 的核心优势在于其高空间分辨率(通常在 20 μm 量级),与 PDMS 器件的特征尺寸相当 ²²。然而,HD-MEA 表面因底层 CMOS 微电路的存在,通常具有微米级三维拓扑结构,这使得通过简单放置实现 PDMS 的均匀贴合变得困难。尝试使用水凝胶 ¹ 或稀释 PDMS¹³ 等缓冲层可能会影响芯片的复用性,导致领域内缺乏可靠的 PDMS-HD-MEA 贴合方案。
¶ 创新点
鉴于 HD-MEA 芯片具有敏感性高、成本高且需复用的特点,优化其操作方法至关重要。因此,本研究旨在提供一套具有适应性与可重复性的方案,并包含替代方法与通用指南,以实现:(1)设计并制备适配特定 HD-MEA 芯片的 PDMS 微结构(“微加工器件”);(2)将这些微结构集成到 HD-MEA 表面;(3)建立延长芯片寿命、提升复用率的清洗流程。
为确保方案对不同拓扑结构的 HD-MEA 平台具有广泛适用性,本研究在嵌入式电极凹陷的 HD-MEA 芯片(3Brain 公司产品)上验证了该方案,同时还展示了在凸起电极的不同系统(Maxwell Biosystems 公司产品)上的代表性结果(详见 Sato 等人的研究 ¹)。
¶ 机构许可
涉及大鼠胚胎组织解剖的原代神经元培养,均遵循巴塞罗那大学动物实验伦理委员会的规定(2015 年 7 月 10 日批准的伦理许可编号 B-RP-094/15–7125)及西班牙加泰罗尼亚自治区的动物实验法律。东北大学所有涉及动物实验的流程均经过该校实验动物研究中心的审核与批准。
¶ 微加工器件设计
⏱️ 耗时:取决于设计复杂度,通常约 1–2 周。
可通过多种光刻方法制备 PDMS 微加工器件(常被称为微流控器件,尽管本研究不涉及流体流动)。本方案概述了 PDMS 微加工的通用方法:首先制备 “母版”(master)反向模板,作为浇筑 PDMS 以形成带腔室微加工器件的模具 ²³。此过程需使用光刻机或直写激光系统:光刻机利用预制光掩模(通常为高分辨率铬玻璃图案)将紫外光投射到光敏树脂上,实现图案转移;而激光直写系统无需物理掩模,可直接绘制图案。两种方法均需基于计算机辅助设计(CAD)生成图案(用于制作掩模或引导激光)。直写方式可快速重新设计,无需为每次设计变更制作新掩模,但实际打印时间显著延长;掩模光刻法则能快速制备大量母版模具图案,但重新设计模具需制作新光掩模。
器件设计必须考虑 HD-MEA 的布局,包括电极区尺寸、细胞腔室与微通道内的电极位置,以及芯片整体结构(不同类型芯片的电极分布差异显著)。例如,部分芯片为高密度电极区(如 3Brain 公司的 CMOS HD-MEA,图 1),电极排列紧密;而其他芯片的电极在表面分布更分散,有时甚至分组集中在特定区域(如 Med64 芯片)。电极形态也存在差异:部分电极表面相对平坦,部分为 “准平坦”(表面整体平坦,但电极尖端因绝缘层存在约 1 μm 的凹陷),还有部分为类三维电极(尖端向 z 轴方向延伸,可实现深度传感,如对类器官的检测)。电极涂层也需纳入考量:铂或碳纳米管涂层电极化学稳定性较强,但易受污染,且与 PDMS 器件直接物理接触时可能损坏,这对 HD-MEA 复用尤为重要。通过精心设计,可使 PDMS 器件的腔室与目标区域对准,避免不必要的电极覆盖。
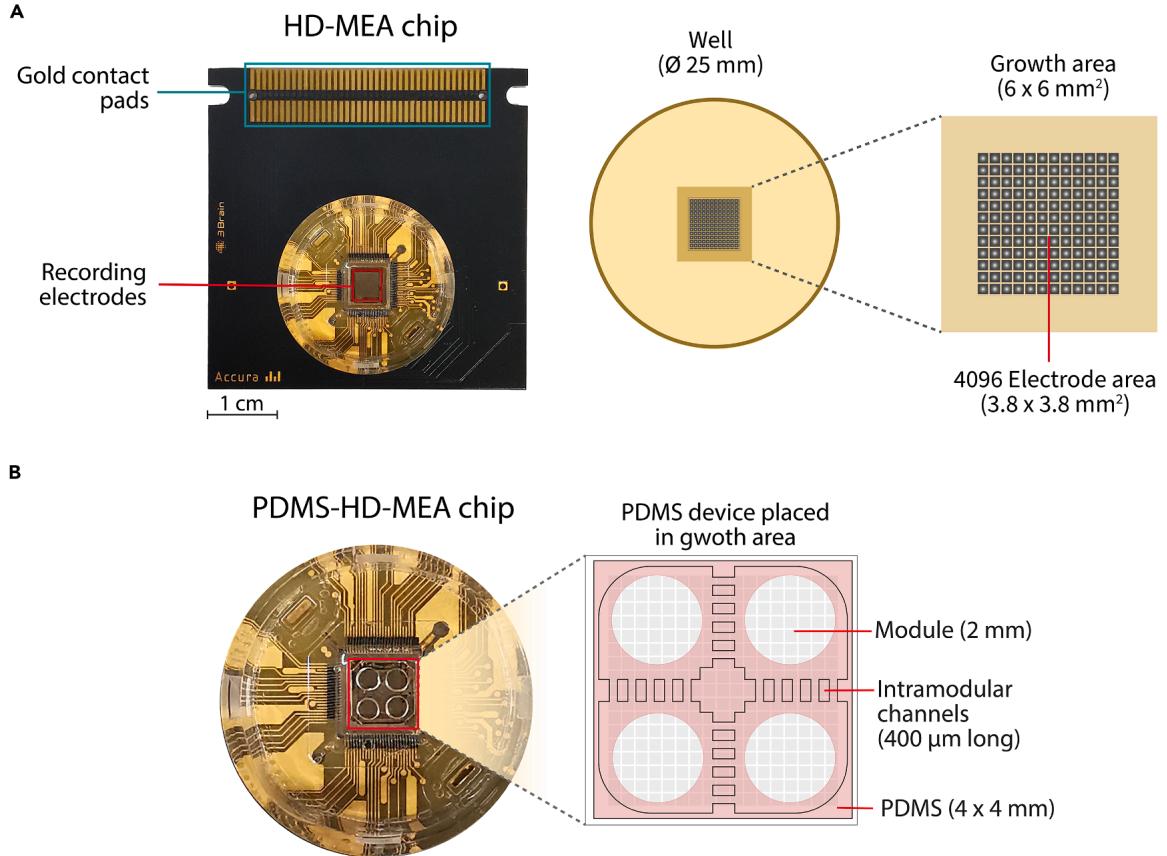
图 1:3Brain 公司代表性 HD-MEA 芯片及 PDMS 器件
(A)标准芯片结构,包含 CMOS 传感器所在的培养孔区域及连接记录系统的接触垫。培养孔细节图显示 64×64 电极阵列,用于记录表面生长细胞的膜场电位。(B)电极区上方放置 PDMS 浇筑件的芯片(已准备好进行细胞培养)。PDMS 结构包含 4 个打孔腔室(模块),用于神经元接种;模块对通过 5 条平行微通道(400 μm 长)正交连接。
⚠️ 关键注意事项:PDMS 器件的设计应确保其与电极区表面良好接触以实现黏附,同时尽可能避免与电极尖端直接接触。这有助于实现稳定贴合,并支持 HD-MEA 的复用。
¶ 计算机辅助设计(CAD)
⏱️ 耗时:取决于设计复杂度,通常约 1–3 天。
选择符合设计需求的软件注:现有多种 CAD 软件可供选择,包括商业许可软件与免费软件,如 AutoCAD、Fusion 360(提供免费教育许可)、FreeCAD、TinkerCAD、SketchUp 及 KLayout 等。注:需明确设计目标 —— 尽管 CAD 通常需生成二维图纸,但许多软件支持三维建模,有助于设计的可视化与说明。
以二维设计形式创建 CAD 布局(通常为单层)注:可获取免费资源指导设计流程。注:确保输出文件格式与后续应用兼容。常用灵活格式包括 .dwg 或 .dxf,但部分光刻系统需 .gds 格式。必要时可使用 KLayout 等软件导入 .dxf 文件并导出为 .gds 格式。
⚠️ 关键注意事项:需在设计初期评估整个生产流程,确保输出文件与设计符合制备工艺及仪器的要求。⚠️ 关键注意事项:需正确设置设计文件中的单位。
CAD 文件制备完成后,即可开始制备母版反向器件。
¶ 母版反向器件制备
⏱️ 耗时:取决于设计与光刻系统,通常约 3–5 天。
可在多种基底上制备设计图案,硅片因具有分子级平整度而被广泛使用。为将 CAD 设计转化为三维模具,需在基底上涂覆光聚合物(光刻胶)。本方案以 SU-8(一种环氧基负性光刻胶)为例,其在 365 nm 紫外光照射后经热固化可实现聚合。SU-8 的型号选择取决于所需图案高度 ²⁴:PDMS 器件通常含微通道(用于连接不同腔室中的神经元),若需细胞跨腔室迁移,微通道高度选择约 100 μm;若需限制细胞胞体但允许轴突通过微通道延伸,微通道高度选择约 10 μm。
¶ 基底准备
a. 用丙酮、异丙醇(IPA)及去离子水(DI 水)清洗合适的基底(硅片);b. 用干燥空气或氮气气流彻底吹干硅片;c. 进行氧等离子体处理(0.2–0.5 mbar,30–50 W,30 秒),确保基底清洁并提升光刻胶的黏附性;d. 加热基底以确保旋涂光刻胶前完全干燥 —— 通常在旋涂前,将基底置于热板上以 ≥100℃ 烘烤 5–10 分钟。
¶ 光刻胶涂覆
a. 若上一步进行了加热,需将基底冷却至 22–25℃ 后再继续操作;b. 滴加足量 SU-8 以完全覆盖基底,根据所需特征高度选择 SU-8 型号:需 10 μm 高度时选用 SU-8 3050,需 100 μm 高度时选用 SU-8 2100;注:PDMS 器件的微通道高度需根据生物学功能选择:约 100 μm 用于支持细胞迁移的腔室,约 10 μm 用于限制胞体但允许轴突延伸的场景。仅微通道高度对功能有关键影响,腔室整体高度仅需容纳细胞与培养基即可。注:选择不同型号的光刻胶是为了在目标厚度范围内获得均匀涂层,同时避免过度边缘 bead 效应或膜不稳定性。替代方案:SU-8 50(高黏度)可形成 ≥25 μm 的均匀厚膜 ²⁵,SU-8 10 则适用于制备更薄、更可控的薄膜。c. 以适当转速旋涂:i. SU-8 3050 光刻胶:先以 500 rpm(加速度 100 rpm/s)旋涂 10 秒,再以 3300 rpm(加速度 300 rpm/s)旋涂 30 秒;ii. SU-8 2100 光刻胶:先以 500 rpm(加速度 100 rpm/s)旋涂 10 秒,再以 3100 rpm(加速度 300 rpm/s)旋涂 30 秒。
⚠️ 关键注意事项:光刻胶厚度受实验室温度、相对湿度(RH)及光刻胶储存时间 / 条件影响显著。因此,必须通过校准(如显微镜观察或轮廓测量)验证局部膜厚,结果可能因设备与烘箱均匀性而异,需遵循制造商指导。注:可通过维持 22–25℃、<50% RH 的环境,并根据局部校准结果调整旋涂转速,以补偿环境与设备差异。需按制造商建议在各实验室进行校准,并记录范围估算值。温度与湿度会导致光刻胶黏度变化,进而影响不同旋涂转速下的膜厚。
¶ 软烘烤(曝光前烘烤)
a. 将涂覆光刻胶的硅片置于水平热板上;b. SU-8 3050 光刻胶:先在 65℃ 烘烤 1 分钟,再在 95℃ 烘烤 20 分钟;SU-8 2100 光刻胶:先在 65℃ 烘烤 5 分钟,再在 95℃ 烘烤 20 分钟;c. 缓慢冷却至 22–25℃(冷却速率 ≤5℃/ 分钟)。
¶ 紫外曝光
a. 使用掩模的情况:i. 将高分辨率光掩模(含图案的醋酸纤维膜)与涂胶硅片接触放置;ii. 必要时使用光刻机或接触曝光装置进行对准;⚠️ 关键注意事项:特征尺寸越小,光刻胶与光掩模间的密封越关键。这可减少折射与图案模糊的影响,对 <10 μm 的特征尤为重要。b. 无掩模光刻的情况:i. 将基底放入仪器并进行对准;ii. 导入 CAD 文件,确保样品书写区域与基底位置匹配;c. 用配备 385 nm 激光的 ML3 仪器,以适当剂量的 365 nm 紫外光曝光:SU-8 3050 光刻胶曝光剂量为 250 mJ/cm²,SU-8 2100 光刻胶为 240 mJ/cm²。注:紫外曝光剂量因灯的类型与使用时间而异,因此需进行剂量响应校准,以确定每种厚度光刻胶的最佳曝光能量。
¶ 曝光后烘烤(PEB)
a. 将硅片正面朝上置于热板上;b. 在 65℃ 烘烤 1 分钟;c. 升温至 95℃ 并烘烤 5 分钟;d. 可进一步升温至约 120℃,以确保溶剂去除并促进 SU-8 完全聚合,这有助于增强 SU-8 与基底的黏附;e. 缓慢冷却至 22–25℃,避免内应力与光刻胶破裂。
¶ 显影
a. 将硅片浸入 SU-8 显影剂(如丙二醇甲醚醋酸酯,PGMEA)中 5–15 分钟,直至未曝光的 SU-8 被去除;b. 将硅片浸入 IPA 等非溶剂中验证显影是否完全 —— 若存在未曝光 SU-8,会形成白色沉淀;c. 若仍有沉淀,需再次浸入显影剂中,直至验证无沉淀产生;d. 显影过程中轻轻搅动溶液;e. 用新鲜 IPA 冲洗硅片;f. 用氮气气流吹干。
¶ 硬烘烤(可选,但强烈建议进行以提升 PDMS 浇筑时的耐用性)
a. 将硅片在 150℃ 烘烤 10–30 分钟;b. 缓慢冷却至 22–25℃。
¶ 母版检查与化学修饰
a. 用光学显微镜检查图案是否存在缺陷;b. 用硅烷处理硅 / SU-8 母版模板,形成疏水涂层以防止 PDMS 黏附;注:该涂层通过硅烷键与硅(通过其天然氧化层)和 SU-8 表面结合。建议先进行氧等离子体预处理,以去除污染物并激活表面,确保硅烷修饰均匀且有效。c. 在模板旁加入约 100 μL 六甲基二硅氮烷(HMDS),降低压力使 HMDS 挥发;⚠️ 危险提示:硅烷及其相关化学过程具有危险性,需严格遵守安全防护措施。务必在化学通风橱中操作,并查阅安全数据表(SDS)以确保正确操作。d. 让母版静置至少 3 小时,确保 HMDS 表面修饰完成;e. 将母版模板存放在洁净、无尘的容器中,待后续 PDMS 浇筑使用。
¶ 关键资源表
| 试剂或资源 | 来源 | 标识号 |
|---|---|---|
| 生物样本 | - | - |
| 健康 E18 大鼠皮层组织(CD 大鼠,Sprague-Dawley 品系,Rattus norvegicus) | Charles River | N/A |
| 化学试剂、多肽与重组蛋白 | - | - |
| 丙酮(99.8%) | Thermo Fisher Scientific | 268310025 |
| 杜氏磷酸缓冲盐溶液(DPBS) | Sigma-Aldrich | D8537 |
| Extran 清洁剂 | Sigma-Aldrich | 1075532500 |
| 六甲基二硅氮烷(HMDS) | Thermo Fisher Scientific | TS-84769 |
| 异丙醇(IPA) | Thermo Fisher Scientific | 149320250 |
| 层粘连蛋白(人源) | Biolamina | LN411-02 |
| 层粘连蛋白(鼠源) | Sigma-Aldrich | L2020 |
| NeuroFluo NeuO 荧光染料 | STEMCELL Technologies | 01801 |
| 多聚 - L - 鸟氨酸(PLO) | Sigma-Aldrich | P4957 |
| 丙二醇甲醚醋酸酯(PGMEA) | Sigma-Aldrich | 484431 |
| 硅酮 RTV 密封剂 QSIL 216(PDMS 替代物) | CHT | 1667371 |
| SU-8 2100 光刻胶 | Kayaku Advanced Materials, Inc. | Y111075 |
| SU-8 3050 光刻胶 | Kayaku Advanced Materials, Inc. | Y311075 |
| SU-8 显影剂 | Kayaku Advanced Materials, Inc. | Y020100 |
| SYLGARD 184 硅酮弹性体基底 | DWO Europe | 01673921 |
| SYLGARD 184 硅酮弹性体固化剂 | DWO Europe | 01673921 |
| Tergazyme 清洁剂 | Sigma-Aldrich | Z273287 |
| 三氯(1H,1H,2H,2H - 全氟辛基)硅烷 | Sigma-Aldrich | 448931 |
| 实验模型:生物 / 品系 | - | - |
| Sprague-Dawley 大鼠(Rattus norvegicus,E18 胚胎脑皮层,雌雄混合) | Charles River | CD 大鼠 |
| 软件与算法 | - | - |
| AutoCAD | Autodesk Inc. | https://www.autodesk.com/ |
| BrainWave 5.5 软件 | 3Brain AG | https://www.3brain.com/ |
| MaxLab Live 软件 | MaxWell Biosystems AG | https://www.mxwbio.com/ |
| 其他 | - | - |
| 醋酸纤维掩模打印服务 | JD Photo Data | https://www.jd-photodata.co.uk/ |
| 醋酸纤维掩模 | JD Photo Data | N/A |
| 活检打孔器 | KaiMedical | BP-60F |
| CorePlate HD-MEA 芯片(3Brain 公司) | 3Brain | CorePlate™ 1W 38/60 |
| MaxOne HD-MEA 芯片(MaxWell 公司) | MaxWell Biosystems | MaxOne Chips |
| HD-MEA 记录系统(3Brain 公司) | 3Brain AG | BioCAM DubleX 2019 |
| HD-MEA 记录系统(MaxWell 公司) | MaxWell Biosystems | MaxOne |
| Heratherm 烘箱 | Thermo Fisher Scientific | Heratherm OMH100 |
| JP Selecta Plactronic 热板 | Fisher Scientific | 12022385 |
| 光刻机 | SUsS Microtec | MJB4 |
| 微定位打孔系统 | CorSolutions | PDMS Port Creator |
| 配备 385 nm 激光的 ML3 系统 | Durham Magneto Optics | Optics ML3 |
| 4 英寸 CZ 硅片(N 型,磷掺杂,厚度 525 μm) | Siegert Wafer GmbH | N/A |
| 旋涂仪 | Laurell Tech | WS-650-23 |
| 等离子体清洗机 | Harrick | PCD-002-CE |
| 真空干燥器(Buerkle 塑料材质) | Thermo Fisher Scientific | 10182391 |
¶ 材料与设备
¶ 试剂储存与制备
- 层粘连蛋白:在 4℃ 解冻,冰上分装为 10 μL aliquots,-20℃ 储存 3–6 个月;
- 多聚 - L - 鸟氨酸(PLO):4℃ 储存,有效期长达 12 个月;
- SYLGARD 184 弹性体套件(基底与固化剂):22–25℃ 储存,直至标注有效期;替代方案:推荐使用德国 CHT Silicones 公司提供的 QSIL 216 PDMS 套件;
- SU-8 光刻胶:22–25℃ 储存,直至标注有效期;
- 硅烷:存放在干燥、通风良好的区域,使用耐化学腐蚀的密封容器,远离不相容物质;
- 丙酮、异丙醇、PGMEA、HMDS:均存放在干燥、通风良好的区域,使用耐化学腐蚀的密封容器,远离不相容物质;
- PLO 替代物(聚乙烯亚胺,PEI):-20℃ 储存,直至标注有效期;
- Extran 5% 溶液:用去离子水配制 1 L 5% Extran 溶液,22–25℃ 储存,直至标注有效期;
- Tergazyme 1% 溶液:4℃ 干燥储存,使用时用无菌去离子水新鲜配制 1% Tergazyme 溶液。
¶ PDMS 成分(基底与固化剂质量比 10:1)
| 试剂 | 最终浓度 |
|---|---|
| 硅酮弹性体基底 | 91% |
| 硅酮弹性体固化剂 | 9% |
¶ 特定细胞模型推荐涂层及其特性 *
| 细胞模型 | 第一层涂层 | 第二层涂层 |
|---|---|---|
| 原代培养细胞 | PLO(50 μg/mL) | 鼠源层粘连蛋白(10 μg/mL) |
| 人诱导多能干细胞(hiPSC)衍生细胞 ²⁶ | PLO(50 μg/mL)或 PEI(100 μg/mL) | 人源层粘连蛋白(20 μg/mL) |
* 注:根据细胞类型与分化阶段,通常需要特定涂层以促进细胞黏附、生长与成熟。E18 大鼠胚胎脑来源的原代皮层细胞培养需 2 小时准备,通常在 5 天内出现初始神经元活性;而人诱导多能干细胞(hiPSC)衍生的神经元培养需约 2 周制备,之后还需约 3 周成熟才会出现首次活性⁴。本方案中,所有结果均来自 E18 大鼠胚胎原代皮层神经元培养。
¶ 详细实验步骤
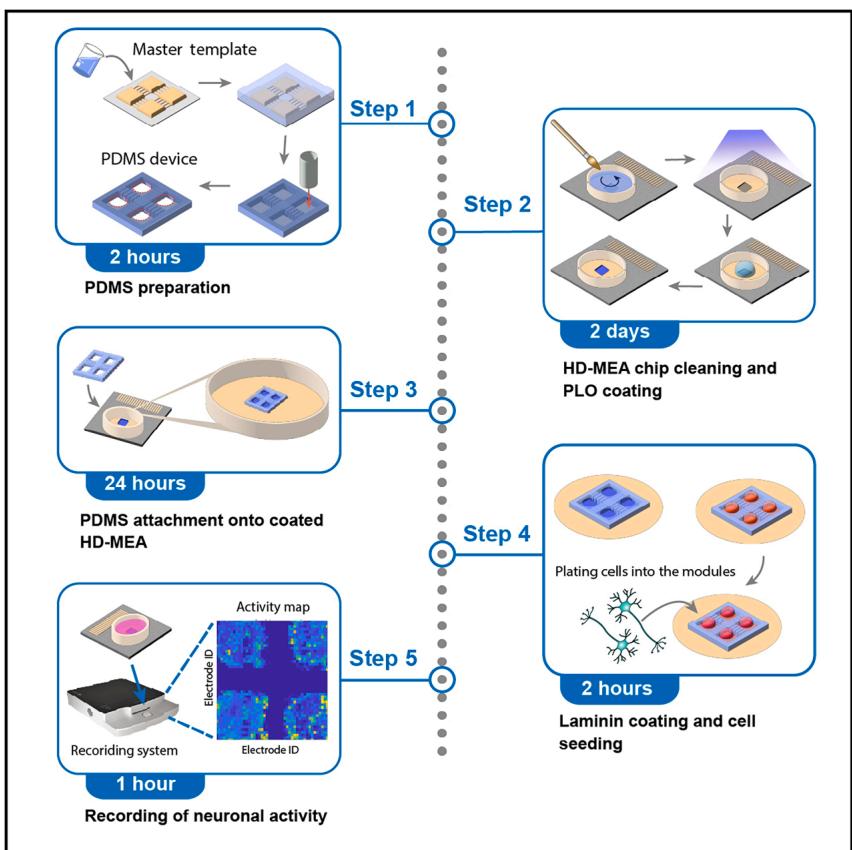
本方案描述了 PDMS 微结构的制备与灭菌、HD-MEA 芯片的准备与清洗,以及在由 4 个互联腔室组成的定制化微结构中培养神经元网络的后续步骤。重点关注 PDMS 结构在 HD-MEA 芯片表面的精准对准与放置,以及涂层和细胞接种流程。方案还包含实验后 HD-MEA 芯片的清洗复用步骤。图 1A 标注了 HD-MEA 芯片的关键结构区域(贯穿整个方案),图 1B 展示了完整组装的 PDMS-HD-MEA 器件(含 4 个 “模块” 腔室,通过微通道正交互联)。
¶ PDMS 制备与清洗
⏱️ 耗时:约 2 天(含固化与清洗)
- 为降低污染风险,后续所有步骤需在无菌环境中进行。由于 PDMS 具有黏性,建议全程使用无菌一次性材料(如塑料培养皿、巴氏吸管)(参见 “问题 1”)。
- 按 1:10 的比例混合 PDMS 固化剂与弹性体基底:先将弹性体基底倒入无菌一次性塑料培养皿(直径 ≥60 mm),再加入固化剂;注:使用分析天平精确称量。由于两种成分黏度高,建议剪开塑料巴氏吸管尖端以扩大开口,便于移液。注:需根据母版模具尺寸调整 PDMS 体积与培养皿大小。注:未固化 PDMS 难以清洗,因此建议使用一次性塑料培养皿作为混合容器(包装无菌无尘,使用后可丢弃),也可在其他无菌容器中进行制备。
- 充分混合两种 PDMS 成分 3–5 分钟,直至混合物中气泡均匀分布且所有滞留空气排出(图 2A);⚠️ 关键注意事项:若 PDMS 成分混合不充分(尤其是容器底部或壁面),可能导致部分固化剂未参与反应,后续出现未固化区域或黏附问题。
- 使用真空干燥器,在约 60 Torr 压力下对 PDMS 混合物脱气 15 分钟;
- 将器件模板放入与母版尺寸匹配的新无菌塑料培养皿中,随后将 PDMS 混合物浇筑在模具上(图 2B);⚠️ 关键注意事项:PDMS 浇筑体积决定最终结构高度,建议厚度为 0.5–1 mm。过厚可能导致与 HD-MEA 芯片脱离,过薄则难以操作。注意:所用培养皿需在 70–80℃ 下保持热稳定性,避免加热时变形。
- 重复步骤 4,去除 PDMS 与母版表面间的滞留空气;注:若仍有气泡,可通过气压去除或再次真空脱气。由于未固化 PDMS 黏度高,气泡自然上浮逸出需较长时间。
- 将装有 PDMS 覆盖母版的培养皿放入烘箱,在 70℃ 下固化 1 小时(图 2C);注:需确认 PDMS 完全固化变硬,且无黏性(用无菌巴氏吸管触碰时不黏附)。注:PDMS 固化速度随温度变化(高温加速、低温减速),建议参考制造商数据表。通常可在 65℃ 下固化 4 小时,或在 80℃ 下固化 30 分钟。
- 冷却后,用无菌手术刀切割出所需图案,塑形后放入新培养皿(图 2D);建议在显微镜下引导切割(参见 “问题 2”);注意:手术刀不要施加过大压力,避免损坏母版模具。
- 为完成 PDMS 浇筑件制备,在所需位置打孔(形成 “模块”)以方便细胞接种:本方案中,在 PDMS 上按 2×2 网格打出 4 个直径 2 mm 的圆形腔室;注:这些打孔腔室用于在微结构中接种细胞(图 2E)。注:需根据 PDMS 设计与用途调整打孔模块大小。本方案示例中,浇筑的 PDMS 器件含一系列平行微通道(宽 10 μm、深 10 μm、长 400 μm),因此打孔模块通过这些微通道实现互联(图 1B、图 2D)。
- 清洗 PDMS 器件以防止后续污染:将 PDMS 浸入 70% 乙醇中 30 分钟;
- 用无菌去离子水冲洗 3 次后,将 PDMS 器件(通道面朝上)放入新培养皿,在紫外杀菌灯下照射 30 分钟;⚠️ 关键注意事项:此步骤至关重要 ——PDMS 可能向培养基中释放有机溶剂,因此需彻底清洗以去除这些溶剂,最大限度减少对细胞活力与实验结果的不良影响 ²⁷。
- 最后,在无菌条件下将 PDMS 器件再干燥 1 小时。完全干燥后,即可将其贴合到预清洗预涂层的 HD-MEA 芯片上。
暂停点:此步骤可暂停,PDMS 器件可存放在无菌容器中备用。
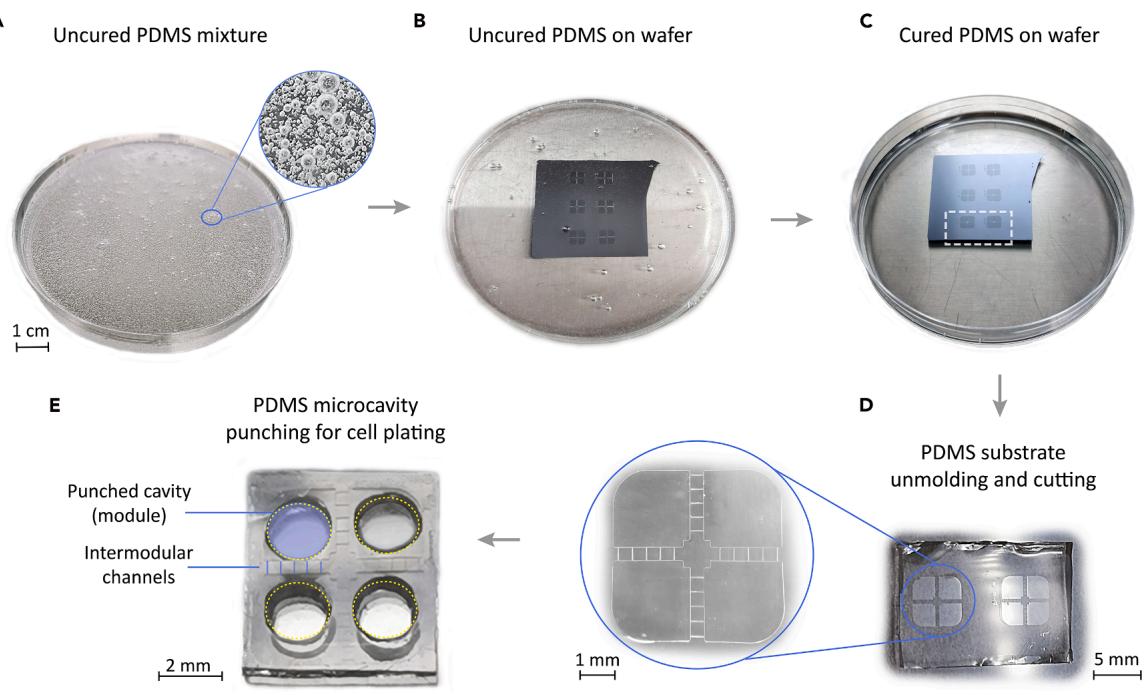
图 2:PDMS 结构制备步骤
(A)未固化 PDMS 混合物;(B)将液态 PDMS 浇筑在培养皿底部的光刻胶母版硅片上;(C)固化后的 PDMS;(D)两个待从母版剥离的 PDMS 器件(对应 C 中白色虚线框图案),左侧器件(蓝色圈出)放大图显示模块对间的交叉通道细节;(E)剥离后的 PDMS 浇筑件,含 4 个打孔微腔室(模块),用于神经元接种。
¶ HD-MEA 芯片清洗
⏱️ 耗时:1–2 天
- 为防止细菌与真菌污染,应尽量避免接触 HD-MEA 芯片的孔区域,仅手持芯片边缘操作。此外,将芯片放入培养皿中进行后续处理,减少直接接触以降低污染风险。
- 向 HD-MEA 孔中加入无菌 DPBS,降低 CMOS 电极区的疏水性,在 37℃ 下孵育 20 分钟;替代方案:可用 1% Tergazyme 溶液(溶于无菌去离子水)替代 DPBS—— 向孔中加满 Tergazyme 溶液,在 37℃ 培养箱中孵育 24 小时,之后去除溶液并用无菌去离子水冲洗孔 3 次。
- 去除 DPBS 后,向孔中加满 5% Extran 溶液,用软刷轻轻清洗;随后用 5% Extran 溶液清洗整个芯片(金接触垫除外);注:避免液体接触金接触垫(图 1A)—— 该区域用于 HD-MEA 与外部电子设备连接,需保持干燥以防氧化。
- 用无菌去离子水重复步骤 3,清洗孔中残留的 Extran;
- 用空气或氮气气流吹干芯片;
- 将芯片转移至超净工作台:用蘸有 70% 乙醇的纸巾清洁芯片表面与接触垫(避开孔区域),然后将芯片放入无菌培养皿;
- 向芯片孔中加满 70% 乙醇,孵育 30 分钟;之后用无菌去离子水冲洗 3 次;
- 在紫外杀菌灯下对芯片灭菌 30 分钟,芯片即可用于后续涂层与 PDMS 贴合。
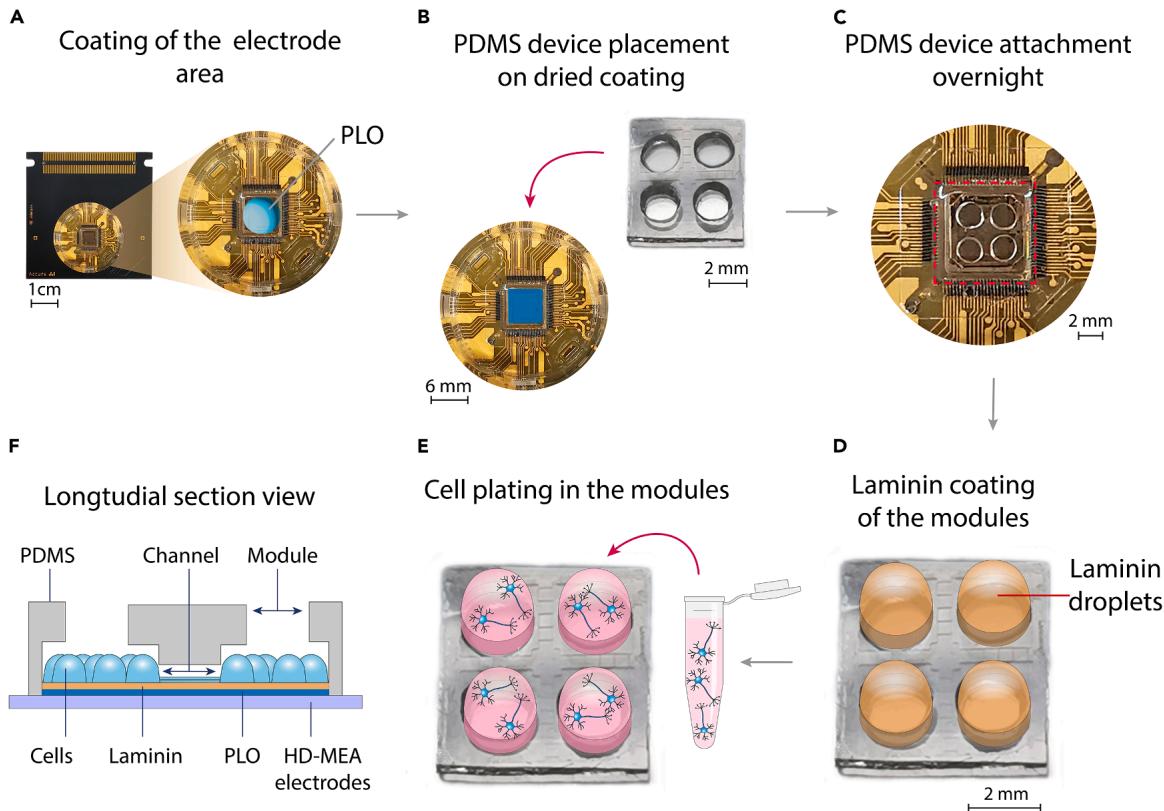
图 3:从 HD-MEA 涂层到 PDMS 器件放置及细胞接种的流程
(A)HD-MEA 孔中预清洗记录电极区的 PLO 涂层;(B)清洗干燥后,在电极区放置 PDMS 浇筑件;(C)PDMS 贴合 20 小时以增强附着力;(D)通过层粘连蛋白液滴对模块内电极进行涂层;(E)仅在模块内接种细胞悬液液滴;(F)PDMS-HD-MEA 系统横截面示意图,显示接种细胞及其通过 PDMS 通道的互联性。
暂停点:此步骤可暂停,HD-MEA 芯片可存放在无菌环境中备用。
¶ HD-MEA 芯片涂层
⏱️ 耗时:2 天
为促进细胞黏附并为 CMOS 电极区营造最佳培养环境,需对芯片表面进行适当涂层。涂层方案可能因细胞类型与实验需求而异。本方案使用大鼠皮层原代神经元培养,因此先涂覆合成涂层 PLO 并干燥,再贴合 PDMS 结构;PDMS 放置后,在接种细胞前涂覆层粘连蛋白。也可使用其他促黏附(生物)化学物质,包括人源层粘连蛋白、聚 - D/L - 赖氨酸(PDL/PLL)、聚鸟氨酸、聚乙烯亚胺(PEI)或其组合。
- 仅在芯片孔内的生长区域涂覆 100 μL PLO(50 μg/mL,用 DPBS 稀释)(图 3A);注:体积不得小于 100 μL,以防孵育过程中蒸发。在大型培养皿中放入装有无菌去离子水的小容器(如 15 mL 离心管盖)和 HD-MEA 芯片,可防止涂层溶液干燥。
- 为确保涂层覆盖整个区域,使用预清洗真空干燥器,在 60 Torr 压力下处理 15 分钟;
- 将涂覆后的芯片在 22–25℃ 下孵育 12–24 小时;
- 用无菌去离子水冲洗 3 次,然后将芯片干燥 3–4 小时;注:第一次冲洗时,使用真空干燥器在 60 Torr 压力下处理 10 分钟,确保去除未结合的 PLO。
¶ PDMS 浇筑件放置
⏱️ 耗时:20–24 小时(含贴合)
- 将 PDMS 浇筑件的通道面朝下,轻轻放置在芯片的目标电极区(图 3B);注:放置前,用显微镜确认 PDMS 微通道方向正确(通道面朝下)。确保 PDMS 器件与 HD-MEA 均完全干燥,以防后续脱离。⚠️ 关键注意事项:PDMS 放置在电极上后,不得移动或重新定位,否则可能损坏记录电极与涂层。操作 PDMS 时避免用镊子触碰电极,确保轻柔放置(参见 “问题 3”)。⚠️ 关键注意事项:不要尝试调整 PDMS 位置,否则可能导致其与 HD-MEA 芯片脱离。
- 在 22–25℃ 下放置 20–24 小时,使 PDMS 与芯片牢固结合(图 3C)。
¶ HD-MEA 芯片二次涂层
⏱️ 耗时:约 2 小时(含孵育)
神经元及其突起将在器件内生长,黏附在 PDMS 打孔模块与微通道暴露的 HD-MEA 表面。为促进神经元网络发育,需在这些表面额外涂覆关键涂层 ——10 μg/mL 鼠源层粘连蛋白。层粘连蛋白的处理与储存细节参见 “材料与设备” 部分。
- 仅在 PDMS 的打孔模块内涂覆涂层:本方案中模块直径为 2 mm,每个模块加入 5 μL 涂层溶液(图 3D);注:需根据打孔模块大小调整涂层体积。注:为防止神经元突起在网络发育过程中生长到 PDMS 表面,涂层溶液仅能加入打孔模块内。
- 将 PDMS - 芯片器件放入真空干燥器,在 60 Torr 压力下处理 5–10 分钟;注:此步骤可确保涂层溶液克服 PDMS 的疏水性,流入微通道。
- 在 37℃、95% 湿度条件下孵育 1–2 小时;⚠️ 关键注意事项:尽管层粘连蛋白常与 PDL 联合使用以促进细胞黏附,但高浓度 PDL 或 PDL 变性(如涂层在细胞接种前干燥)可能产生细胞毒性,降低培养细胞活力。注:由于打孔模块体积小,需每 10 分钟检查一次是否蒸发,必要时补充溶液。若蒸发速率快,可在大型培养皿中放入装有水的容器(如离心管盖),提升湿度。注:若层粘连蛋白干燥,该 HD-MEA 芯片需排除在后续实验之外。注:孵育期间可准备细胞悬液,用于后续芯片接种。
¶ PDMS-HD-MEA 器件上的细胞培养
⏱️ 耗时:2–3 小时(含细胞贴壁)
需根据细胞模型与打孔模块大小调整细胞密度与接种体积。
- 去除涂层溶液,立即向每个 PDMS 打孔模块中加入 5 μL 细胞悬液(密度为 2000 个细胞 /μL)(图 3E)(参见 “问题 5”);注:为防止细胞在 PDMS 表面生长,仅在打孔模块内接种细胞。可用微量移液器将培养基直接注入腔室表面。⚠️ 关键注意事项:去除涂层后需立即加入细胞悬液,防止层粘连蛋白层干燥 —— 脱水层粘连蛋白会导致细胞培养效果不佳 ²⁸。
- 在 37℃、5% CO₂、95% 湿度的培养箱中孵育 1–2 小时,使细胞贴壁;注:由于培养基体积小,建议每 10 分钟检查 PDMS 模块是否保持湿润,必要时轻轻补充细胞培养基。此外,在大型培养皿中放入装有无菌水的容器,与 HD-MEA 芯片一同孵育。
- 根据 PDMS 表面大小,缓慢向 PDMS 上方加入 50–100 μL 细胞培养基,在培养箱中再孵育 30 分钟;⚠️ 关键注意事项:加入培养基时需缓慢轻柔,避免细胞脱落。
- 向孔中缓慢加入 1.5 mL 细胞培养基,完成制备;将芯片放入 37℃、5% CO₂、95% 湿度的培养箱中培养,每周更换一半培养基 2–3 次;注:更换培养基时需保留少量液体,确保 PDMS 始终被液体覆盖,防止细胞脱水。
¶ PDMS-HD-MEA 芯片上的神经元活性记录
⏱️ 耗时:1 小时(含平衡与记录)
HD-MEA 技术可在无菌无创条件下记录模块化神经元网络的活性,支持对同一培养物进行长期动态监测。通常从体外培养第 6–7 天(DIV 6–7)开始记录,每次记录 5–20 分钟(根据实验目标调整)。HD-MEA 系统配备集成加热单元,用于记录过程中温度控制。由于 HD-MEA 的 CMOS 电极对光高度敏感,操作时需用遮光盖覆盖芯片 —— 该盖子通常可作为小型腔室,预留接口连接 CO₂ 气源,有助于在数据采集期间维持培养箱级环境。
- 将 PDMS-HD-MEA 芯片放入记录系统的指定卡槽,盖上遮光盖并连接 CO₂ 气源;
- 在 37℃、5% CO₂ 条件下平衡 10 分钟,让细胞适应环境;
- 根据实验目标,记录 5–20 分钟的神经元活性;注:细胞在系统中最长可记录 1 小时。⚠️ 关键注意事项:不要在更换培养基后立即记录。培养基应在记录前一天或记录后更换,因为新鲜培养基可能影响神经元活性的时空动态。
- 记录结束后,将芯片放回培养箱,待下次使用。注:使用 HD-MEA 软件提取尖峰信号(spike),并通过内置或定制工具进行分析。3Brain 系统的典型采集与数据分析参数为:采样率 20 kHz / 通道,固有噪声水平 11 μV,800 Hz 高通巴特沃斯滤波器(去除低频伪影),基于 “精确定时尖峰检测”(Precise Timing Spike Detection)的尖峰检测算法 ³⁰(阈值为噪声水平的 5 倍)。MaxWell 系统的典型分析参数为:采样率 20 kHz / 通道,固有噪声水平 2.3 μV,300–3000 Hz 带通滤波器(去除低频伪影),自动尖峰检测(阈值为噪声水平的 5 倍)¹。HD-MEA 数据的详细分析及参数影响参见 Wolff 等人的最新研究 ³⁰。
¶ HD-MEA 芯片使用后的清洗
⏱️ 耗时:30 分钟
- 用镊子小心去除 PDMS,避免接触电极;
- 向每个芯片孔中加满 5% Extran 溶液,用软刷轻轻清洗,孵育 30 分钟;
- 用 5% Extran 溶液清洗芯片表面(避开金接触垫);注:不要让液体浸泡接触垫。
- 用无菌去离子水清洗孔和芯片表面 2 次,彻底去除清洁剂残留;
- 用空气或氮气气流吹干芯片,存放在无菌环境中待下次使用(参见 “问题 4”)。
¶ 预期结果
本方案阐述了具有模块化特征的定制化体外神经元培养体系的构建方法,为分隔式神经元回路的形成提供平台,可在可控条件下研究神经元活性与功能连接。对于 3Brain 和 MaxWell 两种系统,所研究的大鼠皮层培养物通常在 DIV 6–7 开始出现神经元活性,同一培养物可在 DIV 21 前每日记录。在此期间,培养物保持稳定活性,约从 DIV 10 开始出现同步的全网络事件。每次记录后,用内置软件处理数据,从电极信号中提取神经元尖峰序列,存储为纯文本文件用于后续分析(如活性定量、有效连接性分析)。
模块化设计对活性的影响从首次记录即可显现:神经元最初在单个模块内稀疏激活,随着模块内连接成熟,逐渐与其他模块建立交互。下文首先展示 3Brain HD-MEA 平台的结果(验证模块化约束对神经元活性的影响),然后演示方案在 MaxWell Biosystems 平台的应用(突出可重复性、跨平台适应性及关键网络特征的保留),最后通过扫描电子显微镜(SEM)图像对比两种平台 HD-MEA 基底的结构,对电极表面拓扑进行表征。
¶ 3Brain 平台:模块化与非模块化网络的神经元动态对比
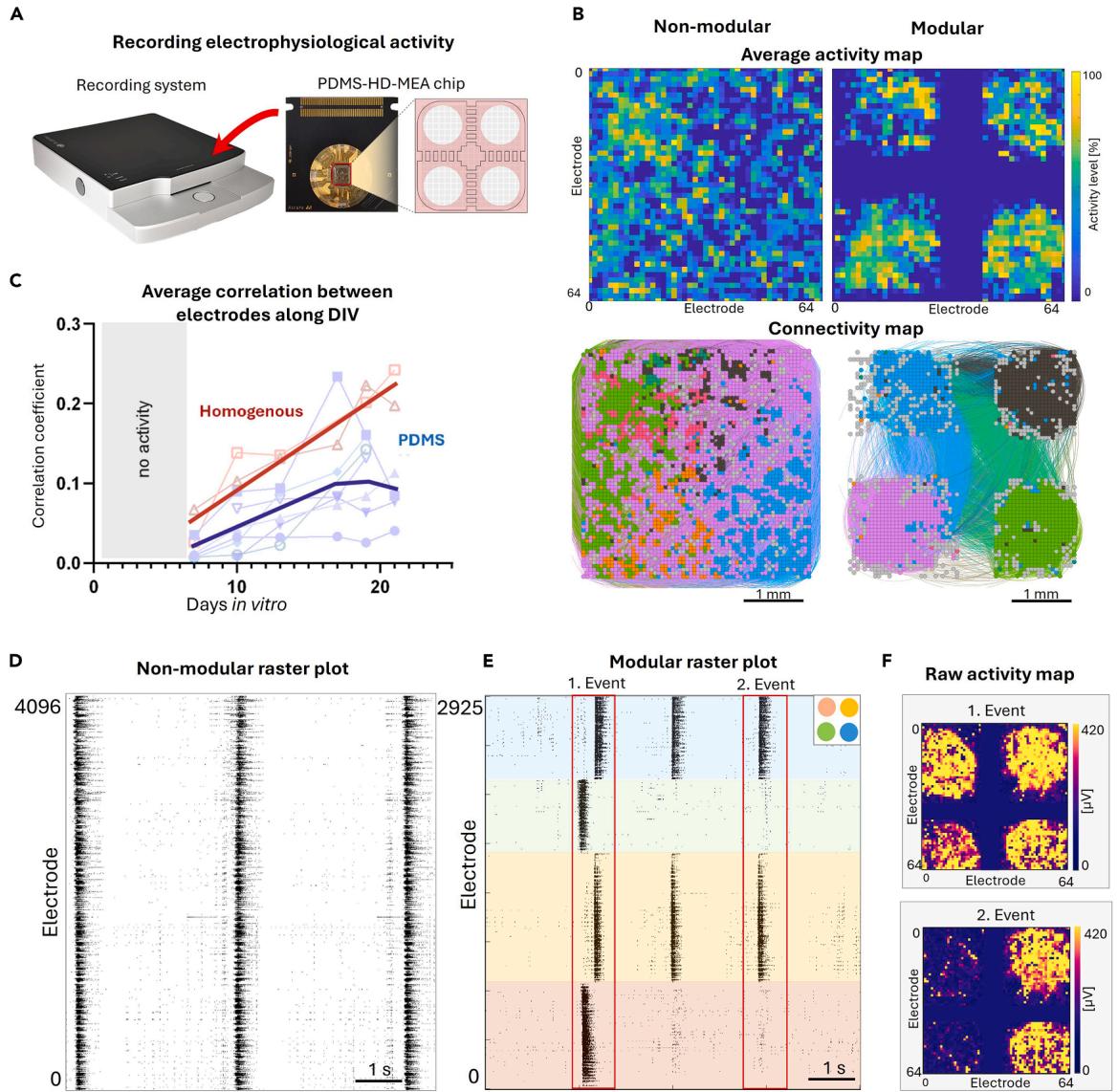
图4. 在3Brain系统上培养的非模块化(均质)和模块化(PDMS实现)皮质网络中神经元动力学的比较结果
(A)记录系统和PDMS-HD-MEA芯片的示意图。(B)上:体外培养第14天(DIV 14)的平均活动图,展示了模块化配置中活动被限制在分隔区域内。颜色亮度与电极的活动程度成正比。下:相应的有效连接图,显示模块通过PDMS装置中内置通道相互作用的能力。颜色突出显示了相互作用强烈的电极组,这种情况在模块内部更为显著。(C)从DIV 7到21,均质网络和模块化网络中活性电极之间的平均相关性。符号表示实验重复,粗线显示每种实验条件的总体平均趋势。(D)均质网络在DIV 14时全芯片自发活动的 raster 图。黑点表示神经元激活。(E)模块化网络的等效数据。彩色条带根据面板右上角提供的配色方案指示特定模块。红色方框突出显示了两个对比鲜明的集体事件,一个是整合性事件(事件1),一个是分离性事件(事件2)。
为验证网络结构对神经元动态的影响,研究在 3Brain 平台的 HD-MEA 芯片上对比了模块化与非模块化网络(图 4A):
- 非模块化神经元培养:活性呈均匀分布(因连接随机);
- 模块化网络:活性局限在 PDMS 定义的模块区域(图 4B)。
网络连接性分析显示:非模块化网络形成广泛互联,而模块化网络的模块内连接密集,模块间连接具有特异性(图 4D)。此外,研究监测了从早期(DIV 7)到晚期(DIV 21)发育过程中的神经元活性,捕捉网络动态的成熟变化:非模块化网络的神经元活性模式平均相关性随时间逐渐上升(同步性增强),而模块化网络在整个发育过程中表现出更多样的活性状态(表明模块化结构支持活性的稳定分离)(图 4C)。
raster 图显示:非模块化网络形成高度同步的集体爆发事件,而模块化网络表现出更丰富的时空动态 —— 包括单个模块内的同步集体爆发,以及跨模块的协同激活,证明模块化网络既能支持模块级活性(分离),也能实现全网络协同激活(整合)(图 4E、4F)。图 4F 的 raster 图中红色方框标注了两个代表性事件:第一个事件中,所有模块在一个时间窗口内依次激活(整合,图 4G 上);第二个事件中,仅两个模块共同激活(分离,图 4G 下)。
综上,这些结果证明 PDMS 微结构可有效约束网络生长与连接,形成明确的模块化结构;该结构可长期保留,并支持比非模块化设计更丰富的复杂动态。
¶ MaxWell 平台:PDMS 细胞图案化的适用性验证
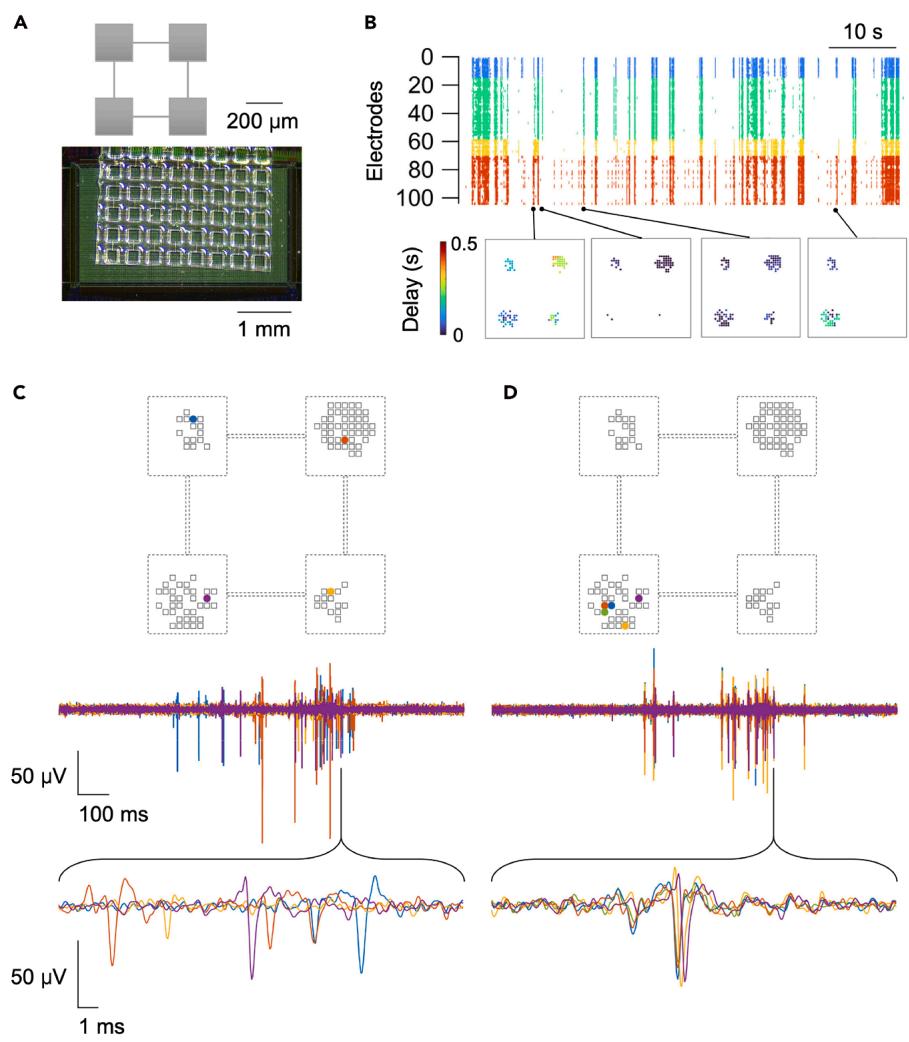
图5. MaxOne系统中模块化培养体系自发活动代表性结果
(A) 模块化网络示意图(上)及置于HD-MEA中的微加工PDMS(下)。
(B) 上:模块化网络神经活动随时间变化的网格图;不同模块电极采用颜色编码。下:不同时间点对应的神经活动传播示意图。
(C和D) 不同模块及单一模块内的活动测量结果(上),下方显示对应颜色的波形图。图经Sato等¹许可转载并改编。
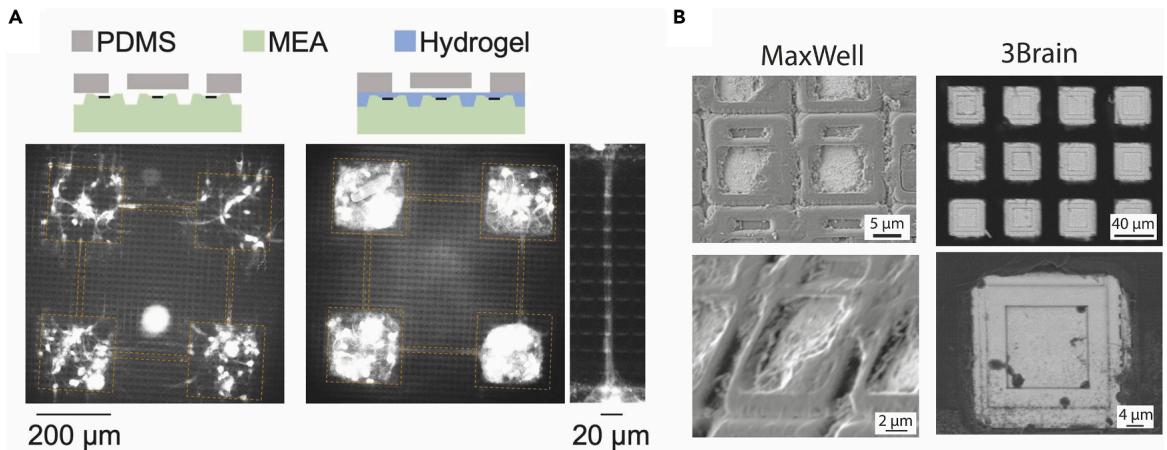
图6. HD-MEA芯片电极区域的表面地形概览
(A) MaxWell HD-MEA芯片上PDMS微结构的集成,使用荧光染料(NeuO)对β-III微管蛋白进行染色,以显示无水凝胶涂层(左)和有水凝胶涂层(右)条件下神经突的生长情况。右侧面板展示了连接两个模块的微通道细节。经Sato等¹许可转载
(B) MaxWell公司HD-MEA芯片(左:无水凝胶涂层)与3Brain公司HD-MEA芯片(右)电极区域的扫描电子显微镜图像。
图 5 和图 6 展示了 PDMS 细胞图案化在其他厂商 HD-MEA 上的应用 —— 使用 MaxWell Biosystems 公司的 MaxOne HD-MEA 芯片,制备的 PDMS 微结构可构建更小的网络。PDMS 中的微孔边长为 200 μm(图 5A),不同于此前的 2 mm 孔。这类器件的制备细节参见 Murota 等人的研究 ³¹。
与前文的大型模块化网络类似(图 4E 右),这些微图案化神经元网络表现出复杂的自发电活性,特征为分离与整合活性模式共存(即使在小尺度下)(图 5B)。在全局同步爆发期间,活性在模块间的传播时间从数毫秒到数十毫秒不等(图 5C)。需注意:数十毫秒级的传播可通过钙成像捕捉 ³²,但毫秒级传播因成像设备的时间限制和钙指示剂的动力学特性难以捕获 —— 这凸显了 HD-MEA 的必要性。HD-MEA 的亚毫秒采样率甚至可解析单个模块内的活性传播(图 5D)。具体实验细节参见 Sato 等人的研究 ¹。
由于原始 MaxOne 芯片表面存在微拓扑特征,需额外处理(水凝胶涂层平整表面)才能贴合 PDMS 器件,且不会降低电极灵敏度(图 6A)¹,¹³。
¶ HD-MEA 电极表面拓扑对比(SEM 分析)
SEM 图像显示不同厂商 HD-MEA 的电极表面拓扑存在显著差异,这对 PDMS 黏附和轴突生长模式有重要影响:3Brain 芯片的电极区域凹陷,而 MaxWell 芯片的电极结构凸起(图 6B)。设计实验时需充分考虑这些差异(可能影响物理界面稳定性和轴突生长导向)。不过,新型 MaxOne+ 芯片表面更平坦,PDMS 器件可直接贴合,且无 PDMS 下方的非特异性轴突生长,因此强烈推荐使用。目前研究仅在 MaxOne+ 芯片上使用了 PEI / 层粘连蛋白涂层,但理论上本方案中 3Brain 芯片使用的 PLO / 层粘连蛋白涂层也适用。
综上,这些结果证明本模块化网络方案对不同 HD-MEA 平台及其空间构型具有兼容性。这种跨平台适应性为神经元动态、突触整合、网络计算和神经元发育研究提供了更广泛的应用可能。
¶ 局限性
¶ 局限性 1:PDMS 设计约束
不同厂商、不同型号的 HD-MEA 芯片,其电极区域和布局存在差异。小面积电极区域可能显著限制 PDMS 结构的设计与最终尺寸。因此,HD-MEA 芯片设计的多样性会约束 PDMS 结构的图案和尺寸(需与电极区域精准对准),导致方案应用于不同芯片时需调整(参见 “微加工器件设计” 部分)。
潜在解决方案:设计 PDMS 浇筑件时,需确认 HD-MEA 芯片生长区和电极区的精确尺寸。例如:
- 3Brain 公司 CorePlate™ 1W 38/60 芯片:PDMS 尺寸需小于生长区(6×6 mm²)以适配孔结构,设计尺寸应接近电极区(3.8×3.8 mm²),确保细胞生长在电极上方(图 1);
- MaxWell 公司 MaxOne 芯片:电极区面积为 3.85×3.85 mm²(图 5A)。
¶ 局限性 2:厂商内部 HD-MEA 拓扑差异
不同型号芯片的电极表面拓扑可能不完全平坦,影响 PDMS 与芯片表面的良好接触和贴合,进而影响数据可重复性及神经元连接约束的预期效果。例如:3Brain 芯片电极凹陷,而 MaxOne+ 芯片电极凸起(图 6B)。
潜在解决方案:实验设计阶段,通过显微镜观察芯片拓扑或向厂商获取芯片信息。若表面非平面,可使用薄中间生物层涂层(如胶原蛋白)提升表面均匀性(图 6A)¹。
¶ 局限性 3:HD-MEA 的非透明性
由于复杂的多层电子结构,大多数 HD-MEA 芯片材料不透明,导致培养细胞时难以监测神经元形态与发育(参见 “PDMS-HD-MEA 器件上的细胞培养” 部分)。
潜在解决方案:
- 使用 NeuO 等活细胞荧光染料(标记 β-III - 微管蛋白),结合正置显微镜观察轴突生长(图 6A)¹;
- 同时在透明表面(如盖玻片)上平行培养神经元,通过钙成像监测活性,辅助分析网络行为(可补充形态与发育信息)。
¶ 局限性 4:PDMS 固化的批次差异
混合精度、固化温度和试剂储存时间的差异,可能导致 PDMS 硬度和收缩率变化,影响特征一致性(参见 “PDMS 制备与清洗” 部分)。
潜在解决方案:通过稳定混合比例、控制固化条件和使用新鲜试剂,最大限度减少差异。对于 >10 μm 的特征,这些影响通常可忽略,不会影响图案保真度。
¶ 局限性 5:SU-8 母版高度差异
旋涂转速、湿度、温度和软烘烤均匀性,可能导致 SU-8 厚度出现 ±10% 的差异(参见 “母版反向器件制备” 部分)。
潜在解决方案:通过轮廓测量或显微镜检查,结合涂层参数的常规校准,确保不同批次母版的可重复性。
¶ 局限性 6:PDMS 长期翘曲
长期培养中,PDMS 可能发生缓慢机械松弛,导致轻微翘曲或尺寸偏移(参见 “PDMS 制备与清洗” 部分)。
潜在解决方案:PDMS 器件需在规定时间内使用(建议制备后 12 个月内),且仅使用新鲜制备的器件(避免复用)—— 长期使用积累的材料形变可能影响新神经元培养。
¶ 局限性 7:HD-MEA 电极老化
反复灭菌和长期使用可能导致 MEA 电极降解,阻抗升高且信号质量下降(参见 “HD-MEA 芯片清洗” 部分)。
潜在解决方案:建议定期监测阻抗并更换电极,以维持稳定的电生理性能。HD-MEA 芯片达到使用寿命后需更换。
¶ 问题排查
¶ 问题 1:污染风险
PDMS 非无菌且具有黏性,易导致 HD-MEA 芯片污染,影响复用(参见 “PDMS 制备与清洗” 部分)。
潜在解决方案:
- 处理 PDMS 时仅使用无菌材料;
- 建议在万级洁净室中制备 PDMS(微结构制备优化环境,减少气溶胶污染);
- 或在生物安全柜中用紫外光灭菌 PDMS 器件;
- 注意:PDMS 可能吸收部分溶剂,因此尽管乙醇灭菌有效,仍需在细胞接种前将 PDMS 器件在缓冲液或培养基中浸泡数小时,确保去除残留乙醇。
¶ 问题 2:打孔微孔的可重复性
PDMS 浇筑件设计需适配 HD-MEA 芯片电极区,而手工放置和对准(尤其是打孔以实现细胞接触)难度大 —— 微孔间距难以一致,导致腔室空间布局差异,进而影响模块间轴突长度和互联性,降低实验可重复性(参见 “PDMS 制备与清洗” 步骤 8)。
潜在解决方案:
- 使用带集成相机的打孔系统(如 CorSolutions 公司的 PDMS Port Creator),提升微孔精度和可重复性;
- 或在显微镜辅助下精准定位打孔器,通过视觉引导提高打孔精度,确保模块放置一致性。
¶ 问题 3:PDMS 贴合区域记录噪声升高
PDMS 长期覆盖电极通常导致噪声显著升高,影响记录质量和数据准确性(参见 “PDMS 浇筑件放置” 部分)。
潜在解决方案:
- 排除与 PDMS 直接接触的电极(不参与记录和分析);
- 若可能,将电极区明场图像与电极图叠加,手动选择并排除受影响电极;
- 关键:需监控记录过程并重新评估活性数据,若检测到 PDMS 诱导的噪声,使用软件滤波识别并去除噪声电极。
¶ 问题 4:PDMS 残留
PDMS 去除清洗后,部分电极可能残留 PDMS,影响后续记录(参见 “HD-MEA 芯片使用后的清洗” 部分)。
潜在解决方案:
- 为去除残留 PDMS 并确保电极洁净,将 HD-MEA 芯片在 Tergazyme 溶液中孵育 2–24 小时;
- 由于 PDMS 疏水,残留物可能包裹气泡(干扰记录),因此孵育后需将芯片连接 HD-MEA 系统,评估电极活性;
- 若观察到噪声升高(提示仍有气泡),使用 Extran 或 Tergazyme 清洁剂重复清洗流程(参见 “HD-MEA 芯片使用后的清洗” 部分)。
¶ 问题 5:细胞接种难题
向微孔中接种细胞时,难以精准滴加小体积细胞悬液(易触碰 PDMS),可能导致 PDMS 与 HD-MEA 芯片脱离;且小体积悬液易蒸发,影响细胞贴壁,导致分布不均甚至完全损失(参见 “PDMS-HD-MEA 器件上的细胞培养” 部分)。
潜在解决方案:
- 实验前使用未使用的 PDMS 浇筑件,练习向微孔中滴加小体积悬液,提升操作熟练度和效率,减少悬液暴露时间(降低蒸发);
- 替代方案:滴加覆盖所有微孔的大体积细胞悬液,但可能导致 PDMS 表面(微孔间区域)出现非特异性细胞黏附与生长;为缓解此问题,可在细胞接种前用琼脂糖涂层 PDMS 表面,防止非特异性细胞黏附。
¶ 资源可用性
¶ 主要联系人
如需获取更多信息或资源,请联系主要联系人霍尔迪・索里亚诺(jordi.soriano@ub.edu)。
¶ 技术联系人
有关方案执行的技术问题,请联系技术联系人:安娜 - 克里斯蒂娜・黑布(haeb.anna@web.de)、山本秀明(hideaki.yamamoto.e3@tohoku.ac.jp)、保罗・罗奇(p.roach@lboro.ac.uk)。
¶ 材料可用性
本研究未产生新的独特试剂。
¶ 数据与代码可用性
本研究未产生新的独特数据或代码。
¶ 致谢
本研究部分得到以下项目支持:
- 日本文部科学省(MEXT)“多细胞神经生物计算” 变革性研究领域(A 类)资助(编号 24H02332、24H02333);
- 日本学术振兴会(JSPS)科研费资助(编号 22KK0177、23H03489);
- 东北大学电气通信研究所(RIEC)合作研究项目;
- 欧盟 “地平线 2020” 研究与创新计划资助(编号 964877,项目 NEU-CHiP);
- 西班牙科学、创新与大学部资助(项目编号 PID2022-137713NB-C22(J.S.)、PID2023-146800OB-I00(D.T.)、CNS2023-143862(D.T.));
- 西班牙加泰罗尼亚自治区资助(项目编号 2021-SGR-01086(D.T.)、2021-SGR-00450(J.S.))。
本研究部分在东北大学电气通信研究所纳米电子学与自旋电子学实验室开展。
¶ 作者贡献
A.-C.H.、Y.S.、J.S.、D.T. 和 H.Y. 构思实验与研究框架;D.M.、A.-C.H.、P.R.、Y.S.、D.T.、J.S. 和 H.Y. 设计图案;D.M. 和 Y.S. 制备母版模具;A.-C.H. 设计并执行 PDMS 方案、3Brain 系统的初始细胞培养与数据分析;Y.S. 执行 MaxWell 系统的初始细胞培养与数据分析;D.M. 和 P.R. 开展 SEM 实验;A.-C.H. 撰写初稿;J.S.、H.Y.、D.T.、Y.S.、D.M. 和 P.R. 修订并审阅手稿。
¶ 利益声明
作者声明无竞争利益。
¶ 参考文献
- Sato, Y., Yamamoto, H., Kato, H., Tanii, T., Sato, S., and Hirano-Iwata, A. (2022). Microfluidic cell engineering on high-density microelectrode arrays for assessing structure-function relationships in living neuronal networks. Front. Neurosci. 16, 943310. https://doi.org/10.3389/ fnins.2022.943310. 2. Soriano, J. (2023). Neuronal Cultures: Exploring Biophysics, Complex Systems, and Medicine in a Dish. Biophysica 3, 181–202. https://doi.org/10.3390/biophysica3010012.
- Obien, M.E.J., Gong, W., Frey, U., and Bakkum, D.J. (2017). CMOS-Based High-Density Microelectrode Arrays: Technology and Applications. In Emerging Trends in Neuro Engineering and Neural Computation (Springer), pp. 3–39. https://doi.org/10.1007/ 978-981-10-3957-7_1.
- Este´ vez-Priego, E., Moreno-Fina, M., Monni, E., Kokaia, Z., Soriano, J., and Tornero, D. (2023). Long-term calcium imaging reveals functional development in hiPSC-derived cultures comparable to human but not rat primary cultures. Stem Cell Rep. 18, 205–219. https://doi.org/10.1016/j.stemcr. 2022.11.014.
- Bullmore, E., and Sporns, O. (2009). Complex brain networks: Graph theoretical analysis of structural and functional systems. Nat. Rev. Neurosci. 10, 186–198. https://doi.org/10. 1038/nrn2575.
- Meunier, D., Lambiotte, R., and Bullmore, E.T. (2010). Modular and hierarchically modular organization of brain networks. Front. Neurosci. 4, 200–211. https://doi.org/10.3389/ fnins.2010.00200.
- Brofiga, M., Losacco, S., Poggio, F., Zerbo, R.A., Milanese, M., Massobrio, P., and Burlando, B. (2023). Multiple neuron clusters on Micro-Electrode Arrays as an in vitro model of brain network. Sci. Rep. 13, 15604. https://doi. org/10.1038/s41598-023-42168-0.
- Xu, S., Liu, Y., Yang, Y., Zhang, K., Liang, W., Xu, Z., Wu, Y., Luo, J., Zhuang, C., and Cai, X. (2023). Recent Progress and Perspectives on Neural Chip Platforms Integrating PDMSBased Microfluidic Devices and Microelectrode Arrays. Micromachines 14, 709. https://doi.org/10.3390/mi14040709.
- Habibey, R., Striebel, J., Meinert, M., Latiftikhereshki, R., Schmieder, F., Nasiri, R., and Latifi, S. (2024). Engineered modular neuronal networks-on-chip represent structure-function relationship. Biosens. Bioelectron. 261, 116518. https://doi.org/10. 1016/j.bios.2024.116518.
- Callegari, F., Brofiga, M., Poggio, F., and Massobrio, P. (2022). Stimulus-Evoked Activity Modulation of In Vitro Engineered Cortical and Hippocampal Networks. Micromachines 13, 1212. https://doi.org/10.3390/mi13081212.
- Pelkonen, A., Mzezewa, R., Sukki, L., Ryyna¨ nen, T., Kreutzer, J., Hyva¨ rinen, T., Vinogradov, A., Aarnos, L., Lekkala, J., Kallio, P., and Narkilahti, S. (2020). A modular brain-on-a-chip for modelling epileptic seizures with functionally connected human neuronal networks. Biosens. Bioelectron. 168, 112553. https://doi.org/10. 1016/j.bios.2020.112553.
- Winter-Hjelm, N., Brune Tomren, A˚ ., Sikorski, P., Sandvig, A., and Sandvig, I. (2023). Structurefunction dynamics of engineered, modular neuronal networks with controllable afferentefferent connectivity. J. Neural. Eng. 20, 046024. https://doi.org/10.1088/1741-2552/ace37f.
- Duru, J., Ku¨ chler, J., Ihle, S.J., Forro´ , C., Bernardi, A., Girardin, S., Hengsteler, J., Wheeler, S., Vo¨ ro¨ s, J., and Ruff, T. (2022). Engineered Biological Neural Networks on High Density CMOS Microelectrode Arrays. Front. Neurosci. 16, 829884. https://doi.org/10. 3389/fnins.2022.829884.
- Stevenson, I.H., and Kording, K.P. (2011). How advances in neural recording affect data analysis. Nat. Neurosci. 14, 139–142. https:// doi.org/10.1038/nn.2731.
- Berdondini, L., Imfeld, K., Maccione, A., Tedesco, M., Neukom, S., Koudelka-Hep, M., and Martinoia, S. (2009). Active pixel sensor array for high spatio-temporal resolution electrophysiological recordings from single cell to large scale neuronal networks. Lab Chip 9, 2644–2651. https://doi.org/10.1039/b907394a.
- Ballini, M., Mu¨ ller, J., Livi, P., Chen, Y., Frey, U., Stettler, A., Shadmani, A., Viswam, V., Jones, I.L., Ja¨ ckel, D., et al. (2014). A 1024-channel CMOS microelectrode array with 26,400 electrodes for recording and stimulation of electrogenic cells in vitro. IEEE J. Solid-State Circuits 49, 2705–2719. https://doi.org/10. 1109/JSSC.2014.2359219.
- Obien, M.E.J., Deligkaris, K., Bullmann, T., Bakkum, D.J., and Frey, U. (2014). Revealing neuronal function through microelectrode array recordings. Front. Neurosci. 8, 423. https://doi.org/10.3389/fnins.2014.00423.
- Bertotti, G., Velychko, D., Dodel, N., Keil, S., Wolansky, D., Tillak, B., Schreiter, M., Grall, A., Jesinger, P., Ro¨ hler, S., et al. (2014). A CMOSBased Sensor Array for In-Vitro Neural Tissue Interfacing with 4225 Recording Sites and 1024 Stimulation Sites. In 2014 IEEE Biomedical Circuits and Systems Conference (BioCAS) Proceedings, pp. 304–307. https://doi.org/10. 1109/BioCAS.2014.6981723.
- Wheeler, B.C., and Brewer, G.J. (2010). Designing Neural Networks in Culture. Proc. IEEE 98, 398–406. https://doi.org/10.1109/ JPROC.2009.2039029.
- DeMarse, T.B., Pan, L., Alagapan, S., Brewer, G.J., and Wheeler, B.C. (2016). Feed-forward propagation of temporal and rate information between cortical populations during coherent activation in engineered in vitro networks. Front. Neural Circuits 10, 32. https://doi.org/ 10.3389/fncir.2016.00032.
- Dworak, B.J., and Wheeler, B.C. (2009). Novel MEA platform with PDMS microtunnels enables the detection of action potential propagation from isolated axons in culture. Lab Chip 9, 404–410. https://doi.org/10.1039/b806689b.
- Lewandowska, M.K., Bakkum, D.J., Rompani, S.B., and Hierlemann, A. (2015). Recording large extracellular spikes in microchannels along many axonal sites from individual neurons. PLoS One 10, e0118514. https://doi. org/10.1371/journal.pone.0118514.
- Haeb, A.-C., Olives-Verger, M., and Soriano, J. (2025). Protocol to generate PDMS topographical patterns for hiPSC-derived or rat primary neuronal cultures. STAR Protoc. 6, 104010. https://doi.org/10.1016/j.
- Shirtcliffe, N.J., Aqil, S., Evans, C., McHale, G., Newton, M.I., Perry, C.C., and Roach, P. (2004). The use of high aspect ratio photoresist (SU-8) for super-hydrophobic pattern prototyping. J. Micromech. Microeng. 14, 1384–1389. https://doi.org/10. 1088/0960-1317/14/10/013.
- Park, J.W., Vahidi, B., Taylor, A.M., Rhee, S.W., and Jeon, N.L. (2006). Microfluidic culture platform for neuroscience research. Nat. Protoc. 1, 2128–2136. https://doi.org/10.1038/ nprot.2006.316.
- Wang, S., Hesen, R., Mossink, B., Nadif Kasri, N., and Schubert, D. (2023). Generation of glutamatergic/GABAergic neuronal cocultures derived from human induced pluripotent stem cells for characterizing E/I balance in vitro. STAR Protoc. 4, 101967. https://doi.org/10.1016/j.xpro.2022.101967.
- Carter, S.-S.D., Atif, A.-R., Kadekar, S., Lanekoff, I., Engqvist, H., Varghese, O.P., Tenje, M., and Mestres, G. (2020). PDMS leaching and its implications for onchip studies focusing on bone regeneration applications. Organs-on-a-Chip 2, 100004. https://doi.org/10.1016/j.ooc.2020.100004.
- Frenzel, J., Kupferer, A., Zink, M., and Mayr, S.G. (2022). Laminin Adsorption and Adhesion of Neurons and Glial Cells on Carbon Implanted Titania Nanotube Scaffolds for Neural Implant Applications. Nanomaterials 12, 3858. https:// doi.org/10.3390/nano12213858.
- Maccione, A., Gandolfo, M., Massobrio, P., Novellino, A., Martinoia, S., and Chiappalone, M. (2009). A novel algorithm for precise identification of spikes in extracellularly recorded neuronal signals. J. Neurosci. Methods 177, 241–249. https://doi.org/10. 1016/j.jneumeth.2008.09.026.
- Wolff, R., Polito, A., Buccino, A.P., Chiappalone, M., and Tucci, V. (2025). Protocol for the enhanced analysis of electrophysiological data from high-density multi-electrode arrays with nicespike and spikeNburst. STAR Protoc. 6, 104195. https:// doi.org/10.1016/j.xpro.2025.104195.
- Murota, H., Yamamoto, H., Monma, N., Sato, S., and Hirano-Iwata, A. (2025). Precision Microfluidic Control of Neuronal Ensembles in Cultured Cortical Networks. Adv. Mater. Technol. 10, 2400894. https://doi.org/10.1002/admt. 202400894.
- Yamamoto, H., Spitzner, F.P., Takemuro, T., Buendı´a, V., Murota, H., Morante, C., Konno, T., Sato, S., Hirano-Iwata, A., Levina, A., et al. (2023). Modular architecture facilitates noisedriven control of synchrony in neuronal networks. Sci. Adv. 9, eade1755. https://doi. org/10.1126/sciadv.ade1755.