¶ 大脑类组装体中的人类小胶质细胞展现区域特异性多样性,并对携带SCN2A突变的过度兴奋神经元作出反应
¶ 小胶质细胞多样性及其在组装体中的反应
吴嘉祥1,2,9, 陈晓玲1,2,9, 张敬亮1,2,9, 凯尔·韦茨楚拉克1,2,9, 摩根·罗宾逊1,2,3, 李伟豪4, 赵元瑞1,2, 柳艺恩1,2, 布罗迪·A·戴明1,2, 阿基拉·D·阿贝亚拉特纳1,2, 阙哲夫1,2, 杜东书5, 马修·泰格迈尔2,6, 袁崇礼3, 威廉·C·斯卡恩斯7, 让-克里斯托夫·罗谢1,2, 吴隆军8, 杨阳1,2,10, *
1 博尔奇药理化学与分子药理学系,普渡大学药学院, 美国印第安纳州西拉斐特市,邮编47907
2 普渡大学整合神经科学研究所,西拉斐特市,印第安纳州 47907,美国
3 普渡大学工程学院戴维森化学工程学院,西拉斐特市,印第安纳州 47907,美国
4 复旦大学眼耳鼻喉科医院耳鼻喉科学系及耳鼻喉研究所,上海 200031,中国
5 上海大学生命科学学院,上海 200444,中国
6 普渡大学生物科学系,西拉斐特市,印第安纳州 47907,美国
5 上海大学生命科学学院,中国上海200444
6 普渡大学生物科学系,美国印第安纳州西拉斐特市47907
7 杰克逊基因组医学实验室,美国康涅狄格州法明顿市06032
8 美国得克萨斯大学休斯顿健康科学中心分子医学研究所神经免疫学与胶质细胞生物学中心,休斯顿,TX 77030,美国
9 这些作者贡献相同
10 主要联系人
*通讯作者:yangyang@purdue.edu
¶ 图文摘要
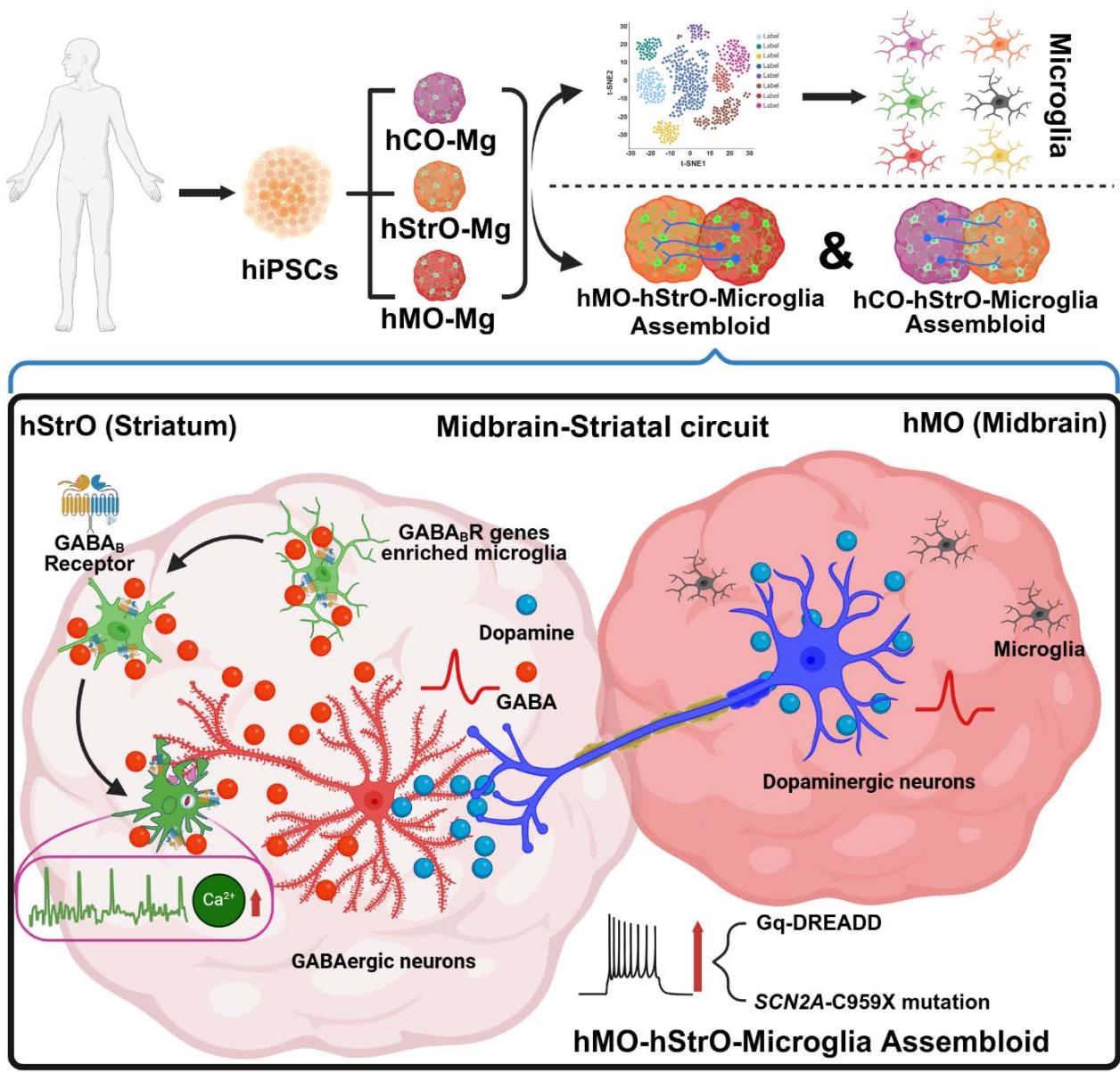
¶ 预告
建模皮质下区域的小胶质细胞区域性多样性具有挑战性。我们构建了包含小胶质细胞的人类类器官及组装体模型,这些细胞能够获得区域特异性异质性。我们的研究揭示了小胶质细胞暴露于高兴奋性的中脑-纹状体神经回路时的动态响应,为研究人类大脑发育和神经精神疾病(包括SCN2A突变介导的单基因自闭症)中的神经免疫相互作用提供了一个激动人心的平台。
¶ 亮点
-
单细胞RNA测序分析揭示了六种不同的小胶质细胞亚型,它们在人皮层、纹状体和中脑类器官中自发获得独特的专化作用。
-
小胶质细胞促进轴突投射跨越区域类器官,从而推动组装体形成。
-
小胶质细胞通过钙信号对过度兴奋的神经元作出反应,并表现出对神经元突触的过度修剪。
-
阻断小胶质细胞GABAB受体可使钙活动恢复正常并减少突触修剪,这为突触缺陷的靶向干预提供了潜在策略。
¶ 摘要
小胶质细胞对神经元环路的发育和功能具有关键塑形作用,但其在人脑不同环路中的区域特异性特征与功能仍不明确。本研究通过构建融合人源小胶质细胞的区域特异性脑类器官(皮质、纹状体、中脑),填补了这一重要空白。单细胞RNA测序揭示了六种具有独特区域标志的小胶质细胞亚型,其中一种亚型在纹状体类器官中高度富集GABAB受体基因。为探究小胶质细胞对神经环路的贡献,我们创建了整合小胶质细胞的中脑-纹状体组装体,模拟了自闭症等神经精神疾病的核心环路节点。通过化学遗传学激活该环路,我们观察到小胶质细胞中涉及GABA 受体的钙信号活动增强。利用该模型,我们进一步研究了在携带SCN2A无义突变(C959X)的神经环路中小胶质细胞的反应——该突变与重度自闭症相关。值得注意的是,小胶质细胞对SCN2A突变介导的神经元过度活跃表现出增强的钙响应,并参与过度的突触修剪。这些病理效应可通过药物抑制小胶质细胞GABA受体得到逆转。我们的研究共同建立了一个先进平台,用于解析皮层下区域的人类神经免疫互作机制,突显了小胶质细胞在塑造神经精神疾病相关关键环路中的重要作用。
¶ 关键词: 小胶质细胞,脑类器官,组装体,中脑-纹状体回路,Nav1.2
¶ 引言
小胶质细胞作为大脑的驻留免疫细胞,起源于卵黄囊中的红系髓系祖细胞,在早期胚胎发育过程中迁移至发育中的大脑,随后分化成熟{1, 2}。除了作为免疫细胞的经典功能外,小胶质细胞在调控神经元成熟、突触修剪以及跨区域神经环路构建等发育过程中发挥着不可或缺的作用{3-7}。值得注意的是,啮齿类动物研究中的新证据揭示了小胶质细胞具有显著的区域特异性特征,在不同神经环路和微环境中呈现出空间异质性并发挥独特功能{8-11}。有趣的是,批量与单细胞转录组分析进一步在啮齿动物模型中揭示了跨脑区和发育阶段、由基因表达谱定义的小胶质细胞亚群{12, 13}。尽管取得了这些进展,人类小胶质细胞(尤其是在与人类神经精神疾病高度相关的皮层下结构,如纹状体和{中脑})的区域异质性仍未得到充分探索{14, 15}。
确实,小胶质细胞功能障碍已被证实与多种神经精神疾病密切相关,包括抑郁症、精神分裂症和自闭症谱系障碍(ASD)(16-18)。在我们最近的研究中,我们在由SCN2A无义突变引起的单基因型ASD中发现小胶质细胞异常,该基因编码电压门控钠通道 (16)。通过使用ASD相关的Scn2a缺陷小鼠模型,我们进一步观察到异常的小胶质细胞介导的突触修剪现象,同时伴随突触形成缺陷和神经元过度兴奋(16,19,20)。值得注意的是,研究还发现小胶质细胞能通过改变钙信号响应过度兴奋的神经元(21,22),而钙信号已知与其吞噬活性及突触修剪功能密切相关(23)。然而,人类小胶质细胞在与ASD相关的关键中脑-纹状体神经回路中如何发挥作用,目前仍未明确。
为了填补这些空白,本研究开发了集成小胶质细胞的人类诱导多能干细胞(hiPSC)来源的类器官和装配体模型,从而能在基于人类细胞的模型中深入探索小胶质细胞的异质性与神经免疫互作。单细胞RNA测序分析识别出具有区域特异性的小胶质细胞亚型,其中纹状体小胶质细胞显著富集编码GABA受体的基因,尤其是GABAB受体。通过化学遗传学与活体钙成像技术,我们观察到纹状体小胶质细胞能对涉及GABAB受体的中脑-纹状体神经环路激活产生主动响应。借助这一先进模型,我们揭示了小胶质细胞能够响应由ASD相关SCN2A无义突变引起的过度兴奋现象,表现为钙信号升高与突触过度修剪。此外,研究发现GABA 受体的药物抑制可使小胶质细胞活动恢复基线水平并减轻抑制性突触损失,这突显了ASD神经环路功能障碍中一条新型的GABAB受体依赖调控轴。
¶ 结果
¶ hCO-Mg、hStrO-Mg 和 hMO-Mg 模型揭示了具有空间相关性的小胶质细胞不同人脑类器官的异质性
为探究人小胶质细胞在由不同神经元类型组成的各脑区中的时空特性,我们构建了区域特异性神经类器官,并与源自hiPSCs的非特化/初始态小胶质细胞共培养(图 S1A)。这些未特化的小胶质细胞随后分别与皮层、纹状体或中脑类器官共培养,建立了三种差异化模型:带小胶质细胞的人皮层类器官(hCO-Mg)、带小胶质细胞的人纹状体类器官(hStrO-Mg)及带小胶质细胞的人中脑类器官(hMO-Mg)(图1A)。这些共培养模型实现了小胶质细胞向特定脑区的浸润,使小胶质细胞能够从其局部神经环境中自然地获得区域特性。初期,小胶质细胞仅定位于类器官外周区域,但在共培养8周内实现了完全浸润与均匀分布(图1B、C)。通过特异性神经元标志物验证了类器官的区域特征:hCO-Mg采用T-box脑蛋白1(TBR1),hStrO-Mg采用γ-氨基丁酸(GABA),hMO-Mg采用酪氨酸羟化酶(TH)(图1D)。小胶质细胞形态随时间发生动态变化——从胞体较大、突起较少的形态逐渐转变为胞体缩小、分支复杂的更成熟阶段(图S2A–C)。我们的结果表明小胶质细胞已成功整合至类器官中。
为了解这些类器官内小胶质细胞的分子特征,我们进行了单细胞RNA测序(scRNA-seq)。通过对整合数据集的转录组分析,采用均匀流形逼近与投影(UMAP)方法识别出九个细胞簇。高表达的区域特异性神经元标记基因(hCO类器官的FOXG1、CAMK2A、GRIA2;hStrO类器官的PPP1R1B、DLX1、GAD1、GAD2;hMO类器官的FOXA2、SHH)验证了区域类器官的身份特征(图1E、F;S1B–I)。小胶质细胞标记基因(AIF1、CSF1R、CD68)在UMAP图中清晰标识出小胶质细胞簇(图1G)。进一步亚聚类分析揭示了六个不同的小胶质细胞亚群(簇a-f)(图1H、I):簇a(H-CP-MG)以DUSP1、CEBPD{24, 25}为标记;簇b(H-SR-MG)表达刺激响应基因JUN、FOS;簇c(H-GR-MG)富集谷氨酸相关基因GRIK2、GRIA2;簇d(H-IR-MG)以免疫响应基因VSIR、IL1B为特征;簇e(H-PR-MG)表达突触修剪基因DKK2、C1QB、FCN1;簇f(H-CC-MG)代表表达TOP2A、MKI67的早期发育阶段小胶质细胞(图1K)。
为进一步评估区域性小胶质细胞的异质性,我们检测了不同类器官中小胶质细胞亚群的分布情况。结果显示显著的富集模式(图1J、K):集群a主要存在于hCO-Mg( )中,并高表达TGFBR2、DOCK8、IGF1和GPNMB基因。通过基因本体(GO)分析,这些基因与增强的增殖能力相关。集群b在 ( )中显著富集,并显示NTRK2、SLC1A3和BNIP3基因的高表达。GO分析表明这些基因参与神经元兴奋性与突触可塑性的调控。集群d主要分布于hMO-Mg( ),显著表达ALOX5AP、PTGS2和MALT1基因,提示其特化的免疫调节功能。 此外,与先前研究提示GABA信号参与小胶质细胞活动及抑制性神经环路形成的结论一致(文献26),hStrO-Mg小胶质细胞整体呈现多种GABA受体相关基因(GABBR1、GABRB1、GABRA2)的富集表达模式(图1M;S2D–F)。特别是集群b(H-SR-MG)主导表达这些GABA受体相关基因(图1L),这与hStrO中丰富的GABA能神经元分布相关联,暗示该类小胶质细胞与GABA能神经元群体之间存在功能交互。 综上,我们的研究为皮质、纹状体及中脑类器官在转录水平上存在区域特异性小胶质细胞异质性提供了有力证据,反映了空间关联的小胶质细胞功能多样性。
小胶质细胞促进轴突投射并增强类器官组装体的形成啮齿动物研究已证明小胶质细胞在塑造神经连接中的关键作用 ,既能影响局部神经回路{v*}(9, 26),也能调控跨脑区投射 。然而,小胶质细胞在基于人类细胞的神经回路模型中的功能仍 largely 未获探索。鉴于纹状体主要接收来自皮质谷氨酸能神经元和中脑多巴胺能神经元的投射,我们通过将人纹状体类器官与小胶质细胞融合形成组装体模型,重构这些神经回路——分别与人类皮质类器官或人类中脑类器官融合构建(图2A)。在成功制备皮质-纹状体-小胶质细胞组装体和中脑-纹状体-在小胶质细胞类组装体(hMO-hStrO-Mg)中,通过标志物表达确认了区域特异性:皮质类器官使用TBR1和CTIP2标志,纹状体类器官使用GAD67和DRD1标志,中脑类器官则使用FOXA2和OTX2标志(图2B)。此外,我们通过皮质-纹状体类组装体中进行GABA/IBA1共免疫染色,以及中脑-纹状体类组装体中进行TH/IBA1共免疫染色,验证了各类组装体在融合后均保持小胶质细胞的存在,从而确认了神经元与小胶质细胞的整合(图2C、D)。
中脑多巴胺能神经元向纹状体神经元的投射形成了一个经典环路,该环路与多种神经精神疾病相关(14)。然而,小胶质细胞对此环路的具体作用尚不明确。为阐明其机制,我们利用来自基因编辑hiPSC系(在AAVS安全位点导入钙离子传感器GCaMP6f)的小胶质细胞,构建了中脑-纹状体组装体(hMO-hStrO-Mg)(图2E、F)。采用GCaMP6f标记的小胶质细胞,能够实现对组装体内小胶质细胞及其钙动力学的活体追踪。在融合前,中脑类器官通过pAAV-hSyn-mScarlet标记以清晰显影中脑区域。免疫染色结果证实GCaMP6f标记的小胶质细胞成功整合入组装体,IBA1与GCaMP6f信号共定位指标明确(图2G)。
融合后活体成像显示,随着时间的推移,mScarlet标记的中脑到纹状体轴突投射逐渐增加(图2H、J)。值得注意的是,在小胶质细胞整合的组装体中,小胶质细胞在第10天时在融合界面处出现初始聚集,随后在后期阶段重新分布。此外,含有小胶质细胞的组装体与不含小胶质细胞的组装体相比,mScarlet标记的轴突投射显著增强(图2H、J),同时融合成功率也显著更高(图2I)。综上,我们的小胶质细胞整合组装体模型研究结果表明,小胶质细胞能主动促进轴突投射,显著增强神经组装的效率,从而推动中脑-纹状体环路的功能整合。
小胶质细胞对hMO-hStrO组装体中hStrO区域神经元活动增强产生响应小胶质细胞已知能对神经元活动的变化作出动态反应(29, 30)。在研究小胶质细胞如何感知人脑中脑-纹状体环路内的神经元活动之前,我们首先通过实验验证了hMO-hStrO组装体的功能连接性。我们采用化学遗传学方法,通过用pAAV-hSyn-hM3(Gq)-mCherry转导hMO-Mg神经元,实现Gq-DREADD介导的hMO神经元激活,这些神经元向hStrO发送轴突投射。随后将这些转导的hMO-Mg与hStrO-Mg融合形成组装体(图3A)。利用高密度多电极阵列(HD-MEA),我们在施加10 M氯氮平N-氧化物(CNO)激活hMO中Gq-DREADD后记录神经活动。正如预期,CNO直接显著增强了hMO区域的神经元放电(图3C左,3D)。值得注意的是,这种增强的活动被有效传递至hStrO区域,表现为hStrO神经元放电同步增加,从而证实了组装体内功能性中脑-纹状体连接的存在(图3C右,3D)。
神经元活动可诱导小胶质细胞钙动力学变化(23)。鉴于先前研究提示小胶质细胞GABA 受体参与调节钙活动(31),结合我们的scRNA-seq数据显示表达GABBR1的小胶质细胞在hStrO区富集,我们在hStrO区域对IBA1与 (GABBR1,即GABAB受体亚基)进行了免疫染色。IBA1与 的共定位证实了GABAB受体存在于小胶质细胞(图3E)。随后我们利用中脑-纹状体回路内源性表达的钙传感器GCaMP6f,探究GABA 受体如何参与hStrO区小胶质细胞的钙动力学。在基础状态下,hStrO区小胶质细胞胞体与突起均表现出极低的自发性钙活动(图3F、H–K)。在CNO诱导环路激活时,我们观察到hStrO内小胶质细胞胞体及突起的钙信号显著增强(图3F, H–K)。随后我们施加了CGP 55845盐酸盐,使用选择性GABAB受体拮抗剂CGP阻断GABAB受体后,我们观察到显著效果:在hStrO区域,CGP处理能显著抑制由CNO诱发的小胶质细胞胞体及突起中钙信号水平的升高(图3G,H–K)。鉴于GABAB受体在神经元中同样表达,我们进一步评估了CGP是否影响神经元兴奋性。虽然hStrO神经元在CGP处理后呈现兴奋性增强趋势,但该变化未达到统计学显著性(图S3A–F),提示我们观测到的效应主要源于小胶质细胞。综上,我们的数据表明阻断GABAB受体能显著减弱纹状体神经元活动增强所诱发的小胶质细胞钙响应。这一发现与既往研究相符——即小胶质细胞可通过GABA信号感知神经元活动,并可能参与抑制性突触的塑造过程。
¶ 小胶质细胞通过GABAB受体依赖性钙信号和过度突触修剪对超兴奋性SCN2A-C959X组装体作出反应
中脑-纹状体回路与自闭症谱系障碍(ASD)密切相关(15)。我们先前在小鼠模型中的研究表明,Scn2a缺失会破坏突触传递并触发小胶质细胞活化,导致突触吞噬增加和神经元可塑性受损(16,32)。然而,在携带ASD致病性SCN2A突变的人源中脑-纹状体组装体中,小胶质细胞的作用仍不清楚。为填补这一空白,我们建立了携带杂合型SCN2A无义突变(C959X)的hMO-hStrO-Mg模型(图4A),该突变此前在重度ASD患者中被发现(33, 34)。电生理分析显示,与同基因野生型(WT)对照组相比,CX组装体的网络活动显著增强(图S4),这与SCN2A缺失的皮质-纹状体组装体中观察到的过度活跃现象一致(35)。为进一步评估神经元兴奋性,我们对hStrO区域的棘状中型神经元(MSNs)进行了膜片钳记录。结果显示,CX组装体中的MSNs表现出电流诱发动作电位放电显著增加(图4B、C),证实了SCN2A缺失情况下中脑-纹状体回路存在过度兴奋的表型。
考虑到小胶质细胞钙信号对神经元活动的敏感性,我们采用实时活细胞钙成像技术监测hStrO区域的小胶质细胞反应(图4D, E)。鉴于已有研究证实SCN2A是一种神经元特异性基因,在小胶质细胞中表达极低(参考文献22),我们采用野生型GaMP6f标记的小胶质细胞来探究其如何在CX中脑-纹状体类组装体中感知神经元过度兴奋状态。与野生型类组装体相比,CX类组装体中的小胶质细胞在胞体和突起均表现出显著增强的钙活动(图4F, G)。小胶质细胞对突触的过度修剪已被证实与多种神经精神疾病相关(参考文献36)。为探究CX类组装体中的小胶质细胞是否导致模型出现突触功能障碍,我们进行了VGAT、IBA1和CD68的三重免疫荧光染色。通过Imaris软件进行三维重建与容积分析显示,CX类组装体中小胶质细胞的溶酶体容积显著增加(图4J),并对VGAT阳性的抑制性突触前末梢吞噬作用增强(图4K),表明抑制性突触遭受过度修剪。此外,使用CGP 55845对GABAB受体进行药理抑制能显著降低CX类组装体中小胶质细胞的钙信号传导。值得注意的是,这种钙活动减弱伴随着VGAT吞噬减少(图4D–G),最终可能缓解SCN2A缺陷中型多棘神经元的突触缺陷。综上,我们的研究证明小胶质细胞可通过涉及GABAB受体的钙信号通路响应SCN2A-C959X诱导的神经元过度活跃,并执行抑制性突触的过度修剪。这些结果揭示了一种导致基于人类细胞构建的ASD模型,并指出一种针对小胶质细胞GABA信号传导的潜在干预策略。
¶ 讨论
脑类器官和组装体在过去十年中迅速发展,使得在三维结构组织的人类细胞中研究神经发育和神经精神疾病成为可能。尽管小胶质细胞在调节神经元功能和神经环路中至关重要(37),但小胶质细胞的区域特异性身份及其在皮层下回路中的作用仍 largely 未知。本研究通过单细胞RNA测序技术,揭示了独特的区域特异性小胶质细胞亚型,其中纹状体小胶质细胞在GABAB受体基因中表现出显著富集。利用化学遗传学结合活细胞钙成像技术,我们证明这些纹状体小胶质细胞能动态响应中脑-纹状体回路中升高的神经元活动。重要的是,我们发现小胶质细胞还能通过增强钙信号传导和进行过度的突触修剪,响应携带自闭症致病性SCN2A蛋白截短变异体C959X的过度兴奋神经回路。此外,药理抑制GABAB受体能有效使小胶质细胞活性正常化,并减轻神经元抑制性突触的丢失。我们的研究由此证明了一个强大平台在理解小胶质细胞在人类脑回路和神经精神疾病中作用的实用性。
啮齿类动物及人类尸检组织研究显示,小胶质细胞具有区域特异性表型,包括独特的形态、细胞密度及基因/蛋白表达谱(38, 39)。这种区域特异性特征被认为是由发育时序、局部神经元特性及微环境信号共同塑造的(8-10, 12, 13, 40, 41)。这些动态局部信号可能促使小胶质细胞执行与突触修剪相关的特定功能,并根据局部环境促进神经环路成熟与轴突投射。鉴于目前对小胶质细胞多样性的认知主要来自啮齿类模型或人类尸检组织,本研究通过构建人脑神经环路模型来探索人类小胶质细胞的特性和功能,填补了关键空白。通过单细胞转录组分析,我们在三种区域特异性脑类器官中鉴定出六个不同的小胶质细胞亚型,每个区域都表现出独特的亚群分布特征。值得注意的是,我们发现的三个亚型(a、b和f)与早期发育阶段人脑组织观察到的小胶质细胞群体存在一定对应关系(39),这强化了本平台在模拟人脑发育中小胶质细胞行为的实用性。特别需要指出的是,hStrO-Mg中的小胶质细胞以b型为主,其GABAB受体基因表达显著富集。考虑到纹状体内富含GABA能神经元,这一发现尤为有趣。值得注意的是,该结果也与小鼠研究证据一致——区域性微环境(如富含GABA或谷氨酸的神经环路)会驱动小胶质细胞亚型转换(29, 42)。综上,我们认为这种新型人源细胞模型提供了一个先进研究平台,结合动物模型和人体组织研究,能够全面阐释不同脑区及物种中小胶质细胞亚型的功能。
已知小胶质细胞通过修剪突触来调节神经元网络兴奋性{29} 。特别是,先前研究发现小胶质细胞能够抑制化学诱发癫痫小鼠模型及携带癫痫相关基因突变的人类细胞中的神经元过度兴奋{22, 30, 43}。值得注意的是,研究还发现小胶质细胞钙动力学与其吞噬功能以及神经元兴奋性的监测调节密切相关{21, 23}。尽管这些发现令人振奋,但现有技术存在局限——目前仅能对二维培养/脑切片(缺乏完整长程环路连接)或表层皮质中的小胶质细胞进行活体成像由于活体双光子显微镜成像深度的限制,这些区域的研究受到制约(21,44)。因此,我们目前的平台为研究皮层下回路中的人类小胶质细胞提供了一种补充性方法。值得注意的是,我们在中脑-纹状体回路中的发现与已发表的结果一致,即在过度兴奋的环境中,小胶质细胞表现出钙信号升高,并在自闭症/癫痫疾病模型中执行突触的过度修剪(16,22)。除了验证已发表的结果外,我们的研究还揭示了人源纹状体类器官中存在一群富含γ-氨基丁酸 的小胶质细胞。我们进一步证明,钙信号升高和突触过度修剪都依赖于小胶质细胞的γ-氨基丁酸B受体,这为了解人类小胶质细胞在调节神经元兴奋性方面的区域特异性功能提供了新的见解,而现有模型很可能无法揭示这一机制。
我们的研究可能存在若干局限性:1)我们的组装体系统缺乏血管成分。然而,已知脑血管系统具有维持稳态并影响小胶质细胞发育与功能的作用(45, 46)。2)虽然本系统能够模拟经典的中脑至纹状体长程轴突投射,但纹状体神经元本身也应具备向其他脑区延伸的长程轴突投射(47-49),这是当前系统未能模拟的。3)我们提出小胶质细胞表达的GABAB受体对介导其钙动力学及突触修剪至关重要。通过药理学阻断GABA 受体,我们观察到小胶质细胞Ca2+响应大幅减弱,且突触过度修剪现象减少。已有研究表明小胶质细胞GABAB受体参与其吞噬功能(26),这支持了我们的发现。但显然GABA 受体同样在神经元中表达,药理试剂也可能同时阻断神经元GABA 受体。我们认为神经元GABAB受体不太可能主导所观察到的效应,因为理论上阻断神经元GABAB受体会增强神经元兴奋性,进而提升小胶质细胞对神经元过度活跃的感知并强化钙信号传导。与此相反,我们的数据显示药理学阻断GABAB受体后小胶质细胞钙动力学显著减弱,这支持了以小胶质细胞为主导的作用机制。
总之,我们的研究建立了一个先进平台,为探索小胶质细胞在神经回路中的功能及其在人类疾病中的功能障碍提供了巨大潜力。尤其令人振奋的是,人脑中小胶质细胞的空间异质性可以通过基于人类细胞的脑类器官和组装体在体外进行部分模拟。我们的发现使得能够详细探索不同脑区(包括历史上受体内成像技术访问限制的皮层下区域)小胶质细胞可能存在的多样化作用。此外,我们的模型允许在基于人类细胞的系统中对小胶质细胞进行活细胞成像和精确的实验操作,从而推动我们对小胶质细胞生物学及其在人类神经精神疾病中作用的理解。
¶ 致谢
我们感谢普渡大学的亚当·金布罗博士(Dr. Adam Kimbrough)慷慨提供Imaris软件的访问权限。本研究中报告的工作得到了美国国立卫生研究院(NIH)国家神经疾病和中风研究所(NINDS)的部分支持(授予Y.Y.的R01NS117585和R01NS123154)。X.C.获得了美国癫痫学会(AES)博士后研究奖学金的支持。作者衷心感谢FamilieSCN2A基金会对Y.Y.获得霍奇金-赫胥黎奖(Hodgkin-Huxley Award)的支持,以及对X.C.、J.Z.和Y.E.Y.的动作电位资助(Action Potential Grant)的支持。作者感谢普渡大学杨实验室所有其他成员富有见地的讨论。
¶ 作者贡献
J.W. 和 Y.Y. 构思并设计了实验。J.W.、X.C.、J.Z.、K.W. 和 M.R. 执行实验并分析了数据。W.C.S.设计并进行了 SCN2A 基因编辑实验。W.L. 和 Y.Z. 参与了数据分析。Y.-E.Y.、B.D.、A.A. 和 Z.Q.参与了实验执行。D.D.、M.T.、C.Y.、W.S.、J.-C.R. 和 L.-J.W. 参与了实验设计。Y.Y. 指导了本项目。J.W.、J.Z. 和 Y.Y. 在全体作者的共同参与下撰写了手稿。
¶ 利益冲突声明作者声明不存在利益冲突。
生成式人工智能和人工智能辅助技术在写作过程中的使用声明在本次著作的撰写过程中,作者使用了ChatGPT 4.5来提升文稿的可读性和语言表达,同时确保主要结论保持不变。使用此工具后,作者对措辞进行了必要的审阅和编辑,并对出版物的内容承担全部责任。
¶ 参考文献
¶ 文献列表
- F. Ginhoux, M. Guilliams. 组织驻留巨噬细胞的发生与稳态[J]. 免疫, 2016, 44: 439–449.
- F. Ginhoux, S. Lim, G. Hoeffel, D. Low, T. Huber. 小胶质细胞的起源与分化[J]. 细胞神经科学前沿, 2013, 7: 45.
- M. Andoh, K. Shibata, K. Okamoto, J. Onodera, K. Morishita, Y. Miura, Y. Ikegaya, R. Koyama. 运动逆转母体炎症后的行为与突触异常[J]. 细胞报告, 2019, 27: 2817–2825 e2815.
- F. Filipello, R. Morini, I. Corradini, V. Zerbi, A. Canzi, B. Michalski, M. Erreni, M. Markicevic, C. Starvaggi-Cucuzza, K. Otero, L. Piccio, F. Cignarella, F. Perrucci, M. Tamborini, M. Genua, L. Rajendran, E. Menna, S. Vetrano, M. Fahnestock, R. C. Paolicelli, M. Matteoli. 小胶质细胞先天免疫受体TREM2是突触清除与正常脑连接所必需的[J]. 免疫, 2018, 48: 979–991 e978.
- H. J. Kim, M. H. Cho, W. H. Shim, J. K. Kim, E. Y. Jeon, D. H. Kim, S. Y. Yoon. 小胶质细胞自噬缺陷损害突触修剪并导致社交行为缺陷[J]. 分子精神病学, 2017, 22: 1576–1584.
- Y. Zhan, R. C. Paolicelli, F. Sforazzini, L. Weinhard, G. Bolasco, F. Pagani, A. L. Vyssotski, A. Bifone, A. Gozzi, D. Ragozzino, C. T. Gross. 神经元-小胶质细胞信号缺失导致脑功能连接与社交行为受损[J]. 自然神经科学, 2014, 17: 400–406.
- M. Jin, R. Xu, L. Wang, M. M. Alam, Z. Ma, S. Zhu, A. C. Martini, A. Jadali, M. Bernabucci, P. Xie, K. Y. Kwan, Z. P. Pang, E. Head, Y. Liu, R. P. Hart, P. Jiang. I型干扰素信号驱动人类iPSC唐氏综合征与阿尔茨海默病模型中小胶质细胞功能障碍与衰老[J]. 细胞干细胞, 2022, 29: 1135–1153 e1138.
- A. S. Warden, S. A. Wolfe, S. Khom, F. P. Varodayan, R. R. Patel, M. Q. Steinman, M. Bajo, S. E. Montgomery, R. Vlkolinsky, T. Nadav, I. Polis, A. J. Roberts, R. D. Mayfield, R. A. Harris, M. Roberto. 小胶质细胞控制酒精依赖小鼠饮酒行为的升级:基因组与突触驱动因素[J]. 生物精神病学, 2020, 88: 910–921.
- Y. J. Liu, E. E. Spangenberg, B. Tang, T. C. Holmes, K. N. Green, X. Xu. 清除小胶质细胞增强成年小鼠皮层神经环路连接与活动[J]. 神经科学杂志, 2021, 41: 1274–1287.
- A. L. Ribeiro Xavier, B. T. Kress, S. A. Goldman, J. R. Lacerda de Menezes, M. Nedergaard. 侧脑室下区存在支持成年神经发生的小胶质细胞特殊群体[J]. 神经科学杂志, 2015, 35: 11848–11861.
- M. Ueno, Y. Fujita, T. Tanaka, Y. Nakamura, J. Kikuta, M. Ishii, T. Yamashita. 出生后发育期间第五层皮层神经元需要小胶质细胞支持以维持存活[J]. 自然神经科学, 2013, 16: 543–551.
- K. Grabert, T. Michoel, M. H. Karavolos, S. Clohisey, J. K. Baillie, M. P. Stevens, T. C. Freeman, K. M. Summers, B. W. McColl. 小胶质细胞具有脑区依赖性多样性及对衰老的区域选择性敏感[J]. 自然神经科学, 2016, 19: 504–516.
- T. R. Hammond, C. Dufort, L. Dissing-Olesen, S. Giera, A. Young, A. Wysoker, A. J. Walker, F. Gergits, M. Segel, J. Nemesh, S. E. Marsh, A. Saunders, E. Macosko, F. Ginhoux, J. Chen, R. J. M. Franklin, X. Piao, S. A. McCarroll, B. Stevens. 小鼠全生命周期及脑损伤中小胶质细胞的单细胞RNA测序揭示复杂的细胞状态变化[J]. 免疫, 2019, 50: 253–271 e256.
- A. A. Grace. 多巴胺系统失调在精神分裂症与抑郁症病理生理中的作用[J]. 自然综述·神经科学, 2016, 17: 524–532.
- P. E. Rothwell, M. V. Fuccillo, S. Maxeiner, S. J. Hayton, O. Gokce, B. K. Lim, S. C. Fowler, R. C. Malenka, T. C. Sudhof. 与自闭症相关的neuroligin-3突变通常损害纹状体环路,从而加剧重复行为[J]. Cell, 2014, 158: 198–212.
- J. Wu, J. Zhang, X. Chen, K. Wettschurack, Z. Que, B. A. Deming, M. I. Olivero-Acosta, N. Cui, M. Eaton, Y. Zhao, S. M. Li, M. Suzuki, I. Chen, T. Xiao, M. S. Halurkar, P. Mandal, C. Yuan, R. Xu, W. A. Koss, D. Du, F. Chen, L. J. Wu, Y. Yang. 在自闭症相关的SCN2A缺陷小鼠和人脑类器官发育过程中,小胶质细胞对突触的过度修剪[J]. Mol Psychiatry, 2024, 29: 2424–2437.
- H. Wang, Y. He, Z. Sun, S. Ren, M. Liu, G. Wang, J. Yang. 抑郁症中的小胶质细胞:小胶质细胞在抑郁症发病机制和治疗中的作用概述[J]. J Neuroinflammation, 2022, 19: 132.
- C. Zhuo, H. Tian, X. Song, D. Jiang, G. Chen, Z. Cai, J. Ping, L. Cheng, C. Zhou, C. Chen. 精神分裂症中的小胶质细胞与认知障碍:将科学进展转化为新型治疗干预[J]. Schizophrenia (Heidelberg), 2023, 9: 42.
- J. Zhang, M. Eaton, X. Chen, Y. Zhao, S. Kant, B. A. Deming, K. Harish, H. P. Nguyen, Y. Shu, S. Lai, J. Wu, Z. Que, K. W. Wettschurack, Z. Zhang, T. Xiao, M. S. Halurkar, M. I. Olivero-Acosta, Y.-E. Yoo, N. A. Lanman, W. A. Koss, W. C. Skarnes, Y. Yang. 恢复兴奋/抑制平衡可提高神经元信噪比并挽救自闭症相关Scn2a缺陷的社交障碍[J]. bioRxiv, 2025: 2025.2003.2004.641498.
- M. Eaton, J. Zhang, Z. Ma, A. C. Park, E. Lietzke, C. M. Romero, Y. Liu, E. R. Coleman, X. Chen, T. Xiao, Z. Que, S. Lai, J. Wu, J. H. Lee, S. Palant, H. P. Nguyen, Z. Huang, W. C. Skarnes, W. A. Koss, Y. Yang. 一种具有电压门控钠通道Na(v)1.2表达大幅降低的Scn2a基因陷阱敲除小鼠模型的构建与基础表征[J]. 基因、大脑与行为, 2021, 20: e12725.
- A. D. Umpierre, L. L. Bystrom, Y. Ying, Y. U. Liu, G. Worrell, L. J. Wu. 清醒小鼠中小胶质细胞钙信号与神经元活动相协调[J]. 生命, 2020, 9.
- Z. Que, M. I. Olivero-Acosta, M. Robinson, I. Chen, J. Zhang, K. Wettschurack, J. Wu, T. Xiao, C. M. Otterbacher, V. Shankar, H. Harlow, S. Hong, B. Zirkle, M. Wang, N. Cui, P. Mandal, X. Chen, B. Deming, M. Halurkar, Y. Zhao, J. C. Rochet, R. Xu, A. L. Brewster, L. J. Wu, C. Yuan, W. C. Skarnes, Y. Yang. 人iPSC来源的小胶质细胞感知并抑制携带癫痫相关SCN2A-L1342P突变的皮层神经元的过度兴奋性[J]. 神经科学杂志:神经科学学会官方期刊, 2024, 45.
- A. D. Umpierre, B. Li, K. Ayasoufi, W. L. Simon, S. Zhao, M. Xie, G. Thyen, B. Hur, J. Zheng, Y. Liang, D. B. Bosco, M. A. Maynes, Z. Wu, X. Yu, J. Sung, A. J. Johnson, Y. Li, L. J. Wu. 小胶质细胞P2Y(6)钙信号促进吞噬作用并塑造癫痫发生中的神经免疫应答[J]. 神经元, 2024, 112: 1959–1977 e1910.
- V. Barbaro, A. Testa, E. Di Iorio, F. Mavilio, G. Pellegrini, M. De Luca. C/EBPδ调节人角膜缘干细胞的细胞周期和自我更新[J]. 细胞生物学杂志, 2007, 177: 1037–1049.
- J. Shen, Y. Zhang, H. Yu, B. Shen, Y. Liang, R. Jin, X. Liu, L. Shi, X. Cai. DUSP1/MKP1在肿瘤发生、进展和治疗中的作用[J]. 癌症医学, 2016, 5: 2061–2068.
- E. Favuzzi, S. Huang, G. A. Saldi, L. Binan, L. A. Ibrahim, M. Fernandez-Otero, Y. Cao, A. Zeine, A. Sefah, K. Zheng, Q. Xu, E. Khlestova, S. L. Farhi, R. Bonneau, S. R. Datta, B. Stevens, G. Fishell. GABA能响应的小胶质细胞选择性塑造发育中的抑制性神经回路[J]. 细胞, 2021, 184: 4048–4063 e4032.
- D. P. Schafer, E. K. Lehrman, A. G. Kautzman, R. Koyama, A. R. Mardinly, R. Yamasaki, R. M. Ransohoff, M. E. Greenberg, B. A. Barres, B. Stevens. 小胶质细胞以活动和补体依赖的方式塑造出生后神经回路[J]. 神经元, 2012, 74: 691–705.
- S. Deivasigamani, M. T. Miteva, S. Natale, D. Gutierrez-Barragan, B. Basilico, S. Di Angelantonio, L. Weinhard, D. Molotkov, S. Deb, C. Pape, G. Bolasco, A. Galbusera, H. Asari, A. Gozzi, D. Ragozzino, C. T. Gross. 小胶质细胞补体信号促进神经元清除和正常脑功能连接[J]. 大脑皮层, 2023, 33: 10750–10760.
- S. Zhao, A. D. Umpierre, L. J. Wu. 通过成年脑中小胶质细胞调节神经回路和行为[J]. 神经科学趋势, 2024, 47: 181–194.
- A. D. Umpierre, L. J. Wu. 小胶质细胞如何感知和调节神经元活动[J]. 神经胶质, 2021, 69: 1637–1653.
- F. Logiacco, P. Xia, S. V. Georgiev, C. Franconi, Y. J. Chang, B. Ugursu, A. Sporbert, R. Kuhn, H. Kettenmann, M. Semtner. 小胶质细胞在出生后早期海马中通过GABA感知神经元活动[J]. 细胞报告, 2021, 37: 110128.
- J. Zhang, X. Chen, M. Eaton, J. Wu, Z. Ma, S. Lai, A. Park, T. S. Ahmad, Z. Que, J. H. Lee, T. Xiao, Y. Li, Y. Wang, M. I. Olivero-Acosta, J. A. Schaber, K. Jayant, C. Yuan, Z. Huang, N. A. Lanman, W. C. Skarnes, Y. Yang. 电压门控钠通道Na(V)1.2的严重缺陷会提高成年小鼠的神经元兴奋性[J]. 细胞报告, 2021, 36: 109495.
- S. J. Sanders, M. T. Murtha, A. R. Gupta, J. D. Murdoch, M. J. Raubeson, A. J. Willsey, A. G. Ercan-Sencicek, N. M. DiLullo, N. N. Parikshak, J. L. Stein, M. F. Walker, G. T. Ober, N. A. Teran, Y. Song, P. El-Fishawy, R. C. Murtha, M. Choi, J. D. Overton, R. D. Bjornson, N. J. Carriero, K. A. Meyer, K. Bilguvar, S. M. Mane, N. Sestan, R. P. Lifton, M. Gunel, K. Roeder, D. H. Geschwind, B. Devlin, M. W. State. 全外显子组测序揭示的新生突变与自闭症密切相关[J]. 自然, 2012, 485: 237–241.
- F. K. Satterstrom, J. A. Kosmicki, J. Wang, M. S. Breen, S. De Rubeis, J. Y. An, M. Peng, R. Collins, J. Grove, L. Klei, C. Stevens, J. Reichert, M. S. Mulhern, M. Artomov, S. Gerges, B. Sheppard, X. Xu, A. Bhaduri, U. Norman, H. Brand, G. Schwartz, R. Nguyen, E. E. Guerrero, C. Dias, C. Autism Sequencing, P.-B. C. i, C. Betancur, E. H. Cook, L. Gallagher, M. Gill, J. S. Sutcliffe, A. Thurm, M. E. Zwick, A. D. Borglum, M. W. State, A. E. Cicek, M. E. Talkowski, D. J. Cutler, B. Devlin, S. J. Sanders, K. Roeder, M. J. Daly, J. D. Buxbaum. 大规模外显子组测序研究揭示自闭症神经生物学中发育与功能变化的共同作用[J]. 细胞, 2020, 180: 568–584 e523.
- X. Chen, J. Zhang, J. Wu, M. J. Robinson, H. Kothandaraman, Y.-E. Yoo, I. M. G. Dopeso-Reyes, T. D. Buffenoir, M. S. Halurkar, Z. Zhang, M. Wang, E. N. Creager, Y. Zhao, M. I. Olivero-Acosta, K. W. Wettschurack, Z. Que, C. Yuan, A. J. Schaser, N. A. Lanman, J.-C. Rochet, W. C. Skarnes, E. J. Kremer, Y. Yang. 自闭症相关SCN2A缺陷破坏人类脑组装体中的皮质-纹状体神经回路[J]. bioRxiv, 2025: 2025.2006.2002.657036.
- S. Hong, V. F. Beja-Glasser, B. M. Nfonoyim, A. Frouin, S. Li, S. Ramakrishnan, K. M. Merry, Q. Shi, A. Rosenthal, B. A. Barres, C. A. Lemere, D. J. Selkoe, B. Stevens. 补体与小胶质细胞介导阿尔茨海默病小鼠模型早期突触丧失[J]. 科学(纽约), 2016, 352: 712–716.
- T. R. Hammond, D. Robinton, B. Stevens. 小胶质细胞与大脑:发育与疾病中的互补伙伴[J]. 细胞发育生物学年度评论, 2018, 34: 523–544.
- Y. L. Tan, Y. Yuan, L. Tian. 小胶质细胞的区域异质性及其在大脑中的作用[J]. 分子精神病学, 2020, 25: 351–367.
- Y. Li, Z. Li, M. Yang, F. Wang, Y. Zhang, R. Li, Q. Li, Y. Gong, B. Wang, B. Fan, C. Wang, L. Chen, H. Li, J. Ong, Z. Teng, L. Jin, Y. L. Wang, P. Du, J. Jiao. 解码发育中人脑小胶质细胞的时空特异性[J]. 细胞干细胞, 2022, 29: 620–634 e626.
- 刘洋、周丽君、王静、李丹、任文静、彭晶、魏晓、徐婷、辛文静、庞瑞萍、李媛媛、秦朝华、穆鲁甘、马特森、吴丽君、刘晓光. TNF-α通过周围神经损伤后小胶质细胞依赖机制在海马和脊髓中差异性调节突触可塑性[J]. 神经科学杂志, 2017, 37: 871–881.
- 增田贵志、桑科夫斯基、斯塔舍夫斯基、博特切尔、阿曼、萨加尔、沙伊韦、内斯勒、孔茨、范洛、科恩、赖纳赫、米歇尔、苏尔、戈尔德、格伦、普里勒、斯塔德尔曼、普林茨. 单细胞分辨率下小鼠和人小胶质细胞的时空异质性[J]. 自然, 2019, 566: 388–392.
- 恰普斯基、斯特罗斯纳杰. 阿尔茨海默病中小胶质细胞-神经元交叉对话中的谷氨酸和GABA[J]. 国际分子科学杂志, 2021, 22.
- 李旭、刘晶、博雷兰、卡帕迪亚、张珊、斯蒂利塔诺、阿博、克拉克、赖洋、刘洋、巴尔、迈尔斯、卡马拉詹、匡文、阿格拉瓦尔、斯莱辛格、迪克、萨尔瓦托雷、蒂施菲尔德、段健、埃登伯格、克雷默、哈特、庞志平. 酒精使用障碍的多基因风险影响人类小胶质细胞模型对乙醇暴露的细胞反应[J]. 科学进展, 2024, 10: eado5820.
- 达米萨、希尔、拉伊、陈飞、罗斯林、高希、格鲁岑德勒. 体内神经元尸体清除过程中星形胶质细胞和小胶质细胞发挥协同作用并尊重吞噬边界[J]. 科学进展, 2020, 6: eaba3239.
- 蒙多、贝克尔、考茨曼、席费雷尔、贝尔、陈健、黄爱珍、西蒙斯、谢弗. 血管旁小胶质细胞动态及其与脉管系统相互作用的发育分析[J]. 神经科学杂志, 2020, 40: 6503–6521.
- 诺普、班克斯、埃里克森. 小胶质细胞与血管血脑屏障的物理关联及其在发育、健康和疾病中的重要性[J]. 神经生物学当前观点, 2022, 77: 102648.
- 布洛姆利、布拉奇. P物质使纹状体投射神经元去极化并促进其谷氨酸能输入[J]. 生理学杂志, 2008, 586: 2143–2155.
- 塔韦尔纳、伊利吉奇、苏迈尔. 纹状体中等多棘神经元的回返侧支连接在帕金森病模型中被破坏[J]. 神经科学杂志, 2008, 28: 5504–5512.
- 比什特、奥科吉、夏尔马、伦特费林克、孙洋洋、陈浩然、乌韦鲁、阿曼切拉、卡尔库塔瓦拉、坎波斯-萨拉查、科利斯、贾布尔、本德罗特、弗里斯特德、米尔斯三世、艾萨克森、特伦布莱、关春燕、埃约. 小鼠中毛细血管相关小胶质细胞通过PANX1-P2RY12耦合调控血管结构和功能[J]. 自然通讯, 2021, 12: 5289.
- 斯卡恩斯、佩莱格里诺、麦克多诺. 提高人类干细胞中同源定向修复效率[J]. 方法, 2019, 164-165: 18–28.
- 斯卡恩斯、宁、詹西拉库萨、克鲁兹、布劳文德拉特、萨维德拉、霍尔登、库克森、沃德、麦克多诺. 使用dCas9控制人类干细胞中的同源定向修复结果[J]. bioRxiv, 2021: 2021.2012.2016.472942.
- 潘塔齐斯、杨、拉腊、麦克多诺、布劳文德拉特、彭、小黒、金谷屋、邹、塞贝斯塔、普拉特、克罗斯、布洛克威克、巴克斯顿、金纳-比博、梅杜拉、汤普金斯、休斯、桑蒂亚纳、法格里、诺尔斯、维塔莱、巴拉德、齐亚阳、拉莫斯、安德森、施塔德勒、纳拉扬、帕帕德梅特里欧、赖利、尼尔森、阿加瓦尔、罗森、基尔万、皮苏帕蒂、库恩、肖尔茨、普里布、奥特、董健、梅杰尔、詹森、洛伦索、范德坎特、克鲁修斯、帕凯、劳林、布、赫尔德、韦因格、加布里埃尔、凯西、雷、阿布-邦斯拉、帕里什、M. S. 贝卡里、D. W. 克利夫兰、E. 李、I. V. L. 罗斯、M. 坎普曼、C. 卡拉塔尤德·阿里斯托伊、P. 韦斯特雷肯、L. 海因里希、M. Y. 陈、B. 舒勒、D. 杜、E. L. F. 霍尔茨鲍尔、M. C. 扎内拉蒂、R. 巴森德拉、M. 德什穆克、S. 科恩、R. 坎纳、M. 拉曼、Z. S. 内文、M. 马蒂亚、J. 范伦特、V. 蒂默曼、B. R. 康克林、K. 约翰逊·蔡斯、K. 张、S. 富内斯、D. A. 博斯科、L. 埃勒巴赫、M. 韦尔泽、D. 克朗伯格-费尔斯特格、G. 吕、E. 阿雷纳斯、E. 科恰、L. 萨拉法、T. 阿费尔特、J. C. 马里奥尼、W. C. 斯卡恩斯、M. R. 库克森、M. E. 沃德、F. T. 默克尔. 用于大规模合作研究的参考人诱导多能干细胞系[J]. 细胞干细胞, 2022, 29: 1685–1702 e1622.
- S. P. 帕斯卡、P. 阿洛塔、H. S. 贝特普、J. G. 坎普、S. 卡佩洛、F. H. 盖奇、J. A. 克诺布利希、A. R. 克里格斯坦、M. A. 兰开斯特、G. L. 明、G. 诺瓦里诺、H. 冈野、M. 帕尔马、I. H. 帕克、O. 赖纳、H. 宋、L. 斯图德、J. 高桥、S. 坦普尔、G. 泰斯塔、B. 特罗伊特莱因、F. M. 瓦卡里诺、P. 范德哈根、T. 扬-皮尔斯. 神经类器官、类组装体及移植研究的框架[J]. 自然, 2025, 639: 315–320.
- Y. 三浦、M. Y. 李、O. 雷瓦、S. J. 尹、G. 楢崎、S. P. 帕斯卡. 构建脑类组装体以探究人类神经回路[J]. 自然实验手册, 2022, 17: 15–35.
- J. 赵、Y. 肖、A. X. 孙、E. 楚库罗格鲁、H. D. 陈、J. 郭克、Z. Y. 陈、T. Y. 肖、C. P. 陈、H. 洛克曼、Y. 李、D. 金、H. S. 高、S. O. 金、J. H. 朴、N. J. 赵、T. M. 海德、J. E. 克莱曼、J. H. 申、D. R. 温伯格、E. K. 陈、H. S. 齐、H. H. 吴. 源自人多能干细胞的类中脑器官包含功能性多巴胺能及神经黑色素生成神经元[J]. 细胞干细胞, 2016, 19: 248–257.
- A. 麦克奎德、M. 布勒顿-琼斯. 人诱导多能干细胞衍生小胶质细胞[J]. 分子生物学方法, 2022, 2454: 473–482.
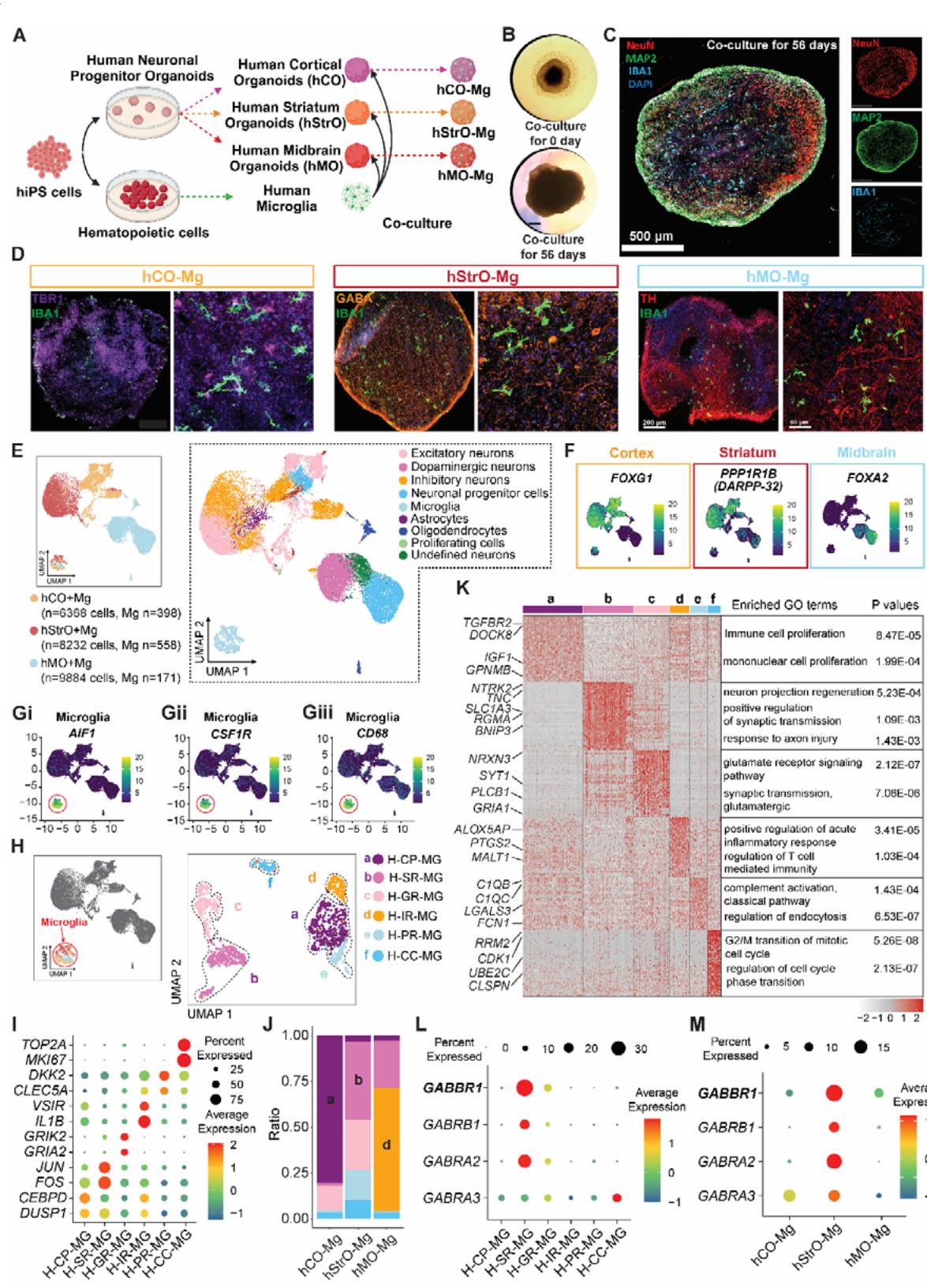
图1
图1:hCO-Mg、hStrO-Mg和hMO-Mg模型揭示了不同人脑类器官中空间分布各异的小胶质细胞异质性。(A) 生成包含小胶质细胞的三维人皮质类器官(hCO-Mg)、人纹状体包含小胶质细胞的人纹状体类器官( )以及包含小胶质细胞的人中脑类器官(hMO-Mg)。 (B) 纹状体类器官与小胶质细胞共培养0天和56天的代表性明场图像。比例尺: 。 © 纹状体类器官与小胶质细胞共培养56天后的代表性四重染色图像(NeuN、Map2、IBA1和DAPI)。比例尺: 。 (D) hCO-Mg(TBR1和IBA1)、 (GABA和IBA1)和hMO-Mg(TH和IBA1)的代表性图像。全尺寸图像(0.5倍)比例尺: ,放大图像(20倍)比例尺: 。(E) 整合的hCO-Mg、hStrO-Mg和hMO-Mg的均匀流形逼近与投影(UMAP)图。 (F和G) 大脑皮质标记物FOXG1、纹状体标记物PPP1R1B、中脑标记物FOXA2以及(Gi-Giii)小胶质细胞标记物AIF1、CSF1R和CD68的UMAP可视化。 (H) 分为6个簇的小胶质细胞的UMAP可视化。H:人,MG:小胶质细胞,CP:细胞增殖,SR:刺激反应,GR:谷氨酸相关反应,IR:免疫反应,PR:修剪反应,CC:细胞周期。 (I) 点图显示每个小胶质细胞簇选定标记物的百分比。 (J) 小胶质细胞簇在不同脑区类器官模型中的分布。 (K) 热图展示各小胶质细胞簇的前50个基因。左侧突出显示与主要类型相关的差异基因,右侧为富集的基因本体论术语。 (L和M) 点图显示GABA受体基因在(L)不同小胶质细胞簇及(M)不同脑区类器官小胶质细胞中的百分比与平均表达量。
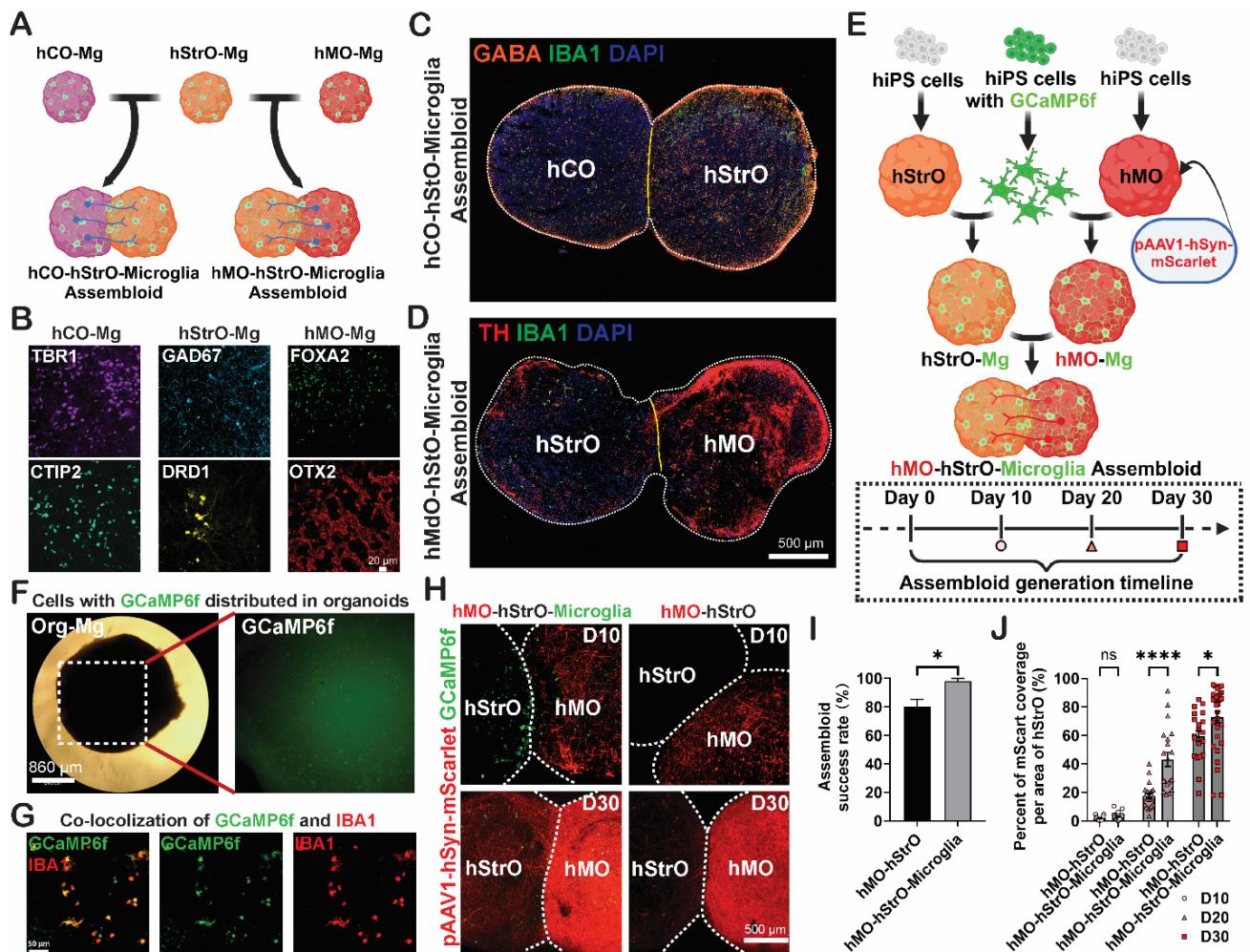
图2
图2。小胶质细胞促进不同脑区间轴突投射并推动类组装体形成。(A) 类组装体模型中整合小胶质细胞的皮层-纹状体通路与中脑-纹状体通路示意图。(B) 区域特异性标志物免疫染色:hCO-Mg(TBR1与CTIP2)、hStrO-Mg(GAD67与DRD1)、hMO-Mg(FOXA2与OTX2)。比例尺: 。(C与D) 三维类组装体代表性图像:© hCO-hStrO-小胶质体与(D) hMO-hStrO-小胶质体。比例尺:5 。(E) 采用GCaMP6f hiPS细胞系生成小胶质细胞及AAV1进行顺向病毒示踪的hMO-hStrO-小胶质类组装体示意图(上);类组装体制备时间轴示意图(下)。(F) 类器官-小胶质模型中出现强GCaMP6f信号的代表性图像。比例尺: 。(G)代表性图像展示类器官-小胶质细胞模型中小胶质细胞携带GCaMP6f信号。比例尺:50 微米。(Hμ)代表性图像显示第10天和第30天不同组的中脑纹状体投射及GCaMP6f+细胞存在情况。比例尺:500 微米。(I)不同组间类器官组装成功率的量化分析。采用非配对学生t检验, 批次。 (*)。(J) 不同组中hStrO每单位面积mScart覆盖率的量化。非配对学生t检验,第10天的hMO-hStrO与hMO-hStrO-小胶质细胞组: 个组装类器官;第20天的hMO-hStrO与hMO-hStrO-小胶质细胞组: 个组装类器官;第30天hMO-hStrO组: 个组装类器官,第30天hMO-hStrO-小胶质细胞组: 个组装类器官。 (*), (****),ns:无显著性差异。数据以均值±标准误表示。
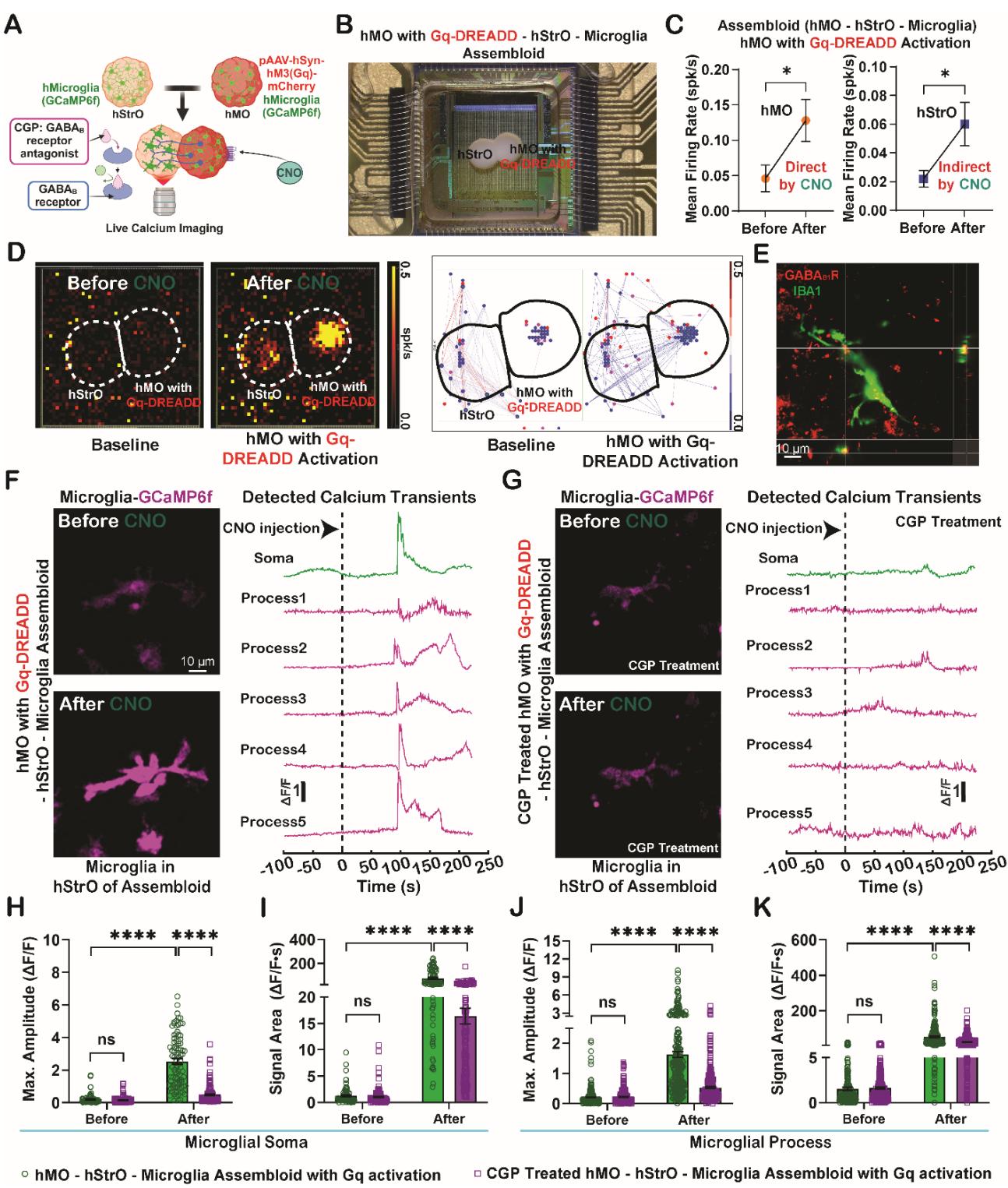
图 3
图 3. 通过CGP拮抗GABAB受体可减弱组装体hStrO区小胶质细胞对神经元活动增强的反应。(A) 示意图展示CNO暴露后对hStrO区小胶质细胞进行活体钙成像。(B) 位于3-脑高密度微电极阵列(HD-MEA)上的hMO-hStrO-小胶质细胞组装体代表性图像系统。使用Gq-DREADD转导hMO区域。(C)在Gq-DREADD激活(CNO暴露)前后,对携带Gq-DREADD的hStrO-小胶质细胞组装体中的hMO区域和hStrO区域平均放电率进行量化。采用非配对Student’s t检验, 个组装体。p < 0.05 (*)。(D) 在Gq-DREADD激活(CNO暴露)前后,通过高清微电极阵列记录在含有Gq-DREADD-hStrO-小胶质细胞组装体的hMO中获取的代表性热图(左)和代表性神经元连接图(右)。(E) 含有Gq-DREADD-hStrO-小胶质细胞组装体的hMO中hStrO区域小胶质细胞的代表性正交图像。三张图中的每个十字标记从三个角度显示GABBR1标记标注的小胶质细胞GABAB受体。比例尺: 微米。(F) Gq-DREADD激活(CNO暴露)前后,含有Gq-DREADD-hStrO-小胶质细胞组装体的hMO中hStrO区域小胶质细胞的钙活动(GCaMP6f)(左)及检测到的小胶质细胞钙瞬变的代表性 F/F曲线(右)。比例尺: 微米。(G) 经GABAB受体拮抗剂CGP处理的、含有Gq-DREADD-hStrO-小胶质细胞组装体的hMO中,Gq-DREADD激活(CNO暴露)前后hStrO区域小胶质细胞的钙活动(GCaMP6f)(左)及检测到的小胶质细胞钙瞬变的代表性 F/F曲线(右)。(H和I) Gq-DREADD激活(CNO暴露)前后不同组别中小胶质细胞胞体钙信号的最大振幅(H)和信号面积(I)量化。每组: 个小胶质细胞胞体/20个组装体。(J和K) Gq-DREADD激活(CNO暴露)前后不同组别中小胶质细胞突起钙信号的最大振幅(H)和信号面积(I)量化。每组: 个小胶质细胞突起/20个组装体。双因素方差分析, (****),ns:无显著性差异。
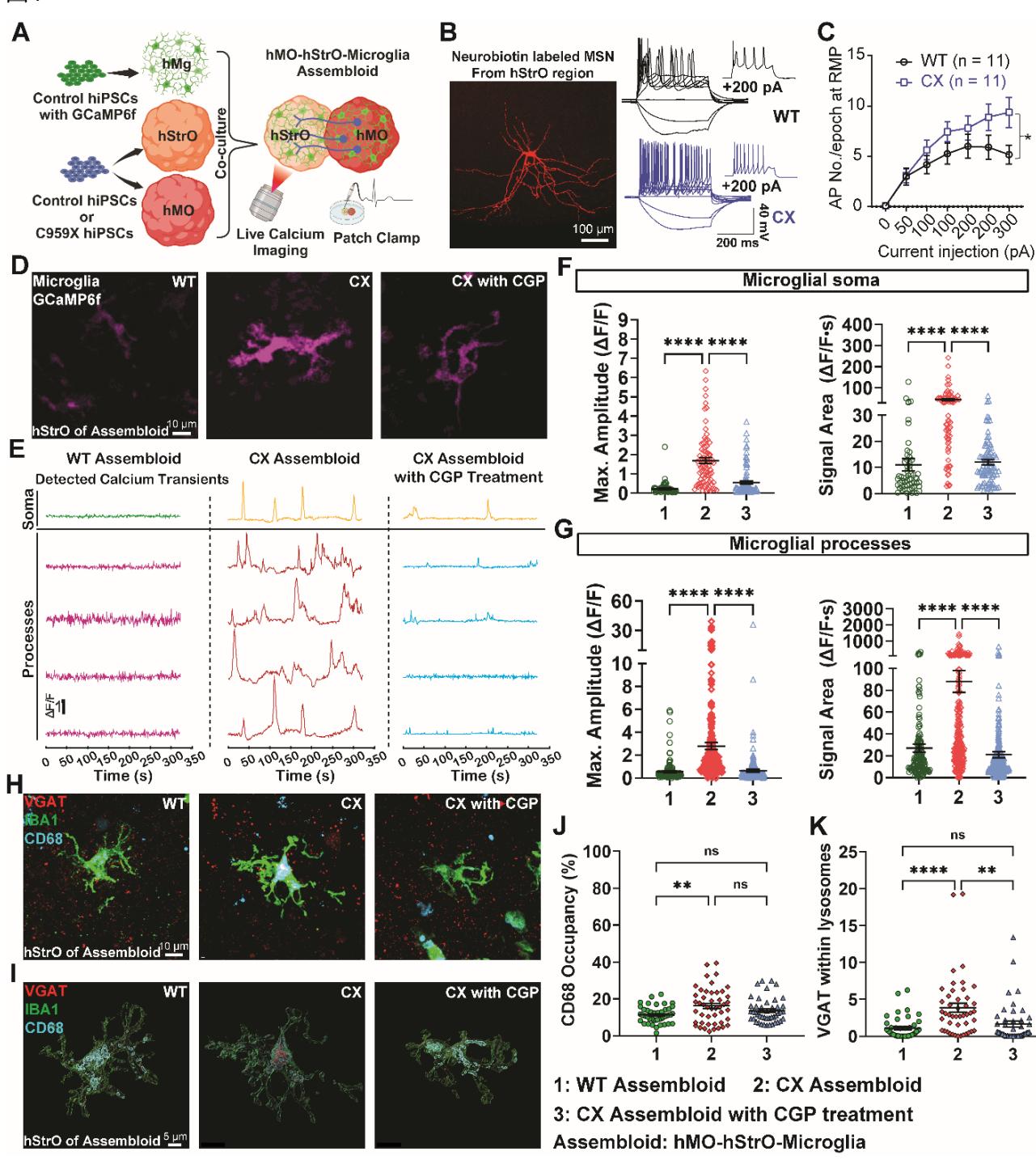
图4
图 4. 小胶质细胞通过改变钙信号传导和过度修剪突触,对携带自闭症致病性 SCN2A 突变的过度兴奋的类组装体作出反应。(A) 发育中含小胶质细胞的 SCN2A C959X 突变类组装体示意图。(B) 神经生物素标记的典型中等多棘神经元(MSN)及各组MSN的代表性电流钳记录。比例尺:10 。(C)去极化电流脉冲诱发的平均动作电位(AP)数量。采用非配对双尾非参数曼-惠特尼U检验对各电流脉冲进行组间比较,每组 。 (***)。(D)各组(WT组、SCN2A C959X突变组及SCN2A组)hMO-hStrO-小胶质细胞组装体hStrO区的小胶质细胞钙活动(GCaMP6f)C959X突变体与CGP组。(E) 各组小胶质细胞钙瞬变的代表性 检测结果。(F) 不同组别小胶质细胞胞体钙信号最大振幅与信号面积的量化分析。WT类组装体: 个胞体/15个类组装体;CX类组装体: 个胞体/20个类组装体; 组: 个胞体/20个类组装体。单因素方差分析, 。(G) 不同组别小胶质细胞突触钙信号最大振幅与信号面积的量化分析。WT类组装体: 个突触/15个类组装体;CX类组装体: 个突触/20个类组装体; 组: 个突触/20个类组装体。单因素方差分析, 。(H与I) 各组代表性三重染色图像(VGAT、IBA1与CD68)(H)及Imaris重构图像 。比例尺: 。(J与K) 各组CD68阳性占比 (J)及溶酶体内VGAT的量化分析 。WT类组装体: 个细胞/9个类组装体;CX类组装体: 个细胞/9个类组装体; 组: 个细胞/9个类组装体。单因素方差分析, , ,ns:无显著性差异。
补充图1
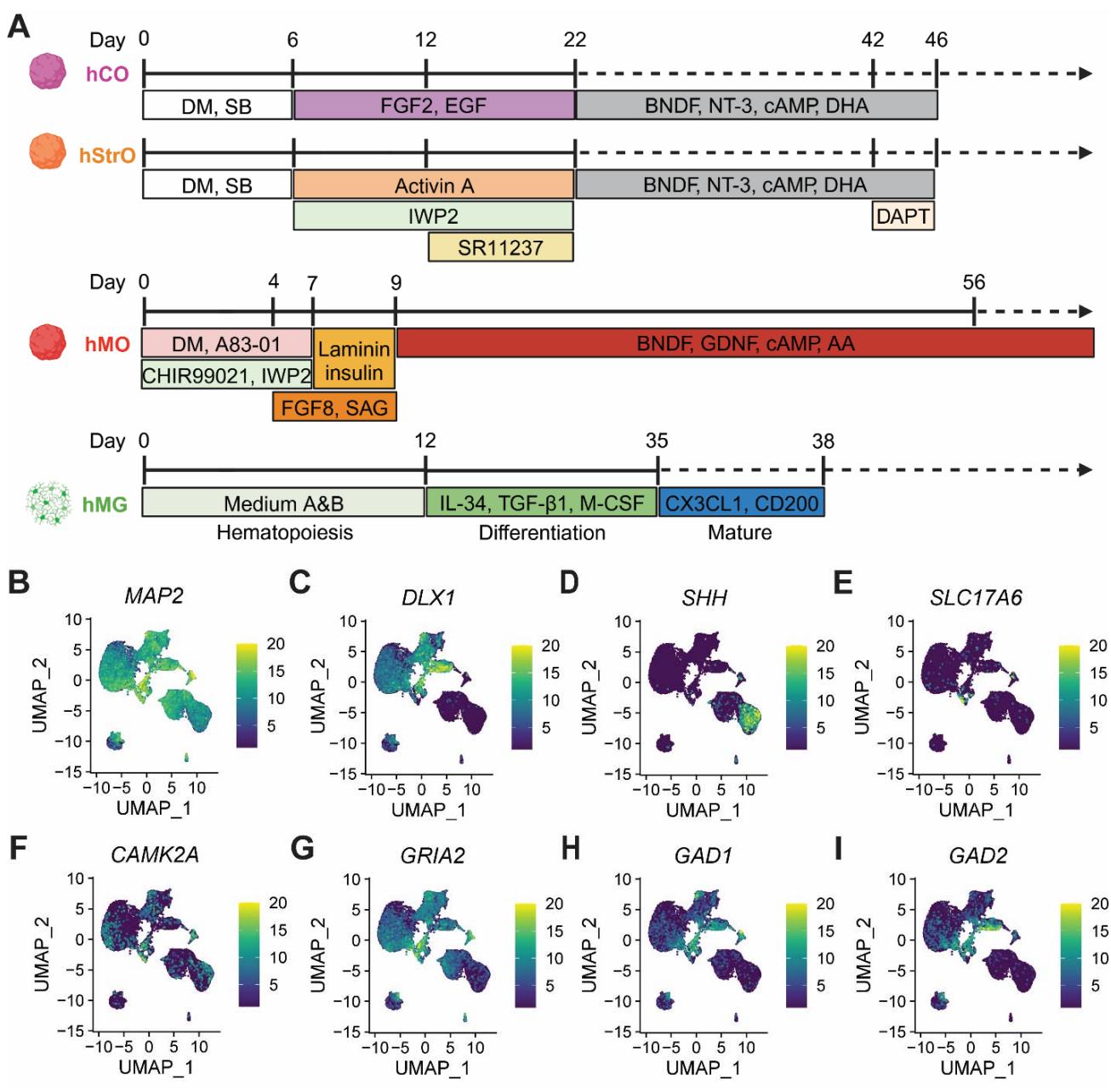
s-图1. 小胶质细胞整合的大脑区域特异性类器官的实验方案及单细胞分析。 不同人脑类器官模型的分化方案示意图。hCO(人皮层类器官)、 (人纹状体类器官)、hMO(人中脑类器官)、hMG(人小胶质样细胞)。 展示不同类器官模型中各细胞群体关键标志基因表达的UMAP图谱。 MAP2:泛神经元标志物,在分化神经元中富集。 DLX1:GABA能中间神经元标志物,提示纹状体及抑制性神经元特征。 SHH:Sonic hedgehog信号通路,对中脑及腹侧前脑模式形成至关重要。 SLC17A6(VGLUT2):兴奋性谷氨酸能神经元标志物。 CAMK2A:兴奋性皮层投射神经元的突触后标志物。 GRIA2:AMPA受体亚基,提示兴奋性神经传递。 GAD1:参与γ-氨基丁酸合成的酶,标记抑制性GABA能神经元。 GAD2:另一种γ-氨基丁酸合成酶,标记抑制性中间神经元。
补充图2
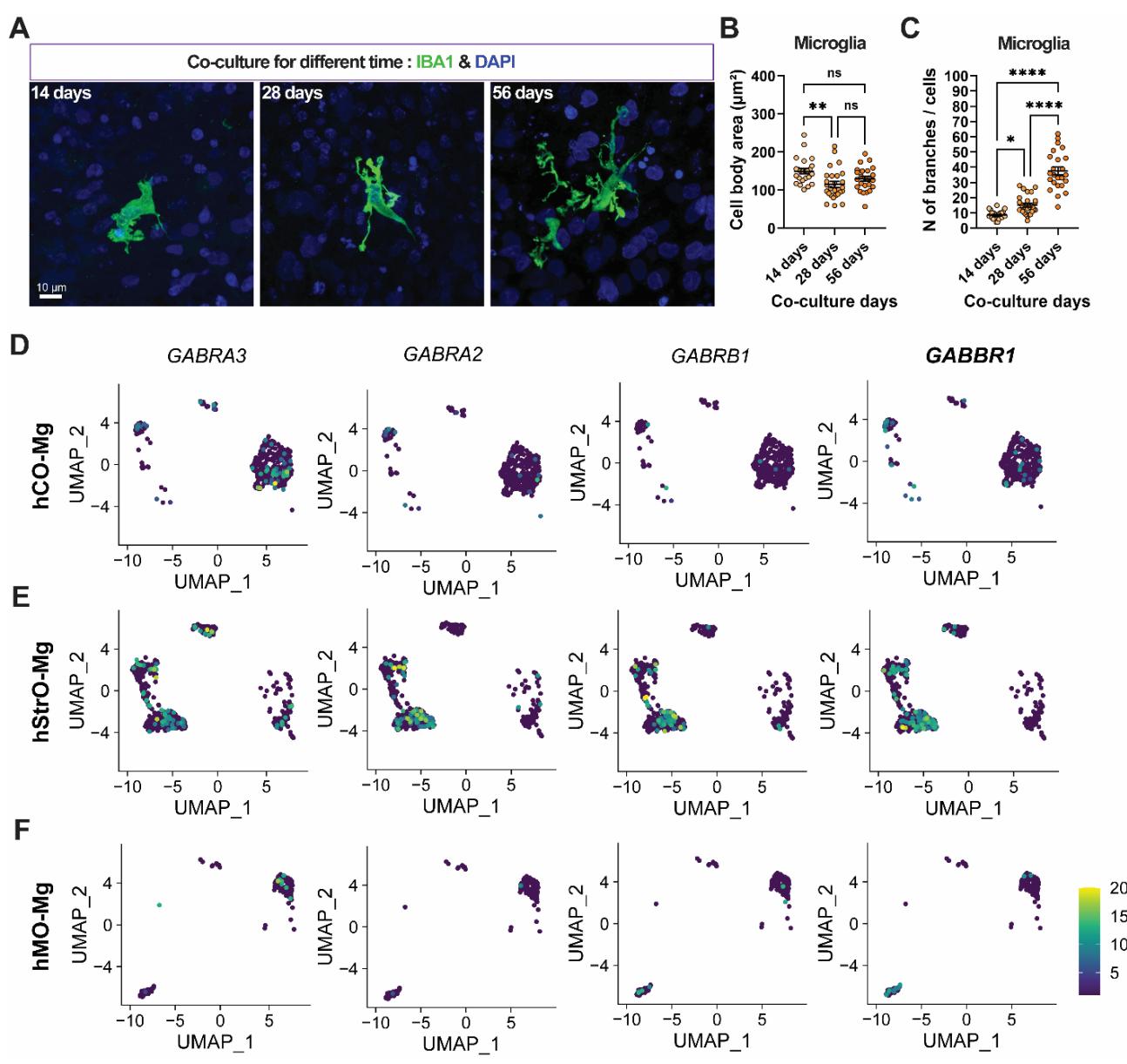
s-图2. 纹状体小胶质细胞的成熟度随共培养时间延长而增加,及其GABA相关受体基因的分布。(A) 组中随共培养时间增加的代表性小胶质细胞形态。比例尺: 。(B和C)各组小胶质细胞胞体面积和分支数量的量化。共培养时间:14天组: 个细胞/12个类器官;28天组:n 个细胞/12个类器官;56天组: 个细胞/12个类器官。单因素方差分析, (*), 0.01(**), (***), (****),ns:无显著性。(D)hCO-Mg单细胞RNA测序分析中,小胶质细胞UMAP内GABA受体相关基因的表达与分布。(E) 单细胞RNA测序分析中,小胶质细胞UMAP内GABA受体相关基因的表达与分布。(F)hMO-Mg单细胞RNA测序分析中,小胶质细胞UMAP内GABA受体相关基因的表达与分布。
补充图3
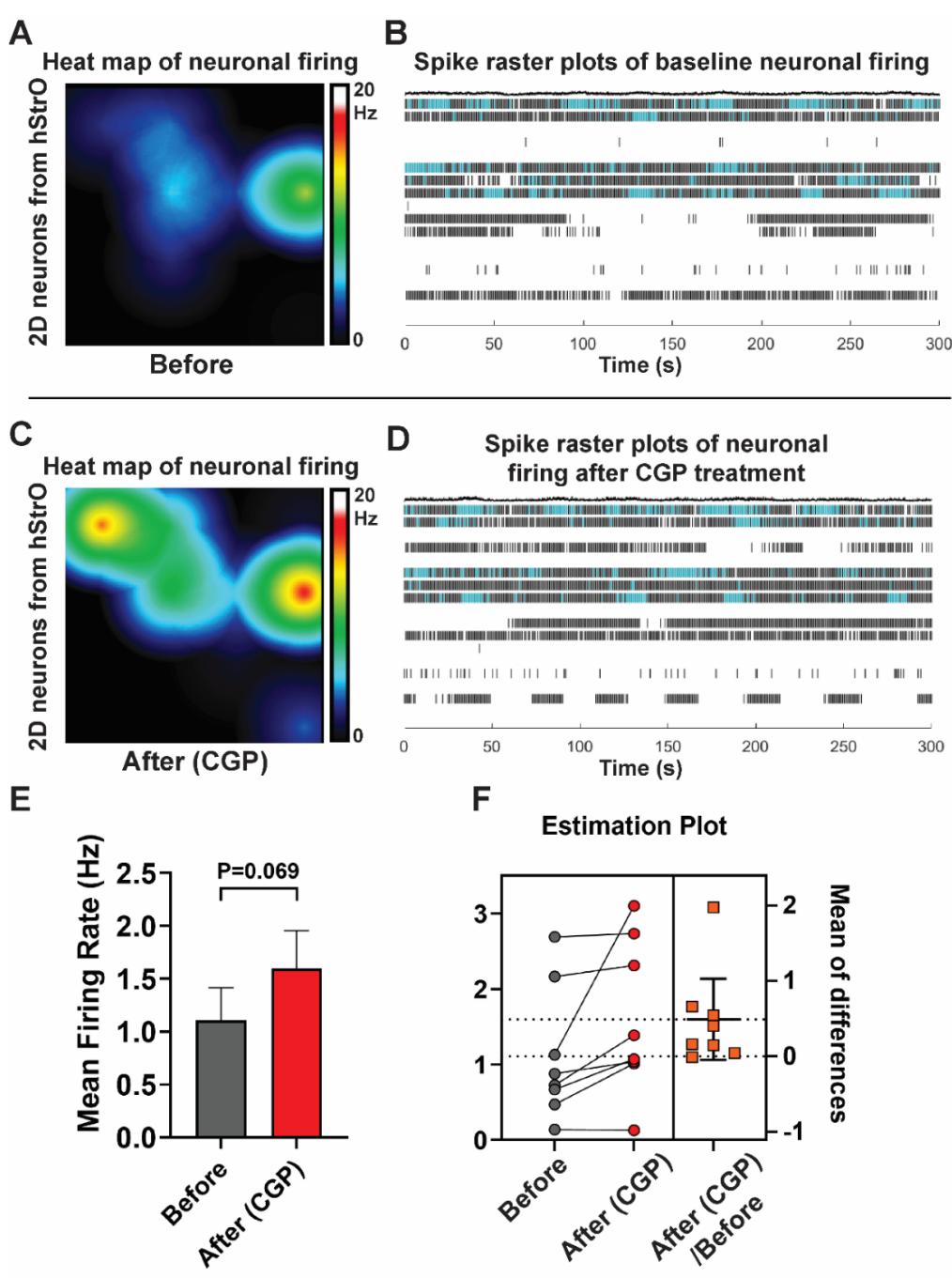
s-图3. CGP处理仅对神经元兴奋性产生有限影响。(A和C)神经元放电的代表性热图,包括CGP处理前(A)和后©。(B和D)代表性的峰电位点阵图,包括CGP处理前(B)和后(D)。每行对应单个电极在300秒内记录的神经元峰电位,每个刻度标记代表一次自发事件。爆发事件由蓝色高亮的刻度簇表示。(E)CGP处理前后平均放电频率(MFF)的量化比较。 个孔。配对Student’s t检验, 。(F)左图:MEA记录显示的神经元平均放电频率(含CGP处理前后)。右图:受试者内差异,实心水平线代表差异均值。
补充图 4
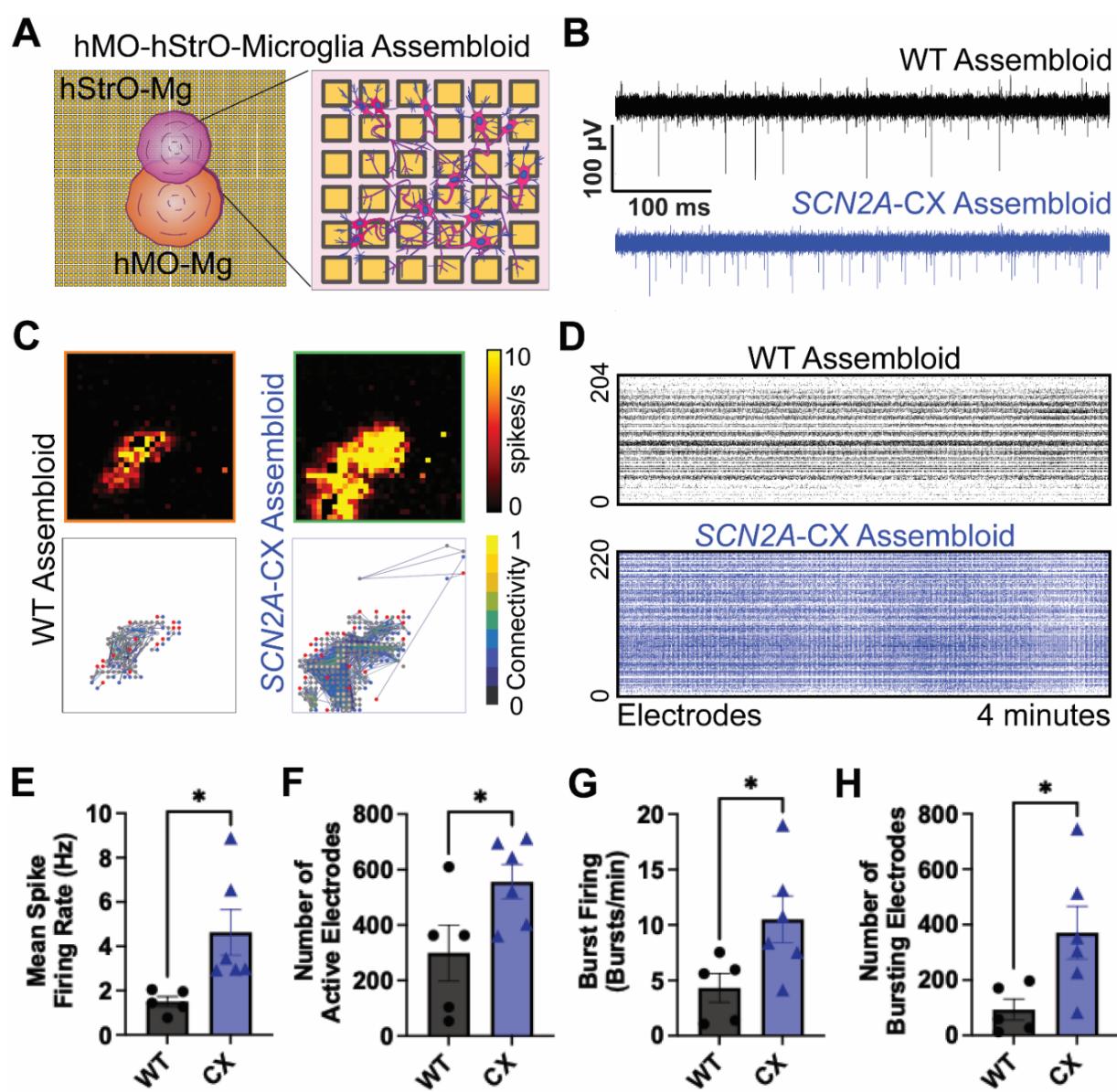
s-图4. SCN2A-C959X导致hMO-hStrO-小胶质细胞类组装体出现网络过度兴奋。(A) 共培养系统示意图,显示中脑类器官(橙色)和纹状体类器官(粉色)接种于高密度微电极阵列上(插图显示单个电极及互连的放大视图)。(B) 单个电极记录到的野生型组(黑色)和SCN2A C959X突变组(蓝色)的原始电压迹线示例;注意SCN2A C959X突变组的放电频率增加。© 通过HD-MEA在野生型组和SCN2A C959X突变组中记录到的尖峰活动代表性热图(尖峰数/秒)(上图)和代表性神经元连接图(下图)。(D) 野生型组(黑色)和SCN2A C959X突变组(蓝色)网络中,汇总自~424个电极的尖峰栅格图,时间跨度为4分钟。每行代表一个电极;每个标记点代表一个检测到的尖峰。(E) 平均尖峰发放频率(赫兹)的量化。(F) 野生型组与SCN2A C959X突变组中“活跃”电极的数量。(G) 簇状放电频率(簇/分钟)。(H) “簇状放电”电极的数量,定义为显示簇状放电活动的电极。E-H,野生型组n 个类组装体,CX组 个类组装体。非配对t检验,条形图显示均值± SEM; )。
¶ 方法
¶ 生成来源于hiPS细胞的类器官(hCO、hStrO和hMO)细胞
SCN2A c.2877C>A (p.Cys959Ter) 突变型 hiPSC 系系采用 CRISPR/Cas9 介导的基因组编辑技术(50,51) 在早期传代(p2)KOLF2.1J 参照 iPSCs(52) 中构建而成。我们重新进行了多能性检测与基因组完整性表征,以确保 hiPSC 的质量(53)。实验共使用五个 hiPSC 系:三个同源对照系(KOLF2.1J、B07 WT 和 B11 WT)以及两个杂合型 SCN2A-C959X 系(A02 HET、E04 HET)。hiPSC 克隆每日于 StemFlex 培养基(Gibco, A3349401)中维持培养,随后以 100 细胞/ 升的密度在 Essential 8培养基(Gibco, A1517001)中聚集形成球状胚状体。胚状体在圆底超低吸附板(Corning Costar, CLS7007)中通过 离心 3 分钟促进其形成。胚状体随后在 Essential 6 培养基(Gibco, A1516401)中培养前 6 天。
为生成人脑类器官,参照所述方法,首先将拟胚体在E6培养基中维持6天,同时添加靶向激活素/节点蛋白/TGF- 和BMP通路抑制剂:多索吗啡( ,Sigma-Aldrich,P5499)与SB-4321542( ,R&D Systems,1614),以及XAV-939( ,Tocris,3748),通过DUAL-SMAD方法诱导神经元分化。随后收集拟胚体,转移至平底六孔悬浮培养板(Corning,3471),并在Neurobasal-A基础培养基(Thermo Fisher Scientific,10888022)中培养,培养基添加Glutamax(Gibco,35050061)、青霉素-链霉素( ,Gibco,15140163)及不含维生素A的B27补充剂(Gibco,12587010),同时加入 人重组FGF2(R&D Systems,233-FB-500)和 mL EGF(R&D Systems,236-EG)。前17天每日完全更换培养基,之后每两天更换直至第23天。随后将补充剂更换为含 BDNF(PeproTech,450-02)、 NT3(PeproTech,450-03)、 cAMP(Santa Cruz,sc-201567A)、 DHA(顺式-4,7,10,13,16,19-二十二碳六烯酸)(MilliporeSigma,D2534)和 AA(L-抗坏血酸-2-磷酸三钠盐)(Wako,323-44822)的配方,每两天更换培养基直至第46天。此后将类器官在仅含 补充剂(无额外生长因子)的Neurobasal-A基础培养基中维持培养至第150天,每4-5天更换培养基。
对于hStrO的生成,遵循了先前概述的方案(54)。第6天,将EB转移到由Neurobasal-A、不含维生素A的B-27、GlutaMAX和青霉素-链霉素组成的神经培养基中。该培养基还添加了 IWP-2(一种WNT通路抑制剂;Selleck Chemicals, S7085)和 重组Activin A(PeproTech, 120-14P)。第11天,在现有补充剂基础上加入视黄醇X受体激动剂SR11237( , Tocris, 3411)。从第22天开始,为促进神经祖细胞向神经元分化,培养基进一步添加 BDNF、 NT-3、 AA、 cAMP和 。自第42日起,在BDNF、NT-3、AA、cAMP和DHA基础上联合添加DAPT( , Stemcell Technologies, 72082)。从第46天起,细胞培养体系仅使用含B-27 Plus补充剂的神经培养基维持,每4天更换一次培养基。
为生成 hMO(55),将EBs培养于脑类器官生成培养基(BGM)中,该培养基包含 1:1 混合的 DMEM/F12(Fisher, 21331020)与 Neurobasal A Medium、 青霉素/链霉素(PS)、 GlutaMAX、 MEM 非必需氨基酸溶液(NEAA)(Thermo Fisher Scientific, 11140050)、 -巯基乙醇(Fisher, 21985023)以及 肝素(Sigma, H3149)。培养基中补充有 补充剂(Fisher, 17502048)、 不含维生素 A 的 B27、 dorsomorphin、A83-01( , PeproTech, 9094360)、CHIR99021( , Tocris, 4423)和 IWP2( , Selleck)。
化学品S7085处理7天。第4天加入100毫克/毫升FGF8b(PeproTech, AF-100-25)与平滑激动剂SAG( , PeproTech, 9128694);第7天引入200纳克/毫升层粘连蛋白(Sigma, L4544)及 克/毫升胰岛素(Sigma, I9278),上述添加物持续维持至第9天。此后将培养基更换为含 N-2、 B27 plus、10纳克/毫升BDNF、10纳克/毫升GDNF(PeproTech, 450-10)、 cAMP及 AA的BGM培养基,并在该条件下持续培养长达6个月。
¶ 人类小胶质细胞分化
小胶质细胞分化实验依据先前建立的方案(56)进行。简言之,首先使用STEMdiff造血试剂盒(STEMCELL TECHNOLOGIES, 05310)将iPSCs(内源性表达GCaMP6f的Kolf2.1J株、B11野生型株及B07野生型株)在12天内分化为造血祖细胞。iPSCs培养于Matrigel(Corning 354277)包被的6孔板中,采用mTeSR™ Plus培养基(STEMCELL TECHNOLOGIES, 100-0276)维持培养。细胞传代时先用 PBS清洗,随后加入1 mL ReLeSR(STEMCELL TECHNOLOGIES, 100-0483)并在 孵育90秒。移除ReLeSR后,沿孔壁缓慢加入1 mL mTeSR Plus培养基。使用大口径移液枪头将30-50个细胞团接种至Matrigel包被的6孔板的单个孔中。细胞接种次日向孔内添加造血祖细胞培养基A。培养2天后进行半量换液。第3天移除培养基A,更换为造血祖细胞培养基B。分别在第5、7、10天进行半量换液。第12天通过多次轻柔吹打收集孔内祖细胞,转移至Matrigel包被的6孔板的单孔中。将获得的祖细胞转入 小胶质细胞分化培养基,该培养基组成如下:DMEM/F12(Gibco, 11320033)、 胰岛素-转铁蛋白-硒化物(Gibco, 41400045)、 Plus(Gibco, A3582801)、 (Gibco, 17502048)、 非必需氨基酸(Gibco, 11140050)、 单硫代甘油(Sigma, M6145-25MG)、 人胰岛素(Sigma I2643-25MG)。使用前向分化培养基中添加 IL-34(Gibco, 200-34-10UG)、 TGF- $\mathsf { \Omega } \cdot \mathsf { { { \beta } \mathrm { 1 } } $ (100-21-10UG)及 M-CSF(Gibco, 300-25-10UG)。细胞在此培养基中持续培养最多24天,每2天补加 新鲜培养基。
小胶质细胞在皮层、纹状体与中脑类器官中的整合 为促进小胶质细胞融入类器官(hCO、hStrO和hMO),将培养超过80天的类器官逐个转移至超低吸附96孔板。在小胶质细胞分化第12天,收集小胶质细胞并以每孔40万细胞的密度接种到类器官表面,所用新鲜培养基由等量混合的小胶质细胞分化培养基与成熟皮层/纹状体/中脑类器官培养基组成。随后将类器官培养7天以实现小胶质细胞的自发性整合,期间每日更换培养基。此后,将类器官移回超低吸附六孔板,并按照标准皮层/纹状体/中脑类器官培养方案继续维持培养7天。
¶ 微胶质细胞整合组装体的生成
为制备hMO-hStrO-Microglia或hCO-hStrO-Microglia组装体,我们首先从hiPSCs分别生成hMO-Mg(或hCO-Mg)和 。随后,将这些含有小胶质细胞的类器官置于1.5 毫升Eppendorf管中紧密接触,培养7天进行融合。在此培养期间,每日轻柔更换一半培养基。第七天时,使用修剪过的P1000移液器吸头将组装体转移至24孔超低吸附培养板,此后每2天更换一次培养基。
¶ 病毒标记与活细胞成像
在组装两种不同的小胶质细胞整合类器官之前,我们分别使用pAAV1-hSyn-mScarlet(Addgene,131001)和pAAV9-hSyn-hM3(Gq)-mCherry(Addgene,50474)对3D神经类器官进行病毒转导,以实现投射可视化并诱导神经元超兴奋性。针对中脑-纹状体-小胶质细胞组装体实验,首先将中脑类器官-小胶质细胞复合体转移至盛有 升培养基的24孔板中,与病毒在培养箱内共孵育过夜。次日添加800 升新鲜培养基。感染三天后,利用病毒标记的中脑类器官-小胶质细胞和纹状体类器官-小胶质细胞进行组装体构建。在组装第10、20和30天时,使用配备培养系统的共聚焦荧光显微镜(LSM900;卡尔蔡司,耶拿,德国)对中脑-纹状体投射区域进行活细胞成像。图像数据后续通过Fiji(ImageJ)软件进行分析。
¶ 化学遗传学刺激与钙成像
在化学遗传学实验中,将hMO-hStrO-小胶质细胞组装体(其中hMO已预先用pAAV-hSyn-hM3(Gq)-mCherry转导)置于神经培养基中的20 毫米盖玻片(位于35 毫米玻璃底培养皿内),并在LSM900蔡司共聚焦显微镜上使用 倍物镜进行成像。为特异性诱导hMO区域的神经元过度兴奋性,加入 M氯氮平N-氧化物(靶向Gq-DREADD受体)(Abcam,ab120019)。通过GCaMP6f监测钙活动,总记录时长为5分30秒:前100秒记录基线活动,随后加入CNO并继续记录230秒。为抑制小胶质细胞GABAB受体信号传导,在钙成像前每6小时更换一次补充有2 M CGP 55845盐酸盐(选择性GABAB受体拮抗剂)(MCE,HY-103516)的培养基。
¶ 钙活性分析
钙成像数据从装配体样本的兴趣区域(ROI)中记录,并导出为Excel文件。为界定小胶质细胞胞体与突起的ROI,用户使用Inscopix软件在覆盖全视野的平均强度投影图上手动勾画这些区域。随后,在平均强度图像中对胞体ROI进行掩膜处理,使其与小胶质细胞突起分离。通过对剩余图像数据设定阈值,突起的ROI被独立提取,并以类似方式量化其平均像素强度。数据集中每列代表单个胞体或突起随时间变化的荧光强度。 为量化钙瞬变,荧光强度值被转换为F/F值: F/F=(F(t)−F0)/F0。针对每个胞体与突起,采用100秒滑动窗口建立动态基线。基线荧光强度(F0)由滑动窗口内强度值的第25百分位数确定。钙瞬变通过基于阈值的方法进行识别,将超过基线标准差三倍阈值的帧归类为活跃瞬变。最大幅度通过检测到的瞬变期间峰值 F/F值计算。信号面积指所有检测到瞬变中超出阈值的累计 F/F值。
¶ 单细胞RNA测序文库制备与数据分析
类器官根据标准方案解离为单细胞悬浮液,方案已针对PIPseq-T20工作流程进行优化调整。简言之,将随机选取的4-5个类器官混合后,置于含 木瓜蛋白酶的酶解溶液中进行孵育。
(Worthington Biochemical,LS003126)和 DNase I(Worthington Biochemical,LS2007)在37 下消化45分钟。酶解后,类器官用含蛋白酶抑制剂的培养基洗涤,并轻柔吹打以获得单细胞悬液。细胞悬液经 Flowmi细胞筛(Bel-Art,H13680-0070)过滤并计数。将活细胞重悬于细胞悬液缓冲液(Fluent BioSciences,PIPseq T20 v3.0)中,终浓度为10000细胞/ L,以确保最佳上样效率。 使用PIPseq-T20 3 单细胞RNA试剂盒v3.0(Fluent BioSciences)按照制造商方案构建单细胞RNA-seq文库。简言之,每个反应加载40,000个细胞至PIPseq预模板化即时分隔单元(PIPs)中,与分隔试剂混合,使单个细胞被带有条形码的磁珠包裹。在PIPs内进行细胞裂解和mRNA捕获,随后采用模板转换寡核苷酸(TSO)法合成cDNA。接着通过全转录组扩增(WTA)对cDNA进行扩增,并利用SPRI磁珠进行纯化。 纯化的cDNA使用PIPseq-T20文库制备试剂盒进行片段化、末端修复和加A尾处理,再进行接头连接。文库通过双索引P7/P5接头进行标记,经PCR扩增后,采用双面SPRI磁珠纯化进行大小筛选。最终文库使用Qubit高灵敏度DNA检测试剂盒(Thermo Fisher,Q33231)定量,并在Bioanalyzer 2100或TapeStation 4200(Agilent)上进行分析。测序在Illumina NovaSeq S4平台上进行,采用 双端测序模式,目标测序深度为每个细胞~20,000条读数。
生成的特征-条形码矩阵被读入R(版本4.2.2),排除了表达少于200个基因的任何细胞以及在任何少于三个细胞中表达的基因。对于所有单细胞样本,Seurat(版本4.3.0.1)移除了线粒体基因比例超过 、特征数少于2,500或超过10,000的细胞。同样地,计数少于2,000或超过50,000的细胞也被过滤掉。我们使用“merge”函数合并了样本。随后,通过“FindNeighbors”和“FindClusters”函数,使用前50个主成分及0.2的分辨率进行总细胞聚类分析,并采用UMAP进行可视化。聚类结果依据已知标记基因的表达进行分组。小胶质细胞的分类基于已知标记物的组合表达进行,方法如前所述(39)。
¶ 高密度多电极阵列(HD-MEA)记录
所有高密度微电极阵列(HD-MEA)记录均采用Multiwell HyperCam Alpha高密度多孔微电极阵列系统(3Brain AG,瑞士)。六孔板首先使用200微升 Tergazyme溶液在 下清洗1小时,再用过量无菌MilliQ水(电阻率 兆欧·厘米)洗涤3次,随后用 乙醇消毒1小时。移除乙醇后,将孔板在紫外线下干燥,接着在室温下用PBS溶液浸泡过夜。随后,HD-MEA依次进行包被处理:先使用聚-L-鸟氨酸(50微克/毫升)在无菌MilliQ水中浸泡过夜,MilliQ水洗涤3次后,再用层粘连蛋白(50微克/毫升)于 孵育4小时。将培养100-150天的类组装体以20微升培养基接种至3Brain微电极阵列上,放回培养箱静置2小时。此后每2小时使用宽口径移液器枪头补加20微升培养基,持续8小时。最后,以同心圆方式缓慢加入2毫升培养基直至填满孔板。每3-4天更换一次培养基。类组装体在培养第10-15天期间进行记录。数据采集与分析采用Brainwave V软件(v5.6,3Brain瑞士)。HD-MEA阵列采用 电极配置,电极间距60微米(有效记录面积 平方毫米)。采样率设置为10,000赫兹,硬件高通滤波器设为100赫兹。记录过程中实施直接光刺激补偿。采用快速傅里叶变换(FFT)进行20-5000赫兹带通滤波的峰电位检测。峰电位检测阈值设为8.0倍标准差,峰值寿命2.0毫秒,不应期1.0毫秒,峰前波形时程1.0毫秒。放电频率低于0.083赫兹(每分钟5个峰电位)的电极予以排除。对于峰电位簇检测,采用简
采用100毫秒的最大峰间间隔(ISI)设置,最小峰电位数设定为5。应用基于3组分PCA结合K-Means与间隙统计聚类的峰电位分类方法。针对峰电位网络爆发活动,采用基于募集度的算法,设置 的电极募集阈值及50个峰电位的最低触发阈值。使用30毫秒的峰电位互相关窗口及3.0毫秒的统计单元生成相关矩阵。
¶ 冰冻切片与免疫荧光
类器官和组装体首先在 多聚甲醛(PFA)的磷酸盐缓冲盐水(PBS)溶液中固定4小时。固定完成后,样本被转移至 蔗糖/PBS溶液中,静置1天直至沉底。脱水完全后,样本包埋于 蔗糖/PBS混合液中,并于- 保存以供后续实验。免疫荧光染色时,使用莱卡冷冻切片机(LeicaCM1860)制备 微米厚切片。冰冻切片首先用PBS冲洗以去除残留OCT,随后在含 正常驴血清(NDS;Millipore Sigma S30-100ML)、 Triton X-100(Millipore Sigma T9284-100ML)及 BSA的PBS封闭液中室温封闭1小时。接着切片与相应一抗溶液于 孵育过夜。次日用0.01M PBS洗涤切片后,室温下二抗孵育2小时。末次洗涤后封片。 所用一抗如下:抗IBA1(Abcam ab178846)、人源抗IBA1(Synaptic Systems 234308)、人源抗CD68(Invitrogen MA5-13324)、人源抗Gabbr1(GeneTex GTX102511)、人源抗DRD1(Thermo Fisher 702593)、抗Ctip2(Abcam ab18465)、抗TBR1(Thermo Fisher 66564)、抗GABA(Thermo Fisher PA5-32241)、抗TH(Thermo Fisher MA1-24654)、抗MAP2(Thermo Fisher PA1-10005)、抗NeuN(Thermo Fisher 702022)、抗GAD67(Thermo Fisher PA5-21397)、抗FOXA2(Thermo Fisher 701698)及抗OTX2(Thermo Fisher MA5-15854)。共聚焦图像使用Z-stack激光扫描共聚焦荧光显微镜(LSM900;Carl Zeiss,耶拿,德国)采集。
使用Imaris 9.9软件进行三维图像分析。测量IBA1和CD68的重建表面,并采用公式(CD68体积/IBA1+细胞体积)计算小胶质细胞内CD68的占有率。此外,为量化CD68+区域内的VGAT+信号,采用以下计算式:(VGAT+体积 / CD68+体积) 。
¶ 电生理学
膜片钳记录操作如前所述(32, 35)。简而言之,将类器官置于含以下成分的冰镇切片液(单位毫摩:110 氯化胆碱、 、 、 、 、 、25 葡萄糖)中使用振动切片机(德国Leica VT1200S)进行切片。
1 抗坏血酸钠与 3.1 丙酮酸钠( ,305-315 毫渗透压摩尔浓度,以 和 通气)。脑片在相同介质中于 孵育 10 分钟,随后转移至人工脑脊液(aCSF;单位 : 、 、 、 、 、 、10 葡萄糖; ,305-315 毫渗透压摩尔浓度,以 和 通气)中,于 维持 10-20 分钟后,在室温下保存至少 30 分钟。使用配备 IR-2000 摄像头(Dage-MTI)的 BX-51WI 显微镜(奥林巴斯)在红外微分干涉相差(IR-DIC)下观察脑片。我们采用薄壁硼硅玻璃电极(BF150-110-10),其开放尖端电阻为 3 。电流钳记录所用的内液成分为(单位 ):122 甲磺酸钾、4 KCl、 、0.2 EGTA、10 HEPES、4 三磷酸腺苷二钠、0.3 三磷酸鸟苷三钠、14 磷酸肌酸三钠盐,用 KOH 调节 pH 至7.25,渗透压为 295-305 毫渗透压摩尔浓度。记录使用 Axon MultiClamp 700B 放大器(MolecularDevices)进行,数据通过 pClamp 11.3 软件采集,经 滤波并以 采样率通过 Axon Digidata 1550B 加 HumSilencer 数字化仪(Molecular Devices)获取。动作电位通过响应对细胞施加一系列从-200 pA到+400 pA、以50 pA为增量的400毫秒超极化与去极化电流阶跃刺激,每次扫描持续时间为5秒,期间细胞均维持在正常静息膜电位状态。
¶ 统计分析
使用 OriginPro 2025 和 GraphPad Prism 10 进行数据分析和曲线拟合。两组间的单次比较采用双尾 Student’s t 检验(参数检验)或非配对双尾 Mann-Whitney U 检验(非参数检验)。其他数据采用单因素或双因素方差分析,随后使用 Bonferroni 校正进行事后检验。各组实验样本数(n)已在图注中标明。结果以均值 均值的标准误差(SEM)表示。显著性判定标准为: , (**), (***), 。