¶ 使用大规模电生理学对阿尔茨海默病中海马体网络水平损伤的表征
¶ 原文下载:network-level_characterization_of_hippocampal_disr.pdf
布雷特·艾迪生·埃默里、沙鲁克·汉扎达、胡鑫、玛丽亚·安娜·马吉、西尔维娅·比斯蒂以及海德尔·阿明*,IEEE会员
本研究得到基础机构基金(DZNE)和ERANETNEURON(ResiPreS)的支持。
B.A.埃默里、S.汉扎达、X.胡和H.阿明就职于德国德累斯顿市塔茨贝格41号德国神经退行性疾病研究中心(DZNE)的生物混合神经电子学实验室(BIONICS)。*通讯作者(电话:+49351210463602-电子邮箱:hayder.amin@dzne.de)。
M. A. Maggi就职于意大利拉奎拉67051,卡尼斯托的Hortus Novus。
S. Bisti就职于意大利罗马市Medaglie D’Oro大街305号的国家生物结构与生物系统研究所(INBB)。
¶ 摘要
阿尔茨海默病(AD)是一种进行性神经退行性疾病,预计到2050年将影响全球超过1.3亿人。虽然大量研究致力于针对β-淀粉样蛋白(Aβ)斑块和tau蛋白病变等分子标志物,但网络层面的功能障碍仍是AD进展中一个关键却未被充分探索的部分。海马-皮质(HC)回路活动的紊乱在AD早期就会出现,损害记忆处理和认知功能。表征这些紊乱需要能够捕捉全网络时空动态的高分辨率平台。为解决这一问题,我们采用了高密度微电极阵列(HD-MEA)生物传感器,来评估已建立的APP NL和APP NL-G-F小鼠模型的离体海马切片中的大规模电生理活动。我们的方法量化了海马振荡紊乱,并研究了藏红花(一种据报道具有神经保护特性的天然化合物)对其的调节作用。结果表明,APP NL-G-F小鼠的海马网络活动逐渐受损,特别是在锐波涟漪(SWR)和多单位活动(MUA)模式中。HD-MEA平台为研究AD相关的网络功能障碍和探索潜在的调节干预措施提供了一种可扩展的工具。
¶ I.引言
网络层面的组织原则依赖于神经集合的动态组织,这些神经集合通过同步放电模式和协调活动形成稳定的结构,用于信息编码和处理。这种协调使得信号能够在大脑区域间传递,并促进感觉输入与记忆过程的整合[1],[2],[3]。在阿尔茨海默病(AD)中,海马-皮质(HC)回路的早期破坏会损害这些协调过程,导致进行性认知衰退[4],[5],[6]。虽然像Aβ聚集和tau蛋白病理等分子和细胞层面的改变已被广泛研究,但这些变化在网络层面的影响仍知之甚少[7],[8]。明确AD中的网络功能障碍对于识别功能性生物标志物和潜在干预靶点至关重要。特别是振荡动力学的变化——从慢δ波和θ波到高频γ节律以及尖波涟漪(SWRs)——为了解海马回路的完整性提供了宝贵的见解。鉴于SWRs对兴奋-抑制(E/I)平衡和突触完整性的敏感性,其破坏可作为神经退行性病变进展的关键标志物[1],[2],[3]。然而,研究这些模式需要先进的电生理平台,该平台能够以高时空分辨率捕捉大规模网络活动。为了研究AD中HC动态和振荡模式的调节,我们采用了一种大规模的芯片上脑生物传感平台,该平台基于高密度、基于CMOS的微电极阵列(HD-MEA)[9],[10],[11],[12]。
借助我们的高清微电极阵列(HD-MEA)平台,我们在两种成熟的阿尔茨海默病(AD)小鼠模型(APpNL和APpNL-G-F)中对海马(HC)网络的异常进行了表征[13],[14]。此外,我们还研究了藏红花(一种据报道具有神经保护特性的天然化合物)对调节电路活动的影响。选择藏红花是因为其已被证实具有抗氧化、抗炎和神经保护作用,这些作用有助于临床前模型中的突触维持和认知增强[12],[15],[16]。与单靶点药物不同,藏红花提供了一种多方面的治疗方法,与阿尔茨海默病复杂的病理机制相契合。这使其特别适合研究阿尔茨海默病模型中全网络的异常以及潜在的电路恢复。
¶ 二、材料与方法
¶ A. 基于CMOS的生物传感器
使用高清微电极阵列(HDMEA)和根据我们的记录设置定制的生物信号传感平台(3Brain AG,瑞士)进行了大规模海马体(HC)记录(图1,a和b)。生物传感器高清微电极阵列芯片包含4096个记录电极,间距为42微米,组成约7平方毫米的有效传感区域,足以记录整个海马体回路。记录经过1Hz至5kHz的带通滤波,确保在宽频谱范围内捕捉局部场电位(LFP)、尖波涟漪(SWR)和多单位活动(MUA)。
¶ B. 急性海马切片制备
所有工作和动物实验均按照欧洲和国家法规(《动物保护法》)进行,并获得了地方当局(萨克森州管理局;25-5131/476/14)的批准。从36周龄的APpNL和APpNL-G-F雌性小鼠中获取急性、水平的300μm厚海马-皮质切片,并根据我们之前发表的研究[9]、[10]、[11]进行制备。切片在0-2°C的高蔗糖灌流液(pH=7.25-7.35;345-355毫渗摩尔/升)中切割,灌流液饱和有95%氧气和5%二氧化碳,其成分(单位:毫摩尔)为:250蔗糖、10葡萄糖、1.25磷酸二氢钠、24碳酸氢钠、2.5氯化钾、0.5抗坏血酸、4氯化镁、1.2硫酸镁、0.5氯化钙。切片在32°C下孵育45分钟,然后在室温下于记录灌流液中恢复1小时,该记录灌流液(pH=7.25-7.35;305-315毫渗摩尔/升)饱和有95%氧气和5%二氧化碳,其成分(单位:毫摩尔)为:127氯化钠、3.5氯化钾、1.25磷酸二氢钠、26碳酸氢钠、10葡萄糖、1硫酸镁、2.5氯化钙。
¶ C. 生物化学调节的海马记录
切片被放置并耦合到HD-MEA芯片上,使用一个定制的铂制琴形装置固定在组织上。一个热稳定灌流系统(美国ALA科学仪器公司)被整合进来,以4.5毫升/分钟的流速向芯片上脑接口输送含氧的记录灌流液,并在整个实验过程中将温度控制在37摄氏度。针对APPNL和APPNL-G-F的首次细胞外记录捕捉了在没有藏红花(0微克/毫升)的情况下,100微摩尔4AP(德国Sigma-Aldrich公司)诱导的基线自发性电路激活。之后,将递增浓度的藏红花(25、50和75微克/毫升)依次加入含有100微摩尔4AP的灌流液中,每种浓度下收集十分钟的细胞外记录[12]。实验前,将来自意大利Hortus Novus srl的藏红花柱头在双蒸水中配制成1毫克/毫升的储备液[12]、[15]、[16]。为了在离线分析期间获得组织相对于细胞外记录的空间排列,将光学成像显微镜与HD-MEA生物信号传感平台相结合,以在记录后捕捉海马脑切片结构。
¶ D. 大规模、全网络分析
为了在空间上表征回路功能,根据相应切片图像的分子结构信息,将活性电极离线分组到特定层中。海马区(HC)亚区域层包括齿状回(DG)、门区、CA3区、CA1区、内嗅皮层(EC)和鼻周皮层(PC)。在商用软件(3Brain AG)中,使用硬阈值法和PTSD算法进行局部场电位(LFP)事件和多单位活动(MUA)检测,而尖波涟漪(SWR)事件检测则按照先前描述的方法进行[10]。检测到的事件分别针对局部场电位(1-100赫兹)、尖波涟漪(120-240赫兹)和多单位活动(300-1000赫兹)模式进行带通滤波,并使用基于自适应波形的阈值平台——DENOISING——进行预处理,以去除伪影并分配时间戳[17]。所有进一步的分析均通过自定义编写的Python脚本完成。
基于事件的参数包括——活动通道数、平均事件率和事件持续时间,这些参数被选用来描述网络和振荡模式的动态变化。为了比较两种浓度下高密度微电极阵列(HD-MEA)电极间的区域激活和时间事件分布,从连续的相位记录中生成了光栅图。为了检查特定的时间信号轨迹,采用有监督的波形阈值算法提取了示例性的区域局部场电位(LFP)、尖波涟漪(SWR)和多单位活动(MUA)信号轨迹。为了确定每个振荡模式的功率分布和主导频率,在选定的时间窗口内构建了伪彩色频谱图中的频率-时间动态。最后,所有统计分析均使用Originlab 2024软件进行。采用单因素方差分析(ANOVA),随后进行Tukey事后检验,以检验组间差异的统计学显著性。p < 0.05被认为具有显著性。
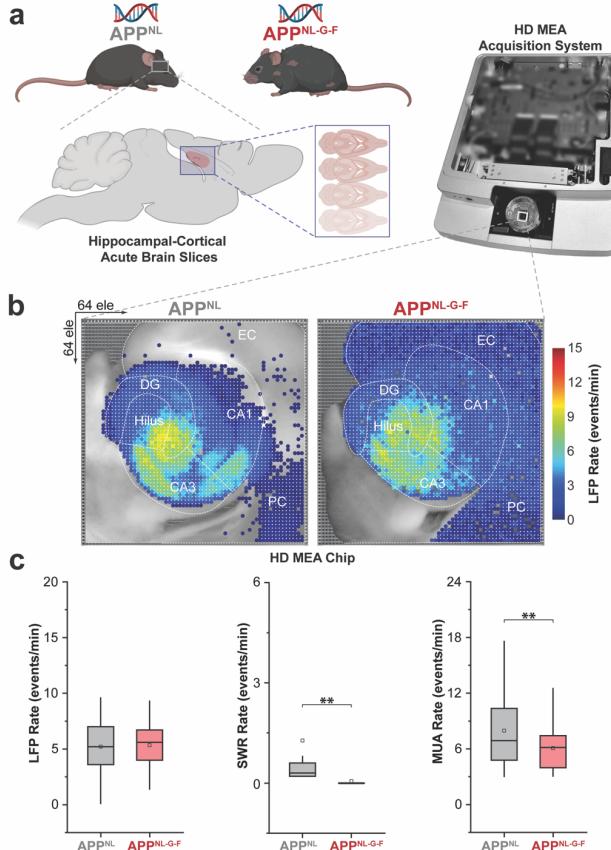
图1:实验范式和高密度微电极阵列(HDMEA)生物传感平台的示意图概述(a),该平台用于记录芯片上海马切片的大规模激活。APP NL和APP NL-G-F的计算局部场电位(LFP)速率平均值的地形表征(b)。APP NL和APP NL-G-F之间的平均LFP、尖波涟漪(SWR)和多单位活动(MUA)速率的量化(c),基于具有3083个(APP NL)和3067个(APP NL-G-F)总 firing电极的代表性切片记录。箱线图显示四分位范围(第25-75百分位数),须线延伸至四分位距的1.5倍。部分内容使用BioRender制作。
¶ 三、结果与讨论
¶ A. 阿尔茨海默病模型中的网络功能障碍
为了评估阿尔茨海默病中的海马回路功能障碍,我们比较了APpNL和APpNL-G-F小鼠模型的局部场电位(LFP)、锐波涟漪(SWR)以及多单位活动(MUA)模式。定量分析显示,虽然不同基因型小鼠的LFP事件发生率相近,但APpNL-G-F小鼠的SWR和MUA发生率显著降低(图1c)。进一步的频谱分析表明,高频振荡功率有所损失,其中对记忆巩固至关重要的SWR存在明显缺陷(图3a和b,无藏红花条件)。这些发现与人类阿尔茨海默病研究一致,在该研究中,海马-皮质解耦与认知障碍相关[18]。此外,APpNL-G-F小鼠脑片的SWR事件持续时间更短,空间分布减少,尤其是在CA3和CA1区(图2d;图4a和c,无藏红花条件),这表明海马亚回路内的复发性兴奋减弱。
这些发现凸显了高频振荡易受晚期阿尔茨海默病(AD)病理影响的特性,在这种病理状态下,突触和结构的完整性受到严重损害,导致记忆巩固和认知功能所需的协调活动中断。APP NL 模型和 APP NL-G-F 模型之间β淀粉样蛋白(Aβ)和tau蛋白病理的差异,或许可以解释为何在 APP NL-G-F 小鼠中观察到更严重的损伤,因为tau蛋白相关功能障碍会加剧神经元兴奋性缺陷和中间神经元介导的抑制作用,从而导致更明显的涟漪损伤和网络去同步化[1]、[3]、[13]、[14]。
¶ B. 藏红花对回路活动的调节作用
为了研究藏红花是否能调节网络功能障碍,我们应用了浓度递增的藏红花(0、25、50和75μg/mL),并对回路活动的变化进行了量化(图2a-c)。藏红花诱导了SWR和MUA活动的剂量依赖性恢复,在25μg/mL时观察到显著效果[12]。在APpNL-G-F切片中,SWR频率(图2b)和MUA尖峰频率(图2c)均显著增加,恢复到各自的APpNL基线反应,尤其是在CA3和CA1海马亚区(图2d)。有趣的是,更高剂量(50-75μg/mL)并未进一步显著增强反应。
SWR活动的这种剂量依赖性增加表明,藏红花可逐步调节网络紊乱并增强CA3-CA1通讯,而APpNL HC电路可能因其更完整的网络完整性而达到功能上限[13]、[14]。有趣的是,APPNL切片的网络活动变化极小,这表明藏红花主要在病理受损的电路中发挥作用,而非增强基线振荡。这种特异性支持了其在网络恢复而非一般兴奋中的作用。
¶ C. 剂量依赖性反应与网络恢复
为了表征APP NL和APP NL-G-F之间的时间特征差异,并突出特定频率对网络恢复的作用,我们在未使用藏红花和使用25μg/mL藏红花的情况下,进行了连续时间轨迹比较和频谱分析。这揭示了APP NL-G-F的海马回路中,尖波涟漪(SWR)活动的时间和频率恢复以及高频振荡功率恢复均受到调控(图3a和b)。为了进一步量化藏红花的作用,我们进行了基于事件的分析。在使用25μg/mL藏红花后,APP NL-G-F脑片中检测到SWR事件的活跃电极数量增加了2.75倍,表明网络参与范围更广(图4a)。SWR事件发生率也成比例增加(图4b),而事件持续时间则与APP NL的值相当(图4c)。
这些研究结果表明,藏红花通过改善突触协调和回路完整性,恢复了海马振荡动力学的功能方面。有趣的是,正如EC50值(约25μg/mL,图2)所量化的那样,SWR的恢复遵循非线性剂量反应关系。在较高浓度下,SWR的增强趋于平稳,这可能反映了网络响应能力的天花板效应。这表明藏红花在一定阈值内促进突触恢复,超过该阈值后,额外的效果会受到潜在病理的限制。
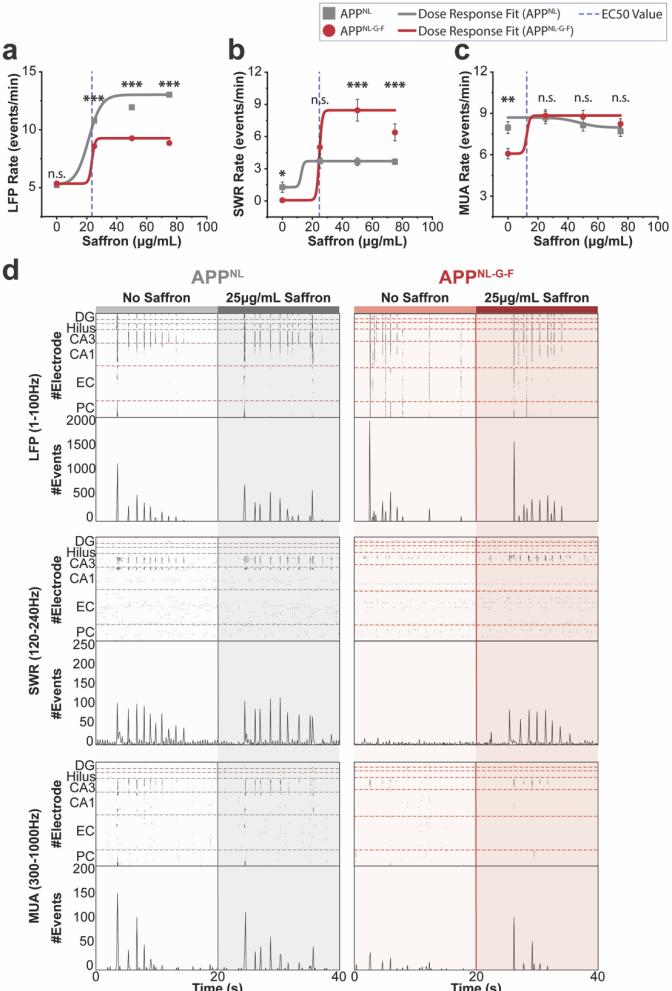
图2:使用Levenberg-Marquardt迭代算法生成的非线性藏红花剂量反应曲线,显示在LFP(a)、SWR(b)和MUA(c)频段的EC50值约为25μg/mL。光栅图比较了每个频段中APP NL和APP NL-G-FHC电路中0μg/mL和25μg/mL藏红花剂量的情况(d)。区间图表示平均值±标准误。
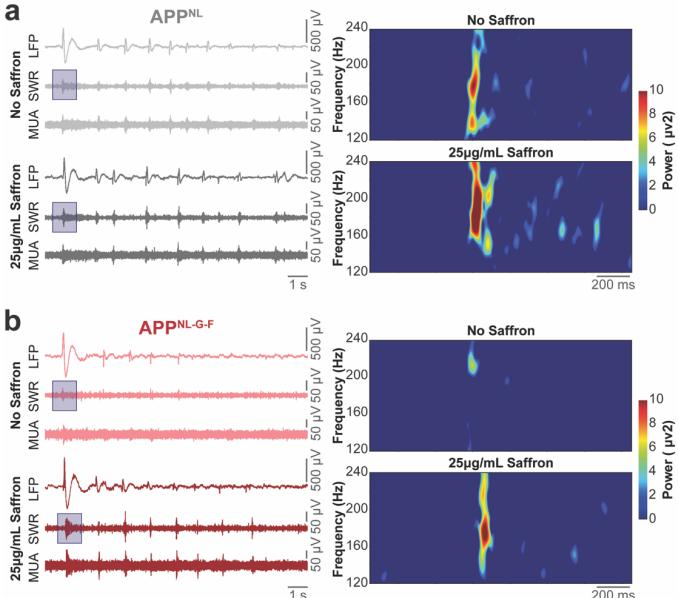
图3:在APPNL(a)和APPNL-G-F(b)海马回路中,比较0μg/mL和25μg/mL藏红花剂量时,海马CA3亚区的带通滤波LFP(1-100Hz)、SWR(120-240Hz)和MUA(300-1000Hz)的10秒时间信号轨迹。伪彩色频谱图插图展示了SWR的频率-时间动态。
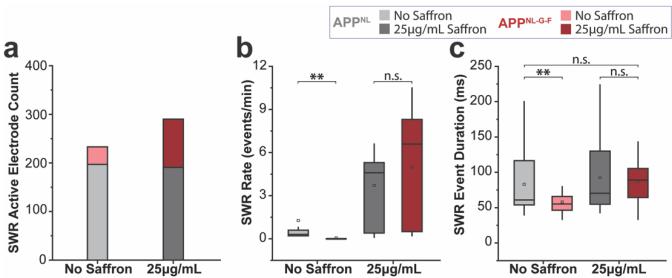
图4:比较APP NL和APP NL-G-FHC电路中0μg/mL和25μg/mL藏红花剂量下,SWR活性电极计数(a)、平均SWR频率(b)和平均SWR事件持续时间(c)的量化结果。箱线图显示四分位距(第25-75百分位数),须线延伸至四分位距的1.5倍。
¶ 四、结论
本研究确立高密度微电极阵列(HD-MEA)作为表征阿尔茨海默病(AD)中海马回路功能障碍的有力平台。我们的研究结果显示,APpNL-G-F模型中的尖波涟漪(SWR)和多单位活动(MUA)存在显著异常,这表明大规模网络损伤是AD进展的一个标志。这些结果强调,有必要超越分子病理学,纳入全网络生物标志物,以更全面地理解神经退行性疾病。
藏红花的应用对网络活动表现出剂量依赖性调节作用,尤其在受损更严重的APpNL-G-F模型中,这表明其在回路水平调节方面可能具有一定作用。然而,高剂量下效果的饱和现象凸显了调节网络活动的复杂性,也说明需要进一步开展机制研究。未来的研究应探索这种调节作用是否能转化为体内长期的功能恢复和认知改善。作为一项概念验证研究,这些发现为未来大规模研究奠定了基础,旨在阐明藏红花神经调节作用的确切剂量依赖性效应及其潜在机制。
除阿尔茨海默病外,本研究还展示了高密度微电极阵列平台在研究神经和精神疾病中电路功能障碍方面的更广泛适用性。大规模电生理学可用于探测癫痫、精神分裂症和创伤性脑损伤等疾病中的网络异常,在这些疾病中,振荡动力学的紊乱起着核心作用。通过将这种方法与行为范式、成像和分子分析相结合,未来的研究可以在电路功能障碍和疾病机制之间建立更紧密的联系,为基于网络的干预措施和精准疗法铺平道路。
¶ 致谢
我们要感谢德累斯顿DZNE的动物行为测试平台所提供的支持。
¶ 参考文献
[1] G.布扎基,“神经元集群的大规模记录”,《自然神经科学》,第7卷,第5期,第446-451页,2004年。
[2] A.德拉古恩与G.布扎基,《皮质网络中的神经元振荡》,《科学》(1979),第304卷
[3] G. 布扎基,“海马体尖波涟漪:情景记忆和规划的认知生物标志物”,《海马体》,第25卷,第10期,第1073-1188页,2015年10月。
[4] J.J.帕洛普和L.穆克,“阿尔茨海默病中的网络异常和中间神经元功能障碍”,《自然评论神经科学》,第17卷,第12期,第777-792页,2016年。
[5] J. J. Palop、J. Chin和L. Mucke,“神经退行性疾病的网络功能障碍视角”,《自然》,第443卷,第768-773页,2006年。
[6] S.F.格里科、T.C.霍姆斯和X.徐,“利用新技术探索阿尔茨海默病的神经回路机制”,20
[7] Z.布雷杰耶和R.卡拉曼,“阿尔茨海默病综合综述:病因与治疗”,2020年12月1日,MDPI。
[8] A.塞拉诺-波佐、M.P.弗罗施、E.马斯利亚和B.T.海曼,“阿尔茨海默病的神经病理学改变”,《冷泉港医学展望》,第1卷,第1期,2011年9月21日。
[9] B.A.埃默里、S.汉扎达、胡晓、D.克卢奇和H.阿明,“在CMOS集成高密度微电极阵列上记录和分析多模态大规模神经元集群动态”,《可视化实验杂志》,第205期,2024年3月。
[10] B.A. 埃默里、X. 胡、S. 汉扎达、G. 肯佩曼和H. 阿明,“用于评估经验依赖性可塑性中海马回路动态的高分辨率CMOS生物传感器”,《生物传感器与生物电子学》,第237卷,2023年10月。
[11] 胡晓、S.汉扎达、D.克卢奇、F.卡莱加里和H.阿明,“在高密度CMOS芯片上实现生物混合嗅球以揭示大规模时空电路信息”,《生物传感器与生物电子学》,第198卷,2022年2月。
[12] H. Amin、T. Nieus、D. Lonardoni、A. Maccione和L. Berdondini,“基于CMOS-MEAs的Aβ诱导网络功能障碍高分辨率生物电成像用于神经毒性及挽救研究”,《科学报告》,第7卷,第1期,第1-13页,2017年。
[13] A.拉蒂夫-埃尔南德斯等,“AppNLG-F基因敲入小鼠突触衰竭的双重表现”,《阿尔茨海默病研究与治疗》,第12卷,第1期,第100页,2020年12月。
[14] 斋藤T. 等人,《阿尔茨海默病的单APP基因敲入小鼠模型》,《自然神经科学》,第17卷,第5期,第661-663页,2014年5月。
[15]M.A. Maggi,S. Bisti,和C. Picco,《藏红花:化学成分与神经保护活性》,《分子》,第25卷,第23期,第5618页,2020年11月。
[16] M.斯皮内尔、A.比安科利洛、G.巴塔利亚、M.福斯基、A.阿莫雷萨诺和M.A.马吉,“通过多学科方法对藏红花进行表征”,《分子》,第28卷,第1期,2023年1月。
[17] 胡晓、B.A. 埃默里、S.汉扎达和H. 阿明,“DENOISING:基于高密度CMOS生物传感器的多模态神经观测动态增强与噪声抑制”,《生物工程与生物技术前沿》,第12卷,2024年9月。
[18] B.A.曼德等人,“β-淀粉样蛋白破坏人类非快速眼动慢波及相关的海马体依赖性记忆巩固”,《自然神经科学》,第18卷,第7期,第1051-1057页,2015年7月。