¶ 《神经科学方法杂志》
¶ 高密度多电极阵列(MEA)在啮齿动物胶质瘤模型中的记录
费迪南德·福尔贝格尔a,1、法比亚娜·桑塔纳·克拉盖伦德a,1、卡特琳·波拉特a、吕迪格·科林a,b、法尔科·兰格a,b、蒂莫·基尔施泰因a,b,*
a 德国罗斯托克18057,罗斯托克大学医学中心奥斯卡-朗根多夫生理学研究所
b 德国罗斯托克18147,罗斯托克大学罗斯托克跨学科神经科学中心
* 通讯作者地址:德国罗斯托克18057,罗斯托克大学医学中心奥斯卡-朗根多夫生理学研究所。电子邮箱:rudolf.forberger@uni-rostock.de(F. Forberger)、fabiana.kragelund@uni-rostock.de(F.S. Kragelund)、katrin.porath@uni-rostock.de(K. Porath)、rudiger.koehling@uni-rostock.de(R. Kohling)、falko.lange@uni-rostock.de(F. Lange)、timo.kirschstein@uni-rostock.de(T. Kirschstein)。
1 这些作者对本研究贡献均等。
¶ 亮点
• 在携带胶质瘤的大鼠急性脑切片中诱发了网络爆发。
• 64×64多电极阵列能够对网络爆发进行详细记录。
• 描述了活动中心轨迹和活动传播分析。
• 胶质瘤荷瘤切片和对照组的网络爆发存在差异。
• 构建了基于尖峰时间覆盖系数的功能连接图。
¶ 关键词:
多电极阵列, 微电极阵列, 神经胶质瘤, 网络爆发, spike 分选, spike 时间平铺系数
¶ 摘要
¶ 背景
高级别胶质瘤是侵袭性的原发性脑肿瘤,会影响周围脑组织,可能导致神经功能缺损、癫痫、认知障碍和肿瘤进展。研究主要集中在谷氨酸能改变上,但对其潜在网络机制的理解仍然有限。
¶ 新方法
为了研究胶质瘤如何影响神经网络的完整性和 spike 活动能力,我们在携带 F98 胶质瘤的大鼠的新皮质切片中诱导了网络爆发事件。我们使用 64×64 高密度多电极阵列记录网络活动,以评估网络长时间高强度活动的能力。我们描述了胶质瘤细胞植入、脑切片制备以及电生理记录的详细数据分析,重点介绍了用于表征全网络爆发事件的计算方法。
¶ 结果
使用Kilosort4进行尖峰分选,并用于识别网络爆发。根据多单位活动估计爆发起源,并评估网络爆发传播速度。基于尖峰时间平铺系数,利用从图表中得出的指标分析网络级功能连接性。我们的结果表明,带有胶质瘤的切片中网络完整性降低。
¶ 与现有方法的比较
高密度多电极阵列与Kilosort4相结合,在检测网络爆发和绘制活动中心轨迹方面,比传统记录技术更具优势。
¶ 结论
该协议为剖析网络活动提供了一个稳健的平台,并为未来的机制研究奠定了基础。我们还讨论了我们的临床前方法在研究胶质瘤对周围神经元网络相关影响方面的局限性和实验挑战。
¶ 1. 引言
高级别胶质瘤是一种侵袭性强且致命的原发性脑肿瘤;尽管采用多模式治疗,患者的中位生存期也很少超过15个月(Guo等人,2023年,Stupp等人,2005年,Wang和Jiang,2013年)。除了预期寿命大幅缩短外,高级别胶质瘤还会损害脑功能,常导致神经功能缺损、认知能力下降和癫痫发作(Amidei和Kushner,2015年,Ghadimi等人,2025年,Samudra等人,2019年)。
在瘤周皮质中,肿瘤细胞与微环境之间的相互作用形成了一个过度兴奋的网络(Campbell 等人,2012,Hatcher 等人,2020,Taylor 等人,2023)。相关机制包括细胞外谷氨酸释放过多、抑制性 GABA 能信号受损、离子通道表达改变以及慢性神经炎症(Barron 等人,2025,Lange 等人,2021,Liu 等人,2019)。此外,有证据表明,神经元与胶质瘤之间的突触使兴奋性神经元输入能够直接促进胶质瘤增殖(Harwood 等人,2024,Huang-Hobbs 等人,2023,Venkataramani 等人,2022,Venkataramani 等人,2019,Venkatesh 等人,2017,Venkatesh 等人,2015)。尽管谷氨酸能传递一直是主要研究焦点,但胆碱能和 GABA 能通路也可能参与肿瘤相关的网络动态(Drexler 等人,2025,Li 等人,2024,Tantillo 等人,2020)。尽管已有这些研究,人们对胶质瘤如何改变神经元群体活动、完整性和网络同步性的理解仍然有限。
计算硬件和信号处理方面的进步现已能够同时捕获和分析来自数千个电极的信号。高密度多电极阵列(HD-MEAs)为研究各种中枢神经系统疾病提供了机会(Emery等人,2025年,Kragelund等人,2025年,Quintanilla等人,2025年)。然而,迄今为止,只有小型MEA系统被用于体外研究胶质瘤的影响(Gill等人,2020年)。在此,我们提出了一种新方法,用于分析来自处于高兴奋性条件下的荷瘤大鼠脑切片的HD-MEA数据,以诱导网络爆发(NBs)。
我们的协议能够对神经球进行详细描述,确定其起源,并捕捉单个单元活动之间的全网交互。
¶ 2. 方法
¶ 2.1. 研究方案
我们研究方案的图形概述如图1所示。我们记录了长期去抑制后,携带F98胶质瘤的大鼠新皮质脑片中化学诱导的活动。该模型再现了人类高级别胶质瘤的弥漫性浸润、快速进展和免疫微环境(Barth和Kaur,2009;Biasibetti等人,2017;Mathieu等人,2007),以及体内癫痫发作(Lange等人,2020)。胶质瘤植入后10至12天,处死大鼠。通过用不含Mg2+、含8 mmol/L K+和50 µmol/L 4-氨基吡啶的人工脑脊液灌注大鼠脑片,诱导网络爆发(NBs)。
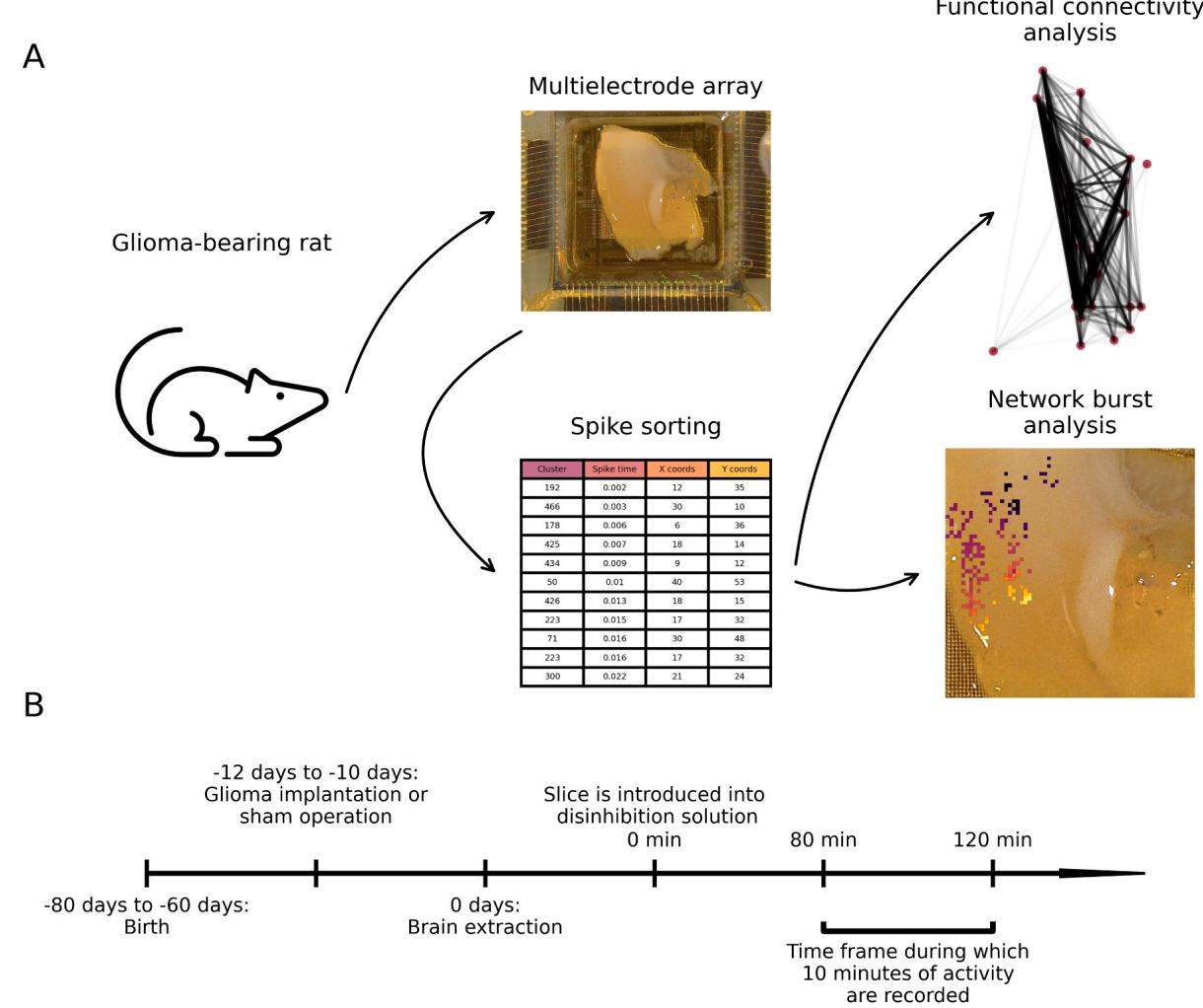
图1. 研究方案。(A)将F98胶质瘤立体定向植入Fischer大鼠的感觉运动皮层。10-12天后,制备急性脑切片,并使用含有0 mmol/L Mg²⁺、8 mmol/L K⁺和50 µmol/L 4-氨基吡啶的人工脑脊液(图B中的“去抑制溶液”)进行药物去抑制处理至少80分钟,然后将其放置到MEA系统上。记录10分钟的自发活动,并使用Kilosort4进行 spike 分选。分析网络爆发,将单细胞活动用于基于图的单位间功能连接研究。(B)实验时间线。
使用Kilosort4对高密度微电极阵列(HD-MEA)记录进行了尖峰排序(Pachitariu等人,2024b)。排序后的单元被用于描述NB的传播,并且基于分离良好的单单元活动之间的尖峰时间平铺系数(Cutts和Eglen,2014)构建和分析了功能连接图。
¶ 2.2. 携带胶质瘤的大鼠
¶ 2.2.1. 细胞培养
大鼠F98胶质瘤细胞系购自美国典型培养物保藏中心(ATCC),并制备了含有确定数量细胞的分装液用于长期储存。实验中,细胞在Dulbecco改良Eagle培养基:营养混合物F-12(DMEM/F12;购自德国艾登巴赫的PAN Biotech公司)中培养,培养基添加10%胎牛血清(购自德国福希特的Bio&SELL公司),培养条件为37°C、5%CO₂湿润环境。持续生长的细胞培养物定期传代,并按固定间隔使用MycoSPY®-PCR支原体检测试剂盒(购自德国慕尼黑的Biontex公司)检测支原体污染。立体定向注射前,通过胰蛋白酶消化收集细胞,制备成磷酸盐缓冲液(PBS)中的细胞悬液(1×10⁵细胞/μL)用于植入。
¶ 2.2.2. 体内F98胶质瘤模型
已建立的同基因Fischer 344大鼠/F98肿瘤模型被用于模拟人类胶质瘤(Lange等人,2020,Mathieu等人,2007)。包括活体大鼠在内的所有操作均按照国家和国际动物伦理使用指南(欧洲理事会指令86/609/EEC,地方当局批准号LALLF M-V/TSD/7221.3–1–020/20)进行。已尽一切努力减少动物的痛苦,并减少本研究中使用的Fischer大鼠数量。动物饲养在环境可控的条件下(12小时光照/黑暗周期,上午6点至下午6点开灯,相对湿度40–60%)。
如先前报道(Lange等人,2020年)所述,在以氯胺酮(100 mg/kg腹腔注射)和赛拉嗪(10 mg/kg腹腔注射)为基础的麻醉条件下,对4只 Fischer大鼠的感觉运动新皮层进行了胶质瘤细胞悬液的立体定向植入。为注射F98胶质瘤细胞,将大鼠头部固定在立体定向架(Narishige,东京,日本)中。做头皮切口后,剥离颅骨外的颅外肌肉,在左侧旁矢状位(相对于前囟:后1.8 mm,左2.5 mm)手动在颅骨上钻一个直径0.7 mm的孔。使用汉密尔顿注射器(Model 701 N SYR;汉密尔顿,里诺,内华达州,美国)以0.5 μL/分钟的速度注射总共1×10⁶个细胞(10 µL),注射器插入深度相对于前囟为2 mm。注射细胞悬液后,钻孔用Heliobond(义获嘉伟瓦登特,沙恩,列支敦士登)覆盖,头皮用缝线缝合。术后两天,为动物口服安乃近(150-200 mg/kg/天,添加在饮用水中)以进行术后镇痛。另外3只假手术动物接受了相同的手术程序,但注射了10 µL不含胶质瘤细胞的PBS。
¶ 2.2.3. 新皮质切片制备
Fischer大鼠在出生后60-80天用乙醚(Avantor Performance Materials,波兰格利维采)麻醉并迅速断头。迅速取出大脑,浸入冰冷的、充氧(95% O2/5% CO2)的解剖液中,解剖液成分如下(单位:mmol/L):87氯化钠、25碳酸氢钠、2.5氯化钾、1.25磷酸二氢钠、0.5氯化钙、7氯化镁、10 D-葡萄糖和75蔗糖,调整pH至7.4,渗透压为320-330 mOsm/L。在冰冷的、持续通 carbogen 的解剖液中,使用振动切片机(Leica VT1200,德国韦茨拉尔)制备感觉运动皮层冠状切片(300 μm)。我们确保假手术组和荷胶质瘤组大鼠切片的大体健康区域具有可比性(假手术组切片:10.0±1.8 mm²,均值±标准差,n=10;荷胶质瘤组切片:10.3±1.3 mm²,n=12)。
随后,将切片转移至一个浸没式孵育 chamber 中,该 chamber 含有经碳合气鼓泡的人工脑脊液(aCSF),其成分如下(单位:mmol/L):124氯化钠、26碳酸氢钠、3氯化钾、1.25磷酸二氢钠、2.5氯化钙、1.5氯化镁和10 D-葡萄糖,pH调至7.4,渗透压为304–312 mOsm/L。切片在该aCSF中于室温下保存1–6小时。在转移至微电极阵列(MEA)之前,将切片在改良的aCSF中预孵育80–110分钟,改良aCSF包含8 mmol/L氯化钾、0 mmol/L氯化镁和50 µmol/L 4-氨基吡啶(4-AP;Tocris,英国布里斯托尔)。我们的初步研究(Forberger等人,2025,Lange等人,2020)表明,通常在40–60分钟时可观察到稳定的网络活动。
对一小部分脑切片进行了苏木精-伊红染色的组织学分析,以验证微电极阵列(MEA)对组织的穿透情况并确认胶质瘤的侵袭。与微电极阵列相邻的切片显示出与电极穿透一致的空泡间隙(补充图1)。
¶ 2.3. 多电极阵列
在电生理记录中,借助体视显微镜(S9i,徕卡体视显微镜,德国韦茨拉尔)的引导,将冠状脑切片转移至3D高清微电极阵列芯片(CorePlate 1 W 38–60,3Brain公司,瑞士普费菲孔ZH)的记录表面,并用切片固定器(3Brain公司,补充图2)固定。该设备的有效区域为3.8×3.8毫米,配备4096个电极(20×20微米,间距60微米,高度90微米)。使用与BioCAM DupleX采集平台(3Brain公司)相连的3D高清微电极阵列芯片,以19.75千赫兹的采样率对感觉运动皮层的细胞外活动进行持续10分钟的记录。数据采集时采用50赫兹的高通滤波器对数据进行滤波。我们记录了10个假手术大鼠的脑切片和12个胶质瘤荷瘤动物的脑切片的活动。
¶ 2.4. spike分类
spike排序是一种计算技术,用于从多神经元细胞外记录中分离不同神经元的单个电脉冲(“spike”)。其工作原理是检测spike,提取其特征,然后将它们分组为簇,每个簇(以下称为单位)理想情况下代表一个不同的神经元。
原始记录(保存为*.brw文件)被分块加载,并以无符号16位整数的形式存储为二进制格式,这使得通过SpikeInterface(0.101.2版本(Buccino等人,2020))能够更高效地加载。通过SpikeInterface使用Kilosort4(4.0.37版本(Pachitariu等人,2024b))进行 spike 分选,其参数经过专门调整以适应我们的记录系统(表1,(Pachitariu等人,2024a))。我们使用NVIDIA GeForce RTX 3060进行Kilosort4基于PyTorch的计算,每个记录的 spike 分选时长约为两小时。
¶ 表1. 与默认设置不同的尖峰分选参数。
| 变量 | 值 | 注释 |
|---|---|---|
| nt | 建议的设置为2×(2毫秒内的采样点数)+1。 | |
| 最小模板尺寸 | 20(微米) | 默认值为10微米,这仅适用于比我们的MEA系统中发现的接触更近的接触。 |
| 最小距离、最小水平距离 | 60(微米) | 垂直和水平电极间距。 |
| x中心 | 每隔200–300 μm应设置中心。 | |
| 最大通道距离 | 85(微米) | 大约是电极之间的对角线距离。 |
通过目视检查发现未被脑片覆盖的通道会被排除在尖峰排序之外,以节省计算资源。
对于每个记录,我们分离出了推定的单单位活动(SUA)。Kilosort4通过基于其相关图计算指标来确定经过 spike 分选的单位是分离良好的,还是包含多单位活动(Pachitariu 等人,2024b)。需要注意的是,此处使用的 Kilosort 自相关图阈值默认值 0.2 与 Pachitariu 等人使用的 0.1 不同。我们将平均放电率高于 1 Hz 且被 Kilosort4 标记为“良好”的 spike 分选单位归类为推定的 SUA。
¶ 2.5. 单单位活动(SUA)分析
我们利用单个单位动作电位(SUA)的放电模式来比较总体趋势,并识别胶质瘤荷瘤切片与假手术切片中SUA的差异。为分析放电模式,我们为每个分离出的单个单位计算了自相关图,其箱宽为0.5毫秒,最大滞后为100毫秒。随后,每个自相关图都通过其L2范数进行归一化处理。我们采用主成分分析(PCA)进行降维,选取了能解释约90%方差的前108个成分用于k均值聚类。k均值聚类采用scikit-learn的默认设置进行。聚类的最佳数量通过2到10个聚类结果的轮廓系数来确定。对于每个聚类数量,我们计算了100次不同随机状态下聚类运行的平均轮廓系数。结果显示,2个或3个聚类时获得了最高的平均分数(均为0.20),而4个及以上聚类时分数则急剧下降。我们选择了3个聚类的解决方案,因为它能提供更有意义的分组:聚类1包含的自相关图具有最高的即时放电后概率;聚类2的放电概率范围更广,且大多在100毫秒内;聚类3在200毫秒内没有显示出明显的最大爆发概率(图2)。通过重复抽样成对样本(每组包含80%的数据,共500次)并使用调整后的兰氏指数比较所得聚类,证实了3个聚类解决方案的稳定性。该分析得出的平均调整后兰氏指数为0.933±0.077,表明其具有较高的稳定性。
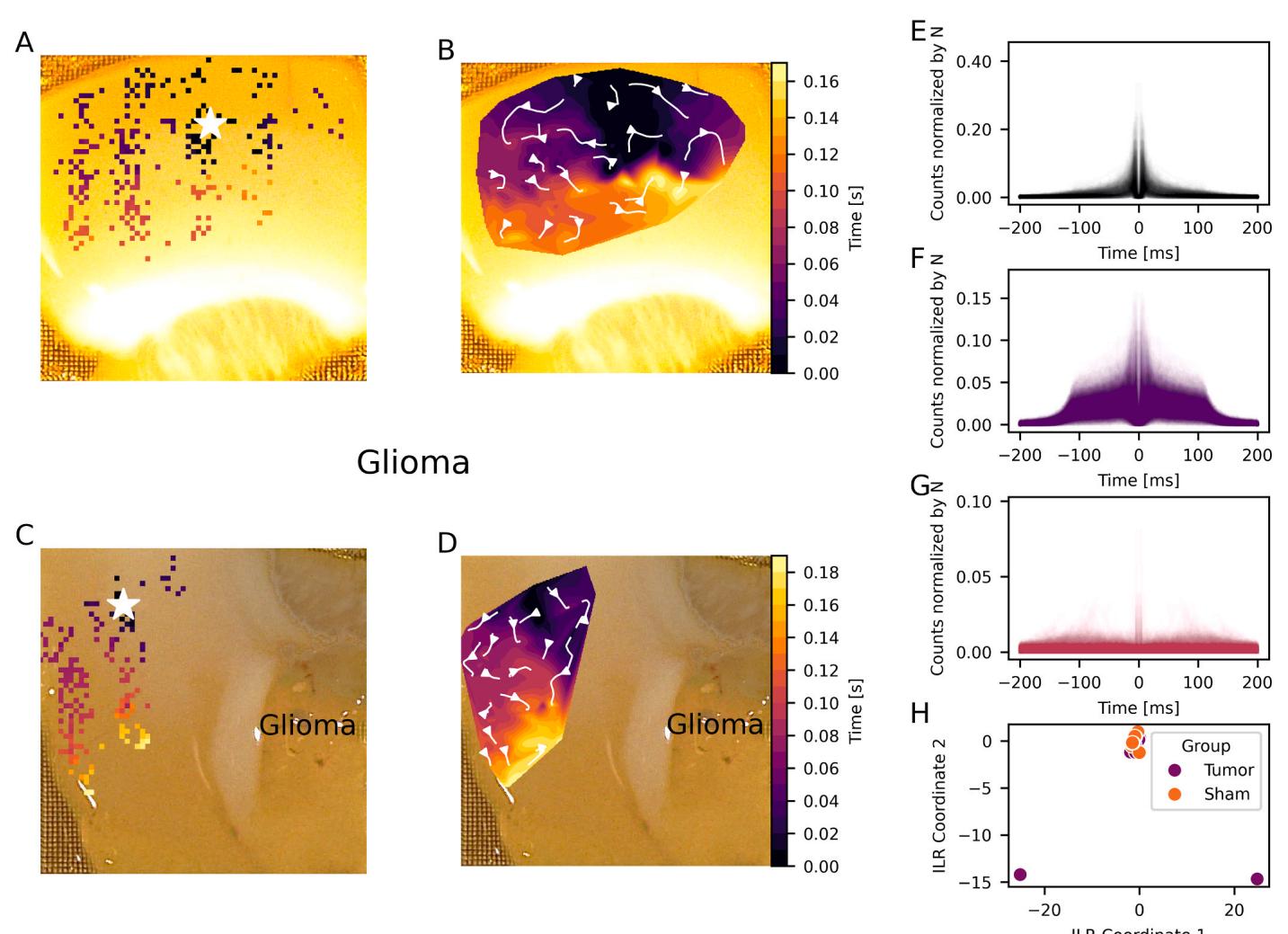
图2. 假手术组和胶质瘤荷瘤组切片中网络爆发的传播及放电模式分析。(A) 单次网络爆发时的切片内活动传播。每个彩色方块代表一个经 spike 分选的单元。颜色表示每个单元爆发活动的起始时间。算法估计的起源用白色星号标记。(B) 根据(A)中所示的爆发起始时间构建的时间表面。白色流线表示根据该时间表面计算出的传播速度。©和(D)显示了胶质瘤荷瘤组切片的爆发起始时间、时间表面和速度流线。(E-G) 三个已识别集群的自相关图。(H) 每个记录所属各集群的相对比例的ILR转换。
对每个组对每个聚类的比例贡献进行了统计分析。对于每个记录,计算了其聚类中属于每个组的百分比。在应用等距对数比(ILR)转换之前,数据中的零值被替换为一个小常数。ILR转换对于成分数据是必要的(Gloor等人,2017)。使用PERMANOVA(scikit-bio,0.7.0版本,Rideout等人,2025)测试了统计显著性。
¶ 2.6. 网络爆发分析
神经元爆发(NBs)采用半自动方式检测。当超过5%的 spike-sorted 单位表现出重叠时间超过5毫秒的爆发活动时,即被定义为神经元爆发。间隔小于100毫秒的神经元爆发会被合并,而持续时间短于50毫秒的则会被舍弃。爆发活动被定义为包含超过5个连续尖峰,且尖峰间间隔为75毫秒或更短,并持续超过7毫秒。(非全网络范围的)爆发检测参数经过优化,以实现高召回率(灵敏度),从而尽可能多地识别潜在的神经元爆发。后续过滤会舍弃过短或爆发单位不足的潜在神经元爆发。额外的人工检查进一步确保只有涉及网络相当一部分的神经元爆发才会被认定为神经元爆发。
我们使用了一个基于Tkinter(8.6版本)和Matplotlib(3.9.2版本)的自定义图形用户界面,这使我们能够手动纠正由噪声伪影引起的网络爆发(NB)误识别。对于单位数量极少或异常多的记录,用于NB识别所需的单位总数百分比阈值会在4%到8%之间手动调整。每个NB的起点和终点以及重新计算参与单位所需的必要信息都被保存下来。需要注意的是,尖峰活动不仅发生在网络爆发期间。因此,本研究中NB的阈值选择方式是,仅用NB这一术语来描述多个位置同时发生的高频尖峰活动。需要注意的是,在识别NB的过程中,我们没有排除包含多单位活动(MUA)的尖峰分类单位。
我们NB分析中的一小部分子集也与使用BrainWave6(3brain AG,补充表3)分析的数据进行了比较。
¶ 2.6.1. 网络爆发起源的估计
每个经过 spike-sorted 处理的单元中心所对应的电极,是通过确定那个在该单元中具有由 Kilosort4 学习到的最大尖峰模板平方和的电极来确定的。
为了估计每个NB的空间起源,首先按照事件期间出现爆发的 spike-sorted 单位及其相关电极在NB内的首次尖峰时间进行排序。目的是先排除可能与NB无关的时间异常值,然后通过计算参与NB的最早单位的质心来估计NB的起源。
通过基于尖峰空间坐标及其关联时间值(记为点pi)的局部邻域统计方法,剔除了尖峰时序中的异常值。在二维空间中,为每个点pi识别最多10个可用邻点(不计入pi本身)。针对每个点,计算其在神经元网络(NB)期间首次尖峰的局部加权平均时间。点pi与邻点pj的权重wij依据公式(1)计算:i为待分析点的索引,j为遍历点i对应邻点集合的迭代索引。
dij描述了点pi和pj之间的欧氏距离。σ描述了一个常数,在我们的案例中,该常数等于电极间距(60微米)。
随后,我们计算了加权局部平均时间 t̄iw(2)。
其中tj表示第j个邻居的时间值。邻居时间值的加权局部标准差siw通过公式(3)计算得出。
当点pi自身的时间ti与其计算出的局部加权平均时间tiw之间的绝对差值超过t的加权局部标准差的两倍时,该点被识别为时间异常值。
接下来,计算了前10%的放电电极中至少有一个邻居在0.95毫米范围内的最大子集。该子集的质心被定义为NB原点(图2A和C中的白色星号)。上述去除离群值的方法减轻了由孤立的随机放电导致的不准确性,否则这些不准确性可能会使原点估计产生偏差。
由于Kilosort4在3brain HD-MEA系统上的准确性尚未得到广泛验证,我们将通过Kilosort得出的神经元爆发(NB)起源与通过一种独立方法获得的结果进行了比较:我们对随机选择的NB在5–20毫秒间隔内计算的通道-wise标准差热图进行了视觉检查(图3B、F)。我们发现,两种方法得出的NB传播情况在视觉上没有明显差异。
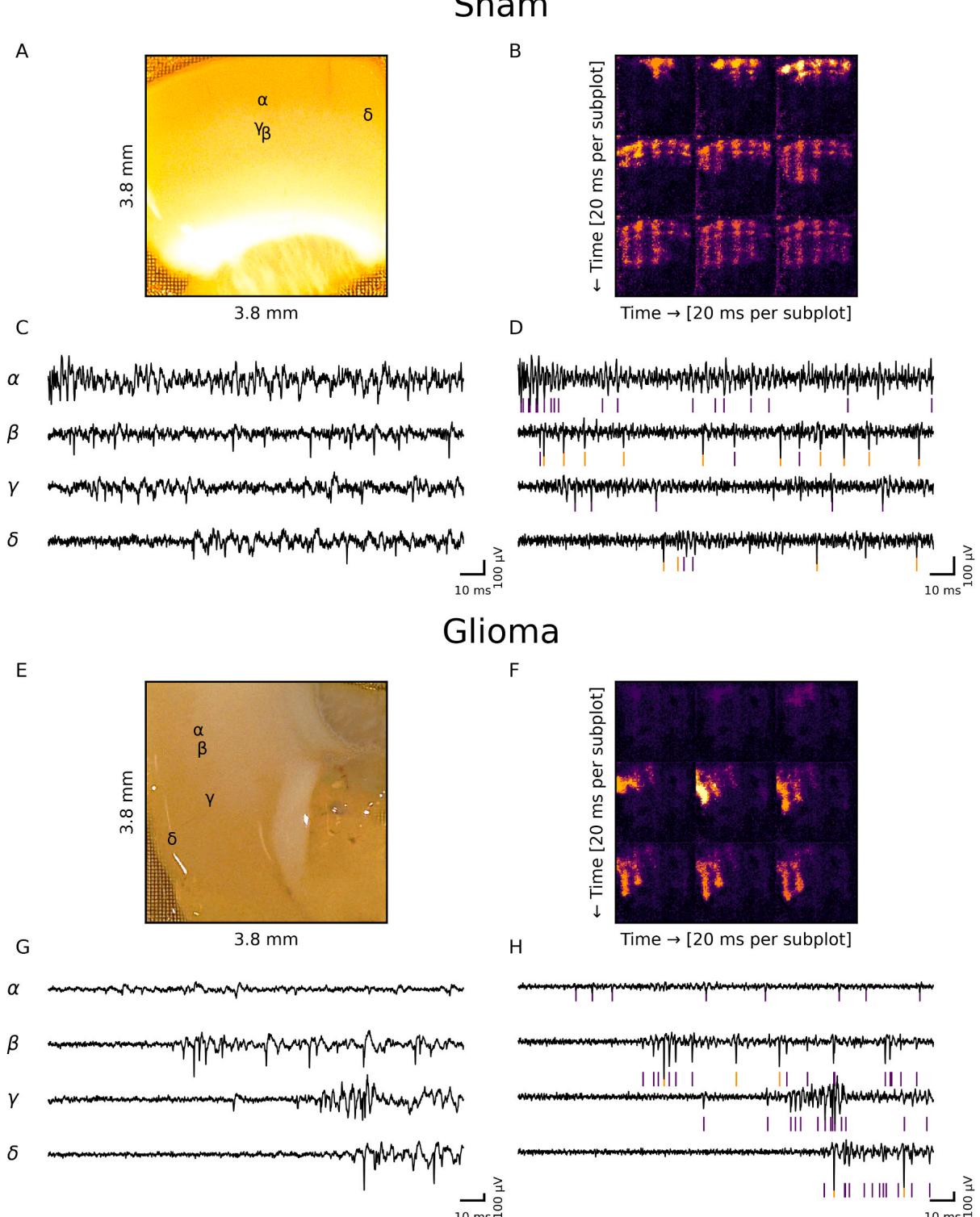
图3. 典型的网络爆发事件。(A) 放置在MEA上的假手术动物脑切片照片。(B) 九个热图,代表网络爆发开始后20毫秒间隔内通道的标准差。© 用50Hz硬件高通滤波器记录的轨迹。它们在切片上的位置用希腊字母表示。(D) 300Hz高通滤波后与©相同的轨迹。检测到的尖峰用彩色垂直线表示。如果一个电极检测到多个单元,尖峰将用不同颜色表示。(E) 放置在MEA上的胶质瘤荷瘤动物脑切片照片。(F) 九个热图,代表网络爆发开始后20毫秒间隔内通道的标准差。(G) 用50Hz硬件高通滤波器记录的轨迹。它们在切片上的位置用希腊字母表示。(H) 300Hz高通滤波后与(G)相同的轨迹。检测到的尖峰用彩色垂直线表示。如果一个电极检测到多个单元,尖峰将用不同颜色表示。
为了评估神经母细胞瘤(NBs)的发生相对于胶质瘤是否存在任何空间趋势,我们对切片进行了对齐,并将所有分析数据配准到一个共同的坐标系中。未观察到明显的空间趋势(补充图3和补充表1)。
¶ 2.6.2. 活动轨迹中心
为了评估神经元活动的传播情况,我们计算了跨事件的活动中心(CoA)轨迹(CoAT)。CoAT的实现类似于Chao等人(Chao等人,2007年),如公式4所示:
CoAx是活动中心的x坐标,CoAy是活动中心的y坐标。ai是第i个 spike sorted单元的活动水平(峰值频率)。xi和yi分别是第i个 spike-sorted单元的x坐标和y坐标。N是spike-sorted单元的总数。然后,从每个NB中选取35毫秒长的活动窗口来计算这个CoA,得到CoAT。窗口重叠25毫秒。需要注意的是,我们在计算CoAT时没有排除MUA。
¶ 2.6.3. 网络爆发传播速度
为了计算爆发活动的传播速度,我们根据爆发开始时间构建了一个时间面。该时间面的梯度使我们能够计算整个空间域内的传播速度。如2.5.1节所述,异常的爆发开始时间已预先进行了过滤。
每个爆发事件的数据包括一组稀疏的电极坐标(xi,yi)及其相应的爆发起始时间(ti)。
首先,通过将这些稀疏数据点插值到覆盖MEA空间范围的高分辨率二维网格(200×200个点)上,生成了一个连续的激活时间表面T(x, y)。这种插值采用三次方法(scipy.interpolate.griddata)进行,选择该方法是为了得到适合稳定梯度计算的平滑表面。
接下来,使用二阶中心差分格式(numpy.gradient)在每个网格点上对该时间面的梯度∇T = (∂T/∂x, ∂T/∂y)进行了数值计算。任意点(x, y)处的传播方向指向负梯度-∇T的方向。
局部传播速度s(x, y)与梯度的大小成反比。梯度越陡,表示波前越慢,因为在更短的距离上会花费更多时间。速度计算如下(5):
这种计算生成了一个二维“速度图”,该图表示网格上每个点的局部传播速度。位于有效电极凸包之外的网格点被屏蔽,并排除在分析之外。每个事件的单一代表性传播速度通过计算图中所有有效速度值的中位数来确定,因为中位数比平均值对插值伪影和异常值的敏感性更低。
通过从负梯度向量场(-∂T/∂x,-∂T/∂y)生成流图,对传播路径进行了可视化。
¶ 2.7. 功能连接分析
为了描述经过峰电位分选的单位如何相互作用,尤其是在爆发期(NBs)期间,我们使用NetworkX(3.5版本)和nx-cugraph(25.04.00版本)构建了无向图,其中将分离良好的单位(平均发放率高于1Hz,Kilosort4标记为“良好”)作为节点。此外,我们只考虑在至少25%的爆发期内表现出爆发活动的单个单位。这一步骤似乎消除了我们认为主要包含噪声的大多数单单位活动(SUA)。节点之间的边由峰电位时间平铺系数(STTC,Cutts和Eglen,2014)加权,该系数是在5ms的Δt下计算的。为了高效处理高密度微电极阵列(HD-MEA)生成的大型数据集,我们修改了elephant库(1.1.1版本,Denker等人,2018)中的STTC实现,使其可通过Numba(0.61.2版本)进行部分编译。Δt的选择基于每个记录中从一个60秒长的片段计算出的互相关直方图数据。大多数记录显示,在5ms的Δt下,经过峰电位分选的单位之间存在相当强的相关性。STTC提供了一种与频率无关的峰电位“相关性”测量方法。我们没有观察到相关的负值(<−0.1),因此通过仅在STTC超过0时建立边来简化基于图的计算。
我们针对每个图(即每个切片)评估了以下指标:
全局加权效率(Latora和Marchiori,2001):全局效率衡量信息在整个图中交换的效率。在我们的加权图中,节点(分离良好的 spike-sorted 单元)之间的“距离”定义为1-STTC。全局效率通过计算网络中所有节点对之间最短路径长度倒数的平均值得到。较高的全局加权效率表明,平均而言,记录切片中任意两个 spike-sorted 单元能够通过具有强功能连接的路径(路径上的STTC值较高)有效地相互影响。这反映了网络的整体信号传播能力,在本研究中即指癫痫样活动在网络较远部分之间的传播能力。
平均加权聚类(瓦茨和斯托加茨,1998):单个节点的聚类系数用于衡量其直接功能伙伴(图中的邻居)彼此之间的功能连接强度。“加权”意味着会考虑这些连接的强度(STTC值)。较高的平均加权聚类系数表明,经过 spike 分选的单元具有形成紧密结合的局部功能组的强烈趋势。
平均加权节点强度(Fornito等人,2016a):在加权图中,节点的强度是连接到该节点的所有边的权重之和。在此,对于特定单元,其强度是该单元与其连接伙伴共享的所有STTC值的总和。平均加权节点强度就是网络中所有单元的这些个体强度的平均值。平均加权节点强度反映了所记录的神经群体内整体同步的一般强度。较高的平均强度表明,总体而言,各单元与其相连的相邻单元在放电模式上表现出强烈的时间“相关性”。
模块化分数(Fornito 等人,2016b):在图论中,模块化是一种量化网络或图可被划分为不同社区或模块程度的指标。在我们的研究中,使用 Louvain 社区检测算法,以 NetworkX 中实现的默认参数来识别社区。模块化分数通过评估社区内部的连接是否比随机预期的更多,以及不同社区之间的连接是否更少,来衡量这种划分的强度。在 spike-sorted 单元的功能网络背景下,较高的模块化分数表明神经群体组织成了不同的、半独立的功能集合。
为了探究网络指标是否受NB持续时间的影响,我们计算了NB持续时间与图指标之间的斯皮尔曼相关性。所有相关性均未达到显著水平(补充数据1)。
¶ 3. 结果与讨论
在本研究中,我们提出了一种详细的方案,利用高密度多电极阵列(HD-MEA)记录携带F98胶质瘤的 Fischer 大鼠急性 neocortical 切片中药物诱导的爆发性网络活动。我们成功记录了去抑制后的网络爆发(NBs),并分析了它们的空间起源、传播模式以及 spikes 活动的网络级相互作用。
通过将急性脑切片在不含Mg2+、含8 mmol/L K+和50 µmol/L 4-氨基吡啶的去抑制溶液中孵育长达110分钟,化学诱导网络活动,之后进行记录。该模型会对兴奋性谷氨酸能活动(Mody等人,1987年)和GABA能抑制性神经元(Codadu等人,2019年,Lado等人,2022年)产生去抑制作用。这种强烈的去抑制作用与其他研究形成对比,其他研究通常在引入去抑制溶液后立即评估活动,且这些溶液往往基于改良的细胞外离子浓度或药理学离子通道抑制。这些模型常被用于评估胶质瘤周围网络的过度兴奋性(Campbell等人,2012年,Gill等人,2020年)。相比之下,我们这种延长的、强烈的去抑制方法通过评估网络持续放电活动的能力来评估其完整性和健康状况。此外,我们研究中提出的数据分析方案也可轻松应用于更早出现的或去抑制程度较低的放电活动。
本研究的一个主要局限性在于样本量较小,包括来自4只动物的12个携带胶质瘤的切片和来自3只动物的10个假手术切片。虽然该样本量足以证明所提出的高密度微电极阵列(HD-MEA)方法和数据分析流程的可行性及实用性,但这对我们研究结果的可解释性构成了显著限制。我们认为,我们的研究结果可为未来更大规模的研究奠定基础,这些研究旨在确凿地描述F98胶质瘤对新皮质网络功能的影响。
¶ 3.1. spike 分选
spike分选通常被认为是准确分析多电极数据的基础,因为它能够将单个spike分配给特定的神经元(Pachitariu等人,2024b,Quiroga,2012,Wu等人,2025)。然而,直接通过spike分选得到的单元可能仍然包含多单元活动和噪声。因此,如果目标只是分析单单元活动(SUA),就必须对初始spike分选得到的输出进行进一步处理。
在本研究中,平均放电率>1Hz且Kilosort4标记为“良好”的经过锋电位分选的单位被归类为推定的单单位活动(SUA)。锋电位分选在大多数记录中识别出了大量这类推定的、分离良好的单神经元单位(图4)。

图4. 良好分离的 spike-sorted 单位数量。假手术大鼠和胶质瘤大鼠的切片之间,良好分离的 spike-sorted 单位数量没有显著差异(Mann-Whitney U检验:p = 0.41;假手术组中位数=49.5,胶质瘤组中位数=42.0)。须线延伸至位于上下四分位数1.5个四分位距内的点。
Kilosort系列算法此前已应用于涉及脑切片和细胞培养的体外实验,包括那些使用高密度微电极阵列(HD-MEAs)的实验(Andrews等人,2024,Habibey等人,2022,Zhao等人,2023)。然而,据我们所知,Kilosort算法尚未用于分析急性新皮质脑切片。基于已识别的单个单位活动(SUAs)数量,我们得出结论:Kilosort4非常适合在合理的时间范围内从离体高密度微电极阵列系统中识别单个单位活动(参见2.4),这证实了Kilosort4能够扩展应用于现代微电极阵列系统的大量电极。
¶ 3.2. 单单位分析
基于自相关图,使用k均值算法将分离良好的单个单位聚为三个集群,形成三个不同的组(图2)。集群1的自相关图具有最高的即时发射后概率。集群2的发射概率范围更广,大多在100毫秒内,而集群3在200毫秒内没有明显的最大爆发概率(图2)。各组对集群的贡献没有显著差异:平均值±标准差:肿瘤组:集群1:0.20±0.15,集群2:0.35±0.21,集群3:0.45±0.16。假手术组:集群1:0.16±0.09,集群2:0.56±0.15,集群3:0.27±0.17(p=0.33,置换多元方差分析)。
虽然可以在特定条件下从放电模式中推断出神经元亚型(Connors 和 Gutnick,1990,Jia 等人,2019,Venkadesh 等人,2019),但目前尚无关于长时间处于强去抑制状态的神经元的经过验证的数据。
¶ 3.3. 网络爆发分析
¶ 3.3.1. 网络爆发持续时间和频率
假手术对照组切片的平均NB持续时间显著长于胶质瘤荷瘤动物切片(假手术组中位数:0.85秒,胶质瘤组:0.41秒,p = 0.001,Mann-Whitney U检验,图5A)。
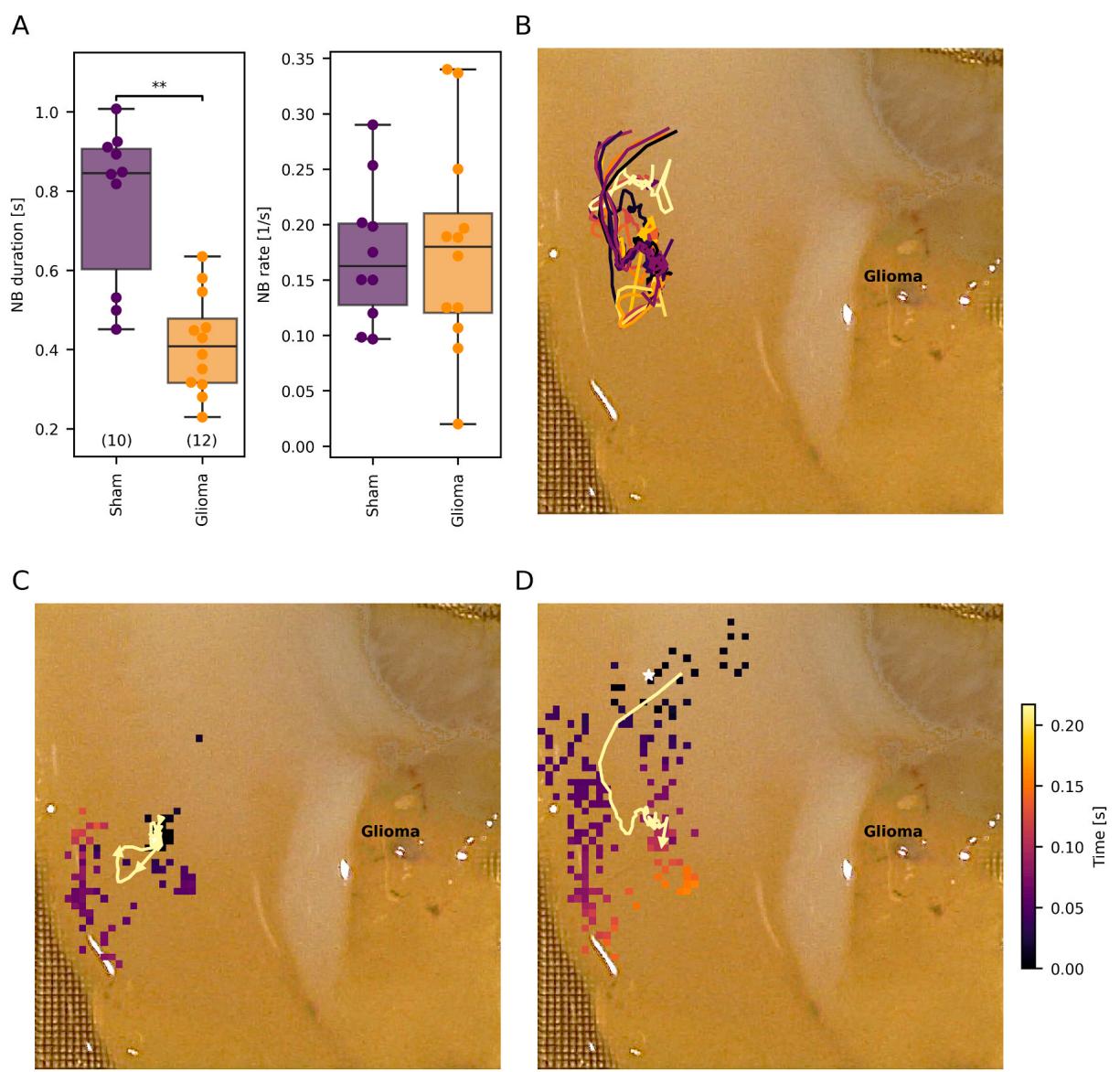
图5. 网络爆发(NB)指标和活动中心轨迹。(A)NB持续时间和速率的箱线图( whisker定义与图4相同)。(B)投射到切片上的示例性活动中心轨迹。(C)局部NB事件在切片小部分区域传播的可视化。(D)一个较大的NB,叠加了活动中心轨迹。彩色方块表示爆发开始时间,白色星号标记NB的估计起源。
然而,两组之间的NB发生率未观察到显著差异(假手术组:0.16次/秒 vs 胶质瘤组:0.18次/秒,p = 0.974,Mann-Whitney U检验)。
在10分钟的记录期内,这些指标未观察到显著变化(补充表2)。
其他研究表明,胶质瘤周围组织中癫痫样事件的发生频率有所增加。然而,这些研究对去抑制的研究时间早于我们的实验,此外,它们仅使用了基于低镁/零镁的去抑制模型(Campbell 等人,2012,Gill 等人,2022,Gill 等人,2020)。相比之下,我们的模型采用了持续且更有效的去抑制方法,因此能够提供关于神经网络维持长时间活动的资源信息,而非即时的过度兴奋,因为长时间的尖峰活动可能导致细胞死亡(Kovac 等人,2012)。这可能解释了为什么我们的模型中,携带胶质瘤的切片和假手术切片之间的NB率没有差异,而参考文献(Campbell 等人,2012,Gill 等人,2022,Gill 等人,2020)中描述携带胶质瘤的脑组织中癫痫样活动的发生率有所增加。
¶ 3.3.2. 网络爆发的传播模式
为了评估NB在切片内的传播情况,我们计算了每个NB的起源,然后在其整个持续时间内追踪最高活动中心的移动,以计算活动中心轨迹(图5B)。
不同神经爆发(NBs)的估计起源存在显著差异,但没有任何神经爆发起源于第1层切片的顶部附近。对于其他任何组织学层(补充图4)或与胶质瘤的特定距离,均没有特定偏好。尽管在切片的所有区域都检测到了爆发活动,且推测这些区域与多电极阵列(MEA)系统接触良好(图2A),但一些神经爆发仍局限于较小的区域(图2C)。鉴于神经爆发起源的变异性,可以预期并证实,活动中心的轨迹也会有所不同。
Pallud等人(2014年)描述了发作间期放电,其定义为与多单位活动爆发相关的场电位,这种放电会自发产生,且更易出现在肿瘤周围胶质瘤组织的3/4层。另一方面,4-AP模型引发的电放电被描述为发生在5/6层(Rheims等人,2008年)。有报道称,零镁模型诱导的癫痫样活动会出现在所有层中,但在每次记录中都保持稳定(Tsau等人,1999年)。因此,我们的研究兼具胶质瘤存在、去抑制条件(4-AP、高钾和零镁)以及较长的预孵育期(而非在去抑制后立即记录)等特点,其理应具有不同的特性。
分析神经爆发(NB)起源和轨迹的主要限制在于切片与电极之间接触质量的可变性。通常,每个切片都存在电极接触不良的区域。如果神经爆发起源于这样的区域,其表面起源会被错误地识别为活动首次到达多电极阵列(MEA)系统中连接良好区域的点。
我们尝试通过用平行金属线网固定切片来缓解这个问题(补充图2),金属线施加的压力改善了接触。我们推测,在未来的研究中,通过减小金属线之间的距离,信号质量可以得到进一步提升,这可能有助于从切片的所有区域持续获得高质量的记录。
两组之间NBs的传播速度没有显著差异,但假手术动物切片中的活动传播有明显加快的趋势(假手术组中位数:10.51毫米/秒,胶质瘤组中位数:8.25毫米/秒,p=0.06,图6E)。
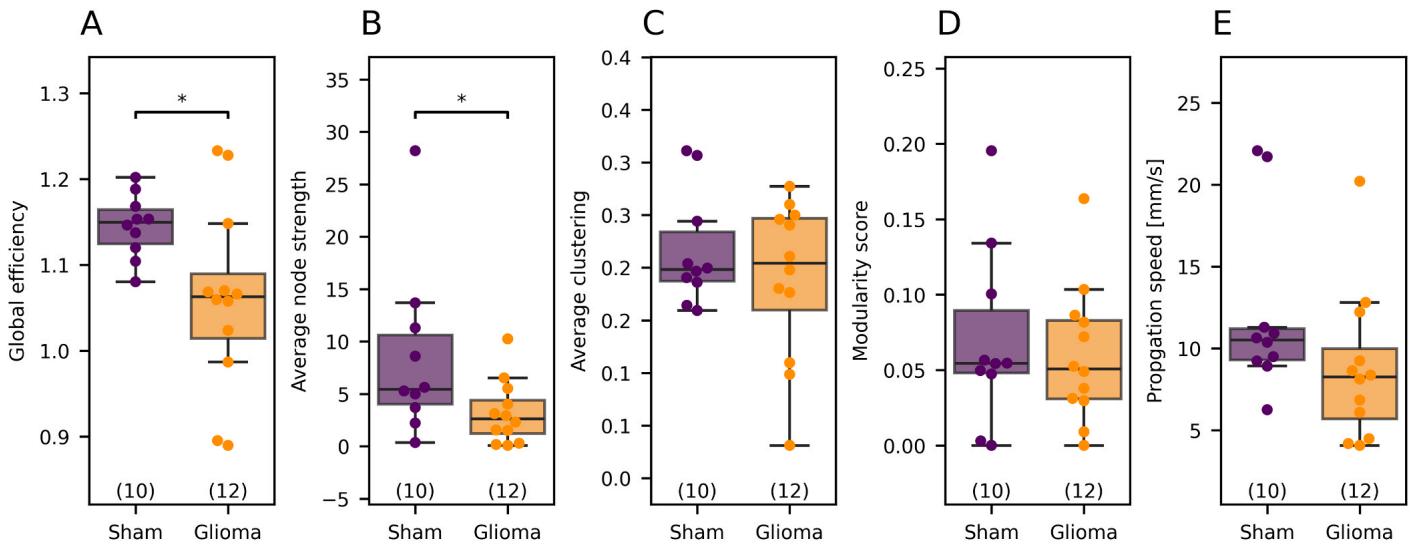
图6. 基于STTC值和传播速度的图论指标。(A)假手术网络显示出显著更高的全局效率(*p = 0.0229)和(B)平均节点强度(*p = 0.0443)。然而,(C)平均聚类系数(p = 0.7667)和(D)模块化分数(p = 0.7169)没有显著差异。(E)传播速度没有显著差异(p = 0.0602),但胶质瘤切片的传播速度有明显降低的趋势。须线延伸至位于上下四分位数1.5倍四分位距内的点。p值参考曼-惠特尼U检验。
为了评估事件的发生相对于胶质瘤是否存在任何空间趋势,我们对切片进行了对齐,并将所有分析数据配准到一个共同的坐标系中。未观察到明显的空间趋势(补充图3和补充表1)。
¶ 3.4. 功能连接分析
仅分析单个神经元的特征和个体SUA(单单位活动)对网络层面的神经元相互作用的了解有限。为了研究这些相互作用,我们使用频率无关的尖峰时间拼接系数(STTC,(Cutts和Eglen,2014))构建了功能连接图。然后,我们使用Mann-Whitney U检验比较了假手术组和荷瘤组切片的关键图论指标:假手术组切片的网络显示出显著更高的全局效率(基于中位数的倍数变化:与肿瘤组相比为0.92倍,p = 0.0229)和平均节点强度(0.48倍,p = 0.0443)。然而,平均聚类系数(1.03倍,p = 0.7667)和模块化得分(0.93倍,p = 0.7169)没有显著差异(图6)。因此,假手术动物的切片表现出显著更整合和更高效的网络拓扑结构。
我们的网络分析显示,在带有胶质瘤的切片中,功能连接受到显著破坏。肿瘤切片中较低的全局效率表明网络处于功能连接较弱的状态。节点强度的降低表明,胶质瘤切片中的神经元形成紧密连接的局部功能群的倾向较弱,并且其放电模式的时间相关性更弱或更少。
我们的网络分析显示,在带有胶质瘤的切片中,功能连接性受到了显著破坏。肿瘤切片中较低的全局效率表明其处于功能连接较弱的网络状态。节点强度的降低意味着胶质瘤切片中的神经元形成紧密连接的局部功能群的倾向较弱,并且在其放电模式中表现出较弱或较少的时间相关性。
F98胶质瘤模型的高浸润性可能是导致胶质瘤切片中功能较弱的连接网络以及较短的神经爆发(NBs)的一个潜在原因。已知这种胶质瘤会侵袭相邻的脑组织,形成孤立的“岛”和血管周围的肿瘤细胞簇(Mathieu等人,2007;Sahu等人,2022),这可能会从物理上破坏已建立的突触连接和电路完整性。这种物理破坏在逻辑上会导致整体整合效率降低(效率下降)。
¶ 4. 结论
本研究开发了一种稳健的方案,使用64×64高密度多电极阵列来研究胶质瘤在急性大鼠脑切片中引起的网络兴奋性和活动传播变化。该方案包括胶质瘤细胞植入、脑切片制备以及侧重于网络爆发(NBs)的详细数据分析。我们使用Kilosort4进行 spike 分选以识别NBs,观察到携带胶质瘤的切片中NBs的持续时间比假手术对照组短。我们还确定了NBs的起源、轨迹和传播速度。基于 spike 时间平铺系数(STTC)的功能连接图分析揭示了两组之间不同的网络级相互作用。该方案为未来旨在分析脑切片中NBs和功能连接的研究提供了可靠的平台。
¶ CRediT作者贡献声明
法尔科·兰格:写作——审阅与编辑、构思。吕迪格·柯林:写作——审阅与编辑。蒂莫·基希施泰因:写作——审阅与编辑、监督、构思。法比亚娜·桑塔纳·克拉盖隆德:写作——审阅与编辑、调研。费迪南德·福尔贝格尔:写作——初稿、可视化、验证、软件、方法、调研、形式分析、数据整理。卡特琳·波拉斯:写作——审阅与编辑、调研。
¶ 资助
本研究未获得公共、商业或非营利部门资助机构的任何专项拨款。
¶ 利益冲突声明
作者声明不存在利益冲突。
¶ 致谢
作者们要感谢Silke Birkmann、Hanka Schmidt和Simone Rackow提供的出色技术支持。
¶ 补充材料
1-s2.0-s0165027025002675-mmc1.pdf
¶ 参考文献
¶ 参考文献
- 阿梅代伊 C, 库什纳 DS. 与脑肿瘤相关的运动功能障碍的临床意义[J]. 神经肿瘤学实践, 2015, 2:179-184. https://doi.org/10.1093/nop/npv017
- 安德鲁斯 JP, 耿 J, 沃伊蒂克 K, 等. 人类海马切片中网络活动和光遗传学干预的多模态评估[J]. 自然·神经科学, 2024, 27:2487-2499. https://doi.org/10.1038/s41593-024-01782-5
- 巴伦 T, 亚尔钦 B, 苏 M, 等. 弥漫性中线胶质瘤中的γ-氨基丁酸能神经元-胶质瘤突触[J]. 自然, 2025, 639:1060-1068. https://doi.org/10.1038/s41586-024-08579-3
- 巴特 RF, 考尔 B. 实验神经肿瘤学中的大鼠脑肿瘤模型:C6、9L、T9、RG2、F98、BT4C、RT-2和CNS-1胶质瘤[J]. 神经肿瘤学杂志, 2009, 94:299-312. https://doi.org/10.1007/s11060-009-9875-7
- Biasibetti E, Valazza A, Capucchio MT, 等. 利用MRI和组织病理学评估对同种异体和同基因大鼠胶质瘤模型的比较[J]. 比较医学, 2017, 67:147-156
- 布奇诺 AP, 赫尔维茨 CL, 加西亚 S, 等. SpikeInterface,一个用于spike sorting的统一框架[J]. eLife, 2020, 9:e61834. https://doi.org/10.7554/eLife.61834
- 坎贝尔 SL, 白金汉 SC, 桑泰默 H. 人类胶质瘤细胞诱发皮质网络过度兴奋[J]. 癫痫, 2012, 53:1360-1370. https://doi.org/10.1111/j.1528-1167.2012.03557.x
- 赵 ZC, 巴库姆 DJ, 波特 SM. 模拟和活体皮质网络中区域特异性网络可塑性:活动轨迹中心(CAT)与其他统计数据的比较[J]. 神经工程杂志, 2007, 4:294-308. https://doi.org/10.1088/1741-2560/4/3/015
- Codadu NK, Graham RT, Berman RJ, 等. 癫痫样发作的不同路径[J]. 生理学报告, 2019, 7. https://doi.org/10.14814/phy2.14226
- 康纳斯 BW, 古特尼克 MJ. 不同新皮质神经元的内在放电模式[J]. 神经科学趋势, 1990, 13:99-104. https://doi.org/10.1016/0166-2236(90)90185-D
- 卡茨 CS, 埃格伦 SJ. 检测脉冲序列中的成对相关性:方法的客观比较及其在视网膜波研究中的应用[J]. 神经科学杂志, 2014, 34:14288-14303. https://doi.org/10.1523/JNEUROSCI.2767-14.2014
- 登克 M, Yegenoglu A, Green S. 使用Elephant框架在HBP协作平台上实现的支持高性能计算的协同工作流[C]//神经信息学, 2018:P19. https://doi.org/10.12751/incf.ni2018.0019
- 德雷克斯勒 R, 德林嫩贝格 A, 加维什 A, 等. 胆碱能神经元活动通过毒蕈碱信号促进弥漫性中线胶质瘤生长[J]. Cell, 2025. https://doi.org/10.1016/j.cell.2025.05.031
- 埃默里 BA, 胡 X, 克吕奇 D, 等. MEA-seqX:大规模电生理和转录网络动态的高分辨率分析[J]. 先进科学, 2025, 12:e2412373. https://doi.org/10.1002/advs.202412373
- Forberger F, 桑塔纳·克拉格鲁德 F, 波拉特 K, 等. Cenobamate降低了离体F98大鼠胶质瘤模型中的癫痫样活动[J]. 神经科学前沿, 2025, 19:1629259. https://doi.org/10.3389/fnins.2025.1629259
- Fornito A, Zalesky A, Bullmore ET (编). 模块性[M]//脑网络分析基础. 圣地亚哥:学术出版社, 2016:303-354. https://doi.org/10.1016/B978-0-12-407908-3.00009-1
- Fornito A, Zalesky A, Bullmore ET (编). 节点度与强度[M]//脑网络分析基础. 圣地亚哥:学术出版社, 2016:115-136. https://doi.org/10.1016/B978-0-12-407908-3.00004-2
- Ghadimi K, 阿巴斯 I, 卡兰迪什 A, 等. 不同治疗方式的胶质母细胞瘤(GB)患者的认知功能下降及未治疗病例的见解[J]. 当代肿瘤学, 2025, 32:152. https://doi.org/10.3390/curroncol32030152
- 吉尔 BJA, 吴 X, 汗 FA, 等. 体外多电极分析揭示了胶质瘤浸润边缘发作行为的时空动态[J]. 神经生物学疾病, 2020, 134:104676. https://doi.org/10.1016/j.nbd.2019.104676
- 吉尔 BJA, 汗 FA, 戈德堡 AR, 等. 单单位分析和宽场成像揭示胶质瘤中兴奋性和抑制性神经元的改变[J]. 大脑, 2022, 145:3666-3680. https://doi.org/10.1093/brain/awac168
- Gloor GB, 麦克莱姆 JM, 帕夫洛斯基-格拉恩 V, 等. 微生物组数据集具有组成性:这一点是必然的[J]. 微生物学前沿, 2017, 8:2224. https://doi.org/10.3389/fmicb.2017.02224
- 郭 X, 顾 L, 李 Y, 等. 组织学和分子学上的胶质母细胞瘤,IDH野生型:基于2021年世界卫生组织中枢神经系统肿瘤分类的真实世界情况[J]. 肿瘤学前沿, 2023, 13. https://doi.org/10.3389/fonc.2023.1200815
- Habibey R, Striebel J, Schmieder F, 等. 人干细胞来源的神经元网络在高密度微电极阵列上的长期形态和功能动态[J]. 神经科学前沿, 2022, 16:951964. https://doi.org/10.3389/fnins.2022.951964
- 哈伍德 DSL, 佩德森 V, 巴格尔 NS, 等. 胶质母细胞瘤细胞在浸润的脑组织中会增加notch信号和突触基因的表达[J]. 自然·通讯, 2024, 15:7857. https://doi.org/10.1038/s41467-024-52167-y
- 哈彻 A, 余 K, 迈耶 J, 等. 基于CRISPR的免疫活性胶质母细胞瘤模型中瘤周过度兴奋的发病机制[J]. 临床研究杂志, 2020, 130:2286-2300. https://doi.org/10.1172/JCI133316
- 黄-霍布斯 E, 程 Y-T, 柯 Y, 等. 远程神经元活动通过SEMA4F驱动胶质瘤进展[J]. 自然, 2023, 619:844-850. https://doi.org/10.1038/s41586-023-06267-2
- 贾 X, 西格尔 JH, 贝内特 C, 等. 高密度细胞外探针揭示树突反向传播并助力神经元分类[J]. 神经生理学杂志, 2019, 121:1831-1847. https://doi.org/10.1152/jn.00680.2018
- 科瓦奇 S, 多米扬 A-M, 沃克 MC, 等. 长时间癫痫发作会损害线粒体的生物能量学并诱导细胞死亡[J]. 细胞科学杂志, 2012, 125:1796-1806. https://doi.org/10.1242/jcs.099176
- Kragelund FS, Spiliotis K, Heerdeven M, 等. 苍白球深部脑刺激的全网络效应使肌张力障碍动物模型中异常的小脑皮质活动恢复正常[J]. 神经生物学疾病, 2025, 205:106779. https://doi.org/10.1016/j.nbd.2024.106779
- 拉多 WE, 徐 X, Hablitz JJ. 小鼠躯体感觉皮层中三个GABA能中间神经元亚群对癫痫样活动的调控[J]. 癫痫研究, 2022, 183:106937. https://doi.org/10.1016/j.eplepsyres.2022.106937
- Lange F, Hartung J, Lieber C, 等. 在体内标准放化疗中添加吡仑帕奈可在啮齿类动物F98胶质瘤模型中促进神经保护作用[J]. 神经科学前沿, 2020, 14:598266. https://doi.org/10.3389/fnins.2020.598266
- Lange F, HörnSchemeyer J, Kirschstein T. 胶质母细胞瘤和肿瘤相关性癫痫中的谷氨酸能机制[J]. 细胞, 2021, 10:1226. https://doi.org/10.3390/cells10051226
- 拉托拉 V, 马尔基奥里 M. 小世界网络的高效行为[J]. 物理评论快报, 2001, 87:198701. https://doi.org/10.1103/PhysRevLett.87.198701
- 李 J, 龙 S, 张 Y, 等. 胶质瘤相关癫痫的分子机制及诊断模型[J]. npj精准肿瘤学, 2024, 8:223. https://doi.org/10.1038/s41698-024-00721-8
- 刘 J, 曲 C, 韩 C, 等. 钾通道及其在胶质瘤中的作用:小型综述[J]. 分子膜生物学, 2019, 35:76-85. https://doi.org/10.1080/09687688.2020.1729428
- Mathieu D, Lecomte R, Tsanaclis AM, 等. 同基因Fischer/F98胶质瘤模型的标准化和详细表征[J]. 加拿大神经科学杂志, 2007, 34:296-306. https://doi.org/10.1017/s0317167100006715
- 莫迪 I, 兰伯特 JD, 海涅曼 U. 低细胞外镁诱导大鼠海马切片中的癫痫样活动和扩散性抑制[J]. 神经生理学杂志, 1987, 57:869-888. https://doi.org/10.1152/jn.1987.57.3.869
- Pachitariu M, Sridhar S, Pennington J, 等. 使用Kilosort4进行尖峰分选[J]. 自然-方法, 2024, 21:914-921. https://doi.org/10.1038/s41592-024-02232-7
- Pachitariu M, Pennington J, Carsen S. 何时调整默认设置——Kilosort4 0.0.1文档[OL]. (2024)[2025-10-07]. https://kilosort.readthedocs.io/en/stable/parameters.html
- Pallud J, Le Van Quyen M, Bielle F, 等. 皮质GABA能兴奋促成人类胶质瘤周围的癫痫活动[J]. 科学·转化医学, 2014, 6:244ra89. https://doi.org/10.1126/scitranslmed.3008065
- 金塔尼利亚 CA, 菲茨杰拉德 Z, 卡肖 O, 等. 高密度多电极阵列使皮质脊髓运动神经元的神经元活动和网络分析达到细胞分辨率水平[J]. 科学报告, 2025, 15:732. https://doi.org/10.1038/s41598-024-83883-6
- 基罗加 RQ. Spike排序[J]. 当代生物学, 2012, 22:R45-R46. https://doi.org/10.1016/j.cub.2011.11.005
- Rheims S, Dam A, Ben-Ari Y, 等. 发育中新皮质切片中癫痫发作的层特异性产生和传播:兴奋性GABA能突触的作用[J]. 神经生理学杂志, 2008, 100:620-628. https://doi.org/10.1152/jn.90403.2008
- Rideout JR, Bolyen E, McDonald D, 等. 科学工具包生物/科学工具包生物:科学工具包生物0.7.0[OL]. (2025). https://doi.org/10.5281/zenodo.15988672
- Sahu U, Barth RF, Otani Y, 等. 实验神经肿瘤学研究中的大鼠和小鼠脑肿瘤模型[J]. 神经病理学与实验神经病学杂志, 2022, 81:312-329. https://doi.org/10.1093/jnen/nlac021
- 萨穆德拉 N, 扎卡利亚斯 T, 普利特 A, 等. 胶质瘤患者的癫痫发作:发病率、病因及治疗概述[J]. 神经科学杂志, 2019, 404:80-85. https://doi.org/10.1016/j.jns.2019.07.026
- Stupp R, Mason WP, van den Bent MJ, 等. 放射治疗联合同步和辅助替莫唑胺治疗胶质母细胞瘤[J]. 新英格兰医学杂志, 2005, 352:987-996. https://doi.org/10.1056/NEJMoa043330
- Tantillo E, Vannini E, Cerri C, 等. 锥体神经元和快速放电的GABA能神经元在控制胶质瘤细胞增殖中的不同作用[J]. 神经生物学疾病, 2020, 141:104942. https://doi.org/10.1016/j.nbd.2020.104942
- 泰勒 KR, 巴伦 T, 许 A, 等. 胶质瘤突触招募适应性可塑性机制[J]. 自然, 2023, 623:366-374. https://doi.org/10.1038/s41586-023-06678-1
- 曹秀英, 关丽丽, 吴俊英. 癫痫样活动可在新皮质的多个层中起始:一项光学成像研究[J]. 神经生理学杂志, 1999, 82:1965-1973. https://doi.org/10.1152/jn.1999.82.4.1965
- 文卡德什 S, 科曼丹托夫 AO, 惠勒 DW, 等. 海马神经元定量放电表型的简单模型:内在多样性的全面涵盖[J]. 公共科学图书馆·计算生物学, 2019, 15:e1007462. https://doi.org/10.1371/journal.pcbi.1007462
- Venkataramani V, Tanev DI, Strähle C, 等. 谷氨酸能突触输入到胶质瘤细胞驱动脑肿瘤进展[J]. 自然, 2019, 573:532-538. https://doi.org/10.1038/s41586-019-1564-x
- Venkataramani V, Yang Y, Schubert MC, 等. 胶质母细胞瘤劫持神经元机制以侵入大脑[J]. Cell, 2022, 185:2899-2917.e31. https://doi.org/10.1016/j.cell.2022.06.054
- 文卡特什 HS, 约洪 TB, 卡雷蒂 V, 等. 神经元活动通过神经连接蛋白-3的分泌促进胶质瘤生长[J]. Cell, 2015, 161:803-816. https://doi.org/10.1016/j.cell.2015.04.012
- 文卡特什 HS, 谭 LT, 吴 PJ, 等. 靶向高级别胶质瘤中神经元活动调节的神经连接蛋白-3依赖性[J]. 自然, 2017, 549:533-537. https://doi.org/10.1038/nature24014
- 王 Y, 蒋 T. 理解高级别胶质瘤:分子机制、治疗与综合管理[J]. 癌症通讯, 2013, 331:139-146. https://doi.org/10.1016/j.canlet.2012.12.024
- 瓦茨 DJ, 斯托加茨 SH. “小世界”网络的集体动力学[J]. 自然, 1998, 393:440-442. https://doi.org/10.1038/30918
- 吴 EG, 鲁德齐特 AM, 博伦 MO, 等. 视网膜神经节细胞电图像的分解用于细胞类型和功能推断[J]. 神经工程杂志, 2025, 22:046007. https://doi.org/10.1088/1741-2552/ade344
- 赵 ET, 赫尔 JM, 明茨·赫梅德 N, 等. 一种基于CMOS的高可扩展性柔性神经电极接口[J]. 科学·进展, 2023, 9:eadf9524. https://doi.org/10.1126/sciadv.adf9524