¶ 基于滤波器的视网膜神经节细胞抑制模型:跨物种和跨刺激的比较与泛化
内达·沙希迪1,2,3,费尔南多·罗森布利特1,2,穆罕默德·H·哈尼1,2,海伦·M·施雷耶1,2,马蒂亚斯·米奇4,5,达里奥·A·普罗蒂6,蒂姆·戈利希1,2,7、
¶ 原文下载:2022.12.01.518577.full_origin.pdf
1 德国哥廷根大学医学中心眼科,哥廷根,德国
2 德国哥廷根,哥廷根伯恩斯坦计算神经科学中心
3 德国哥廷根德国灵长类动物研究中心认知神经科学实验室
4 德国灵长类动物中心实验动物科学部,哥廷根,德国
5 德国心血管研究中心,哥廷根合作站点,德国哥廷根
6 澳大利亚新南威尔士州悉尼市,悉尼大学医学科学学院(神经科学)
7 德国哥廷根大学“多尺度生物成像:从分子机器到可兴奋细胞网络”卓越集群(MBExC)
¶ 摘要
兴奋与抑制的二分法是解释神经活动复杂性的典型机制之一。单个神经元中兴奋与抑制相互作用的计算模型旨在研究这种相互作用如何影响神经元的放电反应,并塑造例如感觉刺激的编码方式。在此,我们比较了三种基于滤波器的刺激编码模型在预测美西螈、小鼠和狨猴视网膜神经节细胞对不同类型时间变化视觉刺激的反应方面的性能。这些模型中的抑制是通过刺激滤波器的减法或除法相互作用,或通过反应驱动的反馈模块来实现的。对于大多数神经节细胞,减法模型和除法模型的表现相似,且优于反馈模型以及没有抑制的线性-非线性(LN)模型。减法模型和除法模型之间的比较取决于细胞类型、物种和刺激成分,其中除法模型在不同时间刺激频率和视觉对比度上的泛化能力最佳,而减法模型尤其能捕捉缓慢的时间刺激动态和缓慢的美西螈细胞的反应。总体而言,我们得出结论:除法模型和减法模型非常适合捕捉神经节细胞中兴奋与抑制的相互作用,并强调了这些相互作用的不同时间机制。
¶ 引言
感觉系统能够动态编码具有广泛时间特征的刺激,这反映了自然界中不断变化的场景和自身运动的复杂性。塑造和支持动态刺激编码的一个关键机制被认为在于兴奋与抑制的相互作用,其中抑制包括抑制性突触信号以及细胞内在的负反馈,后者可通过电压依赖性电导来介导。这种兴奋与抑制相互作用的一个简单例子是反应持续时间的限制,这导致视网膜中的细胞1、丘脑外侧膝状体核2以及听觉3和躯体感觉4、5系统中的细胞在对刺激强度的突然变化做出反应时,会产生明显短暂的反应。在许多情况下,这种反应的短暂性可以用抑制性输入相对于兴奋性输入存在短暂延迟来解释,这使得在抑制占据主导之前,存在一个短暂的活动增强机会窗口。
同样,视觉系统中刺激编码的上下文依赖性(例如通过改变背景光照、对比度、刺激大小或刺激运动所发现的)已被抑制性相互作用所捕捉,这些相互作用起到了 divisive 增益调节的作用6-8。
抑制机制或许还能产生刺激整合时间的动态变化,正如基于电导的抑制编码模型所展示的那样9,10。当信噪比低时,这为整合感觉输入提供了一个较长的时间窗口,使神经元能够平均噪声并产生稳健的反应。另一方面,较短的整合窗口能让神经元使其反应与感觉输入的快速波动同步。
为了理解兴奋-抑制相互作用在产生各种反应动态中的作用,人们提出了几种基于滤波器的编码模型。这些模型背后的典型思路是通过独立的时间滤波器捕捉兴奋性和抑制性信号的特性,然后将这些信号组合起来以产生被建模神经元的活动。在这里,我们重点关注三类此类模型,它们分别通过减法抑制、除法抑制以及活动依赖性负反馈来捕捉视网膜神经节细胞(RGC)反应的时间响应特性。对于减法模型和除法模型,抑制是通过对驱动兴奋的同一输入信号应用滤波器,以前馈方式产生的。另一方面,对于反馈模型,抑制是由模型细胞随机产生的尖峰触发的,这些尖峰为抑制性滤波器提供输入。
为了使不同模型的训练算法和优化约束之间的相似度最大化,我们在统一的计算结构中对三个抑制模型以及一个前馈线性-非线性(LN)模型进行了训练和测试。在该结构中,每个模型都可以通过将特定模型参数固定为特定值来实现。我们将这一框架应用于美西螈、小鼠和普通狨猴视网膜记录的视网膜神经节细胞(RGC)反应,这些反应是在全视野白光噪声光强闪烁刺激下获得的。这种统一的实现方式和数据集使我们能够直接比较这些模型,并确定每种模型在哪些细胞类型和刺激类型上表现优于其他模型。
开发编码模型的主要挑战之一是它们对不同类别刺激的泛化能力。正如对这类模型及类似模型的常规做法一样,我们使用白噪声刺激数据来训练模型,同时在此也测试抑制模型在包含正弦频率和对比度扫描的刺激上的性能。模型对这类非平稳刺激的泛化能力,有助于理解模型在具有变化的刺激统计特性的复杂环境中如何捕捉视网膜的刺激处理过程。
¶ 结果
¶ 统一框架下三种抑制模型的比较
我们分别基于减法、除法和反馈相互作用实现了三种基于滤波器的神经元抑制模型,以及一个具有统一结构的LN模型(见方法;图S1)。这一通用计算框架旨在最大化模型基序以及训练和测试程序中的相似性。在该框架中,每个模型都会生成一个综合信号,该信号包含了兴奋和抑制的效应,并且在经过非线性整流后,通过泊松随机过程用于在小的离散时间窗口中生成时变的 spike 计数。模型之间的差异在于综合信号的获取方式(图1A)。减法模型和除法模型各有两个上游分支,每个分支都有自己的刺激滤波器和后续的非线性变换。然后,这两个分支分别通过减法或除法运算进行组合。上游滤波器不受约束,而非线性变换的形状则受到约束,以支持兴奋或抑制作用:减法模型的兴奋分支和抑制分支以及除法模型的兴奋分支的非线性必须是单调递增的,而除法模型的抑制分支具有“凸形”非线性,即在负输入侧单调递增,在正输入侧单调递减。反馈模型和LN模型各有一个(兴奋性)上游分支,用于对刺激进行滤波并将滤波后的信号非线性转换为放电率。对于反馈模型,会对模型生成的spike应用一个额外的滤波器,然后将上游滤波器信号和反馈滤波器信号相加。请注意,反馈模型和LN模型在随机spike生成之前都有一个额外的非线性,这种在spike生成之前的非线性在所有模型中都是共有的。对于LN模型,这意味着两个连续的非线性阶段共同构成了该模型典型的单一输出非线性。此处将其细分为两个阶段是为了迁就所有模型的统一结构。在训练过程中,模型、滤波器和非线性通过基函数集进行参数化(见方法)。输出整流器使用softplus函数进行参数化(见方法)。所有模型均采用最大似然法结合块坐标上升算法进行训练,在该算法中,我们迭代更新模型的每个块(滤波器或非线性),以最大化似然函数,同时保持其他块不变(见方法)。
这些模型在从美西螈(15次记录)、小鼠(8次)和狨猴(10次)视网膜记录的神经节细胞上进行了训练和测试。使用多电极阵列记录尖峰信号,同时用全视野高斯白噪声刺激视网膜。对于美西螈和小鼠,刺激包括交替序列:30秒(美西螈)或15秒(小鼠)的非重复白噪声,用于模型训练;以及10秒(美西螈)或5秒(小鼠)的“冻结噪声”,即重复呈现的固定白噪声序列,我们将其保留用于测试。在狨猴的数据中,未使用冻结噪声刺激。因此,我们使用15秒的片段进行训练,中间穿插5秒保留的测试片段。通过计算模型为每个尖峰提供的平均信息来评估模型性能,该评估在保留的测试数据片段上进行。请注意,这种模型性能衡量方法不需要重复试验。
我们的分析包含607个美西螈细胞、335个小鼠细胞和370个狨猴细胞,这些细胞对白色噪音刺激有可靠反应。ON-OFF细胞(即对光强度的阶梯式增加和减少均有反应的细胞)被排除在外,因为所有四个模型中应用的单调递增兴奋性非线性函数无法捕捉它们的反应。将三种抑制模型与LN模型的性能进行比较后发现,对于大多数细胞而言,每种抑制模型的反应预测效果都优于LN模型(减法模型:97%,除法模型:96%,反馈模型:85%)。为了量化每个细胞和每个抑制模型因添加所考虑的抑制成分而获得的预测能力提升,我们计算了超额性能,即所考虑的抑制模型与LN模型的模型性能之差。在这项比较中,我们选择了通过图S1的统一结构拟合的LN模型,因为对于几乎所有细胞,该拟合的LN模型的性能均等同于或优于其他LN模型——其他LN模型的刺激过滤器要么通过尖峰触发平均获得,要么通过尖峰触发协方差分析获得的第一主成分获得(图S2)。尽管如此,抑制模型的性能通常优于LN模型,对于95%的细胞,表现最佳的抑制模型的超额性能范围为:美西螈[0.03, 0.94]比特/尖峰,小鼠[0.01, 0.29]比特/尖峰,狨猴[0.001, 0.23]比特/尖峰。在所有细胞中,表现最佳的模型为减法模型的占46%,除法模型的占42%,反馈模型的占12%。
对于美西螈和小鼠视网膜的记录,视觉刺激包括重复插入的相同(随机生成)刺激序列片段(“冻结噪声”)。这些未用于参数拟合的片段可用于测量放电率曲线。随后,将其与模型预测的放电率进行比较,得到了可解释方差的度量(图S3)。这一结果与通过每 spike 信息进行的评估在定性上相似(图1B、C)。特别是,所有抑制模型的可解释方差通常都高于LN模型(p<<0.001),并且,通过从所考虑的减法模型的可解释方差中减去LN模型的可解释方差而获得的超额性能,在减法模型和除法模型中比在反馈模型中更为显著。
¶ 减法模型和除法模型的细胞类型特异性比较
由于减法模型和除法模型在评估的四个模型中总体表现最佳,我们对这两个模型的性能进行了更细致的比较,旨在确定对于哪些细胞而言,这两个模型中的一个优于另一个。在逐个细胞的基础上比较性能(图2A)表明,在美西螈视网膜中,存在一组细胞,对于这些细胞,减法模型的表现优于除法模型。对于其余的美西螈细胞以及小鼠和狨猴细胞,这两个模型的性能相当,其中除法模型的表现略好(p < 0.003;采用虚假发现率进行多重比较校正的威尔科克森符号秩检验15;图2A)。
为了了解美西螈视网膜中细胞的多样性,我们将它们分为ON细胞和OFF细胞,以及慢反应细胞和快反应细胞。为此,我们计算了每个细胞在时间白噪声刺激下的尖峰触发平均值作为其时间滤波器,并在所有滤波器的前两个主成分空间中对细胞进行聚类(图S4)。基于这种分类,我们发现减法模型和除法模型的相对性能取决于所研究细胞的动力学特性。对于快反应细胞,减法模型和除法模型的性能差异较小,其中减法模型略占优势(快反应OFF细胞:平均差异=0.026比特/尖峰,p=0.005;快反应ON细胞:平均差异=0.02比特/尖峰,p=0.7)。另一方面,对于慢反应ON细胞和慢反应OFF细胞,减法模型的性能明显优于除法模型(慢反应OFF细胞:平均差异=0.08比特/尖峰,p<<0.0001;慢反应ON细胞:平均差异=0.1比特/尖峰,p<<0.0001;图2B)。
为了更好地理解减法模型和除法模型中的抑制成分如何改进LN模型,我们更仔细地研究了单个样本细胞的模型成分。对于图3A中的美西螈慢速OFF细胞,减法模型和除法模型在兴奋性和抑制性模型分支上产生的刺激过滤器在性质上相似。然而,对于该细胞,减法模型和除法模型的上游抑制函数存在显著差异:减法模型的抑制作用会随着抑制性过滤器的激活变得更负而逐渐减弱(图3Aii),而除法模型只有单侧的、经过整流的抑制作用,其抑制成分对接近零或小于零的过滤器激活基本不敏感。因此,减法模型捕捉到了该细胞反应中的波动,而除法模型在较小程度上、LN模型在较大程度上产生了近乎平坦的输出片段,对该细胞的调制很小。
对于图3B中的小鼠细胞、图3C中的快速关闭细胞以及图3D中的狨猴细胞,除法模型的抑制性滤波器与兴奋性滤波器相似,只是向右偏移。这导致抑制性反应相较于兴奋性反应有轻微延迟,与LN模型相比,能更及时地预测 firing-rate 反应峰值的下降沿。在所有记录的细胞中,57%的美西螈细胞、79%的小鼠细胞和70%的狨猴细胞的抑制性滤波器比相关的兴奋性滤波器滞后1-2个刺激帧(美西螈约30-60毫秒;小鼠和狨猴约16-33毫秒;图3E)。此外,57%的美西螈细胞、90%的小鼠细胞和88%的狨猴细胞具有对称的除法非线性(图3F;不对称指数<0.5),这意味着将抑制性滤波器上下翻转会产生相似的抑制信号。
另一方面,这三种细胞的减法模型产生了一系列多样化的兴奋性和抑制性过滤器。在所有记录的细胞中,40%的美西螈细胞、12%的小鼠细胞和5%的狨猴细胞的抑制性过滤器比兴奋性过滤器滞后1-2个刺激帧,而32%的美西螈细胞、23%的小鼠细胞和28%的狨猴细胞的抑制性过滤器比兴奋性过滤器超前1-3个刺激帧(图3G)。然而,该模型的性能总体上与除法模型相似,这表明不同的计算动机可能会收敛于本质上不同但同样有效的解决方案。
¶ 持续型细胞和瞬变型细胞之间的模型性能差异
具有与兴奋相似的刺激依赖性的延迟抑制,是一种被提出的产生尖锐瞬态反应的机制1,2。例如,延迟抑制可能源于前馈抑制,与兴奋相比,这种抑制具有额外的突触传递延迟,这会产生一个短暂的窗口,使兴奋能在抑制成分终止反应之前引发尖峰。
抑制对反应瞬态的影响在刺激强度突然大幅增加时最容易评估。对于一部分也曾接受全视野光强阶跃刺激(100%对比度)的狨猴细胞,我们评估了抑制成分在多大程度上有助于预测其对高斯噪声的反应,以及这与它们对光强阶跃反应的瞬态之间的关系。通过比较初始反应峰值强度与刺激开始后300毫秒以上的持续活动强度,将细胞分为瞬态细胞和持续细胞(图4A)。在图4B的样本实验中,与持续ON细胞相比,瞬态ON细胞的抑制超额表现(来自每个细胞的最佳抑制模型)显著更大,这表明持续ON细胞中的抑制作用较弱。6个实验中有4个显示瞬态ON细胞和持续ON细胞之间存在类似差异(图4C)。另一方面,将ON细胞与OFF细胞进行比较时,未发现超额表现存在系统性差异(图S5)。这表明,明确的抑制模型成分确实有助于解释瞬态神经节细胞反应的短暂性。
¶ 对具有不同对比度和时间频率的刺激的泛化能力
到目前为止,所呈现的研究结果大多基于抑制模型在白噪声刺激下的表现。因此,一个重要的问题是,所推导的模型如何推广到具有不同非平稳统计特性的刺激,例如对比度或时间频率的变化。在对狨猴细胞的一部分记录中,我们应用了全视野啁啾刺激16,该刺激包含两段正弦光强度调制,一段是对比度单调增加(“对比度扫描”,从0%开始,到100%结束,扫描持续时间=8秒,频率=4赫兹),另一段是在固定对比度下频率增加(“频率扫描”,从0赫兹上升到15赫兹,扫描持续时间=8秒,对比度=100%)。因此,我们测试了使用白噪声刺激训练的模型在细胞对这些正弦光强度调制的反应上的表现。
如图5A-D所示的两个样本细胞的模型响应所示,每个模型的预测与细胞响应的匹配程度随刺激的频率和对比度而变化。为了量化这种对比扫描刺激的效应,我们在150毫秒持续时间的滑动窗口内计算每个模型的解释方差(R²),该窗口沿着刺激的时间进程以16.7毫秒(1个刺激帧)的步长移动。对于这个狨猴细胞,当对比度高于34%时,除法模型的表现优于其他模型(图5B)。对于每个狨猴细胞,我们将性能范围计算为R²>0时的对比度范围。与其他模型相比,除法模型的性能范围显著更大(p<<0.0001;图5E),这表明除法模型在更广泛的对比度范围内具有通用性。这一发现与之前的一项报告一致,即除法模型捕捉了小鼠ON-α神经节细胞对白光噪声刺激对比度变化的适应。
同样,我们使用频率扫描刺激量化了模型性能的频率依赖性。如图5C中第二个样本细胞所示,当刺激频率低于6Hz时,减法模型的性能优于其他模型,而当频率高于6Hz时,除法模型在测试模型中表现最佳(图5D)。对于每个细胞,我们计算了低频性能,即频率扫描前317毫秒的平均解释方差(150毫秒的分析窗口,移动10次,每次移动16.7毫秒,即一个刺激帧的长度),以及性能范围,即R²>0的频率范围。对于减法模型,其低频性能显著高于其他模型(p<0.03;图5F左侧),这表明该模型在捕捉细胞对调频刺激中低频的反应方面表现更好。另一方面,与对比度扫描的结果类似,除法模型的性能范围最大(p<0.004;图5F右侧),这表明该模型在调频刺激的频率范围内具有更好的泛化能力。
¶ 讨论
兴奋与抑制的相互作用是神经系统对感觉刺激形成反应的核心主题。因此,如何在单细胞计算模型中体现抑制作用是一个广受关注的问题。我们发现,此前提出的三种将抑制作用纳入基于滤波器的模型的不同方法,均能比常用的单滤波器模型(即线性-非线性模型)更好地改进反应预测。此外,对于美西螈、小鼠和狨猴的大多数细胞而言,减法模型和除法模型的表现通常优于反馈模型。
乍一看,减法模型和除法模型对大多数细胞的整体表现颇为相似,这可能有点令人失望,因为缺乏一个明确的“赢家”,使得很难推断兴奋-抑制相互作用的类型。另一方面,这种零结果意味着,从现象学的角度来看,模型中纳入抑制的具体细节远不如存在抑制成分本身重要,这表明不同的相互作用可以通过不同的方式实现相似的功能。不同模型结构的功能等效性让人想起对龙虾胃神经节的研究,在该研究中,同一回路功能存在多种可变实现方式这一点得到了有力证明17。
然而,对这两个模型更详细的比较揭示了在性能如何依赖物种和刺激特征方面存在系统性差异。减法模型在捕捉缓慢的美西螈细胞对白噪声刺激的反应以及狨猴细胞对啁啾刺激低频部分的反应时表现更佳。另一方面,除法模型在更广泛的对比度和频率范围内具有更强的泛化潜力。这表明,不同的神经抑制机制可能在不同的刺激和反应时间尺度上占主导地位,并且这两个模型在捕捉这些特定机制的效果方面存在差异。特别是,减法模型可能尤其适用于解释在缓慢细胞中占优势的生物机制,或者在刺激以低频为主时起作用的生物机制。
可能导致反馈模型性能受限的一个技术方面是,该模型中的事实抑制取决于尖峰的出现,而尖峰在模型中是稀疏且随机的。这限制了抑制机制的有效性(例如,它无法抑制之前没有另一个尖峰事件的尖峰事件),并导致预测响应出现变异性。其他实现方式可能会让反馈依赖于尖峰产生前的连续内部信号18,或者可能采用确定性的尖峰产生过程13,19。
在本研究中,对比模型的实施遵循了一个共同框架的目标,该框架使模型结构和训练具有最大可比性。然而,并非所有模型的自由参数数量都相同。考虑到模型的复杂性,这就引出了一个问题:这种比较是否会受到过拟合的影响,而过拟合可能会降低自由度较高的模型在测试数据上的性能。不过,减法模型和除法模型实际上具有相同数量的自由参数,因此观察到的差异不太可能源于拟合精度的差异。此外,这两个模型的整体性能高于反馈模型和LN模型,而后两者的自由参数更少。因此,过拟合不太可能限制我们研究结果的可解释性。
本研究的一个局限性在于,我们将分析范围限定在使用无任何空间结构的全视野刺激上。我们做出这一选择是为了减少模型中的自由参数数量,同时使细胞类型和模型之间的比较不受空间滤波以及空间刺激整合中潜在非线性因素捕捉效果的影响20–23。但不利的是,使用全视野刺激会使我们的分析对抑制的时空结构不敏感,特别是无法提供来自感受野周围的专用抑制信号通路。
我们研究的一个特定方面是比较不同物种神经节细胞的模型。结果显示,研究发现总体具有高度的一致性;在蝾螈、小鼠和狨猴中,都观察到减法模型和除法模型的表现相近,而反馈模型的表现普遍较低。有一组特别的细胞是慢爪蟾细胞,它们明显更倾向于减法模型而非除法模型。对于这些细胞来说,其迟缓性尤为显著,因为爪蟾的过滤器和反应动力学总体上比其他物种慢,这可能部分是由于爪蟾实验是在较低温度下进行的。这或许使得减法模型——它似乎通常能更好地捕捉缓慢的时间动态——特别适合这种慢速视网膜中的慢细胞。
对于狨猴神经节细胞,我们发现,在反应模型中纳入抑制(无论是通过减法模型还是除法模型),对瞬态细胞而言比对持续细胞更具相关性,尤其是在考虑对光强度阶跃的反应时。在灵长类动物的视网膜中,侏儒神经节细胞和伞状神经节细胞在数量上构成了视网膜神经节细胞群体的大部分,其中,伞状细胞往往具有瞬态反应,而侏儒细胞则具有持续反应。因此,似乎在模型中纳入抑制对伞状细胞而言尤为相关,不过对于当前数据集,我们没有对伞状细胞和侏儒细胞进行独立分类。
与许多其他关于神经元对感觉刺激反应模型的研究一样,我们的模型拟合基于白噪声信号刺激下的记录。然而,人们越来越意识到,一个重要的后续步骤是评估所获得的模型描述和推断出的见解在不同的、通常更复杂的刺激特征(如自然刺激)背景下的适用性如何。在本研究中,我们没有使用自然刺激,而是研究了模型对非白噪声、非平稳刺激的泛化能力,这些刺激改变了特定的刺激成分,如对比度和时间频率。一些关于不含抑制成分的模型的研究通过为每个对比度重新计算刺激成分,将其用于不同的对比度水平。其他研究则提出,通过反馈、 divisive gain control 或非线性滤波与反馈的复杂生物学驱动组合等抑制性元素,可作为捕捉对比度适应从而促进跨对比度水平泛化的机制。这些发现与我们的观察一致,即抑制性模型元素有助于跨对比度水平和频率范围的泛化,且除法模型特别适合这一目的。
¶ 致谢
本研究得到了欧盟“地平线2020”研究与创新计划下欧洲研究理事会(ERC)的资助(资助协议编号724822),以及德国研究基金会(DFG)的资助(项目编号432680300,即SFB 1456项目的B05子项目)。
¶ 贡献
FR、MHK、HS和TG设计了实验。FR在实验室搭建了CMOS记录装置,并收集和预处理了狨猴数据。MHK、MM和DAP负责狨猴视网膜的制备,并协助数据收集。MHK负责小鼠视网膜的制备,以及小鼠数据的收集和预处理。HS收集并预处理了美西螈数据。NS和TG设计了计算分析方案。NS进行了分析和建模工作。NS和TG在所有作者的意见基础上撰写了论文。
¶ 参考文献
文献列表(带序号)
-
崔宇、王Y.V、朴S.J.H.、登布J.B.和巴茨D.A.。divisive抑制解释了视网膜神经节细胞的高精度放电和对比度适应。《eLife》5, e19460 (2016)。
-
巴茨(D. A.)、翁(C.)、金(J.)、阿隆索(J.-M.)和帕宁斯基(L.)。通过兴奋与刺激驱动的抑制之间的相互作用实现视觉通路中的时间精度。《神经科学杂志》,31卷,11313–11327页(2011年)。
-
韦尔(M. Wehr)和扎多尔(A. M. Zador)。平衡抑制是基础。《自然》426,860-863(2003)。
-
Gabernet, L.、Jadhav, S. P.、Feldman, D. E.、Carandini, M. 和 Scanziani, M. 动态丘脑皮质前馈抑制控制的躯体感觉整合。《神经元》48, 315-327 (2005)。
-
Wilent, W. B. 和 Contreras, D. 大鼠躯体感觉皮层中刺激选择性背后的兴奋和抑制动力学。《自然神经科学》8, 1364–1370 (2005)。
-
Heeger, D. J. 猫纹状皮层细胞反应的标准化。《视觉神经科学》9, 181–197 (1992)。
-
Albrecht, D. G. 和 Geisler, W. S. 视觉皮层中简单细胞的运动选择性与对比度-反应函数。《视觉神经科学》7, 531–546 (1991)。
-
Roska, B. 与 Werblin, F. 自然场景中快速的全局变化会阻断特定神经节细胞类型的放电。《自然·神经科学》6, 600–608 (2003)。
-
Roska, B., Molnar, A. 及 Werblin, F. S. 视网膜神经节细胞的并行处理:兴奋和抑制的时空模式整合如何形成尖峰输出。《神经生理学杂志》,95卷,3810-3822页(2006年)。
-
拉蒂默(K. W.)、里克(F.)和皮洛(J. W.)。基于电导的神经编码模型从尖峰中推断突触输入。《eLife》8,e47012(2019)。
-
麦克法兰(J. M.)、崔(Y.)和巴茨(D. A.)。基于生理合理输入推断非线性神经元计算。《公共科学图书馆·计算生物学》9,1003143(2013)。
-
皮洛(J. W.)等人。完整神经元群体中的时空相关性和视觉信号传导。《自然》,454卷,995-999页(2008年)。
-
皮洛(Pillow)、帕宁斯基(Paninski)、厄泽尔(Uzzell)、西蒙切利(Simoncelli)和奇奇尔尼斯基(Chichilnisky)。利用概率 spike 模型预测和解码视网膜神经节细胞反应。《神经科学杂志》,25卷,11003–11013页(2005年)。
-
布伦纳(N.)、斯特朗(S. P.)、科伯勒(R.)和比亚莱克(W.)。神经编码中的协同作用。《神经计算》,12,1531-1552(2000)。
-
本雅明尼,Y. 和霍奇伯格,Y. 控制错误发现率:一种实用且有效的多重检验方法。《英国皇家统计学会会刊B辑》57,289-300(1995)。
-
巴登(T.)等人。小鼠视网膜神经节细胞的功能多样性。《自然》,529卷,345–350页(2016年)。
-
普林茨(A. A.)、布赫尔(D.)和马德(E.)。不同电路参数产生的相似网络活动。《自然·神经科学》,7,1345–1352(2004)。
-
贝里(M. J.)、布里万卢(I. H.)、乔丹(T. A.)和迈斯特(M.)。视网膜对运动刺激的预期。《自然》,398卷,334-338页(1999年)。
-
基特(J.)、赖纳格尔(P.)、里德(R. C.)和迈斯特(M.)。《预测每一个尖峰:视觉神经元反应模型》。《神经元》,第30卷,第803-817页(2001年)。
-
Carandini, M. 等人。我们知道早期视觉系统的功能吗?《神经科学杂志》,25卷,10577–10597页(2005年)。
-
Wienbar, S. 与 Schwartz, G. W. 视网膜神经节细胞的动态感受野。《视网膜与眼研究进展》67, 102–117 (2018)。
-
Zapp, S. J., Nitsche, S. 及 Gollisch, T. 视网膜感受野亚结构:编码与计算的支架。《神经科学趋势》,45卷,430-445页(2022年)。
-
卡拉曼利斯(D.)、施赖尔(H. M.)和戈利施(T.)。《自然场景的视网膜编码》。《视觉科学年度评论》8,171-193(2022)。
-
达西(D. Dacey)。《感知的起源:视网膜神经节细胞的多样性与平行视觉通路的形成》,收录于《认知神经科学》,第281–301页(2011年)。
-
菲尔德(G. D.)和奇奇尔尼斯基(E. J.)。灵长类动物视网膜的信息处理:回路与编码。《神经科学年度评论》,30卷,1-30页(2007年)。
-
Gouras P. 猴视网膜中顺向识别的神经节细胞的逆向反应。《生理学杂志》。204, 407–419 (1969)。
-
de Monasterio, F. M. 与 Schein, S. J. 猕猴视网膜中央凹Y神经节细胞的类红色盲光谱敏感性。《生理学杂志》,299卷,385-396页(1980年)。
-
刘,J. K. 和戈利希,T. 尖峰触发协方差分析揭示视网膜对比度适应的现象学多样性。《公共科学图书馆·计算生物学》11,e1004425(2015)。
-
Gaudry, K. S. 和 Reinagel, P. 非适应性LGN模型中的对比度适应。《神经生理学杂志》98, 1287–1296 (2007)。
-
沙普利(R.)、恩罗斯-库格尔(C.)、邦兹(A. B.)和柯比(A.)。视网膜中的增益控制和视网膜动态。《自然》,236期,352-353页(1972年)。
-
Van Hateren, J. H., Rüttiger, L., Sun, H. 及 Lee, B. B. 猕猴视网膜神经节细胞对自然时间刺激的处理。《神经科学杂志》22, 9945–9960 (2002)。
-
刘,J. K. 等。利用尖峰触发非负矩阵分解推断神经元功能回路。《自然·通讯》8,149(2017)。
-
Schreyer, H. M. 和 Gollisch, T. 视网膜双极细胞中的非线性空间整合塑造了对人工和自然刺激的编码。《神经元》109, 1692-1706.e8 (2021)。
-
Khani, M. H. 与 Gollisch, T. 小鼠视网膜神经节细胞间对比度适应空间范围的多样性。《神经生理学杂志》,118卷,3024-3043页(2017年)。
-
Khani, M. H. 与 Gollisch, T. 小鼠视网膜中的线性和非线性色度整合。《自然·通讯》12, 1900 (2021)。
-
Pouzat, C.、Mazor, O. 和 Laurent, G. 利用噪声特征优化尖峰分选并评估神经元分类质量。《神经科学方法杂志》122期,43-57页(2002年)。
-
Nitsche, S. 等人。灵长类视网膜中神经节细胞对类扫视图像位移的反应多样性。bioRxiv(2022年)。
-
Muthmann, J. O. 等。使用高密度多电极阵列检测大型神经群体的尖峰信号。《神经信息学前沿》9, 1–21 (2015)。
-
Hilgen, G. 等人。用于大规模、高密度多电极阵列的无监督尖峰分选。《细胞报告》18, 2521–2532 (2017)。
-
Samengo, I. 与 Gollisch, T. 触发尖峰协方差:几何证明、对称特性及高斯刺激之外的扩展。《计算神经科学杂志》,34卷,137-161页(2013年)。
-
施瓦茨(O.)、皮洛(J. W.)、拉斯特(N. C.)和西蒙切利(E. P.)。《尖峰触发的神经表征》。《视觉杂志》,6期,484-507页(2006年)。
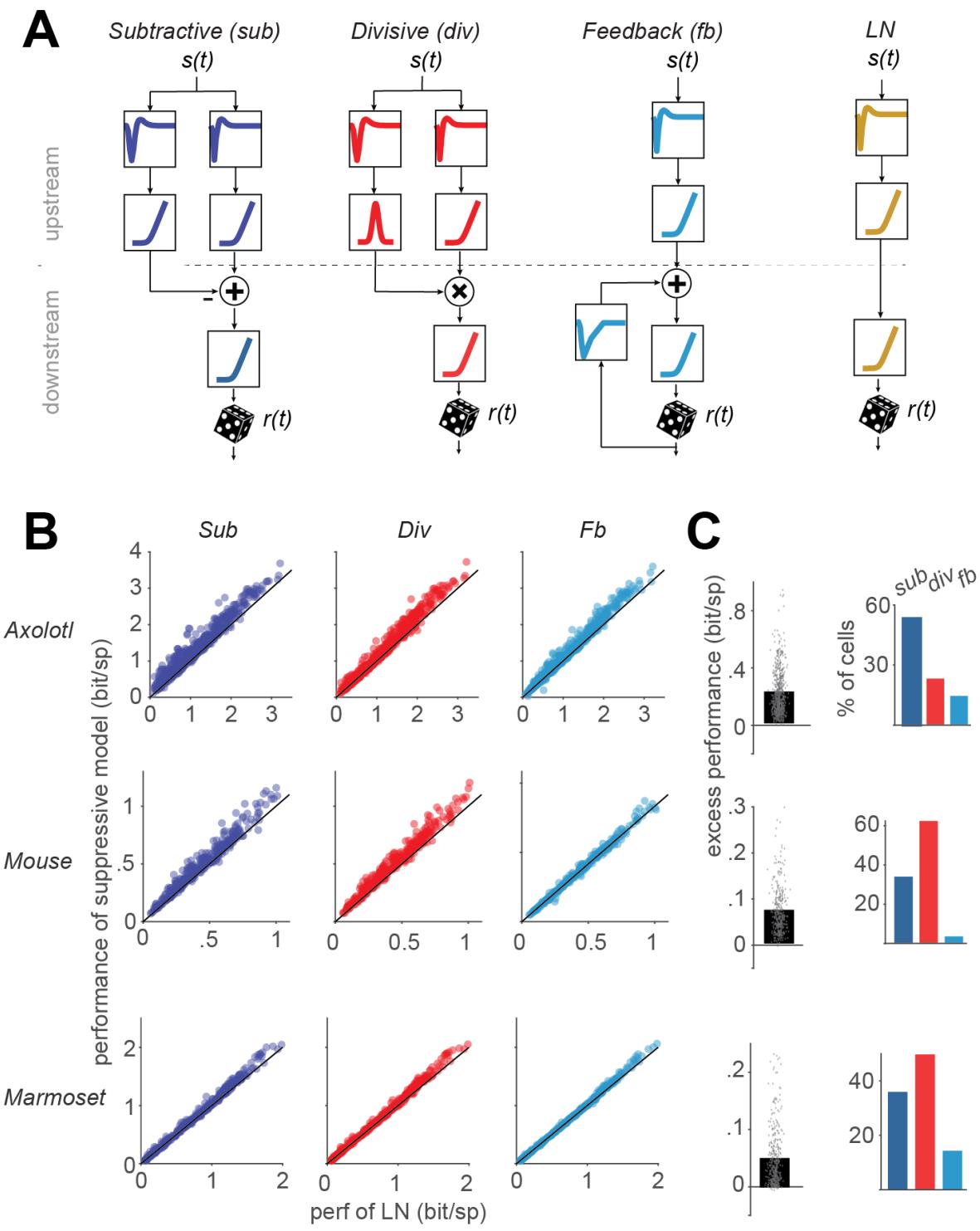
图1. 模型及其整体性能示意图。A)本研究中使用的三种抑制模型(具有减法抑制、除法抑制和反馈抑制)以及LN模型的结构。B)每种模型的性能(以每个尖峰提供的信息衡量)与LN模型性能的比较。每个数据点代表一个细胞。C)左图:为每个细胞确定的性能最佳的抑制模型的超额性能(抑制模型性能减去LN模型性能)。右图:每种抑制模型优于所有其他模型的细胞百分比。
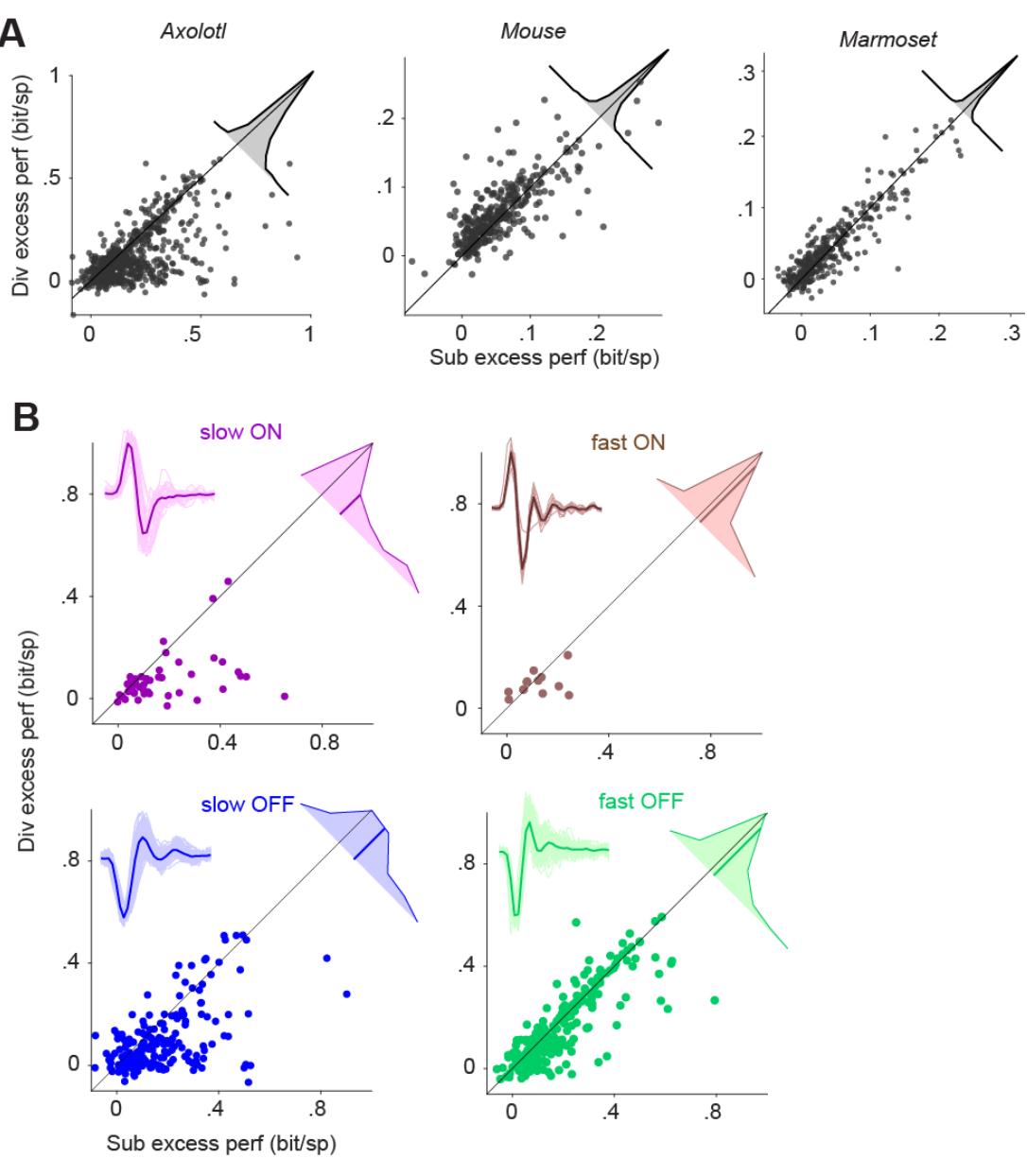
图2. 减法模型和除法模型的超额性能比较。A) 不同物种中减法模型与除法模型的超额性能散点图。每个数据点代表一个细胞。插图:减法模型和除法模型之间性能差异的分布。B) 与A相同,但针对美西螈视网膜记录细胞的慢/快亚群和ON/OFF亚群。插图:亚群内所有细胞的LN模型滤波器(细线)及其平均值(粗线)。
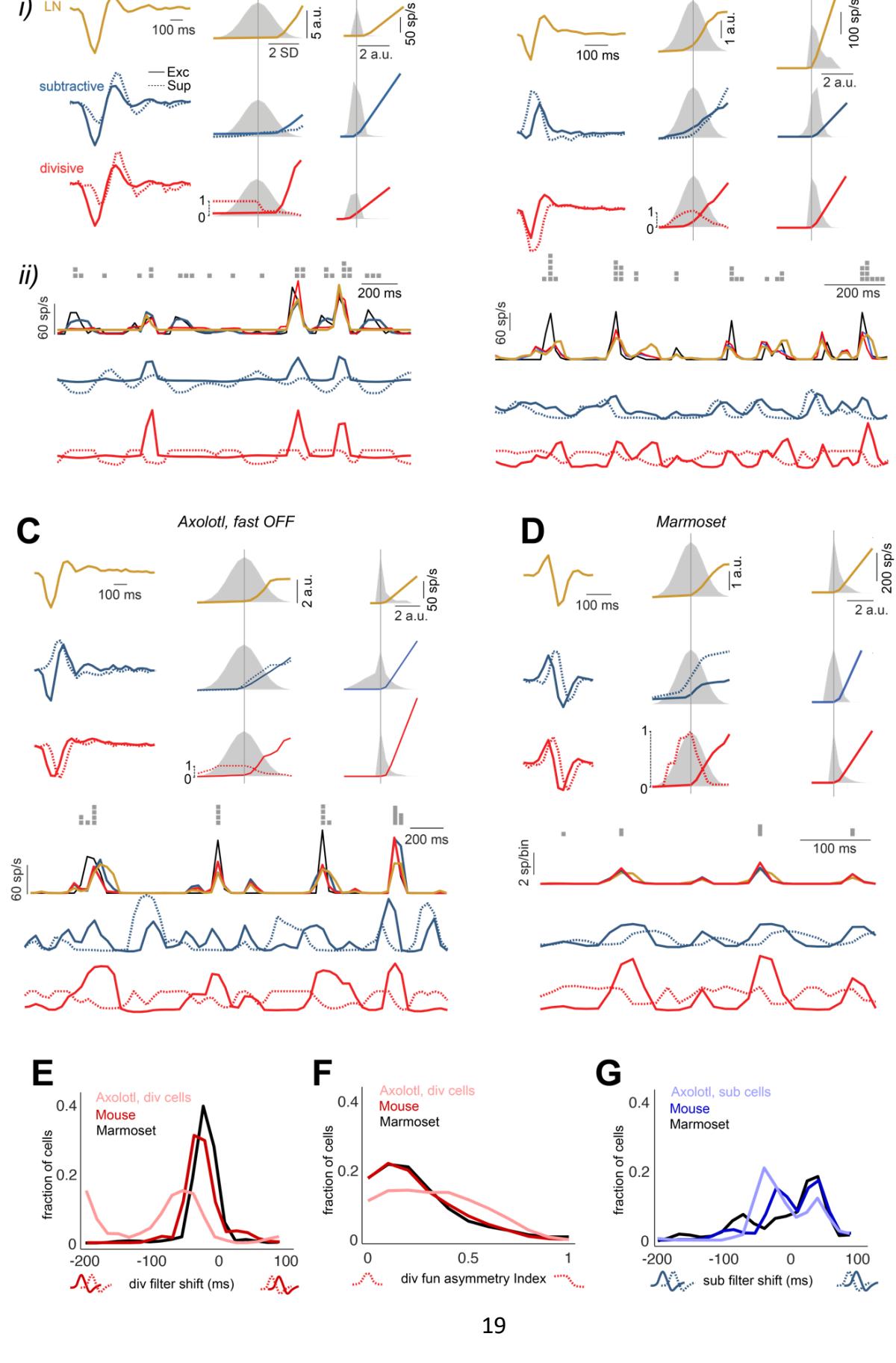
图3. 模型拟合和反应预测来自每个被研究物种的样本细胞。Ai) 兴奋性和抑制性过滤器(左)、上游非线性函数(中),与作为伴随滤波刺激的输入分布重叠,以及输出整流器(右),与作为来自上游的整体电位的输入分布重叠,适用于LN模型、减法模型和除法模型。由于反馈模型性能较低而未显示,但为了比较而包含了LN模型。Aii) 对于测试试验期的一个子部分:第一行:样本测试试验中每个刺激时间仓的尖峰计数。第二行:细胞的放电率(黑色)和三个模型的预测。第三行:减法模型的兴奋性(实线)和抑制性(虚线)上游分支的输出。第四行:与第三行相同,但为除法模型。B、C、D) 其他样本细胞与A相同。E) 除法模型的抑制性过滤器相对于兴奋性过滤器的偏移,计算方式与E类似。F) 除法模型的抑制性非线性函数的不对称指数。该指数计算为负输入和正输入上函数值之和的绝对差除以函数值的总和。G) 所有细胞中减法模型的抑制性过滤器相对于兴奋性过滤器的偏移。为了计算每个细胞的偏移,计算了兴奋性和抑制性过滤器的互相关图,然后找到了互相关图峰值的偏移。
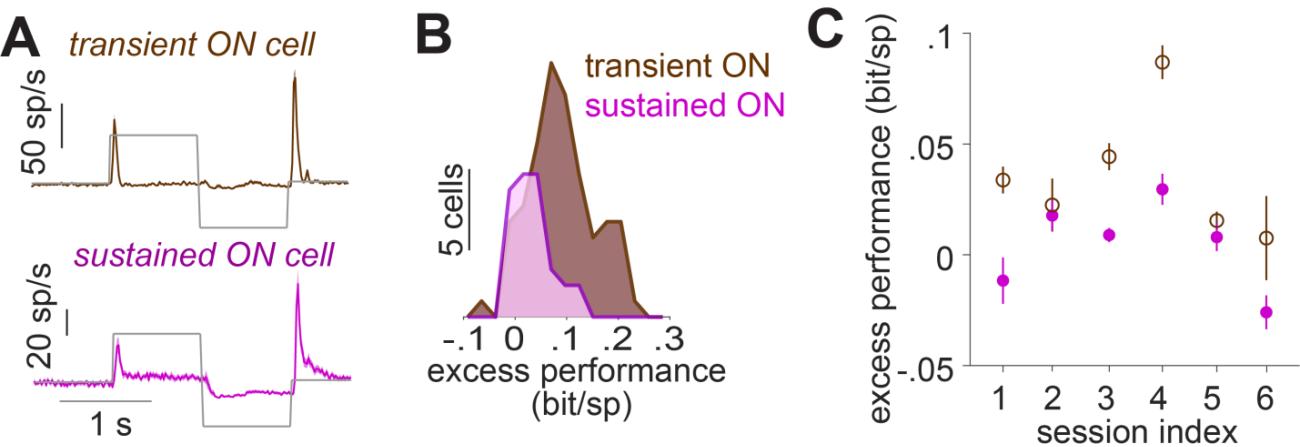
图4. A) 在一个样本会话(会话索引=3)中,所有细胞的平均值显示,狨猴细胞对瞬态ON细胞和持续ON细胞的阶跃刺激的反应。B) 在同一个样本会话中,最佳性能模型的超额性能在瞬态ON细胞和持续ON细胞中的分布。C) 每个记录会话中,瞬态ON细胞和持续ON细胞的超额性能的平均值和标准误差。
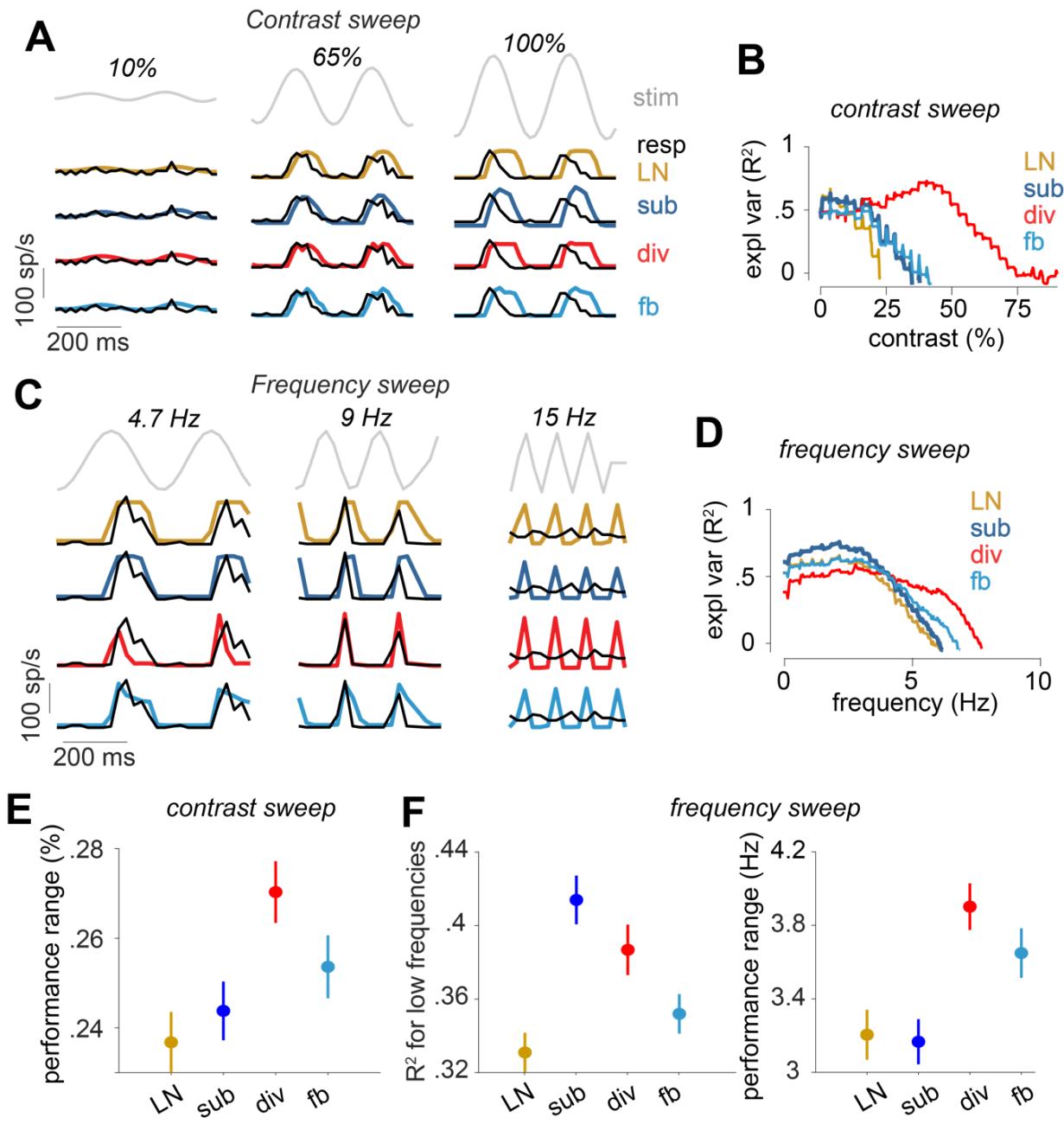
图5 模型对狨猴细胞的对比度扫描和频率扫描响应的评估。A) 部分对比度扫描刺激以及样本细胞的响应和模型预测。展示了对比度扫描的三个部分。刺激、细胞响应和模型预测的完整范围如图S6所示。B) A中细胞的模型解释方差,通过150毫秒滑动窗口计算。对于每个模型,仅显示R2>0的数值范围。C)和D) 与A和B相同,但针对不同样本细胞的频率扫描而非对比度扫描。E) 每个模型的R2>0时的对比度范围(细胞的平均值和标准误差)。F) 左图:频率扫描中前167毫秒(10个刺激帧)时每个模型的R2(细胞的平均值和标准误差)。右图:每个模型的R2>0时的频率范围(细胞的平均值和标准误差)。
¶ 方法
¶ 电生理学
所有实验和操作均符合国家和机构指南,并获得了哥廷根大学医学中心机构动物护理委员会的批准(协议编号T11/35)。
美西螈的记录是使用60电极穿孔多电极阵列(德国罗伊特林根的MultiChannel Systems公司;电极直径30微米,最小电极间距100微米)进行的,如前所述32,33。在暗适应1小时后将眼球摘除,视网膜以视网膜神经节细胞面朝下的方式安装在硝酸纤维素滤膜上1.5-2毫米的孔上。实验过程中,视网膜在室温(约22°C)下持续灌注含氧(95% O₂和5% CO₂)的林格氏培养液(110 mM氯化钠、2.5 mM氯化钾、1 mM氯化钙、1.6 mM氯化镁、22 mM碳酸氢钠、10 mM D-葡萄糖一水合物)。小鼠的记录是使用252电极阵列(德国罗伊特林根的MultiChannel Systems公司;电极直径30微米,最小电极间距100或200微米)进行的,如前所述34,35。小鼠(年龄8-13周,雌雄不限)暗适应至少1小时后,通过颈椎脱臼法处死。迅速取出眼球,转移到含有含氧(95% O₂和5% CO₂)的埃姆斯培养液(德国慕尼黑的Sigma-Aldrich公司)的培养室中,该培养液用22 mM碳酸氢钠缓冲(以维持pH值为7.4),并添加6 mM D-葡萄糖。解剖眼球,小心去除角膜、晶状体和玻璃体液。将视网膜从色素上皮中分离出来,转移到多电极阵列上。记录室的温度保持在32-34°C左右,使用在线加热器(PH01,德国罗伊特林根的MultiChannel Systems公司)和阵列下方的加热元件(由TCX-Control 1.3.4,MultiChannel Systems公司控制),同时视网膜持续灌注含氧的埃姆斯培养液(4-5毫升/分钟)。
对于美西螈和小鼠的记录,神经节细胞的活动均经过放大、带通滤波(300赫兹至5千赫兹)处理,并使用MC-Rack软件(4.6.2版本,MultiChannel Systems公司)以25千赫兹(60通道微电极阵列)或10千赫兹(252通道微电极阵列)的频率进行数字记录。尖峰信号通过基于高斯混合模型和期望最大化算法的定制化尖峰分选程序从记录的电压轨迹中提取出来36。
狨猴视网膜的记录按照先前描述的方法进行37。简而言之,视网膜取自其他研究人员使用过的动物,这一过程符合国家和机构指南,并获得了德国灵长类动物中心机构动物护理委员会以及负责的地区政府部门(下萨克森州消费者保护和食品安全局,许可证编号33.19-42502-04-17/2496)的批准。眼睛被迅速摘除并解剖,以便向视网膜直接供应含氧(95% O₂和5% CO₂)的Ames培养基(Sigma-Aldrich,慕尼黑,德国),该培养基添加了6 mM D-葡萄糖,并以22 mM NaHCO₃缓冲以维持pH值为7.4。随后,视网膜进行1-2小时的暗适应。每次记录时,取一小块周边视网膜(已去除色素上皮),放置在4096通道基于CMOS的微电极阵列上(电极尺寸21 µm,间距42 µm;3Brain AG)。视网膜片以视网膜神经节细胞面朝下的方式放置,覆盖一片半透明聚酯滤膜(Pieper Filter #PE0104700;孔径0.1 µm),并用金属环加压固定。记录过程中,视网膜用含氧的Ames培养基灌注(4-5 ml/min),记录室的温度与小鼠记录时相同,保持在33°C左右。动作电位的提取和分选通过HerdingSpikes2(github.com/mhhennig/HS2)进行。简而言之,使用固定阈值在每个电极上独立检测动作电位事件,然后对相邻电极中的同步事件进行三角测量,以确定动作电位的位置和形状。最后,基于动作电位波形的位置和前两个主成分,使用均值漂移算法将事件聚类为不同的单位38,39。
所有视网膜标本的制备均在配备夜视镜的立体显微镜下,于红外照明条件下进行。
¶ 视觉刺激
所有记录的视觉刺激均由一款使用C++编写并基于OpenGL库的定制软件生成和控制。对于美西螈和狨猴的记录,刺激呈现于经过伽马校正的单色白色OLED显示器(eMagin,800×600像素,刷新率60Hz)上。对于小鼠的记录,刺激通过改良版DLP Lightcrafter投影仪(评估模块(EVM),864×480像素,刷新率60Hz,美国得克萨斯州达拉斯市德州仪器公司)显示,其中蓝色LED已替换为紫外LED(发射峰值为365nm),如前所述35。
白噪声刺激是通过从正态分布中随机抽取新的屏幕强度获得的,频率分别为30赫兹(美西螈)或60赫兹(小鼠和狨猴)。屏幕强度的正态分布以显示器最大强度的一半为中心,标准差为平均光强度的30%。在美西螈和小鼠视网膜的记录中,由300个强度值组成的固定白噪声序列(“冻结噪声”)在每900个非重复白噪声强度值后重复插入。
对比度阶跃刺激、对比度扫描和频率扫描被连续呈现,组合在一起称为 chirp 刺激16。在 chirp 刺激的每个试次中,先呈现120帧的黑暗(0%对比度),之后分别呈现60帧的ON刺激(100%对比度)和OFF刺激(0%对比度)。再经过60帧的黑暗后,呈现正弦频率扫描,从0赫兹开始,到15赫兹结束,持续480帧,围绕平均刺激强度波动,峰值光水平分别为0%和100%对比度。又经过60帧的黑屏后,呈现正弦对比度扫描,从0%开始,到100%结束,频率为4赫兹,持续480帧。最后,再呈现60帧的黑屏。chirp 刺激重复15个试次。chirp 刺激的阶跃部分用于将细胞分为瞬态细胞和持续细胞。频率扫描和对比度扫描用于评估模型对一系列刺激频率和对比度的泛化能力。
¶ 模型构建与训练
每个模型包含一个(用于反馈模型和LN模型)或两个分支(用于减法模型和除法模型),这些分支代表上游计算,之后是输出整流器和尖峰发生器。每个上游分支由一个刺激滤波器和一个非线性函数组成。反馈模型的反馈回路包含一个滤波器,该滤波器应用于近期的尖峰活动历史,且不包含非线性函数(参见手稿图1A)。
为了最大限度地提高实施和训练的一致性,我们将所有四个模型整合到一个主结构中(图S1)。
每个滤波器以及每个上游函数都通过一组基函数进行参数化¹¹(图S7A展示了滤波器的基函数,图S7B展示了非线性的基函数)。
输出整流器被描述为一种“softplus”函数:
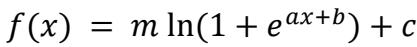
其中a、b、c和m代表自由参数。
在这种统一结构中,每次只训练一个模型组件,即滤波器、上游函数或整流函数。因此,我们可以将该结构的输出描述为:使用基函数对正在训练的分支进行扩展,同时将模型的其余部分描述为如下所示的最小变量集:
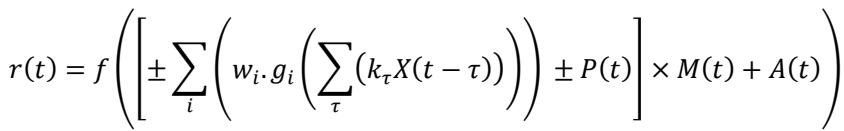
其中,𝑘𝜏和𝑤𝑖分别是滤波器基函数和训练中函数的权重,𝑓是输出整流器,𝑔𝑖是非线性的预先指定基函数。在训练每个模型的每个分支时,变量𝑋、𝑃、𝑀和𝐴的定义来自表1。例如,该表显示,当更新减法模型的兴奋性分支时,它在上述公式中表示为加权和项,而抑制性分支由变量𝑃表示,反之亦然。同样,对于除法模型,当更新兴奋性分支时,抑制性分支由𝑀表示,反之亦然。请注意,𝑀在公式中是乘法项,但起到抑制作用,这是因为由于其非线性函数的约束,抑制性分支的输出被限制在0到1的范围内。
¶ 表1 从统一结构推导出每个模型的变量分配。
| 模型 | 组成部分 | X | P | M | A |
|---|---|---|---|---|---|
| 减法模型 | 兴奋性(exc) | 刺激 | 抑制输出 | 1 | 0 |
| 抑制性(sup) | 刺激 | 兴奋输出 | 1 | 0 | |
| 除法模型 | 兴奋性(exc) | 刺激 | 0 | 0 | 抑制输出 |
| 抑制性(sup) | 刺激 | 0 | 0 | 兴奋输出 | |
| 反馈模型 | 兴奋性(exc) | 刺激 | 0 | 1 | 反馈输出 |
| 抑制性(sup) | 脉冲 | 0 | 1 | 兴奋输出 | |
| LN 模型 | 兴奋性(exc) | 刺激 | 0 | 1 | 0 |
训练中的分支使用块坐标上升算法进行更新,其中𝑘𝜏被更新以最大化似然函数,而wi保持不变,反之亦然。模型的各个组件按以下顺序进行训练:上游兴奋性组件、上游抑制性组件(针对减法模型和除法模型)、反馈回路(针对反馈模型)以及输出整流器。
目标函数为−𝐿𝐿,即似然函数对数的负值,其计算方式为:在时间间隔t内,尖峰数量服从均值为𝑟(𝑡)的泊松分布时,该分布概率的对数。在算法的每一步中,我们使用Matlab®中的fmincon函数,每个模型组件执行10步以最小化目标函数,并且对所有模型组件重复训练100次,或者直到目标函数的变化小于0.01%为止。在fmincon中,我们采用了“信赖域反射”算法。对wi的约束通过序列二次规划算法施加。通过计算−𝐿𝐿对𝑤𝑖或𝑘𝜏的导数,将目标函数的导数提供给fmincon。每个变量的约束条件选自表2。
¶ 表2 各模型组件变量集的优化约束
| 模型 | 兴奋性滤波器 | 兴奋性函数 | 抑制性滤波器 | 抑制性函数 |
|---|---|---|---|---|
| 减法模型 | 范数=1 拖尾=0 |
单调递增 下界=1E⁻¹⁶ |
范数=1 拖尾=0 |
单调递增 下界=1E⁻¹⁶ |
| 除法模型 | 范数=1 拖尾=0 |
单调递增 下界=1E⁻¹⁶ |
范数=1 拖尾=0 |
输入<0时单调递增 输入>0时单调递减 缩放至[1E⁻¹⁶, 1]区间 |
| 反馈模型 | 范数=1 拖尾=0 |
单调递增 下界=1E⁻¹⁶ |
拖尾=0 | - |
| LN 模型 | 范数=1 拖尾=0 |
单调递增 下界=1E⁻¹⁶ |
- | - |
- 滤波器的尾部是最后5个时间仓数值的平均值。
为了降低找到对应于目标函数局部最小值的非最优解的风险,训练重复了5次,每次使用不同的初始化值,这些初始化值由简单的尖峰触发分析指导。然后,我们选择了训练数据的目标函数值(负对数似然)最低的解。初始值选自尖峰触发平均值、从尖峰触发协方差分析中提取的最相关刺激特征40,41、预定义的确定性函数以及表3中的高斯噪声(当每个模型使用不同的初始值时,它们遵循sub / div / fb / LN的格式),其中STA是尖峰触发平均值,STC1和STCN是尖峰触发协方差的第一个和最后一个主成分,Wmono是如上定义的softplus函数,其中a=10,b、c=0,m=0.1,Wbi是0到1之间的倒钟形函数。每次使用Wmono和Wbi时,都会向它们添加均值为0、标准差为0.1的高斯噪声。
¶ 表3 5次训练迭代的初始值
| 迭代轮次 | 兴奋性滤波器 | 兴奋性函数 | 抑制性滤波器 | 抑制性函数 |
|---|---|---|---|---|
| 1 | STA | 单调函数(Wₘₒₙₒ) | STC₁/STC₁/0/- | 单调函数(Wₘₒₙₒ) / 双相函数(Wᵦᵢ) / - / - |
| 2 | STA | 单调函数(Wₘₒₙₒ) / 双相函数(Wᵦᵢ) / 单调函数(Wₘₒₙₒ) / 双相函数(Wᵦᵢ) | STC₅/STC₅/0/- | 单调函数(Wₘₒₙₒ) / 双相函数(Wᵦᵢ) / - / - |
| 3 | STC₁ | 单调函数(Wₘₒₙₒ) | STC₅/STC₅/0/- | 单调函数(Wₘₒₙₒ) / 双相函数(Wᵦᵢ) / - / - |
| 4 | STC₅ | 单调函数(Wₘₒₙₒ) / 双相函数(Wᵦᵢ) / 单调函数(Wₘₒₙₒ) / 双相函数(Wᵦᵢ) | STC₁/STC₁/0/- | 单调函数(Wₘₒₙₒ) / 双相函数(Wᵦᵢ) / - / - |
| 5 | 标准正态分布(N(0,1)) | 单调函数(Wₘₒₙₒ) | 标准正态分布(N(0,1)) | 单调函数(Wₘₒₙₒ) / 双相函数(Wᵦᵢ) / - / - |
对于所有模型和迭代,输出整流器的初始值为10∗ln(1+𝑒0.1𝑥)。
¶ 评估与交叉验证
每个模型针对每个细胞的最佳解决方案都在训练数据和测试数据上进行了评估。对于反馈模型,其性能是通过100次评估的平均值来确定的,每次评估的峰值计数都是根据泊松分布随机获得的,该分布的速率由模型的输出给出。当有冻结噪声数据可用时(美西螈和小鼠数据),这些数据被留作测试数据。否则(狨猴数据),从每25秒的数据中提取5秒作为伪试验用于测试。
¶ 单元的选择
将记录的锋电位分类为单个单位后,基于多个标准选择了一部分单位进行建模:1. 在白噪声刺激下,美西螈单位的平均放电率需大于2Hz,小鼠和狨猴单位的平均放电率需大于5Hz。2. 可解释方差需大于0.5。可解释方差的计算方式为:将细胞对一组冻结噪声刺激的反应分为两个子集,计算每个子集内的细胞反应平均值,然后用第二个子集的反应平均值计算第一个子集反应平均值的可解释方差。可解释方差为20个随机划分的子集的该可解释方差的平均值。3. 在白噪声刺激下,记录早期(小于总记录时间的30%)和晚期(大于总记录时间的70%)的平均放电率差异需小于总体平均放电率的50%。4. 该单位不能是ON-OFF细胞,即它不应同时对光增量和光减量产生反应。ON-OFF细胞通过LN模型的U形非线性函数来检测:将该函数分为左侧(输入<0)和右侧(输入>0)部分,然后为左侧部分拟合一条线(斜率=sL),为右侧部分拟合另一条线(斜率=sR)。如果sL/(|sL|+|sR|)<-0.2,则该细胞被归类为ON-OFF细胞。5. 为减少过拟合的影响,所有四个模型在测试数据上的性能需至少达到其在训练数据上性能的60%。
基于细胞对白色噪声刺激的反应之间的相似性,检测并移除了重复单元。为此,根据刺激帧对每个细胞的放电率进行分箱,然后计算同时记录的群体内所有细胞对的分箱放电率之间的互相关。反应相关性强度随后被计算为互相关图中心的值(滞后=0)。接下来,构建同时记录的细胞的图谱,每个细胞为一个节点,如果两个细胞之间的反应相关性>0.3,则在两个节点之间建立一条边。通过在该图谱中寻找团来检测重复细胞。在每组重复细胞中,除了具有最大可解释方差的细胞外,其余均被移除。
¶ 统计分析
双尾Wilcoxon符号秩检验被采用,除非另有说明使用其他检验方法。当比较多组数据时,采用多重比较的错误发现率(FDR)校正15来校正p值。采用双侧Wilcoxon符号秩检验,另有说明的除外。当比较多组数据时,使用多重比较的错误发现率(FDR)校正来校正p值。
¶ 补充图表
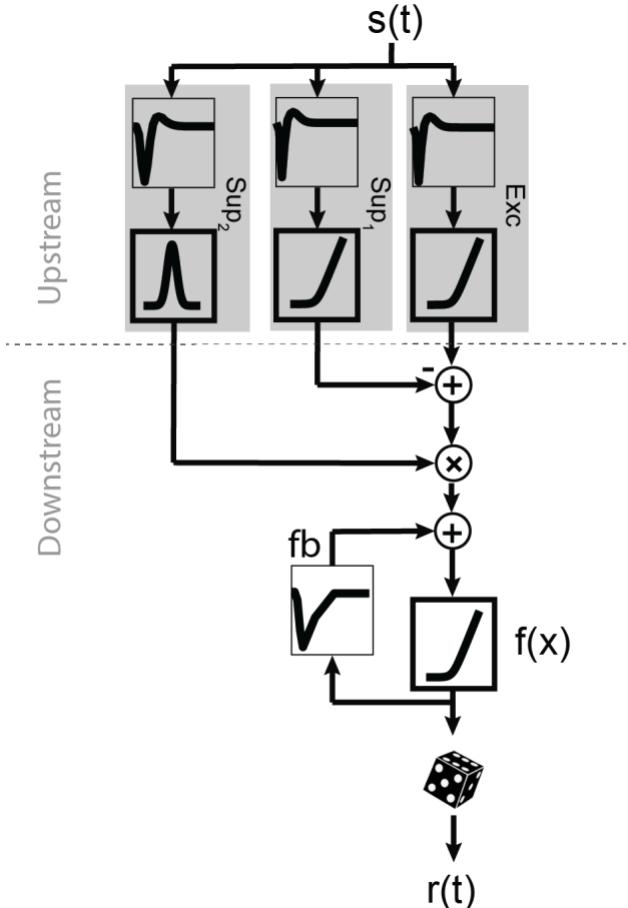
图S1 整合了图1A中模型所有组件的统一模型结构。滤波组件显示在细框中,非线性组件显示在粗框中。Exc上游分支代表兴奋,Sup1代表减法抑制,Sup2代表除法抑制。反馈(fb)被添加到模型的下游部分。
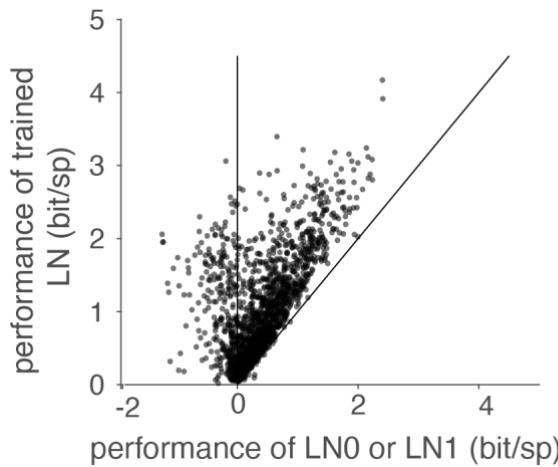
图S2 比较我们训练的LN模型与以下两种LN模型的性能:一种是以STA作为滤波器、以相关的尖峰直方图作为非线性函数的LN模型(LN0),另一种是以STC的第一主成分作为滤波器、以相关的尖峰直方图作为非线性函数的LN模型(LN1)。省略了12个LN0和LN1性能均< -2比特/秒的细胞。
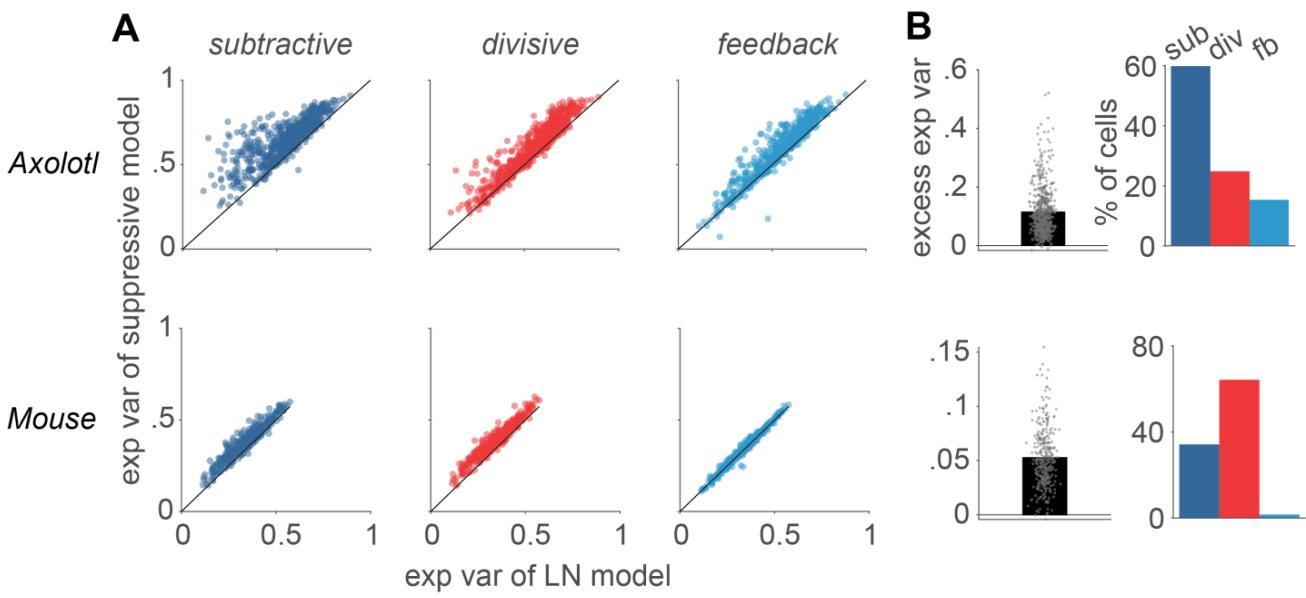
图S3 与图1B-C相同,但针对泊松解释变异性。A) 每个模型的泊松解释变异性与LN模型性能的比较。每个数据点代表一个细胞。B) 左图:最佳表现抑制模型的超额解释变异性(抑制模型的解释变异性减去LN模型的解释变异性),针对每个细胞确定。右图:各抑制模型的解释变异性高于所有其他模型的细胞百分比。
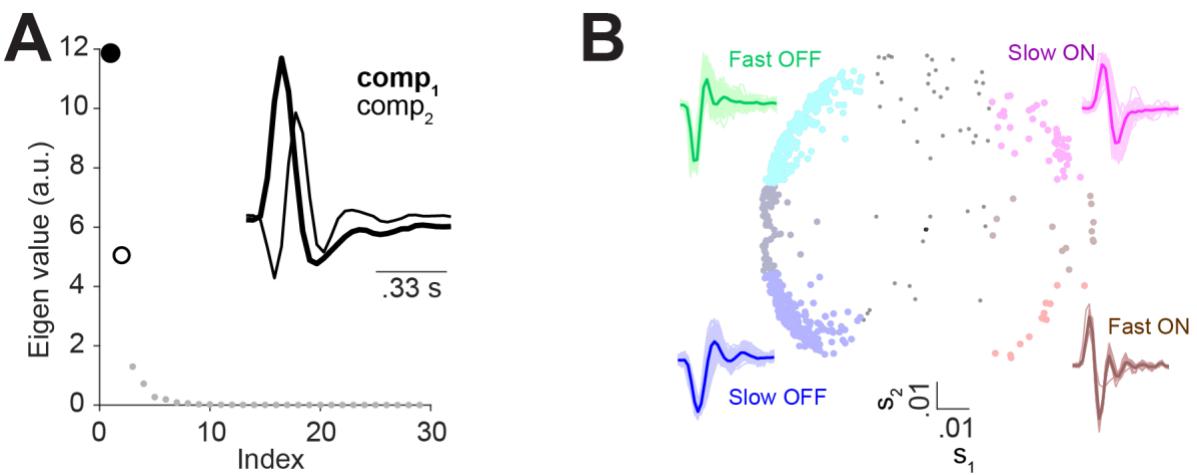
图S4 对兴奋性滤波器形状的主成分分析,以将从美西螈视网膜记录的细胞分为功能类别。A) 与LN模型滤波器的30个主成分相关的特征值。插图:用于分类的第一和第二主成分。B) 中心:所有被分析的美西螈细胞在s1(第一主成分得分)和s2(第二主成分得分)空间中的分布。为了确定类别,每个细胞的得分与第一主成分的0.02和第二主成分的0.5×标准差=0.02进行比较:慢ON细胞(n=48)的s1>0.02且s2>0.02,快ON细胞(n=13)的s1>0.02且s2<-0.02,慢OFF细胞(n=195)的s1<-0.02且s2<-0.02,快OFF细胞(n=208)的s1<-0.02且s2>0.2。143个细胞因未达到任何阈值而未被分类。周围:每个已识别组的LN模型滤波器(细线)及其平均值(粗线)。
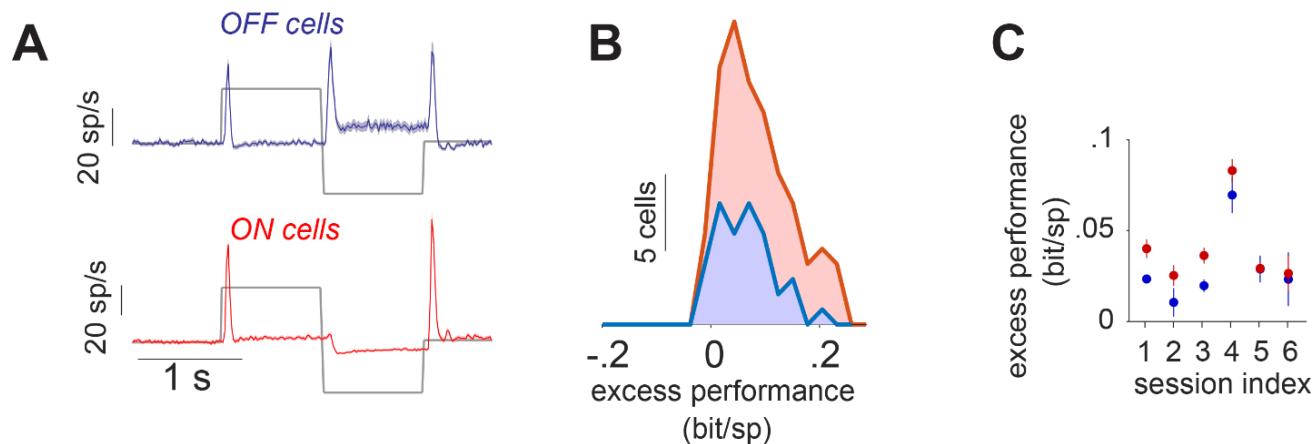
图S5 在光强度阶跃刺激下,狨猴ON细胞和OFF细胞最佳性能模型的表现。分析方法与图4类似。A)根据细胞对阶跃刺激的反应将其分为ON细胞和OFF细胞。显示了某一样本会话中每个类别内反应的平均值。B)在某一样本会话中,最佳性能模型在ON细胞和OFF细胞上的超额性能分布。C)最佳性能模型在每个记录会话中细胞上的表现。
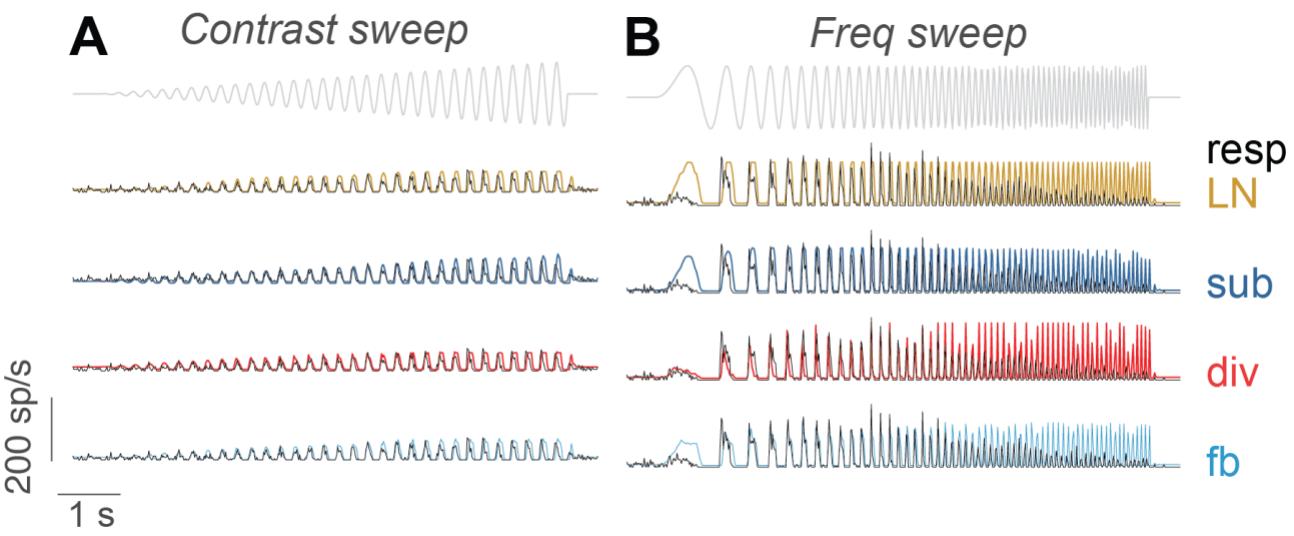
图S6 图5A-D中样本细胞的反应以及模型对对比度扫描和频率扫描整个范围的预测。A)图5A-B中的细胞。B)图5C-D中的细胞。
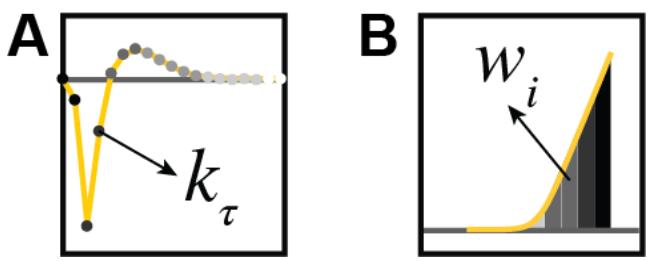
图S7 滤波器的基函数以及上游输出函数。A)每个滤波器的基函数(灰色点)为一个时间仓(刺激帧)。美西螈和小鼠使用30个基函数,狨猴使用15个基函数,这是因为与其他物种相比,狨猴视网膜神经节细胞的反应动态更快。所有细胞的反馈滤波器均使用20个基函数。B)每个输出函数的基函数为帐篷形函数(灰色帐篷)。所有基函数共同提供该函数的分段线性估计。使用了15个基函数,覆盖范围为[-3,3]。