¶ 对引导性和非引导性前脑类器官的多组学分析揭示了细胞组成和代谢谱的差异
¶ 原文下载:piis2667237525003315111.pdf
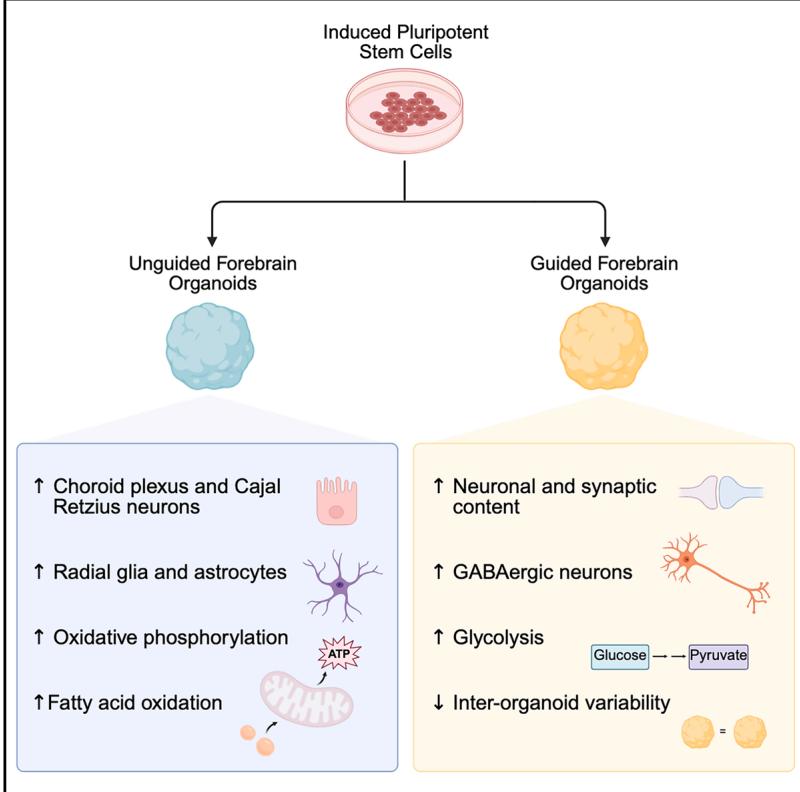
¶ 图解摘要
¶ 作者
Marie SejbergØhlenschlæger、Pia Jensen、Jesper Foged Havelund、…、Madeline A. Lancaster、Martin Røssel Larsen、Helle Bogetofte
¶ 简而言之
Øhlenschlæger等人对通过两种关键方法(引导分化和非引导分化)生成的前脑类器官进行了多组学分析。他们记录了这两种前脑类器官在细胞类型组成和代谢谱方面的显著差异,为神经类器官领域提供了一项资源和方法学指南。
¶ 亮点
• 我们对引导性和非引导性前脑类器官进行了广泛的多组学分析
• 我们展示了神经元和神经胶质细胞类型组成上的显著差异
• 引导性和非引导性前脑类器官具有不同的代谢特征
• 疾病相关表型的建模可能会受到类器官方法选择的影响
¶ 发表在:《细胞报告·方法》
¶ 对引导性和非引导性前脑类器官的资源多组学分析揭示了细胞组成和代谢谱的差异
Marie SejbergØhlenschlæger,1 Pia Jensen,1 Jesper Foged Havelund,1 Sissel Ida Schmidt,1
法杜莫·阿卜杜拉希·穆罕默德,2 玛格达莱娜·萨克利夫,3 索菲·布洛姆贝里·埃尔姆奎斯特,1 卢克蕾齐娅·克里斯库洛,1 史蒂文·W·温格特,3 伊拉莉亚·基亚拉迪亚,3 埃利夫·拜拉姆,4,5 耶普·艾伦·阿比尔德斯滕·尼科莱森,1 莱娜·安德鲁普·雅各布森,1 乔纳森·布鲁尔,6 迈克尔·埃里克森·本罗斯,4,5 克里斯汀·弗罗伊德,2 尼尔斯·约阿基姆·费格曼,1 玛德琳·A·兰卡斯特,3 马丁·勒塞尔·拉森,1 以及赫勒·博厄托夫特1,7,*
1 丹麦南丹麦大学,生物化学与分子生物学系,5230 欧登塞 M
2 哥本哈根大学健康与医学科学学院兽医与动物科学系,丹麦腓特烈斯贝C区1870号
3 英国剑桥市剑桥生物医学园区,医学研究委员会分子生物学实验室,邮编CB2 0QH
4 丹麦哥本哈根市北区2200号,哥本哈根大学健康与医学院临床医学系
5 丹麦哥本哈根大学医院哥本哈根心理健康中心,哥本哈根生物与精准精神病学研究中心,2900 海勒鲁普
6 丹麦南丹麦大学生物化学与分子生物学系DaMBIC,丹麦欧登塞M,5230
7 主要联系人
*通信作者:hbogetofte@bmb.sdu.dk
https://doi.org/10.1016/j.crmeth.2025.101295
¶ 动机
通过引导分化或非引导分化生成的人类前脑类器官,是研究人类大脑发育的重要模型系统。然而,这两种分化方法所产生的差异尚未完全阐明。为解决这一问题,我们对引导分化和非引导分化的前脑类器官进行了大规模多组学分析,发现它们在细胞组成和代谢活动方面存在显著差异。
¶ 摘要
神经类器官是研究神经发育的宝贵模型系统,可通过引导或非引导方法生成。尽管这些模型对该领域很重要,但它们之间的差异尚不清楚。为了进行无偏比较,我们对采用两种广泛应用的引导和非引导方案平行生成的前脑类器官进行了多组学分析。引导性前脑类器官包含更大比例的神经元,包括γ-氨基丁酸能中间神经元,而非引导性类器官在后期则含有明显更多的脉络丛、放射状胶质细胞和星形胶质细胞。我们发现了代谢谱的显著差异,表明非引导性前脑类器官中氧化磷酸化和脂肪酸β-氧化水平升高,而引导性前脑类器官更依赖糖酵解。总体而言,我们的研究全面描述了这些引导性和非引导性前脑类器官之间的多组学差异,并为研究神经发育和疾病的神经类器官领域提供了重要资源。
¶ 引言
3D细胞培养技术的发展极大地提高了体外模型的复杂性。这有利于神经组织的建模,改善了早期大脑发育中关键细胞事件的重现。1–3神经类器官已被用于发育障碍4–7和神经退行性疾病8–10的研究。自问世以来,多种3D神经类器官方案被开发出来,产生了一系列模型。11–13
神经类器官可通过无导向分化或有导向分化生成。2013年,兰开斯特等人提出了无导向分化技术,并将其应用于大脑类器官的生成,该技术依赖多能干细胞(PSCs)在缺乏外在信号的情况下生成神经外胚层的内在能力。早期的类器官被包埋在细胞外基质(ECM)中,这有助于神经上皮芽的形成,进而发育为皮质结构。由此产生的无导向神经类器官可形成多种脑区特征,例如包含视网膜组织以及脉络丛(ChP)等非神经组织。然而,通过对该方案的进一步优化,已能可靠地生成具有前脑特征的大脑类器官,因此我们在此将这些类器官称为无导向前脑类器官(FOs)。
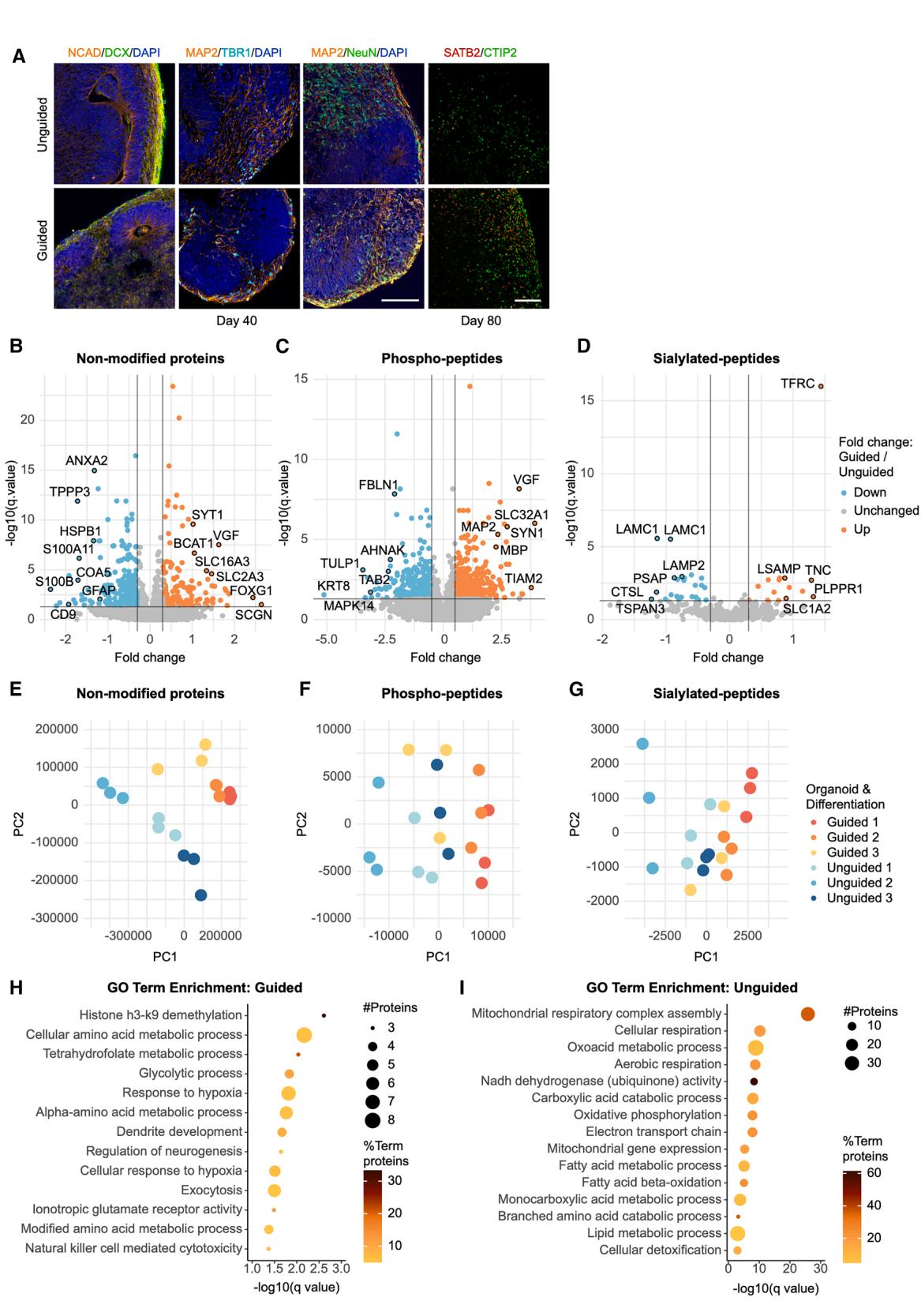
图1. 基于神经元和代谢蛋白的蛋白质组学/翻译后修饰谱可区分引导性和非引导性FOs(A)第40天和第80天FOs中N-钙粘蛋白(NCAD,橙色)、双皮质素(DCX,绿色)、微管相关蛋白2(MAP2,橙色)、T-box脑转录因子1(TBR1,青色)、神经元核蛋白(NeuN,绿色)、DNA结合蛋白SATB2(红色)和CTIP2(绿色)的免疫细胞化学染色,DAPI(深蓝色)复染。比例尺,100 μm。(B-D)火山图显示(B)非修饰蛋白、(C)磷酸肽和(D)第40天FOs中唾液酸化N-糖肽的倍数变化和−log10(q值),数据来自三次分化实验(n=9个FOs,q≤0.05且倍数变化±0.3被视为显著,采用秩乘积检验)。(E-G)对(E)非修饰蛋白、(F)磷酸肽和(G)唾液酸化N-糖肽进行主成分分析(PCA),其中引导性FOs(蓝色)与非引导性FOs(橙色)按分化实验(1-3)标记。(H-I)引导性与非引导性FOs中(H)丰度增加和(I)丰度降低的非修饰蛋白的基因本体(GO)术语富集分析(q≤0.05,倍数变化±0.3)。点的大小表示显著差异蛋白的数量,颜色表示其占通路总蛋白数的百分比(采用双侧超几何检验并进行Bonferroni逐步校正)。另见表S1。
另一方面,引导性类器官分化利用小分子和生长因子来诱导区域特化并促进神经元成熟。17,18 这包括在引导性类器官方案中,使用双重SMAD抑制进行神经诱导,使用表皮生长因子(EGF)和成纤维细胞生长因子(FGF)进行神经扩增,以及后期使用脑源性神经营养因子(BDNF)和神经营养因子3促进成熟。19 这使得能够形成类似背侧或腹侧前脑、中脑或后脑的脑区特异性类器官。19–22 一种常用的引导方案是Pasca等人于2015年开发的背侧FO方案。18,19
这些特定的背侧前脑和大脑类器官方案的商用分化试剂盒的开发,进一步促进了它们的普及和使用。
两种类型的FO在基因表达水平上均已被证实与胎儿脑组织相似,能够复制皮质板发育过程中的细胞事件,并模拟早期皮质层形成的时间和结构。
然而,由于只有少数研究同时包含了有引导和无引导的FO协议,我们对这两种不同协议所产生的差异的总体理解是有限的。24,25
为了为模型系统的选择建立更充分的依据,并考察模型选择对实验结果的潜在影响,我们采用多组学方法对两种最广泛使用的方法进行了直接比较。该比较从分化第40天进行到第120天,旨在检测轨迹中的早期差异。
综合分析表明,与未受引导的类前脑器官(FOs)中星形胶质细胞、脉络丛(ChP)和 Cajal-Retzius 神经元占比较高的情况相比,受引导的类前脑器官中神经元(包括γ-氨基丁酸能中间神经元)含量增加。研究揭示了不同的代谢特征:未受引导的类前脑器官中氧化磷酸化(OXPHOS)和脂肪酸β-氧化(FAO)水平较高,而受引导的类前脑器官更依赖糖酵解。我们在由精神分裂症(SCZ)患者诱导多能干细胞(iPSCs)和年龄匹配的对照组(CTLs)生成的类前脑器官中证实了这些结果,并观察到每种类型的类前脑器官都具有不同的蛋白质组疾病特征。
这些结果凸显了这些有引导和无引导的FO协议在结果上的关键差异,并表明需要对类器官模型进行深入表征和比较,以便在其应用方面做出明智决策。
¶ 结果
¶ 蛋白质组学分析发现神经元蛋白和代谢蛋白的表达存在差异
为了研究使用STEMCELL Technologies公司市售试剂盒通过引导法或非引导法生成的类脑组织(FOs)之间的差异,我们从相同的诱导多能干细胞(iPSCs)出发,平行执行了这两种方案(图S1A)。我们最初选择将引导法生成的类脑组织维持在静态培养中,而非引导法生成的类脑组织则按照方案要求从第10天开始进行振荡培养。通过免疫细胞化学(ICC)检测发现,在第40天和第80天,引导法和非引导法生成的类脑组织在细胞结构以及关键神经发育标志物的分布上总体具有可比性(图1A)。尽管每个类器官起始的诱导多能干细胞数量较少,但非引导法生成的类脑组织明显大于引导法生成的类脑组织(图S1A-S1C),且在第40天时每个类器官的蛋白质含量更高(图S1D)。尽管非引导法生成的类器官在形态上差异较大,但我们观察到其心室长度并无差异(图S1E)。两种方案主要都能诱导出前脑特异性,这一点可通过叉头框蛋白G1(FOXG1)的表达得到证实,FOXG1是前脑发育过程中一种必不可少的转录因子27(图S1F)。
为了对受引导和不受引导的类卵泡(FOs)进行无偏倚比较,我们对来自三个独立分化过程的第40天类卵泡进行了大规模蛋白质组学分析(n = 9)。使用我们之前发表的翻译后修饰(PTM)蛋白质组学方法,我们定量了7082种蛋白质、15775种磷酸肽(来自4238种蛋白质)和663种唾液酸化N-糖肽(来自441种蛋白质)的水平(图1B-1D)。主成分分析(PCA)基于未修饰的蛋白质清晰地将不受引导和受引导的类卵泡区分开来,尽管区分度较低,但也能通过翻译后修饰肽将两者区分(图1E-1G)。受引导和不受引导的类卵泡之间,有757种蛋白质、1079种磷酸肽和44种唾液酸化N-糖肽的水平存在显著差异,这表明分化方法会明显影响蛋白质组学结果(表S1)。
在引导性FO中增加的差异丰度蛋白(DAP)包括FOXG1和其他神经元特异性蛋白,如突触结合蛋白1和神经分泌蛋白VGF,而神经胶质标志物胶质纤维酸性蛋白(GFAP)和S100B在非引导性FO中丰度更高(图1B;表S1A和S1B)。对引导性FO中增加的DAP进行的基因本体论(GO)术语富集分析相应地包括“树突发育”“神经发生调控”和“离子型谷氨酸受体活性”(图1H)。
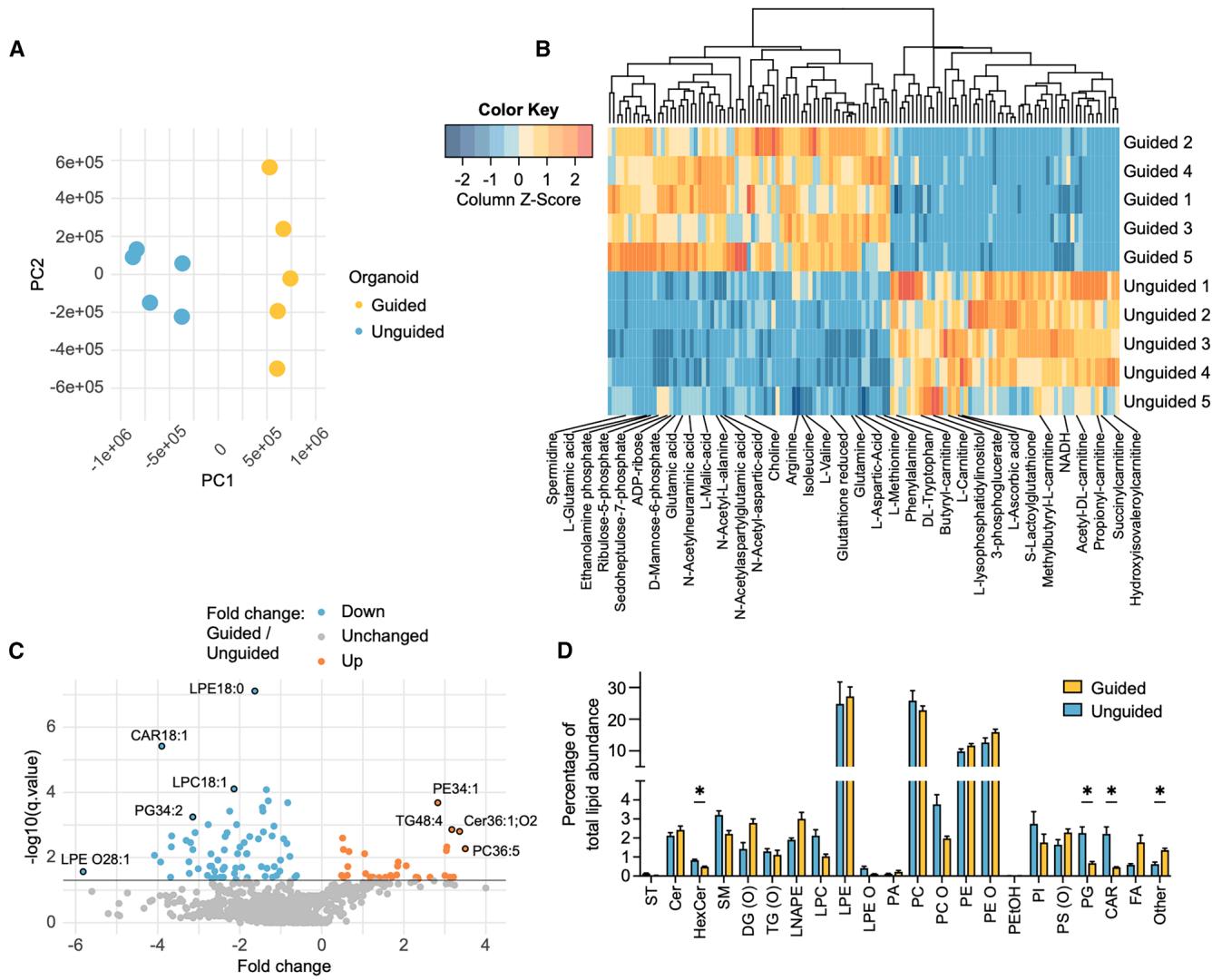
图2. 引导性和非引导性FOs具有不同的代谢组/脂质组谱
(A)在第40天的引导组(蓝色)与非引导组(橙色)类器官(FOs)中对代谢组学数据进行的主成分分析(PCA)(n=5个类器官,1次分化)。(B)通过层次聚类排序的引导组与非引导组类器官中显著差异代谢物(q≤0.05)的热图(n=5个类器官,秩乘积检验)。(C)脂质组学数据的火山图,显示引导组与非引导组类器官的折叠变化和−log10(q值)(n=5个类器官,q≤0.05被视为显著,秩乘积检验)。(D)按脂质类别分类的已鉴定和注释脂质,每个脂质类别的水平以每个类器官中总脂质丰度的百分比表示。平均值±标准误(n=5个类器官,Student t检验,Benjamini-Hochberg校正)。*q≤0.05。
另请参见表S2和S3。
在引导性纤维束(FOs)中,包括VGF、MAP2和突触蛋白1(SYN1)在内的众多神经元/突触蛋白的磷酸化水平有所升高(图1C;表S1C和S1D)。在引导性FOs中唾液酸化丰度显著更高的蛋白质与轴突发生相关,包括促进神经元生长和轴突靶向的LSAMP蛋白,以及突触间隙中的谷氨酸转运体SLC1A2(图1D;表S1E和S1F)。
令人惊讶的是,对在无引导FO中增加的DAP进行GO术语富集分析表明,这些DAP主要参与能量代谢,例如“线粒体呼吸复合体组装”、“氧化磷酸化(OXPHOS)”和“脂肪酸氧化(FAO)”(图1I)。相应地,“糖酵解过程”在有引导FO中增加的DAP中富集(图1H)。
总体而言,蛋白质组学分析指出,在有引导和无引导的FOs之间,神经元和代谢蛋白的丰度及翻译后修饰存在关键差异。
¶ 引导组和非引导组类器官的代谢组学和脂质组学特征存在差异
鉴于能量代谢蛋白存在差异,我们对从新批次诱导多能干细胞(iPSCs)分化而来的5个无引导类卵泡(FOs)和5个有引导类卵泡进行了代谢组学/脂质组学分析。通过分析,我们对300种代谢物和794种脂质进行了注释和定量(表S2和S3)。在主成分分析(PCA)中,代谢物谱能清晰区分有引导和无引导的类卵泡(图2A和2B)。脂质组学谱也存在差异,有引导类卵泡中有35种脂质显著增加,无引导类卵泡中有68种脂质显著增加(图2C)。四类脂质显示出显著差异,无引导类卵泡中己糖神经酰胺、磷脂酰甘油和肉碱的比例较高,而有引导类卵泡中主要是油酰胺(在“其他”亚组中)的比例较高(图2D;表S3C)。油酰胺是一种脂肪酸酰胺,它能与大麻素受体及其他神经递质系统相互作用,并且可能刺激神经发生。己糖神经酰胺对髓鞘的结构和功能至关重要,在少突胶质细胞中含量丰富。结合对有引导和无引导类卵泡的代谢组学/脂质组学分析,这支持了类卵泡中代谢蛋白表达水平存在差异这一发现。
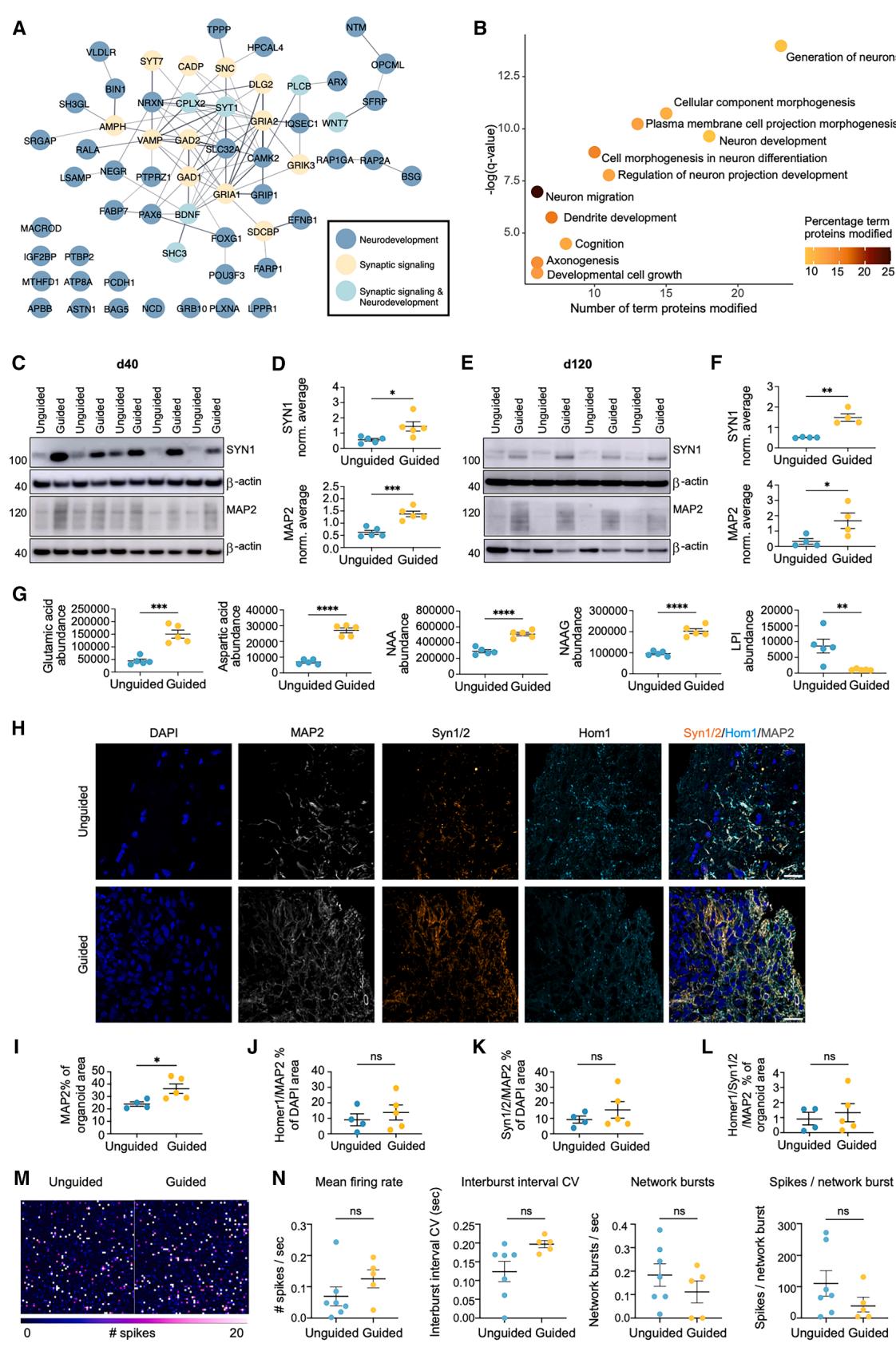
图3. 早期和晚期有引导类卵泡(FOs)中神经元蛋白和突触蛋白的丰度更高
(A)蛋白质组学分析中,在引导性FO与非引导性FO中,参与突触信号传导和/或神经发育的重要蛋白质的字符串网络(q≤0.05,折叠变化±0.3)(n=9个FO,来自3次分化,秩乘积检验)。
(B) 对引导型与非引导型FO中磷酸化水平显著增加(q值≤0.05,倍数变化±0.3)的蛋白质进行GO术语富集分析,显示每个通路/术语中显著蛋白质的数量。点的颜色表示这些蛋白质占通路总蛋白质数量的百分比(双侧超几何检验,Bonferroni逐步下降法)。
(C-F)第40天(C和D)及第120天(E和F)类器官(FOs)中突触蛋白1(SYN1)和微管相关蛋白2(MAP2)水平的代表性蛋白质印迹及定量分析。蛋白质表达以β-肌动蛋白为内参进行标准化,并取每个印迹中所有样本的平均值。均值±标准误(n=4-5个类器官,采用Student’s t检验)。
(G)通过代谢组学量化的神经递质丰度水平。NAA,N-乙酰天门冬氨酸;NAAG,N-乙酰天门冬氨酰谷氨酸;LPI,溶血磷脂酰肌醇。平均值±标准误(n = 5个卵泡,一次分化,秩乘积检验)。
(H-L)第80天FOs中DAPI(深蓝色)、MAP2(白色)、突触蛋白Syn1/2(橙色)和Homer1(Hom1,青色)的ICC,以及(I)MAP2+、(J)Hom1+/MAP2+、(K)Syn1/2+/MAP2+和(L)Syn1/2+/Hom1+/MAP2+区域占类器官或DAPI区域(如所示)百分比的定量分析。比例尺,20μm。平均值±标准误(n=4-5个FOs,来自两次分化,Student t检验)。
(M和N)第120天FOs的MEA记录,显示2分钟内的平均发放率(峰电位/秒)、爆发间隔变异系数(CV)、网络爆发次数以及每次网络爆发的峰电位数量。平均值±标准误(n=5-6个FOs,来自两次分化,Student t检验)。p≤0.05,p≤0.01,p≤0.001,****p≤0.0001。
另请参见图S1。
¶ 与未引导的FO相比,引导的FO中神经元含量增加
在受引导的类卵泡(FOs)中,与突触和神经元相关的差异磷酸化蛋白(DAPs)有所增加,包括谷氨酸受体(GRIK3和GRIA2)、γ-氨基丁酸(GABA)信号传导中的重要蛋白(GAD1、GAD2和SLC32A)、脑源性神经营养因子(BDNF)以及大脑发育中的关键转录因子(FOXG1、PAX6和POU3F3)(图3A)。对受引导的类卵泡中磷酸化水平增加的蛋白质进行基因本体(GO)术语富集分析,进一步支持了神经元和神经元突起生成的增强(图3B)。为了证实这一点,我们对突触蛋白1(SYN1)和微管相关蛋白2(MAP2)进行了蛋白质印迹分析,发现在第40天的受引导类卵泡中,两者的水平均显著增加(图3C和3D)。有趣的是,这些差异在第120天的类卵泡中仍然存在(图3E和3F)。相应地,通过代谢组学分析鉴定出的五种神经递质中,有四种(包括谷氨酸)在受引导的类卵泡中的水平显著升高(图3G)。为了评估是否存在突触接触,我们进行了免疫细胞化学(ICC)实验,以检测突触前蛋白突触素1/2(Syn1/2)和突触后蛋白Homer1在MAP2阳性突起上的共定位情况。在第40天,两种类器官中Syn1/2和Homer1的水平看似相近,且观察到的点状共定位有限(图S1G和S1H)。在第80天,受引导的类卵泡中总MAP2水平显著增加,而总Syn1/2、Homer1水平以及突触数量则相当(图3H、3L和S1G)。为了评估它们的自发电生理活性,我们将第100天的受引导和未受引导的类卵泡放置在多电极阵列(MEA)芯片上,培养20天后,从 spike 活动图中可以看出形成了扩展的轴突网络(图3M)。与ICC观察到的突触数量相近一致,第120天的MEA记录显示两组之间没有任何显著差异(图3N)。总体而言,我们发现大量证据表明,在早期和后期时间点,受引导的类卵泡中神经元含量均有所增加。
¶ 在无引导的FO中,放射状胶质细胞/星形细胞含量增加,且FOXG1定位于细胞质中
基于无引导FO中GFAP和S100B水平的升高,我们推测引导FO中神经元含量的增加是以放射状胶质细胞(RG)含量的减少为代价,或许在后期阶段星形胶质细胞的数量也会减少。免疫细胞化学(ICC)显示,两组在第40天时GFAP染色均较稀疏(图4A;图S1I)。然而,在第80天,引导FO中观察到GFAP的表达显著降低(图4B和4C)。第40天时通过蛋白质印迹法检测GFAP(图4D和4E),以及第120天时检测GFAP和S100B,均证实了这一点,且此时观察到了显著差异(图4F-4H)。令人惊讶的是,在第80天,两种FO类型中GFAP+细胞内FOXG1的亚细胞定位存在显著差异。在无引导FO中,FOXG1与胞质内的GFAP染色共定位,而在引导FO中,FOXG1位于细胞核内(图4B)。在通过MAP2识别的神经元群体中未观察到胞质FOXG1的表达(图4B),这表明这种转变是GFAP+细胞所特有的。由于FOXG1在祖细胞中位于细胞核内,而在分化细胞中位于细胞质内,这可能表明GFAP+细胞在分化阶段存在差异。总体而言,这表明在早期时间点(第40天)放射状胶质细胞的数量存在显著差异,这可能会影响后期阶段(第80天和120天)神经胶质祖细胞和星形胶质细胞的数量。
¶ 非引导性FO中线粒体含量和OXPHOS蛋白增加
或许是由于细胞组成的差异,蛋白质组学分析发现了几种与能量代谢相关的差异表达蛋白(DAPs)。在未受引导的脂肪细胞(FOs)中,发现大量三羧酸循环(TCA cycle)、复合体I、脂肪酸氧化(FAO)及其他线粒体蛋白显著增加,而在受引导的脂肪细胞中,糖酵解相关蛋白显著增加(图5A)。有趣的是,代谢组学分析显示,受引导的脂肪细胞中糖酵解/磷酸戊糖途径(PPP)的代谢物水平显著更高(图5B)。与脂肪酸氧化蛋白的增加相对应,未受引导的脂肪细胞中各种肉碱的水平显著升高(图2B和图5B)。肉碱的主要功能是将长链脂肪酸转运至线粒体进行β-氧化。33
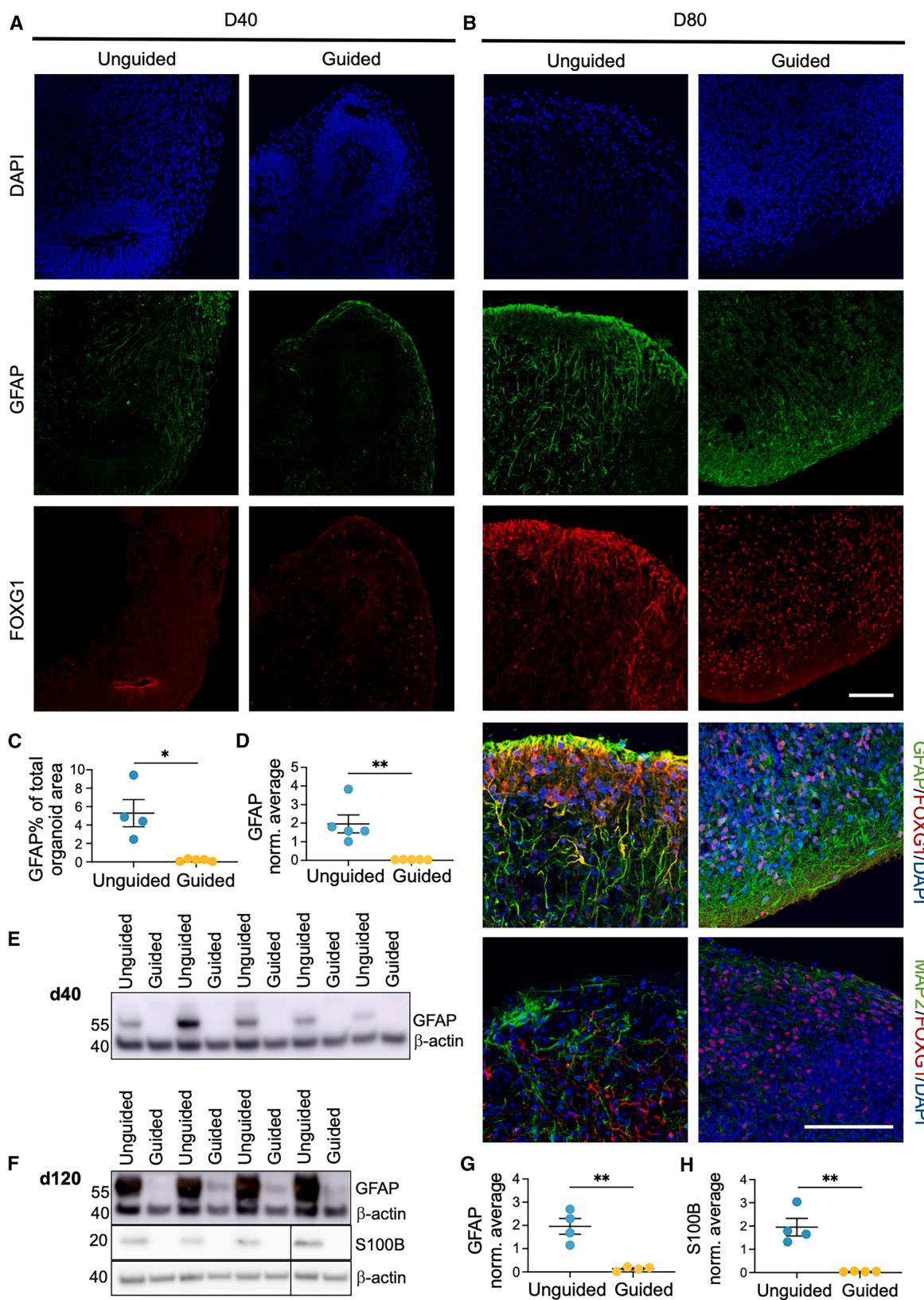
图4. 在无引导的FO中,S100B和GFAP+细胞的丰度更高,且FOXG1的亚细胞定位发生改变
(A–C)第40天(A)和第80天(B)类卵泡(FOs)的免疫细胞化学(ICC)染色,分别显示DAPI(深蓝色)、叉头框G1(FOXG1,红色)、胶质纤维酸性蛋白(GFAP,绿色)或微管相关蛋白2(MAP2,绿色)。比例尺,100μm。(C)第80天GFAP+细胞面积占总DAPI+类器官面积百分比的定量分析。平均值±标准误(SEM)(n = 4–5 个类器官,来自两次分化,采用 Student’s t 检验)。
(D-H)代表性蛋白质印迹及GFAP水平定量分析:(D和E)第40天、(F和G)第120天,以及(F和H)第120天类卵泡(FOs)中的S100B。蛋白质表达量以β-肌动蛋白为内参进行标准化,并取每个印迹中所有样本的平均值。均值±标准误(n = 4-5个卵泡,Student t检验)。*p ≤ 0.05,**p ≤ 0.01。
另请参见图S1。
为了探究未引导卵泡中氧化磷酸化(OXPHOS)相关蛋白的增加是否由线粒体含量增加引起,我们检测了线粒体标志物TOMM20的水平。蛋白质印迹分析显示,在第40天和第120天,TOMM20的水平均显著升高(图5C-5E),这表明未引导卵泡含有相对更多的线粒体。与此一致的是,通过Seahorse分析测量的总ATP生成量在未引导卵泡中显著更高(图5F)。代谢组学分析发现,未引导卵泡中NADH/NAD的比值也显著更大,这与上述结果相关(图5G)。或许由于未引导卵泡中OXPHOS水平较高,与引导卵泡相比,其清除活性氧(ROS)的能力以及还原型谷胱甘肽的水平显著降低(图5H和5I)。
综上所述,我们的研究结果表明,与更多依赖糖酵解的引导脂肪细胞相比,未引导脂肪细胞的线粒体含量更高,且更依赖氧化磷酸化。
¶ 在引导和非引导的FO中,糖酵解蛋白水平与HIF1α水平不相关
考虑到有结果表明受引导的类纤维(FOs)中神经元分化加快,未受引导的类纤维中线粒体含量增加和氧化磷酸化(OXPHOS)增强这一现象似乎有违直觉。在从神经前体细胞向有丝分裂后神经元的正常分化过程中,会发生从糖酵解到氧化磷酸化的代谢转换,同时线粒体含量增加。除了线粒体含量的差异外,我们还观察到与溶酶体相关的变化。在未受引导的类纤维中,参与“溶酶体运输”和“蛋白质靶向溶酶体”的蛋白质的唾液酸化水平显著升高(图5J)。溶酶体标志物LAMP1糖基化形式的蛋白质印迹分析显示,在第40天其丰度显著增加,这证实了蛋白质组学数据(图5K和5L)。像LAMP1这样的溶酶体蛋白需要N-连接糖基化(包括唾液酸化)才能正确靶向溶酶体并在其中发挥作用,它们的上调可能表明溶酶体含量增加。
受引导的卵泡(FOs)中,单羧酸转运蛋白4(MCT4)和己糖激酶2(HK2)的水平显著升高(表S1A和S1B),这两种蛋白在高度糖酵解的细胞中会被上调。37基于这些及其他糖酵解蛋白丰度的增加,受引导的FO蛋白的基因本体(GO)术语富集包括“对缺氧的应答”(图1H)。由于缺氧诱导因子1α(HIF1α)可上调HK2、MCT4和其他糖酵解蛋白的表达,37我们旨在检测是否存在缺氧水平的差异。与它们更大的尺寸一致,在第40天和第120天,未受引导的FOs中HIF1α水平显著升高(图5M-5O)。因此,缺氧程度的差异无法解释受引导和未受引导的FOs在氧化磷酸化(OXPHOS)/糖酵解依赖方面的差异。
¶ 引导性和非引导性FOs的细胞组成差异
为了研究FOs的细胞组成,我们对来自新一批诱导多能干细胞(iPSCs)生成的第20天和第40天的引导型及非引导型FOs(每组n=3)的共9913个细胞进行了单细胞RNA测序(scRNA-seq)(图S2A-S2C)。聚类和差异基因表达分析显示,存在12个祖细胞和神经元集群,与早期前脑发育中发现的主要细胞群相似,且与之前对FOs的scRNA-seq分析结果相当(图6A、6B,数据S1;表S4)。13,19,24 按时间点和类器官类型对细胞进行分类后(图6C-6E)发现,在第40天的非引导型FOs中,皮质血(CH)标志物(图6D;LMX1A;图S2D;RSPO1)和脉络丛(ChP)标志物(图6D;转甲状腺素蛋白[TTR];图S2E;氯离子细胞内通道蛋白6[CLIC6])以及相应的细胞集群水平明显更高(图6C-6E)。相应地,主要起源于CH的Cajal-Retzius细胞(CR)的关键标志物reelin(RELN)在非引导型FOs中表达更高(图6D)。26 令人惊讶的是,表达内侧神经节隆起(mGE)和中间神经元(INs)标志物的细胞群仅在引导型FOs中发现,这一点可通过mGE标志物、迁移标志物(图6D;DLX2;图S2D;DLX1、ASCL1)和成熟中间神经元标志物(图6D;GAD2)得到证实。然而,蛋白质组学分析发现,非引导型FOs中也存在GAD1和GAD2蛋白的表达,尽管其水平显著低于引导型FOs(表S1A、S1B)。
根据蛋白质组学和免疫细胞化学的研究结果,GFAP在无引导的类前脑组织中表达更广泛,而FOXG1在有引导的类前脑组织中水平更高(图S2E)。无引导类器官中FOXG1表达水平较低,可能是由于其脉络膜(CH)和脉络丛(ChP)的比例更高,而这两种结构的特点是不表达FOXG1。此外,鉴于FOXG1在腹侧前脑的表达高于背侧前脑,这也与有引导类器官中抑制性神经元数量增加的情况相符。
为了确定发育轨迹的差异,我们分别对两种类器官的单细胞RNA测序数据进行了拟时序分析(图S2G-S2J)。这证实了在受引导的FO中,存在一条从有丝分裂的放射状胶质细胞(RG)经内侧神经节隆起(mGE)到迁移性和成熟中间神经元的独特谱系(图S2G和S2H)。在无引导的FO中,发现了一条从RG经中间前体细胞(IPCs)到Cajal-Retzius细胞和深层神经元的轨迹,这与间接神经发生相对应(图S2I和S2J)。在受引导的FO中未观察到这一现象,因为其中不存在与IPCs相连的RG群体(图S2G和S2H)。这可能表明,在受引导的FO中,IPCs的形成发生在第20天之前,因为从IPCs到Cajal-Retzius细胞和深层神经元的谱系得以保留。在两种类器官中,都存在一群高表达糖酵解基因和应激标志物(如HSPH1和NEAT1)的神经元(糖酵解神经元)(图6B和6F;表S4),它们似乎是通过RG的直接神经发生产生的(图S2G和S2H)。受引导和无引导FO中糖酵解神经元的比例相似,因此无法解释受引导FO中糖酵解蛋白水平较高的原因。在第40天,受引导FO中所有细胞类型的关键糖酵解蛋白HK2和PDK1的表达普遍增加(图6F)。相比之下,氧化磷酸化(OXPHOS)相关转录本NDUFA4和UQCRB的水平在四种条件之间更为一致,主要在细胞类型间存在差异,其中脉络丛(ChP)和糖酵解神经元中的表达最高(图6G)。鉴于脉络丛中OXPHOS转录本的表达增加,该细胞群主要存在于无引导FO中,这可能是其OXPHOS水平升高的原因之一。支持这一点的是,线粒体生物合成的主要调节因子PGC-1α(PPARGC1A)的转录本在第40天无引导FO的脉络丛中表达水平最高(图S2F)。34
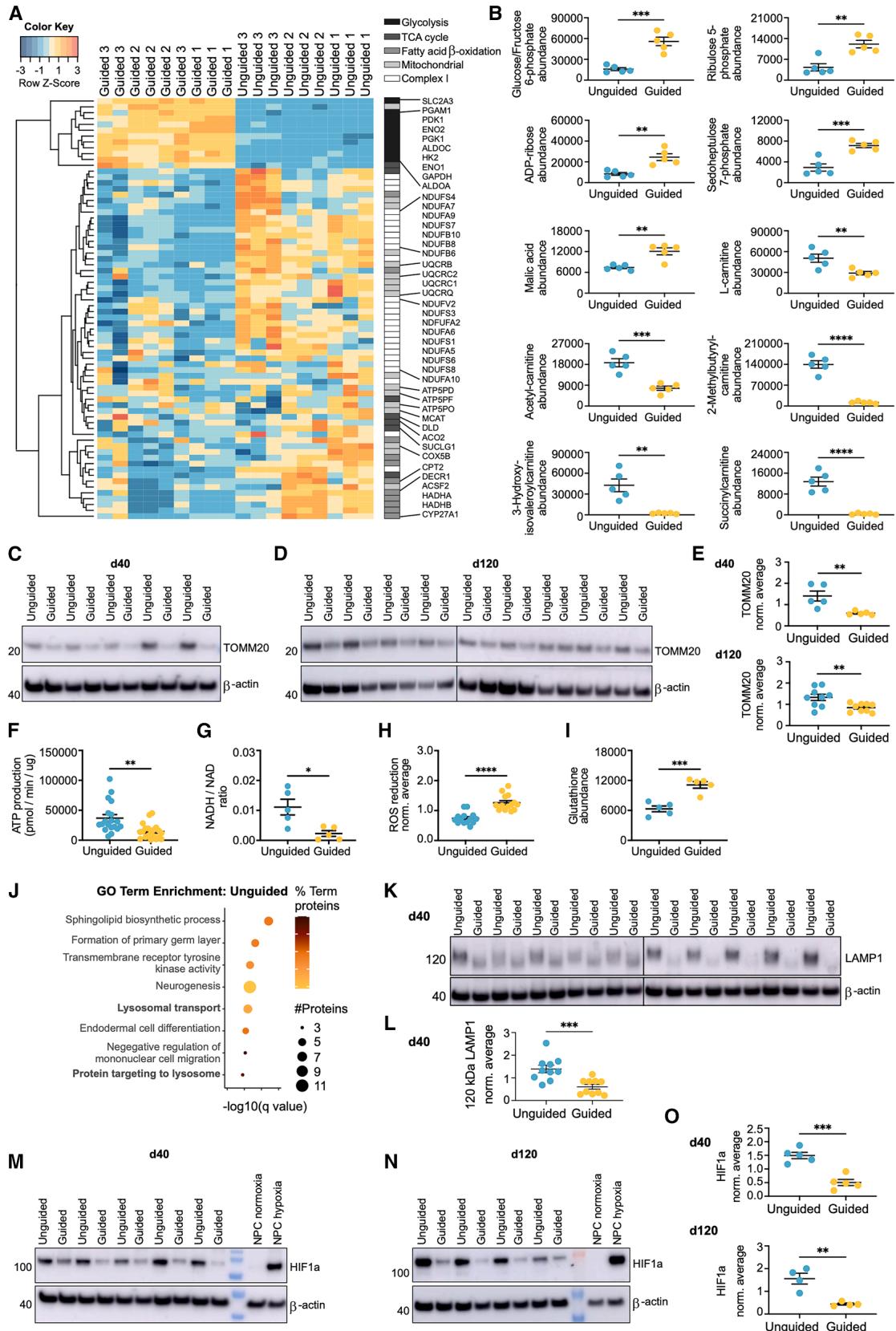
图5. 引导组与非引导组FO中线粒体和OXPHOS水平升高
(A)通过层次聚类排序的引导性与非引导性FO中,与糖酵解、三羧酸循环、脂肪酸β-氧化(FAO)、线粒体和复合体I相关的显著蛋白质(q值≤0.05,倍数变化±0.3)丰度的热图(n=9个FO,来自3次分化,秩乘积检验)。
(B)通过代谢组学定量的与糖酵解/磷酸戊糖途径或FAO相关的代谢物丰度水平。平均值±标准误(秩乘积检验)。(C-E)(C和E)第40天和(D和E)第120天FO中TOMM20水平的代表性蛋白质印迹及定量分析。蛋白质表达以β-肌动蛋白为内参进行标准化,并取每个印迹中所有样本的平均值。平均值±标准误(来自1或2次分化的5/9个FO,学生t检验)。
(F)第80天卵泡(FOs)中,以蛋白质含量(μg)标准化的ATP生成量(pmol/min)。平均值±标准误(n=3次分化得到的20个卵泡,Student’s t检验)。(G)通过代谢组学定量的NADH/NAD比率。平均值±标准误(n=1次分化得到的5个卵泡,秩乘积检验)。
(H) 卵泡(FOs)对活性氧(ROS)的减少作用,相对荧光单位按每次分化所有样本的平均值进行标准化。平均值±标准误(n=14个卵泡,来自三次分化,采用Student t检验)。
(I)通过代谢组学定量的还原型谷胱甘肽的丰度水平。平均值±标准误(n=5个卵泡,来自一次分化,秩乘积检验)。(J)在无引导与有引导卵泡中,唾液酸化水平升高的蛋白质(q≤0.05)的基因本体论(GO)术语富集分析,点的大小表示该通路中显著蛋白质的数量,颜色表示其占通路蛋白质总数的百分比(采用Bonferroni逐步校正的双侧超几何检验)。
(K-O)代表性蛋白质印迹及定量分析:(K和L)第40天类卵泡(FOs)中120 kDa糖基化LAMP1水平,(M和O)第40天及第(N和O)120天类卵泡中的HIF1α水平。神经前体细胞(NPCs)在常氧(20%氧气)或低氧(1%氧气)条件下以2D方式培养4小时作为对照。蛋白质表达水平以β-肌动蛋白为内参进行标准化,并取每个印迹中所有样本的平均值。均值±标准误(n=4-5个类卵泡,Student t检验)。p≤0.05,p≤0.01,p≤0.001,****p≤0.0001。
总体而言,单细胞RNA测序(scRNA-seq)识别出了细胞成分上的差异,这在一定程度上可以解释观察到的代谢差异,同时也证实了在受引导的卵泡(FOs)中,不同细胞类型的糖酵解转录本普遍增加。
¶ 摇动培养受引导的FOs不会改变其缺氧水平,也不会改变其与未受引导的FOs之间的代谢差异
引导性类卵泡(FOs)糖酵解总体增加的一个潜在促成因素可能是其在遵循STEMCELL Technologies协议时的静态培养条件。非引导性类卵泡从第10天开始在轨道摇床上培养,这可能会增加氧合并限制缺氧。因此,我们将静态条件下培养的引导性类卵泡与从第6天到第40天在轨道摇床上培养的引导性类卵泡进行了比较。我们注意到,在摇床培养时,引导性类卵泡的大小显著增加(图7A)。然而,通过比较HIF1α和TOMM20的水平,我们发现缺氧程度或线粒体含量没有差异(图7B-7D),这表明引导性和非引导性类卵泡之间的代谢差异并非由静态培养与振荡培养条件引起。
为了确定这一点并探究类器官模型的选择如何在疾病背景下影响结果,我们从3名精神分裂症(SCZ)患者和3名年龄匹配的对照者(CTLs)的诱导多能干细胞(iPSCs)中生成了引导性和非引导性前脑类器官(FOs),两种类器官均在振荡条件下培养(图S3和S4)。所有6个诱导多能干细胞系都生成了引导性和非引导性前脑类器官,在第20天时,通过TBR2、SOX2和HuC/D的表达可以看出,这些类器官中皮质神经祖细胞的水平相当,且在第40天时它们的大小没有显著差异(图7E和S4)。相应地,对第40天的蛋白质组学数据进行主成分分析(PCA),发现引导性和非引导性前脑类器官分别聚类,与它们来源的诱导多能干细胞的身份无关(图7F)。有趣的是,引导性和非引导性前脑类器官组内不同诱导多能干细胞系之间的变异程度似乎相似(图7F)。比较所有6个诱导多能干细胞系的引导性和非引导性前脑类器官,发现1156种蛋白质的丰度水平存在显著差异。神经元相关蛋白如谷氨酸受体1、MAP2、FOXG1和SOX1在引导性前脑类器官中丰度更高,而脉络丛(ChP)相关蛋白如TTR和CLIC6在非引导性前脑类器官中丰度更高(图7G;表S5A和S5B)。对差异丰度蛋白(DAPs)进行基因本体(GO)术语富集分析,结果证实了早期的研究结果:引导性前脑类器官中富集了“大脑皮质发育”“树突发育”和“轴突延伸调控”等术语,而非引导性前脑类器官中则富集了“线粒体翻译”“有氧呼吸”和“脂肪酸氧化(FAO)”等术语(图7H和7I)。这证实了初始实验的结果并非由细胞系决定,而是由实验方案决定的。此外,由于两种类型的前脑类器官现在均在振荡条件下培养,这就排除了引导性前脑类器官原本的静态培养条件是观察到的代谢差异的原因这一可能性。
为了了解类前脑器官(FOs)的蛋白质表达谱与发育中的人类前脑相比如何,我们对妊娠第9周(GW9)人类胎儿额叶的蛋白质组学数据(Zhao等人)进行了相关性分析。我们的研究识别出GW9胎儿额叶中90%的蛋白质(图S5A;表S6),并显示胎儿与类前脑器官的蛋白质丰度之间存在显著的正相关性,这种相关性在引导性和非引导性类前脑器官中相似(图S5B和S5C)。与胎儿额叶相比,在类前脑器官中具有高标准化丰度的蛋白质并未富集特定的功能或通路。然而,与胎儿额叶相比,在类前脑器官中标准化丰度最低的蛋白质富集了细胞外基质(ECM)蛋白质。这在引导性类前脑器官中最为明显,而非引导性类前脑器官中,包括FOXG1、TBR1和SOX2在内的关键前脑/皮质转录因子的丰度也相对较低(图S5D和S5E)。总体而言,这两种类型的类前脑器官在蛋白质表达上与GW9胎儿额叶都表现出高度且相当的相关性。
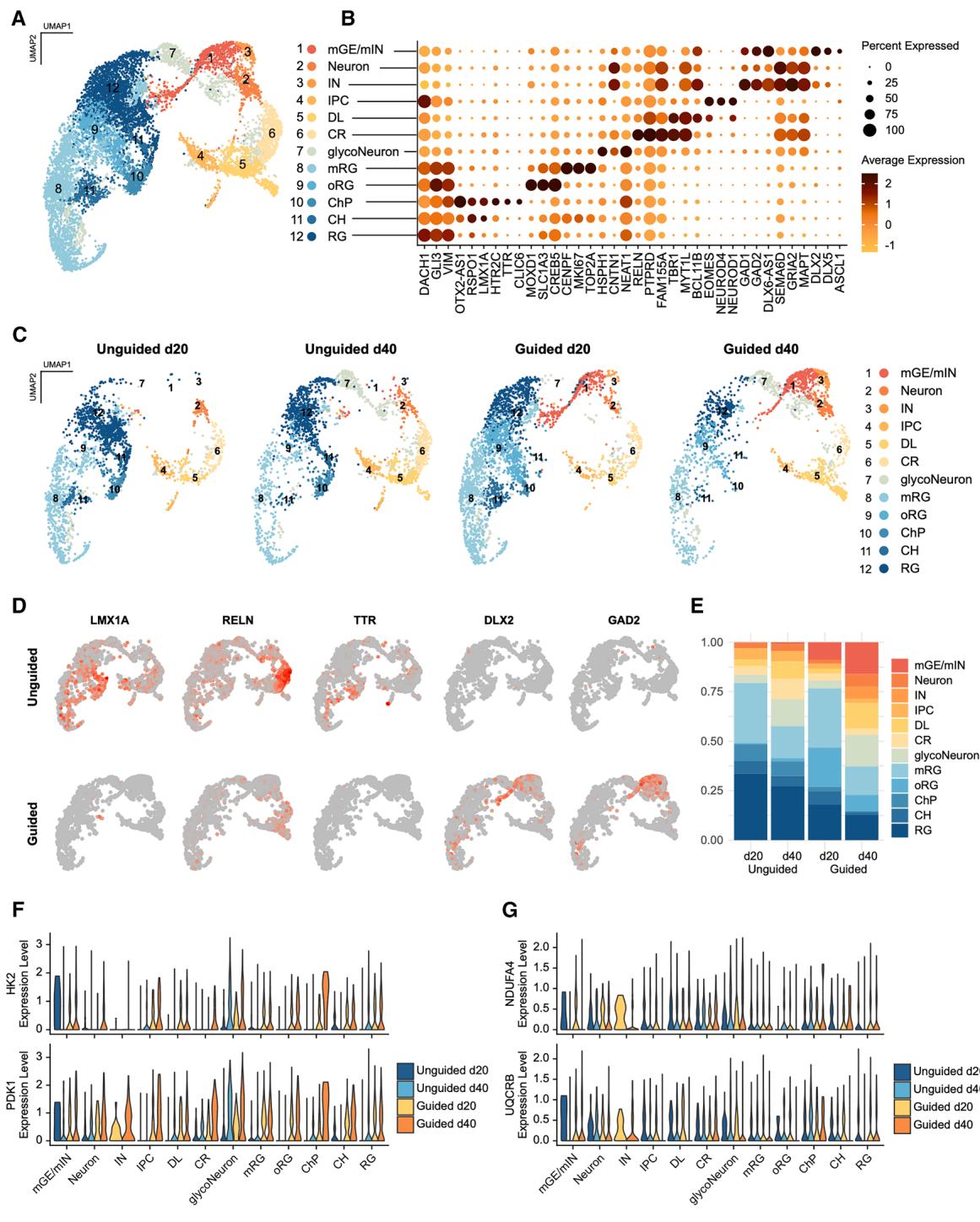
图6. 单细胞RNA测序(scRNA-seq)揭示引导性与非引导性FOs在细胞组成和糖酵解标志物表达上的差异(A)第20天和第40天引导性FOs的单细胞RNA测序(scRNA-seq)数据的均匀流形逼近与投影(UMAP)分析(每个时间点来自一次分化的3个FOs),识别出12个集群:CR,Cajal-Retzius细胞;RG,放射状胶质细胞;oRG,外侧放射状胶质细胞;mRG,有丝分裂放射状胶质细胞;CH,皮质 hem;ChP,脉络丛;DL,深层神经元;IPCs,中间前体细胞;INs,中间神经元;mGE/mIN,内侧神经节隆起/迁移性中间神经元。(B)每个集群关键标志物的表达,颜色表示平均表达水平,点的大小表示表达该标志物的细胞百分比。(C)基于细胞来源划分的UMAP:非引导性或引导性,第20天和第40天。(D)特征图显示第40天FOs中皮质hem标志物(LMX1A)、Cajal-Retzius细胞标志物(RELN)、脉络丛标志物(TTR)以及中间神经元标志物(DLX2、GAD2)的表达水平。
¶ 精神分裂症(SCZ)患者和健康对照(CTLs)的引导性和非引导性FO中不同的蛋白质组疾病特征
我们分别对引导性和非引导性FOs的数据进行了分析,比较了精神分裂症(SCZ)与年龄匹配的对照组(CTLs)之间的蛋白质组差异。在进行多重检验校正后,没有蛋白质的q值≤0.05,这凸显了未来研究中需要更大规模的患者和对照组队列。然而,当采用±0.3的折叠变化阈值和p值≤0.05时,在引导性和非引导性FOs中,分别有84种和104种蛋白质在SCZ与CTLs之间存在丰度差异(图7J-7M;表S5C和S5D)。其中5种蛋白质(PLXNB1、MTERF3、NFX1、LYRM2和KLHL22)在引导性和非引导性FOs中均有重叠,且在SCZ FOs中均表现为丰度降低。基因本体(GO)术语富集分析显示,两种类型的SCZ FOs中受影响的通路不同:在引导性FOs中,基于MAP3K7、DVL3和GBE1,“JUN激酶活性的正向调控”通路被富集(图7J和7L)。在非引导性FOs中,基于SARS2、LARS1和EPRS1,“蛋白质翻译的tRNA氨酰化”通路被富集,且这些蛋白质在SCZ中的丰度均更高(图7K和7M)。在SCZ引导性FOs中,还观察到糖鞘脂相关蛋白质(GALC、IDUA和ARSA)的显著减少(图7J)。综上所述,这表明在比较SCZ和CTL FOs时,所选的类器官系统会对结果产生重大影响。
¶ 讨论
本研究比较了两种广泛使用的有引导和无引导FO方案,为它们在神经学研究中的应用提供参考。两种方案均从相同的诱导多能干细胞批次同步生成,并通过多组学技术对其形态、细胞组成和代谢进行了分析。
未受引导的类器官(FOs)在批次内和批次间的变异性高于受引导的类器官,尽管起始的诱导多能干细胞(iPSCs)数量更少,但到第40天时,其尺寸显著更大。这可能是由于神经元分化速度较慢以及采用了搅拌培养,从而增加了营养物质的流动。作为佐证,在搅拌条件下培养的受引导类器官尺寸显著增大,使得两种类型的类器官尺寸相近。
受引导的类胎儿器官(FOs)在神经元和突触蛋白以及神经递质方面表现出持续增加,尽管在突触数量或电活动方面没有明显的晚期差异。受引导的类胎儿器官中中间神经元的存在如何影响整体活动水平尚不清楚。41 相比之下,未受引导的类胎儿器官含有更多的放射状胶质细胞(RG)、神经胶质祖细胞和星形胶质细胞标志物,这与较低的FOXG1水平和较高的脉络丛样内容物一致。3 8 在未受引导的类胎儿器官中,第80天观察到GFAP+细胞中FOXG1的胞质易位,表明放射状胶质祖细胞分化为星形胶质细胞,32 这可能是由脉络丛(ChP)的FGF2信号驱动的。42,43
单细胞RNA测序显示神经元细胞类型组成存在显著差异,其中无引导的类卵泡(FOs)包含极少的中间神经元。这与先前的研究一致,即无引导的类卵泡在分化后期才会产生中间神经元及其前体。1,12,13 然而,对独立分化样本进行的蛋白质组学分析发现,两种类型的类卵泡中均有GAD1和GAD2的表达,这表明不同分化过程中中间神经元的贡献存在差异。有引导的类卵泡中中间神经元的发育表明存在一定程度的腹侧化;不过,在其他使用有引导的背侧模式类器官的研究中也观察到了这一现象。12,44 此外,研究表明,表达包括DLX亚型在内的腹侧标志物的中间神经元可由背侧脑室区/脑室下区发育而来。45
两种FO类型都与GW9胎儿额叶组织有很好的相关性,不过细胞外基质蛋白含量较低,尤其是在引导性FO中,这可能是由于早期分化过程中未引导性FO嵌入基质胶所致。
出乎意料的是,尽管受引导的类卵泡(FOs)中神经元分化增强,但未受引导的类卵泡却表现出线粒体含量增加和氧化磷酸化(OXPHOS)活性增强。神经元分化通常涉及从糖酵解到氧化磷酸化的代谢转变,并伴随着线粒体质量的增加。47,48 这一过程受PGC-1α和TFAM等转录因子的调控,这些转录因子也会促进溶酶体的生物合成,34,35,49 这或许可以解释未受引导的类卵泡中溶酶体丰度随之增加的原因。此外,已知脉络丛(ChP)细胞具有高线粒体活性,其数量的增加可能进一步解释了未受引导的类卵泡中线粒体含量较高的现象。50
此外,在无引导的类卵泡(FOs)中,视网膜神经节细胞(RG)以及可能的星形胶质细胞谱系所占比例较大,这也可能导致观察到的代谢差异。星形胶质细胞的线粒体富含脂肪酸氧化(FAO)酶,能有效代谢长链脂肪酸。51,52 此外,研究还表明,脂肪酸氧化(FAO)是神经干细胞自我更新的关键。53,54
受引导的类器官(FOs)表现出更高的糖酵解和磷酸戊糖途径(PPP)活性,这与其神经元和突触蛋白表达增加的情况一致。有氧糖酵解和磷酸戊糖途径为突触和神经突的形成提供生物合成支持,并通过产生还原型烟酰胺腺嘌呤二核苷酸磷酸(NADPH)维持谷胱甘肽的还原水平。34,55 受引导的类器官中几种糖酵解蛋白的增加也受缺氧调控,包括单羧酸转运蛋白4(MCT4)、己糖激酶2(HK2)和丙酮酸脱氢酶激酶1(PDK1)。37,56,57 然而,缺氧标志物如缺氧诱导因子1α(HIF1α)在未受引导的类器官中含量更高,这可能是由于它们体积更大,且线粒体活性升高导致氧需求增加。58 有趣的是,缺氧可促进星形胶质细胞分化,这进一步支持了未受引导的类器官中神经胶质含量增加的现象。59
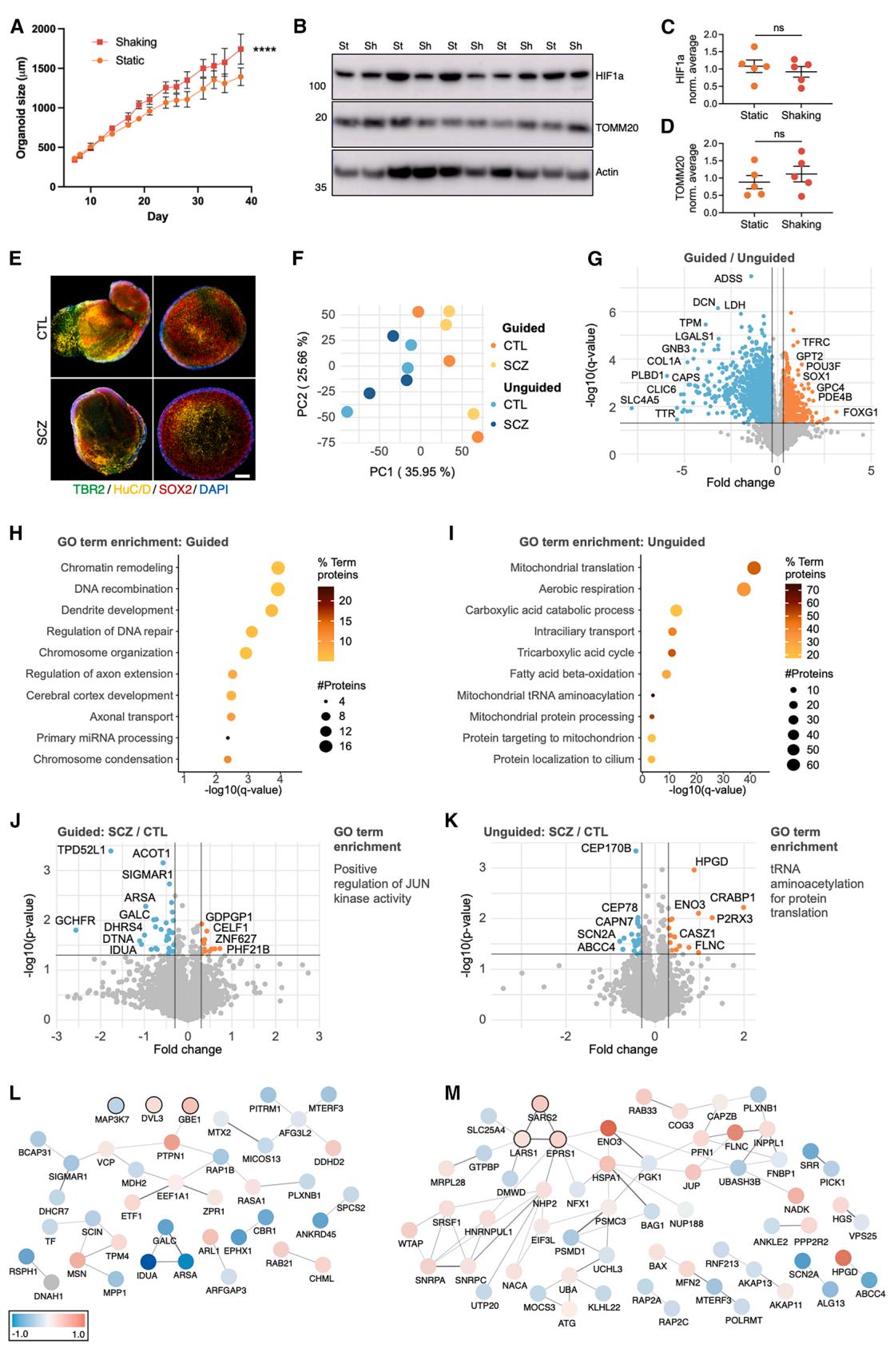
图7. 精神分裂症患者和健康对照者的引导性和非引导性FO显示出不同的蛋白质组疾病特征
(A)在静态或振荡条件下培养的引导类卵泡(FOs)的大小。平均值±标准误,****p≤0.0001(每个时间点3-11个FOs,来自两次分化实验,双因素方差分析)。
(B-D)第40天在静态(st)或振荡(sh)条件下培养的引导性卵泡(FOs)中(B和C)HIF1以及(B和D)TOMM20水平的代表性蛋白质印迹图和定量分析。蛋白质表达以β-肌动蛋白为内参进行标准化,并取每个印迹中所有样本的平均值。均值±标准误(n=5,来自一次分化的卵泡,Student t检验)。
(E) 第20天具有代表性的诱导性皮质类器官(ICC),展示了来自精神分裂症(SCZ)和对照组(CTLs)的有引导和无引导的神经纤维束(FOs),标记物包括4’,6-二脒基-2-苯基吲哚(DAPI,深蓝色)、SRY盒蛋白2(SOX2,红色)、T盒脑蛋白2(TBR2,绿色)和HuC/D(黄色)。比例尺,250微米。
(F)第40天通过蛋白质组学定量的蛋白质的主成分分析(PCA),用于有引导和无引导的FOs(n=6个FOs,结合精神分裂症/对照组,来自一次分化)。
(G) 火山图显示了通过蛋白质组学比较第40天引导性与非引导性FO的蛋白质倍数变化和−log10(q值)(n=6个FO,结合精神分裂症/对照组,q≤0.05且倍数变化±0.3被视为显著,采用秩乘积检验)。
(H和I)对引导性与非引导性FOs(n = 6个FOs,合并SCZ/CTLs)中显著(H)增加和(I)减少的蛋白质(q ≤ 0.05,倍数变化±0.3)进行GO术语富集分析,点的大小表示显著蛋白质的数量,颜色表示其在通路蛋白质总数中的百分比
(双侧超几何检验,采用Bonferroni逐步降阶法)。
(J和K)火山图显示了精神分裂症(SCZ)与对照组(CTL)比较的蛋白质倍数变化和- log10(p值),其中(J)为引导的类器官(FOs),(K)为未引导的类器官(FOs)(n=3个类器官,p≤0.05且倍数变化±0.3被视为显著,采用秩乘积检验)及其基因本体(GO)术语富集情况。
(L和M)(L)引导和(M)非引导的精神分裂症(SCZ)与对照组(CTL)的折叠蛋白(FOs)中重要蛋白质的字符串网络,颜色表示倍数变化。带有黑色轮廓的蛋白质属于富集的基因本体(GO)术语。(L)MAP3K7和DVL3已手动添加到该网络中。
另请参见图S4和S5;表S5。
两种FO类型中均存在的糖基神经元似乎直接起源于放射状胶质细胞,类似于直接神经发生。它们是否更易受缺氧诱导的应激影响,或者是否代表神经祖细胞的过早分化,目前尚不清楚。24,60
对精神分裂症(SCZ)和对照组(CTL)类卵泡的蛋白质组学分析证实,无论是否在搅拌条件下培养,受引导和不受引导的类卵泡之间在神经元和代谢方面存在一致差异,并显示出相似的个体间类器官变异性。然而,我们早期的数据表明,不受引导的类卵泡具有更高的批次间变异性,这可能会影响其在疾病建模中的可靠性。
FO模型的选择应取决于研究重点。FO方案的加速成熟和整体变异性较低,是其在疾病建模方面的明显优势。然而,如果更快的发育是以星形胶质细胞谱系含量为代价,那么非引导性FOs较慢的发育速度可能会揭示出重要的疾病相关特征,否则这些特征可能会被遗漏。从目前的比较来看,非引导性FOs可能更适合研究神经胶质发育、星形胶质细胞与神经元的相互作用、细胞外基质功能,或许还有能量代谢;而引导性FOs则更适合需要增强神经元和突触含量以及稳定中间神经元贡献的应用场景。将这些模型应用于精神分裂症(SCZ)患者的诱导多能干细胞(iPSC)系时,这些差异便显现出来,蛋白质组学分析揭示了不同类型FOs之间存在明显的疾病相关扰动。引导性SCZ FOs显示出JUN激酶相关通路的变化,该通路已被证实与SCZ有关。61相比之下,非引导性SCZ FOs突出了转运RNA氨酰化过程中的扰动,这是另一条与神经精神疾病相关的通路。62引导性SCZ FOs中糖鞘脂相关蛋白的减少也值得关注,因为有证据表明SCZ患者的死后脑组织中鞘脂代谢存在异常。63,64在引导性和非引导性SCZ FOs中均低表达的五种蛋白质中,只有PLXNB1先前被证实与SCZ有关。61值得注意的是,线粒体功能调节因子MTERF3和LYRM265–67也在共同的差异表达蛋白之列。鉴于线粒体功能障碍与SCZ之间存在密切联系68,69,这些蛋白质是未来研究的相关靶点。
总之,本研究对有引导和无引导的FO协议进行了全面比较,强调了在神经元分化、细胞组成和代谢活性方面的显著差异。这些差异可能会影响疾病建模结果,凸显了为特定研究目标选择合适的FO模型的重要性。通过提供详细的资源,本研究有助于优化FO在利用患者来源的诱导多能干细胞(iPSCs)建模神经系统疾病中的应用。
¶ 研究的局限性
目前的结果不能直接外推到其他有引导/无引导的FO方案,部分原因是STEMCELL Technologies未公开培养基的成分。
在精神分裂症(SCZ)和对照组(CTL)的成纤维细胞(FOs)比较中,生物学重复样本数量仅为3个,这限制了统计效力。本文报告了名义p值,需要在更大的队列中重现这些发现和/或通过正交方法进行验证,以推断疾病生物学机制。
¶ 资源可用性
¶ 主要联系人
如需更多信息、资源和试剂,请联系主要联系人Helle Bogetofte(hbogetofte@bmb.sdu.dk),相关需求将由其处理。
¶ 材料可用性
IMR90诱导多能干细胞系可从WiCell公司商购获得。由于与项目相关的伦理规定,本研究中生成的对照组和精神分裂症患者诱导多能干细胞系的获取存在限制。
¶ 数据和代码可用性
• 质谱蛋白质组学数据已通过PRIDE合作存储库存入ProteomeXchange联盟(数据集标识符PRIDE:PXD048559)。单细胞RNA测序数据已存入美国国家生物技术信息中心的基因表达综合数据库(登录号:GEO:GSE253889)。数据自发表之日起公开可用。
• 本研究未报告原始代码。
• 任何重现分析本文所报告数据所需的额外信息,均可应要求从主要联系人处获取。
¶ 致谢
本研究得到了伦德贝克基金会( grant编号:R336+2020-1113和R380-2021-1425)、PLATO研究基础设施(丹麦国家蛋白质组学和生物分子成像质谱平台,grant编号:5229-00012B,www.sdu.dk/PLATO)以及南丹麦大学维勒姆生物分析科学中心的支持。图像采集工作在丹麦分子生物医学成像中心(DaMBIC,南丹麦大学)完成,该中心得到了诺和诺德基金会的支持(资助协议编号:NNF18SA0032928)。
图形摘要由BioRender制作。Bogetofte, H.(2025)https://BioRender.com/3cjc4ja。
¶ 作者贡献
概念构思:M.S.O.、P.J.、M.A.L.、M.R.L.和H.B.;数据整理:M.S.O.、J.F.H.、S.W.W.和H.B.;形式分析:M.S.O.、P.J.、J.F.H.、S.I.S.、F.A.M.、M.S.、S.W.W.、I.C.和H.B.;资金获取:J.B.、M.E.B.、K.F.、N.J.F.、M.A.L.、M.R.L.和H.B.;研究调查:M.S.O.、P.J.、J.F.H.、S.I.S.、F.A.M.、M.S.、S.B.E.、L.C.、E.B.、J.A.A.N.、L.A.J.和H.B.;方法设计:M.S.O.、P.J.、M.A.L.、M.R.L.和H.B.;项目管理:P.J.、M.R.L.和H.B.;资源提供:J.B.、M.E.B.、K.F.、N.J.F.、M.A.L.、M.R.L.和H.B.;验证:M.S.O.、P.J.、S.I.S.、F.A.M.、E.B.、L.A.J.、J.B.、M.E.B.、K.F.、N.J.F.、M.A.L.、M.R.L.和H.B.;可视化:M.S.O.、S.I.S.、F.A.M.和H.B.;初稿撰写:M.S.O.、F.A.M.和H.B.;审阅与编辑:M.S.O.、P.J.、M.A.L.、M.R.L.和H.B.。所有合著者均认可最终版本。
¶ 利益声明
作者声明不存在利益冲突。
¶ STAR★方法
详细方法见本文的在线版本,包括以下内容:
• 关键资源表
实验模型和研究参与者详情
○ 诱导多能干细胞的维持
○ 精神分裂症患者与健康对照者
• 方法详情
○ 外周血单个核细胞分离
○ 游离型重编程
○ 人类诱导多能干细胞系分化潜能检查
○ 拷贝数变异
○ 前脑类器官(FO)分化
○ 免疫细胞化学与成像
○ 蛋白质裂解与消化
○ 用于蛋白质组学分析的TMT标记
○ 磷酸化和糖肽的富集
○ 高pH分馏
○ 纳米液相色谱-质谱联用
○ 蛋白质鉴定和定量
○ 脂质和代谢物提取
○ 代谢组学和脂质组学分析
○ 蛋白质印迹法
○ 多电极阵列(MEA)分析
○ LDH和ROS的功能测定
○ Seahorse分析
○ 单细胞RNA测序(scRNAseq)
○ 胎儿额叶蛋白质组学比较
• 量化和统计分析 ○ 图像和WB量化 ○ 统计分析
¶ 补充信息
补充信息可在网上查阅:https://doi.org/10.1016/j.
crmeth.2025.101295.
收到日期:2025年1月21日
修订日期:2025年3月14日
接受时间:2025年12月12日
¶ 参考文献
-
Camp, J.G., Badsha, F., Florio, M., Kanton, S., Gerber, T., WilschBräuninger, M., Lewitus, E., Sykes, A., Hevers, W., Lancaster, M.等(2015)。人类大脑类器官重现胎儿新皮质发育的基因表达程序。《美国国家科学院院刊》112,15672–15677。https://doi.org/10.1073/pnas.1520760112。
-
兰开斯特(M.A.)、科尔西尼(N.S.)、沃尔芬格(S.)、古斯塔夫森(E.H.)、菲利普斯(A.W.)、伯卡德(T.R.)、大谷(T.)、利夫西(F.J.)和克诺布利希(J.A.)(2017年)。人脑类器官中的引导式自组织和皮质板形成。《自然·生物技术》,35卷,659-666页。https://doi.org/10.1038/nbt.3906。
-
戈登(A.)、尹(S.-J.)、陈(S.S.)、梅金森(C.D.)、朴(J.Y.)、安德森(J.)、巴伦西亚(A.M.)、霍瓦特(S.)、肖(X.)、休格纳德(J.R.)等(2021)。人类皮质类器官的长期成熟与出生后早期的关键转变相匹配。《自然·神经科学》,24,331-342。https://doi.org/10.1038/s41593-021-00802-y。
-
Mariani, J., Coppola, G., Zhang, P., Abyzov, A., Provini, L., Tomasini, L., Amenduni, M., Szekely, A., Palejev, D., Wilson, M. 等(2015)。FOXG1依赖的自闭症谱系障碍中GABA/谷氨酸神经元分化失调。《细胞》162,375–390。https://doi.org/10.1016/j.cell.2015.06.034。
-
李(C. Li)、弗莱克(J.S. Fleck)、马丁斯-科斯塔(C. Martins-Costa)、伯卡德(T.R. Burkard)、塞曼(J. Themann)、施滕普夫伦(M. Stuempflen)、皮尔(A.M. Peer)、韦尔泰希(A. Vertesy)、利特尔博伊(J.B. Littleboy)、埃斯克(C. Esk)等(2023)。单细胞脑类器官筛选识别出自闭症的发育缺陷。《自然》621,373-380。https://doi.org/10.1038/s41586-023-06473-y。
-
Kathuria, A., Lopez-Lengowski, K., Jagtap, S.S., McPhie, D., Perlis, R.H., Cohen, B.M., 以及 Karmacharya, R.(2020年)。精神分裂症中诱导多能干细胞衍生的脑类器官的转录组学景观和功能特征。《美国医学会精神病学杂志》77,745-754。https://doi.org/10.1001/jamapsychiatry.2020.0196。
-
兰开斯特(M.A.)、伦纳(M.)、马丁(C.-A.)、温泽尔(D.)、比克内尔(L.S.)、赫尔斯(M.E.)、霍姆弗雷(T.)、彭宁格(J.M.)、杰克逊(A.P.)和克诺布利希(J.A.)(2013年)。大脑类器官模拟人类大脑发育和小头畸形。《自然》501,373-379。https://doi.org/10.1038/nature12517。
-
崔(S.H.)、金(Y.H.)、赫比施(M.)、斯利温斯基(C.)、李(S.)、达万佐(C.)、陈(H.)、胡利(B.)、阿瑟林(C.)、穆法特(J.)等人(2014年)。阿尔茨海默病的三维人类神经细胞培养模型。《自然》515,274-278。https://doi.org/10.1038/nature13800。
-
赵静、傅颖、山崎洋、任宇、戴维斯(M.D.)、刘聪聪、卢伟、王旭、陈凯、切鲁库里(Y.)等(2020)。APOE4加剧阿尔茨海默病患者诱导多能干细胞衍生脑类器官中的突触丢失和神经变性。《自然·通讯》,11,5540。https://doi.org/10.1038/s41467-020-19264-0。
-
Wulansari, N., Darsono, W.H.W., Woo, H.-J., Chang, M.-Y., Kim, J., Bae, E.-J., Sun, W., Lee, J.-H., Cho, I.-J., Shin, H. 等(2021)。携带帕金森病相关DNAJC6突变的人脑类器官中的神经发育缺陷和神经退行性表型。《科学进展》,7,eabb1540。https://doi.org/10.1126/sciadv.abb1540。
-
钱旭等人(2016)。使用微型生物反应器构建特定脑区类器官以模拟寨卡病毒暴露。《细胞》,165,1238-1254。https://doi.org/10.1016/j.cell.2016.04.032。
-
Velasco, S., Kedaigle, A.J., Simmons, S.K., Nash, A., Rocha, M., Quadrato, G., Paulsen, B., Nguyen, L., Adiconis, X., Regev, A.等(2019)。单个脑类器官可重复形成人类大脑皮层的细胞多样性。《自然》570,523-527。https://doi.org/10.1038/s41586-019-1289-x。
-
Giandomenico, S.L., Mierau, S.B., Gibbons, G.M., Wenger, L.M.D., Masullo, L., Sit, T., Sutcliffe, M., Boulanger, J., Tripodi, M., Derivery, E., 等. (2019). 气液界面处的脑类器官可生成具有功能输出的多种神经束。《自然·神经科学》,22,669-679。https://doi.org/10.1038/s41593-019-0350-2。
-
伦纳(M.)、兰卡斯特(M.A.)、卞(S.)、崔(H.)、库(T.)、皮尔(A.)、钟(K.)和克诺布利希(J.A.)(2017年)。脑类器官中的自组织发育模式和分化。《欧洲分子生物学学会杂志》,36卷,1316-1329页。https://doi.org/10.15252/embj.201694700。
-
Quadrato, G., Nguyen, T., Macosko, E.Z., Sherwood, J.L., Min Yang, S., Berger, D.R., Maria, N., Scholvin, J., Goldman, M., Kinney, J.P. 等人(2017年)。光敏性人类脑类器官中的细胞多样性和网络动态。《自然》545,48-53。https://doi.org/10.1038/nature22047。
-
Giandomenico, S.L.、Sutcliffe, M. 和 Lancaster, M.A.(2021)。用于研究神经发育后期阶段的高级脑类器官的生成和长期培养。《自然·实验手册》,16,579-602。https://doi.org/10.1038/s41596-020-00433-w。
-
门岛(T. Kadoshima)、坂口(H. Sakaguchi)、中野(T. Nakano)、曾根(M. Soen)、安藤(S. Ando)、平陆(M. Eiraku)和笹井(Y. Sasai)(2013年)。人胚胎干细胞衍生的新皮质中轴向极性、内外层模式及物种特异性祖细胞动态的自组织。《美国国家科学院院刊》110,20284-20289。https://doi.org/10.1073/pnas.1315710110。
-
Pașca, A.M., Sloan, S.A., Clarke, L.E., Tian, Y., Makinson, C.D., Huber, N., Kim, C.H., Park, J.-Y., O’Rourke, N.A., Nguyen, K.D.等人(2015年)。3D培养中来自人多能干细胞的功能性皮质神经元和星形胶质细胞。《自然方法》12,671-678。https://doi.org/10.1038/nmeth.3415。
-
Birey, F., Andersen, J., Makinson, C.D., Islam, S., Wei, W., Huber, N., Fan, H.C., Metzler, K.R.C., Panagiotakos, G., Thom, N., 等. (2017). 功能整合的人类前脑类球体的组装。《自然》545, 54–59。https://doi.org/10.1038/nature22330。
-
斯隆(S.A.)、安德森(J.)、帕斯卡(A.M.)、比雷(F.)和帕斯卡(S.P.)(2018年)。《人类大脑区域特异性三维培养物的生成与组装》。《自然·实验手册》13,2062-2085。https://doi.org/10.1038/s41596-018-0032-7。
-
Jo, J., Xiao, Y., Sun, A.X., Cukuroglu, E., Tran, H.-D., Göke, J., Tan, Z.Y., Saw, T.Y., Tan, C.-P., Lokman, H.等(2016年)。来自人多能干细胞的中脑样类器官含有功能性多巴胺能神经元和产生神经黑色素的神经元。《细胞干细胞》19,248-257。https://doi.org/10.1016/j.stem.2016.07.005。
-
Muguruma, K.、Nishiyama, A.、Kawakami, H.、Hashimoto, K.和Sasai, Y.(2015)。人多能干细胞的3D培养中极化小脑组织的自组织。《细胞报告》,10,537-550。https://doi.org/10.1016/j.celrep.2014.12.051。
-
Uzquiano, A., Kedaigle, A.J., Pigoni, M., Paulsen, B., Adiconis, X., Kim, K., Faits, T., Nagaraja, S., Antón-Bolaños, N., Gerhardinger, C. 等人(2022年)。类器官中细胞类别特性的正确获得能够明确人类大脑皮层的命运特化程序。《细胞》185,3770–3788.e27。https://doi.org/10.1016/j.cell.2022.09.010。资源。
-
巴杜里(A. Bhaduri)、安德鲁斯(M.G. Andrews)、曼西亚·莱昂(W. Mancia Leon)、荣格(D. Jung)、申(D. Shin)、艾伦(D. Allen)、荣格(D. Jung)、施蒙克(G. Schmunk)、豪斯勒(M. Haeussler)、萨尔玛(J. Salma)等人(2020年)。皮质类器官中的细胞应激会损害分子亚型的特化。《自然》,578卷,142-148页。https://doi.org/10.1038/s41586-020-1962-0。
-
Chiaradia, I., Imaz-Rosshandler, I., Nilges, B.S., Boulanger, J., Pellegrini, L., Das, R., Kashikar, N.D., 以及 Lancaster, M.A. (2023). 组织形态影响人类脑类器官发育的时间程序。《细胞干细胞》30, 1351–1367.e10。https://doi.org/10.1016/j.stem.2023.09.003。
-
Moore, S.A.和Iulianella, A.(2021)。哺乳动物皮质缘及其衍生物的发育:脉络丛、Cajal-Retzius细胞和海马体。《Open Biol》,11卷,210042页。https://doi.org/10.1098/rsob.210042。
-
侯,P.-S.、hAilín,D.Ó.、沃格尔,T.和花岛,C.(2020年)。转录及其他:阐明FOXG1在皮质发育和疾病中的功能。《细胞神经科学前沿》,14卷,35页。https://doi.org/10.3389/fncel.2020.00035。
-
康(Kang)、延森(Jensen)、黄(Huang)、隆德·克里斯滕森(Lund Christensen)、比勒斯特鲁普(Billestrup)和拉森(Larsen)(2018年)。利用翻译后修饰特异性蛋白质组学(PTM组学)表征分离的胰腺β细胞中葡萄糖刺激胰岛素分泌的分子机制。《分子与细胞蛋白质组学》17,95-110。https://doi.org/10.1074/mcp.RA117.000217。
-
费多罗娃(I.)、桥本(A.)、费西克(R.A.)、赫德里克(M.P.)、哈努斯(L.O.)、博格(D.L.)、赖斯(K.C.)和巴西勒(A.S.)(2001年)。油酰胺与多种神经递质系统相互作用的行为学证据。《药理学与实验治疗学杂志》,299期,332-342页。
-
Roy, A.、Kundu, M.、Chakrabarti, S.、Patel, D.R. 和 Pahan, K.(2021)。油酰胺,一种诱导睡眠的补充剂,通过PPARα上调海马祖细胞中的双皮质素。《阿尔茨海默病杂志》,84卷,1747-1762页。https://doi.org/10.3233/JAD-215124。
-
Fitzner, D.、Bader, J.M.、Penkert, H.、Bergner, C.G.、Su, M.、Weil, M.-T.、Surma, M.A.、Mann, M.、Klose, C.和Simons, M.(2020)。细胞类型和脑区分辨的小鼠脑脂质组。《细胞报告》,32,108132。https://doi.org/10.1016/j.celrep.2020.108132。
-
Regad, T., Roth, M., Bredenkamp, N., Illing, N., 和 Papalopulu, N. (2007). FoxG1的神经祖细胞特异性活性受到CKI和FGF的拮抗调节。《自然·细胞生物学》9, 531-540。https://doi.org/10.1038/ncb1573。
-
Jogl, G.、Hsiao, Y.-S.和Tong, L.(2004)。肉碱酰基转移酶的结构与功能。《纽约科学院年鉴》,1033,17-29。https://doi.org/10.1196/annals.1320.002。
-
Agostini, M., Romeo, F., Inoue, S., Niklison-Chirou, M.V., Elia, A.J., Dinsdale, D., Morone, N., Knight, R.A., Mak, T.W., 和 Melino, G.(2016)。神经元分化过程中的代谢重编程。《细胞死亡与分化》,23,1502-1514。https://doi.org/10.1038/cdd.2016.36。
-
Fame, R.M.、Shannon, M.L.、Chau, K.F.、Head, J.P. 和 Lehtinen, M.K.(2019)。早期前脑的协同代谢转变改变脑脊液蛋白质组,并依赖MYC下调实现线粒体成熟。《发育(剑桥,英国)》,146卷,dev182857。https://doi.org/10.1242/dev.182857。
-
Helenius, A. 和 Aebi, M.(2001)。N-连接聚糖的细胞内功能。《科学》291,2364-2369。
-
布里克斯(Brix)、梅斯特斯(Mesters)、佩勒林(Pellerin)和约伦(Jöhren)(2012年)。内皮细胞衍生的一氧化氮通过HIF1α介导的靶基因激活增强星形胶质细胞的有氧糖酵解。《神经科学杂志》(J. Neurosci.),32卷,9727-9735页。https://doi.org/10.1523/JNEUROSCI.0879-12.2012。
-
Subramanian, L.、Remedios, R.、Shetty, A. 和 Tole, S.(2009)。边缘信号:端脑发育中的皮质hem和antihem。《细胞与发育生物学综述》,20,712-718。https://doi.org/10.1016/j.semcdb.2009.04.001。
-
Martynoga, B.、Morrison, H.、Price, D.J. 和 Mason, J.O.(2005)。Foxg1 是腹侧端脑特化以及背侧端脑前体增殖和凋亡区域特异性调控所必需的。《发育生物学》,283,113-127。https://doi.org/10.1016/j.ydbio.2005.04.005。
-
赵鑫、梁伟、王伟、刘辉、张鑫、刘超、朱聪、崔博、唐颖和刘松(2022年)。人类胎儿额叶蛋白质组在早期发育过程中的变化及不对称性。《通讯生物学》,5卷,1031页。https://doi.org/10.1038/s42003-022-04003-6。
-
艾萨克森(Isaacson)、J.S.和斯坎齐亚尼(Scanziani)、M.(2011)。抑制如何塑造皮层活动。《神经元》(Neuron)72,231-243。https://doi.org/10.1016/j.neuron.2011.09.027。
-
钱晓(Qian, X.)、戴维斯(Davis, A.A.)、戈德里(Goderie, S.K.)和坦普尔(Temple, S.)(1997)。FGF2浓度调节多能皮质干细胞生成神经元和神经胶质细胞。《神经元》(Neuron)18,81-93。https://doi.org/10.1016/s0896-6273(01)80048-9。
-
格林伍德(S.)、斯韦特洛夫(A.)、韦德(A.M.)、寺崎(T.)和费雷蒂(P.)(2008年)。成纤维细胞生长因子2在人类和小鼠胚胎脉络丛中表达,并影响脉络丛上皮细胞行为。《脑脊液研究》,5卷,20页。https://doi.org/10.1186/1743-8454-5-20。
-
Yoon, S.-J., Elahi, L.S., Pașca, A.M., Marton, R.M., Gordon, A., Revah, O., Miura, Y., Walczak, E.M., Holdgate, G.M., Fan, H.C.等(2019)。人类皮质类器官生成的可靠性。《自然·方法》16,75-78。https://doi.org/10.1038/s41592-018-0255-0。
-
Yu, X.和Zecevic, N.(2011)。人类大脑中背侧放射状胶质细胞具有生成皮质中间神经元的潜力,而小鼠大脑中则没有。《神经科学杂志》,31,2413-2420。https://doi.org/10.1523/JNEUROSCI.5249-10.2011。
-
Jain, A., Gut, G., Sanchis-Calleja, F., Okamoto, R., Streib, S., He, Z., Zenk, F., Santel, M., Seimiya, M., Holtackers, R. 等人(2023年)。人类早期脑类器官发育的形态动力学。预印本于bioRxiv。https://doi.org/10.1101/2023.08.21.553827。
-
郑晓、博耶(L.)、金敏、默滕斯(J.)、金勇、马丽、马丽、哈姆(M.)、盖奇(F.H.)和亨特(T.)(2016)。神经元分化过程中从有氧糖酵解到神经元氧化磷酸化的代谢重编程。《eLife》5,e13374。https://doi.org/10.7554/eLife.13374。
-
Beckervordersandforth, R., Ebert, B., Schäffner, I., Moss, J., Fiebig, C., Shin, J., Moore, D.L., Ghosh, L., Trinchero, M.F., Stockburger, C. 等人(2017年)。线粒体代谢在成体海马神经发生中早期谱系进展和衰老表型调控中的作用。《神经元》93,560-573.e6。https://doi.org/10.1016/j.neuron.2016.12.017。
-
Deus, C.M., Yambire, K.F., Oliveira, P.J., 和 Raimundo, N.(2020)。线粒体-溶酶体串扰:从生理学到神经退行性疾病。《分子医学趋势》,26,71-88。https://doi.org/10.1016/j.molmed.2019.10.009。
-
康福德(E.M.)、瓦雷西(J.B.)、海曼(S.)、达米安(R.T.)和罗利(M.J.)(1997年)。脉络丛上皮细胞的线粒体含量。《实验脑研究》,116期,399-405页。https://doi.org/10.1007/pl00005768。
-
Eraso-Pichot, A.、Brasó-Vives, M.、Golbano, A.、Menacho, C.、Claro, E.、Galea, E. 和 Masgrau, R.(2018)。小鼠和人类线粒体组的GSEA揭示星形胶质细胞中的脂肪酸氧化。《神经胶质》66,1724-1735。https://doi.org/10.1002/glia.23330。
-
Fecher, C., Trovò, L., Müller, S.A., Snaidero, N., Wettmarshausen, J., Heink, S., Ortiz, O., Wagner, I., Kühn, R., Hartmann, J. 等人(2019年)。脑线粒体的细胞类型特异性分析揭示了功能和分子多样性。《自然·神经科学》,22卷,1731-1742页。https://doi.org/10.1038/s41593-019-0479-z。
-
谢,Z.,琼斯,A.,迪尼,J.T.,赫尔,S.K.,和班凯蒂斯,V.A.(2016)。长链脂肪酸β-氧化先天性缺陷将神经干细胞自我更新与自闭症联系起来。《细胞报告》,14,991-999。https://doi.org/10.1016/j.celrep.2016.01.004。
-
郭楠、麦克德莫特(K.D.)、施(Y.-T.)、赞加(H.)、戈什(D.)、赫伯(C.)、米拉(W.R.)、科尔曼(J.)、扎古拉思(A.)、王(L.P.)等(2022)。成年海马体神经干细胞增殖的转录调控。《eLife》11卷,e72195页。https://doi.org/10.7554/eLife.72195。
-
戈亚尔(M.S.)、霍里利奇(M.)、米勒(J.A.)、斯奈德(A.Z.)和赖希勒(M.E.)(2014年)。人脑有氧糖酵解与发育及幼态持续基因表达相关。《细胞代谢》,19卷,49-57页。https://doi.org/10.1016/j.cmet.2013.11.020。
-
Kim, J.w.、Tchernyshyov, I.、Semenza, G.L.和Dang, C.V.(2006年)。HIF-1介导的丙酮酸脱氢酶激酶表达:细胞适应缺氧所需的代谢转换。《细胞代谢》,3卷,177-185页。https://doi.org/10.1016/j.cmet.2006.02.002。
-
帕潘德里欧(I.)、凯恩斯(R.A.)、丰塔纳(L.)、林(A.L.)和登科(N.C.)(2006年)。HIF-1通过主动下调线粒体氧消耗介导对缺氧的适应。《细胞代谢》,3卷,187-197页。https://doi.org/10.1016/j.cmet.2006.01.012。
-
奥黑根(K.A.)、科基利亚(S.)、日丹诺夫(A.V.)、坦布瓦拉(M.M.)、康明斯(E.P.)、蒙法雷德(M.)、阿格博尔(T.A.)、加维(J.F.)、帕普科夫斯基(D.B.)、泰勒(C.T.)和艾伦(B.B.)(2009年)。PGC-1α通过增加骨骼肌细胞的线粒体耗氧量与HIF-1α依赖性基因表达相关联。《美国国家科学院院刊》,106卷,2188-2193页。https://doi.org/10.1073/pnas.0808801106。
-
安井T.、上薗N.、中岛H.、野口H.、松田T.、野田安藤T.、冈野H.和中岛K.(2017年)。缺氧通过表观遗传方式赋予人多能细胞衍生的神经前体细胞星形胶质细胞分化潜能。《干细胞报告》,8卷,1743-1756页。https://doi.org/10.1016/j.stemcr.2017.05.001。
-
Pașca, A.M.、Park, J.-Y.、Shin, H.-W.、Qi, Q.、Revah, O.、Krasnoff, R.、O’Hara, R.、Willsey, A.J.、Palmer, T.D. 和 Pașca, S.P.(2019年)。早产儿缺氧性脑损伤的人类3D细胞模型。《自然医学》25,784-791。https://doi.org/10.1038/s41591-019-0436-0。
-
麦圭尔(J.L.)、德帕斯奎尔(E.A.)、芬克(A.J.)、奥多诺万(S.M.)、哈塞尔菲尔德(K.)、马瓦哈(S.)、哈蒙德(J.H.)、哈图尼安(V.)、米多尔-伍德拉夫(J.H.)、梅勒(J.)和麦卡勒姆斯密斯(R.E.)(2017年)。慢性精神分裂症中信号转导网络的异常。《NPJ精神分裂症》,3卷,30页。https://doi.org/10.1038/s41537-017-0032-6。
-
Blaze, J. 和 Akbarian, S.(2022)。神经发育和神经精神疾病中的tRNA调控组。《分子精神病学》27,3204-3213。https://doi.org/10.1038/s41380-022-01585-9。
-
Narayan, S.、Head, S.R.、Gilmartin, T.J.、Dean, B. 和 Thomas, E.A.(2009)。精神分裂症中鞘脂代谢紊乱的证据。《神经科学研究杂志》,87,278-288。https://doi.org/10.1002/jnr.21822。
-
卡斯蒂略、R.I.、罗霍、L.E.、亨利克斯-亨利克斯、M.、席尔瓦、H.、马图拉纳、A.、比利亚尔、M.J.、富恩特斯、M.和加斯帕尔、P.A.(2016年)。从分子到临床:通过鞘脂代谢将精神分裂症与代谢综合征联系起来。《神经科学前沿》,10,488。https://doi.org/10.3389/fnins.2016.00488。
-
黄强、陈子、程鹏、蒋志、王子、黄艳、杨超、潘军、邱峰和黄军(2019年)。LYRM2通过氧化磷酸化直接调节复合体I活性以支持结直肠癌肿瘤生长。《癌症快报》,455期,36-47页。https://doi.org/10.1016/j.canlet.2019.04.021。
-
Dibley, M.G., Formosa, L.E., Lyu, B., Reljic, B., McGann, D., MuellnerWong, L., Kraus, F., Sharpe, A.J., Stroud, D.A., 和 Ryan, M.T. (2020). 线粒体酰基载体蛋白相互作用网络凸显LYRM家族成员在复合体I和线粒体核糖体组装中的重要作用。《分子细胞蛋白质组学》19, 65–77。https://doi.org/10.1074/mcp.RA119.001784。
-
Park, C.B., Asin-Cayuela, J., Cámara, Y., Shi, Y., Pellegrini, M., Gaspari, M., Wibom, R., Hultenby, K., Erdjument-Bromage, H., Tempst, P., 等. (2007). MTERF3是哺乳动物线粒体DNA转录的负调控因子。《细胞》130, 273-285。https://doi.org/10.1016/j.cell.2007.05.046。
-
罗伯茨,R.C.(2021)。精神分裂症中的线粒体功能障碍:聚焦死后研究。《线粒体》56,91-101。https://doi.org/10.1016/j.mito.2020.11.009。
-
近藤(M.A.)、诺里斯(A.L.)、杨(K.)、柴郡(M.)、纽柯克(I.)、陈(X.)、石冢(K.)、贾菲(A.E.)、泽(A.)和佩夫斯纳(J.)(2022年)。精神分裂症患者前扣带回皮层中线粒体和γ-氨基丁酸能中间神经元的功能障碍。《神经科学研究》,185卷,67-72页。https://doi.org/10.1016/j.neures.2022.09.011。
-
Heissel, S.、Bunkenborg, J.、Kristiansen, M.P.、Holmbjerg, A.F.、Grimstrup, M.、Mørtz, E.、Kofoed, T. 和 Højrup, P.(2018年)。宿主细胞蛋白质DIA-LC-MS分析中光谱库和样品制备的评估:以细菌表达的重组生物制药蛋白质为例。《蛋白质表达与纯化》,147卷,69-77页。https://doi.org/10.1016/j.pep.2018.03.002。
-
巴雷特(T.)、威尔海特(S.E.)、勒杜(P.)、埃万杰利斯塔(C.)、金(I.F.)、托马舍夫斯基(M.)、马歇尔(K.A.)、菲利皮(K.H.)、谢尔曼(P.M.)、霍尔科(M.)等(2013)。NCBI GEO:功能基因组数据集档案——更新。《核酸研究》,41卷,D991-D995页。https://doi.org/10.1093/nar/gks1193。
-
施密特(S.I.)、博格托夫特(H.)、里特(L.)、阿格加德(J.B.)、哈默里奇(D.)、卡比利亚吉奇(A.A.)、沃达奇克(A.)、洛佩兹(S.G.)、索伦森(M.D.)、约根森(M.L.)等(2021)。小胶质细胞分泌的因子可促进组织和诱导多能干细胞来源的人神经干细胞向多巴胺能细胞分化。《干细胞报告》,16,281-294。https://doi.org/10.1016/j.stemcr.2020.12.011。
-
UniProt联盟(2021年)。UniProt:2021年的通用蛋白质知识库。《核酸研究》49卷,D480-D489页。https://doi.org/10.1093/nar/gkaa1100。
-
Schwämmle, V.、Hagensen, C.E.、Rogowska-Wrzesinska, A. 和 Jensen, O.N.(2020)。PolySTest:带有缺失值的蛋白质组学数据的稳健统计检验提高了生物学相关特征的检测。《分子细胞蛋白质组学》(Mol. Cell. Proteomics MCP)19,1396-1408。https://doi.org/10.1074/mcp.RA119.001777。
-
Doncheva, N.T.、Morris, J.H.、Gorodkin, J. 和 Jensen, L.J.(2019)。Cytoscape StringApp:蛋白质组学数据的网络分析和可视化。《蛋白质组学研究杂志》,18,623-632。https://doi.org/10.1021/acs.jproteome.8b00702。
-
Bindea, G.、Mlecnik, B.、Hackl, H.、Charoentong, P.、Tosolini, M.、Kirilovsky, A.、Fridman, W.-H.、Pagès, F.、Trajanoski, Z. 和 Galon, J.(2009)。ClueGO:一个用于解读功能分组的基因本体论和通路注释网络的Cytoscape插件。《生物信息学》25,1091-1093。https://doi.org/10.1093/bioinformatics/btp101。
-
R核心团队(2021)。R:一种用于统计计算的语言和环境(R统计计算基金会)。https://www.R-project.org。
-
威克姆,H.(2016)。《ggplot2:数据分析的优雅图形》(施普林格出版社)。https://ggplot2.tidyverse.org。
-
Kind, T.、Liu, K.-H.、Lee, D.Y.、DeFelice, B.、Meissen, J.K. 和 Fiehn, O.(2013)。LipidBlast——用于脂质鉴定的计算机串联质谱数据库。《自然方法》10,755-758。https://doi.org/10.1038/nmeth.2551。
-
Ruttkies, C.、Schymanski, E.L.、Wolf, S.、Hollender, J. 和 Neumann, S.(2016)。MetFrag 重新推出:整合硅片碎裂之外的策略。《化学信息学杂志》,8,3。https://doi.org/10.1186/s13321-016-0115-9。
-
Chong, J.、Wishart, D.S.和Xia, J.(2019)。使用MetaboAnalyst 4.0进行全面和综合性代谢组学数据分析。《Current Protocols in Bioinformatics》68,e86。https://doi.org/10.1002/cpbi.86。
-
罗森伯格(A.B.)、罗科(C.M.)、马斯卡特(R.A.)、库奇纳(A.)、桑普尔(P.)、姚(Z.)、格雷巴克(L.T.)、皮勒(D.J.)、穆克吉(S.)、陈(W.)等人(2018年)。利用分裂池条形码技术对发育中的小鼠脑和脊髓进行单细胞分析。《科学》360期,176-182页。https://doi.org/10.1126/science.aam8999。
-
郝宇、郝松、安德森-尼森(E. Andersen-Nissen)、莫克(W.M. Mauck)、郑颂、巴特勒(A. Butler)、李明俊(M.J. Lee)、威尔克(A.J. Wilk)、达比(C. Darby)、扎格尔(M. Zager)等(2021)。多模态单细胞数据的整合分析。《细胞》(Cell),184,3573–3587.e29。https://doi.org/10.1016/j.cell.2021.04.048。
-
Trapnell, C.、Cacchiarelli, D.、Grimsby, J.、Pokharel, P.、Li, S.、Morse, M.、Lennon, N.J.、Livak, K.J.、Mikkelsen, T.S. 和 Rinn, J.L.(2014年)。单细胞的伪时间排序揭示了细胞命运决定的动态变化和调控因子。《自然·生物技术》,32卷,381-386页。https://doi.org/10.1038/nbt.2859。
-
栾华、吉峰、陈阳和蔡志(2018)。statTarget:一种用于基于定量质谱的组学数据信号漂移校正和解释的流线型工具。《分析化学学报》1036,66-72。https://doi.org/10.1016/j.aca.2018.08.002。
-
Konala, V.B.R.、Nandakumar, S.、Surendran, H. 和 Pal, R.(2022)。使用游离型载体从患者特异性外周血单个核细胞(PBMC)中诱导多能干细胞(iPSC)系的建立。收录于《诱导多能干细胞与人类疾病:方法与方案》,K. Turksen 编(施普林格美国出版社),第 137-151 页。https://doi.org/10.1007/7651_2021_385。
-
施耐德(C.A.)、拉斯班德(W.S.)和埃利塞里(K.W.)(2012年)。《从NIH Image到ImageJ:25年的图像分析》。《自然方法》9,671-675。https://doi.org/10.1038/nmeth.2089。
-
Perez-Riverol, Y., Bai, J., Bandla, C., García-Seisdedos, D., Hewapathirana, S., Kamatchinathan, S., Kundu, D.J., Prakash, A., Frericks-Zipper, A., Eisenacher, M. 等人(2022)。2022 年 PRIDE 数据库资源:基于质谱的蛋白质组学证据中心。《核酸研究》,50,D543-D552。https://doi.org/10.1093/nar/gkab1038。
¶ STAR★方法
¶ 关键资源表
| REAGENT or RESOURCE | SOURCE | IDENTIFIER |
|---|---|---|
| Rat monoclonal anti-CTIP2 | Abcam | Cat# ab18465, RRID: AB_2064130 |
| Rabbit polyclonal anti-DCX | Cell Signaling Technology | Cat# 4604, RRID: AB_561007 |
| Rabbit monoclonal anti-FOXG1 | Thermo Fischer Scientific | Cat# 702554, RRID: AB_2686304 |
| Mouse monoclonal anti-MAP2ab | Millipore Sigma | Cat# M1406, RRID: AB_477171 |
| Mouse monoclonal anti-GFAP | Invitrogen | Cat# MA5-15086, RRID: AB_10981734 |
| Mouse monoclonal anti-N-Cadherin | Cell Signaling Technology | Cat# 14215, RRID: AB_2798427 |
| Rabbit monoclonal anti-NeuN | Cell Signaling Technology | Cat# 24307, RRID: AB_2651140 |
| Rabbit polyclonal anti-Homer1 | Synaptic Systems | Cat# 160 003, RRID: AB_887730 |
| Rabbit polyclonal anti-SATB2 | Abcam | Cat# ab34735, RRID: AB_2304117 |
| Guinea pig polyclonal anti-SYN1/2 | Synaptic Systems | Cat# 106 004, RRID: AB_1106784 |
| Rabbit recombinant monoclonal anti-TBR1 | Abcam | Cat# ab183032, RRID: AB_2936859 |
| Rabbit recombinant monoclonal anti-TOMM20 | Abcam | Cat# ab186735, RRID: AB_2889972 |
| Rabbit polyclonal anti-SOX2 | Abcam | Cat# ab97959, RRID: AB_2341193 |
| Sheep polyclonal anti-TBR2 | R&D Systems | Cat# AF6166, RRID: AB_10569705 |
| Mouse monoclonal anti-HuC/D | Thermo Fisher Scientific | Cat# A-21271, RRID: AB_221448 |
| Mouse monoclonal anti-OCT3/4 | Santa Cruz Biotechnology | Cat# sc-5279, RRID: AB_628051 |
| Goat polyclonal anti-NANOG | R&D Systems | Cat# AF1997, RRID: AB_355097 |
| Mouse monoclonal anti-TRA-1-60 | BioLegend | Cat# 330602, RRID: AB_1186144 |
| Mouse monoclonal anti-Nestin | Millipore | Cat# MAB5326, RRID: AB_2251134 |
| Mouse monoclonal anti-SMA | Agilent | Cat# M0851, RRID: AB_23500 |
| Rabbit polyclonal anti-AFP | Agilent | Cat# A0008, RRID: AB_2650473 |
| Goat anti-Rabbit IgG (H + L), Alexa Fluor 488 | Thermo Fisher Scientific | Cat# A-11008, RRID: AB_143165 |
| Goat anti-Rat IgG (H + L), Alexa Fluor 568 | Thermo Fisher Scientific | Cat# A-11077, RRID: AB_2534121 |
| Goat anti-Mouse IgG (H + L), Alexa Fluor 568 | Thermo Fisher Scientific | Cat# A-11004, RRID: AB_2534072 |
| Goat anti-Rabbit IgG (H + L), Alexa Fluor 647 | Thermo Fisher Scientific | Cat# A-21245, RRID: AB_2535813 |
| Goat anti-Mouse IgG (H + L), Alexa Fluor 647 | Thermo Fisher Scientific | Cat# A-21202, RRID: AB_141607 |
| Donkey anti-Rabbit IgG (H + L), Alexa Fluor 647 | Thermo Fisher Scientific | Cat# A-31573, RRID: AB_2536183 |
| Donkey anti-Goat IgG (H + L), Alexa Fluor 568 | Thermo Fisher Scientific | Cat# A-11057, RRID: AB_2534104 |
| Donkey anti-Sheep IgG (H + L), Alexa Fluor 488 | Thermo Fisher Scientific | Cat# A-11015, RRID: AB_2534082 |
| Donkey anti-Goat IgG (H + L), Alexa Fluor 594 | Thermo Fisher Scientific | Cat# A-11058, RRID: AB_2534105 |
| Donkey anti-Mouse IgG (H + L), Alexa Fluor 594 | Thermo Fisher Scientific | Cat# A-21203, RRID: AB_2535789 |
| Donkey anti-Rabbit IgG (H + L), Alexa Fluor 488 | Thermo Fisher Scientific | Cat# A-21206, RRID: AB_2535792 |
| Goat anti-Guinea pig IgG (H + L), Alexa Fluor 488 | Abcam | Cat# ab150185, RRID: AB_2736871 |
| Mouse monoclonal HRP Anti-γ-antibody | Abcam | Cat# ab49900, RRID: AB_867494 |
| Rabbit monoclonal anti-GAPDH | Cell Signaling Technology | Cat# 21185, RRID: AB_561053 |
| Rabbit recombinant monoclonal anti-SYN1 | Abcam | Cat# ab254349, RRID: AB_2920663 |
| Rabbit polyclonal anti-HIF1alpha | Abcam | Cat# ab51608, RRID: AB_880418 |
| Rabbit polyclonal anti-GFAP | Agilent | Cat# Z0334, RRID: AB_10013382 |
| Rabbit recombinant monoclonal anti-S100B | Cell Signaling Technology | Cat# 90939, RRID: AB_3678716 |
| Rabbit polyclonal anti-LAMP1 | Abcam | Cat# ab24170, RRID: AB_775978 |
| Goat anti-Rabbit IgG, HRP-linked Antibody | Cell Signaling Technology | Cat# 7074, RRID: AB_2099923 |
| Rabbit anti-Mouse IgG H&L, HRP-linked | Abcam | Cat# ab6728, RRID: AB_955440 |
| Matrigel® Growth factor reduced | Corning | 356230 |
| mTESR1 medium | Stem Cell Technologies | 85870 |
| Gentle cell dissociation reagent | Stem Cell Technologies | 07174 |
| Cerebral Organoid Kit | Stem Cell Technologies | 08570 |
| Y-27632, ROCK Inhibitor | Stem Cell Technologies | 72302 |
| Anti-Adherence Rinsing Solution | Stem Cell Technologies | 07010 |
| Matrigel® | Corning | 356234 |
| Penicillin/Streptomycin | Gibco | 15400 |
| Amphotericin B | Thermo Fisher Scientific | 15290026 |
| STEMdiff Dorsal FO Differentiation Kit | Stem Cell Technologies | 08620 |
| STEMdiff Neural Organoid Maintenance Kit | Stem Cell Technologies | 100-0120 |
| Distilled Phosphate Buffered Saline | Thermo Fisher Scientific | 14190 |
| Methylated trypsin | Made in-house, Protein Research Group, University of Southern Denmark¹⁰ | N/A |
| TMTpro 16plex | Thermo Fisher Scientific | A44520 |
| TMTpro-134C & TMTpro-135N Label Reagents | Thermo Fisher Scientific | A52046 |
| Titanium dioxide beads, 5 μm | GL Science | 5020-75010 |
| PNGaseF | New England BioLabs | P0705L |
| Sialidase A | Prozyme | GK80040 |
| SPLASH LIPIDOMIX MS standard | Merck | 330707-1EA |
| NuPage LDS Sample buffer | Thermo Fisher Scientific | NP0007 |
| NuPage Sample Reducing agent | Thermo Fisher Scientific | NP0004 |
| PageRuler Plus pre-stained protein ladder | Thermo Fisher Scientific | 26620 |
| SeeBlue® Plus2 Pre-stained Protein Standard | Invitrogen | LC5925 |
| Immobilion ECL Ultra Western HRP Substrate | Millipore | WBKULS0100 |
| Agriose base | Sigma | 93352 |
| Trizma, low-gelling temperature | Sigma | A9414 |
| Hanks’ Balanced Salt Solution (HBSS) | Thermo Fisher Scientific | 14025 |
| Poly-L-lysine hydrobromide | Sigma | P1274 |
| Laminin | Sigma | L2020 |
| Formaldehyde Solution 16% w/v | Thermo Fisher Scientific | 28908 |
| Phosphate buffered saline | Gibco | 70011-036 |
| OCT Mounting media | VWR | 361603E |
| Triton X-100 | Plusone | 17-1315-01 |
| Donkey serum | BioWest | S2170-100 |
| Goat serum | Gibco | 16210064 |
| ProLong Diamond Antifade mount | Invitrogen | P36965 |
| Dulbecco’s Phosphate Buffered Saline (PBS-/-) | Sigma Aldrich | D8537 |
| Fetal bovine serum | Thermo Fisher Scientific | 11573397 |
| Lymphoprep™ Density Gradient Medium | Stem Cell Technologies | 07801 |
| StemPro-34 SFM | Thermo Fisher Scientific | 10639011 |
| Human Stem Cell Factor (SCF) Synthetic Peptide | Peprotech | 300-07 |
| Recombinant Human Flt3-Ligand | Peprotech | 300-19 |
| Interleukin-3 | Cell Guidance system | GFH180-100 |
| Recombinant Human GM-CSF | Peprotech | 300-03 |
| L-glutamine | Thermo Fisher Scientific | 25030081 |
| Penicillin/Streptomycin | Sigma Aldrich | P0781 |
| ROCK inhibitor (ROCKi) | Sigma Aldrich | Y0503 |
| Sodium Butyrate | Sigma Aldrich | 303410 |
| DMEM/F12 | Thermo Fisher Scientific | 11320033 |
| Bovine serum albumin (BSA) | Sigma Aldrich | A3059 |
| Critical commercial assays | ||
| LDH-Glo™ Cytotoxicity Assay | Promega | J2380 |
| ROS-Glo® H2O2 Assay | Promega | G8820 |
| Seahorse XF Real-Time ATP Rate Assay Starter Pack | Agilent | 103677-100 |
| Seahorse XFe96 FluxPak | Agilent | 102601-100 |
| P3 Primary Cell 4D X Nucleofector Kit L | BioNordika | LZG-V4XP-3024 |
| DNeasy Blood and Tissue Kit | Qiagen | 69506 |
| Evercode™ Cell fixation kit | Parse Biosciences | ECF2001 |
| Evercode™ WT Mini v2 kit | Parse Biosciences | https://www.parsebiosciences.com/products/evercode-wt-mini/ |
| Deposited data | ||
| Proteomics raw data | This paper | PRIDE: PXD048559 |
| scRNAseq raw data | This paper | Gene Expression Omnibus,⁷¹ GEO: GSE253889 |
| Fetal frontal lobe proteomic dataset | Zhao et al.⁴⁰ | https://www.nature.com/articles/s42003-022-04003-6 |
| Experimental models: Cell lines | ||
| IMR90 clone 4 | WiCell | iPS(IMR90)-4; RRID: CVCL_C437 |
| SCZ002 (schizophrenia, male) | This paper | N/A |
| SCZ003 (schizophrenia, male) | This paper | N/A |
| SCZ013 (schizophrenia, male) | This paper | N/A |
| CTL005 (healthy, female) | This paper | N/A |
| CTL014 (healthy, male) | This paper | N/A |
| CTL024 (healthy, female) | This paper | N/A |
| hVM-bcl-xl midbrain neural precursor line | Schmidt et al.⁷² | https://doi.org/10.1016/j.stemcr.2020.12.011 |
| Recombinant DNA | ||
| pCXLE-hOCT3/4-shp53 | Addgene | RRID: Addgene_27077 |
| pCXLE-hSK | Addgene | RRID: Addgene_27078 |
| pCXLE-hUL | Addgene | RRID: Addgene_27080 |
| pCXBB-EBNA1 | Addgene | RRID: Addgene_41857 |
| Software and algorithms | ||
| BrainWave 5 software | 3Brain | N/A |
| ImageJ (v1.53t and 1.54p) | NIH | https://imagej.net/ij/index.html |
| GraphPad Prism (v.) | Graph Pad Software, LLC | https://www.graphpad.com/features |
| Motic Images Plus (v3.0) | Motic | https://www.motic.com/Eur_EuropeDownload/ |
| Xcalibur (v3.0) | Thermo Fisher Scientific | Thermo Fisher Scientific |
| Proteome Discoverer (v2.4) | Thermo Fisher Scientific | https://www.thermofisher.com/dk/en/home/institutional/mass-spectrometry/liquid-chromatography-mass-spectrometry-lc-ms/lc-ms-software/multi-omics-data-analysis/proteome-discoverer-software.html.html?erpType=Global_E1 |
| Mascot server (v2.6) | Matrix Science Ltd. | https://www.matrixscience.com/server.html |
| UniProt database | The UniProt Consortium⁷³ | https://www.uniprot.org/ |
| REAGENT or RESOURCE | SOURCE | IDENTIFIER |
| PolyTest | Schwämmle et al.⁷⁴ | https://computproteomics.bmb.sdu.dk/app_direct/PolyTest/ |
| Cytoscape (v3.9.1) | Cytoscape Consortium | https://cytoscape.org/ |
| StringApp, Cytoscape app | Doncheva et al.⁷⁵ | https://apps.cytoscape.org/apps/stringapp |
| ClueGO, Cytoscape app | Bindea et al.⁷⁶ | https://apps.cytoscape.org/apps/cluego |
| R software (v2025.09.2 + 418) | R Core Team⁷⁷ | https://cloud.r-project.org/bin/windows/base/ |
| ggplot2, R package | Wickham⁷⁸ | https://cran.r-project.org/web/packages/ggplot2/index.html |
| Metaboscape (v2023) | Bruker | https://www.bruker.com/en/products-and-solutions/mass-spectrometry/ms-software/metaboscape.html |
| LipidBlast MS2 library | Kind et al.⁷⁹ | https://doi.org/10.1038/nmeth.2551 |
| MetaboBase MS/MS library | Bruker | https://www.bruker.com/en/products-and-solutions/mass-spectrometry/ms-software/metabolomics-spectral-libraries.html |
| NIST17 MS/MS library | Bruker | https://chemdata.nist.gov/ |
| MassBank of North America (MoNA) | MoNA | https://mona.fiehnlab.ucdavis.edu/ |
| MetFrag | Ruttkies et al.⁸⁰ | https://ipb-halle.github.io/MetFrag/ |
| Metabo-pipe (v0.3.1) | Chong et al.⁸¹ | |
| Split-pipe (v1.0.6p) | Hao et al.⁸², Parse Biosciences | https://www.encodeproject.org/software/split-pipe/ |
| Seurat, R package | Hao et al.⁸³, Trapnell et al.⁸⁴ | https://cran.r-project.org/web/packages/Seurat/index.html |
| StatTarget | Luan et al.⁸⁵ | https://bioconductor.org/packages//release/bioc/html/StatTarget.html |
| Monocle3 | Hao et al.⁸³, Trapnell et al.⁸⁴ | https://cole-trapnell-lab.github.io/monocle3/ |
| Image Lab software | Bio-Rad | https://www.bio-rad.com/en-dk/product/image-lab-software?ID=KRE6P5E8Z |
| Other | ||
| Aggrewell™800 24-well plates | Stem Cell Technologies | 34815 |
| NanoPhotometer N60/N50 | Implen | N/A |
| Oasis HLB column | Waters | 186000132 |
| Empore™ SPE disks C8 | Sigma | 66882-U |
| Empore™ SPE disks C18 | Sigma | 66883-U |
| Oligo™ R3 material | Applied Biosystems | 1-1339-03 |
| Acquity UPLC®-Class CSHTM C18 column | Waters | N/A |
| Dionex Ultimate 3000 HPLC system | Thermo Fisher Scientific | SKU: 20773 |
| Bolt 4-12% Bis-Tris Plus Gels | Thermo Fisher Scientific | NW04125BOX |
| Trans-Blot® Turbo™ Transfer System | BioRad | 1704150 |
| CCD camera, Amersham 680 Imager | GE Healthcare | 29270769 |
| Fluostar Omega Plate reader | BMG Labtech | N/A |
| Leica VT1000S Vibratome | Leica Biosystems | N/A |
| BioCam Duplex MEA system | 3Brain | N/A |
| CorePlate 1W 38/60 microchip plates | 3Brain | N/A |
| Leica CM1860 cryostat | Leica Biosystems | N/A |
| Superfrost® Plus Microscope slides | Thermo Fisher Scientific | J1800AMNZ |
| SepMate™-50 columns | Stem Cell Technologies | 85450 |
| 4D-Nucleofector™ X Unit | BioNordika | LZG-AAF-1003X |
| 70 µm Cell Strainer | Fisherbrand | 11597522 |
| Zeiss LSM 700 confocal microscope | Zeiss | N/A |
| CytoScan 750K Suite | Thermo Fisher Scientific | N/A |
| Nikon A1R confocal unit | Nikon | N/A |
| Nikon Ti-2 LFOV microscope | Nikon | N/A |
| Motic AE2000 microscope | Motic® | N/A |
| Reprosil-Pur 120 C18-AQ, 5 μm | Dr. Maisch GmbH | https://dr-maisch.com/dr-maisch-phases/reprosil-pur/reprosil-pur-120-c18-aq |
| Reprosil-Pur 120 C18-AQ, 3 μm | Dr. Maisch GmbH | https://dr-maisch.com/dr-maisch-phases/reprosil-pur/reprosil-pur-120-c18-aq |
| EASY-nLC | Thermo Fischer Scientific | N/A |
| Orbitrap Exploris 480 | Thermo Fischer Scientific | N/A |
| Vanquish Horizon UPLC | Thermo Fischer Scientific | N/A |
| TimsTOF Flex | Bruker | N/A |
| Trans-Blot® Turbo™ Transfer System | Bio-Rad | N/A |
| Amersham 680 Imager | GE Healthcare | N/A |
| BioCam Duplex MEA system | 3Brain | N/A |
| NextSeq 2000 sequencer | Illumina | N/A |
| P2 flowcell | Illumina | N/A |
¶ 实验模型和研究参与者详情
¶ 诱导多能干细胞的维持
人类诱导多能干细胞系IMR90克隆4购自WiCell,在涂有生长因子减少的基质胶(康宁公司)的培养板上,使用mTESR1培养基(干细胞技术公司)进行培养。传代采用温和细胞解离试剂(干细胞技术公司)进行。细胞培养和分化由多名实验人员操作,以确保观察到的差异并非由单一研究人员的操作方法导致。
¶ 精神分裂症患者与健康对照者
纳入精神分裂症患者和年龄匹配的健康对照者以生成人类诱导多能干细胞系,这一研究已获得丹麦南部地区卫生研究伦理区域委员会(编号:S-20220037)和丹麦数据保护局(编号:P-2022-765)的批准。被诊断为精神分裂症的患者从丹麦首都地区的精神科住院和门诊诊所招募,而健康对照者则通过丹麦的一个网站(Forsøgsperson.dk)招募。所有参与者年龄均在18-50岁之间,且来自同一社区。患者和健康对照者都接受了全面的精神病学评估,包括由认证访谈者进行的、涵盖过去4周的世界卫生组织神经精神病学临床评估量表(SCAN,2.1版)。对于患者,该访谈用于验证纳入研究前临床医生作出的精神分裂症诊断(依据《国际疾病分类第十版》(ICD10)F20);对于健康对照者,其目的是排除精神疾病。健康对照者与纳入的精神分裂症患者在年龄上相匹配。所有参与者的静脉血样本均在哥本哈根大学医院哥本哈根心理健康中心生物与精准精神病学哥本哈根研究中心的研究设施中采集,采集量至少为34毫升,并立即送往哥本哈根大学兽医与动物科学系的设施进行进一步处理。
¶ 方法详情
¶ 外周血单个核细胞分离
34毫升全血与1:1比例的杜尔贝科磷酸缓冲盐溶液(PBS−/−)(Sigma Aldrich公司)混合,该溶液中添加了2%胎牛血清(FBS)(赛默飞世尔科技公司),然后缓慢加入两个独立的SepMate-50离心管(干细胞技术公司)中,每个离心管含有15毫升 Lymphoprep分离液(干细胞技术公司)。随后,样本在室温下以1200×g的离心力离心10分钟。离心后,将上层液体转移至50毫升 Falcon管中,用添加了2%胎牛血清的磷酸缓冲盐溶液稀释,并再次离心。此步骤重复两次,以确保彻底去除分离出的外周血单个核细胞(PBMCs)中的任何残留污染物。
¶ 游离型重编程
通过对来自3名精神分裂症患者及其年龄和性别匹配的对照者的外周血单个核细胞(PBMCs)进行游离型重编程,建立了人诱导多能干细胞(hiPSCs)(图S4D)。
将4×10⁶个分离出的外周血单个核细胞(PBMCs)在PBMC培养基中培养,该培养基由StemPro-34 SFM培养基(赛默飞世尔科技)组成,补充了100 ng/mL人干细胞因子合成肽(Peprotech)、100 ng/mL重组人Flt3配体(Peprotech)、20 ng/mL白细胞介素-3(Cell Guidance system)、1 ng/mL重组人粒细胞-巨噬细胞集落刺激因子(20μg,Peprotech)、2mM L-谷氨酰胺(赛默飞世尔科技)和1%青霉素/链霉素(P/S)(西格玛奥德里奇),培养于低吸附6孔板中,培养2天。在重编程前一天,对每个细胞系计数100万个细胞,并在不含P/S的PBMC培养基中培养。采用改良方案将细胞重编程为人类诱导多能干细胞(hiPSCs)。86每个细胞系约100万个PBMCs,使用P3原代细胞4D X核转染试剂盒L和Lonza核转染仪(BioNordika),以1:1:1:1的稀释比例转染1μg/μL的pCXLE-hOCT3/4-shp53(Addgene)、pCXLE-hSK(Addgene)、pCXLE-hUL(Addgene)和pCXB-EBNA1(Addgene)。核转染所用程序为EO-100。电穿孔后,将细胞在室温下放置3分钟,然后逐滴加入300μL制备好的含1% P/S和10μM ROCK抑制剂(ROCKi)(西格玛奥德里奇)的PBMC培养基,随后在37℃、5% CO₂湿度条件下孵育10分钟。孵育后,每个细胞系在Matrigel(康宁)上用PBMC培养基进一步培养。重编程后第二天,通过倾斜培养板更换为新鲜的含1% P/S的PBMC培养基,缓慢移除1mL用过的培养基,并缓慢加入1mL新鲜培养基。重编程后第3天,将一半培养基更换为干细胞培养基,即含0.1% P/S和250μM丁酸钠(西格玛奥德里奇)的mTeSR1培养基(干细胞技术公司)。此后,每两天更换一次干细胞培养基,直至出现集落。平均在重编程后第16天手动挑取集落。挑取的集落在Matrigel上用干细胞培养基培养,并补充10μM ROCK抑制剂。至少扩增6个集落以生成人类诱导多能干细胞克隆并进行保存。如免疫细胞化学方法部分所述,使用多能性标志物NANOG(山羊源,1:200)、OCT-3/4(小鼠源,1:200)和TRA-1-60(小鼠源,1:200)的一抗,通过免疫细胞化学对每个细胞系的人类诱导多能干细胞克隆进行评估(图S3A和S3B)。
¶ 人类诱导多能干细胞系分化潜能检查
通过胚胎小体形成和自发分化实验,评估了源自外周血单个核细胞(PBMCs)的人诱导多能干细胞(hiPSCs)克隆分化为三个胚层(内胚层、外胚层和中胚层)的潜能。具体步骤如下:在AggreWell 800 24孔板的一个孔中加入500μL抗黏附冲洗液(Stem Cell Technologies公司),以1800转/分钟的速度离心3分钟。随后吸去孔中的液体,更换为1mL添加了10μM ROCKi的mTeSR1基础培养基,置于37℃环境中备用。同时,将人诱导多能干细胞与0.5mM EDTA共同孵育3分钟,然后用mTeSR1基础培养基收集细胞。将1×10⁶个人诱导多能干细胞转移至新的离心管中,以1000转/分钟的速度离心3分钟得到细胞沉淀,用1mL添加了10μM ROCKi的mTeSR1基础培养基重悬后,接种到准备好的AggreWell板中。随后将该板以400转/分钟的速度离心5分钟。更换培养基时,小心吸去1mL用过的培养基,并用新鲜的mTeSR1基础培养基替代。此步骤重复两次,以确保培养基完全更换。第4天,将胚胎小体转移至铺有基质胶的4孔板中,该孔板内含有12mm双酸处理的玻璃盖玻片。将培养基更换为成纤维细胞培养基,即80% DMEM/F12(赛默飞世尔科技公司)添加20%胎牛血清(FBS)和1%青霉素-链霉素(P/S)。成纤维细胞培养基每两天更换一次,持续三周。分化后的细胞通过免疫细胞化学方法进行鉴定(方法详见免疫细胞化学部分),以3%牛血清白蛋白(BSA)(西格玛奥德里奇公司)作为封闭液,检测三个胚层的标志物:巢蛋白(外胚层)、甲胎蛋白(内胚层)和平滑肌肌动蛋白(中胚层)(图S3D和S3E)。一抗稀释比例如下:巢蛋白(小鼠源,1:200)、甲胎蛋白(AFP,兔源,1:500)、平滑肌肌动蛋白(SMA,小鼠源,1:1000)。使用蔡司LSM 700共聚焦显微镜获取图像,并采用Fiji ImageJ 1.53t版本进行图像处理。87
¶ 拷贝数变异
为评估已建立细胞系的基因组完整性,从每个人类诱导多能干细胞克隆的6孔板中取1个长满的孔提取DNA。使用DNeasy Blood and Tissue Kit(Qiagen)按照培养细胞的制造说明进行DNA提取。提取的DNA通过Nanodrop进行测量,然后送往南丹麦大学奥登塞大学医院临床遗传学系,在那里使用赛默飞世尔科技的CytoScan 750K Suite进行拷贝数变异分析。
¶ 前脑类器官(FO)分化
无引导FOs: 使用脑类器官试剂盒(Stem Cell Technologies公司)按照制造商说明生成,并进行了以下修改:第0天,将每孔600,000个诱导多能干细胞接种到预先用抗黏附冲洗液(Stem Cell Technologies公司)处理过的Aggrewell800 24孔板(Stem Cell Technologies公司)中,培养基为包含50μM ROCK抑制剂(Y27632,Stem Cell Technologies公司)的拟胚体(EB)接种培养基。第7天,使用宽口径p1000移液枪头将拟胚体从Aggrewell800 24孔板中转移出来,并用宽口径p200移液枪头将约30个拟胚体与100μL扩增培养基和150μL冷基质胶(Corning公司)轻轻混合,然后将混合物接种到60mm培养皿中,形成直径约10mm的圆形,从而将拟胚体包埋在基质胶中。在37°C下孵育30分钟使基质胶聚合后,每个培养皿中加入4mL扩增培养基。第10天,将培养皿转移到INFORS HT Celltron轨道摇床(设置为57rpm)上,置于37°C培养箱中。第15天,使用宽口径p1000移液枪头轻轻吹吸,使类卵泡从基质胶中脱离,每个培养皿中培养约16个类卵泡,培养基为5mL。
引导FOs: 使用STEMdiff背侧FO分化试剂盒(Stem Cell Technologies)生成,并根据制造商协议使用STEMdiff神经类器官维持试剂盒(Stem Cell Technologies)进行维持,同时进行了以下修改:在扩增期间,引导性FOs在低吸附24孔板中培养,每孔4-5个FOs,以尽量减少FOs的融合。在第20天左右,将FOs转移到60毫米低吸附培养皿中,每皿16个FOs。
对于两种FO分化,从第10天起,培养基中均添加了1%的青霉素/链霉素(Pen/Strep,Gibco)和1μg/mL的两性霉素B(Amp B,赛默飞世尔科技)。随着FO体积的增大,每个培养皿中的FO数量从16个逐渐减少至5个。
¶ 免疫细胞化学与成像
来自2或3次独立分化的FOs用含4%多聚甲醛(赛默飞世尔科技)的PBS(Gibco)在室温(RT)下固定1小时,随后在4℃的PBS中浸泡于30%蔗糖中至少一晚,直至包埋。将FOs包埋于OCT包埋剂中,在低于-50℃的乙醇中冷冻,并在-70℃下储存。使用Leica CM1860冷冻切片机在-17至-20℃下将FOs切成30μm的切片,并铺在Superfrost Plus玻璃显微镜载玻片上。载玻片在-20℃下储存。
切片用PBS水合,在含0.1% Triton X-100(Plusone)的PBS中洗涤2次,每次5分钟,然后用透化封闭缓冲液(含5%驴血清或山羊血清以及0.1% Triton X-100的PBS)孵育30分钟。将切片与含1%血清和0.1% Triton X-100的PBS中的一抗在4℃下孵育过夜(ON)。一抗的使用浓度如下:CTIP2(大鼠,1:500)、DCX(兔,1:800)、FOXG1(兔,1:250)、GFAP(小鼠,1:500)、Map2(小鼠,1:2000)、NCAD(小鼠,1:500)、NEUN(兔,1:50)、Homer1(山羊,1:250)、SATB2(兔,1:500)、SYN1/2(豚鼠,1:250)、TBR1(兔,1:100)、TOMM20(兔,1:250)、SOX2(兔,1:500)、TBR2(绵羊,1:200)和HuC/D(小鼠,1:500)。样本用含0.1% Triton X-100的PBS洗涤3次,每次10分钟,然后在室温避光条件下与二抗孵育1小时。二抗的稀释比例如下:Alexa Fluor 488标记的山羊抗兔(1:500)、驴抗小鼠(1:5000)、驴抗绵羊(1:500)、驴抗兔(1:1000)和山羊抗豚鼠(1:500);Alexa Fluor 568标记的山羊抗大鼠(1:1000)、山羊抗小鼠(1:1000)和驴抗山羊(1:1000);Alexa Fluor 594标记的驴抗山羊(1:1000)和驴抗小鼠(1:1000);Alexa Fluor 647标记的山羊抗兔(1:1000)和驴抗兔(1:500)。切片用PBS洗涤3次,每次10分钟,然后用含DAPI的ProLong Diamond抗荧光淬灭封片剂(Invitrogen)封片。对于第20天的整体染色,未切割的类器官在旋转条件下进行漂浮染色,之后再装片到载玻片上。切片在4℃避光条件下保存,直至图像采集。
图像是使用Ti-2 LFOV显微镜上的Nikon A1R共聚焦装置获取的,两种类器官的设置相同。所示图像使用ImageJ 1.53t.87版本进行编辑。
生长曲线是通过Motic AE2000显微镜获取的活类器官明场图像生成的,类器官大小则使用Motic Images Plus 3.0软件进行量化。
| Secondary antibodies | Company | Cat. No. | Dilution |
| Alexa Fluor 488 goat-anti-rabbit | Life Technologies | A11008 | 1:500 |
| Alexa Fluor 568 goat-anti-rat | Invitrogen | A11077 | 1:1000 |
| Alexa Fluor 568 goat-anti-mouse | Life Technologies | A11004 | 1:1000 |
| Alexa Fluor 647 goat-anti-rabbit | Invitrogen | A21245 | 1:1000 |
| Alexa Fluor 488 donkey-anti-mouse IgG (H + L) | Life Technologies | A21202 | 1:5000 |
| Alexa Fluor 647 donkey-anti-rabbit IgG (H + L) | Life Technologies | A31573 | 1:500 |
| Alexa Fluor 568 donkey-anti-goat | Life Technologies | A11057 | 1:1000 |
| Alexa Flour 488 donkey-anti-sheep | Invitrogen | A11015 | 1:500 |
| Alexa Flour 594 donkey anti-goat | Thermo Fisher | A11058 | 1:1000 |
| Alexa Flour 594 donkey anti-mouse | Thermo Fisher | A21203 | 1:1000 |
| Alexa Flour 488 donkey anti-rabbit | Thermo Fisher | A21206 | 1:1000 |
| Alexa Fluor 488 goat anti-guinea pig IgG (H + L) | Abcam | ab150185 | 1:500 |
¶ 蛋白质裂解与消化
第40天的卵泡(FOs)被转移至低吸附离心管中,用PBS洗涤1次,然后在干冰上快速冷冻。卵泡在含1%脱氧胆酸钠(SDC,Sigma)的50 mM TEAB(Sigma)缓冲液(含10 mM DTT(Sigma),pH 8)中裂解,并在冰上以35%振幅超声处理2次,每次10秒。超声处理后,样品在室温下以5000相对离心力离心10分钟,上清液转移至新的离心管中。通过Nanodrop(Implen)测定蛋白质浓度。每个样品取40μg蛋白质,用20 mM碘乙酰胺(Sigma)烷基化30分钟,然后用5%胰蛋白酶70(w/w)在37℃下消化4小时。
¶ 用于蛋白质组学分析的TMT标记
按照制造商的说明,在使用TMTpro 18重标(赛默飞世尔科技)进行标记之前,样本用1 M TEAB进行碱化处理。反应通过5%羟胺(赛默飞世尔科技)终止,并且通过在Orbitrap Exploris 480质谱仪(赛默飞世尔科技)上对各样本取1微升混合液进行检测,确定以等比例混合样本。使用2%甲酸(FA,默克)从混合样本中沉淀出SDC。
¶ 磷酸肽和糖肽的富集
磷酸肽和唾液酸化N-糖肽的富集方法如前所述。28 简要来说,将肽溶解在二氧化钛(TiO₂)上样缓冲液(80%乙腈(ACN,VWR)、5%三氟乙酸(TFA,默克)、1M乙醇酸(西格玛))中,并与二氧化钛珠(GL Sciences公司)孵育,二氧化钛珠会结合带负电荷的磷酸肽和唾液酸化N-糖肽。二氧化钛富集过程中未结合的“非修饰”组分保留用于定量蛋白质组学分析,修饰组分则使用25%氢氧化铵(默克)(pH 11.3)从二氧化钛珠上洗脱,并与PNGase F(新英格兰生物实验室)和唾液酸酶A(Prozyme)孵育过夜以进行去糖基化。通过第二轮二氧化钛富集,将磷酸肽与先前的唾液酸化N-糖肽分离。
经修饰的肽通过自制反相微柱进行纯化和脱盐。将肽酸化后上样到装有Empore SPE C18圆盘(Sigma)和Oligo R3树脂(Applied Biosystems)的p200移液器吸头中。未修饰的肽同样进行酸化处理,然后上样到Oasis HLB柱(Waters),该柱已用甲醇(VWR)和100%乙腈活化。用0.1%三氟乙酸溶液平衡柱子。所有纯化后的肽用60%乙腈、0.1%三氟乙酸洗脱,并在高pH分馏前干燥。
¶ 高pH分馏
这3个组分(未修饰肽、磷酸肽和唾液酸化N-糖肽)分别溶解在20 mM甲酸铵(pH 9.3)中,上样到Acquity UPLC-Class CSH™ C18色谱柱(Waters公司),并在Dionex Ultimate 3000高效液相色谱系统(赛默飞世尔科技公司)上进行分离。未修饰肽收集了20个合并组分,磷酸肽和唾液酸化N-糖肽各收集了12个合并组分。
¶ 纳米液相色谱-质谱法
样本重悬于0.1%甲酸(缓冲液A)中,上样至自制的双柱系统。该系统包含一根3厘米长的预柱(内径100μm,填充Reprosil-Pur 120 C18-AQ,5μm(Dr. Maisch GmbH))和一根18厘米长的拉制发射极分析柱(内径75μm,填充Reprosil-Pur 120 C18-AQ,3μm(Dr. Maisch GmbH)),并连接于EASY-nLC系统(赛默飞世尔科技)。肽段通过有机溶剂梯度洗脱,从100%缓冲液A(0.1%甲酸)到40%缓冲液B(95%乙腈,0.1%甲酸),流速恒定为250 nL/min,洗脱时间120分钟。EASY-nLC在线连接至Orbitrap Exploris 480质谱仪(赛默飞世尔科技),该质谱仪在正离子模式下运行,采用数据依赖型采集模式。所有全扫描质谱(full MS)在Orbitrap中进行,质量范围为350–1400,分辨率为120000半峰全宽(FWHM),最大离子注入时间为100 ms,归一化自动增益控制(AGC)目标为300%。
在高分辨率(45,000 FWHM)下进行碎片分析,采用200%的标准化AGC目标值,最大注入时间为100毫秒,使用0.7 m/z的隔离窗口和动态排除。原始数据在Xcalibur v3.0(赛默飞世尔科技)中查看。
¶ 蛋白质鉴定和定量
质谱蛋白质组学数据已通过PRIDE88合作存储库存入ProteomeXchange联盟,数据集标识符为PRIDE: PXD048559。原始数据使用Proteome Discoverer(v2.4,赛默飞世尔科技)进行处理,并通过内部Mascot服务器(v2.6,Matrix Science有限公司)在Swissprot人类数据库中进行检索。数据库检索参数如下:前体质量耐受性为10 ppm,碎片质量耐受性为0.02 Da(HCD碎裂),最多2个漏切位点,TMT-Pro(赖氨酸/N端)和氨甲酰甲基(半胱氨酸)作为固定修饰,唾液酸化N-糖肽和磷酸肽中分别将脱酰胺(天冬酰胺)或磷酸化(丝氨酸/苏氨酸/酪氨酸)作为动态修饰。仅q值<0.01(Percolator)、Mascot排名1且Mascot得分>15的蛋白质/肽段被纳入进一步分析(≤1%错误发现率(FDR))。
在非修饰组中,只有含有两种或更多独特肽段的蛋白质才会被纳入进一步分析。基于UniProt73中已知的糖基化和细胞定位(高尔基体/内体/溶酶体/膜/细胞外)信息,对唾液酸化N-糖肽(NxS/T/C基序)进行手动分类,以排除自发性脱酰胺作用。使用PolyStest74对所有三个数据集进行统计学检验,以确定两组之间的显著差异,该检验采用秩乘积检验,通过错误发现率(FDR)=0.05来校正多重检验。
使用Cytoscape StringApp75中的ClueGO76插件进行基因本体论(GO)术语富集分析,以在三个数据集的显著差异蛋白质/肽中识别“生物学过程”类别中功能分组的GO术语的富集情况。对于非修饰蛋白质和磷酸肽,分别采用>0.3或<-0.3以及>0.5或<-0.5的折叠变化阈值。通过双侧超几何检验结合Bonferroni逐步下降法(q值<0.05)确定富集情况。应用智人(9606)标记集,设置如下:选中GO术语融合,网络置信度评分0.5,GO树级别6-12,Kappa评分阈值0.5。在GO术语选择方面,非修饰和唾液酸化N-糖蛋白使用至少3个基因和5%的基因,而更大的磷酸化蛋白质列表则使用至少5个基因和10%的基因。使用R中的ggplot2.77,78进行数据可视化。
使用Cytoscape StringApp75创建了字符串网络,置信度评分阈值为0.4,且仅显示连接的节点。
¶ 脂质和代谢物提取
第40天的卵泡被转移到低结合管中,用50 mM醋酸铵(Sigma)洗涤1次,然后在干冰上快速冷冻。采用改良的Folch法提取代谢物和脂质:在含有SPLASH LIPIDOMIX MS标准内标混合物(Merck)的冰冷1:2甲醇/氯仿溶剂中,对卵泡进行2次10秒的超声处理。向样品中加入1:6的水,然后在4℃、1000 rpm条件下振荡30分钟,接着在4℃、16000 rcf条件下离心10分钟。收集含代谢物的水相(上层)和富含脂质的有机相(下层)。水相用86:14:1的氯仿/甲醇/水溶剂重新提取,在4℃、1000 rpm条件下振荡20分钟,然后在4℃、16000 rcf条件下离心10分钟。收集含代谢物的水相,通过真空离心浓缩仪干燥。将含剩余脂质的下层有机相加入之前的有机相中,在氮气流(N₂)下干燥,并在-20℃下储存至分析当天。
¶ 代谢组学和脂质组学分析
代谢组学样品在注射前用25μL 0.1%甲酸重悬,随后使用Vanquish Horizon超高效液相色谱仪(赛默飞世尔科技)注射3μL样品。该仪器配备了一根分析柱(2.1×150 mm,粒径1.8μm,安捷伦科技),柱温设定为40℃。分析物的洗脱流速为400μL/min,洗脱液A(0.1%甲酸)和洗脱液B(0.1%甲酸乙腈溶液)的组成如下:0-1.5分钟,B相占3%;1.5-3分钟,B相从3%升至40%;3-5分钟,B相从40%升至95%;5-7.6分钟,B相保持95%;7.6-8分钟,B相从95%降至3%,之后在初始条件下平衡3.5分钟。超高效液相色谱的流出物与TimsTOF Flex(布鲁克)质谱仪相连进行质谱分析,扫描范围为40-1500 m/z,采用捕获离子淌度谱,在正离子和负离子模式下运行。碰撞能量设为20和40电子伏特。
脂质组学样本重悬于25 μL氯仿/甲醇(1:1)中,取1 μL注入Vanquish Horizon超高效液相色谱仪(赛默飞世尔科技),该仪器配备Waters ACQUITY Premier CSH色谱柱(2.1×100mm,1.7 μM),柱温设定为55℃。分析物的洗脱流速为400 μL/min。对于脂质,流动相组成如下:流动相A为乙腈/水(60:40),含10 mM甲酸铵和0.1%甲酸;流动相B为异丙醇/乙腈(90:10),含10 mM甲酸铵和0.1%甲酸。洗脱梯度为:0-0.5分钟,流动相B占40%;0.5-0.7分钟,流动相B从40%升至43%;0.7-0.8分钟,流动相B从43%升至65%;0.8-2.3分钟,流动相B从65%升至70%;2.3-6分钟,流动相B从70%升至99%;6-6.8分钟,流动相B保持99%;6.8-7分钟,流动相B从99%降至40%,之后在初始条件下平衡3分钟。
对于代谢物,采用以下流动相组成:流动相A(含0.1%甲酸的水)和流动相B(异丙醇/乙腈(90:10)、含0.1%甲酸的乙腈):0至1分钟保持3% B,1至3分钟从3%升至40% B,3至5分钟从40%升至95% B,5至7.6分钟保持95% B,7.6至8分钟从95%降至3% B,随后在初始条件下平衡3.5分钟。
超高效液相色谱(UPLC)的流出物与TimsTOF Flex仪器(布鲁克公司)相连,该仪器采用捕获离子淌度谱,在正离子和负离子模式下运行。脂质检测的质荷比范围为100至1800,正离子模式下的碰撞能量为30/50电子伏特,负离子模式下为20/30电子伏特。代谢物检测的质荷比范围为40至1500,碰撞能量为20和40电子伏特。
数据在Metaboscape(v2023,布鲁克)中进行处理。脂质组学注释采用内置的基于规则的注释方法和LipidBlast MS2库完成。79
在代谢组学注释方面,首先通过将二级质谱(MS2)光谱与以下串联质谱库进行比对来完成注释:Metabobase(布鲁克)、美国国家标准与技术研究院17(NIST17)以及北美质谱库(MoNA)。接下来,使用Metfrag对未注释的化合物进行计算机模拟注释。80
如果特征在质量控制样本中的平均信号并不比空白样本(水提取物)高5倍以上,则将其移除。在使用statTarget校正信号漂移之前,先将信号归一化至SPLASH混合液中的内标。85最后,在进行对数转换(以10为底)和自动缩放之前,使用质量控制样本对信号进行归一化,所有这些操作均在Metaboanalyst中完成。81
¶ 蛋白质印迹法
第40天和第120天的类器官在含1% SDC的50 mM TEAB(pH8)中裂解,并在冰上以35%振幅超声处理2×10秒。超声处理后,样品在室温下以5000相对离心力离心10分钟,上清液转移至新的离心管中。通过Nanodrop(Implen)测定蛋白质浓度。使用Bolt 4-12% Bis-Tris Plus凝胶(赛默飞世尔科技)分离蛋白质,样品加载于含NuPage样品还原剂(赛默飞世尔科技)的NuPage LDS样品缓冲液(赛默飞世尔科技)中,同时加入PageRuler Plus预染蛋白质标准品(赛默飞世尔科技)或SeeBlue Plus2预染蛋白质标准品(Invitrogen)作为分子量参考。使用Trans-Blot Turbo转移系统(BioRad)将蛋白质转移至PVDF膜上,膜在含5%脱脂奶粉的TBST缓冲液中封闭1小时,然后在4℃下与以下一抗在TBST中孵育过夜:兔抗TOMM20(Abcam #ab186735)1:1000、小鼠抗Map2a+b(Sigma #M1406)1:500、小鼠抗β-肌动蛋白HRP偶联(Abcam #ab49900)1:50000、兔抗GAPDH(Cell Signaling Technology #21185)1:1000、兔抗突触蛋白1(SYN1,Abcam #ab254349)1:1000、兔抗HIF1α(Abcam #ab51608)1:1000、兔抗胶质纤维酸性蛋白(GFAP,Dako #Z0334)、兔抗FOXG1(赛默飞世尔科技 #702554)1:250、兔抗S100B(Cell Signaling Technology #90393S)1:1000或兔抗LAMP1(Abcam #24170)1:500。用TBST洗涤3次后,膜在室温下与以下二抗在TBST中孵育1小时:HRP偶联的抗兔IgG(Cell Signaling Technology #7074)1:10000或HRP偶联的抗小鼠IgG(Abcam #ab6728)1:10000。用TBST洗涤3次后,使用Immobilon ECL Ultra Western HRP底物(Millipore)和Amersham 680成像仪(GE Healthcare)对膜进行显影。所有抗体的代表性全泳道蛋白质印迹如图S6所示。
作为HIF1α印迹的对照,人腹侧中脑神经前体细胞(NPC)系hVM-bcl-xl按照先前描述的方法分化为神经元10天,并在常氧(21%氧分压)或低氧(1%)条件下孵育4小时。72用dPBS快速洗涤神经元一次,收集于含1% SDC的50 mM TEAB中,并在干冰上快速冷冻。
¶ 多电极阵列(MEA)分析
多电极阵列(MEA)记录在BioCam Duplex系统(3Brain公司)上进行。Accura HD-MEA芯片(3Brain公司)的记录区域预先用100μg/mL的多聚-L-赖氨酸(Sigma公司)包被,用dPBS(赛默飞世尔科技公司)洗涤3次,再预先用50μg/mL的层粘连蛋白(Sigma公司)包被。第110天的类卵泡(FOs)接种于HD-MEA芯片时,先移除层粘连蛋白,用无菌刮刀将类卵泡轻轻放置在记录区域,并吸去所有培养基。通过逐步添加少量培养基(10–100μL),每次添加后孵育5–10分钟,以促进类卵泡附着于记录区域。确认类卵泡附着后,向芯片储液池加入1.5mL培养基。类卵泡在HD-MEA芯片上培养,每3–4天更换一次培养基。第120天,在BioCam Duplex系统上进行2分钟的记录,温度设定为37℃,在平衡模式下进行峰电位检测。使用BrainWave 5软件进行分析。
¶ LDH和ROS的功能测定
第40天卵泡(FOs)的乳酸脱氢酶(LDH)释放量通过以下方式测定:将单个卵泡在150μL成熟培养基中孵育过夜(ON),然后按照制造商说明,使用LDH-Glo细胞毒性检测试剂盒(Promega)对培养基中的LDH含量进行定量。
使用ROS-Glo H₂O₂检测试剂盒(Promega)测量第40天的卵泡(FOs)清除活性氧(ROS)的能力,具体方法是将单个卵泡与H₂O₂底物共同孵育2小时,随后根据制造商的说明检测培养基中(有和无卵泡的情况)的H₂O₂水平。
对于这两种测定,相对发光强度均使用Fluostar Omega酶标仪(BMG Labtech公司)进行测量,并根据通过Nanodrop测量的每个FO的蛋白质含量进行标准化。
¶ Seahorse分析
第55-60天的FOs被包埋在含4%(w/v)低凝胶温度琼脂糖的HBSS中,并在振动切片机上切成150μm的切片,设置如下:振幅300μm、频率6、速度5。切片进行自由漂浮培养,次日按照MEA分析所用的相同方法接种到Seahorse XFp微孔板(安捷伦)中。使用Seahorse XF实时ATP速率测定试剂盒(安捷伦),根据制造商说明并稍作修改,对FO切片的ATP生成量进行测量:测定过程中寡霉素的孵育时间延长至15分钟,以使其充分扩散到切片中,且最终毒素浓度调整为寡霉素5μM、鱼藤酮/抗霉素2μM(安捷伦)。ATP生成量以通过Nanodrop(Implen)测量的FO切片蛋白质含量进行标准化。
¶ 单细胞RNA测序(scRNAseq)
对总共7-8个FO(第20天)或2-3个FO(第40天)进行三次重复的单细胞解离。收集FO,在1mL Accumax(Sigma公司,A7089)中于37℃温育20分钟,同时轻轻摇动。每5分钟轻弹样品管一次,15分钟后移液1次,20分钟时最后移液7次。让团块沉淀,上清液通过70μm滤网(Fisherbrand公司,11597522)。计数细胞(Countess II,Invitrogen公司),收集至少1×10⁶个活细胞,按照制造商说明进行后续的Evercode细胞固定(Parse Biosciences公司,ECF2001),固定前缓冲液中不含牛血清白蛋白。对12个样品进行条形码标记,并使用Evercode WT Mini v2试剂盒(Parse Biosciences公司)按照制造商的方案制备测序文库。然后使用NextSeq 2000测序仪(Illumina公司)和P2流动池(Illumina公司)对文库进行200个循环的测序。Illumina测序生成成对的FASTQ文件。使用Parse Biosciences公司开发的生物信息学管道split-pipe(1.0.6p版本)处理这些文件。82该管道执行多种功能,包括识别条形码、将读数映射到人类参考基因组(GRCh38/102版本)以及在单细胞水平上量化基因表达。该管道使用2版化学试剂,按照Parse Mini试剂盒的默认参数运行。单细胞RNA测序数据已存入NCBI的基因表达综合数据库,并可通过GEO系列登录号GEO: GSE253889获取。71
使用Seurat在R中对过滤后的数字基因表达(DGE)矩阵进行了分析。77,78,82 仅对总转录本>100且<150,000、独特转录本<12,000且线粒体转录本占总数<10%的细胞进行了分析(图S2A)。将完整数据集分为四个条件,对每个数据集进行标准化并识别可变特征,然后基于重复可变特征(整合锚点)进行重新整合。对整合后的数据集进行缩放,并使用主成分分析(PCA)进行降维,通过基于前15个主成分生成的UMAP进行可视化(图S2B和S2C)。基于K近邻图的聚类(采用Louvain算法,分辨率=1)得到21个聚类,通过对已知标记基因的差异基因表达分析和文献综述,将这些聚类合并并手动注释为12个聚类。
通过对整合的Seurat对象进行子集划分和转换,分别对引导性和非引导性FOs的数据使用Monocle3进行伪时间分析。83,84 UMAP坐标和聚类从Seurat中分配,轨迹分析不考虑聚类分区。通过将有丝分裂放射状胶质细胞的聚类指定为起点来对细胞进行排序。
¶ 胎儿额叶蛋白质组学比较
蛋白质组学数据下载自(Zhao等人,2022)。40 对妊娠第9周额叶左右半球的无标记定量(LTQ)蛋白质强度进行平均和对数转换,并与引导和非引导FO(精神分裂症和对照组合并)的对数转换蛋白质丰度进行比较。仅纳入妊娠第9周平均LTQ强度>0的胎儿蛋白质。在R语言中进行Spearman相关分析。77,78
将FO的蛋白质对数丰度和胎儿额叶的蛋白质对数LTQ在各组内均归一化至平均值,然后进行比较,以识别FO和胎儿额叶之间归一化丰度相对较高或较低的蛋白质。如前所述,在Cytoscape中对FO对数丰度/胎儿对数LTQ <0.2或>10的蛋白质进行富集分析。相对于胎儿额叶,在FO中丰度较高的蛋白质未观察到富集现象。
¶ 量化与统计分析
¶ 图像和WB定量分析
从每个类器官的两个FO切片中,使用10倍或60倍物镜获取1到3张图像用于定量分析。每个批次培养1到3个类器官,这些类器官来自2到3个批次。图像在ImageJ v1.54p中进行处理和定量分析,处理前先转换为8位图像。
为了量化第80天时的GFAP水平,使用了半径为7的Top Hat滤波器,随后进行半径为15的滚动球背景减除,并启用滑动抛物面,以去除背景信号。运行去斑点处理以去除噪声。
为了量化SYN1/2和Homer1的水平,使用Top Hat滤波器(半径=20像素)和Triangle阈值法去除背景。对于SYN1/2,第40天时的最小阈值设为60,第80天时设为50;对于Homer1,第40天时的最小阈值设为50,第80天时设为25。运行一次去斑处理以去除噪声。MAP2的背景采用Top Hat滤波器(半径=20)和Triangle阈值法去除,第40天时的最小阈值设为30,第80天时采用默认值。运行去斑处理以去除噪声,并在测量重叠区域前使用膨胀处理。仅对与MAP2信号重叠的Homer1或SYN1/2区域进行测量,强度以平均灰度值衡量。对于DAPI图像,采用Huang阈值法,DAPI区域用于标准化,作为10倍物镜获取图像中细胞数量的代表。
在第80天,使用60倍物镜对Homer1、SYN1/2和MAP2之间的共定位进行了测量。对SYN1/2和Homer1图像应用顶帽滤波器(半径=30像素)以去除背景,随后采用三角形阈值法,SYN1/2的最小阈值设为30,Homer1的最小阈值设为15。MAP2图像采用三角形法进行阈值处理,最小阈值设为20,之后进行去斑处理以去除噪声,并应用膨胀函数以确保包含周边共定位。使用多边形选择工具测量类器官面积,并将其用于三重共定位和MAP2面积测量的标准化。
在蛋白质印迹(WB)定量分析中,每条条带的光密度通过Image Lab软件(Bio-Rad)进行定量。
¶ 统计分析
使用PolyStest74对蛋白质组学、代谢组学和脂质组学结果进行统计分析,采用秩乘积检验(FDR = 0.05),并使用内置的基于Benjamini Hochberg的多重检验校正方法。n指每组的FO数量,相关时会在图注中与倍数变化临界值一同注明。
除非上文另有说明,否则数据可视化和统计检验均在Prism(v10.0,GraphPad Software)中进行,采用双尾配对Student t检验,并在适当时采用Benjamini-Hochberg校正进行多重检验。结果以平均值±标准误表示,p值或q值≤0.05被认为具有统计学显著性。每个实验的统计详情可在图注中找到。