¶ 《NETWORK NEURO SCIENCE》
¶ 退化神经元网络中的微尺度功能障碍和中尺度补偿
¶ 原文下载:netn.a.552_origin.pdf
维加德·菲斯库姆¹、尼古拉·温特-耶尔姆¹†、尼古拉斯·克里斯蒂安森¹†、阿克塞尔·桑德维格¹,²,³以及约安娜·桑德维格¹
1 挪威科技大学(NTNU)神经医学与运动科学系,挪威特隆赫姆
2 瑞典乌默奥市乌默奥大学医院临床神经科学系
3 瑞典乌普萨拉大学社区医学与康复系,乌普萨拉
† 这些作者享有同等贡献。
关键词:图论、功能连接性、多电极阵列、肌萎缩侧索硬化症、过度兴奋性、富集俱乐部
¶ 摘要
进行性神经退行性疾病涉及细胞、回路和全脑层面的神经元功能障碍。尽管在解剖学起源、易受损的神经元亚型以及特定的错误折叠蛋白方面存在差异,但这些疾病具有关键的共同特征。在症状出现前阶段,神经网络会启动代偿过程以维持功能,包括增强中心化程度以及对核心节点组成的“富集俱乐部”的依赖。虽然此类机制在某些疾病中已有支持性证据,但在肌萎缩侧索硬化症(ALS)中尚未得到充分证实,这限制了对潜在共有的症状前反应的理解。 为解决这一问题,我们利用纵向多电极阵列记录和基于图论的分析方法,研究了ALS患者来源的运动神经元网络与健康对照组的结构和功能特性。我们观察到以TAR DNA结合蛋白43蛋白病、过度活跃和尖峰振幅降低为特征的微观功能障碍。在结构上,ALS网络表现出神经突肥大,这表明其在尝试形成新的连接。中观层面的分析揭示了功能重构,包括增强的富人俱乐部连接性与更高的网络同配性,表明存在代偿性中心化。 我们的研究结果提供了新的证据,表明ALS的网络特征可以在体外模型中重现,并且这些网络会逐渐变得更加集中以维持计算能力,这会对核心节点提出越来越高的要求,并使其更容易受到进一步的损伤。这些结果支持了关于神经退行性疾病存在共同网络重构机制的模型。
¶ 作者摘要
本研究为神经退行性疾病的临床前建模做出了重大贡献,尤其与肌萎缩侧索硬化症(ALS)研究相关。通过利用人类细胞模型、纵向细胞外电生理学和先进的网络分析,我们发现ALS的已知特征可以在体外工程化神经网络中重现,并且这些网络能够支持新的假设检验以及对症状前病理过程(包括中心化程度增加)的识别。这一现象此前在其他神经退行性疾病中已被观察到,但在ALS中的证据有限。我们的研究结果加深了我们对ALS中运动神经元网络动态的理解,并有助于形成对神经退行性疾病如何影响神经网络的共识——这种影响超越了特定疾病的诊断范畴,揭示了神经网络功能和疾病反应中的基本过程。
TAR-DNA结合蛋白43(TDP-43):一种在肌萎缩侧索硬化症(ALS)中经常发生错误折叠并参与蛋白质聚集形成的蛋白质。
肌萎缩侧索硬化症(ALS):一种进行性神经退行性疾病,会逐渐影响大脑和脊髓的运动神经元。
¶ 引言
在过去十年中,脑网络结构和功能在进行性神经退行性疾病中的作用受到了越来越多的关注。尽管不同的神经退行性疾病起源于中枢神经系统的不同解剖区域,并选择性地影响某些脆弱的神经元群体,但功能连接似乎存在共同的变化模式。这些模式包括症状前阶段的早期代偿性变化,随着疾病的进展,这些变化会以越来越有害的方式失效(Gregory等人,2017年)。即使在微观层面或细胞层面,错误折叠的蛋白质和聚集体的形成也几乎是普遍存在的特征,尽管所涉及的特定蛋白质可能不同,例如肌萎缩侧索硬化症(ALS)中的TAR DNA结合蛋白43(TDP-43)(Peng、Trojanowski和Lee,2020年)。蛋白病是神经退行性疾病几乎普遍存在的特征,以前被认为是某些疾病所特有的蛋白质似乎以相互作用的方式彼此影响(Zhang、Kedia和Klenerman,2025年)。事实上,已发现在多种神经退行性疾病中,TDP-43会发生错误折叠、错误定位、聚集和扩散(Jo等人,2020年;Liao、Ma和Dou,2022年)。了解这些共同的机制和反应可能有助于实现早期检测、广泛的预防策略和更好的治疗。
神经网络对其结构和功能特征进行组织,以在平衡代谢需求和解剖学限制的同时,实现高计算能力,这一点可以通过图论来描述(Bullmore 和 Sporns,2009,2012)。我们此前已指出,功能良好的神经系统通过形成高效计算的几个标志来实现这种平衡,包括无标度性、小世界拓扑结构和模块化组织(Heiney 等人,2021)。这种组织方式有助于信息处理的局部专业化和全局整合,其中全局整合由一组相互连接的高度数枢纽节点(称为“富俱乐部”)介导(Bullmore 和 Sporns,2012;Griffa 和 Van den Heuvel,2018)。在中尺度回路水平和宏观全脑水平上,维持这些特性对于保持网络功能至关重要,而其破坏可能导致功能丧失,这在创伤性脑损伤和神经退行性疾病中均可见到。
受进行性神经退行性疾病影响的神经网络会启动多种过程来维持网络功能,包括放电模式的改变(Bullmore & Sporns, 2009;Gunes 等人, 2022;Pardillo-Díaz 等人, 2022)以及结构和功能连接的变化(Pievani 等人, 2014),其中许多变化发生在临床症状出现之前。Hillary 等人提出的一个颇具前景的模型认为,早期的结构退化会导致活动增强和功能超连接,这是一种短期的适应性反应(Hillary & Grafman, 2017;Hillary 等人, 2015)。从长期来看,这些变化往往会使网络更加集中化,依赖核心节点组成的“富俱乐部”来承担越来越大比例的信息传递工作(Hillary 等人, 2014)。虽然这些变化可能有助于维持功能,但它们也会对网络中的一小部分节点提出越来越高的要求,这些节点面临着不断增加的代谢需求,从而变得越来越容易出现故障(Stam, 2024)。除了这种功能网络的重构外,网络还可能启动其他由退化引发的反应,包括增强神经突生长(Saad、Segal 和 Ayali, 2015),这可能在一段时间内有助于维持网络功能。在肌萎缩侧索硬化症(ALS)中,研究还表明,结构网络疾病的中心区域中,与代谢过程相关的基因表达发生了改变,包括 ATP 生成和线粒体功能(Farahani 等人, 2025)。来自脑代谢网络的研究结果进一步表明,网络组织偏离最佳状态与临床结果相关(Jin 等人, 2025)。功能研究还显示,ALS 脑网络中具有单一连接的节点比例增加,这表明局部连接有所丧失。同时,连接度差异的增大表明,网络对集中式节点的依赖程度不断上升,以促进相互连接(Borgheai 等人, 2020;Sorrentino 等人, 2018)。
自组织的体外神经网络能够模拟大脑中神经元和神经网络的行为(Poli、Pastore和Massobrio,2015年;Schroeter等人,2015年;Shein-Idelson、Ben-Jacob和Hanein,2011年)。在没有行为和认知症状的情况下,图论可以确定与高计算能力相符的网络特征(Heiney等人,2021年)。通过将这些方法与先进的神经工程学和电生理学相结合,我们还证明,有可能探测由选择性诱导的扰动引起的微观和中观尺度动态神经网络重构(Weir等人,2023年),包括神经退行性病变(Valderhaug等人,2020年、2021年)。
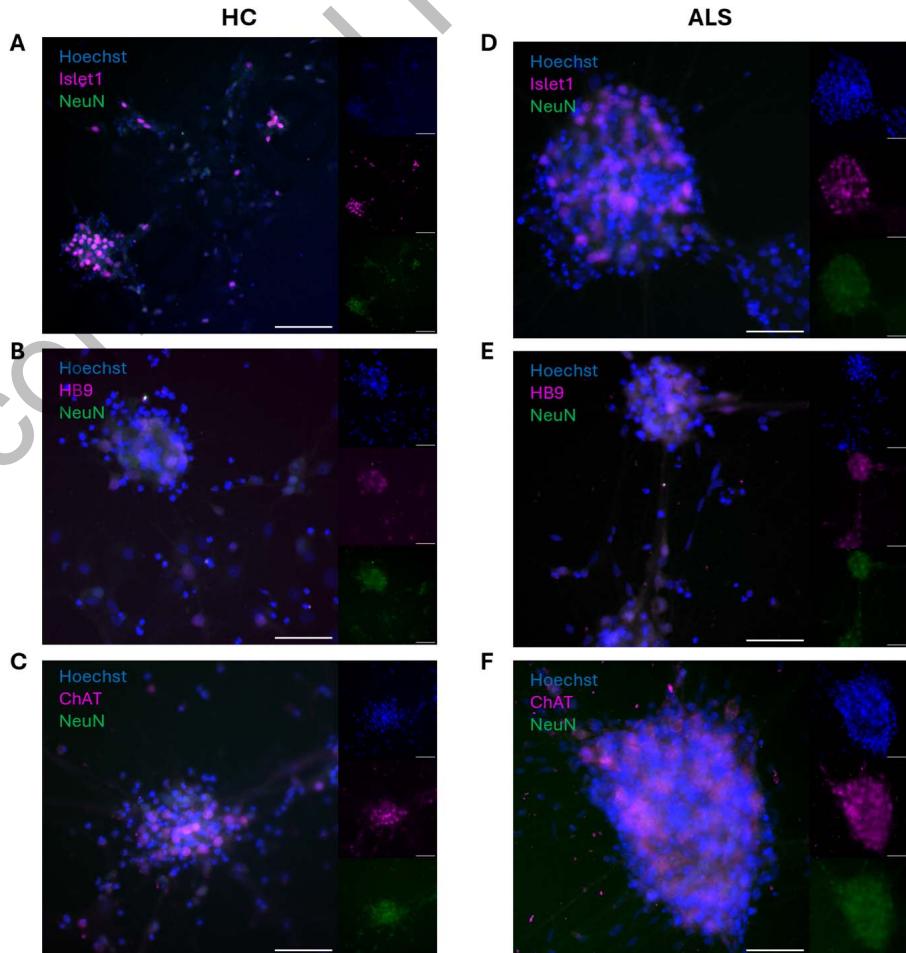
图1. ICC确认运动神经元(MN)细胞特性。健康对照(HC)和肌萎缩侧索硬化症(ALS)患者来源的运动神经元网络均表达运动神经元特异性标志物Islet1(A和D)、HB9(B和E)和ChAT(C和F),同时也表达泛神经元标志物NeuN。比例尺=100μm。
C9orf72:一种易发生扩增突变的基因,该突变会使携带者易患肌萎缩侧索硬化症(ALS)。
多电极阵列(MEAs):带有多个电极的细胞培养容器,用于细胞外电生理记录。
免疫细胞化学(ICC):一种基于抗体的技术,用于对细胞成分进行荧光标记。
在本研究中,我们对比了健康对照组运动神经元(HC MNs),研究了携带C9orf72基因内源性扩增突变的人类肌萎缩侧索硬化症(ALS)患者诱导多能干细胞(iPSC)衍生运动神经元(ALS MNs)的微观和中观尺度动态。我们通过多电极阵列(MEAs)对细胞外电生理学进行复杂网络分析,表征了其结构网络特性,评估了TDP-43蛋白病,并纵向评估了其功能连接性。我们提供了活动变化的证据,且首次证明ALS患者脑网络的内源性连接变化可在体外工程化神经网络中重现,并且这些代偿性特征会使网络走向更脆弱的状态。
¶ 结果
¶ ALS运动神经元表现出内源性TDP-43蛋白病
运动神经元(HC)和肌萎缩侧索硬化症(ALS)运动神经元网络的免疫细胞化学(ICC)证实,运动神经元标志物Islet1、HB9和ChAT以及泛神经元标志物NeuN均有表达,如图1所示。
为了评估ALS运动神经元网络是否存在TDP-43错误定位和蛋白病的迹象,我们对细胞质和细胞核组分进行了分离,通过蛋白质印迹法检测了健康对照(HC)和ALS运动神经元网络中亚细胞位置的TDP-43蛋白水平。如图2A所示,与健康对照运动神经元网络相比,ALS运动神经元网络中细胞质与细胞核TDP-43的比例增加了7.415倍。此外,如图2B所示,对细胞质中TDP-43阳性蛋白包涵体的免疫细胞化学标记显示,与健康对照运动神经元网络相比,ALS运动神经元网络中的聚集物数量显著增加(z值=-9.6858,p=3.47×10⁻²²)。
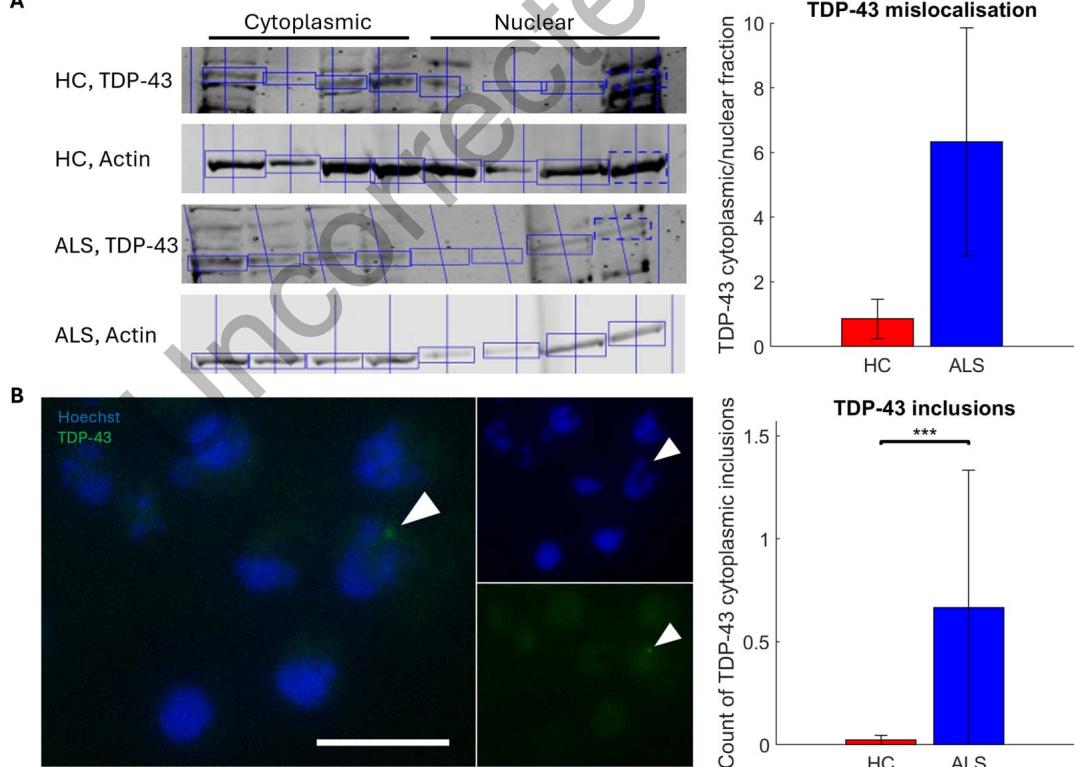
图2. 肌萎缩侧索硬化症运动神经元网络表现出TDP-43蛋白病。TDP-43水平的蛋白质印迹分析显示,与健康对照者相比,肌萎缩侧索硬化症运动神经元网络的细胞质与细胞核蛋白比率增加了7.415倍,健康对照者和肌萎缩侧索硬化症患者的样本量均为4(A)。白色箭头突出显示了肌萎缩侧索硬化症运动神经元中核外(蓝色)积累的TDP-43(绿色)包涵体(B)。比例尺=25μm。与健康对照者运动神经元网络相比,肌萎缩侧索硬化症运动神经元网络中非核TDP-43包涵体的数量显著增加(以细胞核计数为标准化)(p=3.47×10−22),健康对照者样本量=419,肌萎缩侧索硬化症样本量=463。:p<0.05,:p<0.01,:p<0.001。
¶ 肌萎缩侧索硬化运动神经元网络存在微观功能障碍和中观代偿
图3和图4展示了来自高密度多电极阵列(HD-MEAs)和每个包含64个记录电极的六孔MEA(多孔MEA)的MN网络活动,左侧为每次测量的纵向中位数和中位数绝对偏差,右侧为广义线性混合模型(GLMM)估计的组平均值(带有95%置信区间(CI))及统计比较。单个数据点详见支持信息图S1和S2。
体外培养天数(DIV):指的是体外培养中神经元网络建立后的天数。
从体外培养第30天到第46天,每隔一天记录一次高密度微电极阵列(HD-MEAs)中的运动神经元网络活动,每个网络共进行9次重复测量,结果如图3所示。高密度微电极阵列记录的活动的广义线性混合模型(GLMM)结果汇总于表5,更多模型细节见补充信息表S3。如图3A所示,与健康对照(HC)运动神经元网络相比,肌萎缩侧索硬化症(ALS)运动神经元网络的中位放电率显著更高。同时,如图3B所示,与健康对照运动神经元网络相比,肌萎缩侧索硬化症运动神经元网络的尖峰振幅显著更低。健康对照和肌萎缩侧索硬化症网络均表现出与高计算能力网络相关的自发涌现特性。这包括相似水平的小世界性,如图3C所示,所有网络的小世界倾向均>0.6,以及相似程度的模块化,如图3D所示。如图3E所示,网络的节点度分布与幂律拟合非常吻合,这与健康对照和肌萎缩侧索硬化症运动神经元的无标度网络一致。然而,为了确认无标度性,有必要将度分布与其他合理分布进行比较(Broido & Clauset, 2019)。如补充信息图S3、补充信息表S1和补充信息表S2所示,健康对照和肌萎缩侧索硬化症运动神经元网络与幂律分布的拟合度均优于其他分布,表现为更高的调整后R²值。不过,幂律分布和指数分布的拟合优度在统计学上无法区分(p>0.05)。健康对照和肌萎缩侧索硬化症运动神经元网络之间的幂律指数没有显著差异(p=0.281,数据未显示)。个体度分布见补充信息图S4。这些特征与Heiney等人(2021)所述的高计算能力一致。最后,值得注意的是,如图3F所示,与健康对照运动神经元网络相比,肌萎缩侧索硬化症运动神经元网络的富俱乐部系数显著更高。这些特征表明存在中尺度补偿,即通过增加对高度互连节点子集的依赖来维持网络的计算能力。
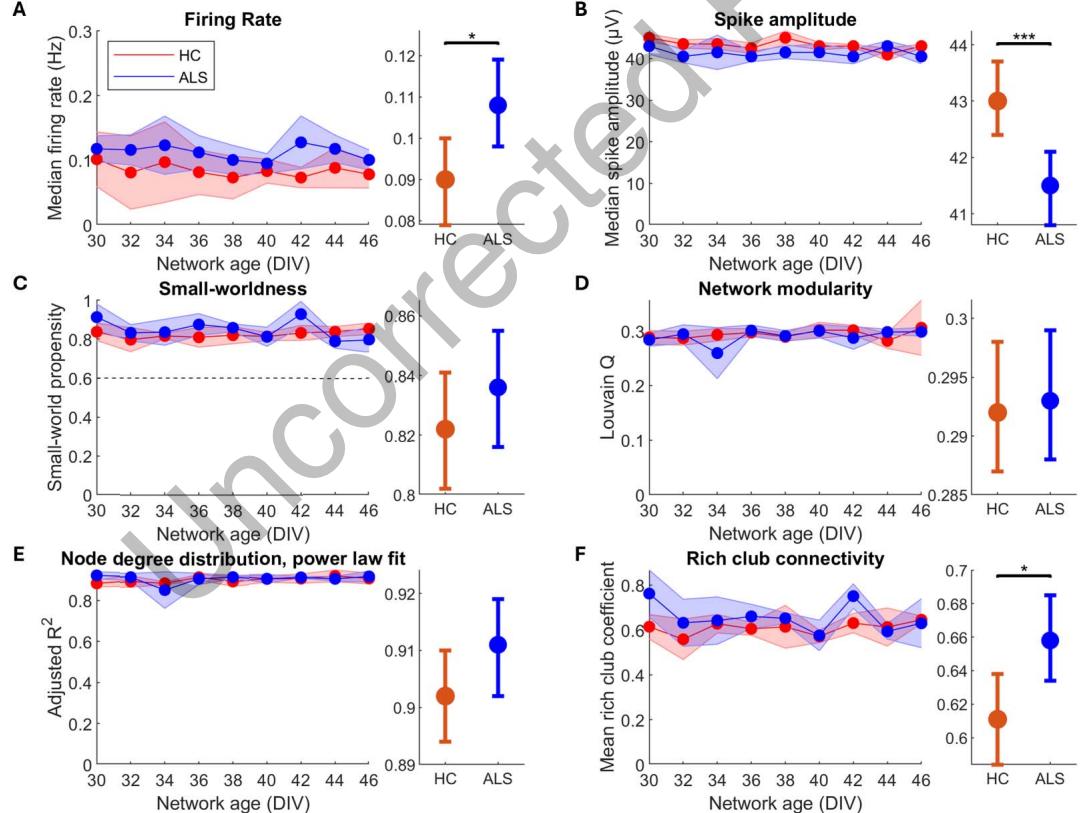
图3. 肌萎缩侧索硬化症患者来源的运动神经元和健康运动神经元在高密度微电极阵列上自组织成具有高计算能力特征的网络。在30-46天体外培养期间,每个网络进行9次高密度微电极阵列记录(健康对照组和肌萎缩侧索硬化症组均n=4),A-F左侧通过广义线性混合模型对健康对照组和肌萎缩侧索硬化症组进行比较,A-F右侧为比较结果。与健康对照组相比,肌萎缩侧索硬化症运动神经元网络具有更高的放电率(A,p=0.0140)、更低的峰电位振幅(B,p=1.09×10⁻⁴)、相似的小世界倾向(C,p=0.315)、相似的模块化程度(D,p=0.831)、相似的符合幂律分布的度分布(与无标度网络一致,E,p=4.11×10⁻³)以及更高的平均富俱乐部系数(F,p=0.0180)。C-E中所示特征的相似性表明,健康和肌萎缩侧索硬化症运动神经元网络均自组织成具有高计算能力的网络。左侧图显示纵向中位数,阴影区域表示中位数绝对偏差。右侧图显示广义线性混合模型估计的组平均值及95%置信区间。:p≤0.05,:p<0.01,:p<0.001。
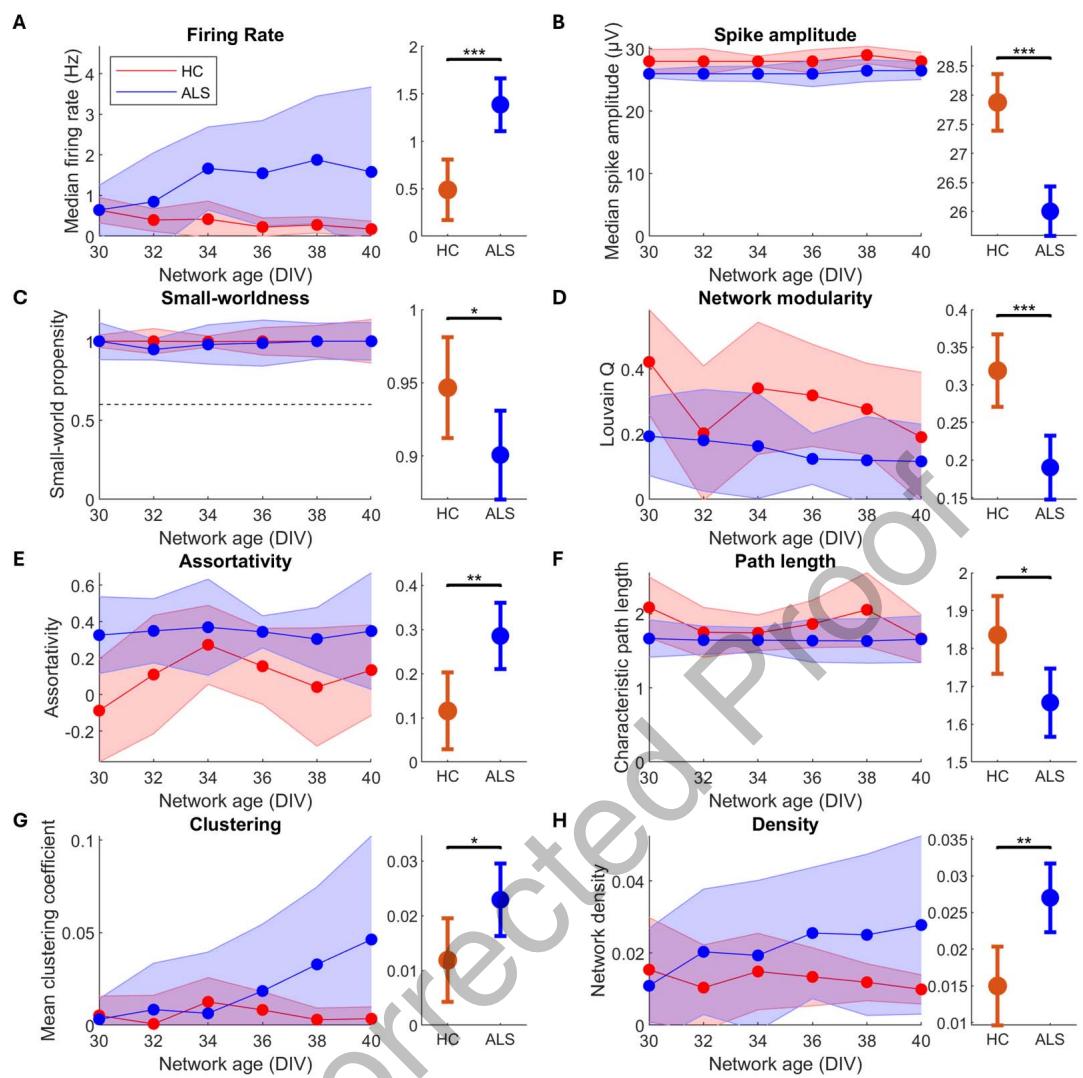
图4. 肌萎缩侧索硬化症(ALS)患者来源的运动神经元(MNs)在多通道微电极阵列(MEAs)上自组织形成的网络与健康对照(HCs)相比存在显著差异。在30-40天体外培养(DIV)期间,每个网络进行6次多通道微电极阵列记录(健康对照组n=9,ALS组n=12),左侧A-H通过广义线性混合模型(GLMM)对健康对照组和ALS组进行比较,右侧A-H为比较结果。与健康对照组相比,ALS运动神经元网络具有更高的放电率(A,p=5.01×10⁻⁵)、更低的尖峰振幅(B,p=8.07×10⁻⁴)、更低的小世界倾向(C,p=0.0498)、降低的模块化程度(D,p=1.21×10⁻⁴)、更高的 assortativity(E,p=4.11×10⁻³)、更短的特征路径长度(F,p=0.0111)、更高的聚类系数(G,p=0.0324)以及更高的密度(H,p=1.07×10⁻³)。左侧图表显示纵向中位数,阴影区域表示中位数绝对偏差。右侧图表显示广义线性混合模型估计的组平均值及95%置信区间(CIs)。:p≤0.05,:p<0.01,:p<0.001。
从第30天到第40天(DIV),每隔一天记录多孔微电极阵列(MEA)的运动神经元(MN)网络活动,每个网络共进行6次重复测量,结果如图4所示。多孔MEA的广义线性混合模型(GLMM)结果汇总于表6,更多模型细节见支持信息表S4。与高密度微电极阵列(HD-MEA)的结果相似,肌萎缩侧索硬化症(ALS)运动神经元网络的中位放电率显著高于健康对照(HC)运动神经元网络,表明其网络存在过度活跃,且尖峰振幅显著降低,如图4B所示。此外,与健康对照运动神经元网络相比,肌萎缩侧索硬化症运动神经元网络的小世界倾向和模块化程度显著降低,如图4C和4D所示,这表明与疾病相关的计算能力下降。而且,我们发现肌萎缩侧索硬化症运动神经元网络的 assortativity 显著高于健康对照运动神经元网络,路径长度显著缩短,聚类显著增加,如图4E、4F和4G所示。最后,与健康对照运动神经元网络相比,肌萎缩侧索硬化症运动神经元网络的密度显著更高,如图4H所示。
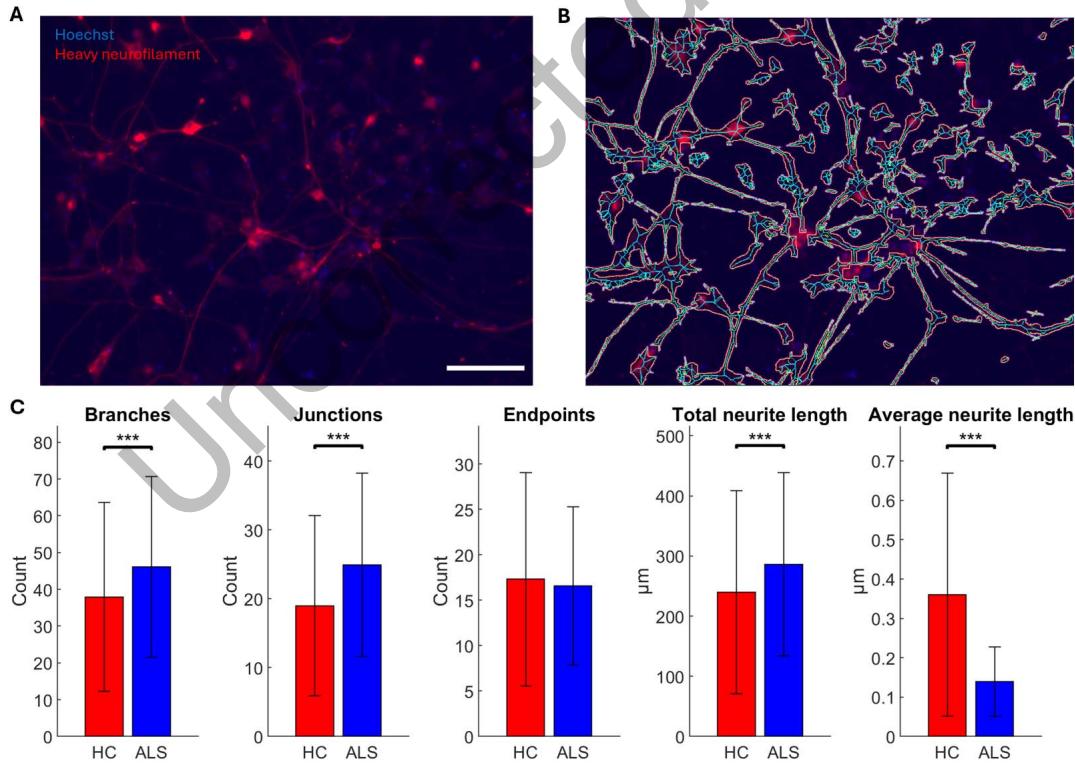
图5. 与健康对照(HCs)相比,肌萎缩侧索硬化症(ALS)运动神经元(MN)网络存在广泛的结构缺陷。通过重神经丝的ICC标记和核Hoechst染色评估运动神经元网络结构(A),使用Fiji/ImageJ的NeuroConnectivity插件(Pani等人,2014)自动识别神经突和细胞核(B)。通过核计数归一化的结构特征量化(C)显示,ALS运动神经元网络的神经突分支(p = 6.45 × 10⁻⁷)和连接点(p = 2.29 × 10⁻⁸)显著多于HC运动神经元网络。同时,ALS运动神经元网络的总神经突长度显著更长(p = 1.03 × 10⁻⁴),而平均神经突长度显著短于HC运动神经元网络(p = 1.87 × 10⁻¹³)。神经突端点数量无显著差异(p = 0.0241)。HC样本量=420,ALS样本量=558。:p < 0.01,:p < 0.002,:p < 0.0002。比例尺=100μm。
¶ ALS运动神经元网络表现出更短神经突的过度生长
我们通过免疫标记的重神经丝和Hoechst标记的细胞核来评估运动神经元(MN)网络的结构特征,以确定肌萎缩侧索硬化症(ALS)运动神经元网络是否偏离健康对照(HC)运动神经元网络。如图5C所示,与健康对照运动神经元网络相比,肌萎缩侧索硬化症运动神经元网络的神经突分支(z值=-4.977,p=6.45×10⁻⁷)和连接点(z值=-5.589,p=2.29×10⁻⁸)显著更多,总神经突长度也显著更长(z值=-3.884,p=1.03×10⁻⁴),而平均神经突长度则显著更短(z值=7.358,p=1.87×10⁻¹³)。两组之间的神经突端点数量没有显著差异(z值=-2.256,p=0.0241)。
¶ 讨论
在本研究中,我们首次证实,来自确诊神经退行性疾病患者的诱导多能干细胞(iPSC)衍生神经网络在功能连接方面存在内源性病理变化。与健康对照(HC)运动神经元相比,在高密度微电极阵列(HD-MEAs)和多孔微电极阵列(multiwell MEAs)中,肌萎缩侧索硬化症(ALS)运动神经元均表现出微观功能障碍,包括图3A和图4A所示的过度活跃,以及图3B和图4B所示的锋电位振幅降低。神经元过度兴奋是ALS(Ronchi等人,2021年;Sommer等人,2022年;Wainger等人,2014年)和其他神经退行性疾病(Chen、Chehade和Chu,2025年;Pardillo-Díaz等人,2022年;Targa Dias Anastacio、Matosin和Ooi,2022年)中广泛报道的特征。此外,图3B和图4B显示ALS运动神经元网络中显著降低的锋电位振幅,与先前在ALS患者衍生的运动神经元网络中的观察结果一致(Sommer等人,2022年)。锋电位振幅降低会减少钙离子(Ca²⁺)内流(Scarnati等人,2020年),这可能是ALS运动神经元网络为最大限度减少钙离子诱导的兴奋性毒性和氧化应激而产生的一种适应性变化。然而,这也会减少释放的神经递质数量(Scarnati等人,2020年),并可能导致网络功能紊乱。总体而言,在微观层面上,我们发现ALS运动神经元网络会产生更多但更强弱的锋电位,这与更高的代谢成本和氧化应激增加相符。
复杂网络分析表明,肌萎缩侧索硬化症运动神经元网络与健康对照网络存在多种偏差,这些偏差表明存在中尺度补偿,包括图3F所示的富人俱乐部系数增加和图4E所示的 assortativity 增加。这表明肌萎缩侧索硬化症运动神经元网络变得更加集中,尤其是枢纽节点之间的互联性更强,导致网络更脆弱。当局部连接受损时(无论是节点丢失,还是如我们研究中所见的尖峰振幅降低导致的信号保真度下降),网络会通过重组其功能连接来适应。由于高度枢纽节点具有高连接性和高活性,它们在概率上更易参与这些适应过程,因此导致通过枢纽的信息路由量增加(Hillary 等人,2014;Roy 等人,2017)。在这种适应的早期阶段,或者如果网络损伤是急性的且需要有限的重新配置,这可能有利于维持网络通信(Hillary 和 Grafman,2017)。然而,这种重新配置会增加枢纽节点的代谢需求,而神经退行性疾病中出现的持续性网络损伤会给这些节点带来不断加剧的压力,这些节点本身已是网络中代谢成本最高的部分之一(Bullmore 和 Sporns,2012;van den Heuvel 等人,2012)。最终,这些节点会因这种负担而崩溃,由于网络的整体通信在很大程度上依赖于它们,没有它们,网络就无法维持其功能(Stam,2014)。虽然在创伤性脑损伤和阿尔茨海默病病例中已发现支持这种损伤和补偿模式的证据(Hillary 等人,2015),但到目前为止,在肌萎缩侧索硬化症病理中,这方面的证据还很有限。
Sorrentino等人先前的研究表明,随着疾病的进展,肌萎缩侧索硬化症(ALS)患者的大脑网络会变得更加集中(Sorrentino等人,2018年)。我们进一步发现,在高密度微电极阵列(HD-MEAs)上,ALS运动神经元(MN)网络中的富人俱乐部连接性增强。我们在多孔微电极阵列中发现的网络 assortativity 增加,进一步表明ALS运动神经元网络内的节点度层级结构更趋严格。这与ALS患者的脑电图(EEG)(Iyer等人,2015年)和功能性磁共振成像(fMRI)(Fekete等人,2013年)结果一致。具有更高 assortativity 的网络更有可能拥有高度互联的富人俱乐部(Rubinov和Sporns,2010年),这支持了我们在高密度微电极阵列网络中的发现,并为ALS运动神经元网络中集中化的病理动态提供了明确证据。
此外,我们发现肌萎缩侧索硬化症(ALS)中的网络密度增加,这表明通过建立新的连接可以产生维持网络功能的代偿性反应。虽然我们确实在多孔微电极阵列(MEAs)中发现ALS运动神经元(MN)网络的小世界性和模块化显著降低(如图4C-D所示),但这些发现在高密度微电极阵列(HD-MEAs)中并未重现(如图3C-D所示)。尽管如图4C所示,多孔微电极阵列上的ALS运动神经元网络的小世界性显著低于健康对照(HC)运动神经元网络,但这些网络的小世界倾向仍>0.6,这表明两组都表现出小世界特征(Muldoon、Bridgeford和Bassett,2016)。高密度微电极阵列和多孔微电极阵列在模块化结果上的差异可能是由于空间采样的不同,已有研究表明空间采样会影响局部和网络特性的测量(Maccione等人,2010)。本研究中使用的微电极阵列模型在电极尺寸上也存在差异,这些不同的空间分辨率可能进一步导致了所观察到的最大模块化差异(Sporns和Betzel,2016)。不同微电极阵列平台上观察到的差异可能表明,ALS模块更小且更分散,因此在具有更高空间分辨率的高密度微电极阵列中更容易被检测到,从而获得更高的最大模块化分数。这与ALS的脑成像研究结果一致(Renga,2022)。此外,我们在高密度微电极阵列网络的度分布中没有观察到任何差异(如图3E所示)。综上所述,这些与健康对照运动神经元网络的差异以及不存在的差异表明,ALS运动神经元网络处于代偿性重构状态,其中适应性机制似乎维持了网络功能,而潜在病理仅产生了轻微的有害影响。因此,我们的结果为ALS早期功能网络变化提供了新的发现。
我们通过两种不同的方法在肌萎缩侧索硬化症(ALS)运动神经元(MN)网络中证实了TDP-43蛋白病的明显迹象。对细胞核和细胞质组分进行分离后,蛋白质印迹分析发现细胞质与细胞核中TDP-43的比例增加了7.415倍,如图2A所示。TDP-43的免疫细胞化学(ICC)标记也发现了显著更多的核外TDP-43包涵体,如图2B所示。TDP-43的细胞质包涵体是ALS和额颞叶痴呆中运动神经元细胞病理学最普遍的迹象之一(Arai等人,2006年;Neumann等人,2006年),并且会因氧化应激增加、抗氧化能力降低和线粒体功能障碍而加重(Kara等人,2023年)。大量证据表明,受ALS影响的运动神经元处于氧化应激升高的状态(Cunha-Oliveira等人,2020年),而加剧这种情况的环境因素可能会增加发病风险并加重病理(D’Amico等人,2013年)。综合来看,这些发现清楚地证实了TDP-43蛋白病和细胞病理学迹象,表明ALS运动神经元网络存在氧化应激升高和代谢成本增加的情况。
结构分析发现,ALS运动神经元表现出神经突生长增加,但长程连接成比例减少,如图5C所示。这些变化支持了我们的功能研究结果,表明在神经退行性病变过程中网络在不断重新配置。事实上,这些结构变化可能解释了我们在多井微电极阵列(MEA)研究中发现的路径长度减少和聚类增加(如图4F-G所示),尽管小世界属性有所降低(如图4C所示)。由于小世界属性与短路径长度和高聚类相关(Muldoon、Bridgeford和Bassett,2016),这些发现似乎相互矛盾。然而,考虑到我们发现神经突密度增加、整体神经突长度缩短,以及功能密度增加,大量的短程连接可能使组平均路径长度和聚类出现偏差。值得注意的是,与小世界指数不同,小世界倾向考虑了密度等属性(Muldoon、Bridgeford和Bassett,2016),使我们能够捕捉到这种看似违反直觉的网络动态。已有研究表明,在急性损伤和慢性疾病中,功能连接性增加(至少部分由 spike 活动增加引起)是对结构网络损伤的一种代偿反应,这可能导致更高的聚类和更短的路径长度(Aswendt和Hoehn,2023)。然而,研究发现,过度活跃、过度连接和蛋白病变之间存在相互关联,上述代偿反应可能导致代谢需求增加、氧化应激、 hub 过载,并最终导致网络衰竭(Hillary和Grafman,2017)。
在此,我们研究了C9orf72基因内源性扩增的肌萎缩侧索硬化症运动神经元,这与CRISPR诱导的遗传易感性或错误折叠蛋白种子诱导的病理不同。未来的研究应检查来自具有各种遗传易感性的肌萎缩侧索硬化症患者、散发性肌萎缩侧索硬化症患者以及具有肌萎缩侧索硬化症相关突变的无症状供体的运动神经元网络,以评估我们的发现是否是肌萎缩侧索硬化症的普遍趋势或特定患者群体的特征。此外,由于包括表观遗传印记在内的其他因素,具有相同遗传易感性的患者可能不会具有相同的网络特征。在这种情况下,基于诱导多能干细胞的网络模型结合复杂网络分析,以及通过绕过干细胞阶段保留表观遗传特征的细胞重编程开发的网络模型,有助于个性化医疗评估(Okano & Morimoto, 2022)。最后,本文中使用的方法和原理可应用于模拟和评估其他神经退行性疾病中的网络功能障碍,并揭示神经网络动态的哪些特征(如果有的话)可能为多种病理所共有。
总之,在本研究中,我们首次表明,源自确诊神经退行性疾病患者的体外神经网络会出现内源性功能网络变化,这些变化反映了体内多种病理状态下观察到的变化。我们提供了明确的证据,证明肌萎缩侧索硬化症运动神经元网络中存在微观尺度的功能障碍和中观尺度的代偿机制,包括网络集中化程度增加的新证据。肌萎缩侧索硬化症网络还表现出细胞质TDP-43蛋白比例升高以及细胞质TDP-43包涵体水平更高,这表明此类网络中存在肌萎缩侧索硬化症常见的病理特征。在微观尺度上,尽管信号传导更弱、更不稳定,肌萎缩侧索硬化症网络仍表现出过度活跃。在中观尺度上,网络在“富俱乐部”内表现出更高的 assortativity 和连接性,表明在持续的网络损伤情况下集中化程度增加,这一点在其他神经退行性疾病中已得到证实,但此前在肌萎缩侧索硬化症中尚未得到明确证明。综上所述,我们的研究结果提供了新的证据,表明肌萎缩侧索硬化症运动神经元网络具有典型的肌萎缩侧索硬化症细胞病理学特征,并能自组织成具有计算能力的网络,但存在代偿性过度活跃和集中化程度增加的情况。
¶ 方法
¶ 实验设计与统计分析
人类诱导多能干细胞(iPSCs)来自一名健康供体(女性,49岁,FA0000011,RUCDR Infinite Biologics和Target ALS)和一名确诊为肌萎缩侧索硬化症(ALS)且存在C9orf72扩增突变的患者供体(女性,64岁,FA0000003,RUCDR Infinite Biologics和Target ALS),两者均采用仙台病毒诱导多能干细胞重编程方法进行重编程。根据Nijssen等人(Nijssen, Aguila, & Hedlund, 2019)的方案,对诱导多能干细胞进行培养并分化为运动神经元(MNs),具体参照关于人类诱导多能干细胞分化为运动神经元的“步骤E”部分,不同之处在于整个类胚体阶段均使用轨道摇床。不同阶段的细胞培养基成分如表1所示。在运动神经元分化方案开始后的第10天接种细胞。每个高密度微电极阵列(HD-MEA)(健康对照和ALS组各4个)接种80,000个活细胞,多孔微电极阵列的每个孔接种100,000个活细胞(健康对照组9个,ALS组12个),六孔板的每个孔接种800,000个运动神经元(健康对照和ALS组各4个),八孔室载玻片的每个孔接种40,000个活细胞。
为了比较健康对照(HC)和肌萎缩侧索硬化症(ALS)运动神经元网络中非核TDP-43包涵体的数量及网络结构参数,我们对每组8个独立网络中20%的样本进行了免疫标记的TDP-43、重神经丝和Hoechst核染色成像(两组均为720张图像)。在对TDP-43包涵体进行量化前,我们剔除了未识别出细胞核或TDP-43包涵体的图像,并将每张图像的TDP-43包涵体计数归一化为细胞核计数(最终健康对照组为419张图像,ALS组为463张图像)。在对网络结构参数进行量化前,我们剔除了未识别出细胞核的图像,并将每张图像的结构参数归一化为细胞核计数(最终健康对照组为420张图像,ALS组为558张图像)。通过柯尔莫哥洛夫-斯米尔诺夫检验对健康对照组和ALS组的非核TDP-43包涵体水平及网络结构参数的数据点分布进行正态性检验,结果显示其不服从正态分布(使用MATLAB R2024a,Mathworks软件)。因此,采用威尔科克森秩和检验(使用MATLAB R2024a,Mathworks软件)评估组间差异,并通过邦费罗尼校正进行多重比较。
表1. 运动神经元分化过程中的细胞培养基成分
| 试剂名称 | Days 1–2 | Days 3–9 | Day 10 | Days 11–12 | Day 13+ | Supplier | Product # |
|---|---|---|---|---|---|---|---|
| DMEM/F12-GlutaMax | 0,5 | 0,5 | Thermo Fisher | 31331028 | |||
| Neurobasal | 0,5 | 0,5 | 1 | 1 | 1 | Thermo Fisher | 21103049 |
| N2 | 0.5X | 0.5X | Fisher Scientific | 12013479 | |||
| B27 | 0.5X | 0.5X | 1X | 1X | 1X | Thermo Fisher | 17504044 |
| Penicillin/Streptomycin | 1X | 1X | 1X | 1X | 1X | Merck | P4333 |
| Y-27632 | 5 μM | 5 μM | Tocris | 6053 | |||
| SB-431542 | 40 μM | Tocris | 1614 | ||||
| LDN-193189 | 200 nM | Tocris | 6053 | ||||
| CHIR-99021 | 3 μM | Tocris | 4423 | ||||
| Retinoic acid | 200 nM | 200 nM | Sigma-Aldrich | R2625 | |||
| SAG | 500 nM | Tocris | 4366 | ||||
| Ascorbic acid | 200 μM | 200 μM | 200 μM | 200 μM | 200 μM | Sigma-Aldrich | A4403 |
| DAPT | 10 μM | 10 μM | Tocris | 2634 | |||
| GDNF | 10 ng/mL | 10 ng/mL | 10 ng/mL | Peprotech | 450-10 | ||
| BDNF | 10 ng/mL | 10 ng/mL | 10 ng/mL | Peprotech | 450-02 |
所有细胞培养基成分均根据Nijssen等人(Nijssen, Aguila, & Hedlund, 2019)的方法获取,并且在由指定比例的DMEM/F12-GlutaMax和Neurobasal混合而成的基础培养基中添加了补充剂。
使用IBM SPSS Statistics(版本29.0.0.0)通过广义线性混合模型(GLMMs)比较了健康对照(HC)和肌萎缩侧索硬化症(ALS)运动神经元网络纵向电生理活动的差异。这些模型将基因型(健康对照或肌萎缩侧索硬化症)作为固定效应,以各种网络特征为目标,利用线性模型对每个网络进行重复测量(作为模型的研究对象)。
¶ 电生理记录
我们研究了MN网络随时间的变化,既使用了具有4096个记录电极的高密度微电极阵列(3Brain Arena),也使用了多孔微电极阵列(Axion Biosystems M384-tMEA-6B)。对于多孔微电极阵列,使用Axion Maestro Pro采集工具和AxIS Navigator软件(3.12.2.2版本)记录网络电生理活动。每次记录在37°C和5% CO₂的环境下持续30分钟,采样率为12.5 kHz。开始记录前,多孔微电极阵列需静置15分钟。所有网络的活动从第30天到第40天每隔一天记录一次。对于高密度微电极阵列,使用Biocam Duplex系统(3Brain)和BrainWave 5记录网络电生理活动。每次记录在37°C下持续15分钟,采样率为18857.72 Hz。开始记录前,高密度微电极阵列需静置5分钟。所有网络的活动从第30天到第46天每隔一天记录一次。
¶ 免疫细胞化学
采用免疫细胞化学(ICC)来确认诱导多能干细胞(iPSCs)分化和成熟后的运动神经元(MN)身份,评估网络结构,并研究TDP43胞质内包涵体的存在情况。该方法基于Richter等人(2018年)的研究。移除细胞培养基,将细胞网络在3%乙二醛溶液中固定15分钟,该溶液由70.1%的超纯水(MQ H₂O)、19.7%的乙醇(Kemetyl 200-578-6)、7.8%的乙二醛(40%重量百分比的水溶液,Sigma Aldrich 128465)和0.75%的乙酸(Merck 1.00063)组成。然后,用PBS(D8662,Merck)洗涤细胞网络四次。接着,用含0.5% Triton-X(T8787,Merck)的PBS对细胞进行透化处理,持续5分钟。之后,用PBS洗涤细胞网络三次,随后加入含5%山羊血清(PCN5000,Fisher Scientific)的PBS封闭液,在室温下于 orbital shaker 上以30 rpm的速度振荡1小时。吸去封闭液后,加入含5%山羊血清的PBS稀释的一抗,在4°C的摇床上孵育过夜。次日,移除一抗,用PBS洗涤细胞网络四次。然后加入含5%山羊血清的PBS稀释的二抗,在 orbital shaker 上以30 rpm的速度振荡3小时,之后进行10分钟的核染色。随后,用PBS洗涤细胞网络四次,再用超纯水洗涤一次。每个洗涤步骤的持续时间均为5分钟。所有细胞网络均在42天体外培养(DIV)时固定。
对运动神经元网络中Islet-1(ab109517,1:250,Abcam)、Chat(ab178850,1:500,Abcam)、HB9(ab221884,1:200,Abcam)、NeuN(ab279295,1:500,Abcam)、重神经丝(ab4680,1:1000,Abcam)和TDP-43(PA5–27221,1:500,Fisher Scientific)的表达进行了检测,所有这些均使用相同的二抗(山羊抗小鼠,ab150113,1:500,Abcam;山羊抗兔,ab175471,1:500,Abcam;山羊抗鸡,ab150171,1:500,Abcam)进行可视化,并进行Hoechst染色(62249,1:2000,Fisher Scientific)。所有图像均使用EVOS M7000显微镜获取,所用的光学滤块如下:DAPI(AMEP4650)、CY5(AMEP4656)、GFP(AMEP4651)和TxRed(AMEP4655),以及Olympus UPLSAP020x镜头(20倍/0.75数值孔径,N1480500)。
表2. 神经连接参数。
| 细胞核参数 | 神经突参数 |
|---|---|
| 分割方法:阈值法 | 启用对比度增强 |
| 预处理: | 启用中值滤波 |
| ・启用背景扣除 | 中值滤波尺度:2 |
| ・启用局部对比度增强 | 管状结构增强尺度:2 |
| ・预处理方法:中值滤波 | 阈值设置: |
| ・滤波器尺寸:8 | ・精细固定阈值:40 |
| 阈值方法:固定阈值 | ・粗略固定阈值:55 |
| 固定阈值:50 | 对象筛选条件,碎片最小面积:400 μm² |
| 对象筛选条件: | 搜索区域: |
| ・最小圆度:0.00 | ・膨胀搜索区域:2像素 |
| ・最小面积:10 μm² | ・细胞核膨胀排除范围:15像素 |
| ・最大面积:500 μm² |
¶ 图像分析
使用Fiji/ImageJ的NeuroConnectivity插件(Pani等人,2014年),按照表2中的设置,对运动神经元网络的五项结构特性(神经突分支、连接点、端点、总长度和平均长度)以及细胞核的识别进行了评估。
我们使用CellProfiler 4.2.8版本来识别未与核标记共定位的TDP-43包涵体。首先,在识别物体之前,我们通过应用阈值,利用Hoechst标记来识别细胞核,所使用的设置如表3所示。
将阈值图像作为反向掩码应用于TDP-43标记,以分离核外TDP-43标记,然后应用阈值并使用表4中的设置识别目标。
¶ 细胞核与细胞质中TDP-43的分离
为了确定ALS患者来源的运动神经元(MNs)中TDP-43从细胞核错误定位到细胞质的程度,我们使用了赛默飞世尔科技的NE-PER核质提取试剂盒(赛默飞世尔科技78833)以及不含EDTA的赛默飞世尔科技Halt蛋白酶和磷酸酶抑制剂混合物(飞世尔科技10127963),操作遵循制造商的说明。简要步骤如下:每组取4个神经网络的细胞,用胰蛋白酶-EDTA(T4049,默克)从六孔板中收获,然后以500×g离心5分钟。将细胞沉淀重悬于PBS(D8662,默克)中洗涤,随后以500×g离心3分钟。移除PBS后,加入添加了蛋白酶和磷酸酶抑制剂的细胞质提取试剂1。将细胞在最高转速(3000转/分钟)下涡旋15秒,孵育10分钟后,加入细胞质提取试剂2。涡旋细胞5秒,孵育1分钟,然后以16000×g离心5分钟。收集含有细胞质提取物的上清液,再将剩余的细胞沉淀悬浮于添加了蛋白酶和磷酸酶抑制剂的核提取试剂中。每10分钟涡旋细胞15秒,持续40分钟,之后以16000×g离心10分钟。随后收集含有核提取物的上清液。所有离心操作均在4°C下进行,整个过程中所有样品、提取物、试剂、小瓶和移液枪吸头均置于冰上。提取物储存于-80°C,直至通过蛋白质印迹法进行分析,分析时使用TDP-43抗体(PA5-27221,1:1000,飞世尔科技),并以肌动蛋白水平为参照对蛋白质水平进行标准化。之后比较健康对照(HC)和ALS运动神经元网络中细胞质与细胞核TDP-43的比例。
表3. 用于细胞核检测的CellProfiler参数
| 阈值设置 | 初级对象识别(IdentifyPrimaryObjects) |
|---|---|
| 阈值策略:全局 | 使用高级设置:否 |
| 阈值方法:最小交叉熵 | 对象典型直径(像素单位):15–30 |
| 阈值平滑尺度:0.0 | 丢弃直径范围外的对象:是 |
| 阈值校正因子:1.15 | 丢弃接触图像边界的对象:是 |
| 阈值上下限:0.0–1.0 | |
| 阈值处理前对数转换:否 |
表4. 用于细胞质TDP-43包涵体检测的CellProfiler参数
| 阈值设置 | 初级对象识别(IdentifyPrimaryObjects) |
|---|---|
| 阈值策略:全局 | 使用高级设置:否 |
| 阈值方法:大津法(双分类) | 对象典型直径(像素单位):10–20 |
| 阈值平滑尺度:0.0 | |
| 阈值校正因子:2 | 丢弃直径范围外的对象:是 |
| 阈值上下限:0.0–1.0 | |
| 阈值处理前对数转换:否 | 丢弃接触图像边界的对象:否 |
¶ 数据分析
对于多井微电极阵列(MEA),原始数据使用200Hz的巴特沃斯高通滤波器和3kHz的巴特沃斯低通滤波器进行滤波。采用自适应阈值交叉法识别尖峰,阈值为6个标准差,尖峰前持续时间为0.84毫秒,尖峰后持续时间为2.16毫秒,同时设置4个电极的巧合发生阈值和80微秒的巧合事件窗口。网络放电率低于每分钟5次尖峰或活跃电极少于7个的井被排除在进一步分析之外,最终HC组有9个网络,ALS组有12个网络。中位放电率通过单个电极记录的尖峰数量除以总记录时间确定,然后取每个网络的中位数。为生成多井MEA网络的网络连接矩阵,先利用电极对的皮尔逊相关性生成加权图,在计算网络特征前,去除90%的最弱连接以删减无关连接。
对于高密度微电极阵列(HD-MEAs),健康状态和肌萎缩侧索硬化症(ALS)状态下的样本量均为4。原始数据采用5阶巴特沃斯高通滤波器进行滤波,以去除200Hz以下的低频噪声。采用精确定时 spike 检测算法(Maccione 等人,2009年)进行 spike 检测。阈值设为噪声标准差的8倍,峰值持续时间设为1.5毫秒,不应期设为1毫秒。滤波和 spike 检测在 BrainWave 5(3Brain)中进行。 中位发放率的计算方法为:单个电极记录到的 spike 数量除以总记录时间,然后取每个网络所有电极的中位数。为生成高密度微电极阵列记录的网络连接矩阵,将 spike 时间划分为100毫秒的时间窗。之后,识别分箱后 spike 时间的共现情况,得出不同电极上 spike 共现的次数。连接越强,共现的可能性越高。 为确定非虚假连接的阈值,通过打乱原始数据生成相应数据的随机序列。此过程重复10次,从连接矩阵中移除共现次数等于或低于打乱数据均值的连接。在这些连接中,进一步筛选出1%的最强连接,得到具有可比连接数量的二元连接矩阵。最后,使用常见的网络指标对其中的巨连通分量进行分析。
表5. 广义线性混合模型(GLMM)估计值和测试结果,高密度微电极阵列(HD-MEAs)
| 电生理指标 | 健康对照(HC)均值 | HC 95% 置信区间 | 肌萎缩侧索硬化症(ALS)均值 | ALS 95% 置信区间 | F统计量与自由度 | p值 |
|---|---|---|---|---|---|---|
| 放电频率 (Firing rate, Hz) | 0.09 | 0.079–0.1 | 0.108 | 0.098–0.119 | F(1, 70) = 6.384 | 0.0140 |
| 锋电位幅度 (Spike amplitude, μV) | 43.0 | 42.4–43.7 | 41.5 | 10.8–42.1 | F(1, 70) = 12.8 | 1.09 × 10⁻⁴ |
| 小世界倾向性 (Small-world propensity) | 0.822 | 0.802–0.841 | 0.836 | 0.816–0.855 | F(1, 70) = 1.023 | 0.315 |
| 模块化系数(Louvain Q值) | 0.292 | 0.287–0.298 | 0.293 | 0.288–0.299 | F(1, 70) = 0.046 | 0.831 |
| 度分布幂律拟合优度(R²) | 0.902 | 0.894–0.910 | 0.911 | 0.902–0.919 | F(1, 70) = 2.176 | 0.145 |
| 平均富俱乐部系数 (Mean rich club coefficient) | 0.611 | 0.584–0.638 | 0.658 | 0.631–0.685 | F(1, 70) = 5.874 | 0.0180 |
不同的连接性度量和阈值是根据多电极阵列(MEA)类型选择的,目的是在运动神经元(MN)网络中最佳识别稳健的功能连接。皮尔逊相关系数往往能识别出更多具有弱权重或中等权重的连接,这对于拥有多达64个节点的多孔板MEA网络来说是理想的,而共现法则对高权重连接的选择性更强。后者更适用于拥有多达4096个节点的高密度MEA(HD-MEA)数据,再加上对边缘权重采用严格的1%阈值,有助于消除虚假连接。
所有图论分析均使用脑连接工具箱(Rubinov & Sporns, 2010)进行。正如Muldoon、Bridgeford和Bassett(2016)所描述的,小世界倾向用于评估每个网络符合小世界原则(即高聚类性和低平均路径长度)的程度。小世界倾向高于0.6的网络被视为小世界网络。平均富俱乐部系数用于衡量高度数节点相互连接的趋势(McAuley、da Fontoura Costa & Caetano, 2007)。 assortativity是衡量相连网络节点度数相关性的指标,而网络密度是网络中实际存在的边与可能存在的边的比例。社区检测使用CDlib(Rossetti、Milli & Cazabet, 2019)进行,模块化评估则根据Clauset、Newman和Moore(2004)的方法,使用NetworkX(Hagberg等, 2008)进行。简单来说,社区检测采用Louvain算法,该算法能识别出相互之间连接比与网络其他部分更紧密的节点集群,从而将节点划分为不同的社区。模块化指标用于量化该算法将节点划分到这些社区的效果(Blondel等, 2008)。分别使用Matlab的fit函数(fitType = ‘power1’、‘exp1’、‘weibull’)以及应用于度分布对数的fitlm函数,来评估节点度分布是否分别遵循幂律分布、指数分布、威布尔分布或对数正态分布(Matlab 2024a, MathWorks)(Broido & Clauset, 2019)。通过调整后的R²评估这些分布的拟合优度,并使用IBM SPSS Statistics(版本29.0.0.0),通过重复测量方差分析以及事后的组间比较(采用Bonferroni校正进行多重比较),对HC和ALS运动神经元网络的拟合优度进行比较。
表6. 广义线性混合模型估计值和测试结果,多孔微电极阵列
| 电生理指标 | 健康对照(HC)均值 | HC 95% 置信区间 | 肌萎缩侧索硬化症(ALS)均值 | ALS 95% 置信区间 | F统计量与自由度 | p值 |
|---|---|---|---|---|---|---|
| 放电频率 (Firing rate, Hz) | 0.488 | 0.169–0.807 | 1.386 | 1.109–1.664 | F(1, 121) = 17.689 | 5.01 × 10⁻⁵ |
| 锋电位幅度 (Spike amplitude, μV) | 27.9 | 27.4–28.4 | 26.0 | 25.6–26.4 | F(1, 121) = 32.651 | 8.07 × 10⁻⁸ |
| 小世界倾向性 (Small-world propensity) | 0.947 | 0.912–0.981 | 0.901 | 0.870–0.931 | F(1, 120) = 3.926 | 0.0498 |
| 模块化系数(Louvain Q值) | 0.319 | 0.471–0.367 | 0.190 | 0.148–0.232 | F(1, 120) = 15.783 | 1.22 × 10⁻⁴ |
| 同配性 (Assortativity) | 0.116 | 0.0286–0.203 | 0.286 | 0.210–0.361 | F(1, 112) = 8.585 | 4.11 × 10⁻³ |
| 特征路径长度 (Characteristic path length) | 1.84 | 1.73–1.94 | 1.66 | 1.57–1.75 | F(1, 120) = 6.660 | 0.0111 |
| 平均聚集系数 (Mean clustering coefficient) | 0.0119 | 0.00424–0.0195 | 0.0229 | 0.0163–0.0296 | F(1, 120) = 4.687 | 0.0324 |
| 网络密度 (Network density) | 0.0150 | 0.00964–0.0203 | 0.0270 | 0.0223–0.0317 | F(1, 120) = 11.245 | 1.07 × 10⁻³ |
¶ 致谢
本研究得到了奥拉夫·托恩基金会、挪威肌萎缩侧索硬化症协会和阿尔夫·哈伯格基金的支持。核和细胞质细胞组分的蛋白质印迹分析由挪威科技大学的蛋白质组学与修饰组学实验核心(PROMEC)以及挪威中部地区卫生局完成。
¶ 支持信息
本文的补充信息可在https://doi.org/10.1162/NETN.a.552获取。
¶ 作者贡献
维加德·菲斯克姆:概念构思;数据整理;形式分析;资金获取;调查研究;方法设计;项目管理;可视化;撰写——初稿。尼古拉·温特-耶尔姆:方法设计;软件编程;撰写——审阅与编辑。尼古拉斯·克里斯蒂安森:形式分析;方法设计;软件编程;撰写——审阅与编辑。阿克塞尔·桑德维格:项目管理;监督指导;撰写——审阅与编辑。约安娜·桑德维格:概念构思;项目管理;监督指导;撰写——审阅与编辑。
¶ 资助信息
Olav Thon基金会Ioanna Sandvig(https://dx.doi.org/10.13039/501100021720)。Alf Harborg基金会Vegard Fiskum。挪威渐冻人症基金会Ioanna Sandvig。
¶ 参考文献
- Abbott, L. F., & Rohrkemper, R. (2007). 构建临界雪崩网络的简单生长模型. 《脑研究进展》, 165, 13–19. https://doi.org/10.1016/S0079-6123(06)65002-4
- Aguzzi, A., Heikenwalder, M., & Polymenidou, M. (2007). 朊病毒毒株与神经毒性的研究进展. 《自然综述:分子细胞生物学》, 8(7), 552–561. https://doi.org/10.1038/nrm2204
- Anastacio, H. T. D., Matosin, N., & Ooi, L. (2022). 阿尔茨海默病中的神经元过度兴奋:这一异常表型背后的驱动因素是什么?《转化精神病学》, 12(1), 257. https://doi.org/10.1038/s41398-022-02024-7, PubMed: 35732622
- Arai, T., Hasegawa, M., Akiyama, H., Ikeda, K., Nonaka, T., Mori, H., … Oda, T. (2006). TDP-43是额颞叶变性和肌萎缩侧索硬化症中泛素阳性、tau阴性包涵体的组成成分. 《生物化学与生物物理研究通讯》, 351(3), 602–611. https://doi.org/10.1016/j.bbrc.2006.10.093, PubMed: 17084815
- Armstrong, C. M., & Bezanilla, F. (1974). 钠通道激活门开闭相关的电荷移动. 《普通生理学杂志》, 63(5), 533–552. https://doi.org/10.1085/jgp.63.5.533
- Arispe, N., Pollard, H. B., & Rojas, E. (1993). 阿尔茨海默病淀粉样β蛋白[AβP-(1-40)]在双层膜中形成的多级大阳离子通道. 《美国国家科学院院刊》, 90(22), 10573–10577. https://doi.org/10.1073/pnas.90.22.10573
- Aswendt, M., & Hoehn, M. (2023). 与脑部疾病相关的功能超连接:适应不良过程还是恢复力的要素?《神经再生研究》, 18(7), 1489–1490. https://doi.org/10.4103/1673-5374.361541, PubMed: 36571347
- Augustine, G. J. (2001). 钙如何触发神经递质释放?《神经生物学新见》, 11(3), 320–326. https://doi.org/10.1016/s0959-4388(00)00214-2
- Babiloni, C., Pizzella, V., Gratta, C. D., Ferretti, A., & Romani, G. L. (2009). 脑电图、脑磁图与功能磁共振成像的基本原理. 《国际神经生物学评论》, 86, 67–80. https://doi.org/10.1016/S0074-7742(09)86005-4
- Bakkum, D. J., Chao, Z. C., & Potter, S. M. (2008). 皮层网络中动作电位传导延迟与幅度的长时程活动依赖性可塑性. 《公共科学图书馆·综合》, 3(5), e2088. https://doi.org/10.1371/journal.pone.0002088
- Bae, E. J., Lee, H. J., Rockenstein, E., Ho, D. H., Park, E. B., Yang, N. Y., et al. (2012). 抗体辅助清除细胞外α-突触核蛋白可阻止聚集体的细胞间传递. 《神经科学杂志》, 32(38), 13454–13469. https://doi.org/10.1523/JNEUROSCI.1611-12.2012, PubMed: 22993411
- Bae, E. J., Kim, D. K., Lee, S., Kim, C., Mante, M., Adame, A., et al. (2018). LRRK2激酶通过RAB35磷酸化调控α-突触核蛋白的播散. 《自然·通讯》, 9(1), 3465. https://doi.org/10.1038/s41467-018-05911-9, PubMed: 30158651
- Barabasi, A.-L., & Bonabeau, E. (2003). 无标度网络. 《科学美国人》, 288(5), 50–59. https://doi.org/10.1038/scientificamerican0503-60
- Baruchi, I., Voman, V., Raichman, N., Shein, M., & Ben-Jacob, E. (2008). 体外偶联皮层网络中相互同步的发生与特性. 《欧洲神经科学杂志》, 28(9), 1825–1835. https://doi.org/10.1111/j.1460-9568.2008.06487.x
- Barnes-Davies, M., & Forsythe, I. D. (1995). 大鼠听觉脑干切片中巨型兴奋性突触的突触前与突触后谷氨酸受体. 《生理学杂志》, 488(第2部分), 387–406. https://doi.org/10.1113/jphysiol.1995.sp020974
- Bassett, S. S., Yousem, D. M., Cristinzio, C., Kusevic, I., Yassa, M. A., Caffo, B. S., et al. (2006). 阿尔茨海默病家族风险改变功能磁共振成像的激活模式. 《脑》, 129(第5部分), 1229–1239. https://doi.org/10.1093/brain/awl039
- Bassil, F., Pena, J., Iba, M., Zhang, B., Gu, X., Soto, C., et al. (2020). β淀粉样蛋白(Aβ)斑块在合并Aβ病理的路易体病小鼠模型中促进α-突触核蛋白与tau的播种和播散. 《神经元》, 105(2), 260–275. https://doi.org/10.1016/j.neuron.2019.10.009, PubMed: 31753836
- Bachhuber, T., Katzmarski, N., McCarter, J. F., Loreth, D., Kamp, F., Tahirovic, S., et al. (2015). α-突触核蛋白对β淀粉样蛋白斑块形成的抑制作用. 《自然·医学》, 21(7), 802–807. https://doi.org/10.1038/nm.3877, PubMed: 26075869
- Bean, B. P. (2007). 哺乳动物中枢神经元中的动作电位. 《自然综述:神经科学》, 8(6), 451–465. https://doi.org/10.1038/nrn2148
- Berdondini, L., Chiappalone, M., Van Der Wal, P. D., De Rooij, N. F., Koudelka-Hep, M., & Tedesco, M., et al. (2006). 集成簇状结构的微电极阵列(MEA),用于研究受限互联神经元亚群的体外神经动力学. 《传感器与执行器B:化学》, 114(2), 530–541. https://doi.org/10.1016/j.snb.2005.04.042
- Berdondini, L., Imfeld, K., Maccione, A., Tedesco, M., Neukom, S., Koudelka-Hep, M., et al. (2009). 用于从单细胞到大规模神经元网络实现高时空分辨率电生理记录的有源像素传感器阵列. 《芯片实验室》, 9(18), 2644–2651. https://doi.org/10.1039/b907394a
- Bero, A. W., Yan, P., Roh, J. H., Cirrito, J. R., Stewart, F. R., Raichle, M. E., et al. (2011). 神经元活动调控脑区对β淀粉样蛋白沉积的易感性. 《自然·神经科学》, 14(6), 750–756. https://doi.org/10.1038/nn.2814, PubMed: 21552265
- Bischofberger, J., Geiger, J. R., & Jonas, P. (2002). 海马苔藓纤维 bouton 中钙通道激活的时程与效率. 《神经科学杂志》, 22(24), 10593–10602. https://doi.org/10.1523/jneurosci.22-24-10593.2002
- Blondel, V. D., Guillaume, J.-L., Lambiotte, R., & Lefebvre, E. (2008). 大型网络中社区的快速展开算法. 《统计力学杂志:理论与实验》, 2008(10), P10008. https://doi.org/10.1088/1742-5468/2008/10/P10008
- Boehler, M. D., Leondopulos, S. S., Wheeler, B. C., & Brewer, G. J. (2012). 基于可靠图案化基底的海马网络构建. 《神经科学方法杂志》, 203(2), 344–353. https://doi.org/10.1016/j.jneumeth.2011.09.020
- Boluda, S., Iba, M., Zhang, B., Raible, K. M., Lee, V. M., & Trojanowski, J. Q. (2015). 脑内注射阿尔茨海默病或皮质基底节变性脑来源的病理性tau后,年轻PS19 tau转基因小鼠中tau病理的差异化诱导与播散. 《神经病理学报》, 129(2), 221–237. https://doi.org/10.1007/s00401-014-1344-0, PubMed: 25413996
- Bolmont, T., Haass, C., & Duff, K. (2007). 脑内输注含β淀粉样蛋白的脑提取物,以及APP×Tau转基因小鼠中β淀粉样蛋白沉积对tau病理的诱导作用. 《美国病理学杂志》, 171(6), 2012–2020. https://doi.org/10.2353/ajpath.2007.070249, PubMed: 17982000
- Bonifazi, P., Difato, F., Massobrio, P., Breschi, G. L., Pasquale, V., Levi, T., et al. (2013). 用于实现双向脑机接口的体外大规模实验与理论研究. 《神经回路前沿》, 7, 40. https://doi.org/10.3389/fncir.2013.00040
- Bonifazi, P., Goldin, M., Picardo, M. A., Jorquera, I., Cattani, A., Bianconi, G., et al. (2009). 海马发育网络中,GABA能枢纽神经元调控同步化活动. 《科学》, 326(5956), 1419–1424. https://doi.org/10.1126/science.1175509
- Bonifazi, P., Ruaro, M. E., & Torre, V. (2005). 神经元网络中信息处理的统计特性. 《欧洲神经科学杂志》, 22(12), 2953–2964. https://doi.org/10.1111/j.1460-9568.2005.04464.x
- Borgheai, S. B., McLinden, J., Mankodiya, K., & Shahriari, Y. (2020). 肌萎缩侧索硬化症相关的额叶功能网络破坏:基于功能性近红外光谱的最小生成树分析. 《神经科学前沿》, 14, 613990. https://doi.org/10.3389/fnins.2020.613990, PubMed: 33424544
- Borghi, T., Gusmeroli, R., Spinelli, A. S., & Baranauskas, G. (2007). 一种高效的多单位记录锋电位检测简易方法. 《神经科学方法杂志》, 163(1), 176–180. https://doi.org/10.1016/j.jneumeth.2007.02.014
- Borst, J. G., & Sakmann, B. (1998). 大鼠脑干大突触前末梢中单个动作电位期间的钙电流. 《生理学杂志》, 506(第1部分), 143–157. https://doi.org/10.1111/j.1469-7793.1998.143bx.x
- Borst, J. G., & Sakmann, B. (1999). 大鼠听觉脑干花萼型突触中,动作电位形态变化对钙电流和递质释放的影响. 《伦敦皇家学会哲学汇刊·B辑:生物科学》, 354(1381), 347–355. https://doi.org/10.1098/rstb.1999.0386
- Borst, J. G., Helmchen, F., & Sakmann, B. (1995). 大鼠斜方体内侧核的突触前与突触后全细胞记录. 《生理学杂志》, 489(第3部分), 825–840. https://doi.org/10.1113/jphysiol.1995.sp021095
- Borst, J. G., & Soria van Hoeve, J. (2012). Held花萼突触:从模式突触到听觉中继站. 《生理学年度评论》, 74, 199–224. https://doi.org/10.1146/annurev-physiol-020911-153236
- Brody, C. D. (1999). 无同步的相关性. 《神经计算》, 11(7), 1537–1551. https://doi.org/10.1162/089976699300016133
- Brookhouser, N., Raman, S., Frisch, C., Srinivasan, G., & Brafman, D. A. (2021). APOE2在等基因hiPSC构建的阿尔茨海默病模型中缓解疾病相关表型. 《分子精神病学》, 26(10), 5715–5733. https://doi.org/10.1038/s41380-021-01122-9
- Broido, A. D., & Clauset, A. (2019). 无标度网络十分罕见. 《自然·通讯》, 10(1), 1017. https://doi.org/10.1038/s41467-019-08746-5, PubMed: 30833554
- Buchs, P.-A., & Muller, D. (1996). 长时程增强的诱导伴随激活突触的超微结构重大改变. 《美国国家科学院院刊》, 93(15), 8040–8045. https://doi.org/10.1073/pnas.93.15.8040
- Bullmore, E., & Sporns, O. (2009). 复杂脑网络:结构与功能系统的图论分析. 《自然综述:神经科学》, 10(3), 186–198. https://doi.org/10.1038/nrn2575, PubMed: 19190637
- Bullmore, E., & Sporns, O. (2012). 脑网络组织的经济性. 《自然综述:神经科学》, 13(5), 336–349. https://doi.org/10.1038/nrn3214, PubMed: 22498897
- Busche, M. A., Eichhoff, G., Adelsberger, H., Abramowski, D., Wiederhold, K. H., Haass, C., et al. (2008). 阿尔茨海默病小鼠模型中,淀粉样斑块附近的神经元过度激活簇. 《科学》, 321(5896), 1686–1689. https://doi.org/10.1126/science.1162848
- Cavaliere, F., Piemonte, F., Lopes, F. M., D’Angelo, E., & Fornai, F. (2017). 利用帕金森病脑来源的路易体提取物,体外研究α-突触核蛋白在神经元与星形胶质细胞间的神经毒性与播散. 《疾病神经生物学》, 103, 101–112. https://doi.org/10.1016/j.nbd.2017.04.009, PubMed: 28411108
- Celone, K. A., Calhoun, V. D., Dickerson, B. C., Atri, A., Chua, E. F., Miller, S. L., et al. (2006). 轻度认知障碍与阿尔茨海默病中记忆网络的改变:独立成分分析. 《神经科学杂志》, 26(40), 10222–10231. https://doi.org/10.1523/JNEUROSCI.2362-06.2006
- Chen, L., Chehade, H. D., & Chu, H.-Y. (2025). 与α-突触核蛋白聚集相关的运动皮层神经元过度兴奋. 《npj帕金森病》, 11(1), 18. https://doi.org/10.1038/s41531-024-00867-z, PubMed: 39809792
- Chiappalone, M., Massobrio, P., & Martinoia, S. (2008). 培养皮层集合体中的网络可塑性. 《欧洲神经科学杂志》, 28(2), 221–237. https://doi.org/10.1111/j.1460-9568.2008.06259.x
- Choi, S. H., Kim, Y. H., Hebisch, M., Sliwinski, C., Lee, S., D’Avanzo, C., et al. (2014). 基于三维人神经细胞培养的阿尔茨海默病模型. 《自然》, 515(7526), 274–278. https://doi.org/10.1038/nature13800
- Clauset, A., Newman, M. E. J., & Moore, C. (2004). 超大型网络中社区结构的发现. 《物理评论E》, 70(6), 066111. https://doi.org/10.1103/PhysRevE.70.066111, PubMed: 15697438
- Clinton, L. K., Blurton-Jones, M., Myczek, K., Trojanowski, J. Q., & LaFerla, F. M. (2010). β淀粉样蛋白、tau与α-突触核蛋白的协同相互作用:加速神经病理与认知衰退. 《神经科学杂志》, 30(22), 7281–7289. https://doi.org/10.1523/JNEUROSCI.0273-10.2010, PubMed: 20519528
- Colizza, V., Flammini, A., Serrano, M. A., & Vespignani, A. (2006). 复杂网络中富俱乐部排序的检测. 《自然·物理学》, 2(2), 110–115. https://doi.org/10.1038/nphys209
- Corder, E. H., Saunders, A. M., Strittmatter, W. J., Schmechel, D., Gaskell, P. C., Small, G. W., et al. (1993). 载脂蛋白E ε4等位基因的基因剂量与晚发家族性阿尔茨海默病的发病风险. 《科学》, 261(5123), 921–923. https://doi.org/10.1126/science.8346441, PubMed: 8346441
- Cope, T. E., Grothe, M. J., Teipel, S. J., & Ourselin, S. (2018). 阿尔茨海默病与进行性核上性麻痹中tau负荷与功能连接组的关联. 《脑》, 141(2), 550–567. https://doi.org/10.1093/brain/awx356, PubMed: 29329399
- Covell, D. J., Stieber, A., Zhang, B., Iba, M., Duda, J. E., Lee, V. M., et al. (2017). 针对不同体外原纤维形式制备的新型构象选择性α-突触核蛋白抗体,在帕金森病中显示出差异化的路易体病理识别模式. 《神经病理学与应用神经生物学》, 43(7), 604–620. https://doi.org/10.1111/nan.12340, PubMed: 28050799
- Cunha-Oliveira, T., Montezinho, L., Mendes, C., Firuzi, O., Saso, L., Oliveira, P. J., & Silva, F. S. G. (2020). 肌萎缩侧索硬化症中的氧化应激:病理生理学与药物干预靶点. 《氧化医学与细胞寿命》, 2020, 5021694. https://doi.org/10.1155/2020/5021694, PubMed: 33274002
- Cutts, C. S., & Eglen, S. J. (2014). 锋电位序列中成对相关性的检测:方法的客观比较及在视网膜波研究中的应用. 《神经科学杂志》, 34(43), 14288–14303. https://doi.org/10.1523/JNEUROSCI.2767-14.2014
- D’Amico, E., Factor-Litvak, P., Santella, R. M., & Mitsumoto, H. (2013). 散发性肌萎缩侧索硬化症中氧化应激的临床视角. 《自由基生物学与医学》, 65, 509–527. https://doi.org/10.1016/j.freeradbiomed.2013.06.029, PubMed: 23797033
- De Vos, W. H., et al. (2019). 用于深度分析神经元突起RNA含量的轴突测序技术(Axon-seq). 《生物实验方案》, 9(14), e3312. https://doi.org/10.21769/BioProtoc.3312, PubMed: 33654821
- Dickerson, B. C., Salat, D. H., Greve, D. N., Chua, E. F., Rand-Giovannetti, E., Rentz, D. M., et al. (2005). 与正常衰老和阿尔茨海默病相比,轻度认知障碍中海马激活增强. 《神经病学》, 65(3), 404–411. https://doi.org/10.1212/01.wnl.0000172591.88395.09
- Ding, F., LaRocque, J. J., & Dokholyan, N. V. (2005). 蛋白质折叠、聚集与朊病毒样构象转换的直接观察. 《生物化学杂志》, 280(49), 40235–40240. https://doi.org/10.1074/jbc.M508199200, PubMed: 16204251
- Dittman, J. S., & Ryan, T. A. (2019). 神经末梢释放概率的调控机制. 《自然综述:神经科学》, 20(3), 177–186. https://doi.org/10.1038/s41583-018-0111-3
- Dobson, C. M. (1999). 蛋白质错误折叠、进化与疾病. 《生物化学科学趋势》, 24(9), 329–332. https://doi.org/10.1016/S0968-0004(99)01445-0, PubMed: 10461194
- Dodson, P. D., Barker, M. C., & Forsythe, I. D. (2002). 两种异聚体Kv1钾通道对动作电位发放的差异化调控. 《神经科学杂志》, 22(16), 6953–6961. https://doi.org/10.1523/jneurosci.22-16-06953.2002
- Dodson, P. D., & Forsythe, I. D. (2004). 突触前钾通道:突触末梢兴奋性的关键电调控因子. 《神经科学趋势》, 27(4), 210–217. https://doi.org/10.1016/j.tins.2004.02.012
- Downes, J. H., Hammond, M. W., Xydas, D., Spencer, M. C., Becerra, V. M., Warwick, K., et al. (2012). 培养神经元中小世界功能网络的涌现. 《公共科学图书馆·计算生物学》, 8(5), e1002522. https://doi.org/10.1371/journal.pcbi.1002522
- Eckert, R., & Ewald, D. (1983). 电压钳下加州海兔完整神经胞体中的钙尾电流. 《生理学杂志》, 345, 533–548. https://doi.org/10.1113/jphysiol.1983.sp014995
- Eguíluz, V. M., Chialvo, D. R., Cecchi, G. A., Baliki, M., & Apkarian, A. V. (2005). 无标度的脑功能网络. 《物理评论快报》, 94(1), 018102. https://doi.org/10.1103/PhysRevLett.94.018102
- Egert, U., Heck, D., & Aertsen, A. (2002). 急性脑切片中锋电位网络的二维监测. 《实验脑研究》, 142(3), 268–274. https://doi.org/10.1007/s00221-001-0932-5
- Eggermann, E., Bucurenciu, I., Goswami, S. P., & Jonas, P. (2012). 哺乳动物快突触中钙通道与胞吐传感器的纳米域耦合. 《自然综述:神经科学》, 13(1), 7–21. https://doi.org/10.1038/nrn3125
- Eisele, Y. S., Obermüller, U., Heilbronner, G., Baumann, F., Kaeser, S. A., Wolburg, H., et al. (2014). 外周诱导脑β淀粉样变性的多因素调控机制. 《神经科学杂志》, 34(30), 10264–10273. https://doi.org/10.1523/JNEUROSCI.4931-13.2014, PubMed: 25057209
- Eytan, D., Brenner, N., & Marom, S. (2003). 皮层神经元网络的选择性适应. 《神经科学杂志》, 23(28), 9349–9356. https://doi.org/10.1523/JNEUROSCI.23-28-09349.2003
- Farahani, A., Hansen, J. Y., Bazinet, V., Shafiei, G., Collins, D. L., Dadar, M., et al. (2025). 肌萎缩侧索硬化症中的网络播散与局部生物学易损性. 《通讯生物学》, 8(1), 1153. https://doi.org/10.1038/s42003-025-08561-3, PubMed: 40760014
- Fellner, L., Irschick, R., Schanda, K., Reindl, M., Klimaschewski, L., Poewe, W., et al. (2013). Toll样受体4是α-突触核蛋白介导小胶质细胞与星形胶质细胞激活的必需分子. 《神经胶质细胞》, 61(3), 349–360. https://doi.org/10.1002/glia.22444, PubMed: 23281159
- Feldt, S., Bonifazi, P., & Cossart, R. (2011). 解析神经元微环路的功能连接:实验与理论见解. 《神经科学趋势》, 34(5), 225–236. https://doi.org/10.1016/j.tins.2011.02.007
- Fekete, T., Zach, N., Mujica-Parodi, L. R., & Turner, M. R. (2013). 多核学习捕捉肌萎缩侧索硬化症的系统水平功能连接生物标志物特征. 《公共科学图书馆·综合》, 8(12), e85190. https://doi.org/10.1371/journal.pone.0085190, PubMed: 24391997
- Fenwick, E. M., Marty, A., & Neher, E. (1982). 牛嗜铬细胞中的钠通道与钙通道. 《生理学杂志》, 331, 599–634. https://doi.org/10.1113/jphysiol.1982.sp014394
- Fitzpatrick, A. W. P., Falcon, B., He, S., Murzin, A. G., Murshudov, G., Garringer, H. J., et al. (2017). 阿尔茨海默病来源tau丝的冷冻电镜结构. 《自然》, 547(7662), 185–190. https://doi.org/10.1038/nature23002, PubMed: 28652354
- Forsythe, I. D., Tsujimoto, T., Barnes-Davies, M., Cuttle, M. F., & Takahashi, T. (1998). 中枢快突触中突触前钙电流的失活参与突触压抑. 《神经元》, 20(4), 797–807. https://doi.org/10.1016/s0896-6273(00)81017-x
- Fuchs, E., Ayali, A., Ben-Jacob, E., & Boccaletti, S. (2009). 模块化神经网络发育过程中同步团簇的形成. 《物理生物学》, 6(3), 036018. https://doi.org/10.1088/1478-3975/6/3/036018
- Friston, K. J. (1994). 神经影像中的功能连接与有效连接:综述. 《人脑图谱》, 2(1), 56–78. https://doi.org/10.1002/hbm.460020107
- Frey, U., Egert, U., Heer, F., Hafizovic, S., & Hierlemann, A. (2009). 用于脑片细胞外电场高分辨率标测的微电子系统. 《生物传感器与生物电子学》, 24(7), 2191–2198. https://doi.org/10.1016/j.bios.2008.11.028
- Frost, B., Jacks, R. L., & Diamond, M. I. (2009). tau错误折叠从细胞外向细胞内的传递. 《生物化学杂志》, 284(19), 12845–12852. https://doi.org/10.1074/jbc.M808515200, PubMed: 19289490
- Furukawa, Y., Kaneko, K., Yamanaka, K., & Nukina, N. (2010). 家族性肌萎缩侧索硬化症中铜锌超氧化物歧化酶聚集体的突变依赖性多态性. 《生物化学杂志》, 285(29), 22221–22231. https://doi.org/10.1074/jbc.M110.103915, PubMed: 20444991
- Games, D., Valera, E., Spencer, B., Rockenstein, E., Mante, M., Adame, A., et al. (2014). 免疫疗法减少C端截短型α-突触核蛋白,可缓解帕金森病样模型中的神经退行性变与病理播散. 《神经科学杂志》, 34(28), 9441–9454. https://doi.org/10.1523/JNEUROSCI.4931-13.2014, PubMed: 25009987
- Ghatak, S., Dolatabadi, N., Trudler, D., Zhang, X., Wu, Y., Mohata, M., et al. (2019). 阿尔茨海默病hiPSC来源神经元与脑类器官相较于等基因对照的过度兴奋机制. 《eLife》, 8, e50333. https://doi.org/10.7554/eLife.50333
- Giasson, B. I., Lee, V. M., Trojanowski, J. Q., & Goedert, M. (2003). tau与α-突触核蛋白原纤维形成的启动与协同效应. 《科学》, 300(5619), 636–640. https://doi.org/10.1126/science.108232