¶ 《干细胞报告》
¶ 适当的兴奋/抑制比例是小鼠皮质培养物中形成同步网络活动所必需的
¶ 原文下载:piis2213671125002504.pdf
埃莱奥诺拉·克罗科,1 卢多维科·扬内洛,2 法布里齐奥·托内利,1 加布里埃莱·拉加尼,2 卢卡·潘多尔菲尼,3 马尔切洛·费罗,4
朱塞佩·阿马托,2 安吉洛·迪·嘉宝,5,6和费德里科·克雷米西1,5,7,*
1 BiologyBio@SNS,Scuola Norman Superiore,比萨,意大利
2 意大利比萨国家研究委员会信息科学与技术研究所(ISTI-CNR)
3 人类技术中心,中央RNA实验室,意大利理工学院,16152热那亚,意大利
4 计算语言学研究所“安东尼奥·赞波利”(CNR-ILC),比萨,意大利
5 国家研究委员会生物研究所,意大利比萨56124
6 比萨大学系,意大利比萨56127
7 主要联系人
* 通信:federico.cremisi@sns.it
https://doi.org/10.1016/j.stemcr.2025.102646
¶ 摘要
兴奋性/抑制性(E/I)平衡被认为在皮层活动发育中起着关键作用。我们对一个体外皮层网络进行了建模,该网络包含通常从腹侧端脑迁移而来的抑制性神经元,并构建了腹侧端脑(VT)培养物以及背侧端脑(DT)和VT神经元按不同比例混合的共培养物,这些培养物中含有不同比例的抑制性神经元。有趣的是,这些纯培养物和混合培养物形成了不同的自发活动模式和功能连接模式。我们的研究结果强调了抑制性成分在形成相关性网络活动中的关键作用。出乎意料的是,含有7%小白蛋白(PV)+神经元的网络由于形成了强烈的网络抑制,尽管其E/I比率最低,却无法产生明显的网络爆发活动。我们的观察结果支持这样一种观点,即皮层发育过程中小白蛋白(PV)+神经元的最佳比例对于建立能够产生和传播相关性活动的局部抑制性网络至关重要。
¶ 引言
小鼠胚胎干细胞(mESCs)或人类诱导多能干细胞(hiPSCs)是通过在精确的时间窗口内控制不同的信号通路,在体外模拟不同脑区发育的关键工具(Chambers 等人,2009;Chiaradia 和 Lancaster,2020)。前脑特性是默认获得的,并主要通过BMP和Wnt抑制来维持(Bertacchi 等人,2015;Watanabe 等人,2005)。背侧端脑(DT)祖细胞可在体外使用 sonic Hedgehog(Shh)抑制剂环巴胺生成(Gaspard 等人,2008),而腹侧端脑(VT)祖细胞则需要通过Shh激动剂SAG激活Shh(Cederquist 等人,2019;Li 等人,2009)。在体内,成熟的大脑皮层是在VT细胞迁移后形成的,这些细胞主要来自内侧神经节隆起(MGE)(Wonders 和 Anderson,2006)。这些细胞分化为GABA能抑制性中间神经元,与局部DT祖细胞生成的谷氨酸能兴奋性神经元相连接,从而建立平衡的兴奋/抑制(E/I)比率(Gelman 和Marı´n,2010;Lodato 等人,2011)。值得注意的是,E/I比率失衡与精神分裂症或自闭症谱系障碍等脑部疾病相关(Nelson 和 Valakh,2015;Sohal 和 Rubenstein,2019)。
迄今为止,使用明确比例的VT和DT神经元重建皮质回路的研究相对较少(Mossink等人,2022年;Parodi等人,2023年、2024年)。这些研究使用的诱导神经元(iNeurons)仅能部分模拟天然端脑神经元。具体而言,Ngn2诱导的神经元由异质群体组成,表现出中枢和外周神经系统谱系的特征(Lin等人,2021年),而Ascl1诱导的神经元分化为小白蛋白阳性中间神经元的能力有限,小白蛋白阳性中间神经元是体内皮质抑制性神经元的主要类型(Zhang等人,2013年)。为了研究具有不同E/I比例的更具生理特性的神经网络,并在发育成熟过程中对其功能进行表征,我们在体外对两种不同的细胞群体进行了建模,即通过调节小鼠胚胎干细胞衍生的端脑细胞中Shh通路获得的DT和VT祖细胞。我们分析了单独的DT祖细胞网络的活动,并将其与VT祖细胞网络以及具有不同DT和VT细胞比例的网络进行了比较。最后,我们分析了基本的结构和功能网络参数,如突触密度、放电活动、网络爆发同步性和连接性,以及对电刺激的反应能力。我们的研究结果表明,E/I平衡显著影响神经元培养物的发育和成熟,强调适当的E/I比例是皮质网络中相关活动形成和扩散所必需的。
¶ 结果
¶ 环巴胺和SAG处理分别诱导背侧端脑(DT)神经元和腹侧端脑(VT)神经元的产生
在小鼠胚胎干细胞(mESC)神经分化的第一周,早期双重抑制骨形态发生蛋白(BMP)和Wnt信号通路(WiBi)会诱导出一种普遍的端脑特性(Terrigno等人,2018)(图1A和1B)。在体外分化第5天(DIV5)至第10天(DIV10),我们向经WiBi处理的mESC中添加环巴胺(3μM)以诱导背侧端脑(DT)特性(Chen等人,2002a),并添加 smoothened激动剂(SAG)(0.1μM)以诱导腹侧端脑(VT)特性(Chen等人,2002b)。在DIV11,我们使用端脑和亚端脑特性的早期标志物确认了细胞的位置特性(Fuccillo等人,2006;Martynoga等人,2005)(图1B–1E和图S1A–S1C)。环巴胺(CYC)处理的细胞高表达背侧标志物Pax6,而SAG处理的细胞高表达腹侧特性标志物Nkx2.1。此外,与未进行Wnt抑制的对照神经分化细胞(中脑)相比,这两种类型的细胞都高表达端脑标志物FoxG1。我们接着分析了亚端脑以及内侧和外侧神经节隆起(MGE-LGE)的特定早期标志物,如Lhx6、Lhx8和Dlx1(Chen等人,2017)以及Ascl1、Dlx2和Sfrp1(Nery等人,2002)。我们发现,与其他神经细胞群相比,SAG处理的细胞中这些基因的表达有所增加(图1F和图S1D–S1I)。
在细胞水平上对标志物表达的分析显示,CYC细胞和SAG细胞中均有高比例的细胞呈Foxg1阳性(图1G和1L)。我们观察到,Nkx2.1的表达主要局限于SAG细胞,在CYC细胞中几乎不存在(图1H和1L),而背侧标志物Pax6和Tbr1在大部分CYC细胞中表达,但在SAG细胞中几乎检测不到(图1I、1J和1L)。到第20天(大致相当于小鼠出生后第0天),皮质标志物Satb2在相当一部分CYC细胞中被发现,但在SAG细胞中几乎不存在(图1K和1L)。这些数据证实,SAG培养物具有类似于内侧神经节隆起和次皮质的腹侧特性。
由于内侧神经节隆起(MGE)是多种皮质中间神经元的来源(Gelman等人,2011年),我们评估了特定的亚型标志物,如小白蛋白(PV)和生长抑素(SST)(图2A和图2B)(Lim等人,2018年)。在第35天(DIV35),我们在SAG培养物中计数到73%的PV+神经元,而在CYC培养物中这一比例低得多,仅为7%(图2A)。SAG培养物中SST+神经元的占比不到10%,而在CYC培养物中几乎不存在(图2B)。在CYC和SAG培养物中均未检测到血管活性肠肽(VIP)神经元,这表明这两种培养条件可能都缺乏来自尾侧神经节隆起的祖细胞,而VIP+神经元主要在尾侧神经节隆起中产生(Marín,2012年)。鉴于PV+中间神经元与神经元周围网(PNNs)存在关联(Lupori等人,2023年),我们还研究了对紫藤凝集素(WFA)的反应性,WFA是PNNs的一种常见标志物。早在第50天(DIV50)就观察到了PNNs的典型染色形态(Dickens等人,2022年),这种蛋白偶尔会围绕少数PV+细胞(图2C),这表明一些早期PNNs已形成,且主要存在于SAG培养物中。
对兴奋性(vGlut1和vGlut2)和抑制性(Pvalb和vGat)皮质神经元的不同标志物进行免疫标记后发现,这两种类型的细胞在SAG和CYC培养物中的作用不同,这证实了兴奋性神经元在CYC培养物中占优势,而抑制性神经元在SAG培养物中占优势(图2D)。我们在第25天(DIV25)研究了早期谷氨酸能标志物vGlut2:通过观察vGlut2斑点与Tubβ3+纤维的共定位来评估囊泡密度,发现CYC神经元中vGlut2+囊泡的密度显著高于SAG神经元(图2E)。此外,通过计数被囊泡转运体包围的DAPI阳性细胞核数量,我们评估出CYC培养物中vGlut2+细胞占70%(Cao等人,2017年),而SAG培养物中仅存在15%的vGlut2+细胞(Kempf等人,2021年)(图S2A和S2B)。我们还分析了晚期谷氨酸能标志物vGlut1,发现CYC神经元中vGlut1阳性斑点的密度显著高于SAG神经元(图2E),80%的CYC神经元被vGlut1+囊泡包围(图S2C和S2D)。针对GABA能标志物,我们分析了培养物在第35天(DIV35)的vGat密度,结果显示SAG神经元中vGat+囊泡的数量显著多于CYC神经元(图2E)。
为了评估CYC和SAG培养物中星形胶质细胞的百分比,我们在成熟的两个时间点(DIV21和DIV30)对GFAP+细胞的存在情况进行了评估。在DIV21时,SAG培养物中GFAP+细胞的百分比高于CYC培养物,这表明它们完成神经发生并更早开始星形胶质细胞发生。然而,到DIV30时,两种培养物中GFAP+细胞的百分比均达到40%(图2F和2G),这表明细胞分化已完成。
总之,我们的数据表明,从DIV5到DIV11及时用CYC或SAG处理,会产生大脑皮层神经祖细胞(NPCs),这些细胞分别有能力分化为具有典型DT和VT神经元基因表达谱的神经元。CYC细胞主要产生谷氨酸能锥体神经元,而SAG培养物中富含γ-氨基丁酸能细胞,主要是PV+中间神经元,与迁移到胚胎发育皮层的细胞相似。两种培养物还产生了比例适宜的星形胶质细胞(40%),这有望支持功能性网络活动。
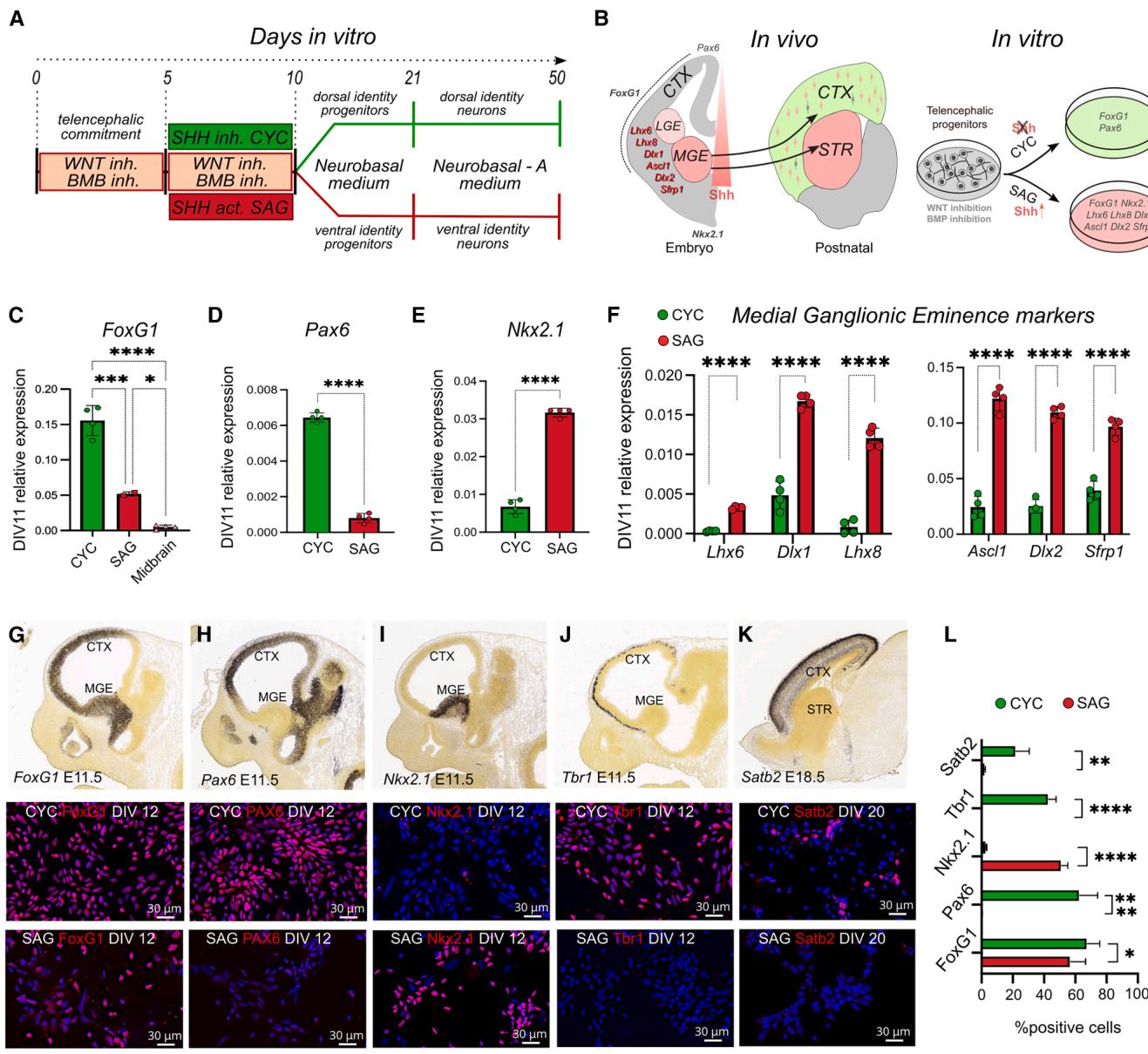
图1. CYC和SAG祖细胞的位置特性及表征
(A) 小鼠胚胎干细胞神经分化方案。
(B)体内和体外标志物表达的示意图。CTX,皮质;STR,纹状体;MGE,内侧神经节隆起;LGE,外侧神经节隆起。
(C–E)通过定量逆转录聚合酶链反应(RT-qPCR)检测早期大脑皮层标志物的相对表达(n = 4个独立实验)。图C中的中脑:未经过WiBi诱导的具有中脑特性的神经化培养物(Bertacchi等人,2015年)。数据以平均值±标准差表示;对Foxg1的表达采用普通单因素方差分析及Tukey多重比较检验;对Pax6和Nkx2.1标志物采用未配对t检验。
(F) 通过RT-qPCR检测MGE-LGE标志物的相对表达(n = 4次独立实验)。数据以平均值±标准差表示;采用多重非配对t检验及Holm-Sidak校正法。p值:*p值<0.05,***p值<0.001,****p值<0.0001。
(G-L)底部:在标记所示的体外分化日(DIV)对CYC和SAG培养物进行所示标志物的免疫标记和定量(DAPI进行蓝色核染色)。比例尺为30μm。图顶部的原位杂交(ISH)插图显示了用于比较的标志物的体内表达,这些插图来自艾伦脑图谱:发育中的小鼠大脑(https://developingmouse.brain-map.org/)。在(L)中,显示了平均值±标准差以及采用Holm-Sidak校正法的多重非配对t检验:**p值<0.01,***p值<0.001,****p值<0.0001。
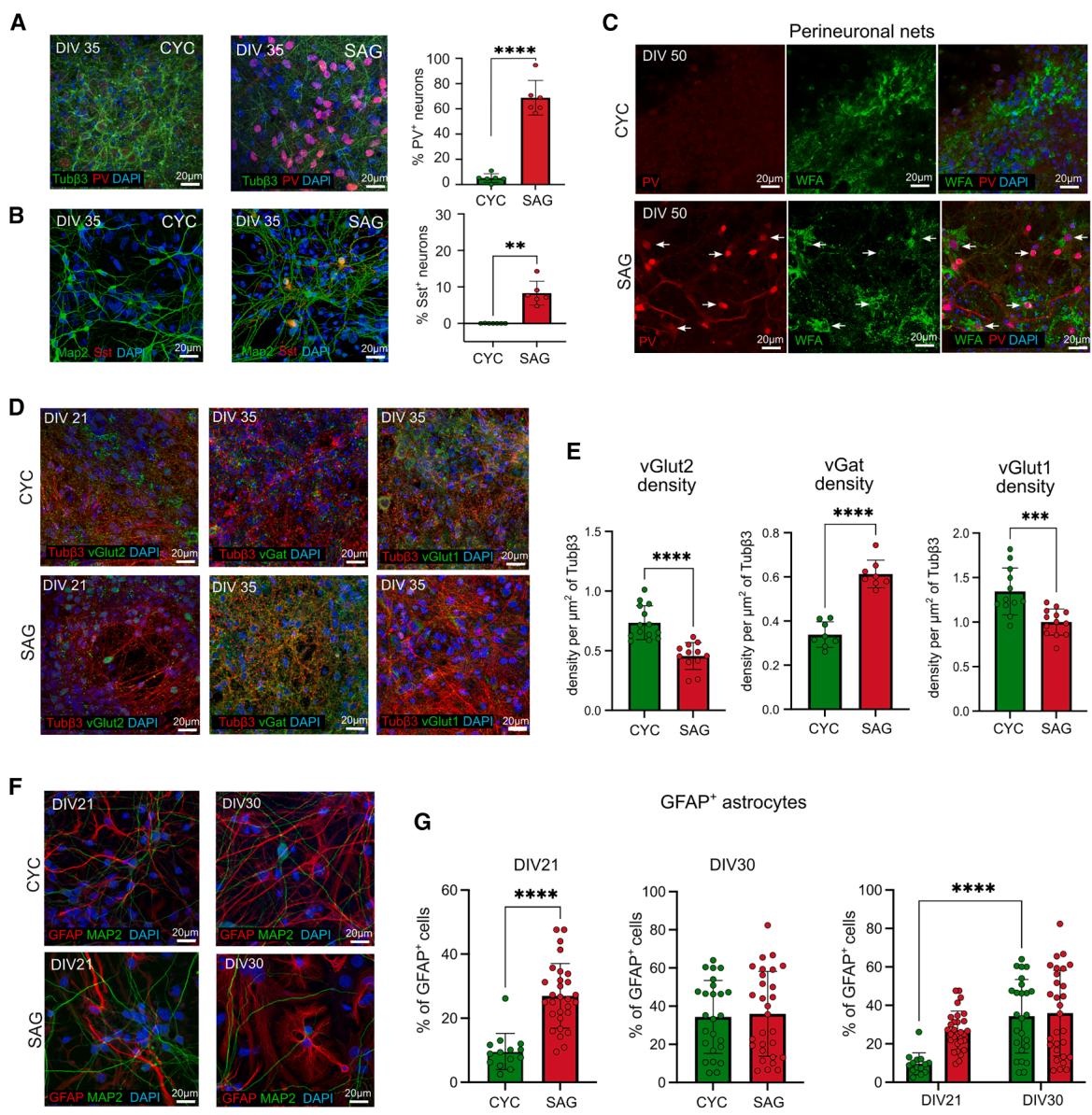
图2. CYC和SAG培养物中兴奋性和抑制性神经元标志物的表达
(A和B)DIV35时,经Tubβ3、Map2、小白蛋白(PV)、生长抑素(Sst)和DAPI染色的CYC和SAG细胞的代表性图像及定量分析。比例尺为20 μm。数据以平均值±标准差表示,并采用非配对t检验,n=3次独立实验:**p值<0.01,****p值<0.0001。
(C) DIV50时,用神经元周围网(PNN)标志物PV和WFA染色的CYC和SAG细胞的代表性图像。白色箭头指示围绕PV+神经元的类PNN结构。比例尺,20 μm。
(D)谷氨酸能和γ-氨基丁酸能标志物的代表性共聚焦图像:vGlut2(第21天)、vGat和vGlut1(第35天)。比例尺,20微米。(E)(D)中所示谷氨酸能和γ-氨基丁酸能标志物的定量分析。突触小泡根据小泡覆盖的Tubβ3阳性区域密度进行测量。比较显示两种处理之间存在统计学差异(n=3次独立实验;非配对t检验)。
(F和G)DIV21和DIV30时的GFAP表达(比例尺,20μm)。在(G)中,显示了不同DIV时的平均值±标准差和未配对t检验;采用双向方差分析(two-way ANOVA)后进行Sı´da´k多重比较检验以比较不同时间点的差异。p值:*p值<0.05,**p值<0.01,***p值<0.001,****p值<0.0001。
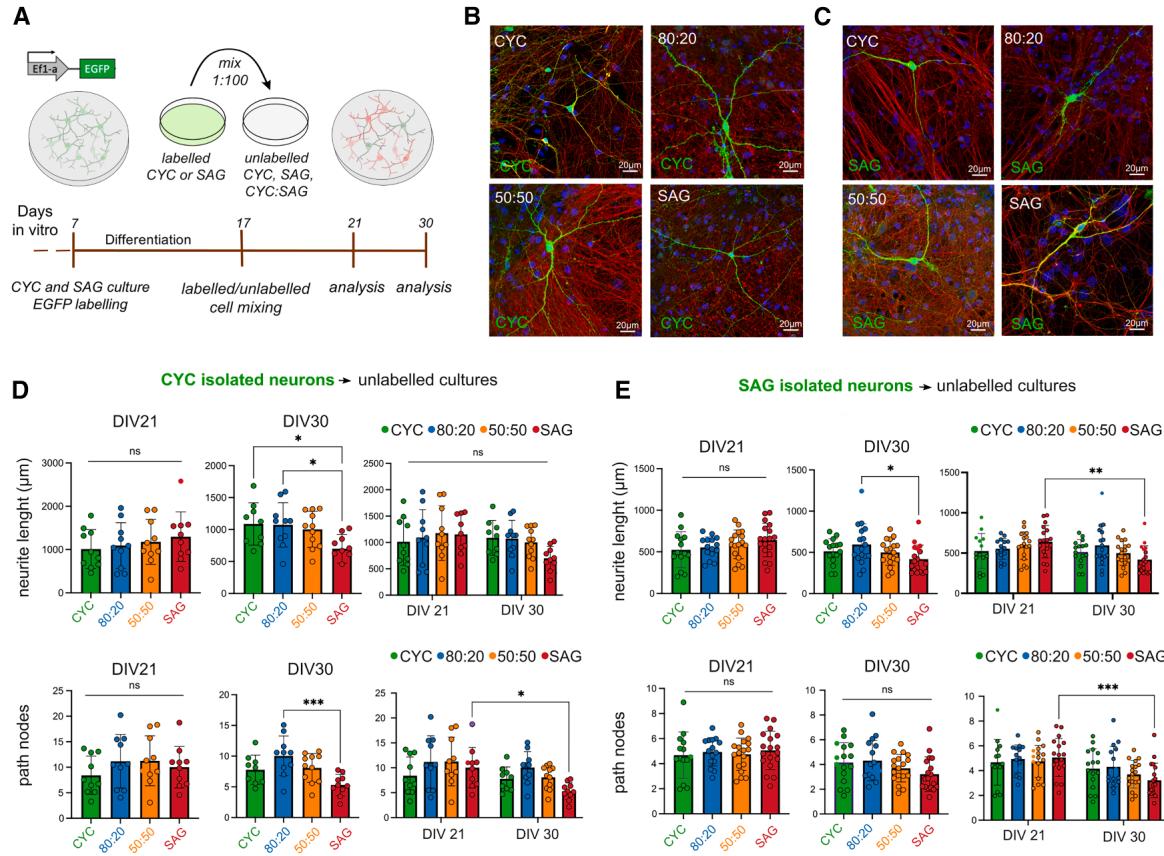
图3. 纯培养和混合培养中CYC和SAG神经元的形态学分析(A)方法概述。(B和C)分别为纯培养和混合未标记培养中EGFP+ -CYC或EGFP+ -SAG神经元的图像。比例尺,20 μm。(D和E)DIV21和DIV30时神经突长度和路径节点的定量分析。显示平均值±标准差以及采用Tukey多重比较检验的普通单因素方差分析,用于比较每个时间点的样本;采用Sidak多重比较检验的双因素方差分析,用于随时间的比较。p值:*p值<0.05,**p值<0.01,***p值<0.001,****p值<0.0001;ns,无显著性差异。
¶ 混合培养物中CYC和SAG神经元的形态学分析
VT神经元正确整合到皮质中是一个受调控的过程,需要跳跃式迁移(Marı´n等人,2010年)。我们在体外环境且缺乏调控迁移的情况下,评估了早期SAG神经元与同龄CYC神经元混合时是否能分化,以及反之亦然的情况。为了评估CYC和SAG神经元的成熟和发育过程,我们首先创建了四种培养条件:纯CYC、纯SAG,以及80:20和50:50(CYC:SAG)的混合比例。因此,为了能够分析单个神经元的形态,我们在第7天使用EGFP标记的CYC或SAG细胞,并以1:100的比例将它们混合到四种未标记的培养物中(图3A-3C、S3A和S3B)。我们在第21天(发育早期)和第30天(成熟开始)观察CYC和SAG神经元,测量神经突长度、分支(节点)和树突棘百分比。在分析中,我们排除了显示神经胶质形态的EGFP标记细胞(图S3E),这些细胞的比例与通过免疫检测发现的比例相似。
在DIV30时,我们发现SAG环境中的CYC神经元与其他环境中的神经元相比,神经突长度缩短且节点数量减少,在80:20的培养物中尤为明显,这导致其成熟度较低(图3D)。同样,与80:20培养物中的神经元相比,SAG神经元在DIV30及之后的时间里,在SAG培养物中的神经突长度显著缩短。此外,对比这两个时间点,我们还观察到节点数量减少,这表明SAG神经元在分支模式上的成熟度发生了改变(图3E)。
对树突棘的分析(图S3A和S3B)显示,在DIV21和DIV30时,50:50和SAG条件下CYC神经元上的棘突百分比均有所降低(图S3C)。相比之下,在抑制性神经元丰富的环境中,SAG神经元棘突的成熟在DIV21时似乎受到损害,但在DIV30时没有差异(图S3D)。然而,仅在50:50和SAG条件下,它们的棘突百分比会随时间增加,这与纹状体中的中型多棘神经元在发育过程中会形成大量树突棘的已知情况一致(Steiner和Tseng,2017)。总体而言,我们的结果表明,周围神经元群体的组成可能会影响神经元的形态成熟。我们观察到,当CYC和SAG神经元在以抑制性神经元为主的环境中培养时,其神经突长度、分支复杂性和树突棘密度均发生了改变,这表明不同的细胞环境可能会影响这些神经元在皮质回路中的功能整合和连接性。
¶ 纯CYC和SAG神经元网络及混合CYC和SAG神经元网络的功能活动发展
培养中的原代皮质神经元会自发形成具有各种活动模式的神经元网络(Charlesworth等人,2015年;Dias等人,2021年)。兴奋/抑制(E/I)平衡是功能性神经网络的基础,为认知和记忆提供支持。这种平衡在单个神经元层面通过兴奋性与抑制性突触输入的适当比例来维持,在网络层面则通过调节各种兴奋性和抑制性回路之间的相互作用来维持(He和Cline,2019年)。为了模拟各种E/I条件,我们分析了纯CYC培养物(缺乏腹侧迁移的中间神经元)、纯SAG培养物(富含γ-氨基丁酸能神经元)以及具有不同E/I比例的混合CYC:SAG培养物。我们的分析重点是网络活动模式的发展,特别针对最丰富的抑制性神经元类型,即PV+和SST+神经元,这些神经元在整个成熟期间保持着稳定的比例。免疫染色分析显示,在DIV30和DIV45时,PV+神经元(图S4A和S4B)和SST+神经元(图S4C和S4D)的相对比例保持不变(图S4E和S4F)。
我们使用包含4096个通道的高密度微电极阵列(HD-MEA),对纯CYC和SAG培养物以及比例为80:20或50:50的混合培养物进行了纵向研究(图4A)。由于CYC培养物含有7%的PV+细胞和可忽略不计比例的SST+细胞(图2A),而SAG培养物含有73%的PV+细胞和7%的SST+细胞(图2B),因此在80:20和50:50的培养物中,PV+和SST+抑制性神经元的理论数量分别为21.6%和43.5%。然而,需要注意的是,纯培养物和混合培养物中PV+和SST+神经元的相对比例与皮质中观察到的不同,在皮质中,抑制性中间神经元PV:Sst:VIP的比例约为40:30:30(Druga等人,2023),因此这代表了一种人工实验条件。
我们首先分析了每个通道的平均放电率(MFR)、平均爆发率(MBR)和持续时间(MBD),以及爆发电极和随机尖峰的百分比。所有培养物的MFR均随时间增加,且它们之间没有显著差异(图4B;视频S1、S2、S3、S4和S5)。然而,在爆发活动中观察到明显差异。混合培养物的爆发电极数量多得多(图4C和4D,补充视频VS1、3、4),其中50:50和80:20培养物首先出现爆发(第33天),随后是SAG培养物(第39天),最后是CYC培养物(第45天)(图4E和4F)。与纯培养物相比,混合培养物的MBR和MBD也更高(图4E和4F),这表明将两种细胞类型结合可显著增强产生爆发活动的能力。尽管纯培养物的MFR与混合培养物相当(图4B),但其随机尖峰的百分比最高(图4G)。
纯CYC网络的黏附特性与SAG培养物不同(图S4G-S4I)。它们倾向于形成细胞簇(图S4G),且细胞层比SAG培养物更厚(图S4I),尽管两种培养物的平均细胞密度相当(图S4H),这表明它们的黏附性和连接性存在差异。这导致CYC培养物中的活性通道数量低于混合培养物和SAG培养物(图S4J)。然而,对双倍密度培养物的分析证实,CYC网络和80:20网络之间的活性差异并非由电极上的细胞比例引起(图S4K)。
由于SAG培养物中抑制性神经元占主导地位(80%为抑制性神经元),而CYC培养物中抑制性神经元仅占7%,因此抑制性神经元似乎在爆发活动的建立中起着关键作用。为了验证这一点,我们使用Izhikevich脉冲神经元模型(2006年)模拟了具有不同神经元E/I比率的自组织人工神经网络。该模型比更复杂的生物物理模型更简单、更快,非常适合研究大规模网络(Izhikevich和Edelman,2008年)。我们对具有不同E/I比率的1000个神经元网络的模拟显示,瞬时网络放电(INF,见方法)——在Izhikevich的公式中,这一指标与生物网络中观察到的爆发率最为接近——遵循与我们的生物网络相似的趋势:最大INF出现在E/I比率为800:200至500:500之间(图S4L)。尽管该模型旨在复制皮质兴奋性和抑制性神经元的兴奋性和连接特性,但它仍然是一种简化模型。尽管如此,两种截然不同的网络类型所得到的一致结果表明,E/I比率对爆发活动的影响是一种从复杂网络相互作用中产生的涌现特性,而非仅由单个神经元的特性决定。
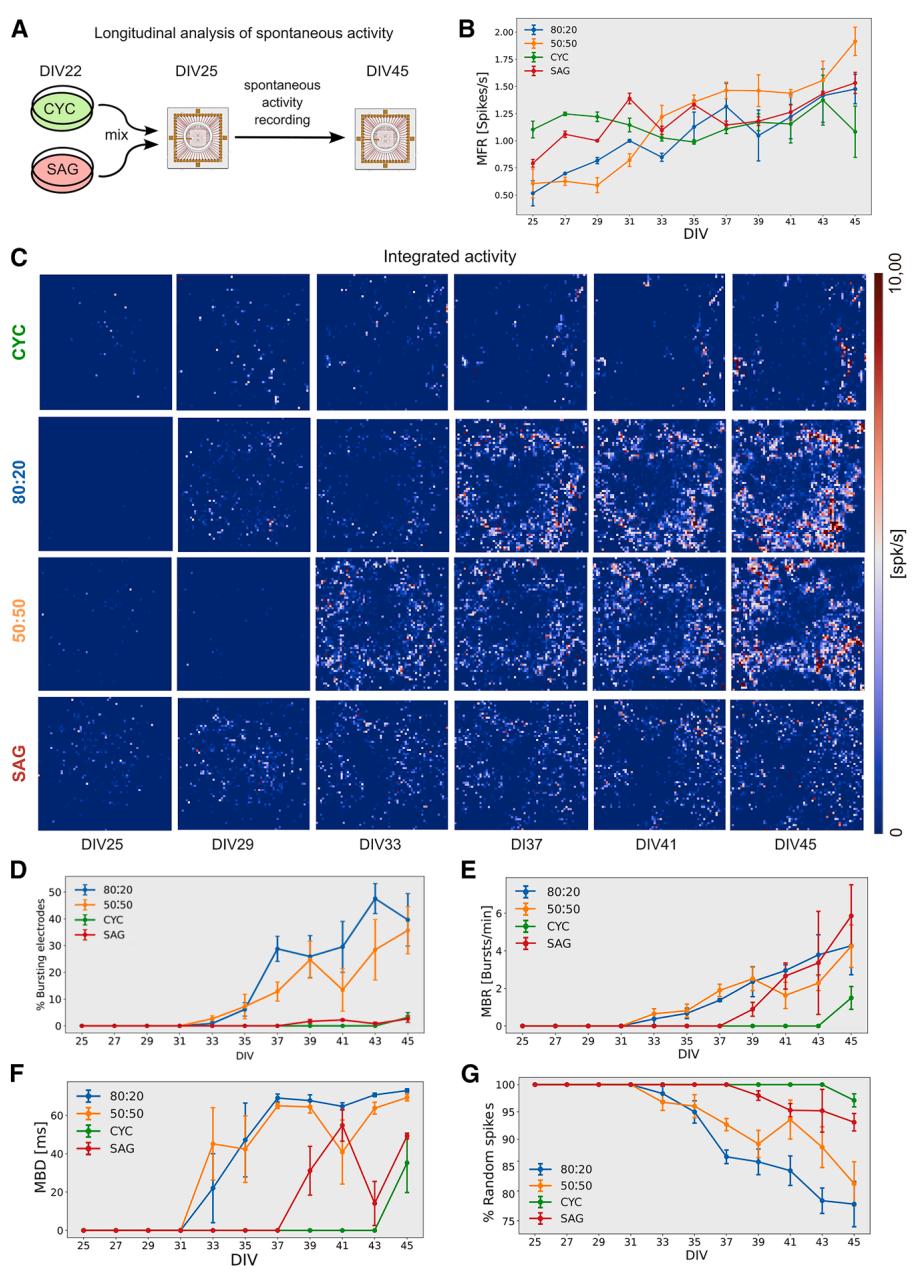
图4. CYC、SAG和混合培养物电生理活动的纵向分析
(A) 实验大纲。
(B) 单个通道随时间的平均发放率(MFR)(n=3次独立实验;显示平均值±标准误)。
(C)代表性高密度微电极阵列(HD-MEAs)的 firing rate(spk/s)热图;每个像素代表不同培养天数(DIV)下一个通道的整合活动(5分钟)。
(D-G)不同DIV时单个通道的爆发电极百分比、平均爆发率(MBR)、平均爆发持续时间(MBD)和随机尖峰百分比(n=3次独立实验;数据以平均值±标准误表示)。
¶ 纯CYC培养物和混合CYC与SAG培养物显示出不同的网络爆发活动模式
自发的网络活动是早期功能性网络发展的基础(Teppola等人,2019年),这种活动的一个关键特征是强烈的网络爆发(NBs)会反复出现,并在培养物中快速传播(Weihberger等人,2013年)。我们对培养物中的网络爆发进行了分析,发现它们首先出现在混合的CYC:SAG培养物中,从第31天开始;之后在纯SAG培养物中也有出现,不过程度很低,从第35天开始;而在纯CYC培养物中几乎没有出现(图5A和5B)。
在第45天(DIV45),四种培养物中的神经爆发持续时间(NBD)具有可比性(图5C),这表明该参数与神经爆发频率无关。尽管CYC和80:20培养物中PV+神经元比例均较低且谷氨酸能神经元比例均较高,但两者的神经爆发趋势存在差异,这提示它们的兴奋性/抑制性连接存在不同。因此,我们研究了GABA、AMPA和NMDA受体在成熟网络(DIV45)神经爆发发生中的作用。AMPA受体拮抗剂(CNQX)和NMDA受体拮抗剂(AP5)可阻断所有培养物中的神经爆发(图S5A-S5E),这与它们在爆发活动中的已知作用一致(Jimbo等人,2000年)。由于四种培养物的GABA能信号传导程度不同(主要是因为PV+和SST+中间神经元的比例不同),它们对GABAA受体拮抗剂荷包牡丹碱(BIC)的反应也不同。混合的80:20和50:50培养物在施用BIC后,神经爆发率略有增加,而纯CYC和SAG培养物的神经爆发率和持续时间均大幅增加(图5D-5F)。值得注意的是,CYC的神经爆发率甚至高于80:20培养物,这表明这种效应涉及新神经元的活动募集,且与细胞密度无关(见图S5F)。CYC培养物中虽然抑制性神经元数量较少,但这一观察结果表明PV+和SST+细胞的比例与神经爆发活动并不直接相关。我们认为,这可能是由于形成了不同的结构和功能连接模式,不过这一假设还需要进一步的实验验证。
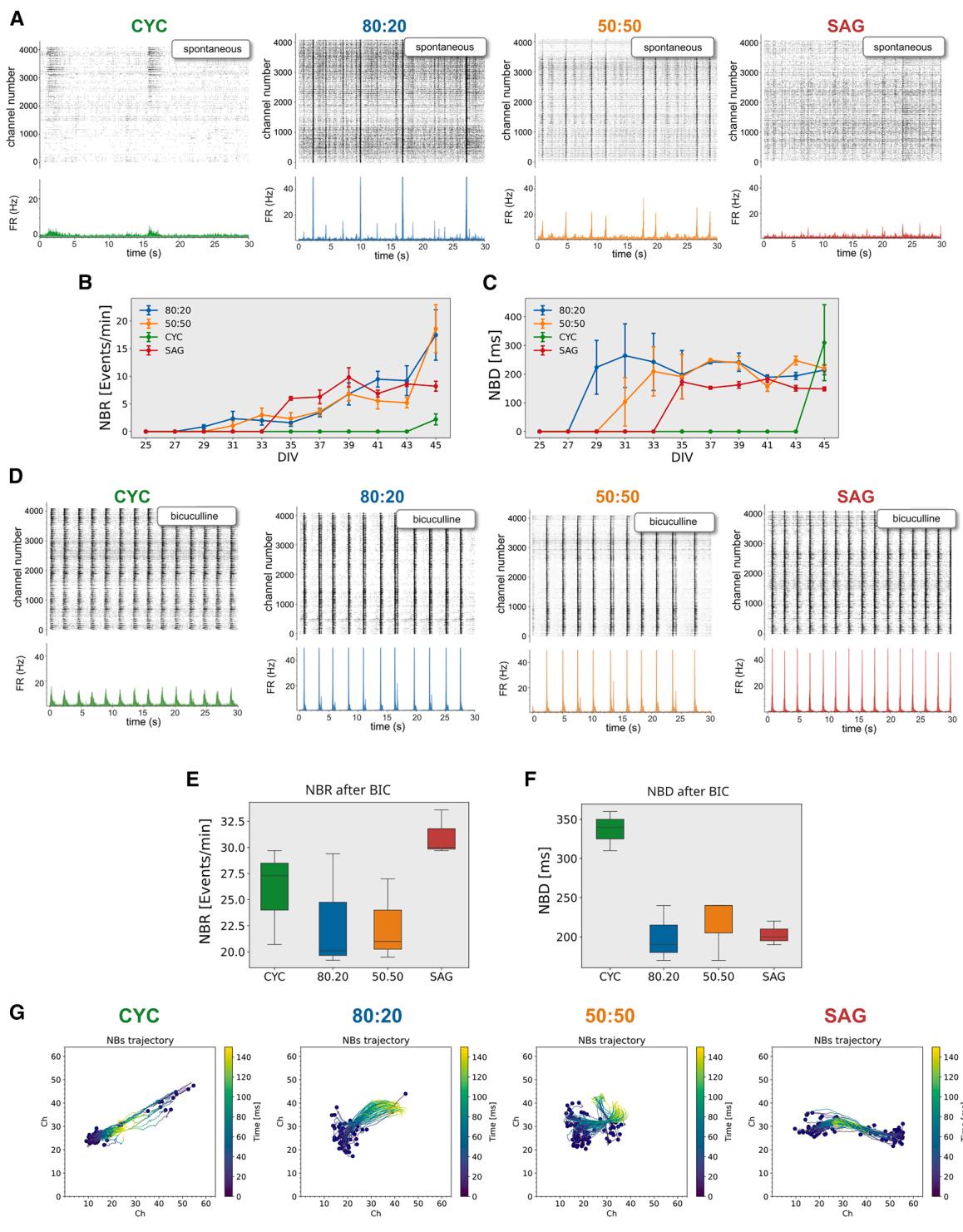
图5. GABA抑制对纯培养及混合培养的CYC和SAG细胞的网络活动有显著影响
(A)顶部:代表性高密度微电极阵列在分析终点(第45天)的活动光栅图(每个通道的尖峰时间);底部:平均网络放电率。
(B和C)网络突发率(NBR)和网络突发持续时间(NBD)(n=3次独立实验;数据以平均值±标准误表示)。
(D) 施用BIC后,按(A)项进行分析。
(E和F)BIC给药后的网络爆发率(NBR)和网络爆发持续时间(NBD)(n=3次独立实验)。
(G)活动轨迹中心(CATs)分析。每个蓝点代表NB开始时活动的物理质心,而彩色线条代表其自身的轨迹。彩色比例尺表示NB传播过程中经过的时间。
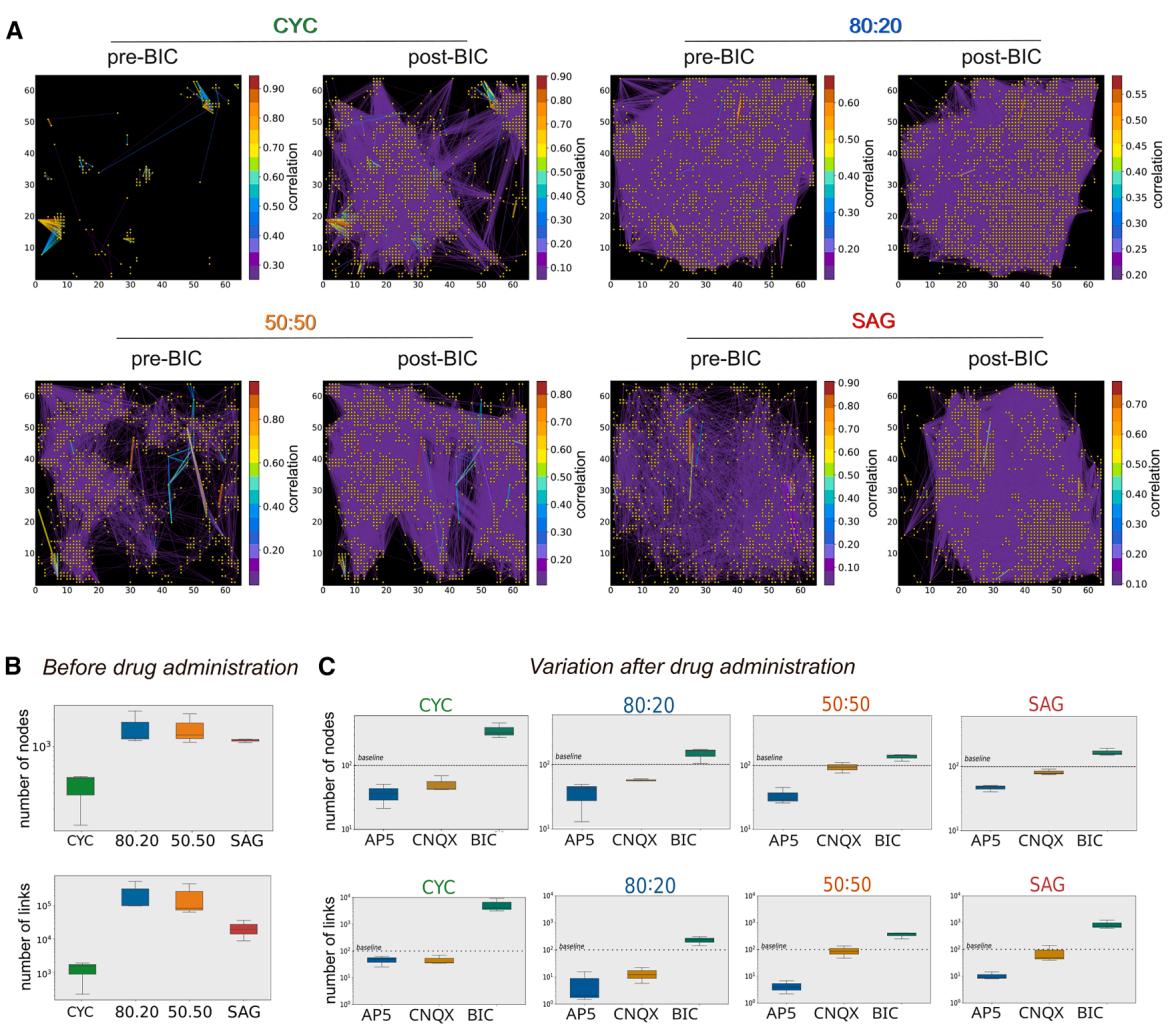
图6. GABA抑制揭示了CYC网络的复杂连接性
(A)具有代表性的神经元培养物在荷包牡丹碱(BIC)施用前(BIC施用前)和施用后(BIC施用后)自发活动期间的连接图。每个黄点代表功能图的一个节点;彩色线条代表两点之间的相关强度(仅显示10%的功能连接)。色条表示相关指数。
(B和C)分别为给药前后的节点数和连接数(n=3次独立实验)。
通过活动轨迹中心分析(Chao等人,2007年)来量化网络爆发事件,我们发现当抑制性活动被BIC抑制时,神经爆发(NBs)在所有四种培养物中以相似的特性传播(图5G)。总之,BIC似乎揭示了CYC和SAG培养物产生和传播神经爆发(NBs)的内在能力。
¶ γ-氨基丁酸能和谷氨酸能成分对纯的及混合的CYC和SAG功能网络的影响不同
由于GABA能抑制会掩盖纯培养物相比混合培养物的内在NB活性,我们研究了特定的功能连接分析是否能解释BIC对四种条件下NB活性的不同影响。我们比较了功能网络连接(即通道间的活动相关性)在施用BIC(图6A)、CNQX和AP5(图S6)前后的情况。相关性分析使我们能够计算自发网络活动的节点和连接数量(图6B)以及药物施用后它们的变化(图6C)。在没有药物的情况下,混合培养物的节点和连接数量相近,而SAG和CYC网络的节点和连接数量较少,其中CYC的数量最少(图6B)。每种药物对四种培养物的影响各不相同(图6C和图S6)。BIC对CYC培养物的影响最为显著,它显著增加了节点和连接的数量。这一点很重要,因为SAG培养物中PV+和SST+神经元的比例远高于CYC培养物。我们的结果表明,CYC功能网络中一个非常复杂的部分受到了强烈的GABA能抑制。这与研究结果一致,即PV+中间神经元可以显著影响锥体神经元的兴奋性活动,以补偿过度活跃的兴奋力量(Haider等人,2006;Xue等人,2014)。最后,与CYC和80:20培养物相比,CNQX对SAG和50:50培养物几乎没有影响,而AP5减少了所有培养物中的节点和连接数量,尽管程度不同(图6C)。这表明NMDA受体的活性在突触传递的发育调节中很重要,这也由AMPA和GABAA受体介导(Lu等人,2011;Marsden等人,2007),并且在建立NB活性和维持微妙的E/I平衡中起着关键作用。
¶ 网络刺激揭示了纯培养物和混合培养物不同的信号传播特性
我们分析了培养物中电刺激诱发的活动模式,并将其与自发活动模式进行了比较。在第50天(DIV50),我们用25个双相脉冲刺激单个通道。我们通过比较每个脉冲前后的尖峰计数,并对25次重复的反应取平均值来测量反应。单通道刺激在5毫秒的延迟内诱发了不同距离处通道的活动,这表明存在直接的功能连接(图7A和图S7A-S7D)。80:20的条件反应最强烈,刺激首先激活了大量正相关通道(图S7B中的红色通道),随后出现负相关通道(图S7B中的黄色通道)。在50:50和SAG培养物中,正相关活性通道的诱导程度适中,而与80:20培养物相比,负相关通道的出现更为明显且更早(图S7C和图S7D)。CYC培养物的表现有所不同,几乎所有被激活的通道都在5毫秒内被激活,负相关通道的出现有60毫秒的延迟,这更类似于80:20培养物(图S7A)。
我们还根据与刺激点的物理距离分析了信号的空间扩散(图7B中的扩散指数)。我们的研究结果揭示了刺激诱发信号的扩散指数与PV+细胞比例之间存在相关性。所有四种培养物在刺激后150毫秒时,扩散指数在0.3–0.4毫米左右都有一个共同的峰值。80:20的培养物总体反应最强,但在早期的扩散指数较低,这表明其有形成局部回路的趋势。相反,50:50和SAG培养物表现出更远距离的初始反应,但总体反应显著较低。我们推测,这些培养物中更强的抑制作用可能会在局部抑制初始反应,促使反应在离刺激部位更远的地方发生。我们得出结论,由于信号传播和抑制之间的平衡,中间比例的抑制性神经元能提供最佳的整体活性。
单通道刺激始终无法传播到整个网络并产生网络爆发(NBs)。我们推测,刺激足够数量的自发活动电极可能会诱发网络爆发。我们在每种培养物中选择了7个最活跃的通道进行同步刺激。在80:20、50:50和SAG条件下,电刺激诱发的同步网络活动与自发网络爆发相当(图7C-7E)。CYC培养物在刺激下未产生网络爆发(图7F):实际上,反应并未传播到受激活通道之外(图7F中 raster 图的放大细节)。这最后的观察结果表明,需要适当的抑制比例来整合和组织能够传播网络爆发的网络回路(Tremblay等人,2016年)。此外,我们评估了诱发的网络爆发持续时间(NBD)。在80:20配置中(图7C),其持续时间与自发网络爆发相似,网络几乎未发生变化。在50:50和SAG条件下,诱发的网络爆发持续时间短于自发网络爆发(图7D和7E)以及化学诱发的网络爆发(图5F)。这些发现表明,PV+中间神经元的存在显著影响神经元活动的扩散,进而影响网络连接性,并决定皮质网络产生同步网络爆发的能力。
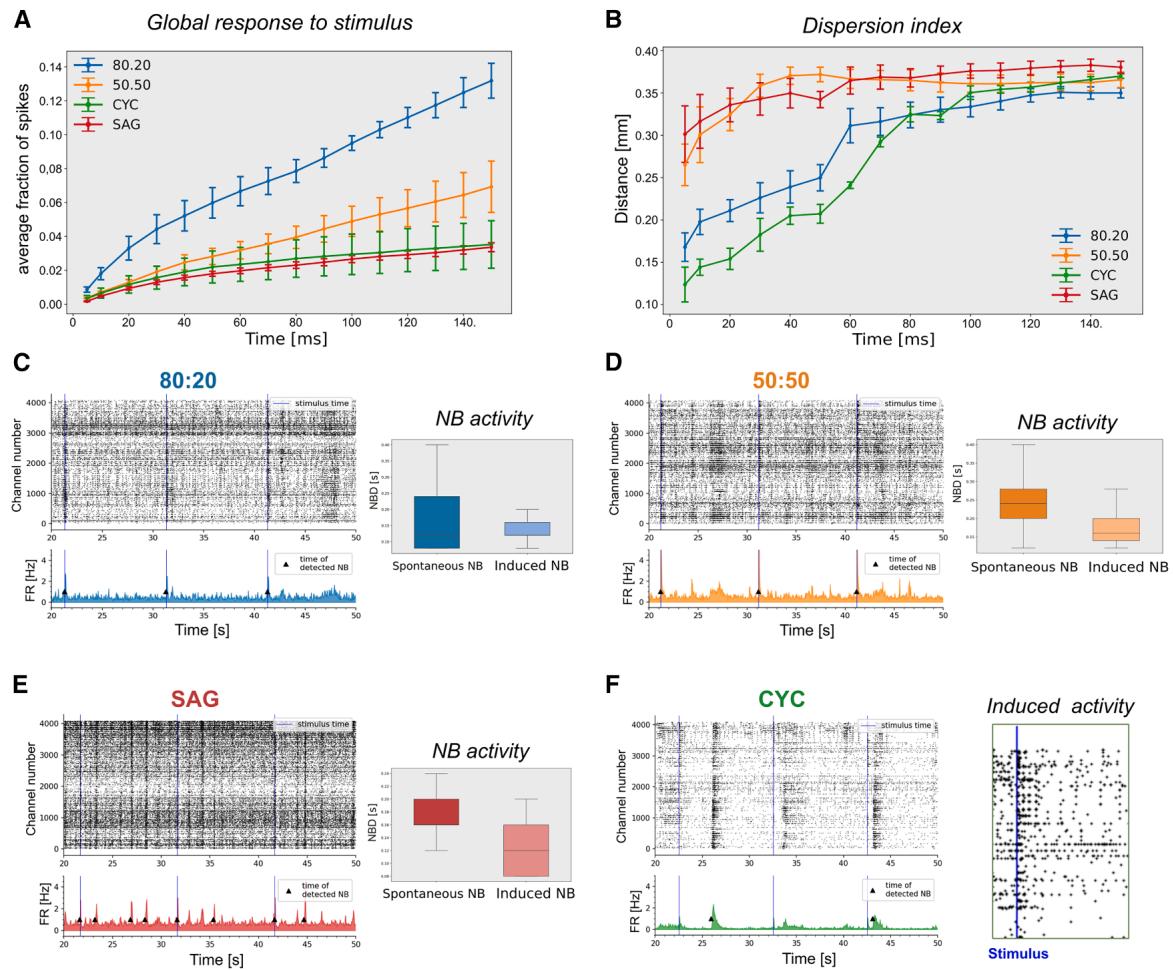
图7. 刺激诱发的整体反应、离散指数和神经元爆发受兴奋/抑制比率的影响
(A)单通道刺激的全局反应分布,显示了从5到150毫秒开始的尖峰平均比例(n=3次独立实验;显示平均值±标准误)。
(B) 分散指数表明在刺激后的不同时间点,反应与受刺激通道之间的距离(n=3次独立实验;数据以平均值±标准误表示)。
(C-F)代表性光栅图(C-F)和箱线图(C-E)分别显示了多电极刺激期间的NBs和NBD。刺激时间由蓝线标示。
(F)右侧:CYC光栅图的放大细节,仅突出显示对刺激有反应的电极(n=3次独立实验)。
¶ 讨论
我们研究了DT和VT神经元的单独培养物及混合培养物在体外如何生长和成熟。我们的分析表明,这些具有不同分子特性的培养物,也会形成不同的网络活动模式。
CYC和SAG培养物表达的关键标记基因与背侧丘脑(DT)和腹侧丘脑(VT)的特性一致,且成熟的PV+和SST+抑制性中间神经元比例相反:SAG培养物中这两种神经元的比例极高(分别为73%和7%),而CYC培养物中则极低(分别为7%和不足1%)。此外,CYC培养物中富含谷氨酸能vGlut1+神经元(73%),而SAG培养物中vGlut1+神经元仅占16%。我们观察到,分离的CYC和SAG神经元能在彼此的培养环境中成熟,这使我们能够研究具有不同兴奋/抑制(E/I)平衡的神经网络的活动特性。我们旨在了解生成能够产生自发性、相关性活动的神经元网络的基本要求,这种活动与早期脑区中观察到的现象相似(Chiu和Weliky,2001;Crochet等人,2005)。尽管纯CYC培养物和混合培养物的平均 firing 率(MFR)相似,但纯CYC培养物几乎没有相关性(爆发性)活动。当加入低比例的SAG神经元时,这种情况发生了改变:80:20的培养物表现出更强的同步放电模式。这也降低了随机尖峰的比例,增加了爆发性电极的数量,显著提高了网络爆发率(NBR)和网络爆发持续时间(NBD)。这是一个令人困惑的发现,因为含有80% PV+和SST+ GABA能神经元的SAG培养物自身几乎没有网络爆发活动。
Sukenik等人通过荧光激活细胞分选术,将E17小鼠胚胎的海马神经元分为GAD+和GAD-群体,随后将这些群体以不同比例接种到微流控培养室的神经胶质层上(Sukenik等人,2021年)。通过膜片钳分析,作者们观察到,在原代神经元培养物中,抑制性神经元比例的增加会导致单个神经元接收的活跃传入连接总数减少。这种机制使网络能够维持相似的兴奋/抑制(E/I)平衡,并因此稳定其自发性兴奋活动,以适应不同的细胞组成。虽然这一观察结果与我们在不同培养物中观察到的通道平均发放率(MFR)的相似值相符(图4B),但它无法解释E/I比例与同步网络活动之间缺乏比例关系的现象。因此,我们推测,需要适当比例的γ-氨基丁酸能神经元,才能使能够形成和传播爆发活动的局部电路成熟。我们的研究结果表明,在体外和计算机模拟的网络中,爆发活动在中等范围的E/I比例内达到峰值。这些截然不同的网络模型(即体内生物系统和计算机模拟系统)之间存在显著的一致性,这表明所观察到的E/I比例与爆发活动之间的关系不仅仅是单个神经元特征的总和。相反,它似乎是一种涌现特性,源于神经网络内部复杂而精密的相互作用。这强调了网络动态在塑造神经元活动模式中的关键作用,而不是仅仅将其归因于细胞的内在特性。然而,这一现象的机制解释仍有待通过计算机网络模型和生物网络来解决。
纯培养物和混合培养物中存在不同的回路,这一点可通过自发条件下、经BIC处理释放GABA能物质或电刺激时产生的不同类型网络活动得以体现。CYC培养物的自发NBR最低,但在BIC处理后与SAG培养物一同产生了最高的NBR,不过在电刺激下无法诱导出NB。这些观察结果,再加上CYC培养物显示出的最短离散指数,表明过高的E/I比值会形成不同的网络回路,这也证实了需要一个最佳的E/I比值才能形成能够产生和传播相关活动的局部抑制性网络。
迄今为止,很少有研究对具有精确兴奋/抑制(E/I)比率的皮质网络进行建模。研究人员通过微电极阵列(MEA)使用不同E/I比率的诱导神经元(iNeurons)来评估化合物的致痫性,发现84/16的E/I平衡最适合检测浓度依赖性变化,并对致痫化合物的作用机制进行分类(Yokoi等人,2022年)。有趣的是,与更高和更低的平衡相比,这种中间E/I平衡显示出最高的爆发(NB)活性,这与我们的观察结果一致,即中间E/I平衡更有利于爆发的产生。Yokoi及其同事观察到,具有最低E/I平衡的诱导神经元培养物活性最高,对γ-氨基丁酸(GABA)抑制剂的反应最低,这与我们在小鼠胚胎干细胞(mESC)培养物中的观察结果相反。这种差异的一个可能解释在于细胞亚型的不同特征和组成(即帕valbumin阳性(PV+)和生长抑素阳性(SST+)中间神经元的比例不同),以及两种培养物中形成的神经回路的连接性存在差异。其他研究小组也利用MEA记录来研究具有不同E/I平衡的人诱导多能干细胞(hiPSC)衍生网络(见引言)(Parodi等人,2023年,2024年)。这些研究使用了不同类型的诱导神经元,报告了具有最高E/I平衡(100:0)的网络的对比行为:在低密度MEA的情况下,其网络活性和爆发率(NBR)低于其他E/I平衡;而在高密度MEA的情况下,则高于其他E/I平衡。然而,与我们的培养物相比,诱导神经元的分子特性不同,特别是非端脑标志物的表达(Lin等人,2021年)以及帕valbumin阳性中间神经元的缺乏(Zhang等人,2013年)(见引言),这使得不同数据集之间难以进行比较。
在我们的研究中,我们通过考察各种网络传播刺激诱导活动的能力,拓展了对这些网络的分析,强调了兴奋/抑制平衡的关键作用。此外,我们的研究从两个层面分析了网络连接性:结构层面(树突分支和节点数量,图3)和功能层面(图4、图5、图6和图7)。通过考虑这些在以往研究中被忽视的网络参数,我们能够更好地解释具有不同兴奋/抑制平衡的网络中存在的不同活动模式。
我们目前的体外皮质网络模型源自体内观察,与完整的体内网络相比存在局限性。这些局限性包括PV+和SST+抑制性中间神经元的比例不同、缺乏VIP+神经元、没有丘脑传入纤维,以及普遍缺乏血管形成、小胶质细胞和精细的细胞复杂性。尽管存在这些差异,我们的研究结果表明,我们的模型相比基于iNeuron的模型具有显著优势,因为它能更忠实地再现谷氨酸能神经元和PV+中间神经元的皮质特性。将其应用于人类诱导多能干细胞时,它成为研究兴奋/抑制平衡在人类神经发育过程中对网络活动塑造作用的有力工具,尤其是在神经发育障碍的背景下。
¶ 方法
小鼠胚胎干细胞(mESCs)按照四步方案分化为背侧丘脑(DT)或腹侧丘脑(VT)谱系。第一步(第0-5天,DIV0–DIV5),细胞在添加了Wnt和BMP抑制剂(WiBi)的化学成分明确的基础培养基中培养,并接种在多聚鸟氨酸/层粘连蛋白包被(PL)的表面上。第二步(第6-10天,DIV6–DIV10),通过在WiBi培养基中分别添加环巴胺(3μM)和SAG(0.1μM),生成背侧丘脑和腹侧丘脑细胞。第三步(第11-20天,DIV11–DIV20),将细胞重新接种到PL包被的表面上,并在Neurobasal-A培养基中培养。从第20天(DIV20)起,神经元在添加了0.2mM抗坏血酸和20ng/mL重组人BDNF蛋白的Neurobasal-A培养基中培养。为了制备80:20和50:50的混合培养物,在特定时间点对神经元进行分离。为制备微电极阵列(MEA),在第22天(DIV22)将环巴胺(CYC)处理的神经元和SAG处理的神经元分离、计数,按设定比例混合后接种到灭菌的高密度微电极阵列(HD-MEA,Accura,3Brain)上(每芯片60,000个细胞),并培养过夜(O/N)使其贴壁。
使用ImageJ突触计数器插件(https://github.com/SynPuCo/ SynapseCounter)对谷氨酸能和γ-氨基丁酸能囊泡的密度进行定量分析。为了研究纯培养和混合培养中的神经元发育,在第7天(DIV7)用EGFP慢病毒转导CYC和SAG细胞,并通过嘌呤霉素抗性基因(PuroR)进行筛选。在第17天(DIV17),将EGFP标记的神经元和未标记的神经元混合,构建纯培养(仅环杷明、仅SAG)和混合培养(80:20、50:50)体系,每种培养体系中EGFP阳性细胞占1%,并接种在经多聚赖氨酸(PL)处理的玻璃上(150,000个细胞/cm²)。在第21天(DIV21)和第30天(DIV30),用2%多聚甲醛固定培养物,并通过免疫荧光进行分析。使用Fiji的SNT插件评估神经长度和节点数量。
使用基于高密度CMOS的4096微电极阵列(Accura,3Brain)进行电生理记录,以评估尖峰活动、爆发行为和网络同步。使用定制的Python脚本分析药物反应和功能连接性,并通过主成分分析和互相关方法进行 spike 分选和网络分析。
通过在规定的时间窗口(5–150毫秒)内比较刺激前后的峰值计数来测量对刺激的反应。刺激被重复25次,对反应进行平均,并计算统计置信区间。在数据可视化方面,反应在网格上显示,像素强度表示反应强度。离散指数用于量化显著反应在网格上的分布情况,其计算方法是估算有反应的电极之间的平均距离。
自组织人工神经网络建模按照Izhikevich于2006年描述的方法进行(参见补充方法)。
所有实验步骤的详细说明均在补充信息的方法部分提供。
¶ 资源可用性
¶ 主要联系人
如需更多信息以及资源和试剂的相关请求,请联系首席联系人费德里科·克雷米西(federico.cremisi@sns.it),他将予以回应。
¶ 材料可用性
本研究未生成新的独特试剂。不过,任何关于所使用的试剂或动物的问题都可以向主要联系人咨询。
¶ 数据和代码可用性
本研究未产生新的测序数据。有关基因表达实验的任何问题都可向主要联系人咨询。
¶ 致谢
我们感谢Robert Vignali和Lucio Calcagnile的有益讨论,感谢Maria Antonietta Calvello、Vania Liverani和Alessandro Puntoni提供的技术支持,感谢Michele Studer和Michele Bertacchi在标志物免疫检测分析方面的建议,以及Stefano Guglielmo、Claudia Alia和Nicola Origlia在培养网络功能分析方面的建议。本研究得到了Matteo Caleo基金会、意大利理工学院(L.P.)和高等师范学院(F.C.)的内部资金、意大利大学和研究部的PRIN grant #2022M95RC7(F.C.)以及托斯卡纳健康生态系统——MUR的THE grant(F.C.和A.D.G.)的支持。这项工作由欧盟——下一代欧盟基金资助,属于使命4组件1(CUP E53C24001460006),项目名称为TNE——NEUROBRIDGE,该项目承担了出版费用。
¶ 作者贡献
E.C.和F.C.构思并设计了本研究,还撰写了手稿。E.C.、F.T.和L.I.实施了实验。E.C.制定了培养处理策略、连接性分析以及纵向功能研究方案。F.T.设置了MEA刺激。L.P.构思了基因表达分析实验。L.I.在A.D.G.的指导下开展了MEA数据的时间序列分析。G.L.在G.A.的监督下进行了MEA刺激分析。M.F.构建了具有STDP的人工神经网络模型。所有作者都对研究结果进行了讨论,并对手稿提出了意见。
¶ 利益声明
作者声明不存在利益冲突。
¶ 补充信息
补充信息可在网上查阅:https://doi.org/ 10.1016/j.stemcr.2025.102646。
收到日期:2025年2月5日
修订日期:2025年8月26日
接受日期:2025年8月27日
发表时间:2025年9月25日
¶ 参考文献
- Bertacchi, M., Pandolfini, L., D’Onofrio, M., Brandi, R., & Cremisi, F. (2015). The double inhibition of endogenously produced BMP and Wnt factors synergistically triggers dorsal telencephalic differentiation of mouse ES cells. Developmental Neurobiology, 75, 66–79. https://doi.org/10.1002/dneu.22209.
- Cao, S.-Y., Hu, Y., Chen, C., Yuan, F., Xu, M., Li, Q., Fang, K.-H., Chen, Y., & Liu, Y. (2017). Enhanced derivation of human pluripotent stem cell-derived cortical glutamatergic neurons by a small molecule. Scientific Reports, 7, 3282. https://doi.org/10.1038/s41598-017-03519-w.
- Cederquist, G. Y., Asciolla, J. J., Tchieu, J., Walsh, R. M., Cornacchia, D., Resh, M. D., & Studer, L. (2019). Specification of positional identity in forebrain organoids. Nature Biotechnology, 37, 436–444. https://doi.org/10.1038/s41587-019-0085-3.
- Chambers, S. M., Fasano, C. A., Papapetrou, E. P., Tomishima, M., Sadelain, M., & Studer, L. (2009). Highly efficient neural conversion of human ES and iPS cells by dual inhibition of SMAD signaling. Nature Biotechnology, 27, 275–280. https://doi.org/10.1038/nbt.1529.
- Chao, Z. C., Bakkum, D. J., & Potter, S. M. (2007). Region-specific network plasticity in simulated and living cortical networks: comparison of the center of activity trajectory (CAT) with other statistics. Journal of Neural Engineering, 4, 294–308. https://doi.org/10.1088/1741-2560/4/3/015.
- Charlesworth, P., Cotterill, E., Morton, A., Grant, S. G. N., & Eglen, S. J. (2015). Quantitative differences in developmental profiles of spontaneous activity in cortical and hippocampal cultures. Neural Development, 10, 1. https://doi.org/10.1186/s13064-014-0028-0.
- Chen, J. K., Taipale, J., Cooper, M. K., & Beachy, P. A. (2002a). Inhibition of Hedgehog signaling by direct binding of cyclopamine to Smoothened. Genes & Development, 16, 2743–2748. https://doi.org/10.1101/gad.1025302.
- Chen, J. K., Taipale, J., Young, K. E., Maiti, T., & Beachy, P. A. (2002b). Small molecule modulation of Smoothened activity. Proceedings of the National Academy of Sciences of the United States of America, 99, 14071–14076. https://doi.org/10.1073/pnas.182542899.
- Chen, Y.-J. J., Friedman, B. A., Ha, C., Durinck, S., Liu, J., Rubenstein, J. L., Seshagiri, S., & Modrusan, Z. (2017). Single-cell RNA sequencing identifies distinct mouse medial ganglionic eminence cell types. Scientific Reports, 7, 45656. https://doi.org/10.1038/srep45656.
- Chiaradia, I., & Lancaster, M. A. (2020). Brain organoids for the study of human neurobiology at the interface of in vitro and in vivo. Nature Neuroscience, 23, 1496–1508. https://doi.org/10.1038/s41593-020-00730-3.
- Chiu, C., & Weliky, M. (2001). Spontaneous Activity in Developing Ferret Visual Cortex In Vivo. Journal of Neuroscience, 21, 8906–8914. https://doi.org/10.1523/JNEUROSCI.21-22-08906.2001.
- Crochet, S., Chauvette, S., Boucetta, S., & Timofeev, I. (2005). Modulation of synaptic transmission in neocortex by network activities. European Journal of Neuroscience, 21, 1030–1044. https://doi.org/10.1111/j.1460-9568.2005.03932.x.
- Dias, I., Levers, M. R., Lamberti, M., Hassink, G. C., Van Wezel, R., & Le Feber, J. (2021). Consolidation of memory traces in cultured cortical networks requires low cholinergic tone, synchronized activity and high network excitability. Journal of Neural Engineering, 18, 046051. https://doi.org/10.1088/1741-2552/abfb3f.
- Dickens, S., Goodenough, A., & Kwok, J. (2022). An in vitro neuronal model replicating the in vivo maturation and heterogeneity of perineuronal nets. bioRxiv Preprint. https://doi.org/10.1101/2022.01.22.477344.
- Fuccillo, M., Joyner, A. L., & Fishell, G. (2006). Morphogen to mitogen: the multiple roles of hedgehog signalling in vertebrate neural development. Nature Reviews Neuroscience, 7, 772–783. https://doi.org/10.1038/nrn1990.
- Gaspard, N., Bouschet, T., Hourez, R., Dimidschstein, J., Naeije, G., Van Den Ameele, J., Espuny-Camacho, I., Herpoel, A., Passante, L., Schiffmann, S. N., et al. (2008). An intrinsic mechanism of corticogenesis from embryonic stem cells. Nature, 455, 351–357. https://doi.org/10.1038/nature07287.
- Gelman, D. M., & Marín, O. (2010). Generation of interneuron diversity in the mouse cerebral cortex. European Journal of Neuroscience, 31, 2136–2141. https://doi.org/10.1111/j.1460-9568.2010.07267.x.
- Gelman, D., Griveau, A., Dehorter, N., Teissier, A., Varela, C., Pla, R., Pierani, A., & Marín, O. (2011). A Wide Diversity of Cortical GABAergic Interneurons Derives from the Embryonic Preoptic Area. Journal of Neuroscience, 31, 16570–16580. https://doi.org/10.1523/JNEUROSCI.4068-11.2011.
- Haider, B., Duque, A., Hasenstaub, A. R., & McCormick, D. A. (2006). Neocortical Network Activity In Vivo Is Generated through a Dynamic Balance of Excitation and Inhibition. Journal of Neuroscience, 26, 4535–4545. https://doi.org/10.1523/JNEUROSCI.5297-05.2006.
- He, H. Y., & Cline, H. T. (2019). What Is Excitation/Inhibition and How Is It Regulated? A Case of the Elephant and the Wisemen. Journal of Experimental Neuroscience, 13, 1179069519859371. https://doi.org/10.1177/1179069519859371.
- Izhikevich, E. M., & Edelman, G. M. (2008). Large-scale model of mammalian thalamocortical systems. Proceedings of the National Academy of Sciences of the United States of America, 105, 3593–3598. https://doi.org/10.1073/pnas.0712231105.
- Jimbo, Y., Kawana, A., Parodi, P., & Torre, V. (2000). The dynamics of a neuronal culture of dissociated cortical neurons of neonatal rats. Biological Cybernetics, 83, 1–20. https://doi.org/10.1007/PL00007970.
- Kempf, J., Knelles, K., Hersbach, B. A., Petrik, D., Riedemann, T., Bednarova, V., Janjic, A., Simon-Ebert, T., Enard, W., Smialowski, P., et al. (2021). Heterogeneity of neurons reprogrammed from spinal cord astrocytes by the proneural factors Ascl1 and Neurogenin2. Cell Reports, 36, 109409. https://doi.org/10.1016/j.celrep.2021.109409.
- Li, X.-J., Zhang, X., Johnson, M. A., Wang, Z.-B., LaVaute, T., & Zhang, S.-C. (2009). Coordination of sonic hedgehog and Wnt signaling determines ventral and dorsal telencephalic neuron types from human embryonic stem cells. Development, 136, 4055–4063. https://doi.org/10.1242/dev.036624.
- Lim, L., Mi, D., Llorca, A., & Marín, O. (2018). Development and Functional Diversification of Cortical Interneurons. Neuron, 100, 294–313. https://doi.org/10.1016/j.neuron.2018.10.009.
- Lin, H.-C., He, Z., Ebert, S., Schörnig, M., Santel, M., Nikolova, M. T., Weigert, A., Hevers, W., Kasri, N. N., Taverna, E., et al. (2021). NGN2 induces diverse neuron types from human pluripotency. Stem Cell Reports, 16, 2118–2127. https://doi.org/10.1016/j.stemcr.2021.07.006.
- Lodato, S., Rouaux, C., Quast, K. B., Jantrachotechatchawan, C., Studer, M., Hensch, T. K., & Arlotta, P. (2011). Excitatory Projection Neuron Subtypes Control the Distribution of Local Inhibitory Interneurons in the Cerebral Cortex. Neuron, 69, 763–779. https://doi.org/10.1016/j.neuron.2011.01.015.
- Lu, W., Gray, J. A., Granger, A. J., During, M. J., & Nicoll, R. A. (2011). Potentiation of Synaptic AMPA Receptors Induced by the Deletion of NMDA Receptors Requires the GluA2 Subunit. Journal of Neurophysiology, 105, 923–928. https://doi.org/10.1152/jn.00725.2010.
- Lupori, L., Totaro, V., Cornuti, S., Ciampi, L., Carrara, F., Grilli, E., Viglione, A., Tozzi, F., Putignano, E., Mazziotti, R., et al. (2023). A comprehensive atlas of perineuronal net distribution and colocalization with parvalbumin in the adult mouse brain. Cell Reports, 42, 112788. https://doi.org/10.1016/j.celrep.2023.112788.
- Marín, O. (2012). Interneuron dysfunction in psychiatric disorders. Nature Reviews Neuroscience, 13, 107–120. https://doi.org/10.1038/nrn3155.
- Marín, O., Valiente, M., Ge, X., & Tsai, L.-H. (2010). Guiding Neuronal Cell Migrations. Cold Spring Harbor Perspectives in Biology, 2, a001834. https://doi.org/10.1101/cshperspect.a001834.
- Marsden, K. C., Beattie, J. B., Friedenthal, J., & Carroll, R. C. (2007). NMDA Receptor Activation Potentiates Inhibitory Transmission through GABA Receptor-Associated Protein-Dependent Exocytosis of GABAA Receptors. Journal of Neuroscience, 27, 14326–14337. https://doi.org/10.1523/JNEUROSCI.4433-07.2007.
- Martynoga, B., Morrison, H., Price, D. J., & Mason, J. O. (2005). Foxg1 is required for specification of ventral telencephalon and region-specific regulation of dorsal telencephalic precursor proliferation and apoptosis. Developmental Biology, 283, 113–127. https://doi.org/10.1016/j.ydbio.2005.04.005.
- Mossink, B., Van Rhijn, J.-R., Wang, S., Linda, K., Vitale, M. R., Zöller, J. E. M., Van Hugte, E. J. H., Bak, J., Verboven, A. H. A., Selten, M., et al. (2022). Cadherin-13 is a critical regulator of GABAergic modulation in human stem-cell-derived neuronal networks. Molecular Psychiatry, 27, 1–18. https://doi.org/10.1038/s41380-021-01117-x.
- Nelson, S. B., & Valakh, V. (2015). Excitatory/Inhibitory Balance and Circuit Homeostasis in Autism Spectrum Disorders. Neuron, 87, 684–698. https://doi.org/10.1016/j.neuron.2015.07.033.
- Nery, S., Fishell, G., & Corbin, J. G. (2002). The caudal ganglionic eminence is a source of distinct cortical and subcortical cell populations. Nature Neuroscience, 5, 1279–1287. https://doi.org/10.1038/nn971.
- Parodi, G., Brofiga, M., Pastore, V. P., Chiappalone, M., & Martinoia, S. (2023). Deepening the role of excitation/inhibition balance in human iPSCs-derived neuronal networks coupled to MEAs during long-term development. Journal of Neural Engineering, 20, 056011. https://doi.org/10.1088/1741-2552/acf78b.
- Parodi, G., Zanini, G., Chiappalone, M., & Martinoia, S. (2024). Electrical and chemical modulation of homogeneous and heterogeneous human-iPSCs-derived neuronal networks on high density arrays. Frontiers in Molecular Neuroscience, 17, 1304507. https://doi.org/10.3389/fnmol.2024.1304507.
- Sohal, V. S., & Rubenstein, J. L. R. (2019). Excitation-inhibition balance as a framework for investigating mechanisms in neuropsychiatric disorders. Molecular Psychiatry, 24, 1248–1257. https://doi.org/10.1038/s41380-019-0426-0.
- Steiner, H., & Tseng, K.-Y. (2017). Handbook of Basal Ganglia Structure and Function. Elsevier Academic Press.
- Sukenik, N., Vinogradov, O., Weinreb, E., Segal, M., Levina, A., & Moses, E. (2021). Neuronal circuits overcome imbalance in excitation and inhibition by adjusting connection numbers. Proceedings of the National Academy of Sciences of the United States of America, 118, e2018459118. https://doi.org/10.1073/pnas.2018459118.
- Teppola, H., Ačimović, J., & Linne, M.-L. (2019). Unique Features of Network Bursts Emerge From the Complex Interplay of Excitatory and Inhibitory Receptors in Rat Neocortical Networks. Frontiers in Cellular Neuroscience, 13, 377. https://doi.org/10.3389/fncel.2019.00377.
- Terrigno, M., Busti, I., Alia, C., Pietrasanta, M., Arisi, I., D’Onofrio, M., Caleo, M., & Cremisi, F. (2018). Neurons Generated by Mouse ESCs with Hippocampal or Cortical Identity Display Distinct Projection Patterns When Co-transplanted in the Adult Brain. Stem Cell Reports, 10, 1016–1029. https://doi.org/10.1016/j.stemcr.2018.01.010.
- Tremblay, R., Lee, S., & Rudy, B. (2016). GABAergic Interneurons in the Neocortex: From Cellular Properties to Circuits. Neuron, 91, 260–292. https://doi.org/10.1016/j.neuron.2016.06.033.
- Watanabe, K., Kamiya, D., Nishiyama, A., Katayama, T., Nozaki, S., Kawasaki, H., Watanabe, Y., Mizuseki, K., & Sasai, Y. (2005). Directed differentiation of telencephalic precursors from embryonic stem cells. Nature Neuroscience, 8, 288–296. https://doi.org/10.1038/nn1402.
- Weihberger, O., Okujeni, S., Mikkonen, J. E., & Egert, U. (2013). Quantitative examination of stimulus-response relations in cortical networks in vitro. Journal of Neurophysiology, 109, 1764–1774. https://doi.org/10.1152/jn.00481.2012.
- Wonders, C. P., & Anderson, S. A. (2006). The origin and specification of cortical interneurons. Nature Reviews Neuroscience, 7, 687–696. https://doi.org/10.1038/nrn1954.
- Xue, M., Atallah, B. V., & Scanziani, M. (2014). Equalizing excitation–inhibition ratios across visual cortical neurons. Nature, 511, 596–600. https://doi.org/10.1038/nature13321.
- Yokoi, R., Shigemoto-Kuroda, T., Matsuda, N., Odawara, A., & Suzuki, I. (2022). Electrophysiological responses to seizurogenic compounds dependent on E/I balance in human iPSC-derived cortical neural networks. Journal of Pharmacological Sciences, 148, 267–278. https://doi.org/10.1016/j.jphs.2021.12.006.
- Zhang, Y., Pak, C., Han, Y., Ahlenius, H., Zhang, Z., Chanda, S., Marro, S., Patzke, C., Acuna, C., Covy, J., et al. (2013). Rapid Single-Step Induction of Functional Neurons from Human Pluripotent Stem Cells. Neuron, 78, 785–798. https://doi.org/10.1016/j.neuron.2013.05.029.
- Druga, R., Salaj, M., & Al-Redouan, A. (2023). Parvalbumin - Positive Neurons in the Neocortex: A Review. Physiological Research, 72(Suppl 2), S173-S191. https://doi.org/10.33549/physiolres.935005. PMID: 37565421; PMCID: PMC10660579.
- Izhikevich, E. M. (2006). Polychronization: computation with spikes. Neural Computation, 18(2), 245-282. https://doi.org/10.1162/089976606775093882. PMID: 16378515.