¶ 一种分层策略:保障人诱导多能干细胞(hiPSC)来源的功能化神经元类组织在大鼠完全性脊髓损伤修复中的安全性及移植物 - 宿主整合
Qing-shuai Wei 1,5,6、Yuan-huan 5,8 、Ke-jun Zhang1,2、Wen-tao Ma 1,2 、Hui-juan Shi5,7、Li-zhi Peng5,7、Jun-hua Wang5,7、 Qi-xing Hu 1,2 、 Hou-ge Li 1,2 、Ying Liu1,2、Bi-qin Lai5,7、Ge Li 5,9、Ying Ding5,7、Yuan-shan Zeng5,7,*、Xiang Zeng1,2,3,4,5,7,*
- 中医药创新研究与干细胞生物学实验室,广东省中医院/广东省中医药科学院/广州中医药大学第二附属医院,广州 510120,中国
- 国家干细胞临床研究机构,广东省中医院/广东省中医药科学院/广州中医药大学第二附属医院,广州 510120,中国
- 中医湿证国家重点实验室,广东省中医院,广州 510120,中国
- 广东省中医难治性慢性疾病防治重点实验室,广州 510120,中国
- 中山大学干细胞与组织工程中心,教育部干细胞与组织工程重点实验室,广州,中国
- 河南科技大学基础医学院与法医学院,洛阳 471023,中国
- 中山大学中山医学院组织学与胚胎学教研室,广州 510080,中国
- 华南理工大学附属广州市第一人民医院广州临床医学研究所,广州 510180,中国
- 广东省人民医院(广东省医学科学院)心血管疾病发病机制与靶向防治重点实验室,南方医科大学,广州 510100,中国
* 通讯作者:曾祥 国家干细胞临床研究机构,广州中医药大学第二附属医院,广州市番禺区大学城内环西路55号,广州 510006,中国 邮箱:zengxiang@gzucm.edu.cn
¶ 摘要
供体神经元与宿主神经通路的功能性整合是治疗脊髓损伤的关键方法。我们构建了携带胸苷激酶基因的人诱导多能干细胞源性神经类组织,将其移植至脊髓损伤大鼠体内。该神经类组织经三维明胶海绵支架培养28天后形成,体外实验证实其具备突触传递特性与神经网络功能。更昔洛韦作为胸苷激酶底物可选择性清除类组织中增殖细胞,同时保留有丝分裂静止的功能化神经元用于移植。经神经类组织治疗的脊髓损伤大鼠后肢运动功能显著恢复,电生理表现明显改善。移植八周后,大量供体细胞存活并弥散分布于整个损伤/移植区域,未出现明显远程细胞迁移,从而实现对损伤/移植区域的密集神经支配。该神经类组织所含的胆碱能人诱导多能干细胞源性神经元在损伤/移植区域存活,通过类突触连接成功与再生神经纤维及神经元整合。部分供体细胞分化为星形胶质细胞,与宿主血管内皮形成嵌合血髓屏障。此类神经类组织可作为结构与功能兼备的神经中继站,重建瘫痪肢体功能。本研究证实了具有安全调控机制的成熟神经组织移植治疗脊髓损伤的安全性与有效性,为未来组织工程化神经类组织的临床应用提供了框架。
¶ 关键词:
人诱导多能干细胞,神经元类器官,移植,运动功能恢复,脊髓损伤。
¶ 1. 引言
在成年哺乳动物中,脊髓损伤(SCI)会导致不可逆的组织损失,包括神经元和胶质细胞[1],从而引起损伤平面以下的运动、感觉及自主神经功能障碍[2]。继发性损伤造成的有限自发再生[3]与恶劣微环境[4],使得成年哺乳动物的内源性再生难以补偿受损组织。外源性神经移植物,包括干细胞疗法和组织工程技术,可能为重建脊髓损伤后的神经通路提供有前景的治疗策略[5,6]。近期,研究领域的鼓舞性进展揭示了外源性神经干细胞/前体细胞移植后具有神经保护[5,7]、免疫调节[8]和神经元替代[9]等潜在治疗能力。然而,供体细胞的单向迁移[10]、异位神经发生[11]及不确定分化[12]所引发的安全性问题阻碍了该方案的临床应用。为增强供体细胞留存及后续神经元分化,需对损伤微环境进行显著改造[13,14]。
在我们先前的研究中,我们采用组织工程学方法构建了干细胞衍生的神经网络组织,以提升安全性并消除供体细胞的不确定性分化问题[15]。将海马源性神经干细胞(NSCs)或骨髓源性间充质细胞(MSCs)衍生的神经网络组织移植到大鼠模型的损伤部位后,观察到供体细胞在损伤/移植部位存活八周,并参与神经通路的重建,且未在脊髓损伤后发生异位迁移。更重要的是,移植后瘫痪后肢的自主运动功能得到显著改善[16,17]。此外,在具有大面积脊髓组织缺损的犬模型中,成功验证了移植NSC或MSC源性神经网络组织的安全性与有效性[18,19]。这些结果表明,通过组织工程方法产生的干细胞源性神经元移植是修复脊髓损伤的一种前景广阔的策略。
然而,我们先前研究中的细胞来源仅限于成体多能干细胞。胚胎/多能干细胞衍生神经元在脊髓损伤治疗中的安全性和有效性尚待充分研究。诱导多能干细胞(iPSCs)因其易获得性、无伦理限制以及多向分化潜能[20–22],可能成为人类神经修复中极具吸引力的替代细胞来源。近期越来越多的证据表明,移植人源iPSC(hiPSC)衍生的神经祖细胞(hNPCs)能够与宿主神经通路整合,促进自主运动功能恢复[23,24]。但完全神经元成熟所需的漫长周期[25,26]可能影响该方法的治疗效果[25],因为人类神经干细胞或hNPCs可能保留其内在的人类发育速率[27]。
有鉴于此,有必要验证人诱导多能干细胞(hiPSC)来源的神经元移植能否在脊髓损伤(SCI)中实现更早期的功能恢复。由于移植物中存在未分化的多能细胞,且为降低移植后畸胎瘤形成风险,必须建立高效的in vitro诱导系统并实施严格的筛选流程以消除致瘤性。因此,本研究采用分步策略确保移植安全性与移植物-宿主整合,包括构建基于自杀基因的安全细胞系统、分步诱导神经元分化、组织样培养以及生物支架内细胞接种。分析显示供体细胞在脊髓损伤/移植部位存活良好,未见异位迁移或畸胎瘤形成。此外,移植的神经元成功整合入宿主神经通路,作为“神经元中继”修复了完全性脊髓损伤大鼠瘫痪后肢的运动功能。
¶ 2. 方法
¶ 2.1. 道德声明
所有动物实验均经中山大学实验动物伦理委员会(批准号:SYSU-IACUC-2018-000273)和广州中医药大学第二附属医院(批准号:2023119)审查批准。动物福利规程严格遵循中华人民共和国国家质量监督检验检疫总局与中国国家标准化管理委员会联合发布的实验动物福利伦理审查指南。我们已尽一切努力减少动物痛苦并控制样本数量。
¶ 2.2. 人诱导多能干细胞系的维持
该hiPSC细胞系由中山大学教育部干细胞与组织工程重点实验室提供[28],并在Matrigel®(美国纽约康宁公司)包被的6孔板中,使用mTESRTM1培养基(加拿大不列颠哥伦比亚省温哥华STEMCELL Technologies公司)于 、含 的条件下培养,每日更换培养基。为鉴定多能性,将hiPSCs在室温下用0.1M磷酸缓冲液(PB, )配制的 多聚甲醛固定1小时,随后进行Nanog、八聚体结合转录因子4(OCT4)的免疫荧光染色。
对经MycAway®支原体实时荧光定量PCR检测试剂盒(2G)(中国上海,Yeasen Biotechnology(Shanghai) Co., Ltd.)验证无支原体污染的人诱导多能干细胞进行了配对盒6(Pax6)和SRY盒转录因子1(Sox1)检测。
¶ 2.3. 诱导人多能干细胞来源的人类神经前体细胞/神经元
人诱导多能干细胞(hiPSCs)按照制造商说明书,使用STEMdiff SMADi神经诱导培养基(STEMCELL Technologies公司,加拿大不列颠哥伦比亚省温哥华)分化为人类神经祖细胞(hNPCs)。简而言之,将hiPSCs接种于Matrigel®包被的6孔板中,使用STEMdiff SMADi神经诱导培养基培养,每日更换培养基。神经诱导效率在14天内通过形态学评估确认。对于免疫表型鉴定,在24小时或14天时使用 多聚甲醛的0.1M PB( )固定衍生细胞,随后采用针对hNestin、Sox1和Nanog(阴性筛选标志物)的抗体进行免疫荧光染色。扩增后的hNPCs随后在神经祖细胞培养基(STEMCELL Technologies公司,加拿大不列颠哥伦比亚省温哥华)中维持培养,每日更换培养基。
神经元分化采用神经元诱导培养基进行,该培养基包含: (V/V)DMEM/F12(Gibco(Thermo Fisher Scientific),美国纽约州格兰德岛)、 (V/V)NeurobasalTM-A(Gibco,美国纽约州格兰德岛)、 (V/V)N-2补充剂(Gibco,美国纽约州格兰德岛)、 (V/V)B-27补充剂(Gibco,美国纽约州格兰德岛)、 BDNF(R&D Systems, Inc.(Bio-Techne旗下品牌),美国明尼苏达州明尼阿波利斯)以及 db-cAMP(Millipore Sigma,美国马萨诸塞州伯灵顿),用以诱导hNPCs分化为神经元,方法如前所述[29]。简言之,将hNPCs接种于层粘连蛋白包被的24孔板中,使用神经元诱导培养基培养,每隔一天更换培养基。14天后,用含 多聚甲醛的0.1M PB( )固定hNPCs分化产生的细胞,随后采用抗微管相关蛋白2(MAP2)、神经丝蛋白200(NF200)、神经元核抗原(NeuN)、 -微管蛋白III(Tuj1)、生长相关蛋白43(GAP43)以及胶质纤维酸性蛋白(GFAP)的抗体进行免疫荧光染色。
¶ 2.4. 表达GFP-TK的人类神经祖细胞(hNPCs-GFP-TK)的制备
该hiPSC细胞系通过重组慢病毒载体进行转导,载体携带由EF1α启动子调控的增强型GFP-胸苷激酶(TK)(Len-EF1 -GFP-TK),感染复数(MOI)为1。转导过程在mTeSR™1培养基中进行,培养基添加了 微克/毫升的聚凝胺(美国马萨诸塞州伯灵顿Millipore Sigma公司)和 微克/毫升的Y-27632二盐酸盐(英国布里斯托尔Tocris Bioscience公司),持续24-48小时。病毒转导后,在使用 微克/毫升的博莱霉素S盐酸盐(美国纽约州格兰德岛Gibco公司)进行筛选前,通过荧光显微镜确认GFP-TK表达,直至表达GFP-TK的hiPSC细胞比例达到 。随后通过流式细胞术进行荧光激活细胞分选,使用 的激发/发射波长,进一步富集表达GFP-TK的细胞群体。
FACS分选纯化的hiPSCs-GFP-TK细胞在启动神经分化前进行扩增,具体方法如第2.3节所述。在诱导后第14天,使用针对确定性神经祖细胞标志物(Sox1、Pax6和hNestin)的抗体进行免疫荧光分析。
¶ 2.5. 使用TK-GCV系统消除增殖细胞
接下来,我们定量评估了更昔洛韦(GCV)的细胞毒性以及TK-GCV系统在清除增殖细胞方面的功效。将hiPSCs-GFP-TK、hNPCs-GFP-TK、野生型hiPSCs和野生型hNPCs以同等密度接种于Matrigel®(美国纽约州康宁公司)包被的24孔板中。细胞贴壁24小时后,对各组设置三个复孔分别给予梯度浓度的更昔洛韦(GCV:0、3、10和 )。在标准培养条件( 、 CO2)下培养七天后,用4%多聚甲醛(PFA)固定细胞,细胞核以Hoechst 33342(美国马萨诸塞州伯灵顿Millipore Sigma公司)进行复染。使用蔡司LSM 800共聚焦显微镜(德国奥伯科亨卡尔·蔡司股份公司)对每孔五个非重叠视野进行系统成像。通过ImageJ软件(美国马里兰州贝塞斯达国立卫生研究院)完成细胞核定量分析。以 GCV对照组的平均细胞计数作为基线(定义为 存活率)对细胞活性进行标准化。各浓度下的存活率按以下公式计算:存活率 ) 。
接下来,我们建立了标准曲线以定量评估hNPCs和hiPSC衍生神经元中残留的未分化hiPSCs 。将hiPSCs与HaCaT角质形成细胞按比例(1:1,000;1:5,000;1:10,000;1:50,000;1:100,000)进行系列稀释后,铺板于Matrigel®(美国纽约州康宁公司)包被的24孔板中。随后使用FastPure Cell/Tissue Total RNA Isolation Kit(中国南京诺唯赞生物科技股份有限公司)分离总RNA,并通过HiScript III RT SuperMix for qPCR(中国南京诺唯赞生物科技股份有限公司)进行cDNA合成。接着在QuantStudio 5系统(美国纽约州格兰德岛赛默飞世尔科技公司)上使用ChamQ Universal SYBR qPCR Master Mix(中国南京诺唯赞生物科技股份有限公司)进行实时定量PCR(qPCR)。经GCV处理后,通过使用以下验证引物测量Teratocarcinoma-Derived Growth Factor 1(TDGF1,基因ID:6997)的表达来确定残留hiPSC污染程度:正向引物5’-TTTGAACTGGGATTAGTTGCCG-3’;反向引物5’-GGGGCCAAATGCTGTCATCT-3’。如上所述,在hiPSCs-GFP-TK衍生的神经元中残留的增殖细胞。相较于OCT4[30],TDGF1被证明在检测残留多能干细胞比例方面更为可靠。
¶ 2.6. 人诱导多能干细胞来源的神经组织样体(Ntoids)构建
三维明胶海绵支架(3D-GS)的制备方法参照先前文献[31]。简言之,将圆柱形3D-GS支架(直径3毫米,长度2毫米)进行环氧乙烷灭菌。在细胞接种至3D-GS前,将支架置于含 克/毫升层粘连蛋白的神经元诱导培养基中浸泡12小时。
总共将 个人源神经前体细胞悬置于 升神经元诱导培养基中,并接种至3D-GS系统。为优化细胞粘附,将植入hNPCs的3D-GS在24孔板中 孵育10分钟,随后加入 升神经元诱导培养基;30分钟后再补加 升神经元诱导培养基。培养期间每48小时更换培养基。分化14-28天后,按前述方法固定神经元样体,并使用系列神经元标志物进行染色:MAP2、突触素I(Syn1)、钠通道蛋白( )、钙通道蛋白(CaV)、胆碱乙酰转移酶(ChAT)、谷氨酸(Glu)及 -氨基丁酸(GABA)。
hNPCs-GFP-TK 被用于构建可移植的类器官。经过14至28天的分化过程中,每个批次进行随机支架取样( ),并通过Tuj1免疫荧光定量检测,以在in vivo植入前确认 的神经元分化效率。
¶ 2.7. 扫描电子显微镜(SEM)分析
采用扫描电子显微镜(SEM)研究Ntoids内的细胞黏附动力学与形态特征。样品经0.1MPB缓冲液( )三次清洗后,置于含 戊二醛的0.1M PB缓冲液( )中 固定4小时;再次使用0.1M PB缓冲液( )清洗三次,并通过梯度乙醇( 、 、 、 )以10分钟为间隔进行脱水处理。干燥后的Ntoids经金膜镀覆后,使用飞利浦场发射扫描电镜(荷兰埃因霍温)在 加速电压、 工作距离条件下,于高真空模式( )下进行成像观察。
¶ 2.8. 透射电子显微镜(TEM)分析
采用透射电子显微镜分析Ntoids中hiPSC源性神经元间的突触连接。分化14-28天后,将Ntoids用0.1M PB 清洗三次,置于含 戊二醛的0.1M PB 中 固定4小时,室温下 锇酸处理1小时,并按梯度乙醇浓度( 、 、 、 )以10分钟间隔脱水。干燥后的Ntoids在室温下于Epon树脂中浸渍过夜, 聚合48小时。最后用超薄切片机制备超薄切片,通过透射电镜(荷兰皇家飞利浦电子公司,埃因霍温)进行观察。
¶ 2.9. 体外电生理学
采用全细胞膜片钳技术研究Ntoids中hiPSC衍生神经元的功能成熟情况。分化28天后,使用EPC Amplifier 10放大器与Patchmaster软件(HEKA Elektronik公司,德国朗根)采集电信号,电极电阻为3-5兆欧 。细胞外液含5mM KCl、 、 、2mM CaCl2、10mM HEPES及 葡萄糖(渗透压 ; )。实验在室温下记录Ntoids中hiPSC衍生神经元的电生理活动,所有药物均通过微量灌流系统施加。细胞接受动作电位测试电位诱导和自发性兴奋性突触后电流 (sEpSC) 的生成。所有数据均使用 Mini Analysis 软件(美国新泽西州利奥尼亚 Synaptosoft 公司)进行采集和分析。
利用高密度微电极阵列系统(HyperCAM Alpha,3Brain,瑞士)对Ntoids进行场电位与神经连接组分析。将Ntoid从培养板轻柔转移至芯片电极区域中心(使用3Brain公司的CorePlate™ 6W-3D三维微电极芯片),精细调整Ntoid位置以覆盖尽可能多的电极区域。轻柔加入500微升Ntoid培养基以维持类器官湿润度,采用专用样本压网进行组织固定。每个样本连续记录5分钟,记录结束后使用BrainWave5软件(3Brain)进行电生理数据分析。
¶ 2.10. 外科手术与移植
在手术前三天,对成年雌性Sprague-Dawley(SD)大鼠(体重180-200克)每日皮下注射他克莫司( )、霉酚酸酯( )和泼尼松( )。所有大鼠均通过腹腔注射戊巴比妥钠( )进行深度麻醉,并监测趾夹反射。在手术显微镜下完成T10全椎板切除术,暴露 脊髓节段;随后采用硬膜外显微外科技术完整切除 的脊髓组织段(含附着神经根)。将培养14天的Ntoids(Ntoid组, )、负载hNPC的3D-GS(hNPCs组, )或无细胞负载的3D-GS(GS组, )植入脊髓缺损处。另设对照组使用非TK-GCV的hNPC负载3D-GS( )进行预实验。彻底止血后逐层缝合肌肉与皮肤。术后给予全面护理:每日肌注青霉素( )连续3天,并皮下注射生理盐水( 日)持续7天。所有动物每日接受三次人工排尿直至自主排尿功能重建。连续8周每日给予免疫抑制剂:他克莫司( )、霉酚酸酯( )及泼尼松( )。
所有动物在手术前均接受训练,使其能够爬上 倾斜网格并自由探索开放场地。术后连续三天及每周均进行Basso、Beattie和Bresnahan(BBB)测试[32]。在开放场地运动能力测试中,所有动物被允许自由探索场地5分钟,以评估后肢运动频率、关节活动范围、承重能力及协调性。最后一周进行 倾斜网格测试[33],根据Ramon-Cueto等人既往报道的方法,定性评估足部定位准确性与协调性。
¶ 2.12. 电生理学
术后八周,记录皮层运动诱发电位(CMEPs, 只/组),采用Neuro-Exam M-800数据采集分析系统(中国珠海Medcom科技有限公司)评估移植Ntoids重建的皮质运动通路的功能连接性。所有大鼠通过吸入含 ( )异氟烷的空气(400-600毫升/分钟)进行麻醉,并使用恒温垫将核心温度维持在 。所有大鼠接受以Bregma为参考点的开颅手术以暴露感觉运动皮层(SMC)。钻孔期间采用持续生理盐水灌注以保持组织水合。刺激电极置于感觉运动皮层(SMC),记录电极则与后肢坐骨神经连接。通过对SMC进行电刺激记录CMEPs,每只动物接受五次单脉冲刺激( ,50毫秒持续时间)。
¶ 2.13. 组织处理
所有动物于术后八周实施安乐死。通过腹腔注射 戊巴比妥钠( )对动物进行深度麻醉,随后用肝素化生理盐水(含 NaNO2、 肝素)进行心内灌注,再用 PBS( )配制的 多聚甲醛(PFA)灌注。取出脊髓并在相同固定液中后固定24小时,随后置于 PB配制的 蔗糖溶液中浸泡两天,再转入 PB配制的 蔗糖溶液中于 下保存5天。将T8-T12节段脊髓连续组织包埋于最佳切削温度(OCT)化合物中,使用CryoStar NX50冷冻切片机(赛默飞世尔科技,美国纽约州格兰德岛)纵向切割为 厚切片。
¶ 2.14. 免疫荧光染色
免疫荧光染色按先前描述进行。简言之,切片在 下用 山羊血清封闭1小时,随后依次与一抗( 过夜)及种属匹配的二抗( 、1小时)孵育;抗体规格详见附表1。封片前使用Hoechst 33342(Hoe)进行核复染。成像使用蔡司LSM 800共聚焦显微镜采集,所有样本均采用一致的参数设置。
¶ 2.15. 形态学定量分析
接下来,我们通过in vitro实验定量评估hiPSCs的多能性维持能力,并通过对比多能性标志物(Nanog+或Oct4+)及hNPCs标志物( 或Sox1+)与Hoe+细胞总数的比值来确定维持效率。为定量评估hiPSCsin vitro的神经分化潜能,通过对比hNPCs标志物(Pax6+、Sox1+或hNestin⁺)、神经谱系标志物(MAP2+或GFAP⁺)和多能性标志物(Nanog+或 )与Hoe+细胞总数的比值来量化hNPCs的分化效率。为定量评估hNPCsin vitro的神经元分化能力,通过对比神经元标志物( 、Sox1+或hNestin⁺)、神经谱系标志物( 、 、NeuN+和Tuj1+)以及星形胶质细胞标志物( )与Hoe+细胞总数的比值来量化神经元的分化效率。所有免疫染色实验均包含三次技术重复与三次生物学重复,标志物特异性均通过同型对照染色进行验证。
为了定量评估供体细胞in vivo的存活情况,我们通过计算脊髓损伤/移植物(I/G)区域内GFP⁺像素面积与总区域的比值来量化GFP荧光密度。此外,通过计算hNu +细胞数量占Ho 细胞总数的比例,对人核抗原( )阳性细胞的比例进行了量化。为定量评估供体细胞的神经元分化程度,通过计算 或Tuj1⁺面积与I/G区域总面积的比例,对NF和Tuj1荧光密度进行了量化。同时,通过计算NeuN⁺细胞数量与Hoe+细胞总数的比值,对NeuN +阳性细胞的比例进行了量化。为定量评估供体细胞的轴突投射情况,对从供体细胞延伸出的GFP+突起(长度 )数量进行了统计,分别在 、 及损伤部位尾侧 处。为量化阳性百分比,从每只动物的全部连续切片中每隔五张选取一张( ${ \bf \dot { \rho } } _ { n } = 5 $ )。
所有高分辨率图像均使用LSM800共聚焦激光扫描显微镜获取。定量图像分析采用Adobe Photoshop软件(美国加利福尼亚州圣何塞市Adobe系统公司)的批量处理阈值工具进行,以确保结果一致性。
¶ 2.16. 统计分析
所有定量数据均采用Student’s t检验或单因素方差分析(ANOVA)进行处理,结果以平均值 标准差表示,并使用SPSS 22.0版软件(美国IBM公司,阿蒙克)进行分析。方差齐性时采用最小显著差异法(LSD)检验;方差不齐时则使用Dunnett’s T3事后检验。显著性水平设定为 。
¶ 3. 结果
¶ 3.1. 神经元类组织体的逐步构建
由人诱导多能干细胞(HiPSCs)衍生的神经元组织样结构通过神经祖细胞(NPC)诱导阶段和基于生物支架的神经组织样结构(Ntoid)构建阶段制备而成(图1A)。经过诱导后,hiPSCs从多能阶段转变为神经祖细胞阶段(补充图1),在二维(2D)诱导14天后呈现 的hNestin表达(图1B、D)、 的Sox1表达(图1C、D)、 的Pax6表达(补充图2C、G)及可忽略的Oct4表达(补充图2E、G)。此过程获得了高纯度的人神经祖细胞(hNPCs),其具备高达10代的强增殖能力和显著的神经元分化潜能。随后,将hNPCs接种于细胞培养皿中诱导神经元分化。14天后,细胞高表达神经元标志物,如MAP2( ,补充图2H、N)、NF200( ,补充图2I、N)、NeuN( ,补充图2J、N)、Tuj1( ,补充图2K、N)以及生长神经纤维标志物GAP43(补充图2M),而星形胶质细胞标志物GFAP表达比例较低( ,补充图2L、N)。接着,将第3-6代(P3-6)的hNPCs接种于具有良好细胞相容性的3D-GS支架中进行Ntoid构建。14天后,Ntoids高表达神经元标志物,如NF(图1F)与Tuj1(图1G)的结果表明,Ntoid主要来源于神经元群体。
为验证神经元与神经功能之间的关系,我们接着对Ntoids进行了形态学和电生理学分析(图1A)。扫描电镜显示海绵状支架内部存在细胞团簇聚集。相邻团簇中的细胞通过类似网络结构的神经突束相互连接(图1J)。支架中细胞神经突束与连接的数量从14天到28天逐渐增加(图1J、K)。免疫染色显示,团簇中的细胞主要是MAP2免疫阳性神经元,且大量共染色突触标记物Syn1(图1L-L1)。成熟突触结构的出现通过透射电镜进一步验证,电镜结果显示突触前成分中存在圆形突触囊泡和增厚的膜结构。突触后成分中亦观察到致密的突触后区域——这是不对称兴奋性突触的典型特征(图1M-N1)。该突触结构属于不对称兴奋性突突。Ntoids中ChAT(图1H)与Glu(图1I)免疫阳性神经元比例显著高于GABA免疫阳性神经元(补充图2Q)。此外,免疫染色显示钠通道蛋白(NaV,补充图2O)和钙通道蛋白(CaV,补充图2P)均在Ntoids的神经元中表达。
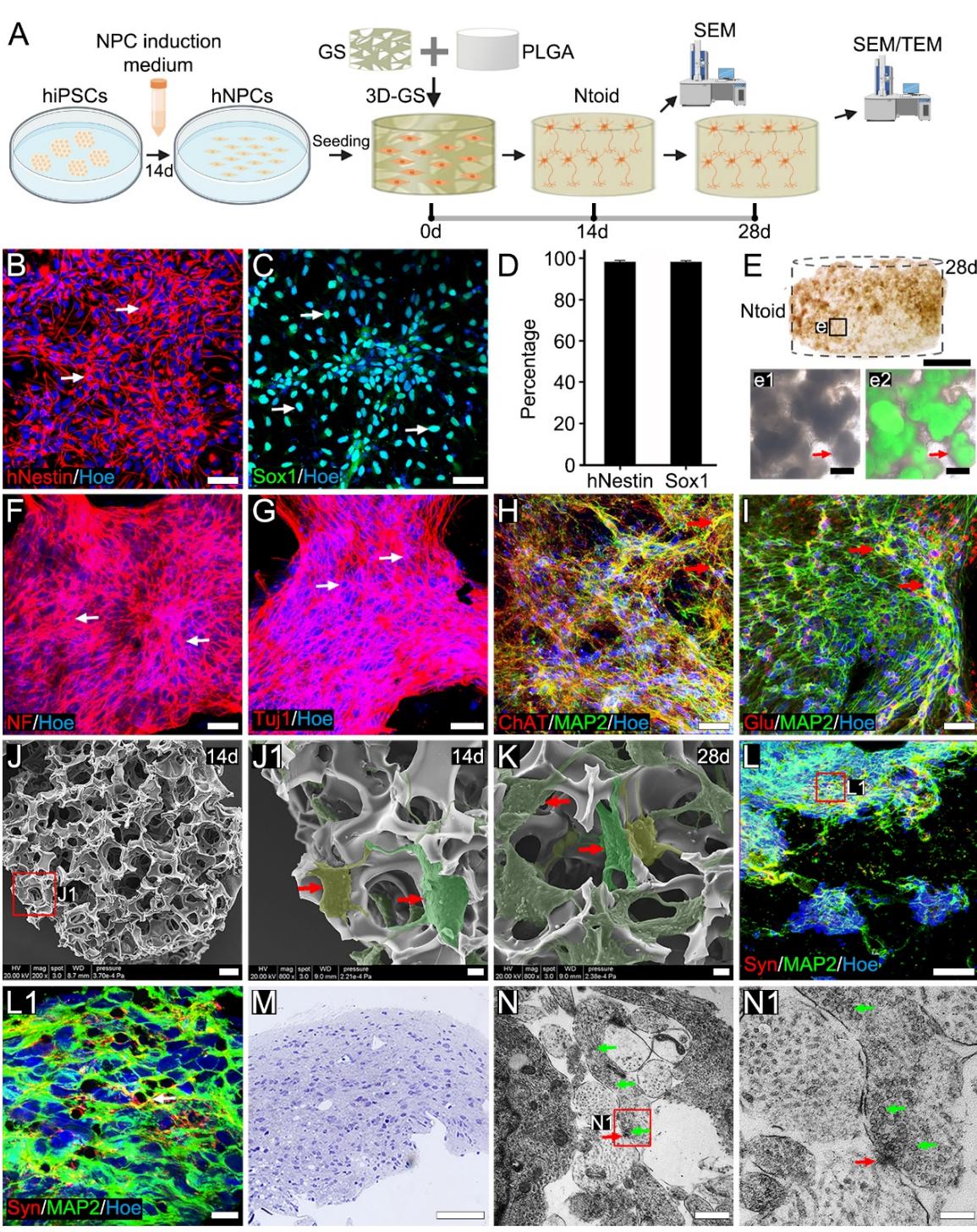
图 1. 神经元类组织的逐步构建。(A):神经元类组织(Ntoids)的逐步构建过程。(B-C):免疫荧光染色显示人神经祖细胞(hNPCs)中hNestin(箭头指示,B)和Sox1(箭头指示,C)的高表达。(D):柱状图显示Hoe+细胞中hNestin+和Sox1+细胞的比例。(E-e2):倒置相差显微镜下hiPSC来源细胞在Ntoid中的分布情况。(F-G):免疫荧光染色显示Ntoid中NF(箭头指示,F)和Tuj1(箭头指示,G)的高表达。(H-I):免疫荧光染色显示Ntoid中的ChAT+/MAP2+(箭头,H)和 (神经元(箭头,I)。(J-K):扫描电镜显示hiPSC来源细胞在Ntoid中接种14天(J-J1)或28天(K)后的形态;框选区域(J)展示了更高放大倍数的图像(J1),显示细胞簇通过神经突束相互连接(箭头,J1)。(L-L1):免疫荧光染色显示Ntoid中的Syn+突触前末梢与MAP2+神经元(L);框选区域(L)展示了更高放大倍数的图像(L1),显示Syn+突触前末梢与MAP2+神经元形成接触(箭头)。(M):光镜显示Ntoid的半薄切片。(N):透射电镜显示神经突与囊泡接触点处的类突触结构(红色箭头)和囊泡(绿色箭头)。(N1):框选区域(N)的更高倍数图像显示连接位点(红色箭头)具有电子致密的细胞膜(类似于突触前膜与突触后膜),以及细胞连接处胞质一侧的若干突触囊泡(绿色箭头)。比例尺: 微米(B-C、F-I、L和M)、 微米(E)、 微米(J与e1-e2)、 微米(J1-K)、 微米(L1)、 微米(N)和200纳米(N1)。
¶ 3.2. Ntoids的功能成熟与神经网络形成
采用全细胞膜片钳技术检测Ntoid中每个选定细胞的成熟神经元功能(图2A)。在培养时间延长至28天的Ntoid样本中,约有 的细胞记录到诱发动作电位——这是成熟神经元电生理功能性的指标(图2B-B1)。除抑制性突触后电流(IPSCs)外,还记录到兴奋性突触后电流(EPSCs,图2C-C1),提示Ntoid内形成了兴奋性神经元群体。采用高密度微电极阵列评估Ntoid中神经元群体的电活动及其相关性(图2A)。电极信号图显示Ntoid覆盖区域的电极记录到丰富的电活动(图2D、E),反映了Ntoid内活跃的神经元群体活动。观察到大量尖峰信号和典型尖峰波形(图2F、G),最大尖峰幅值达 。尖峰幅值分布表明幅值水平在 区间达到峰值(图2H)。光栅图显示Ntoid中存在簇状爆发放电(图2I)。基于电极间互相关分析构建的神经网络连接图谱,显示了信号发送神经元、信号接收神经元在Ntoid内分布着神经元和信号中转神经元,形成互连的神经网络(图2J)。对12条神经信号链路的分析显示,链路的平均路径长度为 毫米(图2K)。通过不同电极信号间的互相关图来表征神经网络活动强度,获得 $0 . 0 6 \pm 0 . 0 1 $ 8的相关性值(图2L),表明跨电极神经信号具有同步性。综上结果表明,Ntoid中已建立起成熟神经网络的各项功能。

图2. 功能Nto的成熟与神经网络形成标识。(A)示意图显示了一个培养28天的Ntoid,用于膜片钳和微电极阵列分析。细胞全膜片钳记录显示了接种28天后神经元的诱发动作电位(B-B1)和微型兴奋性突触后电流(EPSCs,C-C1)。(D) 安装在高密度微电极阵列上的Ntoid。(E) 热图实时显示其上的电活动芯片。(F)所有具有尖峰信号的电极汇总。每个小窗口代表在此期间记录的尖峰信号。(G)典型尖峰波形图显示最大尖峰幅度达到 。(H)尖峰幅度分布表明幅度峰值集中在 范围内。(I)栅状图揭示Ntoid内簇状爆发放电。(J)神经网络连接图与Ntoid的叠加展示。红点表示信号发送神经元,蓝点为信号接收神经元,灰点为信号中转神经元。线条代表神经元间的连接。(K)连接的平均路径长度( 毫米)。(L)互相关图显示神经网络活动的相关性数值( )。
¶ 3.3. TK-GCV系统有效消除了增殖细胞,同时未影响神经组织样结构的形成。
为消除增殖细胞,通过慢病毒基因(GFP-TK-杀稻瘟菌素)转染构建了携带胸苷激酶基因的iPSC(hiPSCs-GFP-TK)(图3A)。经过1-2轮杀稻瘟菌素筛选后,纯化的hiPSCs-GFP-TK表现出绿色荧光(图3B)。通过在hiPSCs-TK-GFP或hiPSCs-TK-GFP衍生的神经祖细胞(hNPCs-GFP)培养基中添加无毒底物GCV,通过剂量反应分析验证了TK的药理学功效(图3B-I)。分析显示 GCV可有效清除大部分hiPSCs-GFP-TK(存活率 ;图3c2,E)或hNPCs-GFP-TK(存活率 ;图 );而 GCV能进一步降低hiPSCs-GFP-TK(存活率 ;图3c3,E)或hNPCs-GFP-TK的存活率( ;图 )。值得注意的是, GCV对野生型hiPSC或hNPC被认为是安全的,因为这两类细胞在药物暴露后群体数量变化可忽略不计(存活率分别为 和 ;图3d3,E,h3,I)。TK基因的导入未影响hNPCs-TK-GFP的表型特征或神经分化能力,其神经玫瑰花结/球体形成及干细胞/祖细胞标志物表达(如Sox1( ,图3J,M)、Pax6( $9 8 . 8 3 { \pm } 0 . 3 $ ,图3K,M)和hNestin( ,图3L,M))与野生型hNPCs表现相似(图3M)。类似地,TK并未影响其神经元分化能力hNPCs-TK-GFP,作为成熟的神经元标志物,如NeuN( ,图3N、Q)、MAP2( ,图3O、Q)或NF200( ,图3P、Q)的表达比例,在 神经元与TK-神经元间比较时结果相似(图3Q)。值得注意的是,尽管逐步Ntoid构建方案产生了极低残留的iPSCs群体( ,补充图3R),但给予GCV处理清除了近半数残留的 多能性细胞(图3R),而对终末分化神经元的存活率未产生明显影响(补充图2S)。
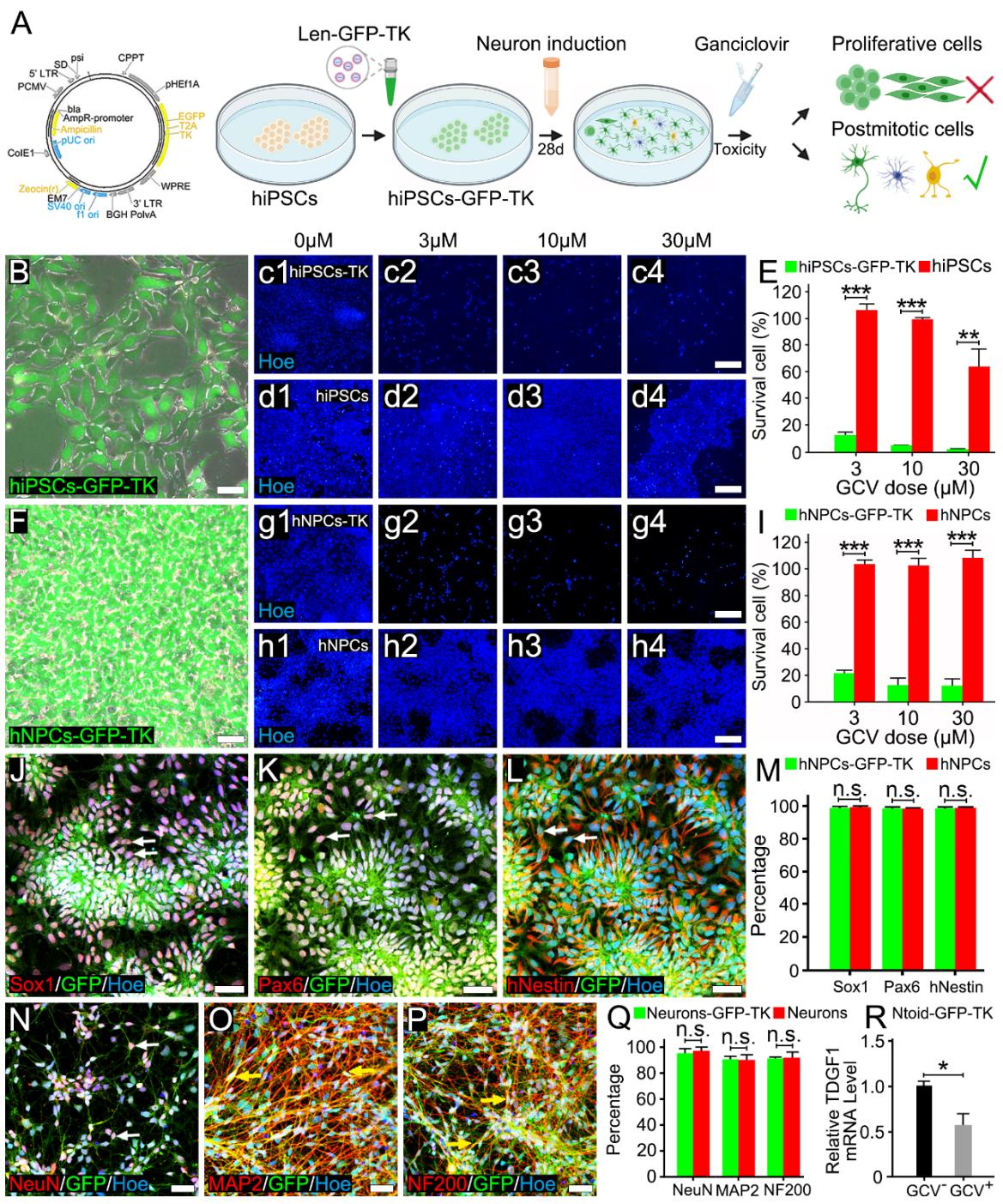
图3. TK-GCV系统在不影响hiPSC衍生神经元形成的情况下消除了增殖细胞。(A):示意图显示hiPSCs-GFP-TK的构建及增殖细胞的消除过程。(B):倒置相差显微镜下培养的hiPSCs-GFP-TK克隆形态。(c1-d4):免疫荧光染色显示,与hiPSCs相比,添加底物GCV后TK-GCV系统有效消除了hiPSCs-GFP-TK。(E):柱状图显示各组存活率的统计学显著差异 。每次实验重复三次,每次重复包含五个生物学重复; 组 , 组 , 组 。(F):倒置相差显微镜下培养的hNPCs-GFP-TK形态。(g1-h4):免疫荧光染色显示,与hNPCs相比,添加底物GCV后TK-GCV系统有效消除了hNPCs-GFP-TK。(I):柱状图显示各组存活率的统计学显著差异 。每次实验重复三次,每次重复包含五个生物学重复; 组 , 组 , 组 。(J-L):免疫荧光染色显示hNPCs-GFP-TK中Sox1(箭头,J)、Pax6(箭头,K)和hNestin(箭头,L)的高表达。(M):柱状图显示hNPCs-GFP-TK与hNPCs的Hoe+ 细胞中 、Pax6+和hNestin+细胞比例无显著差异。每次实验重复三次,每次重复包含五个生物学重复;Sox1组 0.081,pax6组 ,hNestin组 。(N-P):免疫荧光染色显示neurons-GFP-TK中NeuN(箭头,N)、MAP2(箭头,O)和NF200(箭头,P)的高表达。(Q):柱状图显示neurons-GFP-TK与neurons的 细胞中NeuN +、MAP2+和 细胞比例无显著差异。每次实验重复三次,每次重复包含五个生物学重复;NeuN组 ,MAP2组 ,NF200组 。®:柱状图显示GCV使残留相对 水平降低一半。每次实验重复三次; 。比例尺: (B、F、J-L和N-P), (c1-d4和g1-h4)。
¶ 3.4. 人诱导多能干细胞衍生的类神经组织移植改善了后肢运动功能
在进行 Ntoid 移植(Ntoid 组)、人神经前体细胞(hNPC)接种的 3D 凝胶支架(3D-GS)移植(hNPCs 组)或无细胞接种的 3D 凝胶支架移植(GS 组)后,采用旷场实验、斜网格运动实验及电生理学检测对大鼠的运动功能进行评估。大鼠于T10节段接受横断性脊髓损伤,导致BBB评分为0,表明后肢运动功能完全丧失。所有大鼠均观察到后肢运动功能逐渐恢复。值得注意的是,NToid组大鼠在脊髓损伤后八周表现出显著运动功能恢复,BBB评分达 (图4B1-B3、H),表明其后肢可实现涉及两个关节的大范围运动恢复。相比之下,hNPCs组运动功能恢复较弱(BBB评分: ,图4D1-D3、H);GS组在脊髓损伤八周后BBB评分为 (图4F1-F3、H),提示基于凝胶支架递送的hNPCs移植相较于GS组未能为运动功能恢复提供额外获益。倾斜网格测试进一步验证了非反射性自主运动的恢复:脊髓损伤八周后,NToid组可观察到频繁的足底着地伴随间歇性后肢协调运动(图4C1-C3),而hNPCs组(图4E1-E3)和GS组(图4G1-G3)仅见后肢被动运动且无足底着地。通过经颅电生理记录检测皮层运动诱发电位(CMEPs)评估神经连接恢复情况,分析显示NToid组CMEPs潜伏期( )较hNPCs组( .13ms)和GS组( )显著缩短(图4I、J),表明电信号在脊髓损伤/移植物部位的传导速度更快。此外,NToid组CMEPs振幅( )与面积( V)较hNPCs组( , )和GS组( , )显著增大(图4I、K-L),提示运动神经通路中有更多神经元被电激活。虽然基于凝胶支架递送的hNPCs移植在运动功能恢复方面未显示优于GS组的额外效益(图4H),但hNPCs组CMEPs振幅与面积较GS组显著增大(图4K-L),表明其运动神经通路中更多神经元被电激活。综上,在八周内,Ntoids在恢复后肢运动功能方面的治疗效果优于移植的人脐带间充质干细胞(hNPCs)或GS支架。
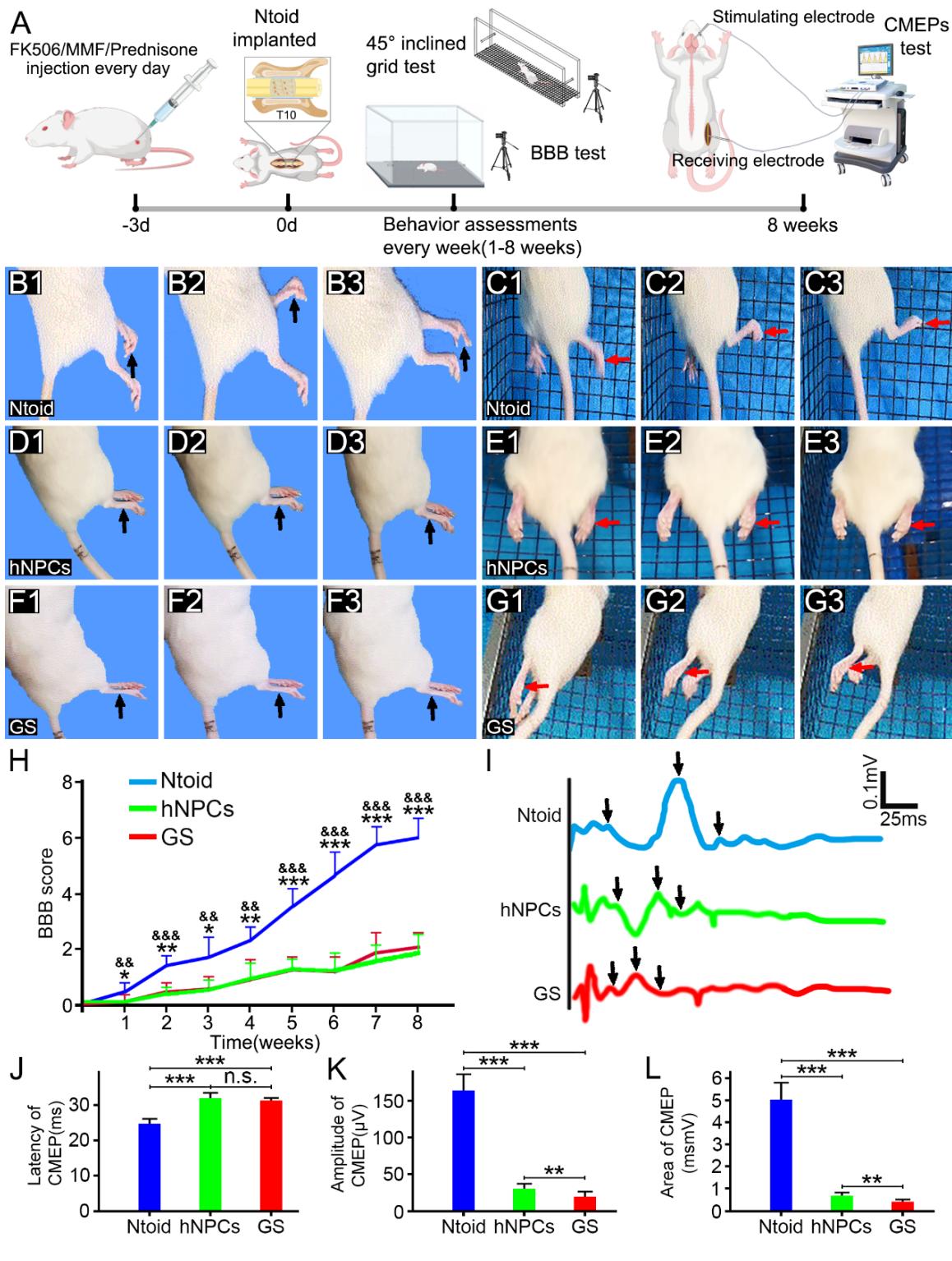
图4. 行为与电生理结果分析。(A): 示意图三组大鼠的手术与移植过程、BBB评分测试、 倾斜网格测试及电生理记录。(B1-B3、D1-D3和F1-F3):分别为Ntoid组(B1-B3)、hNPCs组(D1-D3)和GS组(F1-F3)大鼠的旷场实验观察结果。(H):Ntoid组 大鼠后肢运动功能的BBB评分显著提升移植( 和 表示与hNPCs组相比具有统计学显著性( ,第1、2、3、4、5、6、7、8周时分别为 、0.000193、0.005、0.001、 、 、 .0001、 );而 、 和 表示与GS组相比具有统计学显著性( ,第1、2、3、4、5、6、7、8周时分别为 、0.003、0.01、0.004、0.000202、 、 、 ))。(C1-C3、E1-E3和G1-G3):Ntoid组(C1-C3)、hNPCs组(E1-E3)和GS组(G1-G3)大鼠在 倾斜网格上攀爬时后肢(箭头标示)的代表性图像。(I):各组后肢电生理评估电位示意图。(J-L):柱状图显示平均潜伏期(Ntoid组对比hNPCs组和GS组为 ,hNPCs组对比GS组为 )、振幅(Ntoid组对比hNPCs组和GS组为 ,hNPCs组对比GS组为 )及CMEPs面积(Ntoid组对比hNPCs组和GS组为 ,hNPCs组对比GS组为 )的比较。Ntoid组( )结果与hNPCs组( )或GS组( )之间存在显著差异( 及 )。
¶ 3.5. Ntoid组中供体存活率高
移植后八周,在脊髓损伤/移植部位观察到大量带有绿色荧光的细胞,表明携带TK-GFP的供体细胞存活显著。实际上,GFP+细胞弥漫于整个损伤/移植区域,未出现向损伤/移植部位头尾侧区域的明显长距离细胞迁移(图5A)。人类细胞核( )免疫染色进一步证实这些细胞来源于人类(图5D)。与GFP+细胞的分布情况一致, 免疫阳性细胞同样定位于损伤/移植部位(图5D,E-F)。体视学分析显示损伤/移植区域内 的细胞为hN 阳性细胞,这表明存活供体细胞构成了该区域细胞群的主要部分(图6J)。另一方面,hNPCs组中的供体细胞在损伤/移植部位呈分散分布并形成局灶性簇集(图5B-b)。Ntoid组损伤/移植区域内GFP+细胞密度显著高于hNPCs组( vs ,图5C),表明Ntoid移植相较于hNPCs移植产生了更多的供体细胞存活。值得注意的是,虽然接种于GS支架的hNPCs移植在一例中形成了畸胎瘤hNPCs组大鼠中(1/10),而Ntoid组中未出现致畸性肿瘤形成。(补充图 3)。

图5. 移植的hiPSC来源细胞在损伤/移植部位的存活情况。(A-B):免疫荧光染色显示Ntoid组(A)和hNPCs组(B)损伤/移植部位GFP+细胞的存活情况。(b): 高倍镜图像显示hNPCs组损伤/移植部位的GFP+细胞(箭头标示)。©: 柱状图展示Ntoid组与hNPCs组损伤/移植部位的 面积( ,每组5只动物,每只动物取3-5个切片平均值; $p { < } 0 . 0 0 0 1 $ )。(D): 免疫荧光染色显示Ntoid组损伤/移植部位 细胞的存活情况。(E-F):代表性图像显示Ntoid组损伤/移植部位共表达hNu与GFP的细胞(E-F);(E)图中框选区域的高倍放大图像(E1)。比例尺 微米(A、B、D图), 微米(b、E图), 微米(E1、F图)。
¶ 3.6. 神经元类器官赋予的损伤/移植物部位密集神经支配
神经元组织体移植八周后,脊髓损伤/移植部位出现显著的神经再支配现象,这通过神经纤维常用标记物Tuj1与神经丝蛋白(NF)的强烈免疫信号得以证实。Ntoid组损伤/移植部位的NF荧光强度为 (图6A-A1、G),显著高于hNPCs组( ,图6B-B1、G)或GS组( ,图6C-C1、G)。同样,Ntoid组损伤/移植部位的Tuj1荧光强度( ,图6D-D1、H)也高于hNPCs组( ,图6E-E1、H)和GS组( ,图6F-F1、H)。此外,成熟神经元标志物NeuN的免疫染色显示,Ntoid组损伤/移植部位有大量hiPSCs来源的神经元存活(图6I-I1)。该部位 的细胞为NeuN+阳性。分析表明所有 细胞中 表达NeuN(图6J),提示大多数供体细胞保持着与移植前相似的神经元群体特征。同时,损伤/移植区域NeuN+与hNu-双阳性细胞群稀少,说明该区域主导神经元为供体来源。对这些神经元的表型分析显示,大多数G 标记的供体细胞呈ChAT+阳性(图6K-k1),而Glu+阳性细胞(补充图4A-a2)或GAD67+阳性细胞(补充图4B-b2)极少见。这可能意味着供体细胞在损伤/移植部位倾向于维持胆碱能分化特性,而非谷氨酸能或GABA能分化方向。
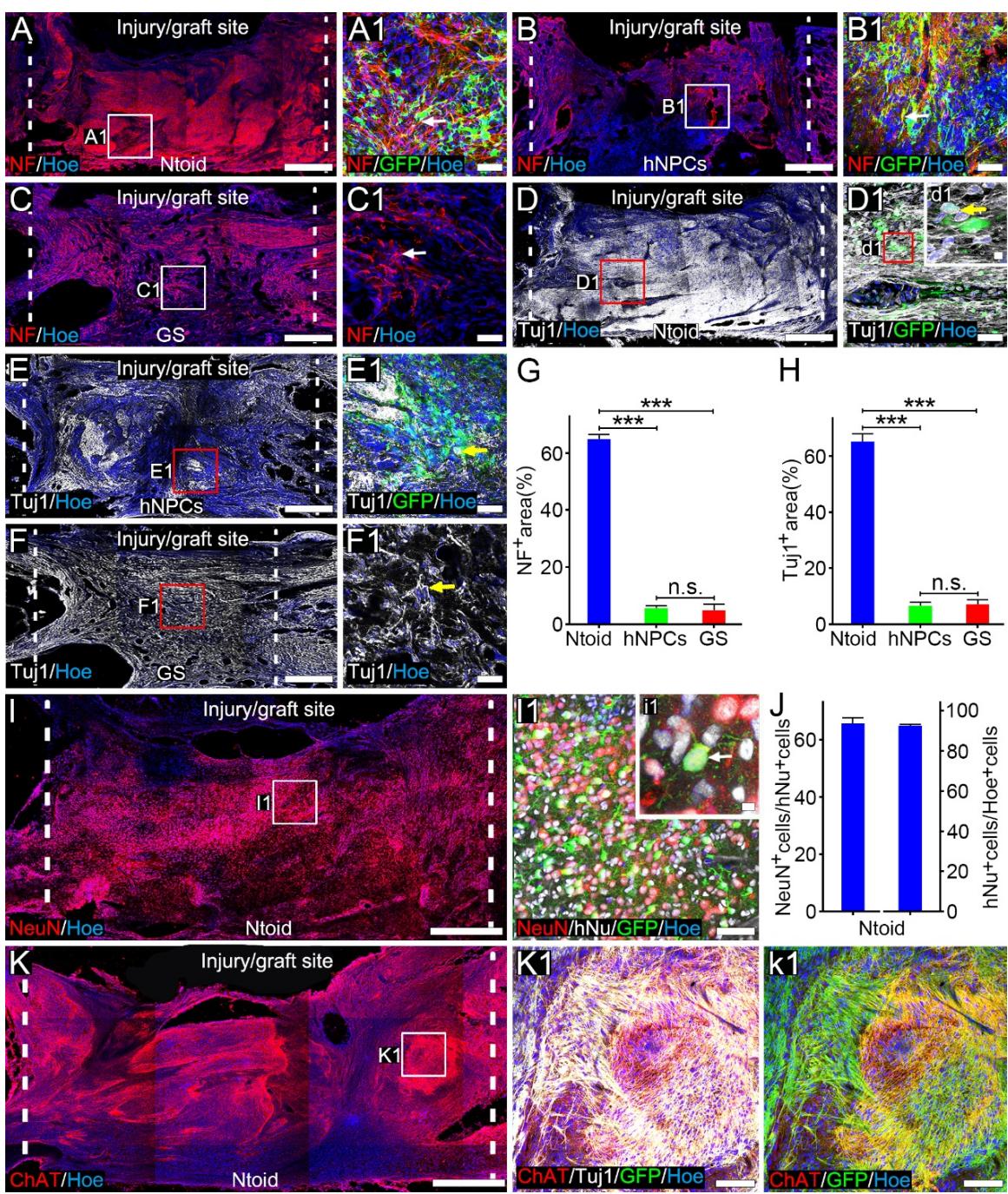
图6. 在损伤/移植部位hiPSC来源的神经元的表型特征分析。(A-C):免疫荧光染色显示 Ntoid(A)、hNPCs(B)和 GS(C)组大鼠损伤/移植部位的 NF 阳性细胞。(A1-C1):展示 Ntoid(A1)、hNPCs(B1)和 GS(C1)组损伤/移植部位 细胞(箭头)的代表性图像。(D-F):免疫荧光染色显示 Ntoid(D)、hNPCs(E)和 GS(F)组损伤/移植部位的 细胞。(D1-F1):展示 Ntoid(D1)、hNPCs(E1)和 GS(F1)组损伤/移植部位 Tuj1+ 细胞(箭头)的代表性图像。插图(d1):框选区域的高倍放大图像,显示一个 双标细胞(箭头)。(G):柱状图显示三组损伤/移植部位的 面积( ,每组五只动物,平均每只动物取3-5个切片;Ntoid组与 组比较 ,hNPCs组与GS组比较 )。 :柱状图显示三组损伤/移植部位的Tuj1+面积( ,每组五只动物,平均每只动物取3-5个切片;Ntoid组与 组比较 ,hNPCs组与GS组比较 )。(I):免疫荧光染色显示Ntoid组损伤/移植部位的NeuN阳性细胞。(I1):代表性图像显示损伤/移植部位共表达NeuN与hNu或GFP的细胞。插图(i1):(I)图中框选区域的高倍放大图,展示NeuN+/GFP+双阳性神经元(箭头所指)。(J):柱状图显示Ntoid组损伤/移植部位中hNu+细胞占Hoechst+细胞的比例,以及NeuN+细胞占 细胞的比例。(K):免疫荧光染色显示Ntoid组损伤/移植部位的ChAT+阳性细胞。(K1-k1):代表性图像显示Ntoid组损伤/移植部位共表达ChAT、Tuj1与GFP的细胞(箭头所指)。比例尺: (A-F、I、K), (A1-F1、I1),1 (K1、k1)及 (d1、i1)。
¶ 3.7. 移植Ntoids中的星形胶质细胞分化
考虑到SCI后持续的胶质增生,我们进行了胶质纤维酸性蛋白(GFAP)免疫荧光染色以评估SCI后星形胶质细胞的分布。反应性星形胶质细胞在损伤/移植物部位与残留脊髓组织交界处的分布被认为参与了慢性SCI过程中胶质瘢痕的形成,正如我们在GS组中所观察到的。在损伤/移植物部位观察到极少GFAP+星形胶质细胞(补充图5)。相比之下,Ntoid组在损伤/移植物部位观察到大量GFAP阳性星形胶质细胞(图7A)。在损伤/移植物部位观察到 细胞(图7B),这表明部分存活的供体细胞分化为星形胶质细胞。此外,许多 神经元分布于GFAP+区域(图7C);同时, 神经纤维长入并穿透GFAP+ 区域(图7D-D1),这表明损伤/移植物部位的星形胶质细胞可能作为再生轴突的“桥梁”而非“屏障”。此外,我们观察到损伤/移植物部位hiPSCs来源的星形胶质细胞上存在足状结构;这些结构与 血管内皮细胞紧密接触(图7E-e2)。这表明供体来源的星形胶质细胞可能参与血脊髓屏障的形成。另一方面,供体细胞的星形胶质分化在人神经祖细胞组中也被检测到细胞,并且hNPCs倾向于更多地分化为星形胶质细胞而非神经元(图7F-H)。
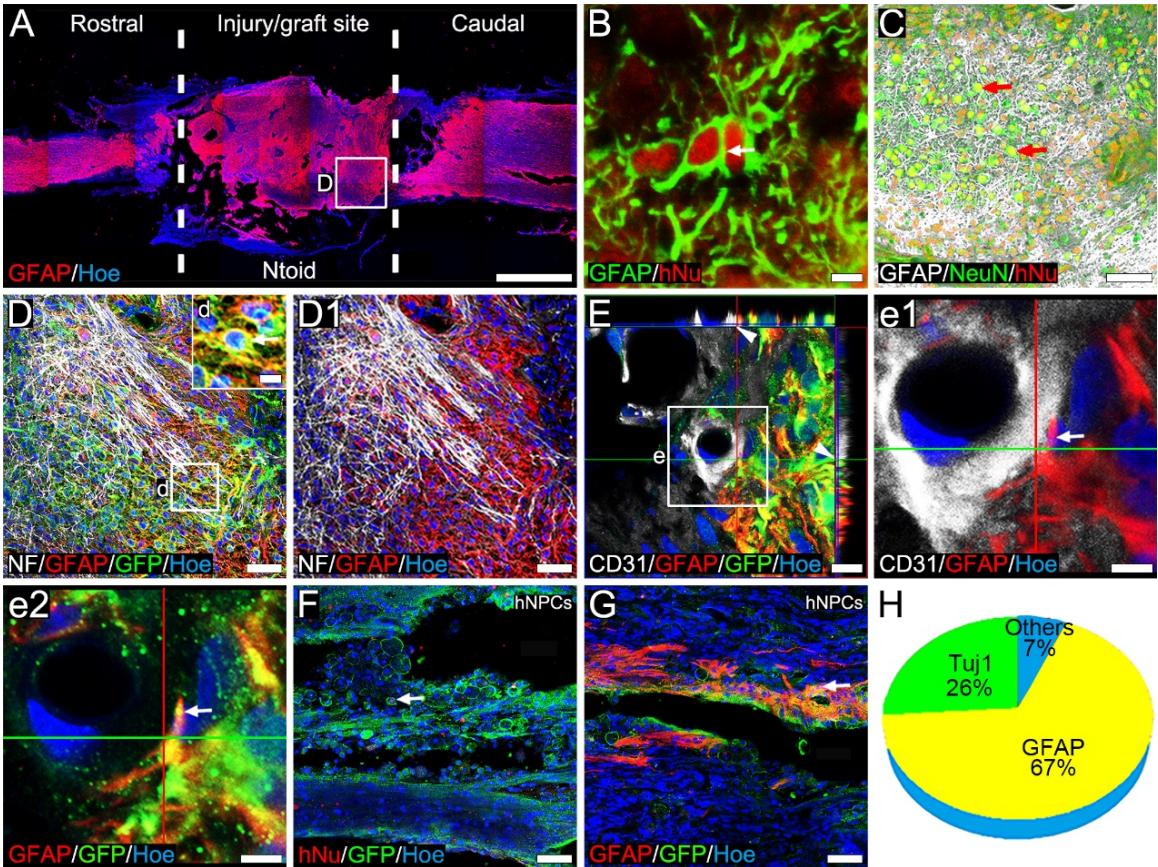
图7. Ntoids的移植调节了损伤/移植部位星形胶质细胞的功能。(A):免疫荧光染色显示Ntoid组脊髓损伤/移植部位星形胶质细胞的分布。(B):高倍放大图像显示损伤/移植部位hNu与GFAP的共表达情况。©:免疫荧光染色显示Ntoid组损伤/移植部位 星形胶质细胞与 神经元的形态及分布。(D-D1):免疫荧光染色显示再生的 神经纤维分布于损伤/移植部位的GFAP+区域。(E-e2):免疫荧光染色显示hiPSCs来源的星形胶质细胞在损伤/移植部位形成足样结构,与 血管内皮细胞接触。(E-G):图像显示hNPCs组损伤/移植部位共表达GFP与hNu(E)或GFAP(F)的细胞。(H):饼图显示hNPCs组损伤/移植部位GFP+细胞中Tuj1+或GFAP+细胞的比例。比例尺: ; (B、d及e1-e2); (C、D-D1、F、G); 。
¶ 3.8. 供体神经元与宿主神经通路的整合
通过检测供体神经元与再生长入移植物的宿主下行/上行神经纤维之间,以及供体神经元神经纤维/树突与宿主残留神经元之间的连接情况,评估供体神经元与宿主神经通路的整合(图8A)。Ntoids中的移植神经元向脊髓损伤/移植区域尾侧延伸出长长的GFP+突起;尾侧突起数量多于头侧纤维。大多数GFP+突起与NF GAP43标记物的共标提示这些是来自供体神经元的长神经纤维(图8B),具有持续显著生长和延长的能力(图8E)。GFP标记的供体神经纤维密度随距离增加而递减。在损伤/移植区域尾侧 处有 根供体神经纤维;该数量高于 处( )或 处( )的纤维数量(图8B-D)。少量供体神经纤维投射至L1-L2腰段脊髓,与背角神经元形成紧密接触(补充图6)。进一步观察发现,GFP+供体神经纤维末梢表达Syn,在腰髓ChAT+神经元胞体表面形成纽扣样结构(图8F-f2),提示突触形成的可能性。 脊髓上神经纤维再生及与移植神经元的突触整合对于修复中断的脑-脊髓连接至关重要。研究使用 神经纤维作为脑源性下行神经纤维的代表,探究其与Ntoids中供体神经元的连接性。尽管数量有限,5-HT+神经纤维仍能再生至损伤/移植区域并与GFP+移植细胞建立连接。该类纽扣样结构表达Syn,表明 神经纤维可能与移植神经元形成突触连接(图8G-g2)。此外,部分CGRP+神经纤维与位于损伤/移植区域中心的GFP+供体细胞发生接触(图8H-H1)。CGRP+神经纤维与表达Syn的GFP+供体细胞间的紧密接触可能提示突触形成(图8H1)。一些延伸至损伤/移植区域尾侧的供体神经纤维与CGRP+神经纤维形成紧密接触(图8I-I1)。综上所述,这些结果表明存活的供体神经元能够整合入宿主神经通路,以修复脊髓损伤后中断的神经通路。
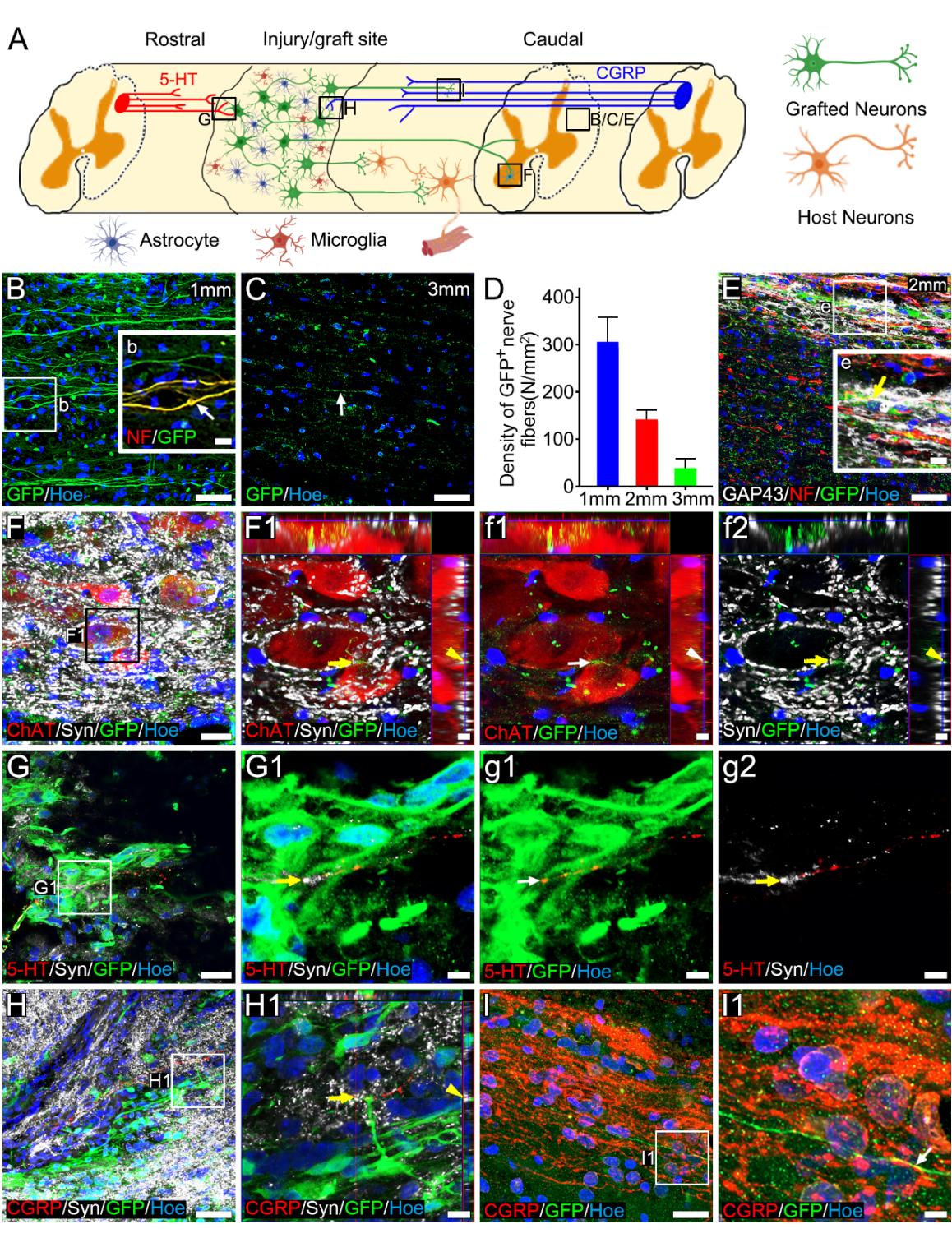
图 8.移植的Ntoid在损伤脊髓中整合到宿主神经通路中。 供体神经元与宿主神经通路整合的示意图。 免疫荧光染色显示,从供体神经元发出的长GFP+突起(箭头)在损伤/移植部位尾侧区域被观察到。插图(b):为(B)图中方框区域的高倍放大图像,显示了距损伤/移植部位1毫米(B)和3毫米©处的N 或GFP+神经纤维(箭头)。 显示损伤/移植部位尾侧区域GFP+神经纤维密度的条形图。 免疫荧光染色显示长GFP+神经纤维与GAP43+生长锥在损伤/移植部位尾侧区域的共定位。(F):显示损伤/移植部位尾侧区域宿主ChAT+神经元、 突触前末梢及供体GFP+神经纤维的代表性图像。(F1-f2):(F)中方框区域的高倍放大图像,显示大量Syn+突触前末梢(箭头)及少量G 神经纤维末梢(箭头)分布于ChAT+神经元胞体表面并与之建立接触。(G):免疫荧光染色显示损伤/移植部位再生的 神经纤维、Syn+突触前末梢及GFP+神经元。(G1-g2):(G)中方框区域的高倍放大图像,展示与GFP+神经纤维(箭头)接触的5-HT+神经纤维及Syn+突触前末梢。(H):免疫荧光染色显示损伤/移植部位再生的CGRP+神经纤维、S 突触前末梢及GFP+神经元与其神经纤维。(H1):(H)中方框区域的高倍放大图像,展示与GFP+树突/神经纤维(箭头)接触的CGRP+神经纤维及Syn+突触前末梢。(I):免疫荧光染色显示延伸至损伤/移植部位尾侧区域的GFP+神经纤维。(I1):(H)中方框区域的高倍放大图像,展示与CGRP+神经纤维(箭头)建立接触的GFP+神经纤维。比例尺 = 50 (B、C、E、H、I), (G), (b和F), (F1-f2、G1-g2、H1、I1)。
¶ 4. 讨论
受到人类iPSC衍生神经元组织oids成功构建的鼓舞invitro,我们在大鼠完全性脊髓损伤模型中研究了移植Ntoids对脊髓损伤修复的功效。首先,我们在Ntoids中验证了功能性突触连接、高神经元分化率以及极低残留多能细胞群的存在in vitro。这种分步式组织oids构建过程,结合基于TK-GCV自杀基因的安全细胞系统,消除了人类诱导多能干细胞分化的不确定性,并提高了其移植安全性。其次,通过包含BBB评分和皮层运动诱发电位的多模态评估组合,我们发现移植Ntoids后大鼠瘫痪后肢的运动功能持续改善。第三,组织学分析显示,人类iPSC衍生神经元存活长达八周,并通过长神经纤维/树突与宿主神经元形成突触连接。宿主再生神经纤维延伸至损伤/移植物部位并与移植神经元形成突触,从而表明存活的hiPSC衍生神经元能够整合到宿主神经通路中。因此,Ntoids中的供体神经元充当了"神经元中继站"以重建神经通路[34],进而促进完全性脊髓损伤大鼠瘫痪后肢运动功能的恢复。
基于iPSC的细胞治疗后患者安全是治疗的关键优先事项。化学重编程技术的最新进展[35]有效解决了与iPSCs相关的多项安全问题,包括重编程因子导致的致瘤性[36,37]或基因突变[38,39],从而推动了iPSC衍生治疗细胞的成功临床应用[40]。然而,多能性本质所导致的不确定性移植后分化,仍是基于iPSC的特定组织修复面临的关键障碍。其中畸胎瘤形成被视为最不理想的供体细胞命运,且无法仅通过多能性阶段的质量控制来解决。通过HSV-TK系统[41]或高纯度iPSC衍生神经祖细胞( )[42]选择性清除未分化细胞的方法,已被证实能有效提升iPSCs移植安全性。因此,本研究开发了分步构建神经类组织的组合方案以获得终末分化群体,并设计了TK-GCV系统纯化有丝分裂后群体。分析显示超过 的hiPSCs被诱导为hNPCs in vitro。这些细胞在3D GS支架中持续成熟,14至28天内实现高达90 的神经元终末分化,形成极低的多能性群体( )。应用 GCV可额外有效清除类组织中神经元间的增殖细胞,且不影响神经元活性。由此我们成功建立了双重保障机制,确保iPSC衍生治疗细胞用于脊髓损伤修复的安全性,该机制也可能为其他基于iPSC的应用提供有效策略。
我们的研究为成熟人类神经元移植修复受损神经器官提供了新方法。事实上,将神经前体细胞接种于三维生物相容性支架中进行神经成熟与组织构建,最终可获得可植入的神经类器官,用于修复神经组织缺损。值得注意的是,与载体生物支架中接种细胞的递送方式相比,组织类器官移植可能提供一种新型细胞治疗方案。实际上,这种神经元类器官培养过程遵循“四维(4D)生物学”原则[43],即在执行特定功能的三维培养过程中引入时间维度,从而促进培养环境下细胞与细胞外基质(ECM)之间的动态相互作用,最终形成具有特定修复功能的稳态类组织实体。本研究结果表明,与基于3D-GS的神经前体细胞移植相比,Ntoids移植能显著提高供体存活率、促进神经元分化,且未出现畸胎瘤形成。这些优越疗效背后的机制主要体现在四个方面:首先,人神经前体细胞在三维支架中持续成熟,实现显著的神经元终末分化,从而确保了hiPSC用于神经修复的理想命运定向;其次,可在移植前诱导特定神经元表型[44,45],为脊髓损伤的“精准治疗”提供可能——本研究采用兴奋性神经元修复脊髓损伤后中断的神经通路,因为脊髓内兴奋性输入对运动功能至关重要[46],未来应移植功能相关的神经元亚型[47,48]并探究其促进功能恢复的能力;第三,细胞与ECM随时间形成的动态相互作用构建出稳态微环境,为细胞行为重塑提供时空线索[49],这可能有助于供体细胞在严苛的脊髓损伤后环境中存活并与宿主神经通路整合;第四,Ntoids构建所需的2-4周 in vitro时间为实时监测批次质量提供窗口期,这为质量控制和现成细胞生产提供了有效途径[50]。这些发现共同表明,Ntoids构建可能是移植人类成熟神经元的有效方法。通过充分利用组织形态发生的时间窗口,结合多样化发育诱导策略可构建功能特化的治疗性细胞亚群,同时实施随机细胞质量抽样方案。
自主运动功能的恢复是脊髓损伤治疗的基本目标之一。在本研究中,多关节(包括髋、膝、踝关节)自主运动功能的恢复在NToid移植后仅四周即首次出现,并持续增强直至研究结束。相比之下,接受NPC移植的大鼠则未表现出有意义的运动功能恢复。这种显著变化的原因可能在于Ntoid移植物中移植细胞的大量存活,而NPC移植则导致移植群体更大程度的损失,这一点通过GFP报告基因追踪供体细胞数量得以证实。作为修复功能的执行者,存活移植细胞的数量可能与神经功能恢复程度相关[51]。因此可以明确得出结论:Ntoid递送系统有效保护了细胞在损伤部位恶劣微环境中的移植存活。此外,神经干细胞或神经祖细胞移植后更倾向于分化为星形胶质细胞而非神经元[52],因此该方案通常采用多种神经营养因子组合来促进供体细胞存活和神经元分化。但值得注意的是,NPC/NSC来源的供体细胞以平均每月2-3毫米的速度向邻近组织迁移,并伴随细胞分裂[53],这可能导致异位神经发生干扰局部神经回路的风险。相比之下,神经元移植仅出现在损伤/移植物部位,排除了异位迁移的可能性。需要说明的是,目前已开发出通过过表达免疫调节转基因实现移植免疫逃逸的免疫调节性iPSC源性神经元移植方案[54]。本研究采用与临床器官移植一致的术后免疫抑制方案,这对异种神经元移植至关重要。免疫抑制剂的使用进一步印证了Ntoid促进移植细胞存活的假设——因为NPC移植后的细胞损失可能并非源于过度免疫排斥,而是供体细胞缺乏类组织微环境支持。当然,该结论仍需更多证据支持。移植后四周即可观测到的运动功能改善,进一步凸显了移植神经元相较于NPC的治疗优势。既往研究表明NPC移植后的功能恢复存在显著延迟(最长可达18周)[26],有时甚至需要超过一年才能显现运动功能改善[27]。研究推断表型和功能成熟的供体神经元是运动功能恢复的关键。综上所述,我们的数据表明:与NPC移植相比,Ntoid移植能使供体神经元获得更高存活率和更佳运动功能改善,这提示其具有更优越的临床应用前景这种疗法前景。
要使供体神经元整合入宿主神经组织,这对修复脊髓损伤后受损的神经通路至关重要。此过程需要宿主与供体神经元之间形成突触连接。因此,供体细胞神经纤维/树突的延伸是与宿主神经元发生突触生成的重要解剖学基础。损伤后的微环境通常被认为会抑制神经纤维再生。然而,近期研究表明,传统上被认为与髓鞘相关的抑制神经纤维生长的分子,如Nogo[55]、髓鞘相关糖蛋白(MAG)[56]和少突胶质细胞髓鞘糖蛋白(OMgp)[57],实际上通过与细胞黏附分子神经生长调节因子1(Negr1)[58]相互作用,促进了从移植的人诱导多能干细胞来源的神经祖细胞中生长出的神经纤维延伸。类似地,本研究也观察到供体的长神经纤维向脊髓损伤/移植部位尾侧区域延伸。这些长神经纤维与宿主神经元或神经纤维形成突触接触,促进了神经通路和环路的重建。另一方面,皮质脊髓束中运动神经元的再生转录组会回归到胚胎转录生长状态[59],从而使成年哺乳动物脊髓损伤后皮质脊髓神经纤维能够强劲再生[5]。通过移植胚胎脊髓来源的神经祖细胞可以维持这种胚胎转录生长状态,促使皮质脊髓神经纤维强劲再生并长入移植物[60]。本研究中,宿主的上行脊髓神经纤维再生并长入移植物,与供体神经元形成突触连接,这提示iPSC来源的神经类组织可能有助于在脊髓损伤后维持大脑中的胚胎转录生长状态,其作用方式类似于胚胎脊髓来源的神经祖细胞。事实上,移植的神经类组织内形成的友好类胚胎发生微环境,允许宿主神经纤维再生并长入脊髓的损伤/移植部位。然而,其中涉及的具体机制仍有待进一步研究。
¶ 5. 结论
基于人诱导多能干细胞(hiPSCs)的功能性神经元类器官在三维培养体系中成功构建。这些神经元类器官作为“神经中继”,有效重建神经回路,促进脊髓损伤大鼠后肢瘫痪的运动功能恢复。移植后未观察到肿瘤形成、异种移植引发的过度免疫反应、异位迁移或痛觉过敏等不良反应。这些发现证实了具有安全调控机制的成熟神经组织移植治疗脊髓损伤的安全性和有效性,为未来采用组织工程化神经组织片进行临床应用奠定了基础。
¶ 作者贡献声明
曾祥、曾元山、魏清帅和马元欢构思了项目设计。魏清帅和曾祥进行了细胞培养、动物实验、显微形态学分析、统计分析并绘制了图表。马元欢、张克军、史慧娟、彭立志和王军华协助了动物实验中的手术和行为评估。马文涛、胡启新、李厚格和刘颖进行了分子生物学实验。丁颖、李戈和赖碧琴进行了形式分析。魏清帅在曾祥和曾元山的协助下撰写了手稿。曾祥监督了研究的各个方面。
¶ 利益冲突声明
作者声明,对于本文所报道的研究工作,不存在任何已知的可能产生影响的经济利益冲突或个人关系。
¶ 致谢
本研究由以下资助支持:曾祥获得国家自然科学基金(82371395和81891000)、广东省自然科学基金(2024A1515010814)、广州市基础与应用基础研究基金(2023A03J0626)、医院干细胞试剂与类器官平台建设经费(GXB202401)及广东省中医医院启动经费(2022KT1032)资助;丁颖获得国家自然科学基金(82374579)和广东省自然科学基金(2023A1515012211)资助;曾元山获得国家自然科学基金(81891003)资助;魏庆帅获得河南省自然科学基金(252300421617)资助。感谢中山大学蒋彬教授在膜片钳记录技术上的支持,以及中山大学向鹏教授为本研究提供的人诱导多能干细胞。
¶ 参考文献
[1] T.M. O’Shea, J.E. Burda, M.V. Sofroniew, 脊髓损伤与修复的细胞生物学, 临床研究杂志 27 (2017) 3259–3270. https://doi.org/10.1172/JCI90608.
[2] R. Ae, T. Dk, H. I, Y. D, Z. X, A. Je, A. Z, K. Sw, W. H, S. Rl, Z. Rd, T. Yd, 通过合成基质辅助人骨髓间充质干细胞植入界定损伤脊髓的恢复神经生物学, 《美国国家科学院院刊》114 (2017). https://doi.org/10.1073/pnas.1616340114.
[3] L. X, Z. Y, C. S, H. S, S. M, C. B, C. X, T. F, W. N, T. Y, W. B, X. Z, Z. S, D. J, 西妥昔单抗修饰胶原支架引导损伤激活内源性神经干细胞神经发生以促进急性脊髓损伤修复, 《生物材料》137卷 (2017年). https://doi.org/10.1016/j.biomaterials.2017.05.027.
[4] 范斌、魏徵、姚旭、史国华、程翔、周晓、周昊、宁冠宇、孔祥熙、冯硕, 《脊髓损伤的微环境失衡》, 细胞移植 27 (2018) 853–866. https://doi.org/10.1177/0963689718755778.
[5] K. Kadoya, P. Lu, K. Nguyen, C. Lee-Kubli, H. Kumamaru, L. Yao, J. Knackert, G. Poplawski, J.N. Dulin, H. Strobl, Y. Takashima, J. Biane, J. Conner, S.-C. Zhang, M.H. Tuszynski, 同源神经移植物重建脊髓可实现强大的皮质脊髓再生, 《自然·医学》22 (2016) 479–487. https://doi.org/10.1038/nm.4066.
[6] P. Assinck, G.J. Duncan, B.J. Hilton, J.R. Plemel, W. Tetzlaff, 脊髓损伤的细胞移植治疗, 《自然-神经科学》第20卷 (2017年) 第637–647页. https://doi.org/10.1038/nn.4541.
[7] J.N. Dulin, A.F. Adler, H. Kumamaru, G.H.D. Poplawski, C. Lee-Kubli, H. Strobl, D. Gibbs, K. Kadoya, J.W. Fawcett, P. Lu, M.H. Tuszynski, 受损的成年运动与感觉轴突再生到神经祖细胞的适当器官型区域移植体, 《自然通讯》9 (2018) 84. https://doi.org/10.1038/s41467-017-02613-x.
[8] M.M.A. 阿尔梅达, K. 古德基, A. 沃罗诺娃, 小胶质细胞功能的调控机制与神经干细胞, Front Cell Neurosci 17 (2023) 1130205. https://doi.org/10.3389/fncel.2023.1130205.
[9] S.M. Hosseini, A. Alizadeh, N. Shahsavani, J. Chopek, J.-E. Ahlfors, S. Karimi-Abdolrezaee, 抑制CSPG/LAR/PTPσ轴有助于神经元人类神经前体移植物的替换与突触发生并改善脊髓损伤后的恢复, 《神经科学杂志》42卷 (2022年) 3096–3121页. https://doi.org/10.1523/JNEUROSCI.2177-21.2022.
[10] R.A. 弗里克, M.K. 卡彭特, C. 温克勒, C. 格雷科, M.A. 盖茨, A. 比约克隆德, 人神经祖细胞的位点特异性迁移和神经元分化在成年大鼠脑内移植后, 《神经科学杂志》19卷 (1999年) 5990–6005页. https://doi.org/10.1523/JNEUROSCI.19-14-05990.1999.
[11] A.C. Lepore, I. Fischer, 谱系限制性神经前体细胞能够存活、迁移,并在移植至受损成人脊髓后的分化, Exp Neurol 194 (2005) 230–242. https://doi.org/10.1016/j.expneurol.2005.02.020.
[12] 曹庆来、R.M. Howard、J.B. Dennison、S.R. Whittemore, 移植神经元限制性前体细胞在创伤性损伤的脊髓中受到抑制, 实验神经学 177 (2002) 349–359. https://doi.org/10.1006/exnr.2002.7981.
[13] 王磊、甘金潞、徐志浩、黄涛、周迎春、姜晓兵、赵鸿阳、雷德强, 层粘连蛋白修饰的多孔GelMA微球维持脊髓损伤中促神经源性微环境用于神经干细胞移植, 《先进功能材料》(2025年). https://doi.org/10.1002/adfm.202510129.
[14] G. Li, B. Zhang, J.-H. Sun, L.-Y. Shi, M.-Y. Huang, L.-J. Huang, Z.-J. Lin, Q.-Y. Lin, 赖碧琴, 马玉华, 江波, 丁颖, 张海波, 李明星, 朱平, 王永强, 徐曾, Y.-S. 曾, 一种释放NT-3的生物支架支持TrkC修饰的神经干细胞衍生的神经网络组织,具有修复脊髓损伤功效, 生物活性材料 6 (2021) 3766–3781. https://doi.org/10.1016/j.bioactmat.2021.03.036.
[15] 赖碧琴、冯波、车梅婷、王利军、蔡帅、黄梦怡、顾海英、姜波、凌恩安、李明、曾晓、曾益新, 脊髓样组织的模块化组装实现横断脊髓的定向组织修复, 《先进科学》(Weinh) 5期 (2018年) 1800261. https://doi.org/10.1002/advs.201800261.
[16] 曾晓、邱秀春、马永辉、段建军、陈宇飞、顾海燕、王建明、凌恩安、吴J.-L.、吴W.、曾Y.-S., 供体间充质干细胞来源的类神经元细胞植入大鼠脊髓横断后的宿主神经网络整合, 生物材料 53 (2015) 184–201. https://doi.org/10.1016/j.biomaterials.2015.02.073.
[17] 赖炳权、王继明、段建军、陈玉芳、顾海燕、凌恩安、吴金良、杨世曾, 大鼠脊髓横断损伤后NSC衍生的神经网络与宿主神经网络的整合研究, 《生物材料》第34卷 (2013年) 第2888–2901页.
[18] 吴国华、石海杰、车梦婷、黄梦瑶、魏庆顺、冯博、马宇航、王利君、姜波、韩王-Q.、凌恩安、曾益新, 犬只完全性脊髓损伤植入MSC来源的神经网络组织后肢体运动功能恢复, 《生物材料》第181卷 (2018年) 第15–34页. https://doi.org/10.1016/j.biomaterials.2018.07.010.
[19] 赖邦启、车明珠、冯波、白一然、李刚、马玉华、王丽君、黄明宇、王永强、姜波、丁艳、曾霞、曾永胜, 组织工程化神经网络移植物在完全横断犬脊髓中传递兴奋性信号的研究, 《先进科学》(Weinh) 6 (2019) 1901240. https://doi.org/10.1002/advs.201901240.
[20] J. Yu, M.A. Vodyanik, K. Smuga-Otto, J. Antosiewicz-Bourget, J.L. Frane, S. Tian, J. Nie, G.A. Jones, R. Ruiz, R. Stewart, I.I. Slukvin, J.A. Thomson, 诱导多能干细胞系来源于人体细胞, 《科学》318 (2007) 1917–1920. https://doi.org/10.1126/science.1151526.
[21] 高桥和孝、田边和彦、大贯真、成田光、市坂毅、友田幸司、S. 山中伸弥, 通过从成人成纤维细胞中诱导多能干细胞的确定因子, 《细胞》第131卷 (2007年) 第861–872页. https://doi.org/10.1016/j.cell.2007.11.019.
[22] 高桥和利、山中伸弥, 通过特定因子诱导胚胎和成人成纤维细胞培养获得小鼠诱导多能干细胞, 《细胞》126卷 (2006年) 663–676. https://doi.org/10.1016/j.cell.2006.07.024.
[23] 小林康浩、冈田泰之、板仓弦、岩井宏昌、西村翔、安田昭夫、则晋吾、引島孝、小野見可奈子、藤吉生、辻雄一郎、外山滋、山中まや、中村雅也、H. 冈野, 预先评估的安全人类iPSC来源的神经干细胞可促进脊髓损伤后普通狨猴的功能恢复且无致瘤性, PLoS One 7 (2012) e52787. https://doi.org/10.1371/journal.pone.0052787.
[24] O. T, N. N, K. J, T. O, S. M, S. S, K. Y, M. M, N. M, O. H, γ-分泌酶抑制剂治疗促进人iPSC衍生细胞移植用于慢性脊髓损伤的功能恢复, 《干细胞报告》11卷 (2018年). https://doi.org/10.1016/j.stemcr.2018.10.022.
[25] P. Lu, G. Woodruff, Y. Wang, L. Graham, M. Hunter, D. Wu, E. Burley, R. Ahmed, G. Poplawski, J. Brock, L.S.B. Goldstein, M.H. Tuszynski, 脊髓损伤后源于人类诱导性多能干细胞的长距离轴突生长, 《神经元》第83卷 (2014年) 789–796. https://doi.org/10.1016/j.neuron.2014.07.014.
[26] S. 田代、S. 西村、H. 岩井、K. 菅井、L. 张、M. 篠崎、A. 岩波、Y. 富山、M. 刘、H. 冈野、M. 中村, 干细胞/祖细胞移植联合跑台训练对小鼠慢性脊髓损伤的神经功能恢复, 《科学报告》6卷 (2016年) 30898. https://doi.org/10.1038/srep30898.
[27] P. Lu, S. Ceto, Y. Wang, L. Graham, D. Wu, H. Kumamaru, E. Staufenberg, M.H. Tuszynski, 延长人类神经干细胞成熟期有助于啮齿动物中枢神经系统损伤后的功能恢复, 《临床研究杂志》127卷 (2017年) 第3287–3299页. https://doi.org/10.1172/JCI92955.
[28] 柯强、李雷、蔡波、刘畅、杨阳、高阳、黄伟、袁雪、王涛、张强、A.L. Harris, L. Tao, A.P. Xiang, 缝隙连接蛋白43参与人源诱导多能干细胞生成, 《人类分子遗传学》22卷 (2013年) 第2221–2233页. https://doi.org/10.1093/hmg/ddt074.
[29] 康思、陈曦、宫莎、于鹏、Yau S.、苏喆、周凌、余静、潘纲、石璐, iPSC衍生神经元神经分化模型的特征分析——从形态学、生理学和全基因组表达模式来看, Sci Rep 7 (2017) 12233. https://doi.org/10.1038/s41598-017-12452-x.
[30] A.S. 阿尔秋霍夫、E.B. 达希尼马耶夫、N.V. 梅谢里亚科娃、A.A. 阿希赫米纳、E.A. 沃罗特利亚克、A.V. 瓦西里耶夫, 采用高灵敏度微滴数字PCR技术检测异质细胞混合物中少量iPSCs的研究, 《分子生物学报告》46 (2019) 第6675–6683页. https://doi.org/10.1007/s11033-019-05100-2.
[31] X. Zeng, Y. Zeng, Y. Ma, L. Lu, B. Du, W. Zhang, Y. Li, W.Y. Chan, 骨髓间充质干细胞在三维明胶海绵支架中减轻炎症、促进血管生成并减少实验性脊髓损伤的空洞形成, 《细胞移植》20卷 (2011年) 1881–1899页. https://doi.org/10.3727/096368911X566181.
[32] D.M. Basso, M.S. Beattie, J.C. Bresnahan, 一套敏感可靠的大鼠旷场实验运动功能评分量表, 《神经创伤杂志》12卷 (1995年) 第1–21页. https://doi.org/10.1089/neu.1995.12.1.
[33] A. Ramón-Cueto, M.I. Cordero, F.F. Santos-Benito, J. Avila, 包鞘胶质细胞的功能性恢复, Neuron 25 (2000) 425–435. https://doi.org/10.1016/s0896-6273(00)80905-8.
[34] 赖邦琦、曾旭、韩文韬、车明涛、丁玥、李刚、曾园山, 干细胞来源的神经元中继策略与功能性电刺激用于治疗脊髓损伤, 生物材料 279 (2021) 121211. https://doi.org/10.1016/j.biomaterials.2021.121211.
[35] J. Wang, S. Sun, H. Deng, 用于细胞命运调控的化学重编程:方法、应用与展望, 《细胞·干细胞》30卷 (2023年) 第1130–1147页. https://doi.org/10.1016/j.stem.2023.08.001.
[36] K. Okita, T. Ichisaka, S. Yamanaka, 可进入种系的诱导多能干细胞生成, 《自然》448 (2007) 313–317. https://doi.org/10.1038/nature05934.
[37] K. 冲田、M. 中川、H. 玄宗、T. 一坂、S. 山中,生成小鼠无病毒载体的诱导多能干细胞,《科学》322(2008)949–953 页。https://doi.org/10.1126/science.1164270。
[38] 国际干细胞倡议组织、K. 安普斯、P.W. 安德鲁斯、G. 安尼凡蒂斯、L. 阿姆斯特朗、S. Avery, H. Baharvand, J. Baker, D. Baker, M.B. Munoz, S. Beil, N. Benvenisty, D.本-约瑟夫、J.-C. 比安库蒂、A. 博斯曼、R.M. 布雷纳、D. 布里森、G. 凯桑德、M.V.卡马拉萨,J. 陈,E. 奇奥,Y.M. 崔,A.B.H. 邱,D. 科林斯,A. 科尔曼,J.M.克鲁克、G.Q. 戴利、A. 多尔顿、P.A. 德索萨、C. 丹宁、J. 唐尼、P. 德沃夏克、K.D.蒙哥马利、A. 费基、A. 福特、V. 福克斯、A.M. 弗拉加、T. 弗鲁姆金、L. 葛、P.J. 戈克哈、Golan-Lev, H·古拉比, M·格罗普, G·吕, A·汉普尔, K·哈龙, L·希利, W·赫拉斯, F·霍尔姆, O. 霍瓦塔, J. 希尔纳, M.S. 因纳姆达尔, A.K. 伊尔万托, T. 石井, M. 雅科尼, Y. 金, S.金伯、S. 基谢廖夫、B.B. 诺尔斯、O. 科珀、V. 库哈连科、A. 库利耶夫、M.A.拉加科娃、P.W. 莱尔德、M. 拉科、A.L. 拉斯莱特、N. 拉冯、D.R. 李、J.E. 李、C. 李、L.S.Lim, T.E. Ludwig, Y. Ma, E. Maltby, I. Mateizel, Y. Mayshar, M. Mileikovsky, S.L.Minger、T. Miyazaki、S.Y. Moon、H. Moore、C. Mummery、A. Nagy、N. Nakatsuji、K.纳尔瓦尼、吴世光、C·奥尔森、T·奥托科斯基、潘峰、朴一熙、S·佩尔斯、M·F·Pera, L.V. Pereira, O. Qi, G.S. Raj, B. Reubinoff, A. Robins, P. Robson, J. Rossant,G.H. 萨莱克德、T.C. 舒尔茨、K. 塞尔蒙、J. 谢赫·穆罕默德、H. 沈、E. 舍雷尔、K.西杜,S. 西瓦拉贾,H. 斯科特曼,C. 斯皮茨,G.N. 斯泰西,R. 斯特雷尔,N. 斯特雷尔琴科,H. 末森、B. 孙、R. 苏罗宁、K. 高桥、T. 图里、P. 维努、Y. 韦林斯基、D.瓦德-范·奥斯特瓦尔德、D·J·韦森伯格、Y·吴、S·山中伸弥、L·杨、Q·周,筛选不同族裔的人类胚胎干细胞鉴定出染色体20个赋予生长优势的最小扩增子,《自然生物技术》29卷(2011年)1132–1144. https://doi.org/10.1038/nbt.2051。
[39] F.J. 鲁哈尼, S. 尼克-扎伊纳尔, A. 伍斯特, Y. 李, N. 孔特, H. 小池-游佐, N. 熊坂,L. Vallier, K. Yusa, A. Bradley,人类细胞谱系的突变历史——从体细胞到诱导多能干细胞,《PLoS遗传学》第12卷(2016年),论文编号e1005932。https://doi.org/10.1371/journal.pgen.1005932
[40] 王 S., 杜 Y., 张 B., 孟 G., 刘 Z., 刘 S.Y., 梁 R., 张 Z., 蔡 X., S.吴,高 W.,庄 D.,邹 J.,黄 H.,王 M.,王 X.,王 X.,梁 T.,刘 J.·顾 N.·刘 Y.·魏 X.·丁 Y.·蒲 Y.·詹 Y.·罗 P.·孙 S.·谢 J.·杨 Y.翁、C. 周、Z. 王、S. 王、H. 邓、Z. 沈,化学移植腹直肌前鞘下诱导多能干细胞衍生的胰岛在一名1型糖尿病患者中,Cell 187 (2024) 6152-6164.e18。DOI:10.1016/j.cell.2024.09.004。
[41] K. Kojima, H. Miyoshi, N. Nagoshi, J. Kohyama, G. Itakura, S. Kawabata, M. Ozaki, T.饭田、菅井、伊藤、福泽、安武、雷诺-三原、柴田、松本、中村、冈野,致瘤细胞的选择性消融——人类诱导多能干细胞来源的神经干/祖细胞脊髓损伤的移植治疗,《干细胞转化医学》第8卷(2019年)第260–270页。https://doi.org/10.1002/sctm.18-0096。
[42] M. 万代, A. 渡边, Y. 栗本, Y. 平见, C. 森永, T. 大門, M.藤原、赤丸、酒井、柴田、寺田、野宮、谷岛、中村、H. 龟尾、S. 杉田、A. 大西、T. 伊藤、K. 藤田、S. 川又、M.J. 吴、C.筱原、K.-I. 秦、M. 泽田、M. 山本、S. 太田、Y. 小原、K. 吉田、J.桑原、Y. 北野、N. 天野、M. 梅景、F. 北冈、A. 田中、C. 冈田、N.高须,S. 小川,S. 山中,M. 高桥,自体的诱导干细胞源性视网膜细胞治疗黄斑变性,《新英格兰医学杂志》376卷(2017年)1038–1046。https://doi.org/10.1056/NEJMoa1608368。
[43] M.W. Tibbitt, K.S. Anseth, 动态微环境:第四维度,《科学·转化医学》4 (2012) 160ps24. https://doi.org/10.1126/scitranslmed.3004804.
[44] R. 横井, T. 重本黑田, N. 松田, A. 小田原, I. 铃木,对致痫性化合物的电生理反应取决于人类iPSC来源皮层神经网络中的兴奋/抑制平衡,《药理科学杂志》148卷(2022年)。
[45] M·G·博萨-莫兰, R·马丁内斯-埃尔南德斯, S·伯纳尔, K·瓦尼施, E·阿尔索-拉略, A·勒赫伦、L. 阿利亚斯、C. 丹尼斯、M. 吉拉尔、J.-K. 伊、E.F. 蒂萨诺、R.J. 亚涅斯-穆尼奥斯,衰变在iPSC衍生的运动神经元分化过程中存活与塑蛋白3水平,《科学报告》5 (2015) 11696。https://doi.org/10.1038/srep11696
[46] K·萨特昆南德拉贾、S·K·卡拉迪马斯、A·M·拉利伯特、G·蒙坦东、M·G·费林斯,颈椎兴奋性神经元在脊髓损伤后维持呼吸,《自然》562期(2018年):419–422. https://doi.org/10.1038/s41586-018-0595-z。
[47] C. Kathe, M.A. Skinnider, T.H. Hutson, N. Regazzi, M. Gautier, R. Demesmaeker, S.科米,塞托,N.D. 詹姆斯,N. 赵,L. 博德,K. 加兰,K.J.E. 马特森,A. 罗瓦尔德,K.金, R. 王, K. 米纳斯西安, J.O. 普赖尔, L. 阿斯博特, Q. 巴罗, S.P. 拉库尔, A.J.莱文、F·瓦格纳、J·布洛赫、J.W·斯奎尔、G·库尔蒂纳,瘫痪后行走的神经元恢复,《自然》杂志 2022 年 第 611 卷 第 540–547 页。https://doi.org/10.1038/s41586-022-05385-7.
[48] V.N. Jensen,E.E. Huffman,F.L. Jalufka,A.L. Pritchard,S. Baumgartner,I. Walling,H.C 吉布斯, D.A. 麦克里迪, W.J. 阿利莱因, S.A. 克龙, V2a神经元恢复膈肌功能——脊髓损伤后小鼠功能恢复的研究,《美国国家科学院院刊》121卷(2024年)e2313594121. https://doi.org/10.1073/pnas.2313594121.
[49] T.H.卡齐、M.R.布拉奇利、M.D.戴维森、F.M.亚维特、M.E.库克、K.S.安塞斯、J.A.Burdick, 《程序化水凝胶探索时空细胞生物学》,《细胞·干细胞》29 (2022) 678–691. https://doi.org/10.1016/j.stem.2022.03.013.
[50] D. Crow, 诱导多能干细胞能否实现“现成”细胞疗法?,《细胞》杂志 177 卷 (2019年) 1667–1669. https://doi.org/10.1016/j.cell.2019.05.043。
[51] K·M·皮尔蒂、G·M·富内斯、S·N·阿瓦基安、A·A·萨利比安、K·I·黄、K·卡尔塔、N·龟井、洛杉矶·弗拉纳根、E.S.·莫努基、内村·信、B.J.·卡明斯、A.J.·安德森,提升人神经干细胞移植剂量改变脊髓损伤后的少突胶质细胞和神经元分化,《干细胞报告》8卷(2017年)第1534–1548页。https://doi.org/10.1016/j.stemcr.2017.04.009。
[52] Q.L. Cao, Y.P. Zhang, R.M. Howard, W.M. Walters, P. Tsoulfas, S.R. Whittemore,多能干细胞植入正常或受损的成年大鼠脊髓后仅限于胶质细胞谱系,《实验神经学》第167卷(2001年)第48–58页。https://doi.org/10.1006/exnr.2000.7536。
[53] B. V. 连、M. H. 图申斯基、P. 陆,星形胶质细胞从人类神经干细胞移植物中迁移并在受伤的大鼠脊髓中实现功能性整合,Exp Neurol 314(2019)46–57. https://doi.org/10.1016/j.expneurol.2019.01.006.
[54] C. 帕万, K.C. 戴维森, N. 佩恩, S. 弗劳辛, C.P.J. 亨特, N. 莫里亚蒂, M.Á.贝罗卡尔·鲁维奥, Z. 埃拉希, A.T. 夸特罗基, K.D. 阿布-邦斯拉, 王L, W. 克洛, H.杨, M. Pellegrini, C.A. Wells, L.H. Thompson, A. Nagy, C.L. Parish, 一种隐匿的人类干细胞衍生的神经移植物——具备功能性整合与免疫逃逸机制在啮齿动物模型中的研究,《细胞·干细胞》第32卷(2025年)第710-726页,e8。https://doi.org/10.1016/j.stem.2025.03.008。
[55] M.S.陈,A.B.胡贝尔,M.E.范德哈尔,M.弗兰克,L.施内尔,A.A.施皮尔曼,F.Christ, M.E. Schwab,Nogo-A是一种髓鞘相关的神经突生长抑制因子(单克隆抗体IN-1的抗原),《自然》杂志第403卷(2000年)第434–439页。https://doi.org/10.1038/35000219。
[56] G·穆克吉、P·多尔蒂、F·S·沃尔什、P·R·克罗克、M·T·菲尔宾,髓鞘相关糖蛋白作为轴突再生抑制剂,《神经元》第13期(1994) 757–767。https://doi.org/10.1016/0896-6273(94)90042-6。
[57] 王国昌、V. 科普里维察、J.A. 金、R. 西瓦桑卡兰、郭岩、R.L. 内夫、何志刚,少突胶质细胞-髓鞘糖蛋白是一种抑制神经突生长的Nogo受体配体,《自然》417 (2002) 941–944. https://doi.org/10.1038/nature00867.
[58] G·H·D· 波普拉夫斯基、R· 利、M· 亨特、H· 熊丸、R· 川口、P· 吕、M·K·E·舍费尔, G. 伍德拉夫, J. 鲁宾逊, P. 卡涅特, J.N. 杜林, C.G. 杰弗里, L. 门泽尔, B.郑、G. 科波拉、M.H. 图申斯基的研究表明,成年大鼠髓鞘能增强神经干细胞的轴突生长,《科学转化医学》10 (2018) eaal2563。https://doi.org/10.1126/scitranslmed.aal2563。
[59] G·H·D·波普拉夫斯基、R·川口、E·范·尼凯克、P·陆、N·梅塔、P·卡涅特、R·李,I. D·拉加特西斯, J·M·梅维斯, B·郑, G·科波拉, M·H·图辛斯基, 受损成年神经元回归胚胎转录生长状态,《自然》581卷(2020年)77–82. https://doi.org/10.1038/s41586-020-2200-5。
[60] 李毅、X. He、R. Kawaguchi、张宇、王强、A. Monavarfeshani、Z. Yang、陈波,Z. Shi, H. Meng, S. Zhou, J. Zhu, A. Jacobi, V. Swarup, P.G. Popovich, D.H.Geschwind, Z. He, 新生小鼠中小胶质细胞介导的无瘢痕脊髓修复,《自然》587 (2020) 613–618. https://doi.org/10.1038/s41586-020-2795-6.