¶ 《科学报告》
¶ 位移视网膜神经节细胞的空间分布与功能整合
¶ 原文下载:s41598-025-91045-5_origin.pdf
萨布丽娜·杜达1, 克里斯托夫·T·布洛克1, Dipti R. Pradhan1, 优素福·阿尔赞尼亚1, Alina Klaiber1, 马丁·格雷斯纳1 和 克里斯蒂安·普勒1、2
1 德国奥尔登堡市卡尔·冯·奥西茨基大学神经科学系视觉神经科学部,邮编26111
2 德国波恩马克斯·普朗克行为神经生物学研究所计算神经行为学系(caesar)。电子邮件:christian.puller@mpinb.mpg.de
¶ 摘要
视网膜包含不同类型的神经节细胞,这些细胞在视野的每个位置与同类型细胞形成镶嵌结构。移位视网膜神经节细胞(dRGCs)的胞体位于内核层(INL),而规则排列的神经节细胞的胞体则位于神经节细胞层。哺乳动物dRGCs的一个例子是M1型内在光敏性神经节细胞(ipRGCs)。然而,关于它们与规则排列的ipRGCs之间的关系,人们知之甚少。我们通过免疫组织化学和光学显微镜鉴定出小鼠的ipRGC类型M1、M2和M4/sONɑ。对M1和sONɑ神经节细胞的免疫标记镶嵌结构进行重建后发现,dRGCs与其规则排列的神经节细胞伙伴共同覆盖视网膜。多电极阵列记录显示,移位的sONɑ神经节细胞具有常规的感受野,这些感受野与其规则排列的对应细胞的镶嵌结构相契合。神经节细胞分布分析表明,特定类型的dRGCs模式既不遵循所有神经节细胞的整体密度分布,也不遵循相应细胞类型的局部密度。神经节细胞胞体移位至内核层的情况以类型依赖的方式发生,其中dRGCs的位置使其能与规则排列的伙伴形成完整的镶嵌结构。我们的数据表明,dRGCs和规则排列的神经节细胞在其相应的神经节细胞群体中发挥着相同的功能作用。
¶ 引言
视网膜神经节细胞(RGCs)在小鼠体内由一组异质性细胞组成,包含40多种不同的细胞类型1,2。它们可根据形态、分子特征和光响应特性的巨大多样性进行区分1,2,3,4。单个RGC类型的细胞体规则排列,其树突以镶嵌方式排列,覆盖视网膜且无间隙5,6。这些镶嵌结构的区域特化存在于整个哺乳动物视网膜中,以适应不同物种的生活方式和栖息地,例如猫的中央区、兔子的视觉条纹或人类的中央凹7,8,9。这些区域的RGC密度增加,以提高特定视野区域的视敏度10,11。在小鼠中,RGCs被认为存在从中央到外周的密度梯度12。然而,最近的研究表明,某些类型的细胞(如持续性ON型α视网膜神经节细胞,即sONɑ RGC)具有独特的密度梯度,这与RGCs的整体密度分布不同11,13,14,15,16。
除了这些特化特征外,所有视网膜神经节细胞(RGC)类型的一个共同特征是它们的胞体位于神经节细胞层(GCL)。然而,这一规则存在一些尚未被充分理解的例外情况,即错位视网膜神经节细胞(dRGCs)的胞体位于内核层(INL)。一个著名的例子是,在包括人类在内的多种哺乳动物视网膜中,内在光敏视网膜神经节细胞(ipRGCs)的胞体常常出现错位,例如17–24。ipRGCs表达光色素黑视蛋白,并在成像和非成像视觉中介导不同的功能25。在小鼠视网膜中,根据形态、功能特性以及投射到不同脑区的轴突,可将六种不同类型的ipRGCs(M1-M6)区分开来18、23、26、27、28、29、30、31。研究表明,M4型ipRGC对应于小鼠视网膜中四种α型视网膜神经节细胞之一,即持续性ON型α(sONɑ)视网膜神经节细胞29、32。
尽管人们对这群异质性的内在光敏视网膜神经节细胞(ipRGCs)及其相应类型的功能作用有所了解,但对位移型内在光敏视网膜神经节细胞(displaced ipRGCs)的特性知之甚少。在小鼠中,约2%的视网膜神经节细胞(RGCs)作为位移型视网膜神经节细胞(dRGCs)位于内核层(INL)。它们在视网膜周边区域出现的频率更高12。单个位移型视网膜神经节细胞在形态上表现出很大的多样性33,但尚未针对细胞特性以及规则分布的视网膜神经节细胞对位移型视网膜神经节细胞进行全面研究。因此,它们的树突突起相对于神经节细胞层(GCL)中规则分布的视网膜神经节细胞的空间排列及其反应特性仍然未知。在研究哺乳动物视网膜中的视网膜神经节细胞镶嵌结构时,位移型视网膜神经节细胞常常被忽略,人们认为它们的错位是由于个体发育异常所致,而非代表一种独立的功能性视网膜神经节细胞类别3,34。然而,在鸟类中,位移型视网膜神经节细胞大多投射到副视系统,推测其有助于视动性眼球震颤和视网膜图像稳定35,36,37。
为了阐明哺乳动物视网膜中位移视网膜神经节细胞(dRGCs)相对于规则视网膜神经节细胞(RGCs) mosaic 结构的解剖和功能排列,我们利用了现有的针对小鼠内在光敏视网膜神经节细胞(ipRGCs)群的免疫标记物。我们分析了M1、M2型ipRGCs以及sONɑ型ipRGCs在视网膜神经节细胞层(GCL)和内核层(INL)中的空间分布和树突排列。位移视网膜神经节细胞(dRGCs)完善了树突mosaic结构,并与位置规则的伙伴细胞共同均匀覆盖视网膜,形成完整的解剖和功能mosaic结构。此外,我们发现已识别的位移视网膜神经节细胞(dRGCs)的分布既不遵循所有视网膜神经节细胞(RGCs)的整体密度分布,也不遵循神经节细胞层(GCL)中相应类型细胞的分布。而且,不同类型细胞的位移比例存在差异。我们的数据表明,细胞体的位移并非随机发生,而是具有类型依赖性。
¶ 材料与方法
¶ 动物与组织制备
所有操作均按照德国联邦政府颁布的《德国动物保护法》(Tierschutzgesetz)进行,并获得当地动物福利官员的批准,符合美国兽医协会(AVMA)的安乐死指南,且报告遵循ARRIVE指南。本研究纳入了野生型C57Bl6/J小鼠和thy1-GFP-O小鼠38,雌雄不限。它们被饲养在12:12小时的光暗循环环境中。用于细胞计数的是11-12周龄的成年C57Bl6/J小鼠。通过二氧化碳吸入法对小鼠实施安乐死,随后进行断头处理。摘除眼球后,将其置于含4%冷多聚甲醛的0.01M磷酸盐缓冲盐水(PBS,pH 7.4)中,在室温下固定15分钟。用PBS冲洗后,特别注意保持眼杯的方向,以脉络膜裂作为标志39。制作四个放射状减压切口,其中最长的一个沿鼻裂方向,接近视神经乳头。然后,在PBS中将视网膜从眼杯中分离出来。操作过程中确保完整保留视网膜,包括最外周区域(外边缘区)。之后,将视网膜置于含30%蔗糖的PBS中进行冷冻保护过夜,并在-20°C下保存直至使用。
使用5-7周龄的thy1-GFP-O小鼠进行多电极阵列(MEA)记录。将小鼠暗适应2小时后,通过颈椎脱臼处死。在室温下,于充有碳合气(95%氧气和5%二氧化碳)的Ames溶液(pH 7.4,USBiological公司)中,在红外光照下从眼球杯中分离出视网膜的背颞区。MEA记录在36.5°C的记录室中进行。
¶ 免疫组织化学
解剖后,视网膜被用作整装标本。采用间接免疫荧光法进行免疫组织化学标记。将组织安装在黑色硝酸纤维素滤膜(Millipore)上,神经节细胞层朝上,并在含有5%正常驴血清(NDS)、1%牛血清白蛋白(BSA)、1%曲拉通X-100和0.02%叠氮化钠的PBS孵育液中,于室温下预孵育2-4小时。一抗和二抗在相同的孵育液中稀释。整装标本与一抗(表1)在室温下孵育3天。二抗(Alexa 488和Alexa 568,Invitrogen,1:500;Alexa 647,Invitrogen或Jackson ImmunoResearch,1:250)在室温下孵育4小时。在漂洗前1小时,将4’,6-二脒基-2-苯基吲哚二盐酸盐(DAPI,Sigma-Aldrich,货号D9542,终浓度0.2μg/ml)加入二抗溶液中。
组织被固定在载玻片上,并使用Vectashield(Vector Laboratories公司产品)进行封片。载玻片和盖玻片之间放置了间隔物,以避免挤压组织。高分辨率图像堆栈通过共聚焦激光扫描显微镜(Leica TC SP8和Leica TCS SL)拍摄,使用40倍/1.25油浸物镜,z轴增量为0.25-0.5μm;或通过配备Apotome2和20倍/0.8空气物镜的Zeiss AxioObserver显微镜拍摄,z轴增量为0.54μm。
用RBPMS、SMI-32、钙结合蛋白或黑视蛋白标记的细胞体被手动勾勒出来,并在Fiji中测量相应区域以计算其直径。
为了计算密度恢复曲线40以及对细胞密度进行大规模量化,使用配备电动载物台和20倍/0.5空气物镜的徕卡DM6 B落射荧光显微镜对整个视网膜的图像堆栈进行平铺扫描。单个图像堆栈在显微镜软件(LAS X,徕卡)中自动拼接在一起。接下来,使用Fiji中的CellCounter插件手动标记单个细胞体的中心。
¶ 表1 一抗列表。
| Primary antibody | Host | Company | Catalogue number | Dilution |
| RBPMS | Rabbit | PhosphoSolutions | 1830-RBPMS | 1:500 |
| RBPMS | Guinea pig | PhosphoSolutions | 1832-RBPMS | 1:200 |
| SMI-32 (Neurofilament H) | Mouse | BioLegend | 801701 | 1:1000 |
| Calbindin | Rabbit | Swant | CB-38a | 1:2000 |
| Osteopontin | Goat | R&D systems | AF1433 | 1:200 |
| Melanopsin | Rabbit | ATS | AB-N38 | 1:2500 |
| Melanopsin | Rabbit | ATS | AB-N39 | 1:2500 |
| GFP | Rabbit | Invitrogen | A-6455 | 1:2000 |
¶ 视网膜整装片的重建
在Fiji和Matlab中标记了多个用于球面重建和密度计算的标志点。这些标志点包括展平视网膜的轮廓,以及该轮廓内切割和撕裂的附加标记、视盘、视网膜内部破裂区域、组织缺失区域,还有血管等显著的解剖学特征。在组织折叠或缺失的罕见情况下,对轮廓进行了估计。随后,使用R包Retistruct41将解剖后的视网膜重建为眼中视网膜形成的部分球体。完整的视网膜估计形成一个球面帽,其边缘角为110°41。利用血管分布模式评估重建质量。基于鼻侧脉络膜裂的切口对不同视网膜的方向进行对齐。图7C显示了平均鼻侧脉络膜裂切口线和平均视盘。视盘中心从帽顶腹侧偏移,角度为5.2±2.6°。根据完整小鼠眼睛的冷冻切片测量,视网膜帽(特别是神经节细胞层)的半径设定为1.5毫米。这与之前的报道一致42。我们舍弃了通过平衡四叶苜蓿形和球面帽面积估计出的半径(1.3±0.0毫米,n=10)。半径差异可能是由于在装片过程中展开视网膜时,四叶苜蓿形中心视神经头周围的组织可能受到压迫,导致展平的整装视网膜面积被低估所致。
局部细胞密度(即细胞体标志物的密度)是在球坐标系中计算的。特定位置的密度是10度半径范围内局部邻域中的标志物数量。该半径对应的弧长为261.8μm,计数盘面积为0.21 mm²。视盘等区域或染色不充分、组织受损的区域不纳入面积计算。不同视网膜的平均密度(图7)是在固定的规则网格上计算的。重建点以等距方位投影的形式可视化(图7)。
¶ 解剖学和电生理学已识别细胞的匹配
视网膜的记录方法如前所述43。简而言之,从眼睛背颞象限分离出的一小块视网膜被固定,视网膜神经节细胞(RGC)面朝下,置于高密度微电极阵列(3Brain)上。记录在离线状态下进行分析,以分离不同细胞的锋电位。使用每个电极上的阈值来检测候选锋电位事件。提取锋电位发生时该电极及邻近电极上的电压波形。如果相似锋电位波形的集群表现出不应期,则将其识别为候选神经元。通过时间互相关识别同一细胞的重复记录并将其移除。在CRT显示器上显示单色二进制空间白噪声,刷新率为120Hz,刺激像素宽度为49μm。呈现刺激像素的网格被随机移位,有效地将空间分辨率提高了一倍。使用平均强度为2.9 mW/m²的明视光水平来表征所记录细胞的反应特性。感受野通过锋电位触发平均值来近似。基于视网膜神经节细胞的时空感受野特性和锋电位自相关函数(鉴于它们形成规则的镶嵌结构),将其功能分类为不同的细胞类型。sONɑ视网膜神经节细胞根据其持续反应、大感受野以及对全视野频率和振幅调制扫描的反应模式来识别1。感受野轮廓绘制在二维高斯拟合的1个标准差等高线上。电图像计算为在细胞锋电位周围5.1毫秒时间窗口内记录的平均电压44。
MEA记录完成后,在视网膜仍固定于MEA上时进行手动平铺扫描。使用配备10倍空气物镜的Leica DMLFS落射荧光显微镜获取图像,并在Fiji中通过成对拼接插件将其拼接在一起。随后,将组织小心地固定在黑色硝酸纤维素滤膜(Millipore)上,使视网膜神经节细胞(RGC)层朝上,并按照上述方法进行免疫染色处理。如前所述,通过免疫标记和功能分析独立识别sONɑ视网膜神经节细胞的 mosaic。当视网膜仍固定在MEA上时,在落射荧光图像中使用Amira(赛默飞世尔科技)对GFP标记的sONɑ视网膜神经节细胞进行追踪,以匹配GFP标记的细胞、清晰可见的电极以及相应的电图像。通过比较所有记录细胞的细胞体和轴突位置与电图像中相应的电压偏转,实现了解剖学和电生理学数据的独特映射。
除非另有说明,所有数据均以平均值±标准差(标准偏差)表示。
¶ 结果
对小鼠视网膜进行了 melanopsin 标记,并结合其他免疫标记物,以研究规则分布的内在光敏视网膜神经节细胞(ipRGCs)和错位细胞的分布情况。如先前研究所示,melanopsin 免疫标记显示小鼠视网膜的染色模式不均匀25,45。在视网膜背侧,M1 和 M2 型 ipRGCs 的胞体和树突清晰可见,且 melanopsin 染色水平相当均匀。相比之下,视网膜腹侧的 melanopsin 染色模式均匀性较差,大多数细胞的染色通常较弱,但有标记强烈的(M1 型)细胞较为突出(图1)。因此,需要更多的标记物来可靠地识别细胞类型及其在所有视网膜区域的特定分布模式。
¶ 骨桥蛋白标记M2内在光敏视网膜神经节细胞
M1和M2型内在光敏视网膜神经节细胞(ipRGCs)的黑视蛋白免疫反应呈强阳性,但目前缺乏能明确区分这两种类型的特异性标记物。胞质蛋白骨桥蛋白46通常被用作小鼠α型视网膜神经节细胞的标记物,但有研究表明,另一种含黑视蛋白的视网膜神经节细胞也对骨桥蛋白有免疫反应2,47。因此,我们分析了骨桥蛋白与黑视蛋白以及其他细胞标记抗体的染色模式,以确定这些组合是否适用于可靠地区分目标视网膜神经节细胞类型(图2A-D,圈出部分)。我们使用SMI-3211,48和钙结合蛋白47来排除与sONɑ型视网膜神经节细胞的混淆(图2E-L,圈出部分),因为sONɑ型视网膜神经节细胞表达骨桥蛋白和低水平的黑视蛋白29,32(以及我们自己的观察结果,图2)。此外,我们还应用了RBPMS(具有多重剪接的RNA结合蛋白49)——一种通用的神经节细胞胞体免疫标记物,以进一步阐明视网膜神经节细胞胞体的一般解剖学特性。sONɑ型视网膜神经节细胞具有异常大的多边形胞体(图2F、G,胞体直径20.7±1.3μm;n=75;另见图3G)。
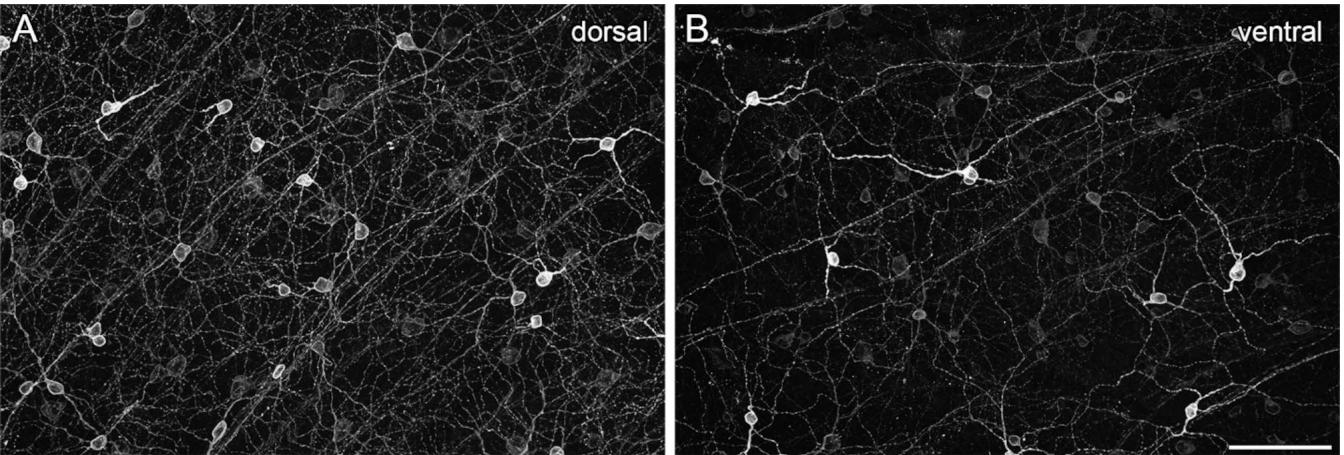
图1. 黑视蛋白在小鼠视网膜中的非均匀染色模式。使用结构照明显微镜拍摄的黑视蛋白标记的最大强度投影 epi 荧光图像分别来自同一视网膜的背侧(A)和腹侧(B)区域。比例尺:50 μm。

图2.用于ipRGC/sONɑ细胞类型分类的免疫标志物。小鼠神经节细胞层(GCL)共聚焦图像堆栈的最大强度投影,以不同组合方式对神经丝标志物SMI-32、黑视蛋白、钙结合蛋白钙调蛋白、具有多种剪接功能的RNA结合蛋白(RBPMS)和骨桥蛋白进行三重标记。(A)-(D):多个黑视蛋白阳性ipRGC的细胞体对SMI-32呈免疫阴性,但被骨桥蛋白标记(虚线圆圈)。(E)-(H):sONɑ视网膜神经节细胞(RGC)的细胞体(虚线圆圈)被SMI-32、钙调蛋白和RBPMS共同标记。(I)-(L):与(E)-(H)相同,但用骨桥蛋白替代RBPMS。比例尺:50μm。
图2)。此外,RBPMS(具有多种剪接的RNA结合蛋白49)是一种通用的神经节细胞体免疫标记物,被用于进一步阐明视网膜神经节细胞体的一般解剖学特性。sONɑ视网膜神经节细胞具有异常大的多边形细胞体(图2F、G,胞体直径20.7±1.3μm;n=75;另见图3G)。
此处呈现的标志物组合使得sONɑ视网膜神经节细胞(RGCs)的明确分类成为可能,因为后者体积非常大,SMI-32呈强阳性,而黑视蛋白仅呈弱阳性。因此,至少有一种其他类型的视网膜神经节细胞也同时对骨桥蛋白和黑视蛋白具有免疫反应性。为了识别这种类型,我们利用树突分层来对同时标记有骨桥蛋白和高水平黑视蛋白的视网膜神经节细胞进行分类。M1或M2型内在光敏视网膜神经节细胞(ipRGCs)的树突分别在内网状层(IPL)的S1或S5亚层分层50。如果黑视蛋白标记的内在光敏视网膜神经节细胞中针对骨桥蛋白的免疫反应性是一种类型特异性特征,那么这应该能通过相应细胞的独特分层模式显现出来。因此,我们分析了骨桥蛋白阳性和阴性的内在光敏视网膜神经节细胞的树突分层,这些细胞均呈强黑视蛋白阳性。这些细胞是通过免疫标记整装标本的显微镜图像堆栈手动追踪的(图3)。在本实验(图3a3)及后续实验中,细胞体位置和树突分层水平是参照DAPI染色来确定的,DAPI染色在此处作为神经节细胞层和内核层的指示剂。
骨桥蛋白阴性但黑视蛋白强阳性的细胞仅分层于内网层(IPL)的最远端部分(S1亚层,图3D)。这些细胞具有稀疏分支的树突 Arbor 和相对较小的细胞体(图3G,胞体直径12.8±1.6 μm;n=114)。我们根据染色强度、整体形态和分层水平将这些细胞鉴定为M1型内在光敏视网膜神经节细胞(ipRGCs)。相比之下,骨桥蛋白阳性、黑视蛋白强标记的内在光敏视网膜神经节细胞仅分层于内网层的最近端部分(S5亚层,图3E)。
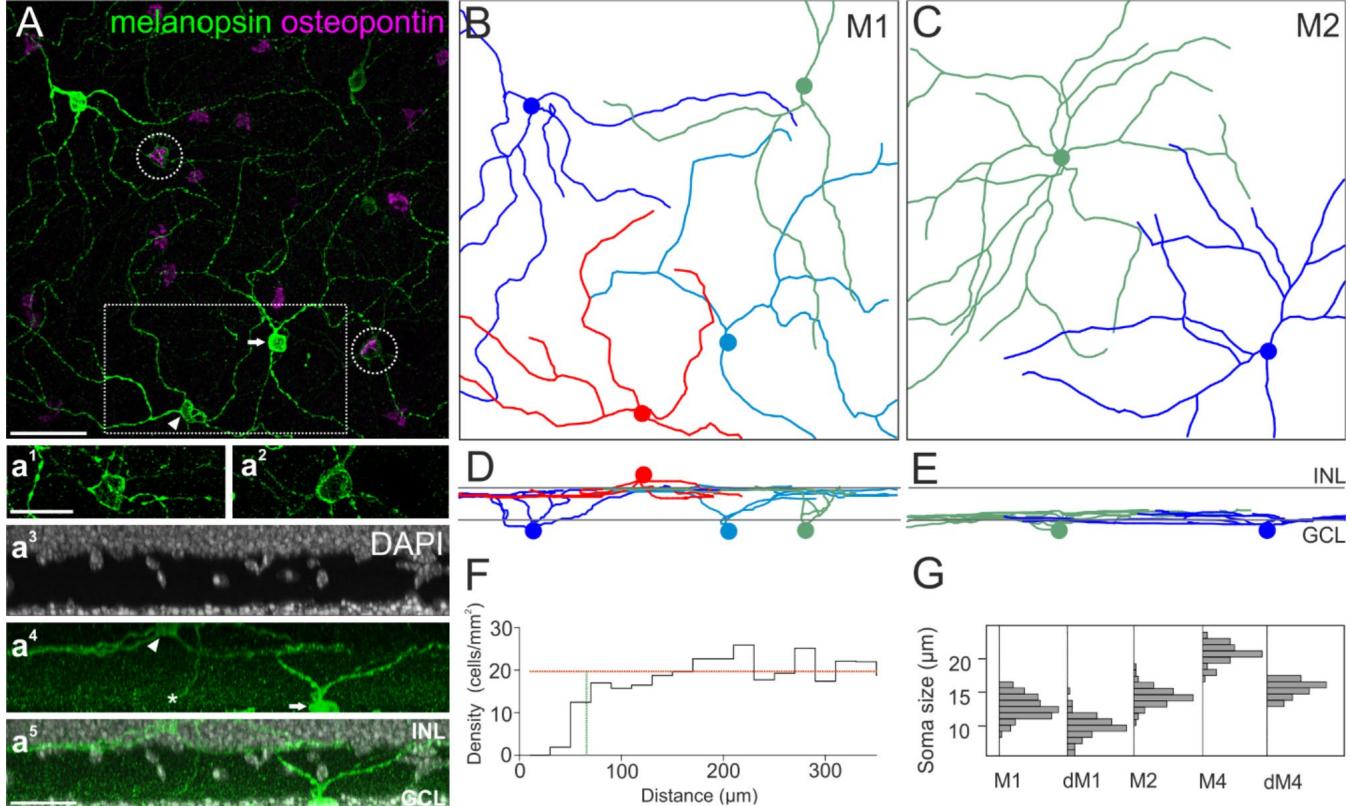
图3. 骨桥蛋白阴性(M1)和阳性(M2)内在光敏视网膜神经节细胞(ipRGCs)的平铺模式和分层水平。(A)全铺视网膜共聚焦图像堆栈的最大强度投影,标记了黑素视蛋白和骨桥蛋白。在Amira软件中,通过图像堆栈手动追踪了M1和M2型ipRGCs的树突。a1和a2显示了A中黑素视蛋白标记的细胞体的染色模式(虚线圆圈),强度有所增加。a3-a5:A中框选区域的侧视投影,包括DAPI染色,指示内核层(INL)和神经节细胞层(GCL)。箭头(A,a4)指向INL中移位的M1细胞的胞体,星号(a4)标记下行轴突。箭头(A,a4)指向胞体位于GCL中的M1细胞。(B)M1型ipRGCs的神经节细胞骨架。彩色圆盘指示细胞体的位置。(B)底部的红色骨架属于移位的神经节细胞。(C)M2型ipRGCs的神经节细胞骨架。(D)、(E)分别是(B)、(C)的垂直视图。灰色线指示通过DAPI染色确定的内网层(IPL)的内外边界。(F)在全铺视网膜中分析的M2细胞(n=281)的密度恢复曲线,显示了M2型ipRGCs之间的距离分布。有效排斥半径(绿色竖线):65.8 μm,在较大一半区间上的细胞密度平均值(橙色水平线):19.71个细胞/mm²,区间宽度20 μm。(G)ipRGC胞体直径的直方图,M1 n=114;dM1 n=81;M2 n=81;M4/sONɑ n=75;移位的M4/sONɑ n=21(所有峰值归一化为相同振幅)。比例尺:A中50 μm,适用于(A)-(E);a1和a5中25 μm。
这些细胞的胞体比M1型内在光敏视网膜神经节细胞(ipRGCs)稍大(胞体直径14.4±1.3μm;n=81)。它们具有对称的树突树,且分支点多于M1型内在光敏视网膜神经节细胞,其形态与文献中描述的M2型内在光敏视网膜神经节细胞相似。
在免疫标记的视网膜中,所有M2候选细胞的胞体位置(n=281)均经过手动标记,并计算了密度恢复曲线。结果显示,一个有效半径为65.8μm的排斥区清晰可见(图3F)。该排斥区进一步支持了这些细胞构成单一类型并平铺视网膜的观点(另见图7M-O)。
这些结果共同表明,被强黑素视蛋白标记且骨桥蛋白阳性、SMI32阴性的细胞代表M2型内在光敏视网膜神经节细胞(ipRGCs)。
¶ 常规和错位视网膜神经节细胞类型的树突平铺模式
我们分析了移位视网膜神经节细胞(RGCs)及其在神经节细胞层(GCL)中正常位置对应细胞的树突结构的空间排列,以了解它们之间相对的树突组织关系。为此,我们如附图2所示,在共聚焦图像堆栈中使用了SMI-32染色。由于SMI-32染色会标记多种不同细胞类型的突起,因此在视网膜内丛状层(IPL)中染色非常密集。因此,我们通过图像堆栈手动追踪了移位RGC类型及其相同类型正常位置邻近细胞的树突树(附图S1、附图4)。
红色的树突骨架来源于移位的sONɑ视网膜神经节细胞(图4A、B)。所有其余细胞的胞体均位于神经节细胞层。尽管SMI-32不能可靠地标记特定树突最外周的树突,但显然所有这些细胞都在视网膜内丛状层的ON层中处于相同的分层水平。此外,移位的sONɑ视网膜神经节细胞填补了其正常位置伙伴所形成的镶嵌结构中的空缺,并且它们共同均匀地覆盖了视网膜(图4C)。
为了确保这种错位细胞的树突平铺模式并非仅与sONɑ视网膜神经节细胞(RGCs)相关,我们还分析了小鼠 ventral 视网膜中,错位的M1内在光敏视网膜神经节细胞(ipRGCs)的树突在规则排列的M1 ipRGCs镶嵌结构中可能的整合情况(图5)。图5A中央的红色骨架显示了胞体位于内核层(INL)的错位M1 ipRGCs。这些细胞与胞体位于神经节细胞层的其余规则排列的同类细胞共同构成了完整的镶嵌结构。所有M1 ipRGCs均在视网膜内网状层(IPL)的远端OFF层同一水平分层(图5B)。与sONɑ RGCs的情况类似,错位的M1 ipRGCs与其同类型的规则排列细胞共同构成了完整的镶嵌结构(图5C)。
¶ 常规和错位sONɑ视网膜神经节细胞的感受野镶嵌
我们提供了解剖学证据,表明移位的视网膜神经节细胞(RGCs)与其同类型的规则排列细胞协同覆盖视网膜,形成完整的树突镶嵌体。假设移位的视网膜神经节细胞在光反应特性方面与规则细胞没有差异,那么当存在移位的神经节细胞时,这种空间模式应该会体现在功能感受野的均匀、连续镶嵌体中。
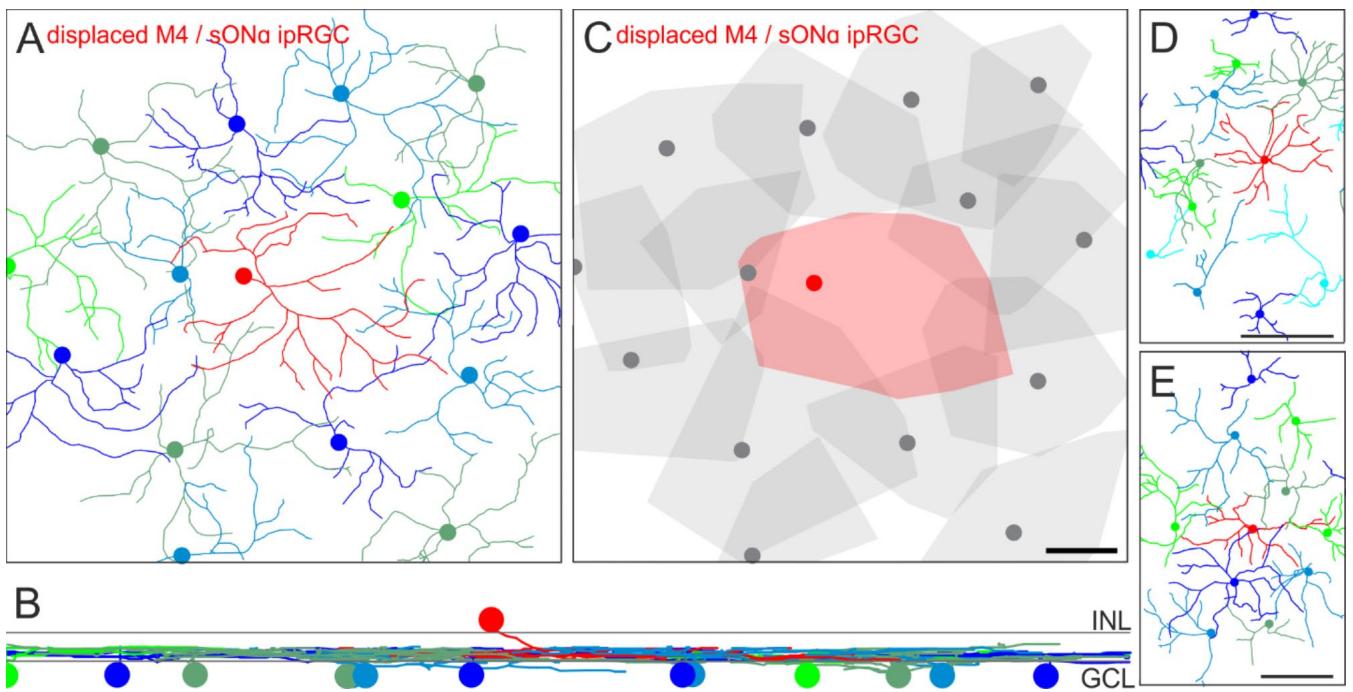
图4. M4/sONɑ视网膜神经节细胞的平铺模式和分层水平。通过标记有SMI-32和DAPI的小鼠视网膜共聚焦图像堆栈,手动追踪sONɑ视网膜神经节细胞的树突。(A)sONɑ视网膜神经节细胞骨架。彩色圆盘指示细胞体的位置。中央的红色骨架属于一个错位的sONɑ视网膜神经节细胞。(B)A中视网膜神经节细胞骨架的垂直视图。灰色线条指示由DAPI染色确定的内网状层的内边界和外边界。INL:内核层,GCL:神经节细胞层。(C)凸包包裹着如(A)中的骨架。错位的细胞以红色显示。注意,图像堆栈外围一些神经节细胞的树突树未被完全捕捉到。(C)中的比例尺:50μm,也适用于(A)。(D)、(E)作为(A)的补充示例,来自另外两只动物。比例尺500μm。
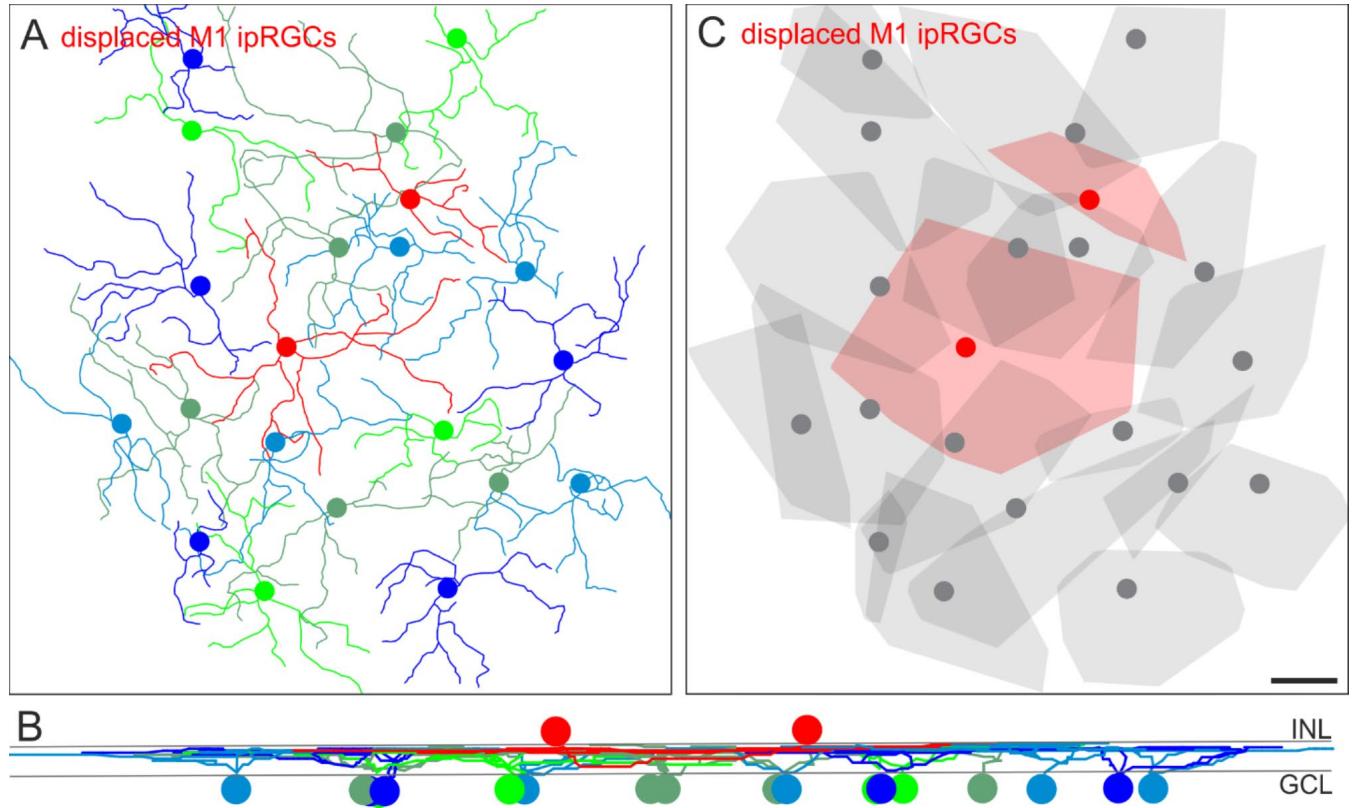
图5. M1型内在光敏视网膜神经节细胞(ipRGCs)的平铺模式和分层水平。(A)利用黑视蛋白免疫染色,在Amira软件中通过图像堆栈追踪M1型细胞的树突。图中显示了得到的M1型内在光敏视网膜神经节细胞骨架。红色骨架代表对移位M1型细胞的追踪结果。(B)(A)中神经节细胞骨架的垂直视图。INL:内核层,GCL:神经节细胞层。(C)凸包包裹着(A)中的骨架。移位细胞以红色显示。注意,图像堆栈外围部分神经节细胞的树突树未被完整捕捉。C中的比例尺:100微米,也适用于(A)。
为了验证这一假设,我们通过MEA记录GFP-O小鼠视网膜在随机噪声光刺激下的尖峰信号,来表征sONɑ视网膜神经节细胞(RGCs)的感受野组织(图6)。使用GFP-O视网膜是为了识别GFP阳性的sONɑ RGCs51。我们从背颞侧视网膜进行记录,以提高在常规RGCs中记录到移位sONɑ RGC的概率(见图7V-X)。同时记录了两个邻近的GFP阳性RGCs(图6A),根据树突形态、强烈的SMI-32标记以及细胞体分别位于神经节细胞层(GCL)和内核层(INL)的位置,随后确认它们分别是一个正常位置的sONɑ(蓝色标记)和一个移位的sONɑ RGC(红色标记)(图6A、B)。通过筛选对应区域内所有记录到的RGCs的候选电图像,将这两个经解剖学鉴定的细胞与MEA记录的功能数据集进行匹配。基于胞体位置和轴突轨迹,我们为这两个细胞都找到了匹配对(图6A)。这些细胞属于sONɑ功能镶嵌体的一部分(图6C),该镶嵌体是独立鉴定的(见材料和方法)。正常位置和移位的sONɑ RGCs在尖峰反应动力学方面表现出相似的感受野特性(图6D-F)。移位RGC的感受野半径与正常位置RGC的感受野半径没有显著差异(威尔科克森秩和检验p > 0.74)。与我们的解剖学结果一致,移位sONɑ RGC的感受野(图6C中的红色椭圆)完善了其推测为正常位置对应细胞的感受野镶嵌体(灰色椭圆)。
¶ 视网膜中视网膜神经节细胞类型的分布
在此,在除了外边缘区之外的区域,观察到的dRGCs数量比预期更多12。因此,我们通过对上述免疫标志物进行大规模分析,以特定类型的方式研究了dRGCs相对于常规RGCs在整个视网膜中的总体分布模式(表2)。
我们将这些标记组合应用于免疫标记整装标本中视网膜神经节细胞体的定位分析(图7)。通过应力释放切口使组织扁平化,得到了典型的四叶苜蓿状样本。在解剖过程中,其中一个切口恰好沿着鼻侧脉络膜裂放置,用于视网膜的定位。我们在完整的视网膜上手动计数了特定标记组合中的每个细胞体(见方法部分),它们的位置在图7中用圆点表示(神经节细胞层和内核层面板左列中的黑点)。我们利用Retistruct将组织的四叶苜蓿形状重建为眼杯原始的近半球形结构,以计算整个视网膜的细胞密度41。
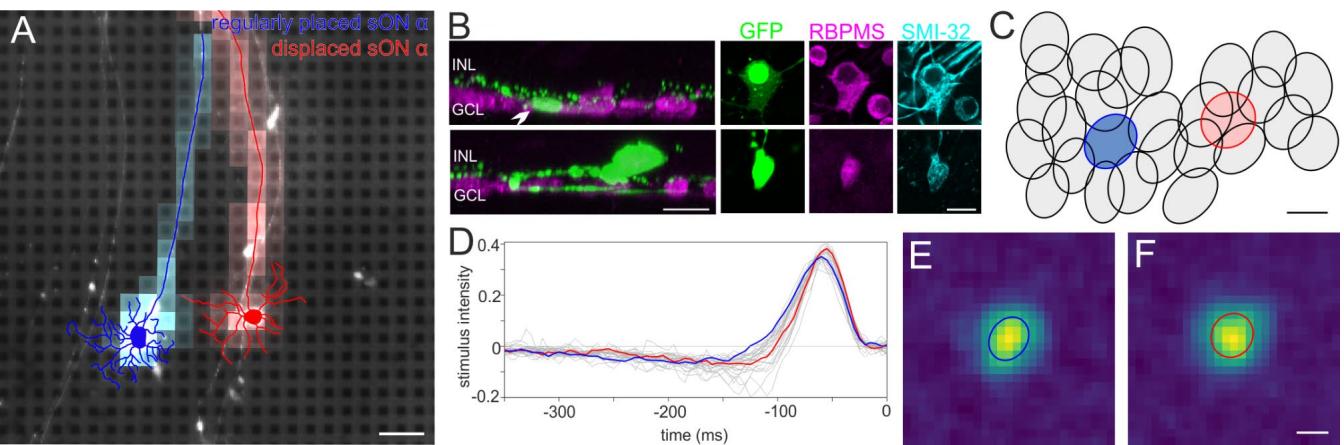
图6. 错位的和正常的sONɑ视网膜神经节细胞(RGC)具有相似的光响应特性。(A)MEA上记录的GFP-O视网膜的落射荧光图像显示,正常位置的sONɑ(蓝色描记)和错位的sONɑ RGC(红色描记)中存在天然GFP荧光,叠加了各自的电图像。比例尺100μm。(B)经抗RBPMS、GFP和SMI-32抗体染色后,(A)中相同细胞的共聚焦图像堆栈投影。左图:正常位置sONɑ(上)和错位sONɑ RGC(下)的细胞体(箭头)和树突的侧视投影。INL:内核层,GCL:神经节细胞层。右图:左图(及(A)中)标记细胞的细胞体的GFP、RBPMS和SMI-32染色的顶部(整装)视图投影。两种细胞均对SMI-32呈强免疫阳性。比例尺20μm。(C)sONɑ RGC镶嵌的感受野轮廓。蓝色和红色椭圆分别表示(A)中正常位置和错位sONɑ RGC的感受野拟合。比例尺100μm。(D)(C)中所示所有sONɑ RGC的脉冲触发平均刺激时间进程。蓝色和红色线分别表示(A)中正常位置和错位RGC的时间进程。(E)(A)-(D)中所示正常位置sONɑ RGC的空间感受野。(F)(A)-(D)中所示错位sONɑ RGC的空间感受野。比例尺100μm。
三维空间中的局部密度被投影到方位等距图中,并由点的颜色表示(图7,神经节细胞层和内核层面板中间列的彩色点)。通过对重建视网膜的密度计算,我们能够观察到每种分析类型下4或5个视网膜的平均数据(图7,神经节细胞层和内核层面板右侧列的彩色圆盘)。
¶ 视网膜神经节细胞(RGC)类型在视网膜中的分布——神经节细胞层(GCL)
我们在完整视网膜的神经节细胞层中识别出51946±3165个视网膜神经节细胞体(n=4),这与之前的报道基本一致12,13。视网膜神经节细胞在小鼠视网膜中的分布并不均匀(图7A-C)。除了总体的从中央到周边的梯度分布外,密度分布显示在背侧半部分,朝着视神经盘上方的视网膜神经节细胞密度最高区域以及 ventral 视网膜,密度有急剧增加。
M1、M2和sONɑ视网膜神经节细胞(RGCs)在神经节细胞层中的分布并不遵循所有RGCs的整体密度梯度,而是呈现出特定类型的分布模式。每个视网膜中M1内在光敏视网膜神经节细胞(ipRGCs)的数量为805±57个(n=5)(图7G-I)。这占神经节细胞层(GCL)中所有RGCs的1.6±0.2%。它们在视网膜的背侧和颞侧周边区域密度更高。M2 ipRGCs在视网膜背侧区域密度较高(n=5,图7M-O)45。我们统计到每个视网膜中有336±43个M2 ipRGCs。这些细胞占GCL中所有RGCs的0.7±0.1%。sONɑ RGCs在视网膜的背颞侧密度达到峰值11(图7S-U)。我们统计到每个视网膜中有1043±49个sONɑ RGCs(n=4)。这些细胞占GCL中所有RGCs的2.0±0.2%。
¶ 视网膜内ipRGC类型的分布——内核层(INL)
dRGCs的胞体位于内核层最靠近近端的部分。它们与无长突细胞的区别在于其更大的胞体和RBPMS免疫反应性。然而,与位置正常的对应细胞相比,dRGCs的胞体大小明显更小(图3G;胞体直径:M1为12.8±1.6μm,n=114;移位的M1为10.0±1.6μm,n=81(威尔科克森秩和检验p<0.001);sONɑ为20.7±1.3μm,n=75;移位的sONɑ为15.5±1.0μm,n=21(威尔科克森秩和检验p<0.001)。
不同类型的规则排列的视网膜神经节细胞(RGC)在视网膜上呈现出不同的密度模式,这与之前关于小鼠视网膜中RGC分布的研究结果一致16。人们曾认为错位视网膜神经节细胞(dRGC)主要出现在视网膜的远周边部(外边缘区12),且分布可能是随机的。然而,对这些错位视网膜神经节细胞的分析显示,内核层(INL)中的细胞体存在细胞类型特异性模式,这种模式既不符合所有视网膜神经节细胞的总体密度分布,也不符合相应细胞类型的密度分布(图7,右侧内核层面板)。
平均每个视网膜可量化出1264 ± 49个dRGC(n = 4)。这一数量占所有RGC的2.4 ± 0.2%。dRGC的胞体聚集在视网膜周边,但在视网膜更靠近中央的部位也观察到了大量dRGC,特别是在视盘上方区域和背颞区(图7D-F)。每个视网膜中计数到的位移M1型内在光敏感视网膜神经节细胞(ipRGC)为154 ± 15个(n = 5),占所有M1型细胞的16.1 ± 1.9%。位移的M1型细胞胞体主要聚集在视盘上方的条纹状区域(图7J-L)。与之形成鲜明对比的是,M2型细胞的胞体很少发生位移,平均每个视网膜中仅计数到5 ± 4个位移的M2型ipRGC(n = 5;图7P-R)。
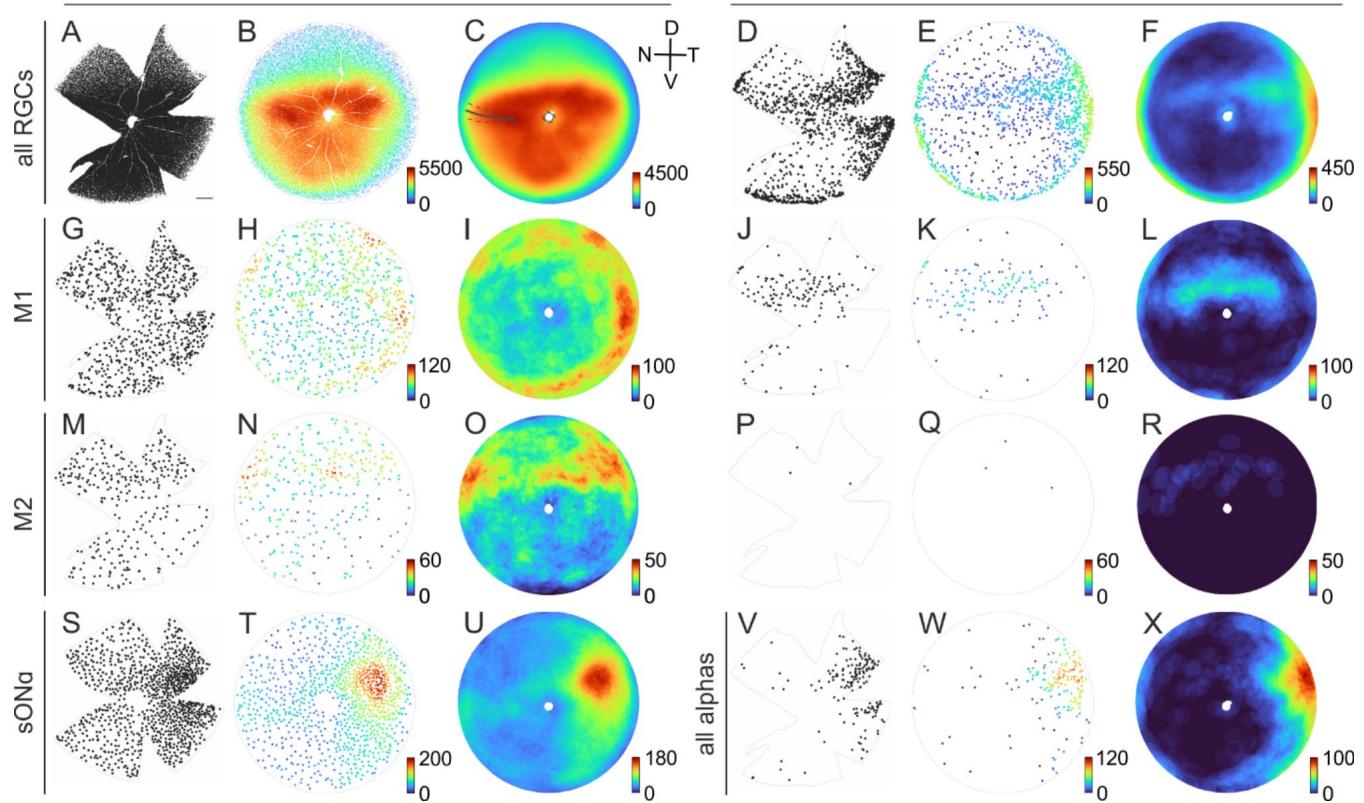
图7. 视网膜中的细胞群密度。(A) 每个点表示单个视网膜神经节细胞(RGC)的位置,其细胞体位于左鼠眼视网膜的神经节细胞层(灰色轮廓),并用RGC标志物RBPMS标记。(A)中的比例尺为500 μm,适用于所有四叶苜蓿形样本。(B) 重建视网膜球体的方位等距投影。点的颜色代表对应细胞在10度半径(球面距离约262 μm)内的局部密度。色标:细胞密度/平方毫米。© 如(B)中的密度分布,取4个视网膜的平均值。对于多个视网膜的平均值,视网膜方向根据鼻侧脉络膜裂的个别切口进行了调整。灰色实线:用于分析的所有视网膜的平均裂隙切口(n = 10);虚线:标准差。(D = 背侧,V = 腹侧,N = 鼻侧,T = 颞侧)(D)-(F) 如(A)-©,为位移视网膜神经节细胞。(G)-(L) 如(A)-(F),为M1型内在光敏视网膜神经节细胞(ipRGCs,黑视蛋白阳性,骨桥蛋白阴性),取5个视网膜的平均值。(M)-® 如(A)-(F),为M2型内在光敏视网膜神经节细胞(黑视蛋白阳性,骨桥蛋白阳性),取5个视网膜的平均值。(S)-(U) 如(A)-©,为神经节细胞层(GCL)中的sONɑ型视网膜神经节细胞(SMI-32阳性,钙结合蛋白阳性,骨桥蛋白阳性);(V)-(X) 如(D)-(F),为内核层(INL)中的所有ɑ型视网膜神经节细胞(黑视蛋白阴性,骨桥蛋白阳性),取4个视网膜的平均值。出于技术原因,分析的是所有ɑ型视网膜神经节细胞而非sONɑ型,详见结果部分的进一步解释。
在对跨平铺扫描的细胞体位置进行这种大规模分析时,我们不得不依赖落射荧光成像(见方法部分),这与上述SMI-32追踪所用的共聚焦扫描不同(图4)。由于光学分辨率存在相关限制,无法可靠地量化移位的sONɑ视网膜神经节细胞(RGCs)的数量和分布。与位置正常的对应细胞一样,它们对SMI-32和钙结合蛋白呈阳性,但细胞体更小(图3G),染色强度相对较低,且常被水平细胞的强荧光所叠加。因此,我们依靠RBPMS、黑视蛋白和骨桥蛋白的组合来分析移位的ɑRGCs群体,而不对这四种类型进行区分(每个视网膜有206±35个移位的ɑRGCs,n=4)。移位的ɑRGCs的分布仅在一定程度上与神经节细胞层(GCL)中sONɑ RGCs的分布相似(图7V-X)。与位置正常的sONɑ RGCs(图7S-U)类似,对移位的ɑRGCs(占ɑRGCs总群体的7.5±1.1%)的分析显示,在视网膜背颞侧存在一个密度峰值区域。然而,与神经节细胞层中sONɑ RGCs的峰值区域相比,移位的ɑRGCs的密度峰值更靠近视网膜的周边边缘。
¶ 讨论
在本研究中,我们引入骨桥蛋白作为α视网膜神经节细胞(α RGCs)和M2内在光敏视网膜神经节细胞(M2 ipRGCs)的标志物,这使我们能够分析方向选择性视网膜神经节细胞(dRGCs)在完整视网膜中的类型特异性分布和空间排列,以及它们与神经节细胞层(GCL)中伙伴细胞的直接关系。我们发现,方向选择性视网膜神经节细胞的分布并不遵循神经节细胞层中细胞的整体密度分布,这与大鼠视网膜的研究结果一致52。此外,我们发现细胞体的位移具有类型依赖性,并且我们提供了解剖学和电生理学证据,证明方向选择性视网膜神经节细胞完善了常规视网膜神经节细胞的平铺模式,从而形成镶嵌结构。
¶ 表2. 细胞计数
| Animal #|RGCs in the GCL | dRGCs in the INL | Total number of RGCs | |
| 1 | 49,199 | 1200 | 50,399 |
| 2 | 50,226 | 1273 | 51,499 |
| 3 | 51,990 | 1318 | 53,308 |
| 4 | 56,369 | 1265 | 57,634 |
| Mean | 51,946 | 1264 | 53,210 |
| SD | 3166 | 49 | 3184 |
| M1 ipRGCs in theGCL | Total number of M1 ipRGCs | ||
| 1 | 847 | 156 | 1003 |
| 2 | 800 | 173 | 973 |
| 4 | 833 | 139 | 972 |
| 5 | 708 | 138 | 846 |
| 6 | 837 | 164 | 1001 |
| Mean | 805 | 154 | 959 |
| SD | 57 | 15 Displaced M2 | 65 |
| M2 ipRGCs in theGCL | ipRGCs in the INL | Total number of M2 ipRGCs | |
| 1 | 356 | 11 | 367 |
| 2 | 384 | 2 | 386 |
| 4 | 302 | 3 | 305 |
| 5 | 281 | 2 | 283 |
| 6 | 356 | 9 | 365 |
| Mean | 336 | 5 | 341 |
| SD | 43 | 4 | 45 |
| sONa RGCs in theGCL | |||
| 7 | 1029 | ||
| 8 | 1092 | ||
| 9 | 1070 | ||
| 10 | 981 | ||
| Mean | 1043 | ||
| SD | 49 | ||
| aRGCs in the GCL | Displaced aRGCs in the INL | Total number of aRGCs | |
| 1 | 2285 | 193 | 2478 |
| 2 | 2367 | 218 | 2585 |
| 3 | 247 | ||
| 4 | 2449 | 164 | 2613 |
| Mean | 2367 | 206 | 2559 |
| SD | 82 | 35 | 71 |
¶ 小鼠视网膜神经节细胞密度梯度
最初,小鼠视网膜神经节细胞(RGCs)的总体密度分布被描述为相当均匀,仅存在轻微的从中心到周边的梯度变化12,53。随着在分子细胞标记物使用以及细胞类型分类功能分析方面的方法学不断进步,研究发现存在复杂的密度梯度模式16。在此,我们为所有视网膜神经节细胞以及各亚型细胞的不同密度分布提供了进一步的证据。与先前对小鼠和大鼠视网膜的研究结果一致13,54,总体视网膜神经节细胞密度呈现出从远背侧视网膜的低密度急剧增加到视盘上方区域的最高密度,且腹侧视网膜的密度通常较高的特点。这种密度增加大致与光感受器视蛋白表达的过渡区相吻合(数据未显示),因此应该与该动物视觉环境中的地平线相对应55,56。
我们观察到的常规sONɑ视网膜神经节细胞和M1型内在光敏视网膜神经节细胞的分布模式也与先前报道的结果相似11,45,57,这些结果表明sONɑ视网膜神经节细胞的背颞侧密度峰值与小鼠视野的双眼区域相吻合。然而,M2型内在光敏视网膜神经节细胞的密度与先前的报道存在差异20,45,即本研究中的密度约为先前报道的一半。这种差异可能是由于本研究分析的是整个视网膜,而其他研究则是对小得多的组织区域进行量化造成的。例如,根据背侧峰值区域的M2型内在光敏视网膜神经节细胞密度(图7O)推算整个视网膜的数量,得出的数值与先前发表的结果相符。由于 melanopsin 免疫染色可能较弱而导致我们在量化时遗漏了大量细胞,这种情况是不太可能的,因为在我们的样本中,即使不使用进一步的增强技术,也经常能观察到 melanopsin 弱阳性的sONɑ视网膜神经节细胞32。因此,melanopsin 阳性的sONɑ视网膜神经节细胞的观察结果可作为染色强度最佳的内在对照。
¶ 移位神经节细胞的密度梯度和空间排列
已有研究表明,移位神经节细胞存在于多种脊椎动物中,如鱼类、鸟类以及包括人类视网膜在内的哺乳动物(例如12,13,52,54,58–65)。然而,移位视网膜神经节细胞(dRGCs)究竟是独立的细胞类型、常规类型群体中的特殊部分,还是神经元发育紊乱留下的无用残余,目前尚不清楚。局部视网膜区域内常规视网膜神经节细胞类型的标志性特征是其均一的树突形态、相应形成的独立镶嵌结构,以及均一的光响应特性66。尽管已知移位视网膜神经节细胞(dRGCs)的存在,但它们相对于正常位置视网膜神经节细胞的空间排列及其光响应特性均尚未被研究过。
我们的数据现在表明,至少对于小鼠视网膜中两种已确定的视网膜神经节细胞(RGC)类型而言,位移型视网膜神经节细胞(dRGCs)是其规则排列对应细胞群体的一部分,并且它们作为相应镶嵌结构的正常细胞成分进行排列。位移型视网膜神经节细胞的树突结构以及它们与邻近细胞的树突重叠程度,与规则排列的视网膜神经节细胞没有明显差异。有趣的是,它们的出现频率并不受其规则排列对应细胞密度的影响——假设规则排列细胞的数量越多,发生位移的可能性就越大。 先前的研究表明,哺乳动物视网膜中的位移型视网膜神经节细胞是由于个体发育异常而错位的34。虽然位移的原因仍不明确,但它不太可能是随机发生的,因为此处所示的位移模式以特定类型的方式出现,且在多个样本中保持一致。尽管如此,发育过程中细胞类型特异性的基因表达水平可能在位移型视网膜神经节细胞模式的形成中发挥作用。有研究表明,细胞外基质蛋白糖原合成酶激酶3(GSK3)有助于视网膜神经节细胞的空间组织67。缺乏一个GSK3等位基因会导致位移型视网膜神经节细胞数量增加,但这并非由于细胞过度生成,因为视网膜神经节细胞的总数是稳定的。 一种推测是,sONɑ和M1型视网膜神经节细胞在发育过程中可能表达较低水平的GSK3,因此与例如M2型视网膜神经节细胞相比,它们向神经节细胞层(GCL)的迁移更容易受到干扰。M2型细胞很少被发现发生位移,这进一步支持了存在细胞类型依赖性机制的观点。
在小鼠视网膜中已证实,移位视网膜神经节细胞(dRGCs)是一个高度多样化的群体,包含形态各异的细胞33,34。我们观察到,移位α视网膜神经节细胞以及移位M1和M2内在光敏视网膜神经节细胞加起来仅占所有移位视网膜神经节细胞的约30%(其中M2内在光敏视网膜神经节细胞占比不足1%)。根据区域差异和密度梯度,不同细胞类型的形态变化16可能导致先前研究中对移位视网膜神经节细胞多样性的估计略有偏高。尽管如此,人们仍有望发现除本文所研究的三种类型之外,许多其他类型视网膜神经节细胞的移位细胞体。所有小鼠移位视网膜神经节细胞是否都遵循我们发现的适用于这组细胞的规则,仍有待阐明。
¶ 移位神经节细胞是否具有特殊的功能作用?
我们的数据显示,位移视网膜神经节细胞(dRGCs)完善了其规则排列同伴的树突及相应的功能性感受野镶嵌结构,且dRGCs与该镶嵌结构中其他细胞的基本光响应特性并无差异。因此,我们得出结论:它们属于同一类型,发挥着相同的功能作用。然而,特定类型的位移模式,以及例如位移的M1型内在感光视网膜神经节细胞(ipRGCs)形成的条纹状区域——这在其规则排列的同伴中并不明显——促使人们认为,小鼠dRGCs的特殊作用仍有待发现。
在鸟类视网膜中,人们确实认为一小群错位视网膜神经节细胞(dRGCs)是一种独立的细胞类型68。错位视网膜神经节细胞仅投射至基底视束核(nBOR),因此被认为与视动性眼球震颤有关,并参与视网膜图像稳定35–37,69。鸟类基底视束核在哺乳动物中的同源结构是内侧终末核(MTN)。研究表明,家兔的这一区域几乎不接收或完全不接收来自错位视网膜神经节细胞的输入70。然而,在转基因小鼠中,错位视网膜神经节细胞数量的增加伴随着内侧终末核中视网膜神经节细胞轴突终末数量的增多67。因此,关于哺乳动物内侧终末核是否接受错位视网膜神经节细胞支配的研究结果仍不明确,需要进一步研究以深入了解错位视网膜神经节细胞类型在眼球运动中可能发挥的作用。
研究表明,移位的内在光敏视网膜神经节细胞(ipRGCs)在小鼠视网膜的视盘上方区域聚集。在此,我们提供的证据表明,这种现象是由于移位的M1型内在光敏视网膜神经节细胞形成了条带状的密度峰值所致。对M1型内在光敏视网膜神经节细胞进行明确分类仍存在挑战,因为它们可能包含不同的亚型,这些亚型表现出功能差异、不同水平的黑视蛋白、不同的基因表达模式,并投射到不同的靶区。考虑到内在光敏视网膜神经节细胞亚型可能形成独立的镶嵌结构,我们不禁推测,一种特定的M1亚型是导致条带状区域中移位视网膜神经节细胞(dRGCs)富集的原因。然而,这仍有待未来的研究,一旦有可靠的工具能够特异性区分推测的M1亚型,相关研究便可开展。
定向的、细胞类型特异性的细胞体位移可能会给错位视网膜神经节细胞(dRGCs)带来哪些益处呢?由于所有树突树都在同一水平分层,且可能与相同的突触伙伴相互作用,因此常见突触环路的变化现在可以被排除。然而,由在最远端内网层(IPL)分层的突触前细胞形成的、直接指向dRGCs细胞体的突触输入可能发挥着关键作用。内网层(IPL)与内核层(INL)交界处存在此类环路的一个例子是核周巢,它由多巴胺能无长突细胞在突触后AII无长突细胞的细胞体周围形成77–79。有研究表明,树突-胞体突触相互作用也会发生在常规神经节细胞体上,且具有重大的功能影响80,这也可能代表着内核层(INL)中无长突细胞与dRGCs相互作用的一种环路模式。此外,已知小鼠视网膜中一部分dRGCs会表达特定的电压门控钙通道亚基,而这些亚基在常规视网膜神经节细胞(RGCs)中并未发现,这表明这些dRGCs可能具有独特的功能特性81。
因此,我们的数据表明,小鼠的离散视网膜神经节细胞(dRGCs)主要履行与其常规对应细胞相同的功能。然而,通过详细研究离散视网膜神经节细胞的生理和遗传特性,并将其与其规则排列的伙伴细胞直接关联,可能会发现其他功能特征。
¶ 数据可用性
数据可根据合理请求从通讯作者处获取。
¶ 参考文献
- 巴登(T.)等人。小鼠视网膜神经节细胞的功能多样性。《自然》,529卷,345–350页(2016年)。
- Tran, N. M. 等人。对损伤恢复力不同的视网膜神经节细胞的单细胞图谱揭示了神经保护基因。《神经元》104, 1039–1055e12 (2019)。
- 土井(Doi)、宇治(Uji)和山村(Yamamura):《小鼠视网膜神经节细胞的形态分类》,《比较神经学杂志》(J. Comp. Neurol.),356卷,368-386页(1995年)。
- 孙伟、李宁和何思。小鼠视网膜神经节细胞的大规模形态学研究。《比较神经学杂志》451,115–126(2002)。
- Wässle, H. 与 Riemann, H. J. 哺乳动物视网膜中的神经细胞镶嵌体。24(1978)。
- Wässle, H., Peichl, L. 及 Boycott, B. B. 猫视网膜神经节细胞的树突区域。《自然》292, 344–345 (1981)。
- 斯通,J. 猫视网膜神经节细胞分布的定量分析。《比较神经学杂志》124,337-352(1965)。
- Oyster, C. W., Takahashi, E. S. 与 Hurst, D. C. 兔视网膜神经节细胞的密度、胞体大小及区域分布。《神经科学杂志》(神经科学学会官方期刊)1, 1331–1346 (1981)。
- Curcio, C. A. 与 Allen, K. A. 人视网膜神经节细胞的拓扑结构。《比较神经学杂志》300, 5–25 (1990)。
- 科林,S. P. 一个基于网络的脊椎动物视网膜细胞分布地形图档案库。《临床与实验视光学》91,85-95(2008)。
- Bleckert, A.、Schwartz, G. W.、Turner, M. H.、Rieke, F. 和 Wong, R. O. L. 小鼠不同视网膜神经节细胞类型的视觉空间由不匹配的拓扑结构表示。《当代生物学》24, 310–315 (2014)。
- Dräger, U. C. 与 Olsen, J. F. 神经节细胞。小鼠视网膜分布 20, 9 (1981)。
- Salinas-Navarro, M. 等人。成年白化病小鼠和有色小鼠的视网膜神经节细胞群:整个细胞群及其空间分布的计算机分析。《视觉研究》,49卷,637-647页(2009年)。
- 张宇、金伊珍、简·R·塞恩斯和迈克尔·迈斯特。小鼠视网膜中数量最多的神经节细胞类型是一种选择性特征检测器。《美国国家科学院院刊》109卷,E2391–E2398页(2012年)。
- Rousso, D. L. 等人。两对ON和OFF视网膜神经节细胞由转录因子表达的交叉模式定义。《细胞报告》,15卷,1930-1944页(2016年)。
- 霍伊坎普(A. S.)、沃里克(R. A.)和里夫林-埃茨昂(M.)。视觉空间视网膜编码的地形变化。《视觉科学年度评论》6,237-259(2020)。
- Provencio, I. 等。内层视网膜中一种新型人类视蛋白。《神经科学杂志》20, 600–605 (2000)。
- 伯森(D. M.)、邓恩(F. A.)和高尾(M.)。调节生物钟的视网膜神经节细胞的光转导。295,5(2002)。
- 哈塔尔(S.)、廖(H. W.)、高尾(M.)、伯森(D. M.)和丘(K. W.)。含黑视蛋白的视网膜神经节细胞:结构、投射及内在光敏性。《科学》,295卷,1065-1070页(2002年)。
- 贝尔森(D. M.)、卡斯特鲁奇(A. M.)和普罗文西奥(I.)。小鼠中表达黑视蛋白的视网膜神经节细胞类型的形态和镶嵌结构。《比较神经学杂志》,18(2010)。
- 纳西尔-艾哈迈德(S.)、李(S. C. S.)、马丁(P. R.)和格吕内特(U.)。人视网膜中表达黑视蛋白的神经节细胞:形态、分布和突触连接。《比较神经学杂志》,527卷,312-327页(2019年)。
- 哈弗坎普(S.)、米奇(M.)和布里格曼(K. L.)。普通狨猴视网膜的发育错误。《神经解剖学前沿》,16,(2022)。
- 菲茨帕特里克,M.J.、克里赞,J.、向,J.C.、沈,N.、克申施泰纳,D. 小鼠和人类的瞳孔对比度反应:神经机制和视觉功能。《神经元》112期,2404–2422e9(2024)。
- 高(J.)等人。实验性青光眼对小鼠内在光敏视网膜神经节细胞的不同影响。《比较神经学杂志》,530卷,1494页(2022年)。
- 阿兰达,M. L. 和施密特,T. M. 内在光敏感视网膜神经节细胞的多样性:回路与功能。《细胞与分子生命科学》(CMLS),78,889–907(2021)。
- 埃克,J. L. 表达黑视蛋白的视网膜神经节细胞光感受器:细胞多样性及其在模式视觉中的作用。12(2010)。
- Quattrochi, L. E. 等人。M6细胞:一种小视野双层感光视网膜神经节细胞。《比较神经学杂志》,527卷,297-311页(2019年)。
- 施密特(T. M.)、陈(S. K.)和哈塔尔(S.)。内在光敏视网膜神经节细胞:多种亚型,多种功能。《神经科学趋势》,34卷,572-580页(2011年)。
- 施密特(T. M.)等人。黑视蛋白在α视网膜神经节细胞和对比度检测中的作用。《神经元》82期,781-788页(2014年)。
- Stabio, M. E. 等人。M5细胞:一种色拮抗型内在光敏视网膜神经节细胞。《神经元》97,150–163e4(2018)。
- 贝里,M. H. 等。一种黑视蛋白神经节细胞亚型形成投射至视上核的视网膜背侧镶嵌体。《自然·通讯》,14,1492(2023)。
- Estevez, M. E. 等人。M4细胞的形态与功能:一种参与膝状体皮质视觉的内在光敏视网膜神经节细胞类型。《神经科学杂志》32,13608–13620(2012)。
- 庞继军、吴世敏。小鼠视网膜中逆行双标神经节细胞的形态学及免疫反应性。《眼科学研究与视觉科学》,52卷,4886页(2011年)。
- 布尔(Buhl)、E. H. 与丹恩(Dann)、J. F. 《大鼠移位视网膜神经节细胞的形态多样性:荧光黄研究》,《比较神经学杂志》(J. Comp. Neurol.),269卷,210-218页(1988年)。
- 辛普森(J. I.). 副视系统. 《神经科学年度评论》, 7, 13-41 (1984).
- Dann, J. F. 和 Buhl, E. H. 大鼠中投射至副视系统的视网膜神经节细胞。《比较神经学杂志》,262期,141-158页(1987年)。
- 库克(J. E.)和波杜戈尔尼科娃(T. A.)。蛙、爬行动物、鸟类和哺乳动物中投射到副视系统的视网膜神经节细胞存在空间规律性的证据。《视觉神经科学》,18卷,289-297页(2001年)。
- 冯国等。在表达多种光谱变体GFP的转基因小鼠中成像神经元亚群。《神经元》28,41–51(2000)。
- Stabio, M. E. 等人。用于在解剖空间中确定视网膜地形方向的新型小鼠眼图谱。《比较神经学杂志》526, 1749–1759 (2018)。《神经科学》6, 95–111 (1991)。
- Sterratt, D. C., Lyngholm, D., Willshaw, D. J. 及 Thompson, I. D. 小鼠视网膜的标准解剖学和视觉空间:利用retistruct软件包对扁平化视网膜进行计算重建和转换。《公共科学图书馆·计算生物学》9, e1002921 (2013)。
- Schmucker, C. 和 Schaeffel, F. 一种用于生长中的C57BL/6小鼠的近轴示意图眼模型。《视觉研究》44, 1857–1867 (2004)。
- Field, G. D. 等人。灵长类视网膜中小双分层神经节细胞的空间特性和功能组织。《神经科学杂志》,27卷,13261–13272页(2007年)。
- Litke, A. M. 等。眼睛告诉大脑什么?视网膜输出活动大规模记录系统的开发。《IEEE核科学汇刊》51,1434–1440(2004)。
- 休斯(S.)、沃森(T. S.)、福斯特(R. G.)、皮尔逊(S. N.)和汉金斯(M. W.)。小鼠视网膜中光敏视网膜神经节细胞的非均匀分布和光谱调谐。《当代生物学》,23卷,1696-1701页(2013年)。
- 段X. 轴突切断后视网膜神经节细胞的亚型特异性再生:骨桥蛋白和mTOR的作用。《信号传导》22(2015)。
- 克里格(B. Krieger)、乔(M. Qiao)、鲁索(D. L. Rousso)、桑斯(J. R. Sanes)和迈斯特(M. Meister)。小鼠视网膜中的四种α神经节细胞类型:功能、结构和分子特征。《公共科学图书馆·综合》,12卷,e0180091(2017年)。
- Straznicky, C., Vickers, J. C., Gábriel, R. 和 Costa, M. 一种神经丝蛋白抗体选择性标记人类视网膜中的一种大型神经节细胞类型。《脑研究》582, 123–128 (1992)。
- 罗德里格斯(A. R.)、德塞维利亚·米勒(L. P.)和布雷查(N. C.)。RNA结合蛋白RBPMS是哺乳动物视网膜神经节细胞的选择性标志物。《比较神经学杂志》,522卷,1411-1443页(2014年)。
- 施密特,T. M. 和科富士,P. 内在光敏视网膜神经节细胞之间的功能和形态差异。7(2009)。
- 诺依曼(S.)、胡塞尔(L.)、翁德雷卡(K.)、奥勒(N.)和哈弗坎普(S.)。小鼠视网膜中神经节细胞的细胞类型特异性双极细胞输入。《神经科学》,316期,420-432页(2016年)。
- 纳达尔-尼古拉斯,F. M. 等。白化大鼠和有色大鼠的视网膜神经节细胞移位。《神经解剖学前沿》8, 99 (2014)。
- 全俊才(Jeon, C. J.)、埃莱奥诺拉·斯特雷托伊(Strettoi, E.)和理查德·H·马斯兰(Masland, R. H.)。小鼠视网膜的主要细胞群。《神经科学杂志》,18卷,8936-8946页(1998年)。
- Salinas-Navarro, M. 等人。成年大鼠整个视网膜神经节细胞群及其空间分布的计算机化分析。《视觉研究》,49卷,115-126页(2009年)。
- 巴登(T.)等人。《两个视网膜区域的故事:通过不对称光感受器分布对自然场景中消色差对比度的近最优采样》。《神经元》80期,1206–1217页(2013年)。
- 纳达尔-尼古拉斯,F. M. 等。真正的S视锥细胞集中在小鼠视网膜腹侧,并通过连接实现上部视野的颜色检测。《eLife》9,e56840(2020)。
- 约翰逊(K. P.)等人。特定细胞类型的双眼视觉指导小鼠的捕食行为。《神经元》109期,1527–1539e4(2021)。
- Dacey, D. M. 等。灵长类视网膜中表达黑视蛋白的神经节细胞可传递颜色和辐照度信号,并投射至外侧膝状体。《自然》433, 749–754 (2005)。
- 钱德拉(A. J.)、李(S. C. S.)和格吕内特(U.)。人类和狨猴内层视网膜中的黑视蛋白和钙结合蛋白免疫反应性。《视觉神经科学》,36卷,E009页(2019年)。
- 星野(H.)和佐藤(F.)。金鱼视网膜中央区域定向偏好的位移大视野神经节细胞的形态学特征。《比较神经学杂志》,526卷,243-261页(2018年)。
- Mey, J. 和 Johann, V. 鸡(Gallus gallus)移位视网膜神经节细胞的树突发育和靶标神经支配。《国际发育神经科学杂志》(国际发育神经科学学会官方期刊),19,517–531(2001)。
- 邦特,A. H. 和明克勒,D. S. 猴子视网膜中移位的神经节细胞。《眼科研究与视科学》,16,95-98(1977)。
- Stell, W. K. 和 Witkovsky, P. 平滑角鲨(Mustelus Canis)的视网膜结构:巨型神经节细胞的一般描述和光学显微镜观察。《比较神经学杂志》,148卷,1-31页(1973年)。
- 橘(Tachibana, M.)。辣根过氧化物酶技术显示鲤鱼视网膜中移位的神经节细胞。《神经科学通讯》(Neurosci. Lett.)9, 153–157(1978)。
- 罗布森(J. A.)和霍兰德(H.)。家兔视网膜中移位的神经节细胞。《眼科研究与视科学》,25卷,1376-1381页(1984年)。
- 弗拉西茨(A. L.)、欧拉(T.)和弗兰克(K.)。功能优先:视网膜细胞类型和回路的分类。《当代神经生物学观点》,56卷,8–15页(2019年)。
- Kisseleff, E. 等。糖原合成酶激酶3调节错位视网膜神经节细胞的生成3。eNeuro 8, ENEURO.0171-21.2021(2021)。
- Haverkamp, S., Albert, L., Balaji, V., Němec, P. 及 Dedek, K. 鸟类视网膜与狨猴视网膜中细胞标志物和转录因子的表达。《比较神经学杂志》,529卷,3171-3193页(2021年)。
- 菲特(K. V.)、布雷查(N.)、卡滕(H. J.)和亨特(S. P.)。鸽子的移位神经节细胞与副视系统。《比较神经学杂志》,195卷,279-288页(1981年)。
- Oyster, C. W., Simpson, J. I., Takahashi, E. S. 及 Soodak, R. E. 投射至兔副视系统的视网膜神经节细胞。《比较神经学杂志》,190期,49-61页(1980年)。
- Valiente-Soriano, F. J. 等。色素小鼠和白化病小鼠中黑视蛋白阳性神经元的分布:小鼠视网膜中黑视蛋白中间神经元的证据。《神经解剖学前沿》8, 131 (2014)。
- Hattar, S. 等。小鼠中表达黑视蛋白的视网膜神经节细胞的中枢投射。《比较神经学杂志》,497卷,326-349页(2006年)。
- Jain, V.、Ravindran, E. 和 Dhingra, N. K. 小鼠内在光敏视网膜神经节细胞中Brn3转录因子的差异表达。《比较神经学杂志》,520卷,742-755页(2012年)。
- 李,J. Y. 和施密特,T. M. M1型内在光敏视网膜神经节细胞亚型的不同投射模式。《比较神经学杂志》526,2010–2018(2018)。
- 伊曼纽尔(A. J.)、卡普尔(K.)和多(M. T. H.)。神经节细胞光感受器M1型内的生物物理变异。《细胞报告》,21卷,1048-1062页(2017年)。
- Laboissonniere, L. A. 等人。通过单细胞分析揭示视网膜神经节细胞的分子特征。《科学报告》9, 15778 (2019)。
- 福格特,T. 和瓦塞尔,H. 哺乳动物视网膜中A II无长突细胞的多巴胺能神经支配。《神经科学杂志》7,4115–4128(1987)。
- Casini, G.、Rickman, D. W. 和 Brecha, N. C. 家兔视网膜中的AII无长突细胞群:通过小白蛋白免疫反应性进行识别。《比较神经学杂志》356, 132–142 (1995)。
- Contini, M. 与 Raviola, E. 视网膜多巴胺能神经元形成的GABA能突触。《美国国家科学院院刊》100, 1358–1363 (2003)。
- Grimes, W. N. 等人。神经节细胞的树突-胞体突触输入与哺乳动物视网膜中的感受野和连接常规相悖。《当代生物学》32,315–328e4(2022)。
- 德塞维利亚·穆勒,L. P.、刘,J.、所罗门,A.、罗德里格斯,A. 和布雷查,N. C. 小鼠和大鼠视网膜中电压门控钙通道Α2δ4亚基的表达。《比较神经学杂志》521,2486–2501(2013)。