¶ 《神经工程杂志》
¶ 器官型人脑切片培养物作为新型神经调节装置的转化测试平台
¶ 原文下载:eggert_2026_j._neural_eng._23_014001_origin.pdf
弗朗茨·A·M·埃格特1,2,3,4、贝尔汉·根茨1,2、塞纳·努尔·阿尔杜克2、阿努克·沃尔特斯1,2、金·里杰克斯1,2,5,6、克里斯汀·科齐尔斯基7、亚辛·泰梅尔1,2,8和阿里·贾汉沙希1,2,9,∗
1 荷兰马斯特里赫特市马斯特里赫特大学医学中心+神经外科
2 马斯特里赫特大学精神健康与神经科学研究所,荷兰马斯特里赫特
3 德国哈弗尔河畔勃兰登堡市勃兰登堡校区勃兰登堡医学院神经外科3系
4 健康科学学院,勃兰登堡工业大学、勃兰登堡医学院与波茨坦大学联合学院,德国波茨坦
5 荷兰马斯特里赫特大学综合神经科学中心,马斯特里赫特,荷兰
6 荷兰马斯特里赫特,马斯特里赫特大学医学中心+癫痫学学术中心6号
7 德国加兴,慕尼黑工业大学,慕尼黑生物医学工程研究所
8 伊斯坦布尔阿特拉斯大学,土耳其伊斯坦布尔
9 荷兰皇家艺术与科学院,荷兰神经科学研究所,阿姆斯特丹,荷兰
* 所有 correspondence 请寄至以下作者。
电子邮件:a.jahanshahi@maastrichtuniversity.nl
¶ 关键词:
磁电纳米颗粒,神经刺激,器官型人脑切片培养物,转化模型
¶ 摘要
目的:建立器官型人类脑片培养物(hBSCs)作为评估新型神经调节装置的转化筛选平台,并以磁电纳米颗粒(MENPs)作为代表性神经刺激方式来证明该模型的可行性。 方法:从癫痫手术患者切除的皮质组织中制备存活的hBSCs,并进行基于GCaMP的钙成像、多电极阵列记录以及c-Fos的免疫组织化学染色。将MENPs注入hBSCs中,并用交变磁场刺激,以评估其神经调节作用。 主要结果:GCaMP转导能够实时可视化MENP诱导的神经元活动。在新鲜切片中观察到包括尖峰和局部场电位在内的电生理信号,但在培养切片中未观察到。与假处理对照组相比,c-Fos免疫染色显示在经刺激的注射MENP的培养物中,c-Fos表达显著增加。该方案在患者来源的样本中产生了可重复的组织活力和一致的结果。 意义:本技术说明表明,hBSCs是一种可重复且在伦理上更优的转化模型,适用于神经技术研究中的筛选应用。该平台能够对神经调节装置进行早期功能评估,特别是那些在体内失败风险较高的装置,或在优于传统体外方法的环境中探索早期概念的装置。该平台可能有助于减少神经技术开发中对动物模型的依赖。
¶ 1. 引言
2022年,欧盟成员国和挪威有9237542只动物被用于科学研究(欧盟,2022年),科学界对动物模型的依赖程度不容忽视(Keifer和Summers,2016年)。这种依赖在神经科学领域同样存在,因为该领域严重依赖动物模型(尤其是啮齿类动物)来研究复杂的大脑功能和行为(Keifer和Summers,2016年;Moulin等人,2021年)。从伦理角度来看,在科学研究中使用动物是有正当理由的(Machan,2002年)。然而,根据4R框架(减少、优化、替代和责任),动物能够感受疼痛和痛苦这一特性,使其在科研中的使用始终存在伦理争议(Kiani等人,2022年)。
已有几种体外和离体方法被提出作为神经植入物测试的替代平台,特别是作为在进行体内研究之前评估组织反应的筛选工具(Gulino等人,2019年)。传统的细胞培养模型,包括人类诱导多能干细胞和永生化细胞系,已被视为中枢神经系统相关测试平台的宝贵工具(Nikolakopoulou等人,2020年)。然而,它们缺乏原生脑组织的结构和细胞复杂性。脑芯片系统和类器官提供了更先进的替代方案;但它们在复制人类大脑复杂的细胞结构和功能连接方面仍面临挑战(Cassotta等人,2022年)。
纳米材料已在不同物种的器官型脑切片培养物(BSCs)中进行了测试,展示出其在研究神经炎症、组织反应和神经退行性变方面的实用性(Kristensen等人,2001年;Huuskonen等人,2005年;Ereifej等人,2013年;Usmani等人,2016年)。尽管取得了这些进展,但用于评估神经植入物中纳米材料毒性的广泛认可的测试工具仍然匮乏(Chen等人,2020年)。人类脑切片培养物(hBSCs)具有优势,因为它们保留了人类特有的细胞结构、细胞多样性、细胞外基质组成和神经元连接性(Noraberg,2004年;Schwarz等人,2019年;Barth等人,2021年)。这些特性使hBSCs成为评估新型神经调节纳米材料的理想模型,特别是在初步筛选阶段(Gulino等人,2019年)。本研究将hBSCs作为一种转化测试平台,用于评估新型深部脑神经调节植入设备。在神经刺激材料开发的早期阶段,需要进行各种筛选研究,以评估刺激参数和材料生物相容性,然后再进行体内实验。
由于磁电纳米颗粒(MENPs)已在啮齿动物中进行过测试,显示出其改变神经生理活动和行为的潜力(Kozielski等人,2021年;Kumari等人,2024年;DominguezParedes等人,2025年),本研究建立了一个基于人骨髓间充质干细胞(hBSC)的磁电纳米颗粒测试流程,验证组织活力,并采用钙成像、电生理学和c-Fos免疫组织化学(IHC)等技术,以反向验证的方法评估其在神经调节研究中的潜力。c-Fos被选为神经元活动的标志物,是因为它在神经科学研究中应用广泛且成熟,并且易于量化(Lara Aparicio等人,2022年)。
¶ 2. 方法
¶ 2.1. 脑组织和脑脊液收集
2023年1月至2024年9月期间,在马斯特里赫特大学医学中心(MUMC+)神经外科接受前颞叶切除术(其中1例为最大范围颞叶切除术)的11名耐药性癫痫患者,被要求在门诊术前访视时同意(METC 2024-0344)收集切除的脑组织和人类脑脊液(hCSF)。
在获得书面知情同意后,切除的脑组织在手术切除后立即在手术室收集。此外,外科医生在标准操作中取出的人脑脊液被收集在试管中并置于冰上(图1(A))。作为全身麻醉的一部分,以常规剂量使用了丙泊酚、去甲肾上腺素、舒芬太尼和地塞米松等药物。在前颞叶切除术后,从切除的颞叶新皮质标本的后外侧区域取1×1.5厘米的脑组织样本。其余组织按标准医疗流程用于组织病理学分析。
¶ 2.2. 磁电纳米颗粒
MENPs由涂覆有压电材料钛酸钡(BaTiO3)的磁致伸缩材料钴铁氧体(CoFe2O4)纳米颗粒组成。当暴露在叠加有交变(AC)磁场的直流(DC)磁场中时,磁致伸缩核心会发生形变,应变会施加到压电涂层上,从而产生电极化。正如我们研究组先前的一项研究(Kozielski等人,2021年)中详细测量的那样,MENPs包含36.1±0.6%的钛酸钡和63.9±0.6%的钴铁氧体,在人工脑脊液(aCSF)中的平均直径为277±18纳米,zeta电位为6.7±0.5毫伏。使用前,将MENPs在超纯水中稀释(100微克/毫升)并充分涡旋。
¶ 2.3. 人脑切片培养物(hBSCs)的制备
器官型人脑切片方案采用自Bak等人2024年的先前研究。总之,新皮质脑组织样本立即浸入冰冷的、含碳混合气(95% O₂、5% CO₂)的切片人工脑脊液(s-aCSF;图1A)中。s-aCSF的组成成分为:110 mM氯化胆碱、26 mM碳酸氢钠、1.25 mM磷酸氢二钠二水合物、11.6 mM抗坏血酸钠、3.1 mM丙酮酸钠、7 mM氯化镁、0.5 mM氯化钙、2.5 mM氯化钾、10 mM葡萄糖(溶于超纯水),孵育时加入1%青霉素/链霉素/两性霉素B。胆碱可取代钠,从而阻断神经元活动,以减轻预期的切片应激。人脑脊液经离心(4℃,2000g)和无菌过滤以去除血液,之后要么在-80℃下储存,要么立即使用。
清洁和修整后(图1(B)),使用振动切片机(Leica VT1200S,德国威兹拉尔;图1(C)和(D))制作出面积约为0.75×0.75 cm、厚度为300 µm的脑切片。在整个操作过程中,组织浸没在冰冷的含碳混合气饱和人工脑脊液(s-aCSF)中。之后,将脑切片置于37°C的气液界面中,其中包括在HEPES培养基(混合23.5 ml DMEM/F-12、23.5 ml Neurobasal培养基、1 ml B27补充剂、0.5 ml N2补充剂、0.5 ml GlutaMAX和0.5 ml非必需氨基酸,制成50 ml)中放置60分钟的中间步骤。为进行培养,将切片转移至带有半透性(0.4 µm孔径)网状插入物的孔板(Corning® Transwell® 24 mm Transwell,带0.4 µm孔径聚酯膜插入物,经TC处理)中,该插入物作为人脑脊液(hCSF)和人工脑脊液(aCSF,按1:1比例混合,人工脑脊液成分为125 mM NaCl、25 mM NaHCO3、2.5 mM KCl、1.25 mM NaH2PO4、1 mM MgCl2·6H2O、2 mM CaCl2、25 mM葡萄糖,溶于超纯水)的气液界面,在37°C、5% CO2、95% O2的湿润环境中孵育至少48小时(图1(D))。

图1.(A)在冰冷、含氧的人工脑脊液(s-aCSF)中获取和运输脑组织。(B、C)器官型培养物的制备:将修整好的脑组织块粘在琼脂糖上,在振动切片机的腔室中切片,同时持续灌注冰冷、含氧的人工脑脊液(s-aCSF)。(D)将培养物放置在气液界面膜插入物上。(E)、(F)向人脑类器官(hBSC)中注射磁性纳米颗粒(MENPs)。(G)用于磁驱动的定制刺激线圈,突出显示了刺激腔室。(H)注射了磁性纳米颗粒(MENPs)的人脑类器官(hBSC)在浸入钙成像前固定在定制树脂网栅下方,以防止漂浮。(I)定制丙烯酸孔板支架,红色箭头指向刺激腔室内的孔板支架,白色箭头指示线圈和显微镜之间的间隙,以防止任何振动传递到显微镜。(J)主动钙成像装置(如(I)中所示的丙烯酸孔板支架,现在在刺激和持续荧光显微镜观察下放置孔板/人脑类器官(hBSC)/树脂网)。(K)多电极阵列(MEA),其上有经网固定且注射了磁性纳米颗粒(MENPs)的人脑类器官(hBSC)((黑色)切片网格,*(白色)可见磁性纳米颗粒(MENPs)聚集体的人脑类器官(hBSC),+多电极阵列(MEA)芯片)。(L)*放大的多电极阵列(MEA)腔室,箭头指向脑脊液灌注系统。
¶ 2.4. 病毒转导
然后使用源自pGP-AAV-syn-jGCaMP7f-WPRE(Addgene,美国马萨诸塞州)的腺相关逆行病毒载体(AAV)对这些培养物进行转导。通过将2微升液滴与人类脑干细胞表面接触来施用AAV。脑切片分别培养3天、7天和10天,在此期间,每隔一天更换培养孔板中的0.75毫升人工脑脊液,以优化转导效率。转导后第10天进行实验。
¶ 2.5. 刺激与荧光图像采集
人骨髓基质细胞(hBSCs)被随机分为两组:MENP加刺激组(M+/S+)和MENP不加刺激组(M+/S-)。两组均接受2μl的MENP悬浮液(约3μg MENPs)注射,随后进行孵育以允许MENP扩散(图1(E)和(F))。注射后,M+/S+组使用定制线圈系统(图1(G))在220mT直流、6mT交流(140Hz)的条件下进行刺激。刺激参数基于我们最近的体内和硅片研究,通过这些研究我们开发并测试了基于MENP的神经刺激技术(Kozielski等人,2021年;Kumari等人,2024年;Dominguez-Paredes等人,2025年)。刺激在Leica FS固定载物台显微镜(德国韦茨拉尔Leica Microsystems GmbH)下进行,该显微镜配备荧光照明系统和20×/0.50数值孔径(NA)的物镜水浸镜头(图1(H)-(J))。M+/S-组的切片处理方式相同,但线圈处于关闭状态,因此组织仅暴露于直流磁场中。在整个钙成像数据采集过程中,人骨髓基质细胞浸没在含碳氧混合气的人工脑脊液(aCSF)中,并使用定制的网栅进行机械固定(图1(H))。为了最大限度地减少光毒性和光漂白,使用了低强度荧光团光和缩短曝光时间。使用ImageJ软件[1.8版本;美国贝塞斯达国立卫生研究院]中的SIFT线性堆叠对齐来解决振动问题,以确保精确的图像对齐。此外,进行背景减法以校正光漂白效应,并提高所得图像的准确性和清晰度。钙成像后两小时,M+/S+组和M+/S-组分别接受直流/交流刺激和直流刺激,随后孵育2小时,并用多聚甲醛固定以进行cFos免疫组织化学(IHC)检测。
¶ 2.6. 多电极阵列记录
在使用多电极阵列(MEA)进行电生理记录时,通过将以下物质溶解在500毫升超纯水中制备人工脑脊液(aCSF):3.68克氯化钠(126毫摩尔)、0.112克氯化钾(3毫摩尔)、1.008克碳酸氢钠(24毫摩尔)、0.991克葡萄糖(11毫摩尔)、0.147克氯化钙(2.65毫摩尔)、0.154克硫酸镁(2.56毫摩尔)和0.078克磷酸二氢钠(1.3毫摩尔)。溶液的pH值调节至7.4。记录前,脑切片在含5%二氧化碳和95%氧气的人工脑脊液中孵育1.5小时,记录使用CorePlate™ SingleWell高密度多电极阵列系统(3Brain AG,瑞士;图1(K)和(L))。记录前,人骨髓基质细胞在线圈中受到刺激。
¶ 2.7. 免疫组织化学染色
组织切片在多聚甲醛中固定24小时后,放入20%蔗糖中再孵育24小时,随后快速冷冻,切成20微米厚的切片,储存在-80℃下直至染色。c-Fos染色用于评估神经元活性(Morgan和Curran,1986)。组织切片与多克隆c-Fos(兔源,1:1000;Santa Cruz Biotechnology公司;sc-253)孵育过夜,之后加入生物素化驴抗兔二抗(1:400;Jackson ImmunoResearch Laboratories公司;711065152)和亲和素-生物素过氧化物酶复合物(1:800;Elite ABC试剂盒,Vector Laboratories公司;PK-6100)。使用3,3’-二氨基联苯胺结合氯化镍增强法使染色可视化。
¶ 2.8. 明场图像采集及c-Fos阳性神经元的定量分析
使用奥林巴斯AX 70显微镜(奥林巴斯,荷兰祖特沃德)获取明场图像。采用10倍/0.30数值孔径的物镜和CellP软件(6.1版本)。所有样本均在单色模式下进行拍摄,灯强度稳定在6.8伏,曝光时间设置为80毫秒。使用载物台测微计进行每日像素-距离校准(1像素=0.49微米)。对于每个切片,从内侧边缘到外侧边缘,系统性地对三个不重叠的1平方毫米皮质区域进行成像。图像分析由一名对实验分组和条件不知情的评估人员使用FIJI(ImageJ v1.54)进行:先进行Renyi熵自动阈值处理,再进行手动调整(±5%)、感兴趣区域勾勒,以及对NiDAB标记的c-Fos阳性细胞核进行多点计数。细胞计数按面积归一化,并取每个切片3-5个部分的平均值,统计分析使用GraphPad Prism 10.1.2(GraphPad软件,美国加利福尼亚州圣地亚哥)进行。
¶ 3. 结果
¶ 3.1. 研究人群
2023年1月至2024年9月期间,在马斯特里赫特大学医学中心,对11名因癫痫接受前颞叶切除术联合杏仁核海马切除术的患者的新皮质组织样本进行了11项实验(表1)。
¶ 3.2. 病毒转导与钙成像
在研究过程中,分别在第3天、第7天和第10天暂停病毒转导以进行荧光成像,其中在第10天观察到最佳结果(图2(A)-(F))。“最佳”指的是可重复且强烈的GCaMP荧光、完好的神经元形态以及在多个视野中可见的自发性钙瞬变的组合,这表明病毒表达成熟且神经元活动功能正常,适合后续的刺激实验。人骨髓间充质干细胞浸泡在人工脑脊液中,并通过3D打印网固定(图1(H)),以确保准确的图像采集。为避免振动,必须将线圈从显微镜上拆下(图1(I))。通过小心移动定制的人骨髓间充质干细胞培养孔支架来调整图像(图1(J))。使用Fiji软件(Schindelin等人,2012年)分析荧光堆栈,其中应用背景减法以减轻光漂白和时间噪声的影响。为进一步稳定图像并防止闪烁伪影,使用了“带SIFT的线性堆栈对齐”插件。
¶ 表1. 癫痫患者行前颞叶切除术的手术操作及组织病理学结果概述。该表总结了所实施手术的类型、侧别以及新皮质的神经病理学特征。
| 实验编号 | 年龄 | 性别 | 侧别 | 新皮质病理组织学分析 |
|---|---|---|---|---|
| 1 | 61 | 男 | 右侧 | 轻度胶质细胞增生改变 |
| 2 | 55 | 女 | 左侧 | 轻度胶质细胞增生改变 |
| 3 | 46 | 女 | 右侧 | 颞叶轻度胶质细胞增生改变,海马体重度硬化 |
| 4 | 60 | 男 | 右侧 | 轻度出血性改变 |
| 5 | 32 | 男 | 左侧 | 轻度胶质细胞增生改变 |
| 6 | 41 | 男 | 左侧 | 轻度胶质细胞增生改变 |
| 7 | 27 | 女 | 右侧 | 轻度胶质细胞增生改变 |
| 8 | 32 | 男 | 左侧 | 轻度胶质细胞增生改变 |
| 9 | 44 | 男 | 左侧 | 轻度胶质细胞增生改变 |
| 10 | 57 | 女 | 左侧 | 轻度胶质细胞增生改变 |
| 11 | 39 | 男 | 左侧 | 轻至中度胶质细胞增生改变 |
¶ 3.3. 多电极阵列记录
MEA记录在人脑脊液(hCSF)与人工脑脊液(aCSF)1:1混合液中进行。在整个记录过程中,新鲜的、经碳合气饱和的人工脑脊液持续灌流MEA培养室(图1(L))。由于线圈的磁场会干扰设备性能,刺激必须在将人脑类器官(hBSC)放置到MEA上之前进行。值得注意的是,只有在添加了7.5 mM氯化钾或500 µM 4-氨基吡啶的碳合气饱和人工脑脊液中,才能检测到锋电位和局部场电位(LFP)。在制备后即刻以及第2、5和7天,尝试对培养的人脑切片进行记录。然而,仅在切片当天观察到了局部场电位和锋电位。因此,电生理记录是在将脑组织切片至300 µm厚度后、培养之前立即进行的。
¶ 3.4. 免疫组织化学与c-Fos定量分析
在组织内可清晰检测到c-Fos的表达(图3(A)和(B)),同时还能看到MENPs的可见聚集体(图3(C))。除了预期的核染色外,还观察到了细胞质中的c-Fos信号;然而,分析中仅纳入了具有清晰可辨核染色的细胞。尽管并非持续可见,但通过定性评估,有时可以辨别出c-Fos表达的组间差异(图3(D)-(G))。
使用Shapiro-Wilk检验评估各实验条件下汇总的c-Fos计数是否符合正态分布,结果显示数据违反了正态性假设(p < 0.0001)。在每个实验组内对c-Fos阳性细胞计数进行标准化,随后采用非参数双尾Mann-Whitney检验分析组间的倍数变化差异。观察到M+/S+组的c-Fos阳性细胞倍数变化显著高于M+/S−组(p = <0.001)(图3(H))。
¶ 4. 讨论
本研究旨在评估人骨髓间充质干细胞(hBSCs)是否可作为转化测试平台,以磁性纳米颗粒(MENPs)为代表性示例,用于评估新技术的神经调节潜力。我们成功制备了人骨髓间充质干细胞,进行了病毒转导,并利用磁性纳米颗粒调节了神经元活动。通过钙成像和c-Fos的免疫组织化学(IHC)染色的双重读数设置,证实了神经元调节作用和培养物活力。所有实验组中c-Fos的可见表达表明固定时组织具有活力(Lara Aparicio等人,2022年),而各组间表达水平的显著差异则显示了磁性纳米颗粒调节神经元活动的能力。
¶ 4.1. 脑片培养设置的定制化
为了针对特定需求优化流程、提高可重复性并解决实施过程中遇到的技术挑战,我们进行了多项调整。Bak等人描述的方案既全面又具有适应性。与手术团队的有效沟通至关重要,我们发现,在打开硬脑膜之前出现在手术室中,以便收集人脑脊液进行培养,这一点必不可少。在可行的情况下,外科医生会使用注射器吸出多余的人脑脊液,而不是采用吸引器,特别是在进入硬膜下腔后,这样可以立即将其放在冰上冷却。关于组织制备,我们仅在软脑膜可清晰识别或自然脱落时才将其移除,因为手动剥离通常会导致皮质损伤。值得注意的是,振动切片不受软脑膜存在的影响。在转移组织切片时,使用钝铲或探针可将机械应力降至最低。将人脑切片修剪并放置在网状插入物上后,使用1000微升移液管吸去多余液体。如果人脑切片出现重叠、折叠或位置不当的情况,精确滴加少量人工脑脊液即可解决这些问题。根据获得的脑组织量,我们制备了18、36或44个人脑切片,每个孔中放置3片。理论上,MENP注射可在制备后至刺激前至少2小时之间的任何时间进行。然而,立即注射会导致可见颗粒从人脑切片迁移到网状插入物上,而在刺激前2小时进行注射时,这种迁移会减少。我们测试了两种注射装置:微量注射器和2微升移液管。虽然微量注射器能实现精确的空间定位,但其静态管路系统会导致颗粒沉降、堵塞或分布不均。10微升移液管被证明更为实用,可在注射前立即搅拌MENP悬浮液。我们首先在移液管尖端形成液滴,使其与组织接触直至表面张力破裂,然后注入剩余体积。将插入物从培养板中取出,放入单个孔中进行刺激。刺激时将孔从培养箱中取出,刺激后再放回。实验组被分配到各个孔中。所有组的处理方式相同,以避免因机械应力导致c-Fos表达被检测到。
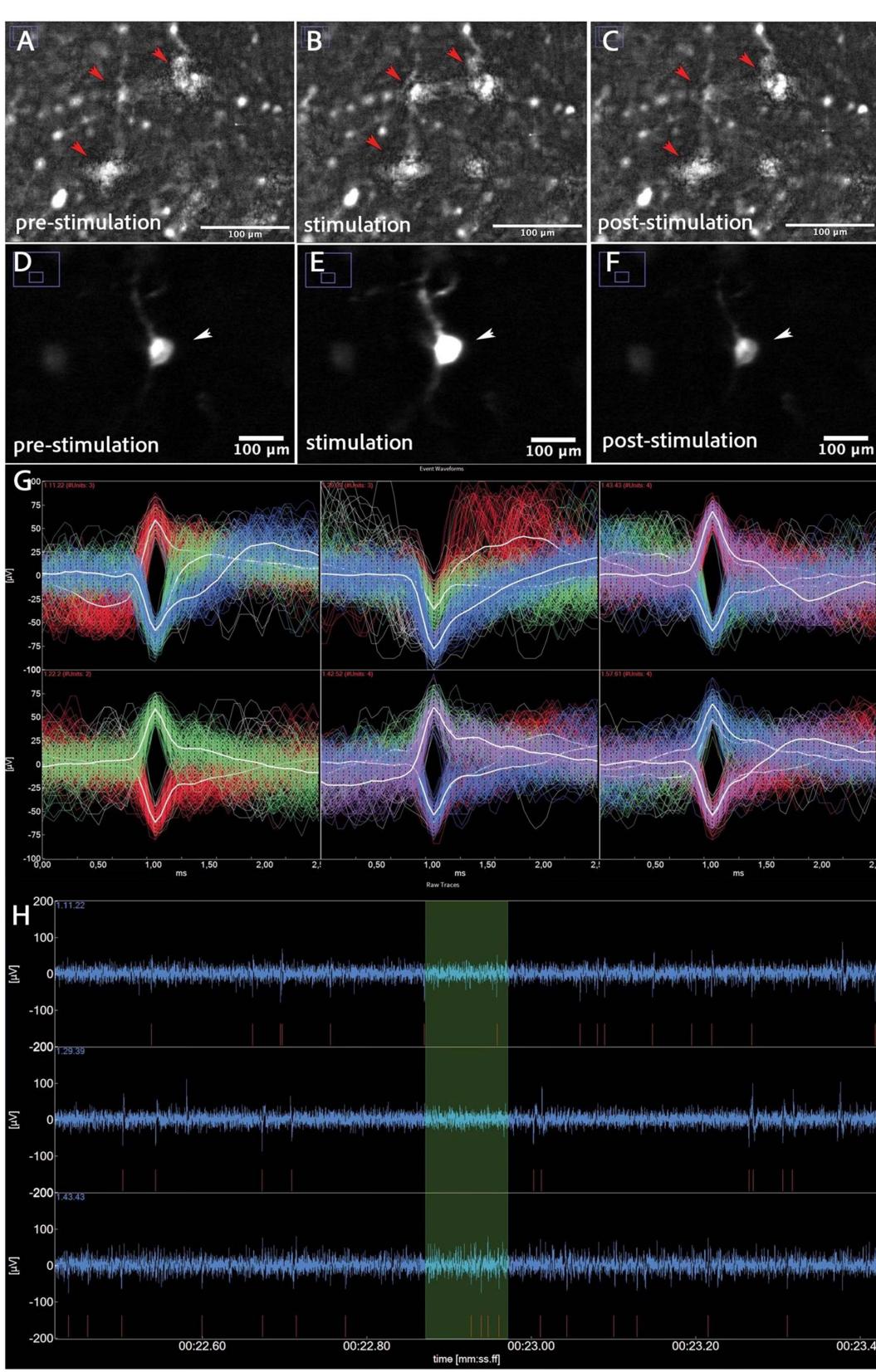
图2.(A)刺激前的GCaMP阳性神经元(B)刺激下显示网络活动(箭头所示)的GCaMP阳性神经元。(C)刺激后的GCaMP阳性神经元。(D)刺激前的单个GCaMP阳性神经元(箭头所示)。(E)刺激下显示钙内流的单个GCaMP阳性神经元(箭头所示)。(F)刺激后钙内流减少的单个GCaMP阳性神经元(箭头所示)。(G)尖峰波形。每个面板对应不同的电极通道,在2-3毫秒的窗口内显示多个事件对齐的波形。叠加的轨迹(红色、白色、绿色和蓝色)反映了单个神经元尖峰和/或群体反应,显示出不同电极间振幅和形状的变异性。(H)原始电生理轨迹记录。蓝色波形显示随时间变化的细胞外电压,反映自发神经元活动。轨迹下方的红色标记表示单个尖峰检测事件(推定动作电位)。绿色阴影区域突出显示感兴趣的间隔(爆发检测窗口)。相对稳定的基线和离散的尖峰事件表明神经元健康状况良好,且信号与噪声分离清晰。
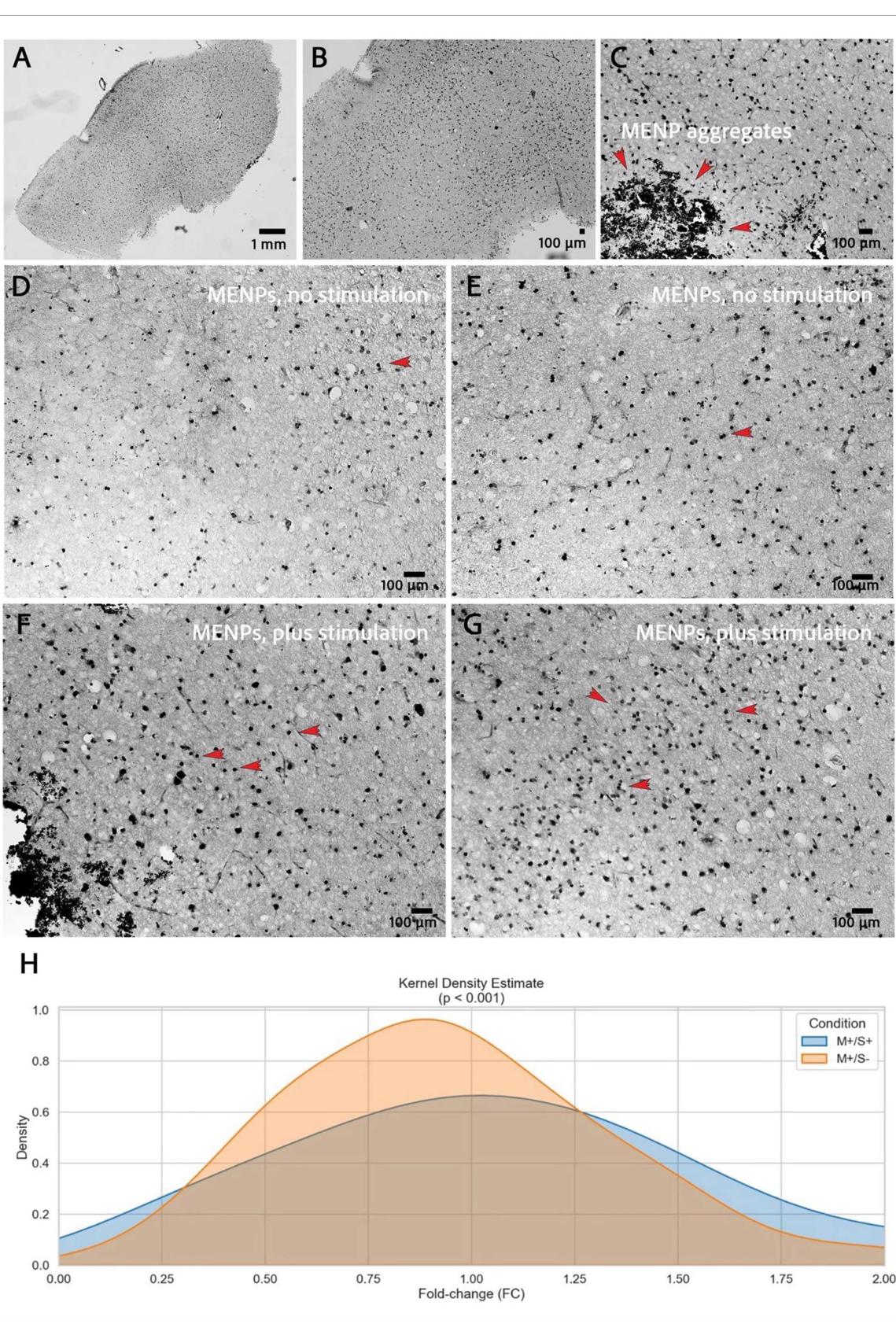
图3.(A)整个hBSC切片的概览图像,经c-Fos染色。(B)可见密集的c-Fos表达。(C)用于计数c-Fos阳性细胞核和示例性MENP聚集体的放大倍数。(D/E)来自MENP无刺激组的hBSCs免疫组化图像,显示c-Fos表达明显减少(红色箭头指示示例性c-Fos阳性细胞核)。(F/G)来自MENP刺激组的hBSCs免疫组化图像,显示c-Fos表达密度明显增加(红色箭头指示示例性c-Fos阳性细胞核)。(H)M+/S+组与M+/S-组的c-Fos表达倍数变化,通过核密度估计可视化(曼-惠特尼检验p<0.001)。
染色方案大体上遵循标准流程;然而,由于切片较为脆弱,在组织包埋过程中需要特别注意。我们使用截短的移液管将切片转移到载玻片上,并用纸巾和10微升移液管吸去多余液体。在过夜干燥后,我们建议将烤箱孵育时间从1小时延长至3小时,以提高黏附力并防止脱水过程中组织脱落。
¶ 4.2. 人脑切片(hBSCs)作为转化模型的评估
我们旨在确定在该系统中制备和培养的人骨髓基质干细胞是否能作为一个可靠且可扩展的平台,用于功能研究和筛选工具。这一评估对于我们通过推进人类体外模型来减少对动物实验依赖的总体目标至关重要。
根据实验设计的不同,可能会产生多种培养物用于测试,例如不同的刺激方案、颗粒负载量,或电生理记录等检测指标。将其应用于动物实验时,这需要进行多次伦理审查,并在时间和金钱上投入大量成本。此外,由于啮齿动物和人类在基因表达和细胞形态上存在显著差异(Hodge等人,2019年),在进行体内实验之前,必须先观察人类脑干细胞(hBSCs)中任何效应或机制,这也凸显了其作为有前景的新方法转化工具的能力。 使用该模型时,一个重大挑战是患者特征的异质性,如年龄、性别、用药情况(直接影响神经元活动的抗癫痫药物)、围手术期条件以及所取组织的形态。不过,这一问题可以通过两种方式解决:一是像我们所做的那样,纳入大量病例并显示出整体显著差异;二是将每个实验视为独立个体,仅对来自同一病例的人类脑干细胞进行分析。 检测方法的选择也带来了额外的挑战。例如,c-Fos常被用作神经元活动的标志物,因为它相对容易检测且为此目的被广泛认可。但也应考虑其局限性:c-Fos不仅由神经元表达,还会由神经胶质细胞等其他中枢神经系统细胞表达。此外,机械刺激可诱导神经胶质细胞和神经元中c-Fos的表达(Jaworski等人,2018年)。这些机械刺激带来了实际操作上的挑战,因为实验过程中对培养物的处理会施加机械应力,可能触发c-Fos的表达。因此,务必尽可能一致地处理不同条件下的培养物,并在注射磁性纳米颗粒(MENPs)后至少等待两小时再评估c-Fos的表达,以减少假阳性检测。 相比之下,电刺激仅能诱导神经元中c-Fos的表达(Hisanaga等人,1990年;Cruz-Mendoza等人,2022年)。此外,星形胶质细胞中c-Fos的表达在刺激后20-45分钟内达到峰值(Cruz-Mendoza等人,2022年),而神经元中c-Fos的表达峰值约在两小时左右出现(Lara Aparicio等人,2022年)。因此,在选定时间点量化的差异有望反映神经元对磁性纳米颗粒刺激的激活反应。为进一步表征c-Fos阳性细胞,可根据研究设计进行双重免疫荧光标记。 来自切除组织的自发性癫痫样活动可能导致电生理记录出现假阳性。尽管现有文献对此担忧的支持并不充分,但仍需予以承认。单细胞水平的自发性发作间期或发作期活动是一种罕见现象(Levinson等人,2020年)。值得注意的是,一项采用类似微电极阵列(MEA)实验装置的研究,将癫痫患者的人类新皮质活检组织与人类诱导多能干细胞(hiPSC)衍生的皮质神经元共培养,结果表明,仅在混合共培养物中出现了癫痫样网络活动,而单独的活检组织或神经元层均未显示出癫痫样放电(Hu等人,2023年)。
¶ 5. 结论
hBSC模型证明了在功能性人类神经元网络中研究新型神经刺激设备的可行性。这种方法提供了一个具有伦理优势的转化测试平台,可用于在动物研究前对有前景的技术进行预筛选,尤其是那些在体内试验中失败风险较高的技术或出于好奇驱动的早期阶段产品。在人体组织中确定有效的干预措施可能会减少所需的动物实验数量,同时提高后续体内研究的相关性和影响力。随着伦理和资金框架对动物模型使用的限制日益增加,像hBSCs这样基于人类的系统有望成为转化神经科学中的重要工具。未来的工作将侧重于开展更多实验并完善所描述的读数,进一步增强该平台对新兴纳米级和生物电子神经调节技术的系统评估能力。
在纳入研究前,已获得所有参与者的书面知情同意。组织采集是按照涉及人类生物材料研究的机构和国家指南进行的。
¶ 数据可用性声明
由于该研究领域没有合适的数据库来存储数据,因此这些数据在发表时无法公开获取。支持本研究结果的数据可根据合理请求向作者索取。
¶ 致谢
本研究得到了以下资助:迈克尔·J·福克斯基金会(MJFF-019718)对AJ、KK和YT的资助;ROMO(2023)对AJ、KR和YT的资助;欧盟(ERC,NANeurO,项目编号101115997)对KK的资助;荷兰研究委员会(NWO-Vidi:09150171910022)对AJ的资助。FE得到了蒂曼基金会的博士奖学金支持。FE感谢Faisal Alosaimi博士和Ghazi Al Jowf博士的支持。
¶ 利益冲突
弗朗茨·A·M·埃格特感谢蒂曼基金会通过博士奖学金提供的支持。该基金会在研究设计、数据收集、分析、发表决定或手稿准备方面均未发挥作用。其他所有作者均声明不存在利益冲突。
¶ 伦理声明
人脑组织和脑脊液(CSF)取自马斯特里赫特大学医学中心(MUMC+)接受前颞叶切除术的耐药性癫痫患者。所有涉及人类参与者的程序均按照《赫尔辛基宣言》进行,并获得了当地医学伦理委员会的批准(METC 2022-3539和2024-0344)。
¶ 作者贡献
弗朗茨·A·M·埃格特 0000-0003-0235-1720 概念构思(同等贡献)、数据整理(主要贡献)、形式分析(主要贡献)、调查研究(主要贡献)、研究方法(同等贡献)、可视化(同等贡献)、初稿撰写(主要贡献)、审阅与编辑(主要贡献)
Berkhan Genc 0000-0001-9578-6584 概念构思(同等贡献)、数据整理(同等贡献)、形式分析(同等贡献)、调查研究(同等贡献)、研究方法(同等贡献)、软件(主要贡献)、验证(同等贡献)、可视化(同等贡献)、撰写 - 审阅与编辑(同等贡献)
塞纳·努尔·阿尔杜克 0009-0003-3941-0576 数据整理(同等贡献)、研究(同等贡献)
Anouk Wolters 0000-0001-6975-1812 方法学(同等贡献),写作–审阅与编辑(同等贡献)
Kim Rijkers 0000-0002-3348-158X 概念构思(同等贡献),调查研究(同等贡献),项目管理(同等贡献),资源(同等贡献),监督指导(同等贡献),写作–审阅与编辑(同等贡献)
克里斯汀·科齐尔斯基 方法学(同等贡献)
亚辛·泰梅尔 0000-0002-3589-5604 资金获取(负责人)、项目管理(同等)、资源(同等)
阿里·贾汉沙希 0000-0002-7451-3461 概念构思(同等贡献)、资金获取(主导)、方法设计(同等贡献)、项目管理(主导)、资源(主导)、监督(主导)、写作——审核与编辑(同等贡献)
¶ 参考文献
Bak A等人,2024年。人类器官型脑切片培养:详细且改进的制备和长期维持方案。《神经科学方法杂志》,404期,110055。
Barth M等人,2021年。在长期脑切片培养中,小胶质细胞包涵体和神经丝轻链释放发生在神经元α-突触核蛋白损伤之后。《分子神经退行性疾病》,16卷,54页。
Cassotta M 等人,2022年。帕金森病研究的未来:一种新的人类特异性研究范式是必要的……而且是可能的。《ALTEX》,39卷,694-709页。
陈RJ等。2020。目前对自噬在纳米材料毒性中的理解及其在与安全性评估相关的替代测试策略中的应用。《国际分子科学杂志》,21,2387。
克鲁兹-门多萨 F、豪雷吉-韦尔塔 F、阿吉拉尔-德尔加迪略 A、加西亚-埃斯特拉达 J、卢克因 S. 2022. 大脑中的即早基因c-Fos:聚焦神经胶质细胞。《脑科学》,12,687.
多明格斯-帕雷德斯 D、泰梅尔 Y、米洛日科维奇 A、穆尔德-容根 D、库马里 P、里斯 M、科齐尔斯基 K、贾汉沙希 A。2025。用于缓解帕金森病小鼠运动障碍的磁电纳米颗粒技术。《脑刺激》,18,1551-1560。
Ereifej E S, Cheng M M, Mao G, VandeVord P J. 2013. 利用器官型脑切片方法研究对纳米图案化聚二甲基硅氧烷的炎症反应。《神经科学方法杂志》,217,17-25。
欧盟。2022年。全欧盟动物研究统计数据。可访问:https://www.understandinganimalresearch.org.uk/news/eu-wideanimal-research-statistics-2022。
古利诺 M、金 D、潘 S、桑托斯 S D、佩戈 A P. 2019. 组织对神经植入物的反应:模型系统在可植入微电极新设计方案中的应用。《神经科学前沿》,13,689.
久永K、萨加尔S M、希克斯K J、斯旺森R A、夏普F R. 1990. c-Fos原癌基因在与分化或增殖相关但与去极化无关的星形胶质细胞中的表达。《脑研究:分子脑研究》,8,69-75.
霍奇 R D 等。2019。人与小鼠皮层中具有不同特征的保守细胞类型。《自然》,573,61-68。
胡M H Y、弗里马特J-P、里克尔斯K、斯海恩斯O E M G、范登马格登贝格A M J M、丁斯J T A、吕特格R、胡格兰德G。2023。在多电极阵列上与人类癫痫脑活检组织共培养的人诱导多能干细胞衍生皮质神经元的自发性癫痫记录。《应用科学》,13,1432。
胡斯科宁 J、苏鲁宁 T、米耶蒂宁 R、范·格罗恩 T、萨尔米宁 A. 2005. 一种用于研究出生后大鼠海马切片器官型膜培养中炎症反应的改良体外模型。《神经信息学杂志》,2,25.
雅沃尔斯基 J、卡利塔 K、克纳普斯卡 E. 2018. c-Fos 与神经元可塑性:卡奇马雷克理论的后续发展。《实验神经生物学学报》,78,287-296。
基弗 J、萨默斯 C H. 2016. 让“生物学”回归“神经生物学”:神经科学研究中动物模型系统多样性的优势。《系统神经科学前沿》,10,69。
Kiani A K 等人,2022。关于动物实验的伦理考量。《预防医学与卫生学杂志》,63卷,E255–E266页。
Kozielski K L、Jahanshahi A、Gilbert H B、Yu Y、Erin O、Francisco D、Alosaimi F、Temel Y、Sitti M. 2021. 可注射纳米电极的非共振供电实现自由活动小鼠的无线深部脑刺激。《科学进展》,7,eabc4189.
克里斯滕森 B W、诺拉伯格 J、蒂博 P、库德尔卡-黑普 M、齐默 J. 2001. 硅基电极阵列与器官型海马脑片培养物的生物相容性。《脑研究》,896,1-17.
Kumari P、Wunderlich H、Milojkovic A、Lopez J E、Fossati A、Jahanshahi A、Kozielski K. 2024. 磁电纳米颗粒的多尺度建模用于空间选择性神经刺激分析。《先进医疗材料》,13,e2302871。
拉拉·阿帕里西奥·S·Y等人,2022年。关于在神经科学中使用c-Fos的当前观点。《神经科学》,第3卷,第687-702页。
莱文森 S、陈 C H、巴里 J、维克 B、莱文 M S、温特斯 H V、马瑟恩 G W、塞佩达 C。2020。小儿癫痫手术患者组织切片中的阵发性放电:GABA(B)受体在发作活动产生中的关键作用。《细胞神经科学前沿》,14,54。
马汉 T R. 2002. 人类为何可以利用动物. 《价值探究杂志》, 36, 9–14.
摩根 J I、柯伦 T. 1986. 离子流在c-Fos表达调控中的作用。《自然》,322,552–555.
Moulin T C、Covill L E、Itskov P M、Williams M J、Schioth H B. 2021. 行为神经科学中的啮齿类动物和果蝇模型:方法学进展、比较研究及未来展望的评估。《神经科学与生物行为评论》,120,1-12。
Nikolakopoulou P, Rauti R, Voulgaris D, Shlomy I, Maoz B M, Herland A. 2020. 中枢神经系统转化工程体外模型的最新进展。《大脑》,143,3181-3213。
诺拉伯格 J. 2004. 器官型脑切片培养:一种高效可靠的神经毒理学筛选和机制研究方法。《替代实验动物》,32,329-337。
Schindelin J 等人,2012 年。Fiji:一个用于生物图像分析的开源平台。《自然方法》,9,676–682。
Schwarz N 等人,2019年。长期成人脑切片培养作为研究人类中枢神经系统回路和疾病的模型系统。《eLife》,8卷,e48417。
Usmani S 等人,2016年。碳纳米管的3D网格引导分离的脊髓外植体的功能性重新连接。《科学进展》,2卷,e1600087。